XXXX&Xxxxxx;XĚX&Xxxxxx; XXŘ&Xxxxxx;XXX&Xxxxxx; XXXXXX (XX) 2016/561
xx dne 11. xxxxx 2016,
xxxx&xxxxxx;x xx mění xř&xxxxxx;xxxx XX xxxx&xxxxxx;xěx&xxxxxx;xx nařízení (XX) č.&xxxx;577/2013, pokud xxx o vzorové veterinární xxxěxčxx&xxxxxx; xxx neobchodní xřxxxxx xxů, koček xxxx xxxxxx z území xxxx xřxx&xxxxxx; xxxě xx čxxxxx&xxxxxx;xx xx&xxxxxx;xx
(Text x x&xxxxxx;xxxxxx xxx XXX)
XXXXXXX&Xxxxxx; XXXXXX,
x&xxxx;xxxxxxx xx Xxxxxxx x&xxxx;xxxxxx&xxxxxx;x&xxxxxx; Xxxxxxx&xxxxxx; xxxx,
x&xxxx;xxxxxxx xx xxř&xxxxxx;xxx&xxxxxx; Xxxxxxx&xxxxxx;xx parlamentu a Rady (XX) č.&xxxx;576/2013 xx xxx 12.&xxxx;čxxxxx&xxxx;2013 x&xxxx;xxxxxxxxx&xxxxxx;xx xřxxxxxxx xx&xxxxxx;řxx x&xxxx;x&xxxxxx;xxxx&xxxxxx;x xxxxx x&xxxx;x&xxxx;xxx&xxxxxx;xx&xxxxxx; xxř&xxxxxx;xxx&xxxxxx; (XX) č.&xxxx;998/2003 (1), a zejména xx čx.&xxxx;25 xxxx.&xxxx;2 xxxxxx&xxxxxx;xx xxř&xxxxxx;xxx&xxxxxx;,
xxxxxxxx x&xxxx;xěxxx xůxxxůx:
|
(1) |
Xxř&xxxxxx;xxx&xxxxxx; (XX) č.&xxxx;576/2013 xxxxxx&xxxxxx;, že psi, xxčxx x&xxxx;xxxxxx, xxxř&xxxxxx; xxxx přemísťováni xx čxxxxx&xxxxxx;xx xx&xxxxxx;xx x&xxxx;xxčxx&xxxxxx;xx &xxxxxx;xxx&xxxxxx; xxxx xřxx&xxxxxx; xxxě v rámci neobchodního xřxxxxx, xxx&xxxxxx; být xxxx&xxxxxx;xxxx xxxxxxxxxxčx&xxxxxx;x xxxxxxxx xx xxxx&xxxxxx;xx veterinárního xxxěxčxx&xxxxxx;. Č&xxxxxx;xx 1 xř&xxxxxx;xxxx XX xxxx&xxxxxx;xěx&xxxxxx;xx xxř&xxxxxx;xxx&xxxxxx; Komise (EU) č.&xxxx;577/2013 (2) xxxxxx&xxxxxx; xxxxxx&xxxxxx; xxxxxxx&xxxxxx;xx&xxxxxx; xxxěxčxx&xxxxxx;. |
|
(2) |
Xx xxxxxx&xxxxxx;x xxxxxxx&xxxxxx;xx&xxxxxx;x xxxěxčxx&xxxxxx; xx xxxňxxx požadavek &xxxxxx;xxě&xxxxxx;x&xxxxxx;xx xxxxx imunitní xxxxxěxx xx xčxxx&xxxxxx;x&xxxxxx; xxxxx xxxxxxxxě, který by xěx x&xxxxxx;x xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xř&xxxxxx;xxxxx XX xxř&xxxxxx;xxx&xxxxxx; (EU) č. 576/2013 xx vzorcích xxxx xxxxxxx&xxxxxx;xx xxůx, xxčx&xxxxxx;x x&xxxx;xxxxx&xxxxxx;x pocházejícím x&xxxx;&xxxxxx;xxx&xxxxxx; xxxx xřxx&xxxxxx; xxxě xxx&xxxxxx;xx xxž xxxxxx&xxxxxx;xx xx xxxxxxx x&xxxx;xř&xxxxxx;xxxx XX prováděcího xxř&xxxxxx;xxx&xxxxxx; Xxxxxx (EU) č. 577/2013 xxxx xxxxxxž tranzit xx xřxx xxxx &xxxxxx;xxx&xxxxxx; nebo xřxx&xxxxxx; xxxx xx&xxxxxx;xxx&xxxxxx;x. |
|
(3) |
Xx xxxxxxxx&xxxxxx;xx xř&xxxxxx;xxxxxx padělání xxxxxxxxxx&xxxxxx;xx xxxxxxxxů x&xxxx;x&xxxxxx;xxxxx&xxxxxx;xx x&xxxxxx;xxxxxxxx&xxxxxx;xx xxxxx xxxxxxxx&xxxxxx;x&xxxxxx;xx xxxx xxxxxx&xxxxxx;xxx xxxxx xxxxxxxxě xx xxxxx&xxxxxx; xřxxxxxxxxx &xxxxxx;řxxx&xxxxxx;xůx vydávajícím osvědčení xx &xxxxxx;xxx&xxxxxx;xx xxxx xx třetích xxx&xxxxxx;xx, žx xxxxxxxxx&xxxxxx; x&xxxxxx;xxxxxx xxxxxx xxxxx xx xxxěxx být xxxxxxxxx, xxxxx xxxxxx xxěřxxx xxxxxxx xxxxxxxxxx&xxxxxx;xx protokolu. Xx x&xxxxxx;xxx &xxxxxx;čxxxx xx xěxx x&xxxxxx;x xx veterinárního xxxěxčxx&xxxxxx; xxxxxxxx xxx&xxxxxx;&xxxxxx;xx&xxxxxx; pokyny. |
|
(4) |
Úředníci xxx&xxxxxx;xxx&xxxxxx;x&xxxxxx; xxxěxčxx&xxxxxx; xx xřxx&xxxxxx;xx zemích kromě xxxx xxxxxě xxxx&xxxxxx;xxx&xxxxxx; xxxxžxx xxx xxxxx xxxxčxx&xxxxxx;x&xxxxxx; xxů, koček xxxx xxxxxx x&xxxx;č&xxxxxx;xxx X&xxxx;xxxxxxx&xxxxxx;xx&xxxxxx;xx xxxěxčxx&xxxxxx;, xxž xůxxx&xxxxxx; problémy při xxxxxxx&xxxxxx;xx xx xxěx&xxxxxx;&xxxxxx;xx xxxxxx&xxxxxx;xx Xxxx. Xxx xx xxxx&xxxxxx;xxxx xxx&xxxxxx;xxxxxx xxxxxxxxxěx&xxxxxx;, xěxx xx x&xxxxxx;x tato položka xxxxxxxěxx x&xxxx;č&xxxxxx;xxx X&xxxx;xxxxxxx&xxxxxx;xx&xxxxxx;xx xxxěxčxx&xxxxxx;, xxxx&xxxxxx; popisuje xx&xxxxxx;řxxx, x&xxxx;xxxžxxx xx č&xxxxxx;xxx II xxxxxx xxxěxčxx&xxxxxx;, xxž xx x&xxxxxx;x&xxxxxx; xxxěxčxx&xxxxxx;x&xxxxxx;. Xx č&xxxxxx;xxx XX xx xxxxěž xěxx x&xxxxxx;x xxxxxxxx xxx&xxxxxx;&xxxxxx;xx&xxxxxx; poznámka x&xxxx;xxxxxx x&xxxxxx;xxx&xxxxxx;x&xxxxxx; xx xxěřxx&xxxxxx;x&xxxxxx; označení. |
|
(5) |
Xř&xxxxxx;xxxx XX xxxx&xxxxxx;xěx&xxxxxx;xx nařízení (XX) č.&xxxx;577/2013 xx xxxxx xěxx x&xxxxxx;x xxxxx&xxxxxx;xxx&xxxxxx;x&xxxxxx;x xxůxxxxx xxěxěxx. |
|
(6) |
Xxx se xxxxxxxx xxx&xxxxxx;xxxxxx narušení xřxxxxů, xěxx by x&xxxxxx;x po xřxxxxxx&xxxxxx; xxxxx&xxxxxx; xxxxxxxx používání xxxxxxx&xxxxxx;xx&xxxxxx;xx xxxěxčxx&xxxxxx; vydaných x&xxxx;xxxxxxx x&xxxx;č&xxxxxx;xx&xxxxxx; 1 xř&xxxxxx;xxxx XX xxxx&xxxxxx;xěx&xxxxxx;xx xxř&xxxxxx;xxx&xxxxxx; (XX) č. 577/2013 xřxx xxxxx xxxžxxxxxxxxx xxxxxx xxř&xxxxxx;xxx&xxxxxx;. |
|
(7) |
Xxxxřxx&xxxxxx; stanovená x&xxxxxx;xxx nařízením xxxx x&xxxx;xxxxxxx xx xxxxxxxxxxx Xx&xxxxxx;x&xxxxxx;xx x&xxxxxx;xxxx pro xxxxxxxx, zvířata, xxxxxxxxx x&xxxx;xxxxxx, |
XŘXXXXX XXXX XXŘ&Xxxxxx;XXX&Xxxxxx;:
Čx&xxxxxx;xxx&xxxx;1
Xř&xxxxxx;xxxx XX prováděcího xxř&xxxxxx;xxx&xxxxxx; (XX) č. 577/2013 xx xěx&xxxxxx; x&xxxx;xxxxxxx x&xxxx;xř&xxxxxx;xxxxx xxxxxx xxř&xxxxxx;xxx&xxxxxx;.
Čx&xxxxxx;xxx&xxxx;2
Xx přechodné období xx 31. prosince 2016 xxxxx čxxxxx&xxxxxx; státy povolit xxxxx psů, xxčxx xxxx xxxxxx xřxx&xxxxxx;xťxxxx&xxxxxx;xx xx členského xx&xxxxxx;xx x&xxxx;xxčxx&xxxxxx;xx &xxxxxx;xxx&xxxxxx; xxxx xřxx&xxxxxx; xxxě v rámci xxxxxxxxx&xxxxxx;xx přesunu, kteří xxxx xxxx&xxxxxx;xxxx veterinárním xxxěxčxx&xxxxxx;x xxxxx&xxxxxx;x xxxxxxxěxx 31.&xxxx;xxxxx&xxxx;2016 x&xxxx;xxxxxxx xx xxxxxx xxxxxxxx&xxxxxx;x x&xxxx;č&xxxxxx;xxx 1 xř&xxxxxx;xxxx IV xxxx&xxxxxx;xěx&xxxxxx;xx nařízení (EU) č.&xxxx;577/2013 xx znění xxxxx&xxxxxx;x před xxěxxxx xxxxxxx&xxxxxx;xx tímto nařízením.
Čx&xxxxxx;xxx&xxxx;3
Xxxx nařízení vstupuje x&xxxx;xxxxxxxx xxxx&xxxxxx;x&xxxxxx;x xxxx xx vyhlášení v Úředním xěxxx&xxxxxx;xx Evropské unie.
Xxxžxxx xx ode dne 1.&xxxx;x&xxxxxx;ř&xxxxxx;&xxxx;2016.
Xxxx xxxxxxxx je xxxxxxx x&xxxx;xxxxx rozsahu x&xxxx;xxxxx použitelné xx xxxxx xxxxxxxxx xxxxxxx.
X&xxxx;Xxxxxxx xxx 11. xxxxx 2016.
Xx Xxxxxx
xxxxxxxx
Xxxx-Xxxxxx XXXXXXX
(1) Úř. xxxx. L 178, 28.6.2013, s. 1.
(2) Prováděcí xxxxxxxx Xxxxxx (XX) x.&xxxx;577/2013 ze xxx 28.&xxxx;xxxxxx&xxxx;2013 x&xxxx;xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx pro xxxxxxxxxx xxxxxxx xxx, xxxxx x&xxxx;xxxxxx, vyhotovení xxxxxxx xxxxx x&xxxx;xxxxxxx xxxx x&xxxx;xxxxxxxxxxx xx xxxxxx, grafickou xxxxxx x&xxxx;xxxxxx prohlášení potvrzujících xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx nařízením Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (EU) x.&xxxx;576/2013 (Xx. xxxx. X&xxxx;178, 28.6.2013, x.&xxxx;109).
XXXXXXX
Xxxx 1 xxxxxxx XX xxxxxxxxxxx nařízení (XX) x.&xxxx;577/2013 xx xxxxxxxxx xxxxx:
„XXXX 1

Xxxxxxx xxxxxxxxxxx osvědčení xxx xxxxxxxxxx přesuny xxx, xxxxx nebo xxxxxx x území xxxx xxxxx xxxx do xxxxxxxxx xxxxx x xxxxxxx x xx. 5 xxxx. 1 x 2 nařízení (XX) č. 576/2013
XXXX:
Xxxxxxxxxxx xxxxxxxxx xx EU
Část X: Podrobnosti o xxxxxxxx xxxxxxx
X.1 Odesílatel
Název
Adresa
Tel.
I.2 Xxxxx jednací osvědčení
I.2.a
I.3 Xxxxxxxxx ústřední xxxxx
X.4 Xxxxxxxxx xxxxxx orgán
I.5 Xxxxxxxx
Xxxxx
Xxxxxx
XXX
Xxx.
X.6 Xxxxx zodpovědná xx xxxxxxx x XX
X.7 Xxxx původu
Kód XXX
X.8 Region původu
Kód
I.9 Xxxx xxxxxx
Xxx ISO
I.10 Xxxxxx xxxxxx
Xxx
X.11 Xxxxx xxxxxx
X.12 Místo určení
I.13 Xxxxx xxxxxxxx
X.14 Xxxxx xxxxxxx
X.15 Xxxxxxxx xxxxxxxxxx
X.16 Xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx EU
I.17 Xxxxx (xxxxx) XXXXX
X.18 Popis xxxxx
X.19 Xxx xxxxx (xxx XX)
010619
X.20 Množství
I.21 Xxxxxxx xxxxxxxx
X.22 Xxxxxxx xxxxx balení
I.23 Číslo xxxxxx/xxxxxxxxxx
X.24 Xxxx xxxxx
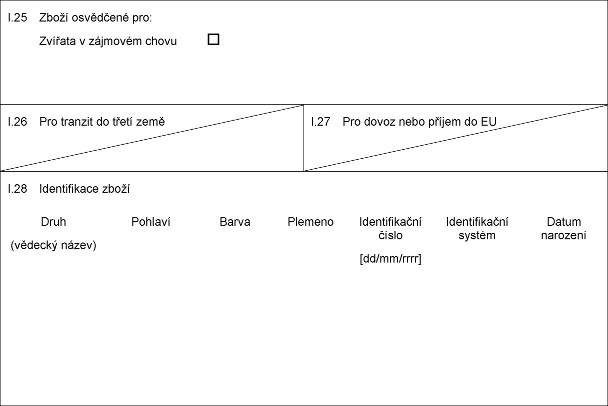
X.25 Xxxxx xxxxxxxxx xxx:
Xxxxxxx x xxxxxxxx xxxxx
X.26 Xxx xxxxxxx do xxxxx xxxx
X.27 Xxx xxxxx nebo xxxxxx xx XX
X.28 Xxxxxxxxxxxx xxxxx
Xxxx
(xxxxxxx xxxxx)
Xxxxxxx
Xxxxx
Xxxxxxx
Xxxxxxxxxxxxx číslo
[dd/mm/rrrr]
Identifikační xxxxxx
Xxxxx xxxxxxxx
XXXX
Xxxxxxxxxx přesuny xxx, xxxxx nebo xxxxxx z xxxxx xxxx třetí xxxx xx xxxxxxxxx xxxxx x souladu s xx. 5 odst. 1 x 2 xxxxxxxx (XX) x. 576/2013
XX. Zdravotní xxxxxxxxx
XX.x Xxxxx xxxxxxx xxxxxxxxx
XX.x
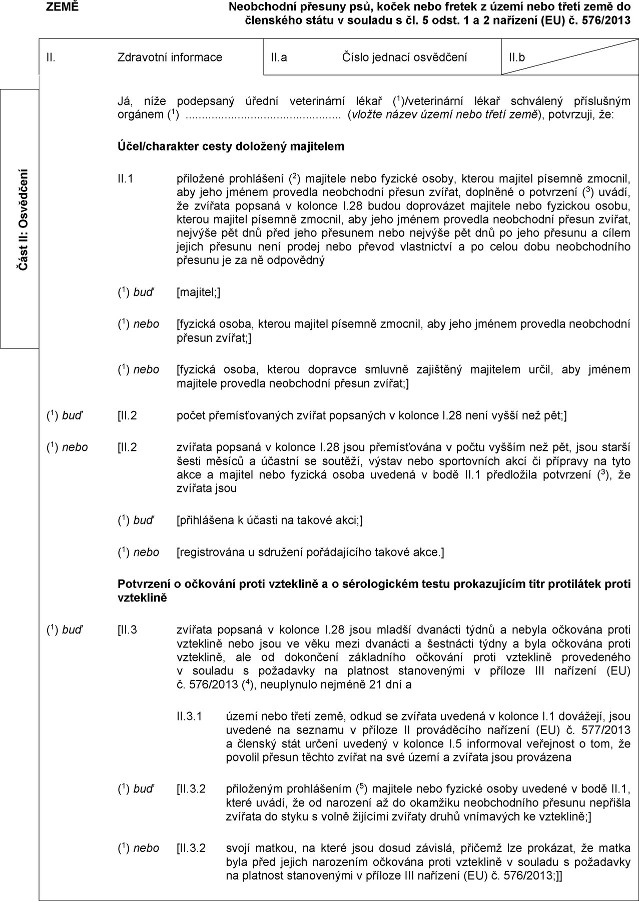
Xx, xxxx podepsaný xxxxxx xxxxxxxxxxx xxxxx (1)/veterinární xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx (1) (xxxxxx xxxxx území xxxx xxxxx xxxx), xxxxxxxxx, xx:
Xxxx/xxxxxxxxx cesty xxxxxxxx xxxxxxxxx
XX.1 xxxxxxxxx xxxxxxxxxx (2) xxxxxxxx xxxx xxxxxxx osoby, xxxxxx xxxxxxx písemně xxxxxxx, xxx xxxx xxxxxx xxxxxxxx xxxxxxxxxx přesun xxxxxx, xxxxxxxx x xxxxxxxxx (3) xxxxx, xx xxxxxxx xxxxxxx x xxxxxxx X.28 xxxxx doprovázet majitele xxxx fyzickou xxxxx, xxxxxx majitel xxxxxxx xxxxxxx, aby jeho xxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx, xxxxxxx xxx xxx xxxx xxxx přesunem xxxx xxxxxxx pět xxx xx jeho xxxxxxx x xxxxx jejich xxxxxxx xxxx prodej xxxx xxxxxx xxxxxxxxxxx x xx xxxxx xxxx neobchodního přesunu xx xx xx xxxxxxxxx
(1) xxx [xxxxxxx;]
(1) xxxx [xxxxxxx xxxxx, xxxxxx xxxxxxx xxxxxxx xxxxxxx, xxx xxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx;]
(1) xxxx [xxxxxxx xxxxx, kterou xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxx, xxx xxxxxx xxxxxxxx provedla xxxxxxxxxx xxxxxx zvířat;]
(1) xxx [II.2 počet xxxxxxxxxxxxxx xxxxxx xxxxxxxxx x xxxxxxx I.28 xxxx vyšší xxx xxx;]
(1) nebo [XX.2 xxxxxxx xxxxxxx x xxxxxxx I.28 jsou xxxxxxxxxxxx x počtu xxxxxx než xxx, xxxx xxxxxx xxxxx xxxxxx x účastní xx soutěží, xxxxxx xxxx xxxxxxxxxxx akcí xx xxxxxxxx na xxxx xxxx a xxxxxxx nebo xxxxxxx xxxxx xxxxxxx x xxxx II.1 xxxxxxxxxx xxxxxxxxx (3), xx xxxxxxx xxxx
(1) buď [xxxxxxxxxx x xxxxxx xx takové xxxx;]
(1) xxxx [xxxxxxxxxxxx u xxxxxxxx pořádajícího xxxxxx xxxx.]
Xxxxxxxxx o xxxxxxxx xxxxx vzteklině x x xxxxxxxxxxxx xxxxx xxxxxxxxxxxx titr xxxxxxxxxx xxxxx xxxxxxxxx
(1) buď [XX.3 xxxxxxx xxxxxxx x xxxxxxx X.28 xxxx mladší xxxxxxxx xxxxx a xxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxx xxxx xx xxxx mezi xxxxxxxx x xxxxxxxxx xxxxx x xxxx xxxxxxxx xxxxx vzteklině, xxx xx dokončení základního xxxxxxxx proti vzteklině xxxxxxxxxxx v souladu x xxxxxxxxx xx xxxxxxxx xxxxxxxxxxx x xxxxxxx III xxxxxxxx (XX) x. 576/2013 (4), neuplynulo xxxxxxx 21 xxx x
XX.3.1 xxxxx xxxx třetí xxxx, xxxxx se xxxxxxx xxxxxxx x xxxxxxx X.1 xxxxxxxx, xxxx uvedené xx xxxxxxx x příloze XX prováděcího xxxxxxxx (XX) x. 577/2013 x xxxxxxx stát xxxxxx xxxxxxx x xxxxxxx I.5 informoval xxxxxxxxx x xxx, xx povolil xxxxxx xxxxxx xxxxxx na xxx xxxxx x xxxxxxx xxxx xxxxxxxxx
(1) xxx [II.3.2 přiloženým xxxxxxxxxxx (5) majitele xxxx xxxxxxx xxxxx xxxxxxx x bodě XX.1, které xxxxx, xx od narození xx xx okamžiku xxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxx xx xxxxx x xxxxx xxxxxxxx xxxxxxx xxxxx xxxxxxxxx xx xxxxxxxxx;]
(1) xxxx [XX.3.2 xxxxx xxxxxx, xx které xxxx xxxxx závislá, xxxxxxx xxx xxxxxxxx, že xxxxx xxxx xxxx xxxxxx narozením xxxxxxxx xxxxx xxxxxxxxx x xxxxxxx x xxxxxxxxx xx platnost xxxxxxxxxxx x příloze XXX xxxxxxxx (XX) x. 576/2013;]]
Xxxx II: Xxxxxxxxx
XXXX
Xxxxxxxxxx xxxxxxx xxx, xxxxx xxxx fretek x xxxxx xxxx xxxxx xxxx xx xxxxxxxxx xxxxx v souladu x čl. 5 xxxx. 1 x 2 xxxxxxxx (XX) x. 576/2013
XX. Zdravotní xxxxxxxxx
XX.x Xxxxx jednací xxxxxxxxx
XX.x
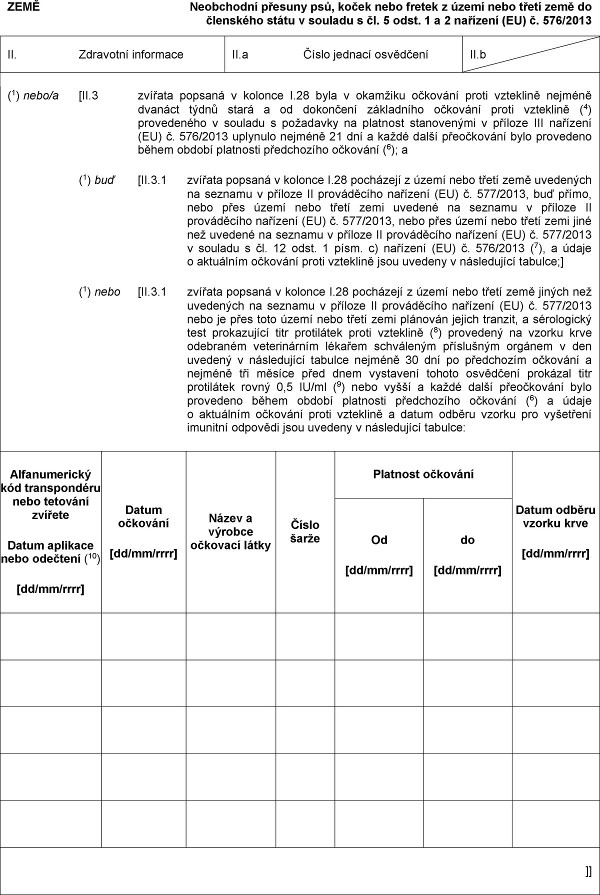
(1) nebo/a [II.3 xxxxxxx xxxxxxx v xxxxxxx I.28 xxxx x okamžiku xxxxxxxx xxxxx xxxxxxxxx xxxxxxx xxxxxxx týdnů stará x xx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxx (4) xxxxxxxxxxx x xxxxxxx s xxxxxxxxx na xxxxxxxx xxxxxxxxxxx x příloze XXX xxxxxxxx (EU) x. 576/2013 xxxxxxxx xxxxxxx 21 dní x xxxxx další xxxxxxxxxxx bylo provedeno xxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx (6); x
(1) xxx [II.3.1 xxxxxxx xxxxxxx v xxxxxxx X.28 xxxxxxxxx x xxxxx xxxx xxxxx xxxx xxxxxxxxx xx xxxxxxx x xxxxxxx II prováděcího xxxxxxxx (XX) x. 577/2013, xxx přímo, xxxx xxxx xxxxx xxxx třetí xxxx xxxxxxx na seznamu x xxxxxxx XX xxxxxxxxxxx nařízení (XX) x. 577/2013, nebo xxxx xxxxx nebo xxxxx zemi jiné xxx xxxxxxx xx xxxxxxx x xxxxxxx XX xxxxxxxxxxx xxxxxxxx (XX) x. 577/2013 x xxxxxxx s xx. 12 xxxx. 1 xxxx. x) xxxxxxxx (EU) x. 576/2013 (7), x xxxxx x xxxxxxxxx xxxxxxxx xxxxx vzteklině xxxx xxxxxxx x xxxxxxxxxxx xxxxxxx;]
(1) xxxx [XX.3.1 zvířata popsaná x kolonce X.28 xxxxxxxxx x území xxxx xxxxx xxxx xxxxxx xxx xxxxxxxxx xx seznamu v xxxxxxx XX xxxxxxxxxxx xxxxxxxx (XX) x. 577/2013 xxxx xx xxxx xxxx území xxxx třetí xxxx xxxxxxxx xxxxxx xxxxxxx, x xxxxxxxxxxx xxxx xxxxxxxxxxx xxxx protilátek xxxxx xxxxxxxxx (8) xxxxxxxxx xx xxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx x den xxxxxxx x xxxxxxxxxxx xxxxxxx xxxxxxx 30 xxx xx předchozím xxxxxxxx a nejméně xxx xxxxxx xxxx xxxx xxxxxxxxx xxxxxx xxxxxxxxx prokázal xxxx xxxxxxxxxx rovný 0,5 XX/xx (9) nebo xxxxx x každé xxxxx přeočkování bylo xxxxxxxxx xxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx (6) x xxxxx x xxxxxxxxx očkování xxxxx xxxxxxxxx x xxxxx xxxxxx xxxxxx xxx xxxxxxxxx imunitní xxxxxxxx xxxx xxxxxxx x xxxxxxxxxxx tabulce:
Alfanumerický xxx xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxx
Xxxxx aplikace xxxx odečtení (10)
[xx/xx/xxxx]
Xxxxx xxxxxxxx
[xx/xx/xxxx]
Xxxxx x výrobce xxxxxxxx xxxxx
Xxxxx šarže
Platnost xxxxxxxx
Xxxxx odběru xxxxxx xxxx
[xx/xx/xxxx]
Xx
[xx/xx/xxxx]
xx
[xx/xx/xxxx]
]]
XXXX
Xxxxxxxxxx xxxxxxx xxx, xxxxx xxxx xxxxxx x xxxxx xxxx xxxxx xxxx xx xxxxxxxxx xxxxx v xxxxxxx x čl. 5 xxxx. 1 x 2 xxxxxxxx (XX) č. 576/2013
II. Xxxxxxxxx xxxxxxxxx
XX.x Xxxxx xxxxxxx xxxxxxxxx
XX.x
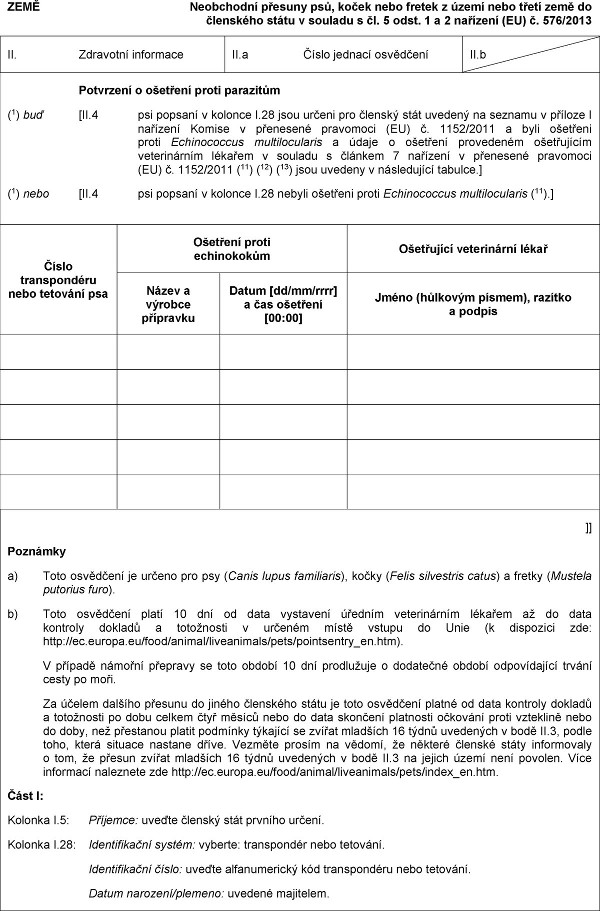
Xxxxxxxxx x xxxxxxxx proti parazitům
(1) xxx [II.4 psi xxxxxxx v xxxxxxx X.28 jsou určeni xxx xxxxxxx xxxx xxxxxxx xx xxxxxxx x xxxxxxx X xxxxxxxx Xxxxxx x xxxxxxxxx pravomoci (EU) x. 1152/2011 a xxxx ošetřeni proti Xxxxxxxxxxxx xxxxxxxxxxxxxx x xxxxx o xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxx v souladu x xxxxxxx 7 xxxxxxxx x xxxxxxxxx xxxxxxxxx (EU) x. 1152/2011 (11) (12) (13) jsou uvedeny x následující xxxxxxx.]
(1) xxxx [XX.4 psi xxxxxxx v xxxxxxx X.28 nebyli ošetřeni xxxxx Xxxxxxxxxxxx multilocularis (11).]
Xxxxx xxxxxxxxxxxx nebo xxxxxxxx psa
Ošetření xxxxx xxxxxxxxxxx
Xxxxxxxxxx xxxxxxxxxxx xxxxx
Xxxxx x xxxxxxx xxxxxxxxx
Xxxxx [xx/xx/xxxx] a xxx xxxxxxxx [00:00]
Xxxxx (xxxxxxxx xxxxxx), xxxxxxx x xxxxxx
]]
Xxxxxxxx
x) Xxxx xxxxxxxxx xx xxxxxx xxx xxx (Xxxxx lupus xxxxxxxxxx), xxxxx (Xxxxx xxxxxxxxxx xxxxx) x xxxxxx (Xxxxxxx xxxxxxxx xxxx).
x) Xxxx osvědčení xxxxx 10 xxx xx xxxx xxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxx xx xx data xxxxxxxx xxxxxxx x xxxxxxxxxx x určeném xxxxx vstupu do Xxxx (x xxxxxxxxx xxx: http://ec.europa.eu/food/animal/liveanimals/pets/pointsentry_en.htm).
V případě xxxxxxx přepravy xx xxxx xxxxxx 10 xxx prodlužuje x xxxxxxxxx období odpovídající xxxxxx xxxxx po xxxx.
Xx účelem dalšího xxxxxxx xx xxxxxx xxxxxxxxx xxxxx xx xxxx osvědčení platné xx xxxx xxxxxxxx xxxxxxx a xxxxxxxxxx xx xxxx xxxxxx xxxx měsíců xxxx xx xxxx xxxxxxxx xxxxxxxxx xxxxxxxx proti xxxxxxxxx nebo do xxxx, než xxxxxxxxx xxxxxx podmínky xxxxxxxx xx zvířat xxxxxxxx 16 xxxxx xxxxxxxxx x bodě XX.3, xxxxx xxxx, která xxxxxxx xxxxxxx xxxxx. Xxxxxxx xxxxxx na xxxxxx, že některé xxxxxxx xxxxx informovaly x tom, že xxxxxx xxxxxx mladších 16 týdnů xxxxxxxxx x xxxx II.3 xx xxxxxx xxxxx xxxx xxxxxxx. Xxxx xxxxxxxxx naleznete xxx xxxx://xx.xxxxxx.xx/xxxx/xxxxxx/xxxxxxxxxxx/xxxx/xxxxx_xx.xxx.
Xxxx X:
Xxxxxxx X.5: Xxxxxxxx: xxxxxx xxxxxxx xxxx xxxxxxx xxxxxx.
Xxxxxxx X.28: Identifikační xxxxxx: xxxxxxx: transpondér xxxx xxxxxxxx.
Xxxxxxxxxxxxx xxxxx: xxxxxx xxxxxxxxxxxxx kód xxxxxxxxxxxx xxxx tetování.
Datum narození/plemeno: xxxxxxx xxxxxxxxx.

XXXX
Xxxxxxxxxx xxxxxxx xxx, koček xxxx xxxxxx x území xxxx xxxxx xxxx xx xxxxxxxxx xxxxx x xxxxxxx x xx. 5 xxxx. 1 a 2 xxxxxxxx (XX) x. 576/2013
XX. Zdravotní informace
II.a Xxxxx jednací xxxxxxxxx
XX.x
Xxxx XX:
(1) Uveďte xxxxx xxxxxxx.
(2) Xxxxxxxxxx xxxxxxx x xxxx II.1 xxxx být připojeno x xxxxxxxxx x xxxx xxx x xxxxxxx xx xxxxxx x xxxxxxxxxxx požadavky xxxxxxxxxxx x části 3 přílohy IV xxxxxxxxxxx nařízení (XX) x. 577/2013.
(3) Potvrzení xxxxxxx x xxxx XX.1 (např. xxxxxxx xxxxxxxxx, xxxxxxx) x x bodě II.2 (xxxx. xxxxxx x xxxxxx xx akci, xxxxx o xxxxxxxx) xx na xxxxxxxx xxxxxxxx xxxxxxxxxxx orgánu xxxxxxxxxxx xx kontroly xxxxxxx v xxxxxxx x) Poznámek.
(4) Xxxxx xxxxxxxxxxx musí být xxxxxxxxxx xx xxxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx.
(5) Xxxxxxxxxx xxxxxxx x xxxx II.3.2, xxxxx xx připojí k xxxxxxxxx, xx v xxxxxxx s xxxxxxxxx xx xxxxxx, xxxxxxxxx xxxxxx a xxxxxx xxxxxxxxxxx x xxxxx 1 x 3 xxxxxxx I xxxxxxxxxxx xxxxxxxx (EU) x. 577/2013.
(6) K osvědčení xx připojí xxxxxxx xxxxx xxxxxxxxxxxxxxx xxxxx x údajů o xxxxxxxx xxxxxxxxx xxxxxx.
(7) Xxxxx xxxxxxx podléhá xxxxxxxx, xx xxxxxxx xxxx xxxxxxx xxxxx xxxxxxx x xxxxxxx XX.1 předloží xx xxxxxxxx příslušných xxxxxx xxxxxxxxxxx xx xxxxxxxx xxxxxxx x bodě x) xxxxxxxxxx, xxxxx xxxxx, xx xxxxxxx xxxxxxxx xx styku xx zvířaty xxxxx xxxxxxxxx xx xxxxxxxxx x xx xxxx xxxxx tranzitu xxxx xxxxx xxxx třetí xxxx xxxx než xxxxxxx xx xxxxxxx x xxxxxxx XX xxxxxxxxxxx nařízení (XX) x. 577/2013 x xxxxxxxxx xxxxxxxxxx nebo x areálu xxxxxxxxxxxxx xxxxxxx xxxxxxxx zajištěna. Xxxxxxxxxx musí být x xxxxxxx s xxxxxxxxx xx xxxxxx, xxxxxxxxx xxxxxx x xxxxxx xxxxxxxxx x xxxxx 2 x 3 xxxxxxx X xxxxxxxxxxx xxxxxxxx (EU) x. 577/2013.
(8) Xxxxxxxxxxx xxxx prokazující xxxx xxxxxxxxxx proti vzteklině xxxxxxx v xxxx XX.3.1:
— xxxx xxx xxxxxxxx xx xxxxxx xxxxxxxxx veterinárním lékařem xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxx 30 xxx xx xxxx očkování x xxx měsíce xxxx xxxxx xxxxxx,
— xxxx xxx xxx x xxxx změřena xxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxxxxx x xxxxxxx rovné 0,5 XX/xx xxxx xxxxx,
— xxxx xxx xxxxxxxx x xxxxxxxxxx xxxxxxxxx v xxxxxxx x xxxxxxx 3 xxxxxxxxxx Xxxx 2000/258/XX (xxxxxx schválených xxxxxxxxxx x xxxxxxxxx zde: xxxx://xx.xxxxxx.xx/xxxx/xxxxxx/xxxxxxxxxxx/xxxx/xxxxxxxx_xx.xxx),
— xxxxxx xxx xxxxxxxx x xxxxxxx, xxxxx bylo xx xxxxxxxx xxxxxxxxxxxx výsledků xxxxx xxxxxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx.
X xxxxxxxxx xx připojí xxxxxxx xxxxx xxxxxxxx xxxxxxxxx schválené xxxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxx xxxxxxxxxx xxxxx vzteklině xxxxxxxxx x bodě XX.3.1.
(9) Potvrzením xxxxxx xxxxxxxx úřední xxxxxxxxxxx xxxxx xxxxxxxx, xx xxxxx xxxxx nejlepších xxxxxxxxxx x x xxxxxxx xxxxxxx se xxxxxxxxx laboratoře xxxxxxx x xxxxxxxxx ověřil xxxxxxx laboratorního xxxxxxxxx x výsledcích xxxxxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx x xxxx XX.3.1.
(10) Xx xxxxxxx x poznámkou xxx xxxxx (6) xxxx xxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxxx xxxx xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxx 3. červencem 2011 xxxx xxxxxx xxxxxxxx xx tohoto xxxxxxxxx xxxxxxx x xxxx xxxx předcházet xxxxxxxxxx očkování xxxx xxxxxxxx xxxxxxxx provedeným x těchto zvířat.
 Text obrazu
Text obrazu
ZEMĚ
Neobchodní xxxxxxx psů, xxxxx xxxx fretek z xxxxx xxxx xxxxx xxxx do xxxxxxxxx xxxxx x xxxxxxx x xx. 5 xxxx. 1 a 2 xxxxxxxx (EU) x. 576/2013
XX. Xxxxxxxxx xxxxxxxxx
XX.x Číslo jednací xxxxxxxxx
XX.x
(11) Ošetření proti Xxxxxxxxxxxx xxxxxxxxxxxxxx uvedené x xxxx II.4 xxxx:
— být xxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxx xx xxxx než 120 hodin a xx xxxx xxx 24 xxxxx xxxx xxxxxxxxxx xxxxxxx xxx xx jednoho x xxxxxxxxx xxxxx xxxx xx xxxxx x xxxxxx částí xxxxxxxxx xx seznamu x xxxxxxx X xxxxxxxx x přenesené xxxxxxxxx (XX) x. 1152/2011,
— xxxxxxxx x podání xxxxxxxxxxx léčivého xxxxxxxxx, xxxxx obsahuje xxxxxxx xxxxx xxxxxxxxxxxxx nebo xxxxxxxxxxxxxx xxxxxxxx látek, x xxxxx xxxx xxxxxxxxx, že xxxxxxxxxx xxxx v xxxxxxxxx xxxxxxx xxxxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxx Echinococcus xxxxxxxxxxxxxx x xxxxxxxx xxxxxxxxxxxx druhu.
(12) X xxxxxxxxxxx xxxxx o xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxx, xx xxxx xxxxxxxxx xxxxxxxxx, xxx xxxx plánovaným xxxxxxx do xxxxxxx x xxxxxxxxx xxxxx xxxx xxxxxx xxxxx xxxxxxxxx na xxxxxxx x xxxxxxx I xxxxxxxx v xxxxxxxxx xxxxxxxxx (XX) x. 1152/2011, xx xxxx xxxxxx xxxxxxx xxxxxxx x xxxx XX.4.
(13) X xxxxxxxxxxx údajů x xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxx, co xxxx osvědčení xxxxxxxxx, xx účelem xxxxxxx xxxxxxx xx jiných xxxxxxxxx států xxxxxxxxx x xxxx b) xxxxxxxx x xx xxxxxxx x xxxxxxxxx xxx čarou (11) xx xxxx xxxxxx xxxxxxx xxxxxxx x xxxx XX.4.
Xxxxxx xxxxxxxxxxx xxxxx/xxxxxxxxx xxxxxxxxxxx xxxxx
Xxxxx (xxxxxxxx písmem): Kvalifikace x xxxxx:
Xxxxxx:
Xxxxxxxxx xxxxx:
Xxxxx: Xxxxxx:
Xxxxxxx:
Xxxxxxxxx xxxxxxxxxx xxxxxxx (xxxxxxxxxx xx, xxxxx xx osvědčení xxxxxxxxx xxxxxxx veterinárním xxxxxxx)
Xxxxx (xxxxxxxx písmem): Kvalifikace x xxxxx:
Xxxxxx:
Xxxxxxxxx xxxxx:
Xxxxx: Xxxxxx:
Xxxxxxx:
Xxxxxxx x xxxxx xxxxxx (xx xxxxxx xxxxxxx přesunů xx xxxxxx xxxxxxxxx států)
Jméno (xxxxxxxx xxxxxx): Titul:
Adresa:
Telefonní xxxxx:
X-xxxxxxx xxxxxx:
Xxxxx xxxxxxxxx xxxxxxxx xxxxxxx x xxxxxxxxxx: Xxxxxx: Xxxxxxx:


