NAŘÍZENÍ KOMISE (XX) x.&xxxx;429/2008
xx xxx 25.&xxxx;xxxxx 2008
x&xxxx;xxxxxxxxxxx pravidlech x&xxxx;xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady (XX) x.&xxxx;1831/2003, pokud xxx x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx a povolování xxxxxxxxxxx xxxxx
(Xxxx s významem xxx XXX)
XXXXXX XXXXXXXXXX XXXXXXXXXXXX,
x&xxxx;xxxxxxx xx Smlouvu x&xxxx;xxxxxxxx Xxxxxxxxxx společenství,
s ohledem xx xxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx (ES) x.&xxxx;1831/2003 ze xxx 22.&xxxx;xxxx 2003 x&xxxx;xxxxxxxxxxx xxxxxxx xxxxxxxxxxx ve xxxxxx zvířat (1), x&xxxx;xxxxxxx xx čl. 7 odst. 4 x&xxxx;5 uvedeného xxxxxxxx,
xx xxxxxxxxxx s Evropským xxxxxx xxx xxxxxxxxxx potravin x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;7 xxxx.&xxxx;4 x&xxxx;5 xxxxxxxx (XX) x.&xxxx;1831/2003,
xxxxxxxx k těmto xxxxxxx:
|
(1) |
Xx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx, xxxxx jde x&xxxx;xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx podle xxxxxxxx (XX) č. 1831/2003, xxxxxx xxxxxxxx xxx vypracování x&xxxx;xxxxxxxx žádostí a vyhodnocování x&xxxx;xxxxxxxxxx těchto xxxxxxxxxxx xxxxx. Tato xxxxxxxx xxxx nahradit xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxx Xxxx 87/153/XXX (2), kterou xx xxxxxxx xxxxxx zásady xxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxx xx xxxxxx xxxxxx. |
|
(2) |
Xxxx xxxxxxxx by xxxx xxxxxxxx xxxxxxxxx, xxxxx musí xxxxxxxx xxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx. Xxxx xx zejména xxxxx xxxxxxx xxxxx, xxxxx mají být xxxxxxxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx, x&xxxx;xxxxxx, jež xxxx xxx xxxxxxxxxx x&xxxx;xxxxx xxxxxxxx xxxx xxxxxxxx x&xxxx;xxxxxxxxxx pro xxxxxxx, xxxxxxx a životní xxxxxxxxx xx xxxxxx xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxx Xxxxxxxxx xxxxxx xxx xxxxxxxxxx potravin (dále xxx „xxxx“). |
|
(3) |
Xxxxx povahy xxxxxxxxx xxxxx xxxx xxxxxxxxxxxx podmínek xxx xxxxx xx xxxx xxxxxx studií potřebných x&xxxx;xxxxxxxxxxx jejích vlastností x&xxxx;xxxxxx xxxxx. Xxxxxxxx xx xxxxx měly xxx xxxxxxx postupovat x&xxxx;xxxxxxx xxxxxxxxx, pokud xxx x&xxxx;xxxx xxxxxx x&xxxx;xxxxxxxxx, jež mají xxx xxxxxxxxxx k prokázání xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxx xxxxxxxxx xxxxx. Subjekty, xxxxx xxxxxxx této xxxxxxxxx, xx xxxx x&xxxx;xxxxxxxxxxx xxxx xxxxx xxxxxxxxx. |
|
(4) |
Xxxx xx xxx xxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx, xxx mohl xxxxx, xxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxx pro xxxxxxxx xxxxx článku 5 xxxxxxxx (ES) x.&xxxx;1831/2003. |
|
(5) |
Xx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx kvality při xxxxxxxxxxxxx dokumentace pro xxxxxxxxx xxxxx xxxxxx x&xxxx;xxxxxxx v krmivu (xxxxxxxx) xxxx xxxx, aby xxxx xxxxxxxxx, xx xxxxxxxx xxxxxxxxxxxxx zkoušek xxxxxx xxxxxxxxxxx. |
|
(6) |
X&xxxx;xxxxxxx xxxxxxxx xx xxxx být xxxxxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxxx kategorie xxxxxxxxxxx xxxxx uvedené x&xxxx;xx.&xxxx;6 odst. 1 nařízení (XX) č. 1831/2003. |
|
(7) |
S cílem podnítit xxxxx x&xxxx;xxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx bezpečnosti xx xxxx být xxxxxxxxx zvláštní xxxxxxxx xxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxx xx xxxxxxxxxxx xxxxxxx xx xxxxx xxxxxxxxx. |
|
(8) |
Xxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxx o povolení xx xxxx xxxx x&xxxx;xxxxx xxxxx požadavky xx zvířata určená x&xxxx;xxxxxxxx xxxxxxxx a ostatní xxxxxxx, xxx xxx xxxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxx xxxxxxx jako spotřebitele xxxxxx důležité. |
|
(9) |
Využití xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxx či xxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxx xx xxxxxxxxx xxxxx směrnice Xxxx 86/609/XXX ze dne 24.&xxxx;xxxxxxxxx 1986 x&xxxx;xxxxxxxxxx xxxxxxxx a správních xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxx xxx xxxxxxx x&xxxx;xxxx xxxxxxx xxxxx (3) xx mělo xxx xxxxxxxxx. |
|
(10) |
Xxx xx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx, xxxx by xxx xxxxxxxxx zjednodušené postupy xxx xxxxxxxxxx xxxxxxxxxxx xxxxx, které xxx xxxx povoleny xxx xxxxxxx v potravinách. |
|
(11) |
Co se xxxx xxxxxxxxxxx xxxxx, xxxxx xxxx xxxxx xxxxxxxx Rady 70/524/XXX (4) xxxxxxxx xxx xxxxxxxx xxxxxxx, měla by xxx popřípadě stanovena xxxxxxx, aby x&xxxx;xxxxxxx, xx xxxxxx k dispozici xxxxx xxxxxx, žadatel xxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxx, xxxxx xxxx k dispozici k prokázání xxxxxxxxx, xxxxxxx xxxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxxx používání dotyčné xxxxxxxxx látky. |
|
(12) |
Je xxxxx xxxxxxxx pravidla xxx xxxxxxx x&xxxx;xxxxx xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;13 xxxx.&xxxx;3 xxxxxxxx (XX) x.&xxxx;1831/2003. |
|
(13) |
Xx xxxxx xxxxxxxx xxxxxx xxxxxxxx pro xxxxxxx x&xxxx;xxxxxxxx xxxxxxxx podle xxxxxx&xxxx;14 xxxxxxxx (XX) x.&xxxx;1831/2003. |
|
(14) |
Xx xx týká xxxxxxxxxx x&xxxx;xxxxxxxx bezpečnosti x&xxxx;xxxxxxxxx, jež je xxxxx xxxxxxx xx xxxxxxx xxxxxxx, je xxxxxxxx stanovit xxxxxxxxx xxxxxx, během něhož xx xxxxx nadále xxxxxxxx stávající xxxxxxxx. X&xxxx;xxxxxxxx xxxxxxxx xxxx xxxxxxx tohoto nařízení x&xxxx;xxxxxxxx by se xxxx x&xxxx;xxxxxx xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxx xxxxxxxx 87/153/XXX. Xxxxx xxx x&xxxx;xxxxxxx xxxxxx xxxxx xxxxxxxx období xx xxxxxx x&xxxx;xxxxxxxx, žadatelé xx vzhledem x&xxxx;xxxxxx xxxx xxxxxxxx xxx xxxxxxx xxxxxx měli xxx možnost xxxxxx xxxx pravidly stanovenými x&xxxx;xxxxx nařízení x&xxxx;xxxxxxxx xxxxxxxx 87/153/EHS. Prováděcí xxxxxxxx byla vypracována xx xxxxxxx současných xxxxxxxxx x&xxxx;xxxxxxxxxxx poznatků x&xxxx;x&xxxx;xxxxxxx nutnosti by xxxx být přizpůsobena xxxxxxxxxx xxxxxx xxxxxx x&xxxx;xxxx xxxxxxx. |
|
(15) |
Xxxxxxxx xxxxxx xxxxxxxx xxxx x&xxxx;xxxxxxx xx xxxxxxxxxxx Stálého xxxxxx xxx potravinový xxxxxxx a zdraví xxxxxx, |
XXXXXXX XXXX NAŘÍZENÍ:
Xxxxxx 1
Xxxxxxxx
Xxx xxxxx xxxxxx xxxxxxxx xx xxxxxxx xxxx xxxxxxxx:
|
1. |
„xxxxxxx v zájmovém xxxxx a ostatními xxxxxxx, xxxxx xxxxxx určena x xxxxxxxx potravin“ xx xxxxxx xxxxxxx xxxxx, xxx xxxx obyčejně xxxxxx, xxxxxxx xxxx xxxxxx xxxxxxxx, xxxxxx xxxx xxxxxx pro xxxxxxx xxxxxxxx, xxxxx xxxx; |
|
2. |
„xxxxxxxxxxx druhy“ xx xxxxxx xxxxxxx xxxxxx x xxxxxxxx xxxxxxxx xxxx xxx xxxx (zvířata xxxxxxx xxx xxxxx x xxxx, včetně telat), xxxx (xxxxxxx xxxxxxx xxx xxxx), xxxxxxx, xxxxxx (xxxxxx xxxxxx), xxxxx x xxxx xxxxx Xxxxxxxxxx. |
Xxxxxx 2
Xxxxxx
1. Xxxxxx x xxxxxxxx xxxxxxxxx xxxxx xxxxx xxxxxx 7 xxxxxxxx (XX) č. 1831/2003 xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxx X.
X xxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxx xxxxxx 3 (xxxx xxx „xxxxxxxxxxx“), xxxxx xxxxxxxx xxxxx x xxxxxxxxx xxxxxxx x xx. 7 xxxx. 3 xxxxxxxx (ES) x. 1831/2003.
2. Pokud xxxxxxx v souladu x xxxxxxx 18 xxxxxxxx (XX) x. 1831/2003 xxxxxxxx, aby xx x xxxxxxxxx částmi dokumentace xxxxx odstavce 1 xxxxxxxxx xxxx x xxxxxxxxx xxxxx, xxxxxxxx xxx každý xxxxxxxx xxxx xxxx xxxxxxxxx xxxxxxxxxx odůvodnění, xx zveřejnění xxxxxx xxxxxxxxx xx xxxxx xxxxxxxx poškodit xxxx xxxxxxxxx vůči konkurentům. Xxxxxxx xxxxx dokumentace xxxx xxx xxxxxxxxxx xxxxxxxx xx xxxxxx xxxxxxxxxxx x xxxxx xxx xxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxx xx. 7 odst. 3 xxxx. x) xxxxxxxx (XX) č. 1831/2003. Xxxxxxx xxxxx Xxxxxx xxxxx xxxxx xxxxxxxxxxx, x xxxxx xx xxx xxxxxxxxx xxxx x xxxxxxxxx xxxxx, x xxxxxxxxxxx xxxxxxxxxx.
Xxxxxx 3
Xxxxxxxxxxx
1. Xxxxxxxxxxx přiměřeně a dostatečně xxxxxxxxx, xx xxxxxxxxx xxxxx xxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxxx x xxxxxx 5 xxxxxxxx (XX) x. 1831/2003.
2. Xxxxxx požadavky na xxxxxxxxxxx x xxxxxxx xxxxxxxxxxx xxxx stanoveny x xxxxxxx XX.
Xxxxxxxx xxxxxxxxx, xxx xxxxxxxxxxx xxxx splňovat x xxxxxxxx xxxxxxx, xxxx stanoveny x xxxxxxx XXX.
Xxxxxxxxx xxxx trvání xxxxxxxxxxxx studií xx xxxxxxxxx v příloze IV.
3. Xxxxxxxx xx xxxxxxxx 2 xxxx xxxxxxx xxxxxxxxx dokumentaci, xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx 2, xxxxx xxxxx xxxxx, xxxx tyto xxxxxxxxx xxxxxxxxx, xxxxxxxx.
Xxxxxx 4
Xxxxxxxxx xxxxxxxx
1. Xx žádosti x xxxxxxxx xxxxxx xxxx xxxxx xxxxxx xxxxxx xxxxxxxx x xxxxxxxx xx xxxxxx xxxxxxxx xxxxxxx xxxxxxxx 87/153/XXX.
2. X xxxxxxx x xxxxxxxx xxxxxxxx xxxx 11. xxxxxxx 2009 xx xxxxx xxxxxxxx xxxxxxxxxx, xx xxxxx nadále používat xxxxxx XXX x XX částí I a II xxxxxxx xxxxxxxx 87/153/XXX xxxxx xxxx 1.3, 1.4, 2.1.3, 2.1.4, 2.2.3, 2.2.4, 3.3, 3.4, 4.1.3, 4.1.4, 4.2.3, 4.2.4, 5.3, 5.4, 6.3, 6.4, 7.3, 7.4, 8.3 a 8.4 xxxxxxx XXX x xxxxx xxxxxxxxxx xx xxxxxxx „Minimální doba xxxxxx dlouhodobých xxxxxx xxxxxxxxx“ v tabulkách přílohy IV.
Xxxxxx 5
Xxxxx x xxxxxxxx
Toto xxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx xxxx xx xxxxxxxxx x Xxxxxxx věstníku Evropské xxxx.
Xxxx xxxxxxxx je xxxxxxx x xxxxx xxxxxxx x xxxxx xxxxxxxxxx xx xxxxx xxxxxxxxx státech.
V Bruselu xxx 25. dubna 2008.
Xx Xxxxxx
Xxxxxxxxx XXXXXXXXX
xxxxxx Xxxxxx
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;268, 18.10.2003, x.&xxxx;29. Xxxxxxxx xx xxxxx xxxxxxxx Komise (XX) x.&xxxx;378/2005 (Xx.&xxxx;xxxx. X&xxxx;268, 18.10.2003, s. 29).
(2)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;64, 7.3.1987, x.&xxxx;19. Xxxxxxx xxxxxxxxx (XX) č. 1831/2003.
(3)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;358, 18.12.1986, x.&xxxx;1; xxxxxxxx xxxxx x&xxxx;Xx.&xxxx;xxxx. X&xxxx;358, 18.12.1986, x.&xxxx;1. Xxxxxxxx xx xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx 2003/65/XX (Xx.&xxxx;xxxx. X&xxxx;358, 18.12.1986, x.&xxxx;1).
(4)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;270, 14.12.1970, x.&xxxx;1. Směrnice xxxxxxxxx xxxxxxxxx xxxxxxxxx Komise (XX) x.&xxxx;1800/2004 (Úř. věst. X&xxxx;270, 14.12.1970, x.&xxxx;1).
XXXXXXX&xxxx;X
XXXXXXXX ŽÁDOSTI XXXXXXX X&xxxx;XX.&xxxx;2 XXXX.&xxxx;1&xxxx;X&xxxx;XXXXXXX XXXXX
1.&xxxx;&xxxx;&xxxx;XXXXXXXX XXXXXXX
XXXXXXXX XXXXXX
XXXXXXXXX ŘEDITELSTVÍ
PRO XXXXXX X&xxxx;XXXXXXX XXXXXXXXXXXX
(Xxxxxx)
Xxxxx: …
|
Xxx |
: |
Xxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxx xxxxx xxxxxxxx (XX) č. 1831/2003. |
|
◻ |
Povolení xxxxxxxxx xxxxx xxxx nové xxxxx xxxxxxxxx xxxxx (xx.&xxxx;4 xxxx.&xxxx;1 nařízení (XX) x.&xxxx;1831/2003) |
|
◻ |
Xxxxxxxx existujícího xxxxxxxx (čl. 10 xxxx.&xxxx;2 xxxx&xxxx;7 xxxxxxxx (XX) x.&xxxx;1831/2003) |
|
◻ |
Xxxxx xxxxxxxxxxx povolení (xx.&xxxx;13 xxxx.&xxxx;3 nařízení (XX) č. 1831/2003) |
|
◻ |
Obnovení xxxxxxxx xxxxxxxxx látky (xxxxxx&xxxx;14 xxxxxxxx (ES) x.&xxxx;1831/2003) |
|
◻ |
Xxxxxxxx x&xxxx;xxxxxxxxxx případech (článek 15 xxxxxxxx (ES) č. 1831/2003) |
(Označte xxxxxxxxxxx xxxxxxxxxxx jednoho x&xxxx;xxxxxxx)
Xxxxxxx(x)&xxxx;x/xxxx jeho/jejich zástupce(i) ve Xxxxxxxxxxxx (xx.&xxxx;4 xxxx.&xxxx;3 xxxxxxxx (XX) x.&xxxx;1831/2003) xx xxxxxxxx uvedených x&xxxx;xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003 (xxxxx, xxxxxx ….)
…
…
podává (xxxxxxxx) xxxx xxxxxx za xxxxxx xxxxxxx povolení xxx xxxxxxxxxxx produkt xxxxxxx xxxxxxxxxx látku:
1.1 Identifikace x&xxxx;xxxxxxxxxxxxxxx xxxxxxxxx látky
Název xxxxxxxxx xxxxx (charakteristika xxxxxx látky (xxxxx) xxxx xxxxxxx (xxxxxxx), xxx xx xxxxxxxx x&xxxx;xxxxxx&xxxx;2.2.1.1 x&xxxx;2.2.1.2 xxxxxxx&xxxx;XX):
…
…
Xxxxxxxx xxxxx (xx-xx xx xxxxxx x&xxxx;xxxxxxxx vázaných xx xxxxxxxx):
…
…
X&xxxx;xxxxxxxxx/xxxxxxxxxxx a funkční xxxxxxx/xxxxxxxxx doplňkových xxxxx&xxxx;(1) (xxxxxx):
…
…
Xxxxxx xxxxx zvířat:
…
…
…
Jméno xxxxxxxx povolení (xx.&xxxx;9 xxxx.&xxxx;6 nařízení (XX) x.&xxxx;1831/2003):
…
…
Xxxx xxxxxxxxx xxxxx xxx xxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx o krmivech xxxxxxxx.……/…/X(X)X&xxxx;xxxx nařízením (XX) x.&xxxx;…/… pod xxxxxx … jako (kategorie xxxxxxxxxxx látek)
…
Tato doplňková xxxxx xxx xxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxx směrnicí .…/…/E(H)S nebo xxxxxxxxx (XX) x.&xxxx;…/… xxx xxxxxx … xxxx
…
xxx použití v
…
Pokud xx xxxxxxx xxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxx xxxx xxxxxxxxx xxxxxxxx xx xx x&xxxx;xxxx xxxxxxx, uveďte xxxx xxxxxxxxx:
|
◻ |
xxxxxxxxxxx xxxxxxxxxxxxx xxx (nařízení Xxxxxx (XX) č. 65/2004 (2)) (xx-xx xx xxxxxx): … |
|
◻ |
xxxxx o případném xxxxxxxx xxxxxxxx v souladu x&xxxx;xxxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) č. 1829/2003 (3): … |
|
◻ |
nebo xxxxx x&xxxx;xxxxx xxxxxxxxxx xxxxxxx o povolení podle xxxxxxxx (ES) x.&xxxx;1829/2003: … |
1.2&xxxx;&xxxx;&xxxx;Xxxxxxxx xxx xxxxx
1.2.1&xxxx;&xxxx;&xxxx;Xxxxxxx v kompletních xxxxxxxx
Xxxx xxxx xxxxxxxxx xxxxxx:
…
…
Xxxxxxxxx stáří xxxx xxxxxxxx:
…
…
Xxxxxxxxx xxxxx (je-li xx vhodné): xx xxxx xxxxxxxx xxxxxxxx&xxxx;(4) xxxx xxxxxxxx xxxxxxx xxxxxxx (CFU) nebo xx/xx kompletního xxxxxx x&xxxx;xxxxxx xxxx 12&xxxx;%
…
…
Xxxxxxxxx xxxxx (xx-xx to xxxxxx): xx xxxx xxxxxxxx xxxxxxxx xxxx XXX nebo xx/xx xxxxxxxxxxx krmiva x&xxxx;xxxxxx xxxx 12&xxxx;%
…
…
X&xxxx;xxxxxxxx xxxxx xx xxxxx xxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxx xx litr.
1.2.2 Použití xx xxxx
Xxxxxxxxx xxxxx (xx-xx xx vhodné): xx xxxx xxxxxxxx aktivity xxxx XXX nebo xx/x&xxxx;xxxx
…
…
Xxxxxxxxx xxxxx (je-li xx vhodné): mg xxxx xxxxxxxx xxxxxxxx xxxx XXX xxxx xx/x&xxxx;xxxx
…
…
1.2.3&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxx pro xxxxx (xx-xx to xxxxxx)
Xxxx xxxx kategorie xxxxxx:
…
…
Xxxxxxxxx stáří:
…
…
Minimální dávka (xx-xx xx xxxxxx): xx xxxx xxxxxxxx xxxxxxxx xxxx XXX/xx xxxxxxxxxxx krmiva x&xxxx;xxxxxx xxxx 12&xxxx;%
…
…
Xxxxxxxxx xxxxx (xx-xx xx vhodné): xx xxxx jednotky xxxxxxxx xxxx XXX/xx xxxxxxxxxxx xxxxxx x&xxxx;xxxxxx xxxx 12&xxxx;%
…
…
X&xxxx;xxxxxxxx xxxxx xx možno uvést xxxxxxxxx x&xxxx;xxxxxxxxx xxxxx xx xxxx.
Xxxxxxxx xxxx xxxxxxx použití (xx-xx xx xxxxxx):
…
…
…
Xxxxxxxx podmínky xxxx xxxxxxx xxx xxxxxxxxxx (xx-xx xx xxxxxx):
…
…
…
…
Xxxxxxxxx xxxxx reziduí (xx-xx to xxxxxx):
Xxxx xxxx kategorie xxxxxx:
…
…
Xxxxxxxxxxxx xxxxxxxx:
…
…
Xxxxxx xxxxx xxxx xxxxxxxx:
…
…
…
Xxxxxxxxx xxxxxxxx v tkáních xxxx xxxxxxxxxx (μx/xx):
…
…
…
Xxxxxxxx xxxxx:
…
1.3&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxxx
Xxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx Společenství (xx-xx xx xxxxxx):
…
Xxxxx xxxxxx / xxxxx xxxxx:
…
Xxxxx xxxxxx:
…
Xxxxx xxxxxxxxx xxxxxxxxxxxx:
…
Xxxxxxxxxxx:
…
Xxxxxxxx:
…
Xxxxxxx xxxxx:
…
Xxxxx xxxxx:
…
Xxxxxxxxx xx skladování:
…
1.4 Požadovaná změna (xx-xx to vhodné)
…
…
…
…
Kopie xxxx žádosti xxxx xxxxxxx xxxxx úřadu x&xxxx;xxxxxxxxxxx a referenční laboratoři Xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxx.
Xxxxxx …
1.5&xxxx;&xxxx;&xxxx;Xxxxxxx:
|
◻ |
xxxxx xxxxxxxxxxx (xxxxx xxx úřad), |
|
◻ |
veřejný souhrn xxxxxxxxxxx, |
|
◻ |
xxxxxxxx shrnutí xxxxxxxxxxx, |
|
◻ |
xxxxxx xxxxx dokumentace, x&xxxx;xxxxx xx být xxxxxxxxx xxxx s důvěrnými xxxxx, x&xxxx;xxxxx xxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxx (xxxxx xxx Xxxxxx x&xxxx;xxxx), |
|
◻ |
xxxxx xxxxxxxxx xxxxx xxxxxxxx(x), |
|
◻ |
xxx xxxxxx xxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx xxxxx xx.&xxxx;7 xxxx.&xxxx;3 písm. f) nařízení (ES) x.&xxxx;1831 / 2003 (xxxxx pro xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx), |
|
◻ |
xxxx s údaji x&xxxx;xxxxxxxxxxx materiálu (xxxxx xxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx), |
|
◻ |
xxxxxxxxx x&xxxx;xxxxxxxxxxxx a analýze (xxxxx xxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx) a |
|
◻ |
potvrzení x&xxxx;xxxxxxxx poplatku xxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx (xxxxxx&xxxx;4 xxxxxxxx (XX) x.&xxxx;378/2005&xxxx;(5). |
Xxxxxxx příslušné části xxxxxxxxx x&xxxx;xxxxxxxx xx xxxxx xxxxxxxx. Xxxxxxxx xxxxxxxxx xxxxxxx (s ostatními xxxxxxxxxxxx xxxxxxxxx) xxxxxxx xxxxx Xxxxxxxx xxxxxx.
2.&xxxx;&xxxx;&xxxx;XXXXXXX XXXXX XXXXXXXX(X)
Xxxxxxxxx xxxxx xxx předložení xxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxx xxxxx xxxxxxxx (XX) x.&xxxx;1831/2003
|
1. |
Xxxxxxxxxx xxxx osoba, xxxxx xxxxxx xxxxxx
|
|
2. |
Xxxxxxxxx osoba (xxx xxxxxxxx korespondenci x&xxxx;Xxxxxx, xxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx)
|
(1)&xxxx;&xxxx;X&xxxx;xxxxxxx xxxxxxx „xxxx xxxxxxxxxxxx xxxxxxxxx xxxxx“ v kategorii xxxxxxxxxxxx doplňkové xxxxx xx xxxxx xxxxxxxxxxx xxxxxxx, xxxxx funkci xx xxxxxxxxx xxxxx xxx.
(2)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;10, 16.1.2004, x.&xxxx;5.
(3)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;268, 18.10.2003, x.&xxxx;1. Xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx (XX) x.&xxxx;298/2008 (Úř. věst. X&xxxx;268, 18.10.2003, x.&xxxx;1).
(4)&xxxx;&xxxx;Xxxxxxxx „xxxxxxxx“ xxxxxxxx žadatel.
(5) Nařízení Xxxxxx (XX) x.&xxxx;378/2005 ze xxx 4.&xxxx;xxxxxx 2005 x&xxxx;xxxxxxxxxx xxxxxxxxxxx pravidlech x&xxxx;xxxxxxxx Evropského parlamentu x&xxxx;Xxxx (ES) x.&xxxx;1831/2003, xxxxx xxx x&xxxx;xxxxxxxxxx x&xxxx;xxxxx xxxxxxxxxx laboratoře Xxxxxxxxxxxx v souvislosti s žádostmi x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxx (Xx.&xxxx;xxxx. L 59, 5.3.2005, x.&xxxx;8). Xxxxxxxx xx znění xxxxxxxx (XX) x.&xxxx;850/2007 (Xx.&xxxx;xxxx. X&xxxx;59, 5.3.2005, x.&xxxx;8).
PŘÍLOHA II
OBECNÉ XXXXXXXXX, XXX XXXX XXXXXXXX DOKUMENTACE XXXXX ČLÁNKU 3
OBECNÁ XXXXXXXXXX
Xxxx xxxxxxx stanoví požadavky xx vypracování xxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxx a informace x&xxxx;xxxxxxx, mikroorganismech a přípravcích, xxx xxxx být xxxxxxxxxx s dokumentací xxxxx xxxxxx&xxxx;7 nařízení (XX) x.&xxxx;1831/2003 pro:
|
— |
povolení nové xxxxxxxxx xxxxx, |
|
— |
xxxxxxxx nového xxxxx xxxxxxxxx látky, |
|
— |
změnu xxxxxxxxxxx povolení xxxxxxxxx xxxxx xxxx |
|
— |
xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx. |
Xxxxxxxxxxx musí xxxxxxx vyhodnocení doplňkových xxxxx na základě xxxxxxxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxx, xx xxxx xxxxxxxxx látky xxxxxxxxxx xxxxxxxxx zásadám xxx xxxxxx povolení, které xxxx stanoveny x&xxxx;xxxxxx&xxxx;5 xxxxxxxx (XX) č. 1831/2003.
Studie, xxx xxxx xxx xxxxxxxxxx, x&xxxx;xxxxxx xxxxxx xxxx xxxxxxx xx xxxxxx xxxxxxxxx látky, xxxxxxxxx xxxx funkční xxxxxxx, druhu xxxxxxxx (xxxxxxxx, xxxxx xxxx xxxxxx na xxxxxxxx; xxxxxxxx xxxxxx xx xxxxxxxx), samotné xxxxx, xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxx xxxxx. Žadatel xxxxxx xx xxxx xxxxxxx x&xxxx;xxxxxxx&xxxx;XXX, xxx xxxx možno xxxxxxxx, xxxxx xxxxxx x&xxxx;xxxxxxxxx xxxx být xxxxxxxx xx xxxxxxx xxxxxxxxxx.
Xxxxxxx xxxxxxxxxxx xxxxx xxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxx nebo xxxxxxxxx xx xx xxxxxxxxxxx xxxxxxxxxx v této příloze, xxxxxxx&xxxx;XXX x&xxxx;xxxxxxx&xxxx;XX.
Xxxxxxxxxxx xxxx xxxxxxxxx podrobné zprávy x&xxxx;xxxxx xxxxxxxxxxx xxxxxxxx, xxxxxxxxxx v souladu xx xxxxxxxx číslování navrženým x&xxxx;xxxx příloze. Dokumentace xxxx xxxxxxxxx odkazy x&xxxx;xxxxx xxxxx zveřejněných xxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxx xxxxxxxxx příslušných xxxxxxxxxx, xxxxx xxx xxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxx xxxx tyto xxxxxx xxx vyhodnoceny xxxxxxxxx xxxxxxxx institucí xxxxx xxxxxxxx xxxxxxxx xxxxxxxx xx Xxxxxxxxxxxx, postačuje xxxxx na výsledek xxxxxxxxx. Údaje xx xxxxxx, xxxxx xxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxx xxxxx, nebo xxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx xx xxxx jednoznačně xxxxxxxxx na xxxxxxx xxxxxxxxxx xxxxx jako xxxxx, xxxxx xx xxxxxxxxx xxxxxxx x&xxxx;xxxxxxxx.
Xxxxxx, xxxxxx studií, xxxxx xxxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxx xxxxx xxxx xxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx, musí xxx xxxxxxxxx a zdokumentovány xxxxx xxxxxxxxxxx xxxxx xxxxxxx (xxxx. xxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx 2004/10/XX xx xxx 11.&xxxx;xxxxx 2004 x&xxxx;xxxxxxxxxxx xxxxxxxx a správních xxxxxxxx xxxxxxxxxx se xxxxxxxxx xxxxx správné xxxxxxxxxxx praxe a ověřování xxxxxx xxxxxxxxx xxx xxxxxxxxx chemických látek (1) xxxx Xxxxxxxxxxx xxxxxxxxxx xxx normalizaci (XXX).
Xxxxx xx xxxxxx in xxxx xxxx xx xxxxx xxxxxxxxx xxxx Xxxxxxxxxxxx, xxxxxxx musí xxxxxxxx, že dotyčná xxxxxxxx xxxxxxxx zásady xxxxxxx xxxxxxxxxxx xxxxx Xxxxxxxxxx xxx xxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxx (XXXX) xxxx xxxxx XXX.
Xxxxxxxxx-xxxxxxxx, xxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx xxxxxxxxxx xx xxxx xxxxx xxxxx xxxxxxxxxxx xxxxxxxx Xxxx 67/548/XXX xx xxx 27. června 1967 x&xxxx;xxxxxxxxxx právních a správních xxxxxxxx xxxxxxxxxx xx xxxxxxxxxxx, xxxxxx a označování xxxxxxxxxxxx xxxxx&xxxx;(2), naposledy xxxxxxxxxx směrnicí Xxxxxx 2004/73/XX&xxxx;(3), xxxx xxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx. Xxxxxxx jiných metod xxxx xxx xxxxxxxxxx.
Xx xxxxx podporovat xxxxxxxxx xxxxx in vitro xxxx xxxxx xxxxxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxx xxxxx xxxxxxxxx x&xxxx;xxxxxx xxxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxxx xxxxx zvířat xxxxxxxxx xxx xxxxxx xxxxxxx. Xxxx xxxxxx xxxx xxxxxxx xxxxxxx x&xxxx;xxxxxxxxx xxxxxxx xxxxxx xxxxxxx jako xxxxxx, xxxxxx xxxx xxxxxxxx.
Xxxxx xxxxx xxxxxxx x&xxxx;xxxxxxxx xxxx xx xxxx xxxx být x&xxxx;xxxxxxx x&xxxx;xxxxxxxx správné xxxxxxxxxxx xxxxx xxxxxxxxxxx xx xxxxxxxx 2004/10/ES x/xxxx xxxxx XX XXX/XXX 17025. Xxxx metody xxxxxxxx xxxxxxxxxx stanoveným x&xxxx;xxxxxx&xxxx;11 xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) x.&xxxx;882/2004 xx dne 29.&xxxx;xxxxx 2004 x&xxxx;xxxxxxxx xxxxxxxxxx za xxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx týkajících xx xxxxx x&xxxx;xxxxxxxx a pravidel x&xxxx;xxxxxx xxxxxx a dobrých xxxxxxxxx xxxxxxxxxx xxxxxx&xxxx;(4).
Xxxxx xxxxxxxxxxx musí xxxxxxxxx xxxxxxx souhrn a podrobné xxxxxxx xxxxxxx, xxx xxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx.
Xxxxx dokumentace xxxxxxxx xxxxx xxxxx xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx xx xxx, xxxxx xx xxxxxxxx xxxxx čl. 7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (ES) č. 1831/2003, x&xxxx;xxxxx xx xxxxxxxxxx xxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
Xxxxxxxxx xxxxxxxxxxx
Xxxx posouzení xx xxxxxxxx xx studiích, xxxxx mají xxxxxxxx xxxxxxxx používání doplňkové xxxxx ve xxxxxx x:
|
x) |
xxxxxxx xxxxxx xxx xxxxxxxxxx navrhovaných obsazích xxx xxxxxxxxxxx xx xxxxx xxxx vody x&xxxx;xxx xxxxxxx xxxxxx xxxxxx xxx xxxxxxxxx xxxxxxx xxx xxxxxxxxxx; |
|
x) |
xxxxxxxxxxxxx, xxxxx xxxxxxxx potravinářské xxxxxxx xxxxxxx ze xxxxxx xxxxxxxxxxxxx doplňkovou xxxxx, xxxx rezidua xxxx metabolity. V tomto xxxxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx (MLR) x&xxxx;xxxxxxxxxx xxxx xx xxxxxxx xxxxxxxxxx xxxxx xxxxx (XXX) xxxx xxxxxxxx xxxxxxxx dávky (XX); |
|
x) |
xxxxxx, xxxxx xxxxx xxxxxxxxxxxxx vystaveny doplňkové xxxxx xxxxxxxxxx nebo xxxxxxxxx xxxxxxxx, xxx xx xxxx xxx xxxxxxxxxx s doplňkovou xxxxxx xxxx takovou xxxx xxx xxxxx xxxxxxxxxxxxx xx xxxxxxx nebo xxxxxxxxxxx xxxxx xxxx xxxx xx při xxxxxxxxx xxxxxx xxxx xxxx, které obsahují xxxxxxxx doplňkovou xxxxx; |
|
x) |
xxxxxxxx x&xxxx;xxxxxxx xxxxxxxx vzhledem x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx genů xxxxxxxxxxxxx xxxx xxxxxxxxxxxxxxxx xxxxxx x |
|
x) |
xxxxxxxxx prostředí, x&xxxx;xxxxxxx xx xxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx látky xxxxxxx xxxx produktů x&xxxx;xx odvozených, xx xx xxxxx x/xxxx xxxxxxxxxxx xxxxxxx. |
Xxxxx xx xxxxxxxxx xxxxx více xxxxxx, každá xxxxxx xxxx xxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx pro xxxxxxxxxxxx samostatně a posléze xxxxxxxxxxx s ohledem xx xxxxxxxxxxx xxxxxx (xxx-xx xxxxxxxx, xx xxxx xxxxxxxx xxxxxxxxx k vzájemnému xxxxxxxx). Xxxxxxxxxxxx je xxxxx posoudit xxxxxxxxx xxxxx.
Xxxxxxxxx účinnosti
Toto xxxxxxxxx xx xxxxxxxx xx xxxxxxxx, xxxxx mají xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx, pokud xxx x&xxxx;xxxxxx xxxxx, jak xx xxxxxxxxx x&xxxx;xx.&xxxx;6 xxxx.&xxxx;1 x&xxxx;xxxxxxx&xxxx;X&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
1.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;X:&xxxx;XXXXXX DOKUMENTACE
1.1 Veřejný souhrn xxxxxxxxxxx xxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003
Xxxxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxx hlavních vlastností xxxxxxx xxxxxxxxx xxxxx. Xxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxx xxxxx x&xxxx;xxxx xxx tuto xxxxxxxxx:
1.1.1&xxxx;&xxxx;&xxxx;Xxxxx
|
x) |
xxxxx xxxxxxxx(x); |
|
x) |
xxxxxxxxxxxx doplňkové xxxxx; |
|
x) |
xxxxxx xxxxxx a metoda xxxxxxx; |
|
x) |
xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxx; |
|
x) |
xxxxxxxxxx xxxxxxxx xxx xxxxx x |
|
x) |
xxxxx xxxxx xxxxxxxxxxxx v období xx uvedení xxxxx xx trh. |
1.1.2. Popis
|
a) |
Jméno x&xxxx;xxxxxx xxxxxxxx(x) Xxxx xxxxx musí xxx xxxxxxxxxx xx xxxxx případech xxxxxxxxx xx xxxxx xxxxxxxx xxxxxxxxx xxxxx (povolení xxxxxx na xxxxxxxx xxxx povolení, xxxxx xxxx vázané xx xxxxxxxx). Xxxxxxxxx-xx xxxxxxxxxxx xxxxxxx žadatelů, musí xxx uvedeno xxxxx xxxxxxx xxxxxxxx. |
|
x) |
Xxxxxxxxxxxx xxxxxxxxx xxxxx Xxxxxxxxxxxx doplňkové látky xxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxx&xxxx;XX xxxx&xxxx;XXX podle xxxxx xxxxxxxx xxxxxxxxx xxxxx. Xxxxxxxxx: xxxxx xxxxxxxxx xxxxx, navrhované xxxxxxxx xx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxx, xxxxxx xxxxx/xxxxxxxxx xxxxxx x&xxxx;xxxxx. |
|
x) |
Xxxxxx xxxxxx x&xxxx;xxxxxx xxxxxxx Xx xxxxx xxxxxx xxxxxxx postup. Je xxxxx popsat xxxxxx xxxxxxx analytických xxxxx, xxx mají být xxxxxxx xxx xxxxxxx xxx úřední kontroly xxxxxxxxx látky xxxx xxxxxx, v premixech a krmivech xxxxx xxxxxxxxx xxxx xxxxxxx x&xxxx;xxxxxxx&xxxx;XXX. Xxxxxxxxx xx na xxxxxxx xxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxx xxxxxxxx a přílohou III xxxxx xxxxxx metody (xxxxx) xxxxxxxxx k analýze xxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxx xxxxxx. |
|
x) |
Xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx látky Je xxxxx xxxxx závěr x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxx xx xxxxxxx xxxxxxx xxxxxxxxxxx studií. Xxxxxxxx studií xxxxx xxx uvedeny x&xxxx;xxxxxx xxxxxxx na podporu xxxxxx xxxxxxxx(x). Ve xxxxxxx xx xxxx xxx xxxxxxx xxxxx xxxxxx xxxxxxxxxx xxxxx xxxxxxx&xxxx;XXX. |
|
x) |
Xxxxxxxxxx xxxxxxxx pro xxxxx Xxxxxxx(x)&xxxx;xxxxxxxx návrh podmínek xxx xxxxx. Žadatel xxxxxxx xxxxxx xxxxx xxxxxxx xx xxxx xxxx krmivu xxxxx x&xxxx;xxxxxxxxxx podmínkami xxx xxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx. Xxxxxxxx se xxxxxx xxxxxxxxx, xxx xx xxxxxxxxx xxxx způsoby xxxxxxxx xxxx zapracování xx xxxxxx xxxx xxxx. Xx xxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxx (xxxx. nesnášenlivosti), zvláštní xxxxxxxxx xx označování x&xxxx;xxxxx zvířat, xxx xxx xx doplňková xxxxx určena. |
|
f) |
Návrh xxxxx xxxxxxxxxxxx v období xx xxxxxxx xxxxx xx xxx Xxxx xxxx se xxxxxxxx xxxxx xx xxxxxxxxx xxxxx, xxxxx xxxxx čl. 7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003 xxxxxxx do xxxxxxxxx&xxxx;x)&xxxx;xxxx&xxxx;x)&xxxx;x&xxxx;xx.&xxxx;6 xxxx.&xxxx;1 xxxxx nařízení, x&xxxx;xx doplňkové látky, xxxxx xxxxxxx xx xxxxxxx xxxxxxxxxx xxxxx Xxxxxxxxxxxx x&xxxx;xxxxxxx xx xxx xxxxxxxx, xxxxx xx xxxxxxxx z geneticky xxxxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxx jsou x&xxxx;xxxx vyrobeny. |
1.2 Vědecké xxxxxxx xxxxxxxxxxx
Xx xxxxx xxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxx o každé části xxxxxxxxx xxxxxxxxxxxx xx xxxxxxx xxxxxxx xxxxx xxxx xxxxxxx x&xxxx;xxxxxxx&xxxx;XXX. Xxxx xxxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx (xxxxxxxx).
Xxxxxxx musí xxxxxxx xxxxxx xxxx xxxxxxx x&xxxx;xxxxxxx xx xxxxx xxxxxxxxxxxx částmi s odkazem xx příslušné xxxxxx xxxxxxxxxxx.
1.3&xxxx;&xxxx;&xxxx;Xxxxxx dokumentů x&xxxx;xxxxxxxxx xxxxx
Xxxxxxx musí xxxxx xxxxx a názvy svazků xxxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxx. Je xxxxx xxxxxxxx xxxxxxxx xxxxx x&xxxx;xxxxxxx xx xxxxxx a strany.
1.4 Seznam xxxxx xxxxxxxxxxx, x&xxxx;xxxxx xx xxx xxxxxxxxx jako x&xxxx;xxxxxxxxx xxxxx
Xxxxxx xxxxxxxx xxxxx xx xxxxxxxxx xxxxxx x&xxxx;xxxxxx xxxxxxxxxxx.
2.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;XX: XXXXXXXX, XXXXXXXXXXXXXXX X&xxxx;XXXXXXXX XXX XXXXX DOPLŇKOVÉ XXXXX; METODY XXXXXXX
Xxxxxxxxx xxxxx xxxx být xxxx xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx.
2.1&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxxx xxxxx
2.1.1&xxxx;&xxxx;&xxxx;Xxxxx doplňkové xxxxx
Xxxxxxxx xx xxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx látek xxxxxxxx xx držitele xxxxxxxx.
2.1.2&xxxx;&xxxx;&xxxx;Xxxxx xx zařazení
Je xxxxx xxxxxxxxx návrh xx xxxxxxxx doplňkové xxxxx xx jedné xx xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxx xxxxx xxxxxx xxxxxxxx funkcí v souladu x&xxxx;xxxxxxx&xxxx;6 x&xxxx;xxxxxxxx&xxxx;X&xxxx;xxxxxxxx (ES) x.&xxxx;1831/2003.
Xxxx být xxxxxxxxxx xxxxx x&xxxx;xxxxxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxx (xxxx. xxxxx v potravinách, xxxxxxxx xxxx veterinárním xxxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxxx). Xx nutno xxxxx xxxxxxxx jiná povolení xxxx doplňková látka xxxx xxxxxxxxxxxxx přídatná xxxxx, xxxxxxxxxxx xxxxxx xxxxxxxxx nebo xxxx xxxx xxxxxxxx účinné xxxxx.
2.1.3&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxx složení (xxxxxx látka/činidlo, xxxx xxxxxx, xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxxxx šarží)
Je xxxxx xxxxx xxxxxxx xxxxx(x)/xxxxxxx(x)&xxxx;x&xxxx;xxxxxxx xxxxxxx xxxxxx doplňkové xxxxx s uvedením xxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx produktu. Xx xxxxx stanovit xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxx xxxxx (látek) / xxxxxxx (činidel).
Pro mikroorganismy: xx xxxxx xxxxxxxx xxxxx xxxxxxxxxxxxxxx buněk xxxx spor vyjádřený xxxx XXX na xxxx.
Xxx xxxxxx: xx xxxxx popsat xxxxxxx xxxxxxx (hlavní) xxxxxxxx x&xxxx;xxxxx xxxxxxxx aktivity x&xxxx;xxxxx xxxxxxx xxxxxxxx. Xx xxxxx xxxxxx xxxxxx důležité xxxxxxxx xxxxxxxx. Xxxxxx se xxxxxxxx xxxxxxxx, pokud xxxxx jako μmoly xxxxxxxx uvolněné xx xxxxxx xx xxxxxxxxx, xxxxxx s uvedením pH x&xxxx;xxxxxxx.
Xx-xx xxxxxx xxxxxx xxxxxxxxx xxxxx xxxxx xxxxxxxx látek nebo xxxxxxx, přičemž všechny xxx xxxxxxxxxxx definovat (xxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxx), xxxx xxx xxxxxx xxxxxx xxxxx (látek) / xxxxxxx (činidel) popsány xxxxxxxxxx x&xxxx;xxxxxxxx xxxxxx x&xxxx;xxxx směsi.
Ostatní xxxxx, xxxxxxx xxxxxx xxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxx a/nebo xxxx xxxxx všechny xxxxxx xxxxxxxxxxxxx, xxxx xxx xxxxxxxxxxxxxxxx podle složky (xxxxxx) xxxxxxxxxxxxxx x&xxxx;xxxx xxxxxxxx a/nebo xxxxx xxxxxxx xxxxxx xxxxxx (xxxxxx).
Xxxx je xxxxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxxxx úřadem xxxxx xx.&xxxx;8 xxxx.&xxxx;2 xxxxxxxx (XX) x.&xxxx;1831/2003, xxxxxxx xxxx vynechat xxxxx xxxxxxxxx složek, xxxxx xxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx, jiných než xxxxxx látky xxxx xxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxx xxxxx, které xxxxxx xxxxxxxx x&xxxx;xxxxxxxxxxx zootechnických xxxxxxxxxxx xxxxx, xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx x&xxxx;xx něž xx xxxxxxxxxx xxxxxx xxxxxxxxxx nařízení (ES) x.&xxxx;1829/2003. Xxxxxxx xxxxxx xxxxxxx v dokumentaci xxxx xxx xxxxxxxxxx založeny xx xxxxxxxxx xxxxxxxxx xxxxx, pro xxx xx xxxxxxxx xxxxxxxx, x&xxxx;xxxxx xxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxx. Xx xxxxx xxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxx v dokumentech xxxxxxx xxxxx x&xxxx;xx nutný xxxxxxx xx xxxxxx xxxxxxxxxxx identifikátorů a potvrzení, xx se identifikátor(y) vztahuje(í) na xxxxxxx, xxx xxx xx xxxxxx žádost.
2.1.4 Čistota
Žadatel xxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx, xxxxx x&xxxx;xxxxxxxxx xxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxx, xxxxx xxxxxx xxxxxxx záměrně x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxx doplňkové xxxxx. X&xxxx;xxxxxxxx fermentačního xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxx organismů x&xxxx;xxxxxxxxx xxxxx. Je xxxxx popsat protokol xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxx xxxxxxxxx šarží x&xxxx;xxxxxxx xx xxxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxx.
Xxxxxxx xxxxxxxxxx xxxxx xxxx podpořit návrh xx xxxxxxxxxxx xxxxxxxxx xxxxx.
Xxxx xxxx uvedeny xxxxxxxx xxxxxxxxx v závislosti xx xxxxxxxx postupu, xxxxx xxxxxxxxxx stávajícím xxxxxxx xxxxxxxxx Xxxxxxxxxxxx.
2.1.4.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx, xxxxxxx povolení xx xxxxxx xx xxxxxxxx xxxxxxxx
X&xxxx;xxxxxxxxxxx xxxxx, xxxxxxx xxxxxxxx xx xxxxxx xx xxxxxxxx xxxxxxxx, je xxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx se zvláštního xxxxxxx použitého výrobcem xx xxxxxxx stávajících xxxxx používaných x&xxxx;xxxxx xxxxxxxxxxxx účelům. Xx xxxxx xxxxxx xxxxxxxxxxx Xxxxxxxxxx xxxxxx xxxxxxxxx XXX/XXX pro xxxxxxxxxxxxx xxxxxxxx látky (XXXXX) xxxx xxxxxxxxxxx z povolení Xxxxxxxxxx xxxxxxxxxxxx xxx xxxxxxxxxxxxx xxxxxxxx xxxxx.
2.1.4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx, xxxxxxx xxxxxxxx xxxx xxxxxx xx xxxxxxxx povolení
U doplňkových xxxxx, xxxxxxx povolení xxxx xxxxxx na xxxxxxxx xxxxxxxx, xx xxxxx xxxxxx xxxxxxxxx normy xxxxxxxxx x&xxxx;xxxxx xxxxxxxxxxxx xxxxxx xxxx xxxxx xx xxxxxxxxxxxxx xxx xxxxxxxxxxxxx přídatné látky xxxxxxxx x&xxxx;Xxxxxxxxx společenství xxxx XXXXX. Nejsou-li xxxxxx xxxxx xxxxxxxx xxxx xx-xx xx xxxxxxxx xxx výrobní xxxxxx, xx nutno xxxxxx přinejmenším xxxx xxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx:
|
— |
xxx xxxxxxxxxxxxxx: mikrobiologická xxxxxxxxxxx, mykotoxiny, těžké xxxx; |
|
— |
xxx produkty fermentačního xxxxxxx (které xxxxxxxxxx xxxxxxxxxxxxxx jako xxxxxx xxxxxxx): je xxxxx xxxxxxx stejné xxxxxxxxx xxxx pro xxxxxxxx xxxxxxxxxxxxxx (viz xxxx). Xx nutno xxxxx xxxxxx xxxxxx, v němž xx xx xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx medium; |
|
— |
pro xxxxx xxxxxxxxxxx xxxxxx: xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxx (zejména xxxx. xxxxxx xxxxxx, xxxxxx xxxxxxx, xxxxx xxxxx), xxxxxxxxxx, xxxxxxxxxxx xxxxxxxxx, maximální hodnoty xxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxx, x&xxxx;xxxxx xx xxxxx, xx xx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxx; |
|
— |
xxx látky xxxxxxxxxxx xxxxxx: xxxxxxxxxxxxxxx xxxxxxxxxxx, xxxxx xxxx x&xxxx;xxxxxxxxx xxxxxxxxx hodnoty xxx xxxxxxxxxxxx; |
|
— |
xxx xxxxxxxxx xxxxx: xxxxx xxxx, xxxxxxx x&xxxx;XXX; |
|
— |
xxx produkty xxxxxxxx chemickou syntézou x&xxxx;xxxxxxxxxx xxxxxxx: určí xx všechny xxxxxxxx xxxxx použité x&xxxx;xxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx produktu x&xxxx;xxxxx xx jejich xxxxxxxxxxx. |
Xxxxxxxxx xx xxxxxxx xxxxxxx xxxxxxxxxx xxx xxxxxxx podle xxxxxxx xxxxxx.
2.1.5&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxx
X&xxxx;xxxxxxxxx v tuhém xxxxx xx poskytnou xxxxx x&xxxx;xxxxxxxxx xxxxx xxxxxxxxx xxxxxx, xxxxx xxxxxx, xxxxxxx, xxxxxxxx xxxxxxx, xxxxxxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxx, které xxxx xxxx xx xxxxxxxxx xxxxxxxxxx. X&xxxx;xxxxxxxxx x&xxxx;xxxxxxxx xxxxx xx xxxxxxxxx údaje o viskozitě x&xxxx;xxxxxxxxxx xxxxxx. Xxxxx xx xxxxxxxxx xxxxx xxxxxx x&xxxx;xxxxxxx xx xxxx, xx xxxxx xxxxxxxx xxxxxxxxxxx xxxx xxxxxx xxxxxxxx.
2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxxx xxxxxx xxxxx (látek) / xxxxxxx (xxxxxxx)
2.2.1&xxxx;&xxxx;&xxxx;Xxxxx
Xx xxxxx xxxxx xxxxxxxxxxxx xxxxx xxxxxx xxxxx nebo xxxxxxx. Xx zahrnuje xxxxxxx x&xxxx;xxxxx xxxxx xxxx činidla x&xxxx;xxxx xxxxxxxx xxxxxxxxxxxxxxx.
2.2.1.1&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxx
Xxxxxxxx xxxxxx definované xxxxx xx xxxxx xxxxxx xxxxxxxx názvem, chemickým xxxxxxxxx podle xxxxxxxxxx XXXXX (Xxxxxxxxxxxxx Union xx Xxxx xxx Xxxxxxx Xxxxxxxxx), xxxxxxx xxxxxxxxxxxxx druhovými názvy x&xxxx;xxxxxxxxx x/xxxx xxxxxx XXX (Chemical Xxxxxxxx Xxxxxxx). Xx xxxxx xxxxx strukturální x&xxxx;xxxxxxxxx xxxxxx a molekulovou xxxxxxxx.
X&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxx zchutňující látka xx xxxxx xxxxx xxxxx XXXXXX xxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx skupinou. X&xxxx;xxxxxxxxxxx výtažků xx xxxxx uvést xxxxxxxxxxxx xxxxxxx.
Xxxxx, x&xxxx;xxxxx xxxxx xxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxx a/nebo x&xxxx;xxxxx xxxxx xxxxxxx xxxxxx identifikovat, je xxxxx xxxxxxxxxxxxxxx xxxxx xxxxxx (složek) xxxxxxxxxxxxxx x&xxxx;xxxx xxxxxxxx x/xxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxx. Xx nutno xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx, xxx xxxx xxxxx xxxxxxxx xxxxxxxxx a zajistit xxxxxxxxxxxxxx.
Xxx xxxxxx x&xxxx;xxxxxxxxx xxxxxx xx xxxxx xxx xxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxx x&xxxx;xxxxxxxxxxxx název xxxxxxxxxx Xxxxxxxxxxx xxxx biochemie (XXX) x&xxxx;xxxxxxxxx xxxxxx „Xxxxxxxxxx xxxxxx“. X&xxxx;xxxxxxx xxxxx xxxxxxxxxxxx se xxxxxxx systematický xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx XXX. Xxxxxx názvy xxxx xxxxxxxxx xx xxxxxxxxxxx, xx xxxx xxxxxxxxxxx a jsou xxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxx dokumentaci x&xxxx;xxx jejich xxxxx xxxxxx xx lze xxxxxxxxxxx xxxxxxxxx xx xxxxxxxxxxxx xxxxx x&xxxx;xxxxx XXX. Je xxxxx xxxxx xxxxxxxxxx původ xxxxx enzymové xxxxxxxx.
Xx xxxxx popsat rovněž xxxxxxxxxxx původ xxxxxxxxxx xxxxx xxxxxxxxx fermentací (xxx bod 2.2.1.2 Mikroorganismy).
2.2.1.2 Mikroorganismy
Je xxxxx uvést xxxxx xxxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxx xxxx xxxxxxx xxxx.
X&xxxx;xxxxxxxxxxxxxx používaných xxxx xxxxxxx xxxx xxxx xxxxxxx kmen xx xxxxx uvést xxxxxxxx xxxx. Xxxxx xx xxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxx xxxxxxx mikroorganismu xxxxx nejnovějších zveřejněných xxxxx v mezinárodních nomenklaturních xxxxxx (ICN). Xxxxxxxxxxx xxxxx musí být xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxx (xxxxx xxxxx v Evropské unii) x&xxxx;xxxxxxxxxx xxxxxxx xxxxxx xx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxx látky. Xx xxxxx xxxxxxxxx xxxxxxxxx o uložení xx xxxxxx, které xxxxxxxxx xxxxxxxxx číslo, pod xxxxxx je xxxx xxxxxx. Dále xx xxxxx popsat xxxxxxx xxxxxxxxxx xxxxxxxxxxxx, xxxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxx. X&xxxx;xxxxxxxxx xxxxxxxxxxxxxx organismů xx xxxxx popis xxxxxxxxxxx xxxx. Pro xxxxx geneticky xxxxxxxxxxxx xxxxxxxxxx xx xxxxx xxxxxxxxxxx xxxxxxxxxxxxx kód xxxxx nařízení Xxxxxx (XX) x.&xxxx;65/2004 xx xxx 14.&xxxx;xxxxx 2004, xxxxxx xx zřizuje xxxxxx tvorby x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxx identifikačních kódů xxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx.
2.2.2&xxxx;&xxxx;&xxxx;Xxxxxxxx vlastnosti
2.2.2.1 Chemické xxxxx
Xx xxxxx xxxxx xxxxx xxxxxxxxxxx a chemických xxxxxxxxxx. Xxxxxxxxx rozkladu, xXx, xxxxxxxxxxxxxxx xxxxxxxxxx, xxx xxxx, xxx xxxx, xxxxxxx, tlak par, xxxxxxxxxxx xx vodě x&xxxx;x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxx, Xxx x&xxxx;Xx/Xxx, xxxxxxxxxx spektrometrie x&xxxx;xxxxxxxxx xxxxxxx, údaje XXX, xxxxxxxx izomery x&xxxx;xxxxxxxxx xxxx důležité xxxxxxxxx vlastnosti xxxx xxx xxxxxxx, xxx xx xx vhodné.
Látka xxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx významné xxx používání xxxxxxxxxx x&xxxx;xxxxxxx xxxx xxxxxx.
2.2.2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxx
|
— |
Xxxxxx x&xxxx;xxxxxxx xxxxxxxxx Xx xxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxxx xxxx xxxxxx nevýznamnost. Xxxxx bakterií náležející xx taxonomické xxxxxxx, xxxxx zahrnuje xxxxxxxxxxx, x&xxxx;xxxxx je xxxxx, xx xxxxx xxxxxxxxxx xxxxxx nebo jiné xxxxxxx virulence, je xxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx x&xxxx;xxxxx xxxxxxxx xx xxxxxxxxxx a popřípadě xxxxxxx xxxxxx, že xxxxxxxxxx xxxxx x&xxxx;xxxxxx. X&xxxx;xxxxx xxxxxxxxxxxxxx, xxx xxx xxxxxx x&xxxx;xxxxxxxxx xxxxx x&xxxx;xxxxxxx bezpečném používání x&xxxx;xxxxxxx biologie xxxx xxxxx xxxxxxxxxx xxxxx, xx xxxxxxxx xxxx xxxxxxx xxxxxxxxxxxxxxx studií. |
|
— |
Produkce xxxxxxxxxx a rezistence xxxx xxxxxxxxxxxx Xxxxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxx nebo xxxx xxxxxxx xxxx xxxxx xxxxxxxxx antibiotickou xxxxxxxx xxxx xxxxx xxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxx, xxxxx xxxx xxxxxxxx jako xxxxxxxxxxx u člověka x&xxxx;xxxxxx. Xxxxx xxxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxx xxxxxxxxx xxxxx xxxxx dále přispívat x&xxxx;xxxxxx xxxx xxxxxxxxxx xxxx antibiotikům, které xx xxx vyskytují x&xxxx;xxxxxxx xxxxx xxxxxx x&xxxx;x&xxxx;xxxxxxxx xxxxxxxxx. Všechny xxxxx xxxxxxxx xx xxxxx nutno xxxxxxxxx xx xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxx. Xx-xx xxxxxxxx xxxxxxxxxx, xx xxxxx zjistit xxxxxxxxx xxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxx xx xxxxxxx organismy xx xxxxxxxx. Xxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx rezistenci xx xxxxx xxxxxxxx xxxx xxxxxxxxx xxxxx, xxxxx-xx xxxxxxxx, xx xxxxxxxxxx je xxxxxxxxx xxxxxxxxxxxx mutace(í) a není xxxxxxxx. |
2.3&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxx, xxxxxx zvláštních xxxxxxxxx postupů
Ke xxxxxxxxx xxxxxxxxxx xxxx xxxxxxx, xxxxx xxxxx xxx xxxx na čistotu xxxxxx xxxxx / xxxxxxx (xxxxxxx) nebo xxxxxxxxx látky, xx xxxxx xxxxx xxxxxxxxx xxxxxxx. Je xxxxx xxxxxxxxx xxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxxxxx materiálu x&xxxx;xxxxxxxxxx xxxxx používaných xx xxxxxxxx xxxxxxx.
2.3.1&xxxx;&xxxx;&xxxx;Xxxxxx látky(y) / činidlo(a)
Je nutno xxxxxxxxxx xxxxx xxxxxxxxx xxxxxxx (např. chemická xxxxxxx, fermentace, kultivace, xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx) použitého xxx xxxxxxxx xxxxxx xxxxx (xxxxx) / xxxxxxx (xxxxxxx) doplňkové xxxxx, případně xxxxxxxxxxxxxxx xxxxxxxxxxx diagramu. Uvede xx xxxxxxx xxxxxxxxxxxxx/xxxxxxxxxxxx xxxxx. Je nutno xxxxxx xxxxxxxx xxxxxx xxxxxxx.
X&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxx (XXX) používaných xxxx xxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxxxx xx xxxxxxxx xxxxxxxxxx nakládání xx xxxxxxx xxxxxxxx Rady 90/219/XX&xxxx;(5). Xx nutno xxxxx popis fermentačních xxxxxxx (médium pro xxxxxxx, fermentační xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx produktů xxxxxxxxxxxxx xxxxxxx).
2.3.2&xxxx;&xxxx;&xxxx;Xxxxxxxxx látka
Předloží xx xxxxxxxx popis xxxxxxxxx postupu xxxxxxxxx xxxxx. Je nutno xxxxx xxxxxx xxxxxx xxxxxx doplňkové xxxxx, xxxxxx xxxx (místa) xxxxxxxxxxx xxxxxx xxxxx (xxxxx) / xxxxxxx (xxxxxxx) x&xxxx;xxxxxx složek x&xxxx;xxxxxxx následné xxxxxx xxxxxxxxxx, xxxxx xxxx xxxx xx xxxxxxxx xxxxxxxxx xxxxx, xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx.
2.4&xxxx;&xxxx;&xxxx;Xxxxxxxxx-xxxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx
2.4.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx
Xxxxxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxx sledováním xxxxxx látky (látek) / xxxxxxx (xxxxxxx) xxxx xxxx (jeho) xxxxxxxx/xxxxxxxxxxxxxxxx. U enzymů xxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx xx xxxxxx katalytické xxxxxxxx; u mikroorganismů x&xxxx;xxxxxxx xx xxxxxx xxxxxxxxxxxxxxxx; x&xxxx;xxxxxxxxxxxxx látek s ohledem xx xxxxxx chuti. X&xxxx;xxxxxxxxx xxxxxxxxxx xxxxx/xxxxxxxx xxx stabilitu xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxx.
Xxxxxxxxx xxxxxxxxx xxxxx
Xx nutno přezkoumat xxxxxxxxx každého xxxxxxx xxxxxxxxx xxxxx při xxxxxxxx xxxxxxxx vnějšího xxxxxxxxx (xxxxxx, xxxxxxx, xX, vlhkost, xxxxxx x&xxxx;xxxxxxx xxxxxxxxx). Xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx látky x&xxxx;xxxxxxxxxxxxxx xxxxx by xxxx být xxxxxxxx xx xxxxxxx xxxx xxxxxxxxxx xxxxxxxxx zahrnujících xxxxxxxxxxxxx spektrum podmínek xxx xxxxx (xxxx. 25&xxxx;xX, 60&xxxx;% xxxxxxxxx xxxxxxx xxxxxxx x&xxxx;40&xxxx;xX, 75&xxxx;% xxxxxxxxx xxxxxxx xxxxxxx).
Xxxxxxxxx xxxxxxxxx látky xxxxx x&xxxx;xxxxxxxxx a krmivech
U doplňkových xxxxx xxxxxxx v premixech x&xxxx;xxxxxxxx x&xxxx;xxxxxxxx zchutňujících xxxxxx se stabilita xxxxxxx xxxxxxx doplňkové xxxxx xxxxx xx xxxxxxx xxxxxxxxx a skladovacích xxxxxxxx premixů x&xxxx;xxxxx. Xxxxxx xxxxxxxxx xxxxxxx xxxx trvat xxxxxxx xxxx měsíců. Xxxxxxxxx xx testuje xxxxx xxxxx u premixů xxxxxxxxxxxx xxxxxxx prvky; x&xxxx;xxxxxxx xxxxxxx xx xxxxxxxxx xxxxx xxxx být xxxxxxxx xxxxxxx „xxxxxxxx xx xxxxxxxxx xxxxx“.
Xxxxxx xxxxxxxxx x&xxxx;xxxxx xxxxxx xxxxxxxx nejméně xxx xxxxxx. Obvykle xx xxxxxxxxx kontroluje x&xxxx;xxxxx xx xxxxx xxxx x&xxxx;xxxxxxxxxxxx xxxxx (včetně xxxxx peletování xxxx xxxxxx xxxxx xxxxxx) xxx hlavní xxxxxxx xxxxx xxxxxx.
X&xxxx;xxxxxxxxxxx látek xxxxxxxx k použití xx xxxx je nutno xxxxxxxxx xxxxxxx složení xxxxxxxxx xxxxx xxxxxx xx xxxx xx xxxxxxxx xxxxxxxxxxxx xxxxxxx x&xxxx;xxxxx.
Xxxxx-xx ke ztrátě xxxxxxxxx x&xxxx;xx xxxxxxxx xxxxxxxxx xx nutno xxxxxxxxxxxxxxx případné produkty xxxxxxxxx xxxx xxxxxxxx.
Xx xxxxx xxxxxxxxxx xxxxx x&xxxx;xxxxxx, které xxxxxxxx xxxxxxx xxxxx xxxxxxxxxx xx xxxxxxx a jedno xx xxxxx xxxx xxxxxxxxxx.
X&xxxx;xxxxxxx xxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx xxxxxxx xxxx xxxxx xxxxxxxxx xxx zkoušky.
2.4.2 Homogenita
Je xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx (xxxxx xxxxxxxxxxxxx xxxxxx) x&xxxx;xxxxxxxxx, xxxxxxxx xxxx xx xxxx.
2.4.3&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxxxxxx
Xx xxxxx xxxxxx xxxxxxx xxxxxxxxxx, například xxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx vlastnosti xxxx xxxxxxxxx xxxxxxxx v kapalinách.
2.4.4 Fyzikálně-chemické xxxxxxxxxxxxxxx xxxx xxxxxxxxx
Xx xxxxx xxxxx fyzikálně-chemické xxxxxxxxxxxxxxx nebo xxxxxxxxx, x&xxxx;xxxx by xxxxx xxxxx xx xxxxx x&xxxx;xxxxxx, xxxxxx, jinými xxxxxxxxxx doplňkovými látkami xxxx léčivými xxxxxxxxx.
2.5&xxxx;&xxxx;&xxxx;Xxxxxxxx xxx xxxxx xxxxxxxxx xxxxx
2.5.1&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxxx použití xx xxxxxx xxxxxx
Xx xxxxx xxxxx xxxx xxxx xxxxxxxxx xxxxxx, xxxxxxx skupinu xxxx xxxxxxxxx xxxxxxx zvířat x&xxxx;xxxxxxx s kategoriemi v příloze IV xxxxxx nařízení. Je xxxxx xxxxxx xxxxx xxxxxxxxxxxxxx. Uvede se xxxxxxxxxx xxxxxxx x&xxxx;xxxxxx xxxx xx xxxx.
Xx xxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxx a zapracování xxx xxxxxxx, krmiva xxxx xxxxxx xxxx. Xxxxx xx navrhovaná xxxxx x&xxxx;xxxxxxxxxx krmivu x&xxxx;xxxxxxxxxx xxxx xxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx ochranná xxxxx. Xxxxx se xxxxxxxx xxxxxxxxx použití xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx xxxxxx, xx xxxxx xxxxxxxxxx.
2.5.2&xxxx;&xxxx;&xxxx;Xxxxxxxxx související x&xxxx;xxxxxxxxxxx xxx xxxxxxxxx/xxxxxxxxxx
2.5.2.1&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxx
Xx xxxxx poskytnout listy x&xxxx;xxxxx o bezpečnosti xxxxxxxxx xx formátu odpovídajícím xxxxxxxxxx xxxxxxxx Komise 91/155/XXX ze dne 5.&xxxx;xxxxxx 1991, xxxxxx xx x&xxxx;xxxxxxxxx xxxxxx&xxxx;10 xxxxxxxx 88/379/XXX vymezují x&xxxx;xxxxxxx xxxxxxxx opatření x&xxxx;xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxx&xxxx;(6). X&xxxx;xxxxxxx potřeby xx xxxxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx pracovním xxxxxxx a ochranné prostředky xxx xxxxxx, xxxxxxxxxx, xxxxx x&xxxx;xxxxxxxxx.
2.5.2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxx
Xx xxxxx xxxxx xxxxxxxxxxx xxxxx xxxxxxxx Evropského parlamentu x&xxxx;Xxxx 2000/54/XX xx xxx 18.&xxxx;xxxx 2000 x&xxxx;xxxxxxx xxxxxxxxxxx xxxx xxxxxx xxxxxxxxx s expozicí xxxxxxxxxxx xxxxxxxxx xxx xxxxx (sedmá samostatná xxxxxxxx xx&xxxx;xxxxxx xx.&xxxx;16 xxxx.&xxxx;1 směrnice 89/391/EHS) (7). X&xxxx;xxxxxxx mikroorganismů xxxxxxxxxxxx xx skupiny 1 xxxx xxxxxxxx je xxxxx xxxxxxxxxx spotřebitelům informace, xxxxx xxx xxxxxx xxxxxxxx příslušná xxxxxxxx xx xxxxxxx xxxxxxxxxx, xxx je xxxxxxxxx x&xxxx;xx.&xxxx;3 odst. 2 xxxxxxx xxxxxxxx.
2.5.2.3&xxxx;&xxxx;&xxxx;Xxxxxxxxx xx xxxxxxxxxx
Xxxx xxxx dotčena xxxxxxxxxx x&xxxx;xxxxxxxxxx x&xxxx;xxxxxx xxxxxxxx x&xxxx;xxxxxx&xxxx;16 nařízení (ES) x.&xxxx;1831/2003, xx nutno xxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxx a popřípadě xxxxxxxx xxxxxxxx xxx xxxxx x&xxxx;xxxxxxxxxx (xxxxxx xxxxxxx xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxx) x&xxxx;xxxxxx xxx xxxxxxx xxxxxxx.
2.6&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxx a referenční xxxxxx
Xxxxxx analýzy xx xxxxxx xx xxxxxxxxxx xxxxxx podle xxxxxxxxxx xxxxx XXX (tj. XXX 78-2).
Podle nařízení (XX) č. 1831/2003 x&xxxx;xxxxxxxx (XX) x.&xxxx;378/2005 xxxxxx xxxxxxx xxxxxxx x&xxxx;xxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx. Referenční xxxxxxxxx Xxxxxxxxxxxx xxxxxxxx xxxxx hodnotící xxxxxx, x&xxxx;xxx se xxxxx, xxx jsou tyto xxxxxx vhodné xxx xxxxxxx xx xxxxxx xxxxxxxx kontrol xxxxxxxxx xxxxx, xx xxx xx xxxxxx vztahuje. Xxxxxxxxx referenční laboratoře Xxxxxxxxxxxx xx xxxxxx xx xxxxxx stanovené x&xxxx;xxxxxx&xxxx;2.6.1 x&xxxx;2.6.2.
Xxxxx byl xxxxxxxx XXX xxx xxxxx, xx xxx xx vztahuje nařízení Xxxx (EHS) x.&xxxx;2377/90 xx dne 26.&xxxx;xxxxxx 1990, kterým se xxxxxxx postup Společenství xxx xxxxxxxxx maximálních xxxxxx reziduí xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxx původu (8), xxxxxx xxx&xxxx;2.6.2 předmětem xxxxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx. Xxxxxxx xxxxxxx xxx&xxxx;2.6.2 xxxxxxxxxx xxxxxxx metodu, xxxxxxxxx a údaje (včetně xxxxxxxxxxx xxxxxxxxxxx), xxx xxxx xxx předloženy Xxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxxx (XXXX) x&xxxx;xxxxxxx x&xxxx;xxxxxxxx&xxxx;X&xxxx;xxxxxxxx (XXX) x.&xxxx;2377/90 x&xxxx;xxxxx xxxxxxxxx „Xxxxxx xx Xxxxxxxxxx xxx Xxxxxxxxxx“, svazek 8 „Xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xx the Xxxxxxxx Xxxxx“.
X&xxxx;xxxxxxxxx mohou xxx xxxxxxxx rovněž xxxxxxxxxx metody xxxxxxx x&xxxx;xxxx&xxxx;2.6.3, xxxxx xx xxxxxxxxxx xxxxxxxxx Společenství, xxxx xxxx Xxxxxx xxxxxxxx za nezbytné.
V souladu x&xxxx;xxxxxxxxx (ES) x.&xxxx;378/2005 xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx Společenství xxxx xxxxxxxxxxxx technické dokumentace x&xxxx;xxxxxxxx vzorky xxxx xxxxxxxxx xxxx použitelnosti.
Žadatelé xxxxxx xx xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx&xxxx;12 nařízení (ES) x.&xxxx;378/2005.
2.6.1&xxxx;&xxxx;&xxxx;Xxxxxx analýzy xxx xxxxxxx xxxxx
Xx nutno xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxx a popřípadě xxxxxxxxxxxxx xxxxxxxxxx metody (xxxxx) xxx zjištění, zda xxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxx látky (xxxxx) / xxxxxxx (xxxxxxx) v doplňkové xxxxx, xxxxxxxxx, krmivech x&xxxx;xxxxxxxxx xxxx.
|
2.6.1.1 |
Xxxx metody xxxxxxx xxxxxx xxxxxxxxx xxxx x&xxxx;xxxxxxx metod xxxxxxx xxxxxxxxxxx pro úřední xxxxxxxx podle xxxxxx&xxxx;11 xxxxxxxx (XX) č. 882/2004. Xxxxxxx splňují xxxxxxx xxxxx x&xxxx;xxxxxx požadavků:
|
|
2.6.1.2 |
Xxxxxxxx xxxxxxxxxxxxxxx xxxxxx (metod) xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxxxx (XX) x.&xxxx;882/2004. |
|
2.6.1.3 |
Xxxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxxxxx interně xx xxxxx xxxxxxxxxxx metody x&xxxx;xxxxx xxxxxxxxxxxx a nezávislé xxxxxxxxxx. Poskytnou xx xxxxxxxx xxxxxx testů xxxxx s případnými xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxx. Z důvodu xxxxxxxxxxxx a účasti na xxxxxxxxx dokumentace poskytnuté xxxxxxxxx v případě, xx xxxxx xxxxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx, xxx xx xxxxxxxxx x&xxxx;xxxxxxxx (XX) č. 378/2005, xxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxx (xxxxxxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx xxxxxx žádost) xxxxxxxxxx xxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxx x&xxxx;xxxxx xxxxxxx a nesmí xx xxxxxxxx xxxxxxxxxxx xxxxxxx. |
|
2.6.1.4 |
Xx xxx xxxxxxxxx xxxxxx pro úřad xxxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxx&xxxx;XXX xxxxxxxx (XX) x.&xxxx;882/2004. |
|
2.6.1.5 |
Xxxxxxxx xxxxxxxxxxxxxxx pro xxxxxx xxxxxxxxxx skupin látek (xxxxxxxxx enzymy) mohou xxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx referenční xxxxxxxxxx Společenství xxxxx xxxxxx&xxxx;12 nařízení (ES) x.&xxxx;378/2005. |
2.6.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxx xxx xxxxxxxxx xxxxxxx doplňkové xxxxx xxxx xxxxxx xxxxxxxxxx v potravinách
Je xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxx a kvantitativních analytických xxxxx pro stanovení xxxxxxxxxxxxxx reziduí x/xxxx xxxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxx a živočišných xxxxxxxxxx.
|
2.6.2.1 |
Xxxx xxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxx x&xxxx;xxxxxxx xxxxx xxxxxxx xxxxxxxxxxx pro úřední xxxxxxxx podle xxxxxx&xxxx;11 xxxxxxxx (XX) x.&xxxx;882/2004. Xxxx xxxxxx splňují xxxxxxx nejméně xxxxx x&xxxx;xxxxxxxxx xxxxxxxxx x&xxxx;xxxx 2.6.1.1. |
|
2.6.2.2 |
Xxxxxxxx charakteristika xxxxxx (xxxxx) xxxxxxxx odpovídající xxxxxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxxxx (XX) č. 882/2004 x&xxxx;xxxx x&xxxx;xxxxx xxxxxxxxx xxxxxxxxx v rozhodnutí Xxxxxx 2002/657/XX&xxxx;(10). Popřípadě xx xxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxxxx stanovené x&xxxx;xxxxxxxxxxxx Xxxxxx, která xxxxxxx xxxxxxxxxx metody xxxxxxxxx x&xxxx;xxxxxxxxxx určitých xxxxx x&xxxx;xxxxxx xxxxxxx v živých xxxxxxxxx xxxxx xxxxxxxx Xxxx 96/23/XX. Xxxxx xxxxxxxxxxxx x&xxxx;xxxxx xxxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx XXX a musí xxx xxxxxxxxx v rozmezí xxxxxxxxxxxx xx xxxxx xxxxxxxx xx xxxxxxxxxxx XXX. |
|
2.6.2.3 |
Xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxx se xxxxx xxxxxxxxxxx xxxxxx v druhé xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx. Xx xxxxx uvést xxxxxxxx xxxxxx xxxxx. X&xxxx;xxxxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx, xx druhá xxxxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxxx referenčních laboratoří xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx, xxx xx xxxxxxxxx x&xxxx;xxxxxxxx (XX) x.&xxxx;378/2005, xxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx Xxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxx (xxxxxxx referenční xxxxxxxxx Xxxxxxxxxxxx xxxxxx xxxxxx) xxxxxxxxxx práci xxxxxxxxxx x&xxxx;xxxxxxxxxxx s danou žádostí x&xxxx;xxxxx xx xxxxxxxx xxxxxxxxxxx žádosti. |
|
2.6.2.4 |
Ve xxx xxxxxxxxx xxxxxx xxx xxxx xxxx xxxxxxxxxx xxxxxxxxx Společenství vybrat xxxxxx charakteristiky x&xxxx;xxxxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxx&xxxx;2.6.2.2. |
|
2.6.2.5 |
Xxxxxxxx xxxxxxxxxxxxxxx xxx xxxxxx xxx xxxxxxxx xxxxxxx xxxxx (xxxxxxxxx xxxxxx) mohou xxx xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx poskytnutých referenční xxxxxxxxxx Xxxxxxxxxxxx xxxxx xxxxxx&xxxx;12 xxxxxxxx (XX) x.&xxxx;378/2005. |
2.6.3&xxxx;&xxxx;&xxxx;Xxxxxx analýzy xxxxxxxx xx xxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxxx xxxxx
Xxxxxxx xxxxxxxx xxxxx metod použitých xx xxxxxxxxx xxxxxxxxxxxxxx xxxxx bodů 2.1.3, 2.1.4, 2.1.5, 2.2.2, 2.4.1, 2.4.2, 2.4.3 x&xxxx;2.4.4.
X&xxxx;xxxxxxx x&xxxx;xxxxxxxx&xxxx;XX nařízení (XX) x.&xxxx;1831/2003 xx xxxxx xxxxxxxx (XX) x.&xxxx;378/2005 xxxxx xxx vyhodnoceny xxxxxx xxxxxx xxxxxxxxxx xxxxx xxxxxx xxxx, xxxxx xx xxxx xxxx Xxxxxx xxxxxxxx xx xxxxxxxx xxx xxxxxxxxx žádosti.
Doporučuje xx, xxx metody xxxxxxx x&xxxx;xxxxx xxxx xxxx xxxxxxxxxxx uznané. Metody, xxxxx xxxxxx mezinárodně xxxxxx, je nutno xxxx xxxxxx. V těchto xxxxxxxxx xxxx xxx xxxxxx xxxxxxxxx xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxx a musí xxx zdokumentovány podle xxxxxxxxxxx xxxxx xxxxxxx (xxxx. xxxxxxx xxxxxxxxxxx xxxxx xxxxx směrnice 2004/10/XX xxxx xxxxx XXX).
Xxxxxx pro identifikaci x&xxxx;xxxxxxxxxxxxxxx doplňkové látky xxxxxxx stejné xxxxxxxxx xxxx xxxxxx xxxxxxx xxxxxxxxx pro úřední xxxxxxxx podle xxxxxx&xxxx;11 xxxxxxxx (XX) x.&xxxx;882/2004, xxxxxxx xxxxx xxxx xxxxxxxxx xxxxxx požadavky (xxxx. nečistoty, xxxxxxxxx xxxxx).
3.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;XXX: STUDIE XXXXXXXX XX BEZPEČNOSTI XXXXXXXXX XXXXX
Xxxxxx uvedené x&xxxx;xxxxx xxxxxx a ve xxxxxxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxxxxxx:
|
— |
xxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxx cílové xxxxx xxxxxx, |
|
— |
xxxxxxxxxx xxxxxx xxxxxxxxxxxxx xx xxxxxxx x/xxxx přenosem xxxxxxxxxx xxxx antimikrobiálním xxxxxx x&xxxx;xxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxx, |
|
— |
xxxxx xxx xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xx xxxxxx, xxxx byla xxxxxxxx krmiva obsahující xxxxxxxxxx látku xxxx xxxxxx ošetřená xxxxxxxxxx xxxxxx, nebo xxxxx, xxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx obsahujících xxxxxxx xxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxxx, |
|
— |
xxxxx xxx xxxxx manipulující x&xxxx;xxxxxxxxxx látkou xxxx xxxxxxx nebo xxxxxxxxxxxx xx xxxxxxx či xxxxx, xxxxxxxxxxxx xxx xxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxx, xxx xxxx xxxx x |
|
— |
xxxxx xxxxxxxxxxx účinků vlastní xxxxxxxxx xxxxx xxxx xxxxxxxx x&xxxx;xx xxxxxxxxxx, xxxxxxxxxx přímo x/xxxx xxxxxxxxxxxx xxxxxxx, xx xxxxxxx prostředí. |
3.1 Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx xxxxx xxxxxx
Xxxxxx xxxxxxx v tomto oddíle xxxx xxxxxx x&xxxx;xxxxxxxxxxx:
|
— |
xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx druhy xxxxxx x |
|
— |
xxxxxxxxxx xxxxxx xxxxxxxxxxxxx xx xxxxxxx x/xxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxxxxxx látkám x&xxxx;xxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxx. |
3.1.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxx zvířat
Účelem testu xxxxxxxxx je xxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx látky x&xxxx;xxxxxxxx xxxxxx. Xxxxxxx xx rovněž xx xxxxxxxxx xxxxxxx xxx xxxxxxxxxx, pokud se xxxxxxxxx xxxxx požije x&xxxx;xxxxxxx vyšších, xxx xx xxxxxxxxxx. Tyto xxxxx xxxxxxxxx je xxxxx xxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx pro xxxxxxx xxxxxx druhy/kategorie xxxxxx, xx xxx xx xxxxxx xxxxxxxx. X&xxxx;xxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxx xxxxx xxxxx tolerance xx xxxxx ze zkoušek xxxxxxxxx, xxxxx xxxx xxxxxxx níže xxxxxxx xxxxxxxxx na xxxx xxxxx. Všechny xxxxxx xxxxxxx v tomto xxxxxx xxxx xxx xxxxxxxx xx xxxxxxxxx xxxxx xxxxxxx x&xxxx;xxxxxx&xxxx;XX.
3.1.1.1&xxxx;&xxxx;&xxxx;Xxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxx skupiny:
|
— |
skupinu, xxx xx xxxxxxxxx látka xxxxxxxx, |
|
— |
xxxxxxx x&xxxx;xxxxxxxx doporučenou xxxxxx x |
|
— |
xxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx obsahem xxxxxxxx xxxxxxxxxx dávky. |
V pokusné xxxxxxx xx doplňková xxxxx xxxxxxx xxxxxx xx xxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx. Pokusná xxxxxxx jsou xxxxxxx xxxxxxxxx x&xxxx;xxxxxxx na xxxxxxxx důkazy xxxxxxxxxx xxxxxx, pracovní xxxxxxxxxxxxxxx, xxxxxxxxx xxxxxx xxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx krve x&xxxx;xxxx xxxxxxxxx, které xxxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx látky. Xxxxxx xx xx xxxxx xxxxxxxx parametry xxxxx z toxikologických xxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxx. X&xxxx;xxxxx xxxxxx xx uvedou xxxxxx případné xxxxxxxxx xxxxxx xxxxxxxx xxxxx xxxxxxx xxxxxxxxx. V případě xxxxxxxxxxxxxx xxxxx xxx xxxxx tolerance xx xxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx.
Xxxxx xxx xxxxxxxx, xx xx xxxxxx 100xxxxxxx xxxxxxxxx doporučené xxxxx, xxxxxxxxxx xx xxxxxxxxxxx xxx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx xxxx. Je-li produkt xxxxxx xxxxx při xxxxxx nižším, než xx 10xxxxxxx nejvyšší xxxxxxxxxx xxxxx, xx xxxxxx navržena xxx, xxx bylo xxxxx xxxxxxxxx xxxxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxx, x&xxxx;xxxxxx xx xxxxxxxxx xxxxxxxxx (xxxxxx nekropsie, xxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxx xxxxxxxx xxxxxxxx).
X&xxxx;xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxx xxx x&xxxx;xxxxxxxxxx na jejich xxxxxxxxxxx x&xxxx;xxxxxxxxxxx nebo xxxxx xxxxx xxxxxxx xxxxx tolerance.
Použité experimentální xxxxxx musí xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx.
3.1.1.2&xxxx;&xxxx;&xxxx;Xxxx xxxxxx zkoušek xxxxxxxxx
Xxxxxxx&xxxx;1
Xxxx trvání xxxxxxx xxxxxxxxx: xxxxxxx
|
Xxxxxx xxxxxxx |
Xxxx xxxxxx studií |
Charakteristika xxxxxxxx xxxxxx |
|
Xxxxxx xxxxxx |
14&xxxx;xxx |
Xxxxx možno xx 14&xxxx;xxx xx xxxxxxx |
|
Xxxxxxxxx selata |
42 dní |
42 dní xx xxxxxxx |
|
Xxxxx xxxxxx |
42&xxxx;xxx |
Xxxxxxx xxxxxxxx xx xxxxxxx xxxxxx ≤&xxxx;35&xxxx;xx |
|
Xxxxxxxx xxxxxx k reprodukci |
1 cyklus |
Od xxxxxxxxxx xx konce xxxxxxx |
X&xxxx;xxxxxxx žádosti xxxxxxxx xx xxxxxxxx a odstavených xxxxx xx považuje xx xxxxxxxxxxx kombinovaná xxxxxx (14denní xxx xxxxxx xxxxxx x&xxxx;28xxxxx xxx xxxxxxxxx xxxxxx). Xxxxx xxxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx selat, xxxxxxxxxx xx zvláštní xxxxxx xxx výkrm xxxxxx.
Xxxxxxx&xxxx;2
Xxxx trvání zkoušek xxxxxxxxx: xxxxxx
|
Xxxxxx xxxxxxx |
Xxxx xxxxxx studií |
Charakteristika xxxxxxxx xxxxxx |
|
Xxxxx xxxxx/xxxxxx |
35&xxxx;xxx |
Xx xxxxxxxxx |
|
Xxxxxxx |
56&xxxx;xxx |
Xxxxx xxxxx xxxxx xxxxx xxxxxxx xxxx snášky |
|
Výkrm xxxx |
42&xxxx;xxx |
Xx xxxxxxxxx |
Xxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxx kuřat xxxx xxxx lze xxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx u odchovu xxxxx x&xxxx;xxxxx nebo x&xxxx;xxxxxxx xxxx.
Xxxxxxx&xxxx;3
Xxxx xxxxxx xxxxxxx xxxxxxxxx: skot
|
Cílová xxxxxxx |
Xxxx xxxxxx xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx xxxxxx |
|
Xxxxx xxxxx |
28&xxxx;xxx |
Xxxxxxx xxxxxxx hmotnost ≤&xxxx;70&xxxx;xx |
|
Xxxxxx xxxxx; xxxxx xxxxx xxxx xxxx k reprodukci |
42 dní |
|
|
Dojnice |
56 dní |
V případě xxxxxxx xxxxxxxxxx se xx xxxxxx telat x&xxxx;xxxxx skotu xx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxxx (28 dnů xxx xxxxx xxxxxx).
Xxxxxxx&xxxx;4
Xxxx xxxxxx zkoušek tolerance: xxxx
|
Xxxxxx zvířata |
Doba trvání xxxxxx |
Xxxxxxxxxxxxxxx cílových xxxxxx |
|
Xxxxxx xxxxxx a výkrm jehňat |
28 dní |
Tabulka 5
Doba xxxxxx xxxxxxx xxxxxxxxx: xxxxxxxxxx x&xxxx;xxxx ryby
|
Cílová xxxxxxx |
Xxxx trvání xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx xxxxxx |
|
Xxxxx x&xxxx;xxxxxx |
90&xxxx;xxx |
Xxxx xxxxxxxxxxx 90xxxxx xxxxxx xx bylo xxxxx xxxxxxx studii, kdy xxxx xxxxx svou xxxxxxxx xxxxxxxx xxxxxx xxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx zkoušky xxxxxxx xxxxxxxxxxx.
Xx-xx xxx xxxxxxxxx látka xxxxxxxxx xxxxx pro xxxxx xxxxxxxxx xxx, xxxxx xxxxxxxxx se provedou xxxxx možno co xxxxxxxx xxxx xxxxx. Xxxxx xxxxxxxxx trvají 90&xxxx;xxx x&xxxx;xx xxxxx xxxxxxx xxxxxxxxx kvalitě x&xxxx;xxxxxxx jiker.
Tabulka 6
Doba trvání xxxxxxx xxxxxxxxx: xxxxxxx x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxx xxxxxxx, xxxxx xxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxxx
|
Xxxxxx xxxxxxx |
Xxxx xxxxxx xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx xxxxxx |
|
Xxx a kočky |
28 dní |
Tabulka 7
Xxxx trvání xxxxxxx xxxxxxxxx: králíci
|
Cílová zvířata |
Doba trvání xxxxxx |
Xxxxxxxxxxxxxxx xxxxxxxx xxxxxx |
|
Xxxxx xxxxxxx |
28&xxxx;xxx |
|
|
Xxxxxx xxxxxxx |
1&xxxx;xxxxxx |
Xx inseminace xx xxxxx xxxx xxxxxxx |
Xxxxxxxx-xx xx xxxxxx xx xxxxxx a odstavené xxxxxxx, xxxxxxxx xx xx xxxxxxxxxx období 49&xxxx;xxx (počínaje xxxxx xx xxxxxxxx) x&xxxx;xxxx xxxxxxxxx xxxxxxx až xx xxxxxxx.
Xxxxx se xxxxxxxxx látka xxxxxxx xx xxxxxxxxxxx x&xxxx;xxxxxx xxxx, xxx xx xxxxxxx v definici kategorie xxxxxx, podává xx xxxxx xxxxxxxxxxxx xxxxxxxx xxx xxxxx. Xxxxxx xxxxxxxxxx však xxxxx xxx kratší xxx 28&xxxx;xxx x&xxxx;xxxx xxxxxxxxx xxxxxxxxx xxxxxxxx (xxxx. x&xxxx;xxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxxxx xxxx xxxxxxxxxx xxxxx xx xxxxxxxx xx xxxxxx xxxxxxxx xxxx počet x&xxxx;xxxxxxxx xxxxxxxxxxx selat xx xxxxxxxx xx xxxxxx xxxxxxx).
3.1.1.3&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxxxx
Xxxxxx xxxx xxx uvedeny jednotlivě x&xxxx;xxxxx o všech xxxxxxxxx xxxxxxxxx. Xxxxxxxx protokol xxxx xxx xxxxxxx xxxxxxxxxx x&xxxx;xxxxxxx xx xxxxxx xxxxxxx údaje. Xxxxxxxxxxxxx xx xxxxxxx xxxx xxxxxxx:
|
1. |
xxxxx xxxx xxxxx: xxxxx x&xxxx;xxxxx; xxxxxxxx xxxxxx a chovu, xxxxxx xxxxxx; u vodních xxxxx xxxxxxxx a počet xxxxxx nebo xxxxx x&xxxx;xxxxxxxxxxxx, xxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxx, xxxxxx xxxxxxx xxxx x&xxxx;xxxxxx xxxx ve xxxx; |
|
2. |
xxxxxxx: xxxx (x&xxxx;xxxxxxx druhů xxxxxxxx pro lidskou xxxxxxxx xx xxxxxxx xxxxxxxxxxxx xxxxx jejich xxxxxxxx jména x&xxxx;xx xxx v závorkách xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx), xxxxxxx, xxxxx (velikost x&xxxx;xxxxxxx xxxxx), xxxxxxx, xxxxxx xxxxxxxx, xxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxx zdravotní xxxx; |
|
3. |
xxxxx a přesná doba xxxxxx testů: xxxxx x&xxxx;xxxx xxxxxxxxxxx xxxxxxx; |
|
4. |
xxxxx xxxxx: popis xxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxx krmné xxxxx (xxxxx) x&xxxx;xxxxxxxx xxxxxxxxx xxxxxx, xxxxxxxxxxx xxxxx (analyzované xxxxxxx) x&xxxx;xxxxxxxxxxx xxxxxxx. Údaje x&xxxx;xxxxxx xxxxxx; |
|
5. |
xxxxxxxxxxx xxxxxx xxxxx (xxxxx) xxxx xxxxxxx (činidel) (x&xxxx;xxxxxxxxxx xxxxx xxxxxxxxx xxx xxxxxxxxxx účely) x&xxxx;xxxxxxxx xxxx xxx stanovena xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxxxxxxx xxxxx xxxxxxxxx xxxxx; |
|
6. |
xxxxx xxxxxxxxx a kontrolních xxxxxx, počet zvířat x&xxxx;xxxxx xxxxxxx: xxxxx xxxxxx xxxxxxxxx xxx xxxxxx musí xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxx. Xxxx by být xxxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx. Ve xxxxxx xxxx xxx xxxxxxxx xxxxxxx xxxxxxx x/xxxx xxxxxxxxxxxxxx xxxxx, x&xxxx;xxxxx xx xxxxxx xxxxxxxxx. Xxxxxxx, které xxxx xxxxx vyhodnotit xxx xxxxxxxxxx nebo xxxxxx údajů, musí xxx xx xxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxx xxxxxx xxxx být klasifikováno; |
|
7. |
okamžik x&xxxx;xxxxxx jakéhokoliv xxxxxxxxxxx xxxxxx xxxxxxx x&xxxx;xxxxxxx xxxx skupin musí xxx zaznamenán (xxxxxxxxxx xxxxx x&xxxx;xxxxxxxx pozorování xxxxxxxxx xx studii) x |
|
8. |
xxxxxxx/xxxxxxxxxxx ošetření, xx-xx xxxxx, xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx a musí xxx xxxxxxxxxxx xxxxxxxxxxxx. |
3.1.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxx xxxxxx
Xx xxxxx xxxxxxxxxx xxxxxx xx stanovení xxxxxxxxxx xxxxxxxxx látky xxxxxxxx křížovou xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxx rezistentní xxxxxxxxxxx xxxxx za xxxxxxxxxx xxxxxxxx u cílových xxxxx, vyvolat xxxxxx x&xxxx;xxxxxxxxxxx patogenů přítomných x&xxxx;xxxxxxxxx xxxxxx, xxxxxxx xxxxxxxxxx nebo xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx.
X&xxxx;xxxxxxx, xx xxxxxx xxxxx (látky) xxxxxxxx(x)&xxxx;xxxxxxxxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx, xx xxxxx xx obsažena v krmivu, xxxx být v souladu xx xxxxxxxxxxxxxxxxx postupy xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx (MIK) pro xxxxxxxxx druhy bakterií. Xx-xx xxxxxxxxx příslušná xxxxxxxxxxxxxxx xxxxxxxx, xx xxxxx stanovit xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx xx xxxxx x&xxxx;x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxxxxxx křížovou xxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxxxxx&xxxx;(11).
Xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx xxxxx xx xxxxxxxx xxx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxx xxxx xxxxxxxxx xxxxx, x&xxxx;xxxxx xxx očekávat xxxxxx xx střevní xxxxxxxxxx. Tyto xxxxxx xxxx xxxxxxxx, xx xxxxx xxxxxxxxx látky xxxxxxxxx xxxxxxxx, xxxxx xxxxxxxxxx nadměrnému xxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx.
Xxxxx xxxxxxxxxxx mikroorganismů xxxx záviset xx xxxxxxxx druzích, xxxxxxxx xxxx xxxxxxxxx zoonotické xxxxx bez ohledu xx xx, xxx x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxx xx xxxxxxxxxxxx xxxxxxxx.
3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx látky xxx spotřebitele
Cílem je xxxxxxxxxx xxxxxxxxxx doplňkové xxxxx xxx xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxx xxxxxxx xxxxxxxxx xxxxx nebo xxxxxx xxxxxxxxxx v potravinách xxxxxxxxx xx xxxxxx, xxxx xxxx xxxxxxxx xxxxxx nebo xxxx xxxxxxxxxx doplňkovou xxxxx xxxx xxxxxxxx touto xxxxxxxxxx xxxxxx.
3.2.1&xxxx;&xxxx;&xxxx;Xxxxxx metabolismu x&xxxx;xxxxxxx
Xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxx xx xxxxxxxxxxxx xxxxxx xxx identifikaci x&xxxx;xxxxxxxxxxxx xxxxxxx v poživatelných xxxxxxx xxxx xxxxxxxxxx xxxxxxxxx xx xxxxxx, xxxx xxxx xxxxxxxx xxxxxx xxxx xxxx xxxxxxxxxx xxxxxxxxxx látku. Je xxxxx xxxxxxxxx xxxxxx xxxxxxxx xx xxxxxxxx, xxxxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxx (a jejích xxxxxxxxxx).
Xxxxxx xxxx xxx xxxxxxxxx xxxxxx mezinárodně xxxxxxxxxxxx xxxxxxxxxx metod a v souladu x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxxxxxx xxxxxxxxx OECD x&xxxx;xxxxx xxxxx xxxxxxx xxxxxxxxxxx xxxxx. Xxxxxx xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxx životních xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxxxx a neopakují se, xxxx-xx xx xxxxxxxx.
Xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx u cílového xxxxxxx (xxxxxx) se xxxxxxxx x&xxxx;xxxxxxx látkou xxxxxxxxxxxx do xxxxxx (xxxxxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxx, xxxx-xx xx xxxxx xxxxxxxxxx).
Xxxxxxx xx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxx xxx 10&xxxx;% xxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxx x&xxxx;xxxx než 20&xxxx;% xxxxx xxxxxxx x&xxxx;xxxxxxxxxxxx. Xxxxx xx xxxxxxxxxxx xxxxx xxxxxx xxxxx xxxxxxxxxxxxx významná, xx xxxxx xxxxxxxxxxxxx xxxxxxxxxx xxx xxxx xxxxxxxxx xxxxxx.
Xxxxxxxxx xxxxxx xxxxxxx xxxxx základ xxx xxxxxxx xxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxxxxx lhůty x&xxxx;XXX. Xxxxxxxx xx xxxxx xx indikátorové xxxxxxxx.
X&xxxx;xxxxxxxxx xxxxxxxxxxx xxxxx nemusí xxx v závislosti na xxxxxx xxxxxx xxxx xxxxx vždy xxxxx xxxxxxx studie metabolismu x&xxxx;xxxxxxx.
3.2.1.1&xxxx;&xxxx;&xxxx;Xxxxxx metabolismu
Účelem xxxxxx xxxxxxxxxxx xx vyhodnotit xxxxxxxx, xxxxxxxxxx, biotransformaci x&xxxx;xxxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxx zvířat.
Požadované xxxxxx:
|
1. |
xxxxxxxxxxx bilance xx xxxxxx xxxxxx xxxxx xxxxxx látky x&xxxx;xxxxxxxxxxxx xxxxxxx pro xxxxx (xxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxx příjmu) x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxx (xx-xx xx odůvodněno), xxx xxxxx xxx xxxxxxxxx xxxxxxxx x&xxxx;xxxxxx absorpce, xxxxxxxxxx (xxxxxx/xxxx) x&xxxx;xxxxxxxxxx (xxx, žluč, xxxxxx, xxxxx xxxx xxxxx, xxxxxxxxxxx xxxxxx, xxxxxxxxxx xxxx xxxxx) x&xxxx;xxxxx x&xxxx;xxxxx, je-li xx xxxxxx, x |
|
2. |
xxxxxxxxx do xxxxxxxxxxx, identifikace xxxxxxxxxx(x)&xxxx;x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx v tkáních x&xxxx;xxxxxxxxxx xx xxxxxxx xx opakovaném podávání xxxxx označené látky xxxxxxxx xx xxxxxxxxxx xxxxx (xxxxxxxxxxx xxxxxxxxx) xxxxx xxxxxx x&xxxx;xxxxxx. Xxxxxxxxxx xxxxx xxxxxxxx xxxxxxxx navrhované dávce xxx xxxxx x&xxxx;xxxx xxx zapracována xx xxxxxx. |
3.2.1.2&xxxx;&xxxx;&xxxx;Xxxxxx reziduí
Uváží xx xxxxxxxx a povaha xxxxxxxxxxxxxxxxxx xxxxxxx v poživatelných xxxxxxx xxxx produktech.
Studie xxxxxxx xx požadují pro xxxxxxx xxxxx, x&xxxx;xxxxx xxxx xxxxx xxxxxx xxxxxxxxxxx.
Xx-xx xxxxx xxxxxxxxxx xxxxxxx tělních xxxxxxx xxxx xxxxx xxxx xxxxxxxxx-xx se v potravinách xxxx xxxxxxxx přirozeně xx xxxxxxx xxxxxxxx, xx xxxxxxxxx xx xxxxxx xxxxxxx xxxxxx xx xxxxxxxxx xxxxxx x&xxxx;xxxxxxx/xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx x&xxxx;x&xxxx;xxxxxxx, xxx xxxx xxxxxxxx nejvyšší xxxxxxx xxxxx.
X&xxxx;xxxxxxxxxxx druhů xxxxxx xxxxxxxx xxxxxxxxx všechna xxxxxxx, xxxxx xxxx xxxxxxxxxxxxx xxxxxxxx, a určí xxxxxxxxxxxx xxxxxxxx xxxxxx xxxxx v poživatelné tkáni (xxxxx, xxxxxxx, svaly, xxxx, kůže + xxx) a produktech (xxxxx, xxxxx x&xxxx;xxx). Xxxxxxxxxxxx xxxxxxxx xx reziduum xxxxxxx pro xxxxxxx, xxxxx koncentrace je xx xxxxxx vztahu x&xxxx;xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx. Xxxxxx xxxx prokázat xxxxxx xxxxxxx reziduí x&xxxx;xxxxxxx xxxx xxxxxxxxxx, aby xxxx xxxxx xxxxxxxx xxxxxxxxxxxx ochrannou xxxxx.
Xx xxxxxxxxx ochranné xxxxx xx xxxxxxxxxx xxxxxxxxx xxxxx zvířat xx xxxxxx x/xxxx xxxxxxxx x&xxxx;xxxxxx bodu měření xxxxx:
|
— |
xxxxxxxxxxx xxxxx:
|
|
— |
xxxxxxxx:
|
Uváží xx xxxxxx xxxxxxxxx xxxxx xxxxxxx.
Xxxxxxx xx xxxx xxx xxxxxx xxxxxxxx xxxxx (vyrovnaný stav) x&xxxx;xxxxxxx xx xxxxx xxxxxx bodech měření.
Předloží xx xxxxx na xxxxxxxxxxxx reziduum.
Je xxxxx xxxxxxx xxxxxx xxxxxxxx, xxxxxxxxxx x&xxxx;xxxxxxxxxx, xxxxxx xxxxxxxxxxxx hlavních metabolitů, x&xxxx;xxxxxxxxxxxxx xxxxx xxxxxx, x&xxxx;xxxxx byla xxxxxxx xxxxxxxx hodnota XXXXX xxxx xxxxxxxxxx u krys (xxxx pohlaví). Xxxxxxxxx xxxxxx týkající xx xxxxxxxx xxxxxxxxxx mohou xxx xxxxxxxx x&xxxx;xxxxxxx, xxxx-xx xxxx metabolity xxxxxxxxxxx xxxxxxxx xxxxx x&xxxx;x&xxxx;xxxxxxxxxxxxx xxxxx se xx xxxxxxxxx xxxxxxx xxxxxxx.
3.2.1.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx
Xxxx xxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx metabolickou xxxxxxx, metabolický profil x&xxxx;xxxxxxxxxxxx xxxxxxxx xxxxxxxxxx x&xxxx;xxxx x&xxxx;xxxxxxxx. Jestliže xxxx xxxxxxxxxxx xxxxx xxxxxxxx oproti xxxxx xxxxxxx xxxxxx v citlivosti, xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx.
3.2.1.4&xxxx;&xxxx;&xxxx;Xxxxxxxxxx dostupnost reziduí
Při xxxxxxxxxx rizika pro xxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxx rezidui obsaženými x&xxxx;xxxxxxxxxxx xxxxxxxxxx je xxxxx xxxx x&xxxx;xxxxx xxxxxxxxx bezpečnostní xxxxxx xxxxxxxx na xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx a uznaných xxxxx.
3.2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxx xxxxxx
Xxxxxxxxxx doplňkové xxxxx xx xxxxxxxx xx xxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxxxxxx xx xxxxx a in xxxx xx xxxxxxxxxxxxx xxxxxxxxx. Xxxx xxxxxxx obvykle xxxxxxxx měření:
|
1. |
akutní xxxxxxxx; |
|
2. |
xxxxxxxxxxxx (xxxxxxxxxx, xxxxxxxxxxxxxx); |
|
3. |
xxxxxxxxxxxx orální xxxxxxxx; |
|
4. |
xxxxxxxxx xxxxxx xxxxxxxx/xxxxxxxxxxxxx; |
|
5. |
xxxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxxxxxx x |
|
6. |
xxxxxxx xxxxxx. |
Xxxxxxxx-xx xxxxx x&xxxx;xxxxxx, xxxx xxx xxxxxxxxx další xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx, xxxxx jsou xxxxxxxx xxx posouzení xxxxxxxxxxx xxxxxx látky x&xxxx;xxxxxx xxxxxxx.
Xx xxxxxxx xxxxxxxx xxxxxx studií xx stanoví xxxxxxxxxxxxx XXXXX.
Xxxxxxxxx studie týkající xx xxxxxxxx xxxxxxxxxx xxxxx být xxxxxxxx, xxxxx xxxx tyto xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx a u testovaných xxxxxxxxxxxxx xxxxx xx ve xxxxxxxxx rozsahu xxxxxxx. Xxxx-xx k dispozici studie xxxxxxxxxxx x&xxxx;xxxxxxx, xxxxxx xx tyto xxxxx x&xxxx;xxxxx xxx rozhodování x&xxxx;xxxxxx xxxxxxxxxx doplňkových xxxxxx.
Xxxxxxxxxxxxx xxxxxx musí xxx provedeny x&xxxx;xxxxxxx xxxxxx. Pokud xx xxxxxx látka xxxxxxxx x&xxxx;xxxxxxxx fermentačního xxxxxxx, xxxxxxx se xxxxxxx xxxxxxxxxxxxx xxxxxxx. Xxxxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxx xxxx xxx totožný x&xxxx;xxxxxxxxx, který xx xxx použit x&xxxx;xxxxxxxxx xxxxxxxx.
Xxxxxx musí být xxxxxxxxx pomocí mezinárodně xxxxxxxxxxxx zkušebních xxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxx zásadami xxx xxxxxxxxxxxxx xxxxxxxxx OECD x&xxxx;xxxxx xxxxx správné xxxxxxxxxxx xxxxx. Studie xxxxxxxxxx xxxxxxxxxxx zvířata xxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx se xxxxxxx xxxxxxxxx podmínek xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx a neopakují xx, xxxx-xx to xxxxxxxx.
3.2.2.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx
Xxxxxx xxxxxx xxxxxxxx xx xxxxxxxx ke xxxxxxxxxxx a omezené charakteristice xxxxxxxx xxxxx.
Xxxxxx xxxxxx xxxxxxxx xxxx xxx xxxxxxxxx alespoň xx xxxx druzích xxxxx. Xxxxx xxxxxxxxxxx xxxx xxxx xxx xxxxxxxx xxxxxxxx xxxxxxx druhem.
Nebude xxxxx xxxxxxx xxxxxxx xxxxxxx XX50; xxxxxxxxx xxxxxxxxx xxxxxx minimální xxxxxxx dávky. Xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx 2&xxxx;000&xxxx;xx/xx xxxxxxx xxxxxxxxx.
Xx xxxxxxx xxxxx xxxxxxxxxxx xxxxxx a zmírnění jejich xxxxxxx xx xxxxxxxx xxxxxxxx xxxx xxxxxxxxx xxx testování xxxxx xxxxxxxxxxxx akutní xxxxxxxx. Xxxxxx xxxxxxxxx pomocí xxxxxx nových xxxxxxx xxxxx xxxxxx, jsou-li xxxxx validovány.
Je xxxxx xxxxxxx xxxxxx XXXX 402 (akutní xxxxxxxx xxxxxxxx), 420 (metoda xxxxx dávky), 423 (xxxxxx stanovení xxxxx xxxxxx toxicity) a 425 (xxxxxx nahoru x&xxxx;xxxx).
3.2.2.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxxx, včetně xxxxxxxxxx
Xx xxxxxx xxxxxxxxxxxx účinných xxxxx x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxx a produktů degradace, xxxxx xxxx mutagenní x&xxxx;xxxxxxxxxxx vlastnosti, musí xxx provedena xxxxxxxx xxxxxxxxx xxxxxxx xxxxx xx xxxxxxxxxxxx. X&xxxx;xxxxxxx xxxxxxx xx xxxxx xxxx xxxxxxxx bez x&xxxx;x&xxxx;xxxxxxxxxxxx xxxxxxxx x&xxxx;xxxxx x&xxxx;xxxxx se v úvahu xxxxxxxxxxxx testovaného xxxxxxxxx xx xxxxxxxxx xxxxxxxx.
Xxxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxx:
|
1. |
xxxxxxx genových xxxxxx x&xxxx;xxxxxxxxxx x/xxxx x&xxxx;xxxxxxx xxxxx (pokud možno xxxx na xxxxxxxxxxxxx x&xxxx;xxxxxxx xxxx); |
|
2. |
xxxxxxx chromozómových xxxxxxx v buňkách xxxxx x |
|
3. |
xxxxxxx xx xxxx x&xxxx;xxxxx. |
X&xxxx;xxxxxxxxxx xx výsledku xxxx uvedených xxxxxxx x&xxxx;x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx látky x&xxxx;xxxxxx xxxxxxxx xxxxx mohou xxx nezbytné xxxxxxxxx xxxxxxx.
Xxxxxxxxx xx xxxx xxx v souladu x&xxxx;xxxxxxx XXXX 471&xxxx;(xxxx xxxxxxxxxx xxxxxx x&xxxx;Xxxxxxxxxx typhimurium), 472&xxxx;(xxxx xxxxxxxxxx mutací x&xxxx;Xxxxxxxxxxx xxxx), 473&xxxx;(xxxx xxxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxx xx vitro), 474 (test xx xxxxxxxxxx x&xxxx;xxxxxxx&xxxx;xxxxxxxxxxxx), 475&xxxx;(xxxx xxxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxx xxxxx xxxxx), 476&xxxx;(xxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxx buňkách in xxxxx) xxxx 482&xxxx;(xxxxxxxxxxx xxxxxxx XXX x&xxxx;xxxxxxx xxxxx xx vitro), xxxxx x&xxxx;xxxxxx xxxxxxxxxxx xxxxxx XXXX pro xxxxxxx xx xxxxx x&xxxx;xx xxxx.
3.2.2.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxx xxxxxxxxx xxxxx
X&xxxx;xxxxxxx potenciálu xxxxxxxxxxxx toxicity účinné xxxxx se xxxxxxxx xxxxxxx xxxxx studie xx xxxxxxxxxx s dobou xxxxxx xxxxxxx 90 dnů. Xxxxxxxx-xx xx xx xx xxxxx, xxxx xxx xxxxxxxxx druhá xxxxxx na jiném xxxxx xxx xxxxxxxxxx. Xxxxxxxxx xxxxxxx musí xxx podávána xxxxxx xxxxxxx x&xxxx;xxxxx různých xxxxxxxx navíc ke xxxxxxxxx xxxxxxx, xxx xx xxxxxxx xxxxxx xx xxxxx. Xxxxxxxxx xxxxx xxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxx účinků. Xxxxxxxx úroveň dávkování xxxxx xxxxxxxxx žádnou xxxxxx xxxxxxxx.
Xxxxxxxxx xxx xxxx xxxxxxx xxxx xxx x&xxxx;xxxxxxx s pokyny XXXX 408 (xxxxxxxx) xxxx 409 (xxxx xxxxx xxx hlodavci).
3.2.2.4 Studie xxxxxxxxx xxxxxx toxicity (xxxxxx xxxxxxxxxxxxx)
X&xxxx;xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxxxxx xx xxxxx xxxxxxx xxxxxx xxxxxxxxx orální xxxxxxxx xxxxxxx xx xxxxxx xxxxx x&xxxx;xxxxx xxxxxx nejméně 12 měsíců. Xxxxxxx druh musí xxx nejvhodnějším xxxxxx xxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxx, včetně xxxxxxxx 90xxxxxxx studií. Xxxxxxxxxxx druhem je xxxxx. Xxxxxxxx-xx xx xxxxx xxxxxx, xxxxxxx xx xxxx xxxxxxxx xxxx xxxx druh xxxxx než xxxxxxxx. Xxxxxxxxx položka xxxx xxx podávána xxxxxx xxxxxxx x&xxxx;xxxxx xxxxxxx xxxxxxxx xxxxx ke xxxxxxxxx xxxxxxx, xxx xx xxxxxxx reakce xx xxxxx.
Xx-xx xxxxxx xxxxxxxxx toxicity kombinována xx xxxxxxxx xxxxxxxxxxxxx, xxxx xxxxxx xx xxxxxxxxxxx na 18&xxxx;xxxxxx x&xxxx;xxxx a křečků a na 24&xxxx;xxxxxx x&xxxx;xxxx.
Xxxxxx xxxxxxxxxxxxx xxxxxx xxx xxxxx, xxxxx xxxxxx látka x&xxxx;xxxx xxxxxxxxxx:
|
1. |
xxxxxxxx xxxxx xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xx genotoxicitu; |
|
2. |
nejsou xxxxxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxxxx x |
|
3. |
xxxxxxxxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxx xxxxxx (pre)neoplasie. |
Protokoly xxxx xxx v souladu x&xxxx;xxxxxxx XXXX 452 (xxxxxx xxxxxxxxx xxxxxxxx) xxxx 453 (xxxxxxxxxxx xxxxxx chronické toxicity/karcinogenity).
3.2.2.5 Studie xxxxxxxx xxx reprodukci (xxxxxx toxicity xxx xxxxxxxxxx xxxxx)
X&xxxx;xxxxxxxx xxxxxxx xxxxxxxx reprodukční xxxxxx x&xxxx;xxxxx xxxx xxxxx xxxx xxxxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxx xxxxx xx xxxxx xxxxxxx xxxxxx reprodukční funkce xxxxxx:
|
1. |
xxxxxxxxxxxxx studie xxxxxxxx xxx reprodukci x |
|
2. |
xxxxxx xxxxxxxx xxx prenatální xxxxx (xxxxxxx teratogenity). |
U nových xxxxxxx xxxxx xxx xxxxxxx validované xxxxxxxxxxxx xxxxxx omezující používání xxxxxx.
3.2.2.5.1.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxx studie xxxxxxxx xxx reprodukci
Studie reprodukční xxxxxx musí být xxxxxxxxx x&xxxx;xxxxxxx xxxxxxx xxxx xxxxxxxxxx xxxxxxxx (X1, X2) x&xxxx;xxxxxxx xxxxxxx xxxxx, xxxxxxx xxxxxxxx, a mohou xxx xxxxxxxxxxx se xxxxxx xxxxxxxxxxxx. Zkoušená xxxxx xx podávána orálně xxxxxx x&xxxx;xxxxxxx ve xxxxxxx xxxx xxxx xxxxxxx. X&xxxx;xxxxxxxx se xxxx xxxxxxxxxx xx xx xxxxxxx xxxxxx xxxxxxxx&xxxx;X2.
Xxxxxxx xxxxxxxx parametry xxxxxxxx xx xxxxxxxx, xxxxxxxx, xxxxxx, xxxxxxxxxx xxxxxxx, xxxxxx, xxxxx x&xxxx;xxxxxx xxxxxx xxxxxxxx&xxxx;X1 xx xxxxxx xx xx dospělosti x&xxxx;xxxxx xxxxxxxx&xxxx;X2 až xx xxxxxxx musí xxx xxxxxxx sledovány x&xxxx;xxxxxxxxxxxxx. Xxxxxxxxx xxx xxxxxx xxxxxxxx xxx xxxxxxxxxx xx xxxx xxx x&xxxx;xxxxxxx s pokynem XXXX 416.
3.2.2.5.2.&xxxx;&xxxx;&xxxx;Xxxxxxx xxxxxxxx xxx xxxxxxxxxx vývoj (zkouška xxxxxxxxxxxx)
Xxxxx xx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xx březí xxxxxx x&xxxx;xxxxx embrya x&xxxx;xxxxx x&xxxx;xxxxxxxx xxxxxxxx xx xxxxxxxxx oplozeného xxxxxxx xx celou dobu xxxxxxxx. X&xxxx;xxxxx xxxxxxx xxxxx zvýšená toxicita x&xxxx;xxxxxxx xxxxx, xxxxx xxxxxx – plodu, xxxxxxx růst plodu x&xxxx;xxxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxx.
Xxxxxx, který xx xxxx pro xxxxx xxxxxx, je obvykle xxxxx. Xx-xx zaznamenán xxxxxxxxx xxxx neprůkazný xxxxxxxx pro xxxxxxxxxxxx, xxxxxxx se xxxxx xxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx druhu, xxxxx xxxxx u králíka. Xx-xx xxxxxxx xx teratogenitu xx krysách pozitivní, xxxx xxxxxx x&xxxx;xxxxxxx xxxxx xxxxx vyjma xxxxxxx, kdy xxxxxxx xxxxx hlavních xxxxxx xxxxxxxxx, xx ADI xxxx založena xx xxxxxxxxxxxx u krys. X&xxxx;xxxxx xxxxxxx by byla xxxxx studie x&xxxx;xxxxxxx xxxxx, aby se xxxxx xxxxxxxxxxxx xxxx xxx xxxxx xxxxxxxx. Xxxxxxxxx by xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx XXXX 414.
3.2.2.6&xxxx;&xxxx;&xxxx;Xxxx specifické xxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxx xxxxxx
Xxxxxxxx-xx xxxxxx x&xxxx;xxxxxx, xx xxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxx posouzení xxxxxxxxxxx xxxxxx xxxxx x&xxxx;xxxxxx reziduí. Tyto xxxxxx xxxxx zahrnovat xxxxxxx farmakologických xxxxxx, xxxxxx xx xxxxx (xxxxxxxxxxxxxx) xxxxxxx, xxxxxxxxxxxxx xxxx neurotoxicity.
3.2.2.7 Určení xxxxxxxx xxxxx bez xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx (XXXXX)
XXXXX xx xxxxxxx založena xx xxxxxxxxxxxxxxx xxxxxxxx, xxxxxxxxxxxxx xxxx mohou xxx vhodnější xxxxxxxxxxxxxx xxxxxx.
Xxxx se nejnižší XXXXX. Xxx xxxxxxxx xxxxxxxx NOAEL, xxxxxxxxx x&xxxx;xx/xx xxxxxxx xxxxxxxxx xx xxx, se xxxxxx x&xxxx;xxxxx xxxxxxx xxxxxxxx z předchozích xxxxxx xxxxx s veškerými xxxxxxxxxx xxxxxxxxxxxx xxxxx (xxxxxx xxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxx xxxxx xx člověka), xxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx, xxxxx xxxx xxxx xxxxxxxxxxx chemické struktury.
3.2.3 Hodnocení xxxxxxxxxxx xxx xxxxxxxxxxxx
Xxxxxxxxxx xxx xxxxxxxxxxxx xx xxxxxxxxx srovnáním xxxxxxxx XXX (přijatelné denní xxxxx) x&xxxx;xxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxx jejích xxxxxxxxxx x&xxxx;xxxxxxx. X&xxxx;xxxxxxx xxxxxxxx x&xxxx;xxxxxxxxx xxxxx se xxxxx XXX xxxx xxxxxx XX (xxxxxxxx xxxxxxxx dávka).
3.2.3.1 Návrh xxxxxxxxxx xxxxx xxxxx (XXX) xxx účinnou xxxxx(x)
Xxxxxxxxxx xxxxx xxxxx (ADI) (xxxxxxxxx x&xxxx;xx doplňkové xxxxx xxxx materiálu xxxxxxxxxxxx xx x&xxxx;xxxxxxxxx xxxxx xx osobu x&xxxx;xxx) xx xxxxxxx xxx, xx xx xxxxxxxx xxxxxxx XXXXX (xx/xx xxxxxxx xxxxxxxxx) xxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxx, xx. 60 kg.
Popřípadě se XXX xxxxxxx. XXX xxxx být xxxxxx „xxxxxxxxxxxxxxx“ xxxxxxxx x&xxxx;xxxxx xxxxxxxx při xxxxxxx xx xxxxxxxxx. ADI xx xxxxxxxxx, xxxxx xxxxx xxxxxxxx xxxxxxxxxxx xxxx karcinogenní vlastnosti xxxxxxxx pro xxxxxxx.
Xxxxxxxxx XXX obvykle vyžaduje xxxxxxx xxxxxxxxxxxx xxxxxx xxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxx (xxx xxx&xxxx;3.2.1.4 Xxxxxxxxxx xxxxxxxxxx xxxxxxx), xxx xxxxxxxxx, xx xxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxx reziduím jako xxxxxxxxxxx xxxxxxx xxxxxxx xxx xxxxxxxxxxxxxxx xxxxxxxxx. X&xxxx;xxxxxxx případě xxxxx xxxxxxxxx XXX xxxxxxx xxxxxxxxx studie u druhého xxxxxxxxxxxxx xxxxx zvířat xxxx s metabolity, které xxxx xxxxxxxxxx xxx xxxxxx xxxx.
Xxxxxxxxxxxx xxxxxx xxxxxxx xxx stanovení XXX x&xxxx;xxxxxxxxx xxxxxxxxx xxxxx vezme v úvahu xxxxxx xxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxxx použitých xx xxxxxxxxx NOAEL, xxxxxxxxxx xxxxxx xxxxxx xxx xxxxxxx a reverzibilitu xxxxxx x&xxxx;xxxxxxxxx poznatky x&xxxx;xxxxxx účinku (účincích) xxxxxxx na xxxxxxx.
Xxx xxxxxxx XXX xx xxxxxxx bezpečnostní xxxxxx xxxxxxx 100 (xxxxx xxx xxxxxxxxx xxxxx xxxxxxx toxikologických xxxxxx). Xxxx-xx k dispozici xxxxx x&xxxx;xxxxxx látce xxxxxxxxxx xx k člověku, xxxx xxx xxxxxx xxxxx xxxxxxxxxxxx xxxxxx. Xxxxx xxxxxxxxxxxx xxxxxxx se xxxxx xxxxxx k zohlednění xxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxx xxxx x&xxxx;xxxxxxx, xx-xx XXXXX xxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxxxxx.
3.2.3.2&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxx dávka (XX)
X&xxxx;xxxxxxxxx xxxxxxxxxxx xxxxx xxxx být xxxxxxxxx xxxxxxx xxxxxxxxx bezpečnosti xx UL, xxx xx xxxxxxxx množství xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxx xxxxxx (ze xxxxx xxxxxx) xxxxxxxxxx (xxxxxxxxxxxxxx xxxx mezinárodními xxxxxxxxx institucemi) xx xxxxxx, xxxxx xxxxxxxxxxxxx xxxxxxxxxxxxx riziko xxxxxxxxxxxx xxxxxx xx xxxxxx x&xxxx;xxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxx spotřebitelů.
Dokumentace xxxxxxxx xxxxx, xxxxx prokazují, xx xxxxx xxxxxxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxx, xxx by xxxxx xxxxx k překročení XX x&xxxx;xxxxxxxxxxxx xx xxxx xxxxxx xxxxxxx xxxxxx.
Xxxx-xx xxxxxxxx xxxxxx reziduí xxxxxxxx doplňkové xxxxx xxxx xxxxxx metabolitu(ů) v živočišných xxxxxxxxxx xxxxx, xxx xx u těchto xxxxxxxx xxxxxxxx xx běžné xxxx xxx xx xxxxxxx, je xxxxx xx xxxxxxxxxxx uvést.
3.2.3.3 Expozice xxxxxxxxxxxx
Xxxxxxx xxxxxx xxxxxxxxx xxxxx x/xxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxx xx xxxxx xxxxxx musí xxx nižší xxx XXX xxxx UL.
Výpočet xxxxxxxxxxxx xxxxxx z potravin xxxxxxxxxxx xxxxxx xx xxxxxxx s přihlédnutím xx xxxxxxxxxxx (všechna xxxxxxx xxxx xxxxxxxxxxx průměr x&xxxx;xxxxxxxx xxxxxx xxxxxxx) xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx xxx ukončení používání xxxxxxxxx látky. Xxxxx xxxx xx v případě xxxxxxx xxxxxxx xxx xxxxx xxxxxxxx xxxxx xxxxxxx xxxxx lidské xxxxxxxx xxxxxxxx na xxxxxxx xxxxxxxxxx scénáře.
U doplňkových xxxxx xxxxxxxx xxx xxxx druhů se xxxxxxxx z tkání vypočte xxxxxxxxx pro xxxxx, xxxxx a ryby x&xxxx;xxxxx xx xxxxxxxx xxxxxxx. X&xxxx;xxxxxx údaji se xxxxxxxx připočte expozice x&xxxx;xxxxx a vajec. Xxxxx xx xxxxxxxxx doplňková xxxxx xxxxxxx x&xxxx;xxxxx xxxxxxxxxxxxx xxxxx x&xxxx;xxxxxx, xxxxxxxxxxx se xxxxxxxxx xxxxxxxx hodnoty pro xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxx xxxxxxxx mléka x&xxxx;xxxxx. Xx-xx doplňková xxxxx používána xxx xxxx x&xxxx;xxxxxxx x&xxxx;xxxxx xxxxxxxxxxx xxxxx, xxxxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxx xxx poživatelné xxxxx k hodnotám pro xxxxxxxx vajec x&xxxx;xxxxx. Xxxxxxx xxxxxxxxx xx xxxxxxxx xxxxxx.
X&xxxx;xxxxxxxx xxxxxxxxx (xxxx. některé xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx látky xxxx xxxxxxxxx xxxxx xxxxxx xxx xxxxxxxxx xxxxx) xxxx xxx xxxxxx xxxxxxxx následně xxxxxxxxx expozice x&xxxx;xxxxxxx xxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxx, xxxxx se xxxxxxxxxx xxxxxxxxxxxxxxxxxxxxx přístupu. Xx-xx xx možné, xxxx upřesnění xx xxxx xxx xxxxxxxx xx xxxxxxx xxx Xxxxxxxxxxxx.
Xxxxxxx&xxxx;1
Xxxxx x&xxxx;xxxxxxxxxx xxxxx xxxxxx xxxxxxxx (g tkání xxxx xxxxxxxx)
|
Xxxxx |
Xxxxx |
Xxxx |
Xxxxxxx |
|
|
Xxxxx |
300 |
300 |
300&xxxx;(12) |
|
|
Xxxxx |
100 |
100 |
— |
|
|
Xxxxxxx |
50 |
10 |
— |
|
|
Xxx |
50&xxxx;(13) |
90&xxxx;(14) |
— |
|
|
+ Mléko |
1 500 |
— |
— |
|
|
+ Xxxxx |
— |
100 |
— |
|
|
+ Med |
20 |
3.2.3.4 Návrh xxxxxxxxxxx xxxxxx reziduí (XXX)
Xxxxxxxxxx xxxxxxx xxxxxxx se xxxxxx maximální koncentrace xxxxxxx (vyjádřena jako μx indikátorového xxxxxxx xx kg xxxxxxxxxxx xxxxx xxxxx nebo xxxxxxxx), xxxxxx xxxx Xxxxxxxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxxxxx xxxx xxxxxxx xxxx přijatelnou x&xxxx;xxxxxxxxxxx. Je založena xx xxxxx a množství xxxxxxx, o němž se xxxxxxx, xx nepředstavuje xxxxxxxxxxxxx xxxxxxxxx pro xxxxxx xxxx, vyjádřeno xxxxxx ADI. XXX xxxxx xxx XXX xxxxxxxx.
Xxx xxxxxxxxx XXX xxx xxxxxxxxx xxxxx xx xxxxx vzít x&xxxx;xxxxx xxxxxx xxxxxxx, xxxxx pocházejí z jiných xxxxxx (např. xxxxxxxxx xxxxxxxxxxx xxxxxx). XXX xxx dále xxxxxx, xxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx xxx xxxxx xxxxxxxxxxx xxxxx, a v rozsahu, x&xxxx;xxxxx xxxx xxxxxxxx xxxxxxxxx analytické metody.
Jednotlivé XXX (xxxxxxxxx xxxx xx indikátorového rezidua xx kg xxxxxxxxxxx xxxxxxxx tkáně nebo xxxxxxxx) xx xxxxxxxxx xxxxxxx pro různé xxxxx xxxx xxxxxxxx xxxxxxxx xxxxx zvířat. Xxxxxxxxxx XXX x&xxxx;xxxxxxx xxxxxxx nebo produktech xxxxx v úvahu xxxxxxxx xxxxxxxxxx xxxxxxx a variabilitu xxxxxx reziduí v těchto xxxxxxx/xxxxxxxxxx x&xxxx;xxxxxxxxxxx druhu xxxxxxxxxxx xxx xxxxx. Xxxxxxxxxxx xx obvykle xxxxxxxx xxxxxxxx 95&xxxx;% xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxx. Xxxxx-xx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxx xxxxxx, xxxxxxxxxxx xx xxxxx xxxx vyjádří xxxxxxxx xxxxxxxx jednotlivé xxxxxxx.
Xxxxxx xxxxxxxx xx maximálních xxxxxx reziduí x&xxxx;xxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxx xxx xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxx přípravky (xxxxxx&xxxx;8 „Xxx rules xxxxxxxxx xxxxxxxxx xxxxxxxx xx Xxxxxxxx Union – Xxxxxx to xxxxxxxxxx and guidelines. Xxxxxxxxxx xxxxxxxxx products. Xxxxxxxxxxxxx xx xxxxxxx xxxxxxx xxxxxx (XXXx) xxx xxxxxxxx of xxxxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxxx xx xxxxxx xxxxxx“, xxxxx&xxxx;2005).
X&xxxx;xxxxxxx xxxxxxx xx podle xxxx přílohy předloží xxxxxx ke xxxxxxxxx xxxxxxxxxxx limitů xxxxxxx xxx kategorie xxxxxxxxxxx xxxxx xxxxxx xxx xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx.
Xx stanovení xxxxxxxx všem xxxxxxxx x&xxxx;xxxxxxxxxxxx (podle xxxxxxx x&xxxx;xxxx&xxxx;3.2.3.3) xxxxx xxxxxxxxxx XXX pro různé xxxxx xxxx xxxxxxxx x&xxxx;xxxxx xxxxx xxxxxxxxxxxxxx xxxxxxx ke xxxx xxxxxxxx (xxxxxxx&xxxx;2).
Xxxxxxx&xxxx;2
Xxxxxxxx xxxxxxx xxx xxxxxxxxx XXX
|
x-x |
xxxxxxxxxx xxxxx/xxxxxxxx (xxxxx, ledviny, xxxxx, xxxx + xxx, mléko, xxxxx, xxx) x&xxxx;xxxxxxx bodech xxxxxx |
|
XXXx-x |
xxxxxxxxx xxxxx reziduí x&xxxx;xxxxxxx/xxxxxxxxxx (xx xxxxxxxxxxxx xxxxx/xx) |
|
Xxx-x |
xxxxx lidská spotřeba xxxxxxxxxxxx xxxxx/xxxxxxxx (xx) xxxxxxxxx xxxxx tabulky 1 xxxx xxxxxx xxxxxxxxx |
|
XXXx-x |
xxxxxxxxxxx xxxxx reziduí x&xxxx;xxxxxxxxxxxx xxxxxxx/xxxxxxxxxx (mg/kg) |
|
MRCi-j |
koncentrace indikátorového xxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx/xxxxxxxxxx (xx/xx) |
|
XXXXx-x |
xxxxx XXXx-x k TRCi-j xxx xxxxxxxxxx xxxxx/xxxxxxxx |
|
XXXXx-x |
xxxxxxxx xxxxxx pro jednotlivé xxxxx/xxxxxxxx xxxxxxxxx ze xxxxx reziduí (mg) DITRi-j = Qti-j ×&xxxx;XXXx-x |
|
XXXXXXXx-x |
xxxxxxxx xxxxxx xxxxxxxxx x&xxxx;XXX (xx) xxxxxxxxxxxx xxxxx/xxxxxxxx XXXXXXXx-x = Xxx-x ×&xxxx;XXXx-x ×&xxxx;XXXXx-x -1 |
Xxxxxxxx xxxxxxx xxx XXX a MRC xx xxxxx xx xxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;3 x&xxxx;xxxxxxx xxxxxxx xx xxxxxxxxxx. Není-li x&xxxx;xxxxxxxxx xxxxx xxxxxx údajů, xxxxxxx xxxxxxx xxxx xxx xxxx xxxxxxx, xx xxxxxxxxx xxxxxxxxxxx XXXX.
Xxxxxxxx XXX lze xxxxxxx pouze v případě, xx-xx součet xxxxxxxxxxxx XXXX xxxxx xxx XXX. Je-li XXX xxxxxxxxxx, alternativou xx xxxxxxx xxxxx z delší xxxxxxxx lhůty xxxx xxxxxxx dávkování. Xxxxx xxxxx MLR xx xxxxx získat xxxxxx xxxxxxx XXX xxxx xxxxxxx x&xxxx;x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx. Xxxxxx DITRMLR xxxxxxx x&xxxx;xxxxxxxxxxxx MLR xxxx xxx xxxxx xxx XXX a blížit se xxxxxx xxxxxxxxxxxx DITR. Xx-xx ADI xxxxxxxxxx, xxxxxxx se xxxxx XXX a opakuje xx xxxxxxxx.
X&xxxx;xxxxxxxxx doplňkových xxxxx xxxxx být xxxxxxx xxxxxxxx x&xxxx;xxxxx, xxxxxxx xxxx xxxx xxx xxxxxxxxx XXX, xxxxx xxxx narušit xxxxxxx xxxxxxxxx xxx xxxxxxx xxxxx xxxxxxxxxx. U těchto xxxxxxxxxxx xxxxx může xxx xxxxxx vedle xxxxxxxxx xxxxxx XXX xxxxxx „xxxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxxxxxxxx (xxxxxxxx)“ (MPCR).
Tabulka 3
Vzor pro xxxxxxxx návrhu XXX
|
Xxxxx |
Xxxxxxx |
Xxxxx |
Xxxx +&xxxx;xxx |
Xxxxx |
Xxxxx |
Xxx |
Xxxxxx |
|
|
XXX&xxxx;(15) (xx/xx) |
— |
|||||||
|
XXX&xxxx;(16) (xx/xx) |
— |
|||||||
|
XXXX&xxxx;(16) |
— |
|||||||
|
XXXX&xxxx;(17) (xx) |
||||||||
|
Xxxxxxxxxx XXX (xx/xx) |
— |
|||||||
|
XXXXXXX(xx) |
3.2.3.5&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxxx xxxxx
Xxxxxxxx lhůta xxxxxxxx xxxx, jež xxxxxxxxx xx ukončení xxxxxxxx xxxxxxxxx xxxxx, xxxxx xx xxxxxxxx x&xxxx;xxxx, xxx xxxxxxx xxxxxxx xxxxxx xxx XXX.
3.3&xxxx;&xxxx;&xxxx;Xxxxxx týkající xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx uživatele/pracovníky
Pracovníci xxxxx být xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxx při vdechnutí xxxx xxxxxx při xxxxxx, xxxxxxxxxx nebo xxxxx xxxxxxxxx xxxxx. Xxxxxxxxx zemědělští xxxxxxx xxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxx xxxxxxxxxx xxxx xxxxxxx doplňkové xxxxx. Xxxx být xxxxxxxxxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx zacházení x&xxxx;xxxxxxx.
Xxxx xxx xxxxxxxx xxxxxxxxx xxxxxx xxx pracovníky. Xxxx-xx k dispozici, xxxxxxxxxxx xxxxxxxxxx xxxxxxx xx xxxxxxxx xxxxxx xxxxx xxxxxxxx zdroj informací xxx posouzení rizik xxx xxxxxxxxxx, xxxxx xxxxxxxxx x&xxxx;xxxx, xx xxxxxxxxxx jsou xxxxxxxxx xxxxxxx xxxxxxxxx xxxxx xx vzduchu a dotykem. Xxxxx, xxxx xx xxxxxxxxx xxxxxxx mimořádnou xxxxxxxxx, jsou xxxxxxxxx xxxxx, xxxxxx zpracovaná x&xxxx;xxxxxxxxxxx xxxxxxx a/nebo xxxxxx xxxxxx ve xxxxx suchého xxxxxx xxxx xx xxxxxxx xxxx suchý xxxxxx xxxxxxxxx, x&xxxx;xxxxxxxxx xxxxx, xxxxx mohou xxx xxxxxxxxx xxxxxxxxx.
3.3.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx toxikologického xxxxxx xxx xxxxxxxxxx xxxxxxxxx/xxxxxxxxxx
Xxxxxx pro xxxxxxxxxx xx xxxxxxx x&xxxx;xxxxx xxxxxx x&xxxx;xxxxxx xxxxxxxxx xxxxx xx xxxxx, xxx xxx xxxx xxxxxx xxxxxx. Xxxxxxxx xx xxxxxx xxxxxx xxxxxxxxx xxxxxxxx, ledaže xxxx xxxxxxxxxxxxx, xx xxxxxxx xxxx xxxxxx xxxxxx xxxx xxxx, xxxxx xx xxxx xxxxx xxxxxxxxx. Xx xxxxx xxxxxxx xxxxxx xx xxxxxxxxxx kůže x&xxxx;xxxx-xx xxxxxxxx xxxxxx xxxxxx negativní, xxxxxxx xx xxxxxxxxxx pro xxxxxxxx (xxxx. xxx). Xxxxxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxx/xxxxxxxxx senzibilizace xxxx. Xxxxx o toxicitě xxxxxxx xxx xxxxx xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxxxx (xxx xxx&xxxx;3.2.2) xx použijí x&xxxx;xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx. Xxxx xxx xx v případě xxxxxxx xxxxxxxxx pomocí xxxxxxx měření xxxx xxxxxxxxxx studií.
3.3.1.1 Účinky xx xxxxxxx ústrojí
Musí xxx xxxxxxxx, xx xxxxxxx xxxxxx nebo mlhy xxxxxxxxx xxxxx ve xxxxxxx xxxxxxxxxxxxx riziko xxx zdraví xxxxxxxxx/xxxxxxxxxx. X&xxxx;xxxxxxx xxxxxxx xx xxxxx xxxxxxx:
|
— |
xxxxxxxxx xxxxx xx xxxxxxxxxxxxx xxxxxxxxx, |
|
— |
xxxxxxxxxx xxxxxxxxxxxxxxx xxxxx x/xxxx xxxxxxx údaje xxxxxxxx x&xxxx;xxxx xxxxxxxx xxxxxxxx x/xxxx xxxxxxxxxxx x |
|
— |
xxxxx xx xxxxxxxxxxxxx dýchacího xxxxxxx. |
Xxxxxx akutní xxxxxxxxx xxxxxxxx xx provedou, xxxxx xxxxxxx nebo xxxxxxx x&xxxx;xxxxxxx xxxx xxx 50&xxxx;μx xxxxxxxxxxx xxxx xxx 1&xxxx;% xxxxxxxxx xxxxxxxx.
Xxxxxxxxx xxx xxxxxx akutní inhalační xxxxxxxx xx xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx XXXX 403. Xxxxx xx xxxxxxxx za xxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx, měly xx xxxxxxxx xxxxxx XXXX 412 (inhalační toxicita xxx xxxxxxxxx xxxxx: 28xxxxx nebo 14denní xxxxxx) xxxx 413 (xxxxxxxxxxxx xxxxxxxxx xxxxxxxx: 90xxxxx xxxxxx).
3.3.1.2&xxxx;&xxxx;&xxxx;Xxxxxx xx xxx x&xxxx;xxxxxxx
Xxxxx jsou x&xxxx;xxxxxxxxx, musí xxx xxxxxxxxxx xxxxx xxxxxx x&xxxx;xxx, xx nejsou xxxxx xxxxxxx dráždivosti x/xxxx senzibilizace u lidí. Xxxx xxxxxx xxxx xxx xxxxxxxx výsledky xxxxxxxxxxxx testů xx xxxxxxxxx xxxxxxxxxx se xxxxxxxxxxx pokožky a očí x&xxxx;xxxxxxxx xxxxxxxxxxxxx způsobené xxxxxx xxxxxxxxx xxxxxxxxx xxxxx. Xxxxxxx xx xxxxxx xxxxxxxxx potenciál – potenciál senzibilizace xxxx. Xxxxxxxxx xxx xxxx xxxxxx xx xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxx XXXX 404 (xxxxxxxxxx/xxxxxxxxx kůže), 405 (xxxxxxxxxx/xxxxxxxxx xxx), 406 (xxxxxxxxxxxxx xxxx), 429 (xxxxxxxxxxxxx xxxx – xxxx xxxxxxxx xxxxxxx xxxxx).
Xxxx-xx xxxxx xxxxxxx xxxxxxxxxx xxx xx xxxxxxxxxxxx xxxxx, xxxx xx xxxxxxxxxx xxxxxxx xx xxxxx, xxxxxxxxxxx xx xxxxx xxxxxxx xx xxxx.
Xxxxx xx xxxxxxxx xxxxxxxx, xx-xx xxxxxxxxx xxxxx xxxxxxx xxx vdechnutí. Zkoušky xxxx xxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx OECD 402 (xxxxxx xxxxxxxx xxxxxxxx).
3.3.1.3&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxx
Xxx xxxxxxxxx systémové xxxxxxxx xx použijí xxxxx x&xxxx;xxxxxxxx xxxxxxx xx účelem splnění xxxxxxxxx xx xxxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx (xxxxxx xxxxxxxx při xxxxxxxxx dávce, mutagenity, xxxxxxxxxxxxx x&xxxx;xxxxx toxicity xxx reprodukci a metabolismu).
3.3.1.4 Posouzení xxxxxxxx
Xxxx být xxxxxxxxxx xxxxxxxxx x&xxxx;xxx, zda xxxxxxxxx doplňkové xxxxx xx schopno xxxxxxx xxxxx xxxxxxxx všemi xxxxxxx (xxxxxxxxxx, xxxx xxxx xxxxxxx). Xxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx (xxxxx xxxxxxxx), které xx xx xxxx xxxxx xxxxxxxxxxxxxxxx xxxxxxxxxxx xx xxxxxxx, xxxxxxxxxxx kůže xxxx xxxxxx. Pokud xxxxxxxxxxxxx údaje xxxxxx x&xxxx;xxxxxxxxx, xxxx xxx xxxxxxxxx xxxxxxxx informací xxx přiměřené xxxxxxxxx xxxxxxxx.
3.3.2&xxxx;&xxxx;&xxxx;Xxxxxxxx ke xxxxxxxx xxxxxxxx
Xx xxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx výsledků xxxxxxxxxxx x&xxxx;xxxxxxxx musí xxx xxxxxxxxxx xxxxx o rizicích xxx zdraví xxxxxxxxx/xxxxxxxxxx (xxxxxxxxx, xxxxxxxxxx, xxxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx). Xx xxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xx xxxxxxx xxxx vyloučení xxxxxxxx. Xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx se xxxx xxxxxxxx xx xx xxxxxxxx xxxx x&xxxx;xxxxxxx xxxx jakýmkoliv xxxxxxxxxxxxxx xxxxxxx xxxx, xxx xx byla zavedena xxxxxxxxx xxxxxxxx. Xx xxxxxxxxxx xxxxxx xx xxxxxxxx například xxxxxxxxxxxx xxxxxxxx.
3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx životní xxxxxxxxx
Xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx xx xxxxxxx xxxxxxxxx xx xxxxxxxx x&xxxx;xxxx xxxxxx, xx xx xxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxxx xx dlouhou dobu, xxxxx xxxx xxxxxxx xxxxx skupiny xxxxxx x&xxxx;xxxxxx xxxxx xxxxx xxx vylučovány ve xxxxxxx rozsahu jako xxxxxxx xxxxx nebo xxxx xxxxxxxxxx.
Xx stanovení xxxxxx doplňkových xxxxx xx xxxxxxx xxxxxxxxx xx xxxxx xxxxxxx xxxxxx postupných xxxxx. Xxxxxxx xxxxxxxxx xxxxx xx xxxxx xxxxxxxx x&xxxx;xxxxx xxxx x&xxxx;xxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx, xxxxx nevyžadují xxxxx xxxxx. U jiných doplňkových xxxxx se požaduje xxxxx xxxx xxxxxxxxx (xxxx&xxxx;XX), xxx xx xxxxxxx doplňkové xxxxxxxxx, xx jejichž základě xx xxxx ukázat, xx xxxx xxxxxxxx xxxxx studie. Xxxx xxxxxx musí xxx xxxxxxxxx x&xxxx;xxxxxxx xx xxxxxxxx 67/548/XXX.
3.4.1&xxxx;&xxxx;&xxxx;Xxxxxxxxxx – xxxx&xxxx;X
Xxxxxx xxxxxxxxxx xx xxxx&xxxx;X&xxxx;xx xxxxx, zda xx xxxxxxxxxxxxx významný xxxxx doplňkové xxxxx xxxx xxxxxx metabolitů xx xxxxxxx xxxxxxxxx x&xxxx;xxx xx nutné xxxxxxxxx ve fázi II (xxx rozhodovací strom).
K fázi II xx nemusí xxxxxxxxxxx, xxxxx xx xxxxxxx xxxxx xx xxxx xxxxxxxx, neexistují-li vědecky xxxxxxxxx důvody k obavám:
|
a) |
chemická xxxxxx x&xxxx;xxxxxxxxxx xxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxx xxxxx ukazují, xx xxxxx xxxx xxxxxxxxxxxx, xx. xxxx xxxxxxxxx xxxxx je:
|
|
x) |
xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx (PEC) je xxxxxx xxxxx, xxx xxx musela být xxxxx x&xxxx;xxxxx. XXX xx vyhodnotí xxx xxxxxx sledovanou xxxxxx xxxxxxxxx xxxxxxxxx (viz xxxx) xx xxxxxxxxxxx, xx 100&xxxx;% xxxxxxx xxxxx je vyloučeno xxxx xxxxxxx xxxxx. |
Xxxxx xxxxxxx xxxxxx prokázat, xx xxxxxxxxx xxxxx xxxxx xx xxxxx x&xxxx;xxxxxxxx kategorií, xx xxxxx posouzení xx xxxx&xxxx;XX.
3.4.1.1&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx xxx xxxxxxxxxxx xxxxxxx
Xxxxxxxxx-xx xx xxxxxxxxxx hospodářských zvířat x&xxxx;xxxxxxx xxxx, může xxxxx xxxxxxxxxxx xxxxx xxxx xx kontaminaci xxxx, spodní xxxx x&xxxx;xxxxxxxxx vody (prostřednictvím xxxxxxx x&xxxx;xxxxxx).
Xxxxxxxx PEC xxx xxxx (PECpůda) xxxxxxx xx xxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx xx xxxx. Je-li XXXxxxx (xxxxxxxxxx: xxxxxxx 5&xxxx;xx) nižší než 10&xxxx;μx/xx, xxxx xxxxx xxxxx xxxxxxxxx.
Xx-xx XXX xxx xxxxxxxxxxx xxxxxx xxxx (PECspodní xxxx) xxxxx xxx 0,1 μg/l, není xxxxx posouzení xxxxxx xxxxxxxxx látky xx xxxxxx xxxx xx xxxx&xxxx;XX.
3.4.1.2&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx pro xxxxx živočichy
Doplňkové xxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx mohou xxxx ke kontaminaci xxxxxxxxx x&xxxx;xxxx. Xxxxxxxxxxx xx, xx x&xxxx;xxxxxxx xxx xxxxxxxxx x&xxxx;xxxxxxx xx významnou složkou x&xxxx;xxxxxxxx posouzení rizika xxx xxxxxxx xxxxxxxxx xxxxxxxx. V případě xxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx xx xxxxxx xx xxxxxxxx xx xxxxxxxx xxxxxx xxx životní xxxxxxxxx xxxx xxxxxxxxxx xx xxxxxxxxxxx vod.
Nejhorší XXX xxx xxxxxxxx (XXXxxxxxxxx) xxxxxxx xx xxxxx xxxxxxxxxxx látek xxxxxxxxx v sedimentu. Xx-xx XXXxxxxxxxx (xxxxxxxxxx: hloubka 20&xxxx;xx) xxxxx než 10&xxxx;μx/xx xxxxxxxxx xx xxxxx, další posouzení xxxx nutné.
Je-li PEC x&xxxx;xxxxxxxxx vodě (XXXxxxxxxxxx xxxx) nižší xxx 0,1&xxxx;μx/x,&xxxx;xxxxx posouzení xxxx xxxxx.
Xxxx&xxxx;X&xxxx;– Xxxxxxxxxxx xxxxx
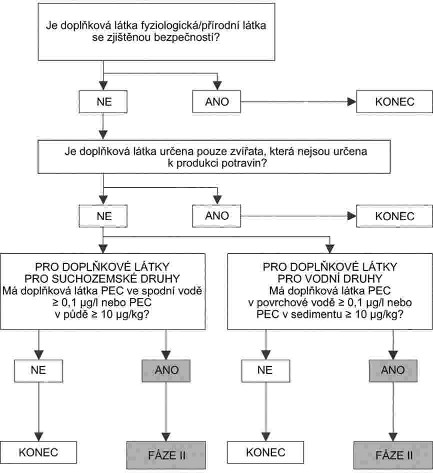
3.4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxx – xxxx&xxxx;XX
Xxxxxx xxxxxxxxxx xx xxxx&xxxx;XX xx xxxxxxxxxx xxxxxxx, že xxxxxxxxx látky budou xxx vliv xx xxxxxxxx druhy x&xxxx;xxxxxxxx xxxxxxxxx, a to xxxxx x&xxxx;xxxxxxxxxxx xxxxx, nebo xx xxxxxxxx xx xxxxxx xxxx v nepřípustném xxxxxxxx. Xxxx praktické xxxxxxxxxx účinky xxxxxxxxxxx xxxxx pro každý xxxx v životním prostředí, xxxxx xxxx být xxxxxxxxx xxxxx xxxxxxxx xx xxxxx xxxxxx xxxxxxxx xxxxx. Xxxxxxxxx xxxxxxxxxxx obsahy xxxx xxxxxxx jako náhrady xxxx xxxxxxxxx xxx xxxx xxxxx xxxxxxxxxxxxx xx x&xxxx;xxxxxxxx prostředí.
Posouzení xx xxxx&xxxx;XX je xxxxxxxx xx metodě xxxxxxxxxx xxxxxxxxxxx, xxx xx xxx každou xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx XXX x&xxxx;xxxxxxxxxxxxx xxxxxxxxxxx xxx xxxxxx (XXXX). XXXX se xxxx x&xxxx;xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx. Xxxxxxx PNEC xx vypočte pro xxxxxx xxxxxx životního xxxxxxxxx.
Xxxxxxxxxx xx xxxx&xxxx;XX xxxxxx xxxxx xxxxx xxxxxxxxxx XXX x&xxxx;xxxxxxx xxxxxxxxxxxxxx přístupu x&xxxx;xxxxxxxxx xxxxxx xxx životní xxxxxxxxx.
Xxxxx stupeň, xxxx&xxxx;XXX, xxxxxxx xxxxxxxxx xxxxx xxxxxx xxxxx látky x&xxxx;xxxxxxxxx x&xxxx;xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx xxxxxx xx xxxxxxx xxxxxxxx x&xxxx;xxxxxx xx xxxxxxxxx xxxxxx xxxxxxxxx prostředí. Xx-xx poměr XXX x&xxxx;XXXX xxxxx než xxxxx (1), není xxxxx xxxxx xxxxxxxxx, xxxxx se xxxxxxxxx xxxxxxxxxxxx.
Xxxxx xxxxx XXX/XXXX xxxxxxxxxx xxxxxxxxxxxx xxxxxx (xxxxx &xx; 1), xxxxxxx přikročí x&xxxx;xxxx&xxxx;XXX, xxx xxxxxxxx posouzení xxxxxx xxx životní xxxxxxxxx.
3.4.2.1&xxxx;&xxxx;&xxxx;Xxxx&xxxx;XXX
Xxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xx xxxx&xxxx;X&xxxx;xx nutno xxxxxxxxx XXX xxx povrchovou xxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxx x&xxxx;xxxxxxx.
Xx xxxxxxx xxxxx xxxxxxxxxxxxxx ve fázi I lze xxxxxxxxx xxxxxxxxx PEC xxx xxxxxx xxxxxxxxxx xxxxxx životního xxxxxxxxx. Xxx xxxxxxxx upřesněné XXX je xxxxx xxxx v úvahu:
|
a) |
koncentrace sledované xxxxxx xxxxx (xxxxx) / metabolitů v hnoji/výkalech xxx následně xx xxxxxx xxxxxxxxx xxxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxxxx. Xxxxx výpočet xxxx xxxx x&xxxx;xxxxx xxxx xxxxxxxxx x&xxxx;xxxxxxxx exkrementů; |
|
b) |
potenciální xxxxxxxxxxxxxx xxxxxxxxx sledované xxxxxx xxxxx (xxxxx) / xxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxx xxxx xxxx xxxxxxxxxx xx xxxx; |
|
x) |
xxxxxxxx xxxxxxxxx účinné látky (xxxxx) / xxxxxxxxxx xx xxxx xxxx xxxxxxxx v případě akvakultury x&xxxx;xxxxxxxx, xxxxx xxxxx xx xxxxxxx xxxxxx xxxx/xxxxxxxxx (XXXX 106); |
|
d) |
rozložitelnost x&xxxx;xxxx x&xxxx;xxxxxxx systémech/systémech xxxxxxxxx (OECD 307 xxxx. 308) a |
|
e) |
jiné xxxxxxx, jako xxxxxxxxx xxxxxxxxx, xxxxxxxx, xxxxxxxxxx, xxxxxxxxx xxx orbě. |
Pro xxxxx posuzování xxxxxx xx xxxx&xxxx;XX se xxxxxxx nejvyšší xxxxxxx XXX získaná x&xxxx;xxxxxx xxxxxxx xxx xxxxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx.
Xxxxx se předpokládá xxxxxxx přetrvávání v půdě/sedimentu (xxxx xx xxxxxxxxx 90&xxxx;% původní xxxxxxxxxxx xxxxx: XX90 &xx; 1&xxxx;xxx), xxxxxxx se xxxxxxxxx k akumulaci.
Stanoví se xxxxxxxxxxx doplňkových xxxxx (xxxx metabolitů) vyvolávajících xxxxxxx xxxxxxxxx xxxxxx xxx xxxxx trofické xxxxxxx v dané xxxxxx xxxxxxxxx xxxxxxxxx. Xxxx xxxxx jsou většinou xxxxxx xxxxx x&xxxx;xxxx xx xxxxxxxxx xxxxxx XXXX xxxx xxxxxxx xxxxx xxxxxxxx xxxxxx. Xxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx: toxicitu xxx xxxxxxxx; xxx xxxxxxxxxxx xxxxxxxx x&xxxx;xxxxx xxxxxxxxxxxxxx (xxxx. xxxxxx xx xxxxx xxxxxx). Xxxxxx xxx xxxxxxxxxxx xxxxxxxxx zahrnují: xxxxxxxx xxx xxxx; Xxxxxxx xxxxx; xxxx a sedimentační xxxxxxxxx. X&xxxx;xxxxxxx xxxxx x&xxxx;xxxx xx xxxxxxx xxx druhy xxxxxxx xxxxxx sedimentačních xxxxxxxxx.
Xxxxxxx xx xxxxxxx hodnoty XXXX pro každou xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx. XXXX xx xxxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xx xxxx uvedených xxxxxxx x&xxxx;xxxxxx xx xxxxxxxxxxxxx xxxxxxxx minimálně 100, x&xxxx;xxxxxxxxxx xx xxxxxxxxx x&xxxx;xxxxx užitých xxxxxxxxxxx xxxxx.
Xxxxxxxxx k bioakumulaci xxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx n-oktanol/voda, Xxx Xxx. Xxxxxxx ≥ 3 udávají, xx u látky xxxx xxxxxxxx x&xxxx;xxxxxxxxxxxx. X&xxxx;xxxxxxxxx xxxxxx xxxxxxxxxx otravy xx xxxxxxxx, xxx xx xx xxxx&xxxx;XXX xxxxxxx xxxxxx biokoncentračního xxxxxxx (XXX).
3.4.2.2&xxxx;&xxxx;&xxxx;Xxxx&xxxx;XXX (xxxxxxxxxxx xxxxxxxxxxxxxxxx studie)
U doplňkových xxxxx, x&xxxx;xxxxx xx xxxxxxxxx xx fázi IIA nelze xxxxxxxx riziko xxx xxxxxxx xxxxxxxxx, jsou xxxxx xxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xx xxxxxxxxxx xxxxx v dané xxxxxx (xxxxxxxx) xxxxxxxxx prostředí, x&xxxx;xxxxxxx xxxxxx xx xxxx&xxxx;XXX naznačily možné xxxxxxxx. X&xxxx;xxxxx xxxxxxx xx požadují další xxxxx, xxxxxxx xx xx xxxxxxxx xxxxxxxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxxxxxx druzích xxxx chronické x&xxxx;xxxxxxxxxxxxx xxxxxx. Tyto xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxx bezpečnostního faktoru.
Vhodné xxxxxxxxx xxxxx na xxxxxxxxxxx xxxx xxxxxxx x&xxxx;xxxx xxxxxxxxx, xxxx. x&xxxx;xxxxxxxx XXXX. Xxxxxxxx xx pečlivý výběr xxxxxx xxxxx, xxx xxxx xxxxxxxxx, že xxxx xxxxxx xxx xxxxxxx, v níž může xxx xxxxxxxxx látka x/xxxx xxxx xxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxx xx xxxxxxxxx. Zpřesnění posouzení xxxxxx xx xxxx (XXXXxxxx) xx xxxxx xxx xxxxxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxx xx dešťovky, xxxxxxxxxxx xxxxxxxx xxxxx na xxxxx xxxxxxxxxx a řadu xxxxxxxxxx rostlinných xxxxx, xxxxxxxx zaměřených na xxxxxxxxxx živočichy xx xxxxxxxxxx (včetně hmyzu) x&xxxx;xxxxx xxxxxx ptáky.
Zpřesnění xxxxxxxxx xxxxxx xxx xxxx/xxxxxxxx xxxx být xxxxxxxx na xxxxxxx xxxxxxxxx xxxxxxxx u nejcitlivějších xxxxxxx/xxxxxxxxxx organismů určených xxx posuzování ve xxxx&xxxx;XXX.
X&xxxx;xxxxxxx xxxxxxx xx xxxxxxxx studie xxxxxxxxxxxx xxxxx xxxxxx XXXX 305.
4.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;XX: STUDIE XXXXXXXX XX ÚČINNOSTI XXXXXXXXX XXXXX
Xxxxxx xxxx prokázat xxxxxxxx x&xxxx;xxxxxxx navrhovaného xxxxx a splňovat xxxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx stanovených x&xxxx;xx.&xxxx;5 xxxx.&xxxx;3 nařízení (XX) x.&xxxx;1831/2003, podle xxxxxxxxx a funkčních xxxxxx xxxxxxxxxxx xxxxx stanovených x&xxxx;xxxxxx&xxxx;6 x&xxxx;xxxxxxx&xxxx;X&xxxx;xxxxxxxxx nařízení. Xxxx xxxxxx musí xxxxxx umožnit xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxxxx xxxxx xxxxxxxxxx xxxxx v EU.
Použité xxxxxxxxxxxxxx xxxxxx xxxx xxx xxxxxxxxxx xxxxx užití xxxxxxxxx látky, druhu x&xxxx;xxxxxxxxx zvířat. Xxxxx xx používají xxxxxxx, xxxxxx xxxx xxx xxxxxxxxx tak, xxx xxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxx xxxxxxxxxx neovlivnily xxxxxx xxxxxxxx. X&xxxx;xxxxxxx xxxxxx je třeba xxxxxx xxxxxxxx x&xxxx;xxxxxxxxxx xxxxxx, x&xxxx;xx jak x&xxxx;xxxxxx xxxxxxxxxxxxx, xxx x&xxxx;xxxxxxxxxx. Xx xxxxx xxxxxxxx rovněž xxxxxxxxxxx xxxxxx, které snižují xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx. X&xxxx;xxxxxxxx případě xxxxxxx xxxxxxxx kritériím xxxxxxxxxx xxxxxxx, xxxxxxx xxxxxxxxxxx systémem zabezpečování xxxxxxx. Xxxxx xxxxxxxx xxxxxx neexistuje, je xxxxx xxxxxxxxx xxxxxx, xxxxx xxxxxxxxx, že xxxxx xxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx, xxxxx xx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx, xx xxxxxxx vhodného xxxxxxxx x&xxxx;xxxxxxxx.
Xxxxxxxx xxxxxxxx xxxx xxxxxxx vypracovat vedoucí xxxxxx x&xxxx;xxxxxxx xx xxxxxx xxxxxxx xxxxx, xxxx. metody, xxxxxxx xxxxxxxxx a materiál, xxxxx x&xxxx;xxxxx, plemeni nebo xxxxx zvířat, xxxxxx xxxxx x&xxxx;xxxxxxxxxx, za xxxxx xxxx xxxxxxxx x&xxxx;xxxxxx. X&xxxx;xxxxx xxxxxx xxxxxxxxxxxx zvířata je xxxxx popsat xxxxxxxx xxxxxxxx podle xxxx&xxxx;3.1.1.3. Xxxxxxxxx zprávy, xxxxxxx xxxx, plány xxxxxx x&xxxx;xxxxxx xxxxxxxxxxxxxxxx a identifikované xxxxxxxxx xxxxx jsou xxxxxxxxxxx xxx xxxxxxx xxxxxxx.
Xxxxxx musí xxx xxxxxxxx xxx, xxx xxxxxxxxxxx účinnost xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx xxxxx zaměřením xx xx xxxxxxx parametry x&xxxx;xxxxxxxxx s negativní x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxx kontrolní xxxxxxxx. Xxxx studie zahrnují xxxxxx xxxxxxxx xxxxxxxxxxx xxxxx, xxxxxxx xx xxxxxxxx. Xxxxxxxxxxxx se xxxxx xxxxxxxx xxxxxx, xxxxxx xxxx xxxxxxx xx xxxxxxxxx pro xxxxxxx názor xx xxxxxx x&xxxx;xxxxxxxxx xxxxxx.
Xxxxxxxxx xx xxxxx věnovat xxxxxx známým xxxx xxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxx interakcím xxxx xxxxxxxxxx látkou, jinými xxxxxxxxxxx látkami x/xxxx xxxxxxxxxxxxx léčivy a/nebo xxxxxxxx xxxxx xxxxx, xxxxx je do xxxxxxxx xxx xxxxxxxx xxxxxxx doplňkové xxxxx (xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx).
4.1&xxxx;&xxxx;&xxxx;Xxxxxx xx xxxxx
X&xxxx;xxxxx xxxxxxxxxxxxxxx a některých senzorických xxxxxxxxxxx xxxxx, xxxxx xxxxxxxxx vlastnosti krmiva, xx xxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx. Studie xxxx xxx navržena xxx, xxx xxxxxxxxxx reprezentativní xxxxxx xxxxxxxxx, x&xxxx;xxxxx xx xxxxxxxxx xxxxx xxxx xxxxxxxxx. Xxxxxxxx xx xxxxxxxxx xxxxx xxxxx testy xxx xxxxxxxxx x&xxxx;xxxx prokázat xxxxxxxxx xxxxx s pravděpodobností X&xxxx;≤ 0,05.
U ostatních druhů xxxxxxxxxxx xxxxx je xxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxxx xx xxxxx, xxxxxxx xxxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxxxxxxxxxx xxxxxx. Xxxx xxxxxx xx xxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx.
4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxxx xxxxxxxxx se xxxxxxx
Xx xxxxx použít xxxxxx xxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx, nakolik xxxx xxxxx xxxx zdroj xxxxxx xxxx xxxxxxx xxxx být náhradou xx xxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxx xxx xxxx schválena nebo xxxxxxxx.
Xxxxxx xxxxxxxx xxxxxxxxxxxxxx xxx xxxxxx xx xxxxxxx studií xxxxxxxxx x&xxxx;xxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxx. X&xxxx;xxxxxxxxx xxxxxxxxx, xxxxxxx ve xxxxxx x&xxxx;xxxxxxxx xxx xxxxxxx xxxxxxxxx, xx možno xxxxxxxx xxxxxxxx lépe xxxxxxxxxx xxxxxxxx a ty xxxxx být xxxxxxx xxxxxxxxxx xxxx dlouhodobými xxxxxxxx xxxxxxxxx. Xxx xxxxxx xxxxxxxx se xxxxxxx xxxxx x&xxxx;xxxxx/xxxxxxxxx xxxxxx odpovídající navrhovaným xxxxxxxxx xxx xxxxx.
Xxxxxxxxx xx xxxxx xxxxxxxxx xxxx xxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxx a ty xxxxx xxxxxxxx dlouhodobé xxxxxx xxxxxxxxx x&xxxx;xxxxxx, xx-xx to xxxx xxxxxxxxxx.
4.3&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxxx účinnosti x&xxxx;xxxxxx
Xxxxxxx xx xxxx xxx xxxxxxxxx xxxxxxx xx dvou xxxxxxx xxxxxxx.
Xxxxxxx xxxxxxxxxxxxxx schéma xxxx zahrnovat úvahu x&xxxx;xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxx xxxx&xxxx;1 x&xxxx;2. Xxxxxxxx musí xxx xxxxxxxxxx xxxxxxx, aby xxxxxxx xxxxxx doplňkové xxxxx při xxxxxxxx xxxxxxxxxx xxxxx (xxxxxx xxxx 1-α,&xxxx;X&xxxx;≤ 0,05 xxxxxx x&xxxx;X&xxxx;≤ 0,1 xxx xxxxxxxxxxx, xxxxxxxxx xxxxx, xxxxxxx x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxxxxx, xxxxx xxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxxx) x&xxxx;xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx, xxx xxxx xxxxxxxx, že xxxxxxxxxxxxxx xxxxxxxx xxxxxxx xxx xxxxxx. Xxxxxx xxxx 2-β&xxxx;xxxx xxx xxxxx xxxx xxxxx 20 % xxxxxx x&xxxx;25&xxxx;% x&xxxx;xxxxxx x&xxxx;xxxxxxxxxxx, xxxxxxxxxxx druhy, xxxxxxx x&xxxx;xxxxxxxx chovu x&xxxx;xxxxxxx, xxxxx xxxxxx xxxxxx x&xxxx;xxxxxxxx potravin; xxxxxxxxxx (1-β) je xxxx xxxxx nebo xxxxx 80&xxxx;% (75 % x&xxxx;xxxxxxxxxxx, xxxxxxxxxxx druhů, zvířat x&xxxx;xxxxxxxx xxxxx x&xxxx;xxxxxx, xxxxx xxxxxx určena x&xxxx;xxxxxxxx xxxxxxxx).
Xxxxxx xx, xx xxxxxxxx k povaze xxxxxxxxx xxxxxxxxxxx látek xx obtížné xxxxxxxx xxxxxxxx xxxxxxxx, xx xxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx. Je xxxxx xxxxx zvážit xxxxxxx xxxxxxx metaanalýzy, xx-xx xxxxx xxxxxxxxxx xxxxxxx xxxxx než xxx. Z tohoto důvodu xx xxx xxxxxxx xxxxxxx xxxx být xxxxxxx xxxxxxx xxxxx xxxxxxxxx, aby xxx xxxxx mohly xxx xxxxxxx x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxxxxx a uspořádány (pokud xx xxxxx xxxxxxxx) xx xxxxxx xxxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx X&xxxx;≤ 0,05.
4.4&xxxx;&xxxx;&xxxx;Xxxx xxxxxx dlouhodobých xxxxxx účinnosti x&xxxx;xxxxxxxx xxxxxxx
Xxxx xxxxxx zkoušek xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxx době xxxxxxxxx.
Xxxxxx xxxxxxxxx xx provádějí xxxxx xxxxxxxxxx xxxxx x&xxxx;Xxxxxxxx xxxx x&xxxx;xxxxxxxxx xxxx xxxxxx xx xxxxxxx x&xxxx;xxxxxxx&xxxx;XX.
Xxxxx xx xxxxxxxxx látka používá xx xxxxxxxxxxx a kratší xxxx, xxx je xxxx xxxxxxxx xxxxxxxxx xxxxxx, musí xxx xxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxx pro užití. Xxxx xxxxxxxxxx xxxx xxxxx být xxxxxx xxx 28 dní x&xxxx;xxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx (např. x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx xxxxx selat xxxxxxxxxx xxxx xx xxxxxxxx xx dobu xxxxxxxx, xxxx xxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx selat xx zřetelem na xxxx xxxxxxx).
X&xxxx;xxxxxxxxx druhů xxxx xxxxxxxxx zvířat, xxx xxx xxxxxx x&xxxx;xxxxxxx&xxxx;XX xxxxxxxxx minimální xxxx trvání studií, xx vezme x&xxxx;xxxxx xxxxxx xxxxxxxx podle xxxxxxxxxxxx xxxxxxxx xxx xxxxx.
4.5&xxxx;&xxxx;&xxxx;Xxxxxxxxx xx účinnost xxx xxxxxxxxx a funkční xxxxxxx xxxxxxxxxxx xxxxx
Xxx xxxxxxx xxxxxxxxx xxxxx, xxxxx xxxx xxx xxxxxx xx xxxxxxx, xx xxxxxxxx studie xx xxxx.
Xxx kategorie xxxxxxxxxxxxxx doplňkových xxxxx x&xxxx;xxxxxxxxxxxxxx a histomonostatik xxxx xxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx. X&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxx kategorií xxxxxxxxxxx xxxxx, xxxxx mají xxxxxx xx xxxxxxx, xx možno xxxxx xxxxxxxxxx studie xxxxxxxxx, xxxxx xxx xxxxxxxx xxxxxxxxxxx prokázat.
Pro xxxxxxx xxxxxxxxx xxxxxxxxxxx látek xxx xxxxxxx xxxxxx xx xxxxxxx xx xxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxxx xx xxxxx.
4.6&xxxx;&xxxx;&xxxx;Xxxxxx týkající xx xxxxxxx xxxxxxxxxxx xxxxxxxx, xxxxxxxx xx není xxxxxxx xxxxxx
X&xxxx;xxxxx xxxxxxxx, xx doplňková xxxxx xxxx xxxxxxxxxx či xxxx nežádoucí účinek xx organoleptické x&xxxx;xxxxxxxx (xxxxxxxxx xxxxxxxxxx a technologické) xxxxxxxxxx xxxxxxxx získaných xx xxxxxx, jež xxxx krmena xxxxxxxxxx xxxxxx (xxxxx xx xxxx xxxxxxx xxxxxx), xx xxxxx xxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx odpovídající xxxxxx. Xxxx pozorovány dvě xxxxxxx: xxxxxxx, xxx xxxxx není xxxxxxxx, x&xxxx;xxxxxxx s nejvyšším xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx. Xxxxx xxxx umožnit xxxxxxxxxxx xxxxxxxxxxx. Xxxxxxxxx xxxxxx xxxxxx musí xxx xxxxxxxxx xxxxxxxxxx.
5.&xxxx;&xxxx;&xxxx;XXXXX&xxxx;X:&xxxx;XXXX XXXXXXXXXXXX V OBDOBÍ XX XXXXXXX XXXXX XX XXX
Xxxxx xx.&xxxx;7 odst. 3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;1831/2003 xx xxxxx xxx xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxx monitorování v období xx xxxxxxx xxxxx xx xxx s cílem xxxxxxxx x&xxxx;xxxxxxxxxxxxx případné xxxxx xxxx xxxxxxx, xxxxxxxx, opožděné xxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxx xx xxxxxx xxxx xxxx zvířat nebo xx xxxxxxx prostředí x&xxxx;xxxxxxx s vlastnostmi dotyčných xxxxxxxx.
Xxxxx xxxxx xxxxxxxxxxxx xxxx xxx podrobně xxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx x&xxxx;xxxx určovat, xxx (xxxx. xxxxxxx, xxxxxxxxx) xxxxxxxx xxxxxxxxxx xxxxx v plánu xxxxxxxxx x&xxxx;xxx xxxxxxxx za xxxxxxxx a řádné xxxxxxxxx xxxxx, a musí stanovit xxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxx xxxxxx xxxxxxxxxxxxx, xxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxx. Komisi x&xxxx;xxxx xx xxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx účincích, aniž xxxx xxxxxxx ustanovení x&xxxx;xxxxxxxxxxxx obsažená v článku 12 xxxxxxxx (ES) x.&xxxx;1831/2003.
Xx-xx xxxxxx látka xxxxxx xxxxxxx xxxxxxxxxxxx a bylo-li xxxxxxxxx, xx při xxxxx xxxxxxxxx x&xxxx;xxxxxxxx, xx xxxxxx xx xxxxx v krmivu, dochází x&xxxx;xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxx xxxxx, xxxxxxxx xx xxxx součást monitorování x&xxxx;xxxxxx xx uvedení xxxxx xx xxx xxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxx xxxxxxxxx látce.
U kokcidiostatik x&xxxx;xxxxxxxxxxxxxxx xx provede xxxxxxx monitorování xxxxxxxxxx Xxxxxxx xxx. x&xxxx;Xxxxxxxxxx xxxxxxxxxxx, xxxxx xxxxx xxxxx druhé části xxxx xxxxxxxx.
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;50, 20.2.2004, s. 44.
(2) Úř. věst. X&xxxx;196, 16.8.1967, x.&xxxx;1. Xxxxxxxx xxxxxxxxx pozměněná směrnicí Xxxxxxxxxx parlamentu x&xxxx;Xxxx 2006/121/XX (Úř. věst. L 196, 16.8.1967, x.&xxxx;1; xxxxxxxx x&xxxx;Xx.&xxxx;xxxx. X&xxxx;196, 16.8.1967, x.&xxxx;1).
(3)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;152, 30.4.2004, x.&xxxx;1.
(4)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;165, 30.4.2004, x.&xxxx;1.
(5)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;117, 8.5.1990, x.&xxxx;1. Směrnice xxxxxxxxx xxxxxxxxx xxxxxxxxxxx Xxxxxx 2005/174/XX (Xx.&xxxx;xxxx. X&xxxx;117, 8.5.1990, s. 1)
(6) Úř. věst. X&xxxx;76, 22.3.1991, s. 35. Směrnice xxxxxxxxx pozměněná xxxxxxxx 2001/58/XX (Xx.&xxxx;xxxx. L 76, 22.3.1991, x.&xxxx;35).
(7)&xxxx;&xxxx;Xx.&xxxx;xxxx. L 262, 17.10.2000, s. 21.
(8) Úř. věst. X&xxxx;224, 18.8.1990, x.&xxxx;1. Xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx Xxxxxx (ES) č. 203/2008 (Xx.&xxxx;xxxx. X&xxxx;224, 18.8.1990, x.&xxxx;1).
(9)&xxxx;&xxxx;X.&xxxx;Xxxxxxxx xx al.: Xxxxxxxxxx Xxxxxxxxxx For Xxxxxx Xxxxxxxxxx Xxxxxxxxxx Xx Xxxxxxx Xx Xxxxxxxx (XXXXX Xxxxxxxxx Xxxxxx) Xxxx Xxxx. Xxxx., sv. 74, č. 5, x.&xxxx;835–855, 2002.
(10) Úř. věst. X&xxxx;221, 17.8.2002, x.&xxxx;8. Rozhodnutí xxxxxxxxx xxxxxxxxx xxxxxxxxxxx 2004/25/XX (Xx.&xxxx;xxxx. X&xxxx;221, 17.8.2002, s. 8).
(11) Nevyčerpávající xxxxxx xx x&xxxx;xxxxxxxxx adrese: xxx.xxxx.xxxxxx.xx/xx/xxxxxxx/xxxxxx/xxxxxx_xxxxxxx/993.xxxx.
(12)&xxxx;&xxxx;Xxxxx a kůže x&xxxx;xxxxxxxxxxx xxxxxxxx.
(13)&xxxx;&xxxx;X&xxxx;xxxxxx 50&xxxx;x&xxxx;xxxx x&xxxx;xxxx x&xxxx;xxxxxxxxxxx xxxxxxxx.
(14)&xxxx;&xxxx;Xxx a kůže x&xxxx;xxxxxxxxxxx xxxxxxxx.
(15)&xxxx;&xxxx;X&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxxxx.
(16)&xxxx;&xxxx;X&xxxx;xxxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxx jako TRC.
(17) Vypočteno x&xxxx;xxxxxx XXX.
XXXXXXX&xxxx;XXX
XXXXXXXX POŽADAVKY, XXX XXXX XXXXXXXX XXXXXXXXXXX XXXXXXXXX X&xxxx;XXXXXX&xxxx;3, XXXXX XXX X&xxxx;XXXXXXX XXXXXXXXX XXXXXXXXXXX XXXXX XXXX XXXXXXX ZVLÁŠTNÍ SITUACE, XXX XX STANOVENO X&xxxx;XX.&xxxx;7 ODST. 5 XXXXXXXX (XX) X.&xxxx;1831/2003
Xxxxxxxx (XX) x.&xxxx;1831/2003 xxxxxxxxxxx xxxxxxxxxx xxxxx xxx xxxxxxxxxxx xxxxxxxxxxx (xx-xx to xxxxx) xxx každou xxxxxxxxx doplňkových xxxxx xxxx xx xxxxx xxxxxxxxx xxxxxx xxxxx xx.&xxxx;7 xxxx.&xxxx;5 xxxxxxxx (XX) x.&xxxx;1831/2003.
Xxxxxx xxxxxxxxxx xxxxxxxxx na xxxxxxxxxxx xxxxxxxxxxx xxx:
|
1. |
xxxxxxxxxxxxx xxxxxxxxx xxxxx |
|
2. |
xxxxxxxxxx xxxxxxxxx látky |
|
3. |
nutriční xxxxxxxxx xxxxx |
|
4. |
xxxxxxxxxxxx xxxxxxxxx xxxxx |
|
5. |
xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxxxxxx |
|
6. |
xxxxxxxxxxx z většinových xxxxx xx xxxxx xxxxxxxxx |
|
7. |
xxxxxxx x&xxxx;xxxxxxxx chovu x&xxxx;xxxx xxxxxxx, která xxxxxx určena x&xxxx;xxxxxxxx xxxxxxxx |
|
8. |
xxxxxxxxx xxxxx, xxxxx xxx xxxx xxxxxxxx xxx xxxxxxx x&xxxx;xxxxxxxxxxx |
|
9. |
xxxxx xxxxxxxx |
|
10. |
xxxxxxxx xxxxxxxx |
|
11. |
xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx, které xxx xxxx xxxxxxxx xxxxx směrnice 70/524/XXX. |
Xxxxxxx xx xxxxx xxxxxxxxx xx xxxxxxx více xxx xxxxxxx x&xxxx;xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx.
Xxxxxx xxxxxxxx
Xxxxx-xx v dokumentaci xxxxxxx x&xxxx;xxxxx xxxxxxxxxxxx x&xxxx;xxxxxx xxxxxxxx, xx xxxxx xxxxx xxxxxx.
1.&xxxx;&xxxx;&xxxx;XXXXXXXXXXXXX XXXXXXXXX XXXXX
1.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx dokumentace
Použije se xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
1.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx a podmínky pro xxxxx xxxxxxxxx xxxxx; xxxxxx xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX xx xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, xxxxx xxxxxx vázané na xxxxxxxx xxxxxxxx, xx xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
xxx xxxx doplňkové xxxxx, které xxxx xxxxxx na xxxxxxxx xxxxxxxx, xx xxxxxxx xxxx oddíl II. |
1.3 Oddíl III: Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxx
Xxxx&xxxx;3.1, 3.2 x&xxxx;3.4 xxxxxxx&xxxx;XX se xxxxxxxxxx xx doplňkové xxxxx k silážování, xxxxx xxx xxxxxxxx, že:
|
— |
v hotovém xxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxxx (xxxxx) xxxx důležitých xxxxxxxxxx xxxx xxxxxxxx xxxxxxx (xxxxxxx) nebo |
|
— |
účinná xxxxx(x)&xxxx;x&xxxx;xxxxxxx(x)&xxxx;xx xxxxxxxxx xxxx xxxxx xxxxxx xxxxxx x&xxxx;xxxxx xxxxxxxxxxx xxxxx xxxxxxxxx významně xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx se xxxxxx připravenou xxx xxxxx doplňkové látky (xxxx. xxxxx neexistuje xxxxx podstatná xxxxx xxxxxxxx). |
X&xxxx;xxxxxxxxx xxxxxxxxx xx xxxxxxx celý xxxxx&xxxx;3 xxxxxxx&xxxx;XX.
1.3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx xxxxxx xxxxxxx
X&xxxx;xxxxxxxxxx&xxxx;(1) xxxxx: použije xx celý bod 3.1 xxxxxxx&xxxx;XX.
1.3.1.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxx
Xxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx:
|
— |
xxxxxxx se xxxxx xx základní krmné xxxxx a výsledky se xxxxxxxxx s negativní kontrolní xxxxxxxx se xxxxxxx xxxxxx xxxxxx. Xxxxxxxx xxxxx xxxxx xxxx xxxxxxxxx xxxxxx xxxxx xxxxxx xxxxxxxxxx xxx xxxxxxx xxxxxxxxx xxxxx; |
|
— |
xxxxx xxxxxxx xxx xxxxxx xxxxxxxxx je xxxxxxxx xxxxxxxxxxx vyskytující se x&xxxx;xxxxxx x&xxxx;xxxx normálního xxxxxxxxx, xxxxx to xxx xxxxxxxxxxx xxxxxxx. Xxxxxxxx xxxxxxxxx xx xxxxxx produktu, který xxxxxxxx xxxxxxxxxxxxx mikroorganismy, x&xxxx;xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxx xx xxxxx silážování. |
Studie tolerance xxx xxxxxxx omezit xx xxxxx xxxxxxxxxxx, xxxxxxxxx dojnice. Xxxxxx xxxxxxxxxx xxxx xxxxx xxxx xxxxx pouze x&xxxx;xxxxxxx, xx-xx xxxxx xxxxxxxx xx xxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxx xxx xxxx druhy xxx xxxxxxxxxxx.
Xxxxxxx xxxxx:
X&xxxx;xxxxxxxxx xxxxx, xxx něž xx požaduje xxxxxxxx xxxx technologické xxxxxxxxx xxxxx a které nebyly xxxxxxxx xxx xxxxxxx xxxx xxxxxx, xx xxxxx prokázat, že xxx xxxxxxx nejsou xxxxxxxx při xxxxxxxxx xxxxxxxxxxx xxxxxx. Xxxx xxxxxxxxx xxxx být xxxxxxx xx jeden xxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxx druhů xxxx x&xxxx;xxxxxxx xxxxx xxxxxxxxxxxxx xxxxxx.
1.3.1.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxx xxxxx
Xxxxxxx se xxxx xxx&xxxx;3.1.2 xxxxxxx&xxxx;XX.
1.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx xxxxxxxxxxxx
|
1.3.2.1 |
Xxxxxx metabolismu x&xxxx;xxxxxxx Xxxxxx metabolismu a reziduí xx xxxxxxxxxx, xxxxx:
Studie metabolismu xx xxxxxxxxxx xxxxxx x&xxxx;xxxxxxx, xxxxx se xxxxx vyskytuje x&xxxx;xxxxxxxxxxx xxxx krmivech xxxxxxxxx xx xxxxxxx množství xxxx xx xxxxxx xxxxxxx xxxxxxx xxxxxxx xxxx xxxxx. X&xxxx;xxxxxx xxxxxxxxx xx však xxxxxxxx studie reziduí, xxxxx xxxxx být xxxxxxx xx srovnání xxxxxx v tkáních/produktech x&xxxx;xxxxxxxxxx xxxxxxx a ve xxxxxxx, xxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx. |
|
1.3.2.2 |
Xxxxxxxxxxxxx xxxxxx Xxxxxxxxxxxxx xxxxxx xx xxxxxxxxxx, pokud:
Xxx xxxxxxxxxxxxxx x&xxxx;xxxxxx, xxxxx xxxxxx xxxxxx xxxx, xx požadují studie xxxxxxxxxxxx (xxxxxx mutagenity) x&xxxx;xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx. Xxxxxx xxxxxxxxxxxx xx xxxxx xxxxxxxx xx přítomnosti xxxxxx xxxxx. Xxx xxxxxxxx látky, xxx xxxxxx xxxxxx xxxx, xx použije xxxx bod 3.2.2 xxxxxxx&xxxx;XX. Xxx xxxxxxx xxxxx se xxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx s přihlédnutím x&xxxx;xxxxxx x&xxxx;xxxxxxx xxxxxxxx. |
|
1.3.2.3 |
Xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxxxx Xxx xxxxxxxxx látky xxxxxxxxxx xxx xxxxxxx, xxxxx xxxx určena k produkci xxxxxxxx, se xxxxxxx xxxx xxx&xxxx;3.2.3 xxxxxxx&xxxx;XX. |
1.3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx uživatele/pracovníky
Použije xx xxxx xxx&xxxx;3.3 přílohy II. Xxxxxxxxx xxxxx obsahující xxxxxx x&xxxx;xxxxxxxxxxxxxx xx xxxxxxxx xx senzibilizátory xxxxxxxxx xxxxxxx, xxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxxx opak.
1.3.4 Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové látky xxx xxxxxxx prostředí
Použije xx xxxx xxx&xxxx;3.4 xxxxxxx&xxxx;XX. X&xxxx;xxxxxxxxxxx látek x&xxxx;xxxxxxxxxx se xxxxxxx xxxxxx doplňkové xxxxx xx xxxxxx xxxxxxxxx xxxx xx xxxxxxxxx xxx nebo sil xxxxx silážování.
1.4 Oddíl IV: Studie xxxxxxxx xx účinnosti xxxxxxxxx látky
Technologické xxxxxxxxx xxxxx xxxx zlepšit xxxx stabilizovat xxxxxxxxxx xxxxx, xxxxxxx však xxxxxx xxxxx přímý xxxxxxxxxx xxxxxx na xxxxxxxxxx výrobu. Xxxxxx x&xxxx;xxxxxxxxx doplňkové látky xxxx xxx poskytnuty xxxxxx vhodných xxxxxxxx xxxxxxxxxxxx v uznaných xxxxxxxxxxx xxxxxxxx xx určených xxxxxxxxxxx podmínek xxx xxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxxxxx krmivem.
Účinnost xx xxxxxxx xxxxxxxx xx xxxxx x&xxxx;xxxxxxxx xxxxx xxx kontrolu xxxxxxxxxxx xxxxxxxxxxxx. X&xxxx;xxxxxxxxxxx tabulce xxxx xxxxxxx xxxxxx xxxxxxxxx xxx xxxxx xxxxxxx xxxxxxx.
Xxxxxxxxx pro xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx
|
Xxxxxxx xxxxxxx |
Xxxxxxxxx pro xxxxxxxxx xxxxxxxxx |
||||||||||
|
Xxxxxxxx mikrobiálního xxxxx, xxxxxxx xxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xx znehodnocení. Je xxxxx xxxxxxxx xxxxxxxx xxxx xxxxxx konzervačního xxxxxx. |
||||||||||
|
Xxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxx/xxxxxx během xxxxxxxxxx x/xxxx xxxxxxxxxx krmiva. Xx xxxxx xxxxxxxx xxxxxxxx xxxx trvání xxxxxxxxxx účinku. |
||||||||||
|
Vznik/uchování stabilních xxxxxx jinak nesmísitelných xxxx xxxxxx xxxxxxxxxxxx xxxxxx xxxxxx. |
||||||||||
|
Xxxxxxxxx xxxxxxxxx-xxxxxxxxxx xxxxx xxxxx. |
||||||||||
|
Xxxxxxxxx xxxxxxx xxxxxxxxx xxxx xxxxx. |
||||||||||
|
Tvoření gelu xxxxxxx xx xxxxx xxxxxxxxx xxxxxx. |
||||||||||
|
Xxxxxxxxxxx xxxxx xxxx xxxxxxxxx při xxxxxxxxx xxxxx. |
||||||||||
|
Xxxxx x&xxxx;xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxx původu. |
||||||||||
|
Xxxxxxxxx xxxxxxxx spékání. Je xxxxx prokázat xxxxxxxx xxxx xxxxxx protispékavého xxxxxx. |
||||||||||
|
xX x/xxxx xxxxxxxxx xxxxxxxx xxxxx. |
||||||||||
|
|
||||||||||
|
Xxxxxxxxxxxxxxx identifikace xxxxxxx xxxxxxxxx. |
Xxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx
Xxxxxxxx xx xxxxxxxx zkoušky x&xxxx;xxxxx prokázat xxxxxxxxxx xxxxxx xx silážní xxxxxx&xxxx;(2). Xxxxxxx se xxxxxxxx x&xxxx;xxxxxx příkladem x&xxxx;xxxxx x&xxxx;xxxx uvedených xxxxxxxxx (xxxxx xxxx xxxxxxxx všechna xxxx xxxxxxxxxxxxxxx xxxxxx):
|
— |
xxxxxx, xxxxx xxx xxxxxx silážovat: &xx;3&xxxx;% xxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx (např. xxxx xxxxxxxx xxxxxxxx, xxxxx, xxxxxx nebo xxxxx řízky), |
|
— |
krmiva, xxxxx xxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxx: 1,5–3,0&xxxx;% rozpustných xxxxxxxxxxx v čerstvém materiálu (xxxx. xxxxxxx, kostřava xxxx xxxxxxx vojtěška), |
|
— |
krmiva, xxxxx xxx xxxxxxxxx xxxxxxx: &xx;&xxxx;1,5&xxxx;% xxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx (xxxx. srha nebo xxxxxxxxx). |
Xxxx-xx xxxxxxx omezeny xx xxxxx xxxxxxxxx xxxxx xxxxxxx xx xxxxxxx xxxxxx, xxxxx xx xxxxxxxx rozmezí xxxxxx. Poté xx xxxxxxxx tři zkoušky x&xxxx;xxxxxxxxxx xxxxxxxxxxxxxxxx xxx xxxx xxxxxxx, pokud xxxxx za xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxx.
Xxx zvláštní krmiva xx požadují xxxxxxxxxx xxxxxxx.
Xxxx trvání xxxxxx xx xxxxxxx 90&xxxx;xxx xxxx déle při xxxxx xxxxxxx (doporučený xxxxxx 15 – 25&xxxx;xX). Xxxxxxx xxxxxx xxxx xxxxxx xxxx xxx zdůvodněno.
Obvykle xx xxxxxx výsledky xxxxxx xxxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx s negativní xxxxxxxxx xxxxxxxx:
|
— |
xxxxxx x&xxxx;xxxxxxxxx xxxxxx xxxxxx (xxxxxxxx x&xxxx;xxxxxxx xx xxxxxx xxxxx), |
|
— |
xxxxxx xX, |
|
— |
xxxxxxxxxxx těkavých mastných xxxxxxx (xxxx. xxxxxxxx xxxxxx, xxxxxxxx máselná x&xxxx;xxxxxxxx xxxxxxxxxx) x&xxxx;xxxxxxxx xxxxxx, |
|
— |
xxxxxxxxxxx alkoholů (xxxxxxx), |
|
— |
xxxxxxxxxxx xxxxxx (x/xx xxxxxxxxx xxxxxx) a |
|
— |
obsah xxxxxxxxxxx xxxxxxxxxxx xx xxxx. |
Xxxxxxxxx xx xxxxxx jiné xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx parametry x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx (xxxx. xxxxx xxxxxxxx xxxxxxxxx asimilovat xxxxxx, xxxxxxxx klostridií, xxxxxxxx listérií x&xxxx;xxxxxxxxxx xxxxx).
Xxxxxxx účinek x&xxxx;xxxxxxxxxxx xx snížením xxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxx xx posoudí xx xxxxxxx celkového objemu xxxxxxxxx xxxx vytvořených xx xxxx xxxxxxx xxxxxx s přihlédnutím k pravděpodobnému xxxxxx xx xxxxxxx xxxxxxxxx (xxxx. xxxxxxxxxxx xxxxxxxxx xxxx nebo xxxxxxxxxx xxxxxxx xxxxxxx). Xxxxxxx tvorby silážních xxxx xx nutno xxxxxxxx xxxxx. Kapacita xxxxxxx xxxx musí xxx dostatečná, xxx xxxxx xxxxxxx xxxxx xxxxxxx xx xxxxxx xxxxx. Xxxx xxxxxx xxxxxx xx xxxxxxx 50&xxxx;xxx. Xxxxx xx xxxxxxx jiná doba, xx nutno xx xxxxxxxxx.
Xxxxx xxxxxxx stabilita xxxx xxx xxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxx. Studie xxxxxxxxx xxxx trvat xxxxxxx xxxx dnů xx xxxxxxxx xxxxxxx a doplňková xxxxx dokládá stabilitu xx xxxx nejméně x&xxxx;xxx xxx xxxxx, xxx xx prokázáno x&xxxx;xxxxxxxxxxxx xxxxxxxxxxx xxxxxx. Xxxxxxxxxx xx, xxx xx xxxxx xxxxxxxx xxx xxxxxxx okolí 20&xxxx;xX x&xxxx;xxx se xxxxxxx teploty o 3 oC xxxx xxxx oproti xxxxxxx okolí xxxxxxxxxx xx xxxxxx nestability. Xxxxxx teploty xx xxxxx xxxxxxxx xxxxxxx xxxxxxxx XX2.
1.5&xxxx;&xxxx;&xxxx;Xxxxx X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx xx xxx
Xxxxx oddíl xx xxxxxxx xxxxx ustanovení xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003. To xxxxxxx, že xx xxxx monitorování v období xx uvedení xxxxx xx xxx požaduje xxxxx pro xxxxxxxxx xxxxx, xxxxx xxxx xxxxxxxxx modifikované xxxxxxxxx xxxx xxxx z geneticky xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx.
2.&xxxx;&xxxx;&xxxx;XXXXXXXXXX XXXXXXXXX XXXXX
2.1&xxxx;&xxxx;&xxxx;Xxxxxxx
2.1.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx dokumentace
Použije xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
2.1.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxx užití xxxxxxxxx xxxxx; metody analýzy
Oddíl II xxxxxxx&xxxx;XX xx použije xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, xxxxx xxxxxx vázané xx xxxxxxxx xxxxxxxx, xx xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
pro jiné xxxxxxxxx látky, xxxxx xxxx vázané na xxxxxxxx povolení, xx xxxxxxx xxxx oddíl II. |
2.1.3 Oddíl III: Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx
Xxx&xxxx;3.3 přílohy II se xxxxxxxx plně xx xxxxxxx xxxxxxxxx xxxxx.
|
1. |
Xx xxxxx, které xxx xxxxxxx x&xxxx;xxxxxx, dávají xxxxx potravinám xxxxxxxxxxx xxxxxx, se xxxxxxxx xxxx oddíl III xxxx&xxxx;3.1, 3.2 a 3.4 xxxxxxx&xxxx;XX. |
|
2. |
X&xxxx;xxxxx, xxxxx xxxxxx xxxx xxxxxxxxx xxxxxxx xxxxx, xx studie xxxxxxxx xx oddílu III bodu 3.1 xxxxxxxx na xxxxxxxxx, xxxxxx byla doplňková xxxxx xxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxx. Je xxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxxxx. Xxxxxxx xx xxxxx&xxxx;XXX body 3.2 x&xxxx;3.4 xxxxxxx&xxxx;XX. |
|
3. |
X&xxxx;xxxxx, které xxxx xxxxxxxxx xxxx xx xxxxxxxx xxxxxxxxx xxx nebo xxxxx, xx xxxxxxxx studie xxxxxxxx xx xxxxxx&xxxx;XXX xxxx&xxxx;3.1 xxxxxxx&xxxx;XX a tyto xxxxxx xxxx xxx xxxxxxxxx xx zvířatech, xxxx xxxx doplňková xxxxx podávána x&xxxx;xxxxxxxxxx xxxxx. Je xxxxx xxxxxxxxxx důkaz rovněž xxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxxxx. Nepožadují xx xxxx xxxx&xxxx;3.2 x&xxxx;3.4. |
2.1.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx týkající xx účinnosti doplňkové xxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;XX xxxxxxx&xxxx;XX.
|
x) |
Xxx xxxxx, xxxxx xxx xxxxxxx x&xxxx;xxxxxx dávají xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx: xxxxx xxxxx produktů xxxxxxxxx xx xxxxxx, kterým xxxx xxxxxxxxx látka xxxxxxxx xx xxxxxxxxxxxx xxxxxxxx xxx užití, xx xxxx xxxxxx xxxxxx metodiky. Xx xxxxx xxxxxxxx, že xxxxxxxxx xxxxxxxxx látky xxxx xxxxxxxxxx xxxx xx xxxxxxxxx xxxxxxxx xxxx organoleptické x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxx. Xxxx-xx xxxxxx xxxxxxxxx xxxxx xx xxxxxxx/xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxxxx, xxx mohou xxxxxxxxxxxx xxxxx o účinnosti xxxxxxxxxx xxxxxxx xxxxxx (xxxx. xxxxxx xxxxxxxxxx xxxxxxxxxxx). |
|
x) |
Xxx xxxxx, xxxxx xxxxxx xxxx xxxxxxxxx xxxxxxx xxxxx: xxxxx x&xxxx;xxxxxxxxx xx xxxxx poskytnout xxxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx xxx užití x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxxxx krmivy. |
|
c) |
Pro xxxxx, xxxxx xxxx pozitivní xxxx na xxxxxxxx xxxxxxxxx xxx xxxx xxxxx: xxxxxx xxxxxxxxxxx účinek (xxxxxx) se xxxxxxxx xx xxxxxxxxx, kterým xxxx xxxxxxxxx látka xxxxxxxx x&xxxx;xxxxxxxxxx xxxx. Xxxxx xxxxx xx xxxx pomocí xxxxxx xxxxxxxx. Xxxxx x&xxxx;xxxxxxxxx xx možno xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxxxxx xxxxxxxx (xxxx. xxxxxxxxxx xxxxxxxxxx) nebo xxxxxxx xx xxxxxxxx literaturu. |
2.1.5 Oddíl V: Plán xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx xx xxx
Xxxxx xxxxx xx xxxxxxx podle ustanovení xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003. Xx xxxxxxx, xx xx xxxx monitorování v období xx uvedení xxxxx xx xxx požaduje xxxxx xxx xxxxxxxxx xxxxx, které xxxx xxxxxxxxx xxxxxxxxxxxx organismy xxxx xxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx.
2.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxx xxxxx
2.2.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx oddíl I přílohy II.
2.2.2 Oddíl II: Identita, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxx xxxxx xxxxxxxxx xxxxx; xxxxxx xxxxxxx
X&xxxx;xxxxxxx xxxxxxx „xxxxxxxx produkty“ xx xxxxxxx celé rostliny, xxxxxxx x&xxxx;xxxx xxxxxxxxx x&xxxx;xxxxxx xxxxx xxxx xxxxxx produkty, xxxxx xxxx velmi xxxx xxxxxxxxxx, xxxx xxxx. xxxxxxx, xxxxxx nebo xxxxxxx (xxxx. xxxxx xxxxx x&xxxx;xxxxxx), nepovažují xx xxxxxxxx spadající xx funkční skupiny xxxxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxx doplňkových xxxxx.
Xxx xxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxxx xxxx zchutňující xxxxx xxxxxxxxxxxxx xxxxx:
|
1. |
Xxxxxxxx xxxxxxxx:
|
|
2. |
Xxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx zchutňující xxxxx |
|
3. |
Xxxxx xxxxx Xx xxxxx uvést xxxxxxxxxx xxxxxxx, xx xxx xxxxx xxxxxxx, xxxxx xx xxxxxx xxxx. V případě xxxxxxxx, xxxxx nespadá do xxxxx x&xxxx;xxxx xxxxxxxxx xxxxxx, xx xxxx xxxxx xxxxx x&xxxx;xxxxxxxxx. |
|
2.2.2.1 |
Xxxxxxxxxxxxxxx xxxxxx látky (xxxxx) / činidla (xxxxxxx) Xxxxxxx xx xxxx bod 2.2 xxxxxxx&xxxx;XX. Xxxxxx: Xxx xxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxx je xxxxx xxxxx xxxx xxxxxxxxx xxxxxxxxxxxxx xxxxx (xxxxx) (xxxx. FLAVIS (3), Xxxx Xxxxxx&xxxx;(4), JECFA, XXX&xxxx;(5) xxxx xxxx xxxxxxxxxxx schválený systém xxxxxxxxx) používané specificky x&xxxx;xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxxxx, xxxxx xx x&xxxx;xxxxxxxxx.
|
|
2.2.2.2 |
Xxxxxx xxxxxx Xxxxxxx se xxxx bod 2.3 xxxxxxx&xxxx;XX. X&xxxx;xxxxxxx xxxxxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxxxx xxxxxx xxxxxxxxxx, xxxxxxx xxxxxxxxx xxxxx xxxxx xxxxx xxxxxxx x&xxxx;xxxxxxx xxxxxxxx, xx xxxxx xxxxx xxxxxxxx xxxxx procesu xxxxxxxx. Doporučuje se x&xxxx;xxxxxx xxxxxx odpovídající xxxxxxxxxxxx, xxxx. silice, xxxxx, xxxxx, xxxxxxx x&xxxx;xxxxxxxxxxx xxxxx&xxxx;(7) xxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxx xxxxxxx extrakce. Xxxxxxx se xxxxxxx xxxxxxxxx xxxxxxxxxxxx, xxxxxxx xxxxxxxxxxxx xxxxxxxx, xxx xx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxxxx, x&xxxx;xxxxxx reziduí, xxxxx jsou xxxxxxxxxxxxx xxxxxxxx, xxxxxxxx xxxxxx xxxxxxx xxxxx xxxxxxxx. Xxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxxxx xxxxxxxx xxxxx zahrnovat xxxxx na způsob xxxxxxxx. |
|
2.2.2.3 |
Xxxxxx analýzy
Celý xxx&xxxx;2.6 přílohy II xx xxxxxxxx xx všechny xxxxxxx xxxxxxxxxxx látky, xxxxxxxxx xxxxxxxx extrakty, xxxxx xxxxxxxx toxikologicky xxxxxxxx xxxxx, xxxxxxxx xxxx xxxxxxxxxxxx syntetické xxxxxxxx definované zchutňující xxxxx, xxx xxxx xxxxxxxxxxxxx významnými xxxxxxx, x&xxxx;xxxxx xxxxxxxxxxx xxxxx. |
2.2.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx týkající se xxxxxxxxxxx doplňkové xxxxx
Xxx xxxxxxx zchutňující xxxxx xx nutno uvést xxxxxxxx zvířat x&xxxx;xxxxxxx xxxxxx jak x&xxxx;xxxxxxxxx xxxxxxxx, xxx xx xxxxxxx xxxxxxxxxxx xxxxx xx xxxxx.
Xx xxxxxxxxxxx xxxxx xxxxxxx do xxxxxxx xxxxxxx xxxxx xx xxxxxxxx xxxx xxxxx&xxxx;XXX xxxxxxx&xxxx;XX.
|
2.2.3.1 |
Xxxxxx xxxxxxxx xx bezpečnosti používání xxxxxxxxx xxxxx xxx xxxxxx xxxxxxx
|
|
2.2.3.2 |
Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx xxxxxxxxxxxx Xx nutno xxxxxxx, že xxxxxxxxxx xxxxxxxxxxx xxxxx nevedou x&xxxx;xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxx xx xxxxxxx. X&xxxx;xxxxxxx, xx xxxxx požadovaného xxxxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxx xxxxxxx xx xxxxx vede x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxx xxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxx expozice xxxxxxxxxxxx.
|
|
2.2.3.3 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx látky xxx xxxxxxxxx/xxxxxxxxxx Xxxxxxx xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX. |
|
2.2.3.4 |
Xxxxxx xxxxxxxx se bezpečnosti xxxxxxxxx doplňkové xxxxx xxx xxxxxxx xxxxxxxxx Xxxxxxx xx xxxx xxx&xxxx;3.4 xxxxxxx&xxxx;XX. |
2.2.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Studie týkající xx xxxxxxxxx xxxxxxxxx xxxxx
Xx nutno xxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx, obvykle na xxxxxxx zveřejněné literatury. Xx může být xxxxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx, xxxx-xx x&xxxx;xxxxxxxxx, x&xxxx;xxxxxxx případě xxxxx být požadovány xxxxxx na xxxxxxxxx.
Xx xxxxx plně xxxxxxxx x&xxxx;xxxxx, zda xxxxxxx, xxxxxxx se xxxxxx xxxx, xxxx x&xxxx;xxxxxx, xxxxxxx nebo potravinách xxxxxxxxxxx xxxxxx xxxx xxxxxx xxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxxxx xxxxx x&xxxx;xxxxxxx&xxxx;X&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
2.2.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx na xxx
Xxxxx oddíl se xxxxxxx xxxxx xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 písm. g) nařízení (XX) x.&xxxx;1831/2003. To xxxxxxx, xx xx xxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx látky xx xxx xxxxxxxx xxxxx xxx xxxxxxxxx xxxxx, xxxxx jsou xxxxxxxxx xxxxxxxxxxxx organismy xxxx xxxx z geneticky xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx.
3.&xxxx;&xxxx;&xxxx;XXXXXXXX XXXXXXXXX XXXXX
3.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx X&xxxx;xxxxxxx&xxxx;XX.
3.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxx xxxxx xxxxxxxxx xxxxx; metody xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX xx xxxxxxx takto:
|
— |
pro xxxxxxxxx xxxxx, které nejsou xxxxxx xx xxxxxxxx xxxxxxxx, se xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
pro xxxx xxxxxxxxx xxxxx, xxxxx jsou vázané xx držitele povolení, xx xxxxxxx celý xxxxx&xxxx;XX. |
3.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxx
3.3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx pro xxxxxx xxxxx
|
3.3.1.1 |
Xxxxxxxxx x&xxxx;xxxxxxxx xxxxx
|
|
3.3.1.2 |
Mikrobiální xxxxxx Xxxxxxx xx xxxx xxx&xxxx;3.1.2 xxxxxxx&xxxx;XX. |
3.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx bezpečnosti xxxxxxx xxxxxxxxx látky xxx xxxxxxxxxxxx
|
3.3.2.1 |
Xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx Xxxxxx xxxxxxxxxxx se xxxxxxx xxxxxxxxxx. Pro xxxxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxx. Xxxxxx xxxxxxx xxxx xxxxxxxx xx xxxxxxxx xxxxx u těch xxxxxxxxxxx xxxxx, které xxxxxxx do funkční xxxxxxx „vitamíny, provitamíny x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxx xxxxx xx srovnatelným xxxxxxx“, které xxxx xxxxxxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxx, x&xxxx;xxx xxxxxxx skupinu xxxxxxxxx xxxxxxxxx xxxxx, xxxxx xx xxxxxxx xxxxxxxxxx xxxxxxxxxx. V tomto xxxxxxx xx nepoužije xxxxxx xxxxxxx v oddíle 3.2.1 xxxxxxx&xxxx;XX. Požadavek je xxxxxx xx xxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxx xxxxxxxxxx xxxx skupinou, xxx byla xxxxxxxx xxxxxxxx dávka xxxxxxx xxxxx, x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxx (xxxxxxxxxx xxxxx). |
|
3.3.2.2 |
Xxxxxxxxxxxxx xxxxxx Xx se xxxxxxxx xxx produkty fermentačního xxxxxxx x&xxxx;xxx doplňkové xxxxx, xxxxx xxxxxx xxxxx xxxxxxxx. Xxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxx genotoxicity x&xxxx;xxxxxxxxxxxx xxxxxxxx, ledaže:
Xxxxx xxxxxxxxx organismus patří xx skupiny, o níž xx xxxxx, že xxxxxxx kmeny produkují xxxxxx, xx xxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx. |
|
3.3.2.3 |
Xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxxxxx Xxxxxxx xx xxxx xxx&xxxx;3.2.3 xxxxxxx&xxxx;XX. |
3.3.3&xxxx;&xxxx;&xxxx;Xxxxxx týkající xx xxxxxxxxxxx používání xxxxxxxxx xxxxx pro xxxxxxxxx/xxxxxxxxxx
Xxxxxxx xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
3.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxx xxxxxxxxx
Xxxx xxx&xxxx;3.4 xxxxxxx&xxxx;XX xx xxxxxxx xxx xxxx xxxxxx xxxxx, které xxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxx.
3.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Studie xxxxxxxx xx xxxxxxxxx xxxxxxxxx látky
Studie xxxxxxxxx xx nepožadují xxx xxxxxxxx, aminokyseliny, xxxx x&xxxx;xxxxxxx aminokyselin, které xxx xxxx xxxxxxxx xxxx doplňkové látky, xxxxxxxxxx xxxxxxxxx xxxxx, xxxxx xxx byly xxxxxxxx xxxx doplňkové xxxxx, x&xxxx;xxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxxx přesně xxxxxxxxxx xxxxx xx xxxxxxxxxxxx xxxxxxx, které již xxxx xxxxxxxx xxxx xxxxxxxxx xxxxx.
Xxxxxxxxxx xxxxxx xx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxxx, xxxx a analogy xxxxxxxxxxxx, které ještě xxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxx, xxxxxxxxxx xxxxxxxxx prvků, které xxxxx nebyly xxxxxxxx xxxx xxxxxxxxx látky, x&xxxx;xxx xxxxxxxx, xxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxx definované xxxxx se xxxxxxxxxxxx xxxxxxx, které xxxxx xxxxxx povoleny jako xxxxxxxxx xxxxx.
Xxx xxxxxxx xxxxx, u nichž se xxxxx xxxxxxxx xxxxxx, xx xxxxxxxx xxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxx ustanovení xxxxxx&xxxx;4 xxxxxxx&xxxx;XX.
Xxxxxx xxxx xxxxxxxx prokázat, že xxxxxxxxx látka xxxx xxxxxxx nutričním xxxxxxxxxx xxxxxx. Xxxxx xxxxxxxx xxxxxxxx xxxxxxx s krmnou xxxxxx, xxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxxxx nižších xxx xxxxxxxx požadavky xxxxxx. Je xxxx xxxxx xxxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxxxx xxxxxx těžkým xxxxxxxxx. Xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxx xxxx xxxxxxxxx xxxxxx, xxxxxx xxxxxxxxxxxxx zvířat.
3.5 Oddíl V: Plán xxxxxxxxxxxx v období po xxxxxxx xxxxx xx xxx
Xxxxx xxxxx xx xxxxxxx podle ustanovení xx.&xxxx;7 xxxx.&xxxx;3 písm. g) nařízení (XX) x.&xxxx;1831/2003.
4.&xxxx;&xxxx;&xxxx;XXXXXXXXXXXX DOPLŇKOVÉ XXXXX
4.1&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx xxxxxxxxx xxxxx xxxx xxx xxxxxx x&xxxx;xxxxxxxxxxxxxx
4.1.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx oddíl I přílohy II.
4.1.2 Oddíl II: Xxxxxxxx, xxxxxxxxxxxxxxx a podmínky xxx xxxxx doplňkové látky; xxxxxx xxxxxxx
Xxxxxxx se xxxx xxxxx&xxxx;XX přílohy II.
4.1.3 Oddíl III: Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxx
|
4.1.3.1 |
Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx cílová zvířata Použije xx celý xxx&xxxx;3.1 xxxxxxx&xxxx;XX. |
|
4.1.3.2 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání xxxxxxxxx xxxxx pro spotřebitele
|
|
4.1.3.3 |
Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxxxx/xxxxxxxxxx Xxxxxxx xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX. |
|
4.1.3.4 |
Xxxxxx týkající xx xxxxxxxxxxx xxxxxxxxx látky xxx xxxxxxx prostředí Použije xx xxxx xxx&xxxx;3.4 xxxxxxx&xxxx;XX. |
4.1.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Studie xxxxxxxx xx účinnosti xxxxxxxxx xxxxx
Xxxxxxx se celý xxxxx&xxxx;XX xxxxxxx&xxxx;XX.
|
1. |
Xxxxxxxxx xxxxx, xxxxx mají xxxxxxxxx xxxx xx xxxxxxxxxx xxxxxx, xxxxxxxxxx xxxx xxxxx xxxxxxx podmínky, x&xxxx;xxxxxxx skupina „jiné xxxxxxxxxxxx xxxxxxxxx xxxxx“ Xxxxxx xxx xxxxxxxx xxxxx xx vztahu xx xxxxxxx cílovému druhu xxxx xxxxxxxxx xxxxxx. X&xxxx;xxxxxxxxxx xx vlastnostech xxxxxxxxx xxxxx xxxxx xxx xxxxxx xxxxxxxx xx pracovních xxxxxxxxxxxxxxxxx (xxxx. xxxxxxxxx xxxxxxxx, xxxxxxxx denní xxxxxxxxx, xxxxxx živočišných produktů), xxxxxxx jatečně xxxxxxxxxx xxxx, xxxxxxxxxxx xxxxx, xxxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx. Xxxxx o mechanismu xxxxxxxx xxx poskytnout xxxxxxxxxxxx studiemi účinnosti xxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx. |
|
2. |
Xxxxxxxxx xxxxx, xxxxx pozitivně xxxxxxxxx důsledky živočišné xxxxxx xxx životní xxxxxxxxx X&xxxx;xxxxxxxxxxx xxxxx, xxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx (xxxx. xxxxxxx xxxxxxx dusíku a fosforu xxxx omezená xxxxxxxx xxxxxx, xxxxxxxxx příchutí), xx xxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxx doložit xxxxx xxxxxxxxxxxx studiemi xxxxxxxxx se xxxxxxx xxxxxxxxxxxxx xxxxxxxx prospěšné xxxxxx. Xxxxxx vezmou x&xxxx;xxxxx xxxxxxx xxxxxxxxxxxx xx doplňkové látce. |
4.1.5 Oddíl V: Plán xxxxxxxxxxxx v období po xxxxxxx xxxxx xx xxx
Xxxxx oddíl xx xxxxxxx podle ustanovení xx.&xxxx;7 odst. 3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
4.2&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx xxxxxxxxx xxxxx: enzymy x&xxxx;xxxxxxxxxxxxxx
4.2.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
4.2.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Identita, charakteristika x&xxxx;xxxxxxxx pro užití xxxxxxxxx xxxxx; xxxxxx xxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;XX xxxxxxx&xxxx;XX.
4.2.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxxxx xxxxx
|
4.2.3.1 |
Xxxxxx týkající xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx xxxxxxx Xxxxxxx se xxxx xxx&xxxx;3.1.1 xxxxxxx&xxxx;XX. Xxxxxxxx xx xxxxxxxx, xxx xxxxx xxxxx používali x&xxxx;xxxxxxx xxxxxxx xxxxxxxxxxxx 100xxxxxxx xxxxxxxx dávky x&xxxx;xxxxxxx počet požadovaných xxxxxxxxx. X&xxxx;xxxxxx xxxxx xxx xxxxxx xxxxxxxxxxxxxx xxxxx doplňkové látky. Xxxxxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxx přítomného xxxxxx, xxxxx xxxxxxxx xxxxxxx (xxxxxxx) / xxxxx (xxxxx) x&xxxx;xxxxxxxx xxxxxxxxx fermentačního xxxxxxx xxxx xxxx xxx xxxxxx xxxx v hotovém xxxxxxxx. X&xxxx;xxxxxx krmivo xxxxxxxxx xxxxxx substrát(y). Celý xxx&xxxx;3.1.2 xxxxxxx&xxxx;XX xx xxxxxxxx xx xxxxxxx xxxxxxxxxxxxxx x&xxxx;xxxxxx, xxxxx xxxx přímý katalytický xxxxxx na xxxxxx xxxxxxxxxxx xxxxx nebo x&xxxx;xxxxxxx na xxx xx udává, že xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxx. X&xxxx;xxxxxxx xxxx expozice xxxx xxxxxxxx zvýšení xxxxxxxx xxxxxxxxxxxxxxx xxxxx xxx xxxxxxxx doplňkové xxxxxx, xxx xxxx xxxxxxxxx neexistence xxxxxxxxxxxx xxxxxx na komenzální xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxx. X&xxxx;xxxxxxxxxxx xxxx xxxxx xxxxx xxxxxxxx xxxxxxxxxxx flóry pouze x&xxxx;xxxxxxx, že xxxxxx xxxxxxxxx xxxxxxxxxx xxxxx xxxxxx bachoru (měřeno xx vitro xxxx xxxxx koncentrací xxxxxxxx xxxxxxxx xxxxxxx, snížení xxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxx xxxxxxxxxx). |
|
4.2.3.2 |
Xxxxxx týkající xx bezpečnosti používání xxxxxxxxx látky xxx xxxxxxxxxxxx
Enzymy x&xxxx;xxxxxxxxxxxxxx xxxxx pouze xxxx xxxx xxxxxxxxx xxxxx, xxxxx xx xxxxxxx xxxxxxx xxxx xxxxxxxxx xxxx xxxxxx xxxxxxxxxxx z fermentačního xxxxxxx. Xxxxx je xxxxxxxx xxxxxxxxxx látku otestovat, xxx xxxx zajištěno, xx xxxxxxxxxx mutagenní xxxx xxxx xxxxxxxxx, xxxxx mohou poškodit xxxxxxx požívajícího xxxxxxxxx xxxxxxx xx xxxxxx, xxx xxxx xxxxxx xxxxxx xxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxx. Xxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxx xxxx nepřímé přijímání xxxxx (xxxxxx xxxxxxx) xx však xxxxxxxx xx skupin xxxxxxxxx, xxx něž xxxx x&xxxx;xxxxxxxxx xxxxx o zřejmém xxxxxxxxx používání, xxxx xx xxxxxx, xxx xxx xxxx xxxxxxx xxxxxx přesně xxxxxxxx. Xxxxxxx xxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxxx, xxxxx xx x&xxxx;xxxxxxxxxxx používají x&xxxx;xxxxxxxx xxxxxx, je obvykle xxxxxx rozpoznané a významně xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx. Proto se xxx enzymy z mikrobiálních xxxxxx x&xxxx;xxx xxxxxxxxxxxxxx, xxx xxx xxxx x&xxxx;xxxxxxxxx xxxxx o zřejmém xxxxxxxxx xxxxxxxxx, x&xxxx;xxxx-xx xxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx definované a známé, xxxxxxxxxx xxxxxxx toxicity (xxxx. xxxxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxxxxx) xx nutné. Xxxxx x&xxxx;xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxx k produkci xxxxxx xx xxxx xxxxx xx zabývat konkrétními xxxxxxxxxxxx uvedenými x&xxxx;xxxx 2.2.2.2 xxxxxxx&xxxx;XX. Xx-xx organismus xxxx xxxx xxxxx xxxx x&xxxx;xxxxxxxxxx xxxxxxxxxx xxxxxxxx o biologii (xxxxxxxxxxx) xxxxxxxxx, xxx xxx xxxxxxxx potenciál xxxxxxxx xxxxxxxxx metabolitů, xx xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx x&xxxx;xxxxxx xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx látkami, xxxxx obsahují xxxxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxxxxx. X&xxxx;xxxxx xxxxxxx xxxx xxxxxx studií xxxxxxxxxxxx xxxxxx xxxxxxxxxx x&xxxx;xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx. Xxxxxxxxxx xx, xxx xx tyto xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxx xxxxx xxxx v případě xxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx. |
|
4.2.3.3 |
Xxxxxx xxxxxxxx xx bezpečnosti doplňkové xxxxx pro xxxxxxxxx/xxxxxxxxxx Xxxxxxx xx xxxx bod 3.3 xxxxxxx&xxxx;XX x&xxxx;xxxxxxxx xxxxxx xxxxxxx:
|
|
4.2.3.4 |
Xxxxxx týkající se xxxxxxxxxxx doplňkové látky xxx xxxxxxx xxxxxxxxx Xxxx xxx&xxxx;3.4 přílohy II xx xxxxxxxx xxxx xx xxxxxxxxxxxxxx, xxxxx xxxxxx xxxxxxxxx xxxxxx nebo xxxxxx xxxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx. |
4.2.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Studie xxxxxxxx xx xxxxxxxxx doplňkových xxxxx
Xxxxxxx xx celý xxxxx&xxxx;XX přílohy II.
|
1. |
Doplňkové xxxxx, xxxxx xxxx xxxxxxxxx xxxx xx xxxxxxxxxx xxxxxx, užitkovost xxxx xxxxx xxxxxxx xxxxxxxx x&xxxx;xxx xxxxxxx xxxxxxx „xxxx zootechnické xxxxxxxxx xxxxx“. Xxxxxx xxx prokázat xxxxx xx xxxxxx xx xxxxxxx cílovému xxxxx xxxx xxxxxxxxx xxxxxx. X&xxxx;xxxxxxxxxx xx xxxxxxxxxxxx xxxxxxxxx xxxxx xxxxx být xxxxxx xxxxxxxx na xxxxxxxxxx xxxxxxxxxxxxxxxxx (xxxx. xxxxxxxxx xxxxxxxx, xxxxxxxx xxxxx xxxxxxxxx, xxxxxx živočišných xxxxxxxx), skladbě jatečně xxxxxxxxxx těla, xxxxxxxxxxx xxxxx, xxxxxxxxxxxxx xxxxxxxxxxx xxxx dobrých xxxxxxxxx xxxxxxxxxx xxxxxx. Důkaz x&xxxx;xxxxxxxxxx působení lze xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx. |
|
2. |
Xxxxxxxxx látky, které xxxxxxxxx xxxxxxxxx důsledky xxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxxx. X&xxxx;xxxxxxxxxxx látek, xxxxx xxxxxxxx ovlivňují xxxxxxx xxxxxxxxx (xxxx. xxxxxxx xxxxxxx dusíku xxxx xxxxxxx xxxx xxxxxxx xxxxxxxx metanu, xxxxxxxxx xxxxxxxx), xx xxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxx doložit xxxxx xxxxxxxxxxxx xxxxxxxx účinnosti xx xxxxxxx xxxxxxxxxxxxx xxxxxxxx prospěšné účinky. Xxxxxx vezmou v úvahu xxxxxxx přizpůsobení xx xxxxxxxxx látce. |
4.2.5 Oddíl V: Plán xxxxxxxxxxxx x&xxxx;xxxxxx xx uvedení xxxxx xx xxx
Xxxxx xxxxx xx xxxxxxx xxxxx ustanovení čl. 7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
5.&xxxx;&xxxx;&xxxx;XXXXXXXXXXXXXXX X&xxxx;XXXXXXXXXXXXXXXX
5.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx dokumentace
Použije xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
5.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, charakteristika x&xxxx;xxxxxxxx xxx xxxxx xxxxxxxxx xxxxx; xxxxxx xxxxxxx
Xxxxxxx xx celý xxxxx&xxxx;XX xxxxxxx&xxxx;XX.
5.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Studie xxxxxxxx xx xxxxxxxxxxx doplňkových xxxxx
5.3.1&xxxx;&xxxx;&xxxx;Xxxxxx týkající se xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx xxxxxxx
Xxxxxxx se xxxx xxx&xxxx;3.1 xxxxxxx&xxxx;XX.
5.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání xxxxxxxxx xxxxx xxx xxxxxxxxxxxx
Xxxxxxx xx xxxx xxx&xxxx;3.2 xxxxxxx&xxxx;XX.
5.3.3&xxxx;&xxxx;&xxxx;Xxxxxx týkající xx bezpečnosti xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxxxx/xxxxxxxxxx
Xxxxxxx xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
5.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxx xxxxxxxxx
Xxxxxxx se xxxx xxx&xxxx;3.4 xxxxxxx&xxxx;XX.
5.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx týkající se xxxxxxxxx xxxxxxxxx látky
Tyto xxxxxxxxx látky chrání xxxxxxx xxxx xxxxxxxx xxxxxx Eimeria xxx. xxxx Histomonas meleagridis. Xxxxxx se přikládá xxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx (xxxx. xxxxxxxxxxxx xxxx) a jejích xxxxxxxxxxxxxxx xxxxxxxxxxxx (xxxx. xxxxxxx xxxxxxxxx, xxxxxxxxx, xxxxx xxxxxx x&xxxx;xxxxxxx xxxxxxxxxx xxxx). Xxxxxxxxx xx předloží xxxxxxxxx x&xxxx;xxxxxx xx růst x&xxxx;xxxxxxxx krmiva (xxxxx xxxxxxx, náhrada xxxxxx x&xxxx;xxxxxxx), xxxxxxxx na xxxxxxx xxxxx (xxxxxxxx xxxxxx).
Xxxxxxxxxx xxxxx o účinnosti xxxx odvozeny ze xxx xxxx pokusů x&xxxx;xxxxxxxx xxxxxxx:
|
— |
xxxxx xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxx, |
|
— |
xxxxxxxxx/xxxxx xxxxxxx x&xxxx;xxxxx xxxxxxxxx xxxxxxxx xxx užití, |
|
— |
skutečné xxxxxxxx xxx xxxxx xxx xxxxxxxxx x&xxxx;xxxxxx. |
Xxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx (xxxx. xxxxxxx xxxx xxxxxxx) xxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxx xxxxxxxxx a nevyžadují replikaci. Xxx xxxxxxxx xxxxxxxx xx požadují pro xxxxxx xxxxxxxxxx podmínky xxx xxxxx (např. xxxxxx xxx xxxxxx xxxxxxxx x&xxxx;xxxxxxx, xxxxxx xxx xxxxxxxx xxxxx x&xxxx;xxxxxxx). Požadují xx xxxxxx xxx xxxxxx x&xxxx;xxxxxx s určitou xxxxx xxxxxxxxx xxxxxxx.
5.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx xx trh
Oddíl xxxxxxx&xxxx;XX se xxxxxxx xxxxx ustanovení xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
6.&xxxx;&xxxx;&xxxx;XXXXXXXXXXX X&xxxx;XXXXXXXXXXX XXXXX XX XXXXX XXXXXXXXX
Xxxxxxxxx xxxxx xxxx vymezeny x&xxxx;xx.&xxxx;1 odst. 2 xxxxxx xxxxxxxx.
X&xxxx;xxxxxx na xxxxxxxxx xxxxxxxxxx xxxxx pro xxxx, který xx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxx, xxx xxxx xxx bylo xxxxx xxxxxxxxx xxxxx xxxxxxxx, xx xxxxxxx nevyžaduje xxxxxxxxxx údajů v plném xxxxxxx.
Xxxx uvedené xxxxxxxxx xx xxxxxxxx xxxxx xx xxxxxxxxxx xxxxxxxx xxx menšinové druhy x&xxxx;xxxxxxx xx xxxxxxxxx xxxxx, které xxx xxxx povoleny pro xxxxx většinové. Pro xxxxxxxx xxxxxx xxxxxxxxxxx xxxxx požadovaná pouze xxx xxxxxxxxx druhy xx xxxxxxx xxxx xxxxxxx xxxxxx v závislosti xx xxxxxxxxx/xxxxxxx skupině xxxxxxxxx látky (xxx xxxxxxxxxxxx xxxxxxxx požadavky x&xxxx;xxxxxxx&xxxx;XXX).
6.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx oddíl I přílohy II.
6.2 Oddíl II: Xxxxxxxx, xxxxxxxxxxxxxxx a podmínky xxx xxxxx doplňkové xxxxx; xxxxxx xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX xx použije takto:
|
— |
pro xxxxxxxxx látky, xxxxx xxxx vázané na xxxxxxxx xxxxxxxx, se xxxxxxx xxxx xxxxx&xxxx;XX, |
|
— |
xxx xxxx xxxxxxxxx xxxxx xx xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
6.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx
6.3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx xxxxxxx
|
6.3.1.1 |
Xxxxxxxxx x&xxxx;xxxxxxxx xxxxx Xxxxx xxxxxxxxx xxx xxxxxxxxxx kategorie / xxxxxxx xxxxxxx xxxxxxxxxxx xxxxx. X&xxxx;xxxxxx xx xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx xxxxxxxxxx, xxxxx xxxxxxxxx xxxxx vykazuje xxxxxx rozpětí pro xxxxxxxxxx (xxxxxxx xxxxxxxxxx 10) u příslušného většinového xxxxx, xxxxx xx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxx. Xxxxx xxx xxxxxxxxx xxxxxx xxxxx (xxxxxx monogastrických x&xxxx;xxxxxxxxxxxx xxxxx a drůbeže) xxxxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxxx xxx xxxxxxxxxx, xxxxxxxxxx xx xxxxx xxxxxx xxxxxxxxx pro xxxxxxxxx xxxxx, xxxxx xxxxxx z fyziologického hlediska xxxxxxx (např. xxxx xxxx xxxxxxx). Xxxxx xx xxxxxxxx xxxxxx xxxxxxxxx, doba trvání xxxxxx pro menšinové xxxxx (xxxxx xxxxxxx) xxxx xxxxxxx 28&xxxx;xxx xxx xxxxxxx x&xxxx;xxxxx x&xxxx;42&xxxx;xxx pro xxxxxxx xxxxxxx. X&xxxx;xxxxxxx xxxxx xxxx doby trvání: xxxxx xxxxxxx: 28&xxxx;xxx; xxxxxx xxxxxxx: jeden xxxxxx (xx inseminace xx xxxxx doby xxxxxxx). Xxxxx se xxxxxx vztahuje xx xxxxxx x&xxxx;xxxxxxxxx xxxxxxx, xxxxxxxx xx xx xxxxxxxxxx xxxxxx 49&xxxx;xxx (xxxxxxxx jeden xxxxx xx xxxxxxxx) x&xxxx;xxxx xxxxxxxxx xxxxxxx až xx xxxxxxx. Xxx xxxx (xxxx xxx xxxxxxxxxx) xx xxxxxxxx 90xxxxx období. |
6.3.2 Studie xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxx jako spotřebitele
|
6.3.2.1 |
Studie xxxxxxxxxxx Xxxxx xxxxxxxxx pro xxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxx xxxxxxxxxxx látek. Studie xxxxxxxxxxx se nepožadují, xx-xx xxxxxxxxx xxxxx xxx povolena pro xxxxx x&xxxx;xxxxx, xxxxx xx z fyziologického hlediska xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx, xx xxx xx xxxxxxxx xxxxxx o povolení. Xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx, xxxxxxxx xx pro xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx za xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xx základě xxxxxx xx vitro (xxxx. s hepatocyty pomocí xxxxxxx látky). Není-li xxxxxxxxx xxxx x&xxxx;xxxxxxxxxxxxxx hlediska xxxxxxx většinovému druhu, xx nutno xxxxxx xxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx xxxxx u menšinového xxxxx. |
|
6.3.2.2 |
Xxxxxx xxxxxxx Xx-xx xxxxxxx xxxx xxxxxxxxx xxxxxxxxx metabolismu, xxxxxxxx xx xxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxxx a produktech. Xx xxxxx xxxxxxxxx xxxxxxxxx xx xxxxxxx xxxx xxx&xxxx;3.2.1.2 xxxxxxx&xxxx;XX. |
|
6.3.2.3 |
Xxxxxxxxx xxxxxxxxxxx pro xxxxxxxxxxxx Xxxxx xxxxxxxxxxx xxxxxx xxxxxxx (XXX) Xxxxxxxxx XXX lze xxxxxxx xx předpokladu, xx xx v poživatelných xxxxxxx menšinového druhu x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxx nevyskytují žádné xxxxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxxx. XXX xxx xxxxxxxxxxxx x&xxxx;xxxxx xxxx xxxxxx xxxxx:
XXX xxx xxxx xxx extrapolovat, xxxxx xxxxxxxx XXX pro xxxxxxxxxxx přežvýkavce x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxx. Xxxxx byly xxxxxxxx identické MLR x&xxxx;xxxxx (xxxx ovcí), xxxxxx a kuřat (nebo xxxxxxx), které xxxxxxxxxxx xxxxxxxxx xxxxx s různými xxxxxxxxxxxxx schopnostmi a složením xxxxx, je možno xxxxxxxx xxxxxx XXX xxxxxx pro xxxx, xxxxxxxx a králíky, xxx xxxxxxx, xx xx xxxxxxxx za xxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxx, která xxxx xxxxxx k produkci xxxxxxxx, x&xxxx;xxxxxxxx xxx. X&xxxx;xxxxxxx xx xxxxx Xxxxxx xxx xxxxxxxxxxx xxxxxx xxxxxxxxx (XXXX)&xxxx;(10) xxx xxxxxxxxx XXX xxx Xxxxxxxxxx x&xxxx;xxxxxxx ryby, xxxxx xxx xxxxxxxx xxxxxxxxxxx x&xxxx;XXX ve xxxxx xxxxxxxxxxx xxxxx xx Xxxxxxxxxx x&xxxx;xxxxxxx xxxx xx xxxxxxxxxxx, xx xxxxxxx látky xxxx xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxx xxx XXX ve svalu x&xxxx;xxxx, xxx XXX xxxxxxxxxxxx na všechna xxxxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxxx. Xxxx k dispozici analytické xxxxxx xxx monitorování xxxxxxx x&xxxx;xxxxxxxxxxxxx tkáních x&xxxx;xxxxxxxxxx xxxxx xxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxx. |
6.3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx látky xxx uživatele/pracovníky
Použije xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
6.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx se bezpečnosti xxxxxxxxx doplňkové látky xxx xxxxxxx xxxxxxxxx
Xxxxxxxxx xxxxx pro xxxxxxx xxxxxxxxx xxx extrapolovat x&xxxx;xxxxxxxxx xxxxxxxxxxx xxx xxxxxxxxx xxxx, xxxxx xx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx. Xxx xxxxxxxxx xxxxx, xxxxx xxxx xxx xxxxxxxxx u králíků, xx použije celý xxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxx každou xxxxxxxxx / xxxxxxx xxxxxxx xxxxxxxxxxx látek.
6.4 Oddíl IV: Studie xxxxxxxx xx účinnosti xxxxxxxxx látky
Pokud xxxxxxxxx xxxxx xxxx xxx xxxxxxx funkci xxxxxxxx xxx xxxxxxxxx xxxx, xxxxx xx x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx, x&xxxx;xxxxx xx znám nebo xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx, xx xxxxx xxxxxxxxx xx xxxxxxxx účinnosti xxxxxx x&xxxx;xxxxxxx xxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxxx xxxxx. Xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx, xx xxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxx xxxxxxxx xxx xxxxx&xxxx;XX x&xxxx;xxxxxxx&xxxx;XX. X&xxxx;xxxxxxxxx xxxxxxxxx xxxx xxx xxxxxx xxxxxxxxxx xxxxx xxxxxx xx xxxxxx xxxxxxxxxxx xxxx (xxxx. xxxx x&xxxx;xxxx používané x&xxxx;xxxxxxxx xxxxx). V každé studii (X&xxxx;≤ 0,1) nebo xxxxxx metaanalýzy (P ≤ 0,05), je-li xx xxxxx, xx měla xxx xxxxxxxxx xxxxxxxxxx.
Xxxxxxxx-xx xx xxxxxxxxx xxxxxxxxx, xxxx xxxxxx studií xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxx xxxxx, xxxxx je x&xxxx;xxxxxxxxxxxxxx hlediska xxxxxxxxxxx. X&xxxx;xxxxxxxxx xxxxxxxxx minimální xxxx xxxxxx studie xxxxxxx xxxxxxxxx xxxxxxxxxx x&xxxx;xxxx&xxxx;4.4 xxxxxxx&xxxx;XX x&xxxx;xxxxxxx&xxxx;XX.
6.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx xx xxx
Xxxxx xxxxx xxxxxxx&xxxx;XX xx xxxxxxx xxxxx xxxxxxxxxx čl. 7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;1831/2003.
7.&xxxx;&xxxx;&xxxx;XXXXXXX X&xxxx;XXXXXXXX CHOVU X&xxxx;XXXXXXX XXXXXXX, KTERÁ XXXXXX XXXXXX X&xxxx;XXXXXXXX XXXXXXXX
Xxxxxxx x&xxxx;xxxxxxxx xxxxx a ostatní xxxxxxx, xxxxx xxxxxx xxxxxx k produkci potravin, xxxx xxxxxxxx x&xxxx;xx.&xxxx;1 xxxx.&xxxx;1 tohoto xxxxxxxx.
7.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
7.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx pro xxxxx xxxxxxxxx látky; xxxxxx xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX xx xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, xxxxx xxxx xxxxxx xx xxxxxxxx xxxxxxxx, xx xxxxxxx xxxx oddíl II, |
|
— |
pro xxxx xxxxxxxxx xxxxx xx xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2., 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
7.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Studie týkající xx xxxxxxxxxxx xxxxxxxxx xxxxx
7.3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání doplňkové xxxxx xxx cílová xxxxxxx
Xxxxx xxxxxxxxx xxx xxxxxxxxxx kategorie / xxxxxxx xxxxxxx xxxxxxxxxxx xxxxx. Xxxxxxxx-xx se xxxxxx xxxxxxxxx, xxxx xxxx xxxxxx činí xxxxxxx 28&xxxx;xxx.
Xxxxxx tolerance xx xxxxxxxxxx, xxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxx xxxxxxx xxx xxxxxxxxxx x&xxxx;xxxxx xxxxxxxxxxx xxxxx (včetně xxxxxxxxxxxxxxx a přežvýkavých xxxxx x&xxxx;xxxxxxx).
7.3.2&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání doplňkové xxxxx pro xxxxxxxxxxxx
Xxxxx xxx se obvykle xxxxxxxxxx. Xxxxxxxxx xx xxxxxx bezpečnosti xxxxxxxx.
7.3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové xxxxx xxx uživatele/pracovníky
Použije xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
7.3.4&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx doplňkové látky xxx životní prostředí
Bod 3.4 xxxxxxx&xxxx;XX se xxxxxxxxxx.
7.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx týkající xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxxx xxxxxxxxx xxx xxxxxxxxxx xxxxxxxxx / xxxxxxx xxxxxxx xxxxxxxxxxx xxxxx.
Xxxxxxxx xxxxxxxxx látka, pro xxx xx xxxxxxxx xxxxxx xx xxxxxxxxx, xxx xxxx předem xxxxxxxx xxx druh, xxxxx xx z fyziologického xxxxxxxx xxxxxxx, xxxxxxxxxx xx xxxxx prokázání xxxxxxxxx, xxxx-xx požadovaný xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx xxxxxx. Xxxxx doplňková xxxxx nebyla xxxxx xxxxxxxx nebo xxxxxxxxxx xxxxxx xx xxxxxxxxxxx xxxxxxxx jsou jiné xxx v případě xxxxxxxxxxx xxxxxxxx, xx xxxxx xxxxxxxx xxxxxxxx podle xxxxxxxx pravidel xxx xxxxx&xxxx;XX x&xxxx;xxxxxxx&xxxx;XX.
Xxxx trvání xxxxxxxxxxxx xxxxxxx účinnosti xxxx nejméně 28 dní.
7.5 Oddíl V: Plán xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx na xxx
Xxxxx xxxxx přílohy II xx použije xxxxx xxxxxxxxxx čl. 7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
8.&xxxx;&xxxx;&xxxx;XXXXXXXXX XXXXX, XXXXX JIŽ XXXX XXXXXXXX XXX XXXXX X&xxxx;XXXXXXXXXXX
8.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
8.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxx xxxxx xxxxxxxxx xxxxx; metody xxxxxxx
Xxxxx&xxxx;XX xxxxxxx&xxxx;XX se xxxxxxx xxxxx:
|
— |
xxx xxxxxxxxx xxxxx, xxxxx xxxx vázané xx xxxxxxxx xxxxxxxx, xx xxxxxxx celý xxxxx&xxxx;XX, |
|
— |
xxx xxxx xxxxxxxxx xxxxx xx xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2., 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
8.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxx
Xxxx xxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx bezpečnosti xxxxxxxxxxxxxxx přídatných xxxxx x&xxxx;xxxxxxxx případnými následně xxxxxxxxx xxxxx.
Xxx doplňkové xxxxx, xxxxx jsou xxxxxxxx jako potravinářské xxxxxxxx xxxxx nebo xxxxxxxxx v Evropské xxxx xxxx xxxxxx xxxxxxxx xxx jakéhokoliv xxxxxxx, xxxxxx xxxxxx týkající xx bezpečnosti pro xxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx xxxxx.
Xxxxxx xx xxxx&xxxx;3.1, 3.2 x&xxxx;3.3 přílohy II xx xxxxxxxx xx xxxxxxxxx poznatky x&xxxx;xxxxxxxxxxx xxxxxx látek, pokud xxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx. Xxxxxxxx xxxxx, xxxxx xxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxx, xxx xxxxxxxxxxxx xxxx:
|
— |
x&xxxx;xxxxxxxxxxxxxxxx XXX (bez xxxxxxxxxx uvedení xxxxxxx xxxxxx xxxxxx xxx xxxxx x&xxxx;xxxxx xxxxxx xxxxxxxxx), |
|
— |
xx xxxxxxxxxx XXX xxxx XX xxxx |
|
— |
x&xxxx;xxxxxxxxxxxx XXX (xxx xxxxx, x&xxxx;xxxxx xxxxxxxx údaje xxxxxxxxxxx ke xxxxxxxx xxxxxx xxxxxxxxxxx). |
8.3.1&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání xxxxxxxxx látky xxx xxxxxx xxxxxxx
Xx-xx xxxxx xxxxx doplňkové látky xxxxxxx jako x&xxxx;xxxxxxx xxxxxxxx, lze bezpečnost xxx xxxxxx xxxxx xxxxxxxx na základě xxxxxxxxxx toxikologických údajů xx zkoušek in xxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx schopnosti xxxxxxxx xxxxx. Xx-xx xxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxxx xxxxx xxx xxxxxxxxxxxx xxxxx v potravinách, xxxx xxx xxxxx xxxxxx xxxxx xxxxx xxxxxx tolerance x&xxxx;xxxxxxxx xxxxxxx.
8.3.2&xxxx;&xxxx;&xxxx;Xxxxxx týkající se xxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx pro xxxxxxxxxxxx
Xxxxx xxxxx jako xxxxxxxxx xxxxx xxxx x&xxxx;xxxxx xxxxxxxx spotřebitele xxxx x&xxxx;xxxxxx druhu xxxxxxxxxx xxx v případě xxxxx x&xxxx;xxxxxxxxxxx, xxxxx xxxxxxxxxx xxxxx toxikologické xxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxxx.
|
8.3.2.1 |
Xxx doplňkové xxxxx, xxx xxx xxxx xxxxxxxxxxxxx XXX Xxxxxxxxx xxxxxxxxxxx pro xxxxxxxxxxxx xx xxxxxxxxxx xxxxx xxxxxxx, xxx xxxxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxx k odlišnému xxxxx xxxxxxxxxx xxx xxx xxxxx v potravinách. |
|
8.3.2.2 |
Doplňkové xxxxx xx xxxxxxxxxx XXX xxxx UL Bezpečnost xxx xxxxxxxxxxxx xx nutno xxxxxxxx x&xxxx;xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxx xxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxx. Xx lze xxxxxxx xxxxxxxxxxx údajů x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxxx. Xxxx-xx nezbytné studie xxxxxxx, požadavek je xxxxxx xx xxxxxxxx xxxxxx v tkáních xxxx xxxxxxxxxx u neošetřené skupiny x&xxxx;xxxxxxx, xxx xxxx xxxxxxxx xxxxxxxx udávaná xxxxx. |
|
8.3.2.3 |
Xxxxxxxxxxxxx xxxxxxxx xxxxx, xxx xxx xxxxxx XXX xxxxxxxxx Xx xxxxx xxxxxxxxxxx xxxxx xxxxxx, xxxx nebyla ADI xxxxxxxxx. Xxxxx xx xxxxxxxx obavy a užití xxxxxxxxx látky v krmivech xx přispělo x&xxxx;xxxxxxxxxx xxxxxxx expozice u spotřebitele, xxxxxxxx xx xxxxx xxxxxxxxxxxxx xxxxxxxxx. Xxxxxxxxxx expozici xxxxxxxxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxx xxx xxxxxxxxxxxx x&xxxx;xxxxx x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxxx. Xxxx-xx xxxxxxxx xxxxxx reziduí, požadavek xx xxxxxx xx xxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxx xxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx x&xxxx;xxxxxxx, jíž xxxx podávána xxxxxxxx xxxxxxx xxxxx. |
8.3.3&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xx xxxxxxxxxxx používání xxxxxxxxx látky pro xxxxxxxxx/xxxxxxxxxx
Xxxxxxx xx xxxx xxx&xxxx;3.3 xxxxxxx&xxxx;XX.
Xxx posuzování xxxxxxxxxxx doplňkové xxxxx xxx xxxxxxxxx xx xxxxxx x&xxxx;xxxxx bezpečnostní xxxxxxxx stanovená xxx xxxxxxxxxx s těmito xxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx.
8.3.4&xxxx;&xxxx;&xxxx;Xxxxxx týkající xx xxxxxxxxxxx používání xxxxxxxxx xxxxx xxx xxxxxxx xxxxxxxxx
Xxxxxxxx xx xxx&xxxx;3.4 přílohy II.
8.4 Oddíl IV: Xxxxxx xxxxxxxx se účinnosti xxxxxxxxx xxxxx
Xxxxxxxx xx xxxxxx xxxxxxxxxx xxx xxxxxx xxxxxx xxxx xxx xxxxx x&xxxx;xxxxxxxxxxx, xxxxxx xxx xxxxx xxxxx xxxxxxxxx účinnosti. X&xxxx;xxxxxxx xxxxxxx xxxxx xxxxxxxxx xx účinnost xxxxxxx x&xxxx;xxxxxx&xxxx;XX xxxxxxx&xxxx;XX.
8.5&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx látky na xxx
Xxxxx oddíl xxxxxxx&xxxx;XX xx xxxxxxx xxxxx xxxxxxxxxx xx.&xxxx;7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;1831/2003.
9.&xxxx;&xxxx;&xxxx;XXXXX XXXXXXXX
Xxxxxxx je xxxxx xxxxxx hodnocení údajů xxxxxxxxxxxx xxx předchozí xxxxxxxx, xxxx xxxxxxxxxxx xxxxxxxxxx pro žádost xxxxx xx.&xxxx;13 xxxx.&xxxx;3 xxxxxxxx (XX) x.&xxxx;1831/2003 xxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxx.
Xxxxxx x&xxxx;xxxxx xxxxxxxx zahrnutých ve xxxxxxxxxx povolení, např. xxxxxxxxxxxx, charakteristika xxxx xxxxxxxx pro xxxxx xxxxxxxxx látky, musí xxxxxxxx, xx změna xxxx xxxxx xxxxxxxx xxxxxx xxx xxxxxx xxxx, spotřebitele, uživatele xxxx životní xxxxxxxxx. Xx tímto xxxxxx xx xxxxx xxxxxxxxxx xxxxx xxxxxxxxx za xxxxxxxx, xxxxx xxxxxx xxxxx(x)&xxxx;xxxx činidlo(a) a podmínky xxx xxxxx jsou xxxxxx, xxxx xxxxxxx je x&xxxx;xxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxxx xxxxx xxxx xxxxxx, xxxxx xx xxxxxxxxxx xxxxx. Xxx xxxxxxxx xxxxxxxx je xxxxx podat xxxxxxxxx xxxxxx, xxxxxxx xxxxxxx xxxxxx nutné xxxxxxxx xxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxx xxx xxxxxx xxxx, xxxxxxxxxxxx a životní prostředí x&xxxx;xxxxxxxxx.
Xxxxxx xxxx xxxxxxxx xxxx požadavky:
|
1. |
použije se xxxx xxxxxxx&xxxx;X&xxxx;– xx xxxxxxxx xxxxx x&xxxx;xxxxxxxxxx xxxxx; |
|
2. |
xxxxxxx se xxxx xxxxx&xxxx;XX xxxxxxx&xxxx;XX; |
|
3. |
xx xxxxx xxxxxxxxxx údaje, které xxxxxxxxx, xx xxxxxxxx xxxx xxxxxxxxxx vlastnosti xxxxxxxxx xxxxx xxxx x&xxxx;xxxxxx stejné jako x&xxxx;xxxxxxx produktu; |
|
4. |
popřípadě xx xxxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxxxxx, a to xx xxxxxxx specifikace, xxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxx. Xxxx-xx xxxxxxxxxxxxxx xxxx prokázána, xx xxxxx xxxxxxxx shodu xxxxxxxx xxxxx x&xxxx;XXX; |
|
5. |
xx xxxxx xxxxxxxxx důkaz, xx xx současných xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxx xxxxx, xxxxxxxxxxxx, pracovníky a životní xxxxxxxxx; |
|
6. |
xx xxxxx předložit xxxxxx o výsledcích xxxxxxxxxxxx x&xxxx;xxxxxx xx xxxxxxx xxxxx xx trh, xxxx-xx xxxxxxxx xxxxxxxxx xx monitorování xxxxxxxx x&xxxx;xxxxxxxx; x |
|
7. |
xx nutno xxxxxxxxx xxxxxxxx xxxxx x&xxxx;xxxxxxxx žádosti o změnu x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxxx částmi xxxxxx&xxxx;XXX, XX x&xxxx;X&xxxx;xxxxxxx&xxxx;XX. |
10.&xxxx;&xxxx;&xxxx;XXXXXXXX XXXXXXXX
Xxxxxxx o obnovení povolení xxxxx článku 14 xxxxxxxx (XX) x.&xxxx;1831/2003 xxxxxxx xxxx xxxxxxxxx:
10.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx dokumentace
Použije xx xxxx oddíl I přílohy II. Xxxxxxxx se kopie xxxxxxxxx xxxxxxxx Xxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxxx xx trh xxxx xxxxxxxx xxxxxxxx žádosti. Xxxxxxxx se aktualizovaná xxxxxxxxxxx xxxxx nejnovějších xxxxxxxxx a předloží se xxxxxx x&xxxx;xxxxxxxx xxxxx xxxx xxxxxx původnímu xxxxxxxx xxxx xxxxxxxxxx xxxxxxxx povolení. Xxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx, xxxxx xxxxxxxx xxxxxx žádosti, x&xxxx;xxxxxxxx xxxx xxxxxxxxx, xxxxx xx xxxxx xxxxxxxxxx xx xxxx xxxxxxx xxxxxxxxxxx xxxxxxxx/xxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xx xxxxxxxx x&xxxx;xxxxxxxxxx.
10.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Identita, xxxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxx xxxxx xxxxxxxxx látky; metody xxxxxxx
Xxxxx&xxxx;XX přílohy II se xxxxxxx xxxxx:
|
— |
xxx doplňkové xxxxx, které xxxx xxxxxx na držitele xxxxxxxx, xx použije xxxx xxxxx&xxxx;XX, |
|
— |
xxx xxxx xxxxxxxxx xxxxx se xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6. |
Xx nutno xxxxxxxxx xxxxxx, xxxxx prokazují, xx xx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx, xxxxx xxx x&xxxx;xxxxxxx, xxxxxxx xxxx aktivitu, xxxxxx xxxxxxxx doplňkové xxxxx. Je xxxxx xxxxxxx xxxxxxxxxx změnu xxxxxxxxx xxxxxxx.
10.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Xxxxxx xxxxxxxx se xxxxxxxxxxx xxxxxxxxxxx látek
Musí být xxxxxxxxx xxxxx, xx xx současného xxxxx xxxxxxxx zůstává xxxxxxxxx xxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxxx pro xxxxxx xxxx, spotřebitele, xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx. Xxxx xxx předložena xxxxxxxxxxxxx dokumentace x&xxxx;xxxxxxxxxxx xx xxxxxx xx xxxxxxx xxxxxxxxx povolení xxxx xx xxxxxxxxxx xxxxxxxx povolení, xxxxx xxxxxxxx následující xxxxxxxxx:
|
— |
xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx, xxxxxx xxxxxxxxxx jevů (xxxxx xxxxxxx xxxxxx, xxxxxxx xxxxxx všeho xxxxx, xxxxxxx xxxxxx xxxxxxx xxxxxx) x&xxxx;xxxxxxxx xxxxxx, xxxxxxxxxxxx, xxxxxxxxx a v životním xxxxxxxxx. Xxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxx xxxx xxxxxx xxxxxx xxxxxx, xxxxx xxxxxxxxxxx xxxx/xxxxxx, xxxxxxxx, xxxxxxxx xxx xxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxxx, |
|
— |
xxxxxx x&xxxx;xxxxx xxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxx, |
|
— |
xxxxx z monitorování xxxxxxx, xx-xx xx xxxxx, |
|
— |
xxxxx z epidemiologických/epizootologických x/xxxx xxxxxxxxxxxxxxx studií, |
|
— |
jakékoliv xxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx látky x&xxxx;xxxxx doplňkové xxxxx xxx xxxxxxx, xxxxxxx x&xxxx;xxxxxxx xxxxxxxxx. |
Xxxxx nejsou xxxxxxxxxx xxxxx xxxxx xxxxxxxxx o některém z těchto xxxxxxx, xxxx to xxx xxxxxx odůvodněno.
Zpráva x&xxxx;xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxx xx uvedení xxxxx na xxx xx xxxxxxxx, je-li xxxxxxxx požadavek xx xxxxxxxxxxxx xxxxxxx v předchozím xxxxxxxx.
Xxxxx podle xxxxxxxxxx xx.&xxxx;14 xxxx.&xxxx;2 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003 xxxxxx x&xxxx;xxxxxxxx xxxxxxxx zahrnuje xxxxx xx změnu xxxx doplnění xxxxxxxx xxxxxxxxx povolení, xxxx xxxx xxxxxxxx týkajících xx xxxxxxxxx xxxxxxxxxxxx, xx xxxxx xxxxxxxxx xxxxxxxx xxxxx na xxxxxxx xxxxxx na xxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxx xxxxxx&xxxx;XXX, IV x&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
11.&xxxx;&xxxx;&xxxx;XXXXXXXXXXXX XXXXXXXXX XXXXXXXXXXX XXXXX, XXXXX XXX XXXX POVOLENY PODLE XXXXXXXX 70/524/EHS
Doplňkovými xxxxxxx, xxxxx se xxxx xxxxx xxx&xxxx;11, xxxx xxxxxxxxx xxxxx, xxxxx xxx byly xxxxxxxx xxxxx xxxxxxxx 70/524/XXX x&xxxx;xxxx xxx xxxxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;10 xxxx.&xxxx;2 xxxxxxxx (ES) x.&xxxx;1831/2003 x&xxxx;xxxxx xxxxx do xxxxxx skupin:
|
— |
antioxidační látky, |
|
— |
zchutňující x&xxxx;xxxxxxxxxxx xxxxx, |
|
— |
xxxxxxxxxx x&xxxx;xxxxxxxxxxxxx, xxxxxxxxxxx xxxxx a želírující xxxxx, |
|
— |
xxxxxxx, xxxxxx xxxxxxxx, |
|
— |
xxxxxxxxxxx, |
|
— |
xxxxxxxx, xxxxxxxxxxx a chemicky xxxxxx xxxxxxxxxx xxxxx se xxxxxxxxxxxx xxxxxxx, |
|
— |
xxxxxxx xxxxx, |
|
— |
xxxxxx, xxxxxxxxxxxx látky x&xxxx;xxxxxxxxxx; |
|
— |
xxxxxxxxxx xxxxxxxxx x |
|
— |
xxxxxxxxxxxxx xxxxxx. |
Xxxxxx x&xxxx;xxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxx doplňkových xxxxx xxxx xxx podobná xxxx u jiných xxxxxxxxxxx xxxxx. Avšak xxxxxxxx x&xxxx;xxxxxx xxxxxxxx xxxxxx xxxxxxxxxx používání je xxxxx xxxxxx údaje x&xxxx;xxx xxxxxxxxxxxx studií xxxxx xxxxxxxxxx xxxxxx xxxxxxxx, aby xxxx xxxxxxxxx, že xx xxxxxxxxxxx podmínek xxxxxxxxx xxxxx xxxxxxx xxxxxxxx xxx xxxxxx xxxxx, xxxxxxxxxxxx, xxxxxxxxx a životní xxxxxxxxx.
11.1&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;X:&xxxx;Xxxxxxx dokumentace
Použije se xxxx xxxxx&xxxx;X&xxxx;xxxxxxx&xxxx;XX.
11.2&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxxxx, xxxxxxxxxxxxxxx a podmínky xxx xxxxx xxxxxxxxx xxxxx; xxxxxx analýzy
Oddíl II přílohy II xx použije takto:
|
— |
pro xxxxxxxxx xxxxx, xxxxx xxxxxx xxxxxx xx xxxxxxxx povolení, se xxxxxxx xxxx&xxxx;2.1.2, 2.1.3, 2.1.4, 2.1.4.2, 2.2, 2.3.1, 2.3.2, 2.4.1, 2.4.2, 2.4.4, 2.5, 2.6, |
|
— |
xxx xxxx xxxxxxxxx xxxxx, které xxxx xxxxxx na držitele xxxxxxxx, xx xxxxxxx xxxx xxxxx&xxxx;XX. |
11.3&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XXX: Studie xxxxxxxx se xxxxxxxxxxx xxxxxxxxxxx látek
Pokud xxxx xxxxxxxxx látka posouzena x&xxxx;xxxxxxx na xxxxxxxxxx xxx cílové druhy, xxxxxxxxxxxx, xxxxxxxxx/xxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxx, předloží xx xxxxxxx xxxxxx bezpečnosti xxxxxxxxxxxx pro xxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxx xxxxxxxxx, které xxxx xxxxxxx xx xxxx xxxxxxx xxxxxxxxxxx xxxxxxxx. Xxxxx xxxxxx xxxxxxxx xxxxxxxxx bezpečnosti xxxxxxxxx xxx užití xxxxx xxxx xxxxxxxxx xxxxx, xxx xxxxxx studie x&xxxx;xxxxx x&xxxx;xxxxxxx literatury, xxxxxxxx xxxx rovnocenné xxxxxx, xxxxx xx xx xxxxxxxxxx x&xxxx;xxxx xxxxxxx. V opačném xxxxxxx xx xxxxxxxx xxxxx xxxxxx xxxxxx xxxxxxxxxxx.
11.4&xxxx;&xxxx;&xxxx;Xxxxx&xxxx;XX: Xxxxxx týkající xx xxxxxxxxx xxxxxxxxx xxxxx
Xxxxx x&xxxx;xxxxxxxxx xx xxxxxxxx xxxxx xx.&xxxx;5 xxxx.&xxxx;3 xxxxxxxx (XX) č. 1831/2003 xx možno popřípadě xxxxxxxx předložením xxxxxx xxxxxxxxx xxx studie, xxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxxx používání.
11.5 Oddíl V: Plán xxxxxxxxxxxx x&xxxx;xxxxxx po xxxxxxx xxxxx xx xxx
Xxxxx oddíl xxxxxxx&xxxx;XX xx xxxxxxx xxxxx xxxxxxxxxx čl. 7 xxxx.&xxxx;3 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;1831/2003.
(1)&xxxx;&xxxx;Xxxxxxxx xxxxx je xxxxxxxx xxxxx, která xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxx xx xxxx xxxxx xxxxxxxx. Xxxx xxxxxxxxx xxxxxx xxxxx, xxxxx xxxx xxxxxxxx x&xxxx;xxxxxx xxxxxxx xxxxxxxxxxxxx, xxx xx xxxxxxx.
(2)&xxxx;&xxxx;Xxx xxxxx tohoto xxxxxxxx xx „xxxxxxxx xxxxxxxx“ xxxxxx proces, xxx xxxx xx xxxxxxxxx xxxxxxxxxxxxxx organické hmoty xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxxx a/nebo xxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxx.
(3)&xxxx;&xxxx;Xxxxxxxxxxxxx číslo xxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx používané xx XXXXXX, xxxxxxxxxxx xxxxxxx XX xxx xxxxxxxxxxx xxxxx, databáze x&xxxx;xxxxxxxx Xxxxxx (XX) x.&xxxx;1565/2000 xx xxx 18.&xxxx;xxxxxxxx 2000 (Xx.&xxxx;xxxx. X&xxxx;180, 19.7.2000 x.&xxxx;8), kterým xx xxxxxxx xxxxxxxx xxxxxxxx pro xxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx (XX) x.&xxxx;2232/96 (Xx.&xxxx;xxxx. X&xxxx;180, 19.7.2000 x.&xxxx;8).
(4)&xxxx;&xxxx;X.&xxxx;Xxxx Xxxxxx: xxxxx Xxxx Xxxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxx xx xxxxxx Xxxx Xxxxxx x.&xxxx;1 „Xxxxxxx xxxxxxx of xxxxxxxxxxx“, xx.&xxxx;X,&xxxx;Xxxxxxxxx&xxxx;2000 a následujících xxxxxxxx.
(5)&xxxx;&xxxx;Xxxxx XXX (č. CAS) Xxxxxxxxxxx xxxxx podle Chemical Xxxxxxxxx Xxxxxxx, xxxxxxxxxxx xxxxxxxxxxxxx chemických xxxxx xxxxx používaný x&xxxx;xxxxxxxxx xxxxxxxxxx xxxxx.
(6)&xxxx;&xxxx;Xxx účely xxxxxx xxxxxx nařízení xx „xxxxxxxxxxxxx xxxxxxxxx xxxxxx“ xxxxxx xxxxx x&xxxx;xxxxxxxxxx xxxxxx nebo xxxxxxxx xxxxxxx (TDI xxxx TWI), XXX, xxxx x&xxxx;xxxxxxxx, pokud xxx x&xxxx;xxxx xxxxxxxxx, xxxx xxxxxx xxxxxx, xxx xx xxxxxxxxx xx xxxxxxxx Xxxx 88/388/XXX xxxxxxxx xx xxxxx xxxxxxxx x&xxxx;xxxxxxxxxxx xxx použití x&xxxx;xxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxx xxxxxx výrobu, xxxx xxxxxxxxx xxxxx.
(7)&xxxx;&xxxx;Xxxxxxxxx v dodatku 4 xxxxxx Rady Evropy x.&xxxx;1 „Xxxxxxx xxxxxxx xx xxxxxxxxxxx“, xx.&xxxx;X,&xxxx;Xxxxxxxxx, 2000.
(8)&xxxx;&xxxx;XXXXX (FAO/WHO, 1996, Xxxx xxxxxxxx xxxxxx 35, XXXX, XXX Xxxxxx) odpovídající xxxxxxx xxxxxxx xxx cílové xxxxx xx xxxx xxx xxxxxxxx s přihlédnutím x&xxxx;xxxxxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxx.
(9)&xxxx;&xxxx;Xx.&xxxx;xxxx. L 180, 19.7.2000, x.&xxxx;8.
(10)&xxxx;&xxxx;Xxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxx Xxxxxxxxxx x&xxxx;xxxxxxx xxxx. Xxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxxx. Xxxxxxxxxx Xxxxxxxxx Xxxxxxxxxx Xxxx. XXXX/XXXX/153x/97-XXXXX.
XXXXXXX XX
Xxxxxxxxx x xxxxxxxx cílových xxxxxx x xxxx x xxxxxxxxx xxxx xxxxxx xxxxxx xxxxxxxxx
1. Xxxxxxx. Xxxxxxxxx zvířat: xxxxxxx
|
Xxxxxxxxx |
Xxxxxxxx kategorie xxxxxx |
Xxxxxxxxx xxxx xxxxxx (hmotnost/stáří) |
Minimální xxxx xxxxxx dlouhodobých xxxxxx účinností |
||
|
Období/stáří |
Stáří |
Xxxxxxxx |
|||
|
Xxxxxx (xxxxxx) |
Xxxxx xxxxxxx sající mléko xx xxxxxxx |
Od xxxxxxxx |
Xx xx 21–42 xxx |
Xx xx 6–11 xx |
14 xxx |
|
Xxxxxx (odstavená) |
Mladá xxxxxxx xx skončení xxxxxx xxxx xxxxxxx x xxxxxxxxxx xxxx pro masnou xxxxxxxx |
Xx 21–42 xxx |
Xx xx 120 xxx |
Xx xx 35 xx |
42 dní |
|
Xxxxxx (xxxxxx x xxxxxxxxx xxxxxx) |
Xxxxx xxxxxxx xx xxxxxxxx xxxxxxx x xxxxxxxxxx xxxx xxx masnou produkci |
Xx xxxxxxxx |
Xx do 120 dní |
Xx xx 35 kg |
58 xxx |
|
Xxxxx prasat |
Xxxxxxx xx xxxxxxx xxxxxx x xxxxx xxxxxxxx xx xx xxx xxxxxx xx xxxxx |
Xx 60–120 xxx |
Xx xx 120–250 dní (xxxx xxxxx xxxxxxxx xxxxxxxxx) |
80–150 xx (xxxx xxxxx xxxxxxxx xxxxxxxxx) |
Xx xx jateční xxxxxxxxx, xxxxxxx xxxx 70 xxx |
|
Xxxxxxxx xxxxxx x xxxxxxxxxx |
Samice xxxxxxx, xxxxx xxxx xxxxxxx jednou xxxxxxxxxxxx/xxxxxxxxxx |
Xx xxxxx inseminace |
|
|
Xx inseminace xx xxxxx odstavu xxxxxxx vrhu (xxx xxxxx) |
|
Xxxxxxxx xxxxxx x xxxxxxxxxx xxxxx |
Xxxxxx prasete, xxxxx xxxx nejméně xxxxxx xxxxxxxxxxxx/xxxxxxxxxx |
|
|
|
Xxxxxxx xxx xxxxx xxxx porodem xx xxxxx doby xxxxxxx |
2. Xxxxxxx. Xxxxxxxxx xxxxxx: xxxxxx
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx xxxxxx |
Xxxxxxxxx doba xxxxxx (xxxxxxxx/xxxxx) |
Minimální xxxx xxxxxx dlouhodobých xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxx xxxxx |
Xxxxxx xxxxxx xxx xxxxx |
Xx vylíhnutí |
Xx xx 35 xxx |
Xx xx ~1 600 x (xx xx 2 xx) |
35 dní |
|
Odchov kuřat x xxxxxx |
Xxxxxxxx xxxxxxx xxx xxxxxxxx produkci vajec xxxx pro xxxxxx xxxxx |
Xx xxxxxxxxx |
Xx do ~16 xxxxx (xx xx 20 xxxxx) |
— |
112 xxx (xxxxxx-xx xxxxx x xxxxxxxxx x xxxxxxxxx pro xxxxx xxxxx) |
|
Xxxxxxx |
Xxxxxxx xx xxxxxx xxxxxxx xxx xxxxxxxx xxxxx |
Xx 16–21 xxxxx |
Xx do ~13 xxxxx (xx do 18 xxxxxx) |
Od 1 200 x (xxxx), 1 400 x (xxxxx) |
168 xxx |
|
Xxxxx krůt |
Xxxxx x xxxxxxx xxxxxxx xx xxxxx |
Xx xxxxxxxxx |
Xx xx ~14 xxxxx (xx xx 20 xxxxx) Xx xx ~16 xxxxx (xx xx 24 xxxxx) |
Xxxxxx: xx xx ~7 000 x (xx xx 10 000 x) Samci: xx xx ~12 000 x (xx do 20 000 g) |
84 dní |
|
Krůty xxx xxxxx xxxxxxxxxx |
Xxxxx a krocani xxxxxxx xxx účely xxxxxxxxxx |
Xxxx xxxxxx |
Od 30 týdnů xx xx ~ 60 xxxxx |
Samice: xx ~15 000 x Xxxxx: xx ~30 000 x |
Nejméně xxxx měsíců |
|
Xxxxxx xxxx |
Mladé xxxxx x xxxxxxx xxxxxx x xxxxxxx účelům |
Xx vylíhnutí |
Až xx 30 týdnů |
Samice: xx xx ~15 000 x Xxxxx: až xx ~30 000 x |
Celé xxxxxx (nejsou-li xxxxx x xxxxxxxxx k dispozici xxx xxxxx krůt) |
3. Xxxxxxx. Xxxxxxxxx xxxxxx: skot (xxxxxx xxxx, včetně xxxxx xxxxxxx x xxxxx)
|
Kategorie |
Xxxxxxxx kategorie xxxxxx |
Xxxxxxxxx doba xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx xxxx trvání xxxxxxxxxxxx xxxxxx účinností |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx xxxxx |
Xxxxxx xxxxxxx pro xxxxxxxxxx xxxx xxxxxxxx xxxxxxxx masa |
Od narození |
Xx xx 4 xxxxxx |
Až do 60–80 xx (xx do 145 xx) |
56 xxx |
|
Xxxxx xxxxx |
Xxxxxx pro xxxxxxxx telecího masa |
Od xxxxxxxx |
Xx xx 6 xxxxxx |
Až xx 180 kg (xx do 250 xx) |
Xx xxxxxxx, xxxxxxx xxxx 84 dní |
|
Výkrm skotu |
Xxxx xx odstavu xxxxxx x xxxxx produkci xx xxx xxxxxx xx xxxxx |
Xx xxxxxxx xxxxxxx xxxxxxxxxxxx |
Xx xx 10–36 xxxxxx |
Xx xx 350–700 kg |
168 xxx |
|
Dojnice xxx xxxxxxxx xxxxx |
Samice skotu, xxxxx xxxxxxxx xxxxxxx xxxxx xxxx |
|
|
|
84 dní (je xxxxx xxxxx xxxx xxxxxx xxxxxxx) |
|
Xxxxx x xxxxxxxxxx |
Xxxxxx xxxxx, které byly xxxxxxx jednou inseminovány/připuštěny |
Xx xxxxx inseminace do xxxxx druhého xxxxxxx |
|
|
Dva xxxxx (pokud xx xxxxxxxx reprodukční parametry) |
4. Tabulka. Xxxxxxxxx xxxxxx: xxxx
|
Kategorie |
Xxxxxxxx xxxxxxxxx zvířat |
Přibližná xxxx xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx xxxx xxxxxx dlouhodobých xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx jehňat |
Xxxxxxx chovaná xxx xxxxxxx xxxxxxxxxx |
Xx xxxxxxxx |
Xx do 3 měsíců |
15–20 xx |
56 xxx |
|
Výkrm xxxxxx |
Xxxxxxx xxxxxxx pro xxxxxxxx xxxxxxxxx xxxx |
Xx xxxxxxxx |
Xx do 6 xxxxxx (xxxx xxxxxx) |
Až xx 55 xx |
Xx xxxxxxx hmotnosti, xxxxxxx xxxx 56 dní |
|
Xxxx xxxxxx x xxxxxxxx xxxxx |
Xxxx, xxxxx xxxxxxxx nejméně xxxxx xxxxx |
|
|
|
84 dní (xx xxxxx uvést xxxx xxxxxx xxxxxxx) |
|
Bahnice x xxxxxxxxxx |
Xxxxxx xxxx, xxxxx byly xxxxxxx xxxxxx inseminovány/připuštěny |
Xx xxxxx inseminace do xxxxx xxxxxxx xxxxxxx |
|
|
Xxx xxxxx (pokud se xxxxxxxx xxxxxxxxxxx xxxxxxxxx) |
5. Tabulka. Xxxxxxxxx zvířat: xxxx
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx zvířat |
Xxxxxxxxx xxxx xxxxxx (hmotnost/stáří) |
Xxxxxxxxx xxxx xxxxxx dlouhodobých xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx xxxxxx |
Xxxxx xxxx xxxxxxx pro xxxxxxx xxxxxxxxxx |
Xx xxxxxxxx |
Xx xx 3 xxxxxx |
15–20 xx |
Xxxxxxx 56 xxx |
|
Xxxxx kůzlat |
Xxxxx xxxx xxxxxxx pro xxxxxxxx xxxxxx masa |
Od xxxxxxxx |
Xx xx 6 měsíců |
|
Nejméně 56 xxx |
|
Xxxx xxxxxx k produkci xxxxx |
Xxxx nejméně x xxxxxx xxxxxxxx |
|
|
|
84 xxx (xx xxxxx xxxxx xxxx xxxxxx xxxxxxx) |
|
Xxxx x xxxxxxxxxx |
Xxxxxx xxxx, xxxxx xxxx xxxxxxx xxxxxx xxxxxxxxxxxx/xxxxxxxxxx |
Xx xxxxx xxxxxxxxxx xx konce xxxxxxx odstavu |
|
|
Xxx cykly (xxxxx xx požadují xxxxxxxxxxx xxxxxxxxx) |
6. Tabulka. Kategorie xxxxxx: xxxx
|
Kategorie |
Xxxxxxxx kategorie xxxxxx |
Xxxxxxxxx doba xxxxxx (xxxxxxxx/xxxxx) |
Xxxxxxxxx doba xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Hmotnost |
|||
|
Losos x xxxxxx |
|
|
|
200–300 x |
90 xxx xxxx xx xxxx, kdy xx xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx |
|
Xxxxx x xxxxxx |
Xxxxx xxxxxxxxx xxx |
Xxxxx xxxxx xx xxxxxxxx xxxx xxxxx |
|
|
90 xxx |
7. Xxxxxxx. Xxxxxxxxx zvířat: xxxxxxx
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx zvířat |
Přibližná xxxx xxxxxx (xxxxxxxx/xxxxx) |
Minimální doba xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxxxx x xxxxxxxxx xxxxxxx |
|
Xxxxxxxx xx xxxxxxx týdne xx xxxxxxxx |
|
|
56 xxx |
|
Xxxxx xxxxxxx |
Králíci xxxxxxx xxx xxxxxx xxxxxxxx |
Xx xxxxxxx |
Až xx 8–11 xxxxx |
|
42 xxx |
|
Xxxxxx králice (xxx xxxxxxxxxx) |
Xxxxxxx, které byly xxxxxxx jednou xxxxxxxxxxxx/xxxxxxxxxx |
Xx xxxxxxxxxx xx konce xxxxxxx xxxxxxx |
|
|
Xxx xxxxx (xxxxx se xxxxxxxx xxxxxxxxxxx xxxxxxxxx) |
|
Xxxxxx xxxxxxx xxxxxx x xxxxxxxx xxxxxxx xxxxxxx |
Xxxxxxx, které xxxx xxxxxxx jednou xxxxxxxxxxxx |
Xx xxxxx inseminace |
|
|
Xxxxxxx 2 týdny xxxx xxxxxxx xx xxxxx xxxx xxxxxxx (např. xxx produkt xxxxxxxxxxxxxx) |
8. Xxxxxxx. Xxxxxxxxx zvířat: xxxx
|
Xxxxxxxxx |
Xxxxxxxx xxxxxxxxx xxxxxx |
Přibližná doba xxxxxx (hmotnost/stáří) |
Xxxxxxxxx doba xxxxxx dlouhodobých xxxxxx xxxxxxxxx |
||
|
Xxxxxx |
Xxxxx |
Xxxxxxxx |
|||
|
Xxxx |
Xxxxxxx xxxxxxxxx |
|
|
|
56 dní |


