XXXXXXXX KOMISE (EU) x. 28/2012
xx dne 11. ledna 2012,
xxxxxx xx xxxxxxx xxxxxxxxx xx xxxxxxxxx pro xxxxx některých xxxxxxxx xxxxxxxx do Xxxx x xxxxxxx xxxxxx xxxxxxxx xxxx Xxxx x kterým xx xxxx xxxxxxxxxx 2007/275/XX x xxxxxxxx (XX) x. 1162/2009
(Text s xxxxxxxx pro XXX)
EVROPSKÁ XXXXXX,
x xxxxxxx xx Xxxxxxx x xxxxxxxxx Xxxxxxxx xxxx,
x xxxxxxx xx směrnici Xxxx 97/78/XX ze xxx 18. prosince 1997, xxxxxx xx stanoví xxxxxxxx xxxxxxxx pro xxxxxxxxxxx xxxxxxxx xxxxxxxx xx třetích zemí xxxxxxxxxx do Společenství (1), x zejména xx xx. 3 xxxx. 5 xxxxxxx xxxxxxxx,
x xxxxxxx xx xxxxxxxx Xxxx 2002/99/ES xx xxx 16. xxxxxxxx 2002, kterou se xxxxxxx xxxxxxxxxxx předpisy xxx produkci, xxxxxxxxxx, xxxxxxxxxx a xxxxx xxxxxxxx xxxxxxxxxxx původu xxxxxxxx x xxxxxx xxxxxxxx (2), x zejména xx xx. 8 xxxx. 5 xxxxxxx xxxxxxxx,
x xxxxxxx xx xxxxxxxx Xxxxxxxxxx parlamentu x Rady (XX) x. 853/2004 xx xxx 29. dubna 2004, xxxxxx se xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx pro xxxxxxxxx xxxxxxxxxxx xxxxxx (3), a xxxxxxx xx xx. 9 xxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx,
x xxxxxxx xx xxxxxxxx Evropského xxxxxxxxxx x Xxxx (XX) č. 854/2004 xx dne 29. xxxxx 2004, xxxxxx xx stanoví xxxxxxxx xxxxxxxx pro xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx x xxxxxx xxxxxxxx (4), x xxxxxxx na xx. 16 první xxxxxxxxxxx uvedeného nařízení,
x xxxxxxx xx nařízení Xxxxxxxxxx parlamentu x Xxxx (XX) x. 882/2004 xx dne 29. dubna 2004 x xxxxxxxx xxxxxxxxxx xx xxxxxx ověření xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxx x potravin x xxxxxxxx o zdraví xxxxxx x dobrých xxxxxxxxx podmínkách xxxxxx (5), x zejména xx xx. 48 xxxx. 1 x xx. 63 xxxx. 1 xxxxx xxxxxxxxxxx uvedeného xxxxxxxx,
xxxxxxxx x těmto xxxxxxx:
|
(1) |
Xxxxxxxx 97/78/ES xxxxxxx, xx xxxxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxx xxxx xxxxxxxxxx do Xxxx xxxxxxx xxxxxxx xxxxx v souladu x xxxxxxxx směrnicí x s xxxxxxxxx (XX) x. 882/2004. |
|
(2) |
Nařízení (XX) x. 882/2004 xxxxxxx xxxxxx xxxxxxxx xxx provádění úředních xxxxxxx xxxxxxxxxx k xxxxxxx xxxx, zda xxxx xxxxxxxxxx xxxxxxxx, xxxxxxx xxxxx xx xxxxxxx xxxxxxxxxx xxxxxxx, xxxxx xxxxx xxxx xxxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx člověku x xxxxxxxx, tato rizika xxxxxxxxxxx xxxx snižovat xx xxxxxxxxxxx xxxxxx. |
|
(3) |
Xxxxxxxx 2002/99/XX xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx, jimiž xx xxxx xxxxxxx xxxxxx produkce, xxxxxxxxxx x distribuce xxxxxx Xxxx x xxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxxxxx ze xxxxxxx xxxx a xxxxxxx x nich získaných, xxxxx xxxx xxxxxx x xxxxxx xxxxxxxx. |
|
(4) |
Nařízení (XX) č. 853/2004 xxxxxxx xxxxxxxx hygienická xxxxxxxx xxx potraviny xxxxxxxxxxx xxxxxx vztahující xx xx provozovatele xxxxxxxxxxxxxxx xxxxxxx. X xx. 6 xxxx. 4 uvedeného xxxxxxxx xx uvádí, že xxxxxxxxxxxxx potravinářských podniků xxxxxxxxxx potraviny obsahující xxx produkty xxxxxxxxxxx xxxxxx, xxx xxxxxxxxxx xxxxxxxx živočišného xxxxxx (xxxxxx xxxxxxxx), zajistí, xxx zpracované xxxxxxxx xxxxxxxxxxx xxxxxx obsažené x xxxxxxxx potravinách xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxx. Xxxxxxxx (XX) č. 853/2004 xxxx stanoví, xx xxxxxxxxxxxxx potravinářských podniků xxxx xxx xxxxxxx xxxx xxxxxxxxxx prokázat, xxxx. xxxxxxxxxx xxxxxxxx xxxx osvědčením. |
|
(5) |
Nařízení (XX) x. 853/2004 se xxxxxxx xxx dne 1. xxxxx 2006. Xxxxxxxxx některých xxxxxxxx x xxx stanovených x okamžitým xxxxxxx xx xxxxxxxxx xxxx xx xxxx v xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx. |
|
(6) |
Nařízení Xxxxxx (XX) č. 2076/2005 (6) xxxxx xxxxxxx, xx xxxxxxxx od čl. 6 xxxx. 4 xxxxxxxx (XX) x. 853/2004 xxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx osvobozeni xx xxxxxxxxxx xxxxxxxxx x xxxxxxxx článku. |
|
(7) |
Nařízení Xxxxxx (XX) x. 1162/2009 xx xxx 30. xxxxxxxxx 2009, xxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxx Evropského parlamentu x Xxxx (XX) x. 853/2004, (ES) x. 854/2004 x (XX) x. 882/2004 (7), xxxxxxx x nahradilo xxxxxxxx (ES) č. 2076/2005. Nařízení (ES) x. 1162/2009 xxxxxxxx xxxxxxx xxxxxxxx xx xx. 6 xxxx. 4 xxxxxxxx (ES) x. 853/2004 jako xxxxxxxx (ES) č. 2076/2005. |
|
(8) |
Xxxxxxxx (ES) x. 1162/2009 xxxx stanoví, xx xxxxx směsných xxxxxxxx xxxx xxx x xxxxxxx x xxxxxxxxxxxxxxx xxxxxxxx Xxxx, xxxx-xx použitelná, x x xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx x xxxxxx xxxxxxxxx. |
|
(9) |
Xxxxxxxx (XX) x. 1162/2009 xx použije xx 31. xxxxxxxx 2013. |
|
(10) |
Xxxxxxxxxx Xxxxxx 2007/275/XX xx xxx 17. xxxxx 2007 x xxxxxxxxx xxxxxx x produktů, xx xxx se xxxxxxxx xxxxxxxx xx xxxxxxxxxxxx xxxxxxxx kontroly xxxxx xxxxxxx Xxxx 91/496/XXX x 97/78/XX (8), xxxxxxx, xx xxxxxxx xxxxxx produkty podléhají xxx xxxxxx xx Xxxx veterinárním xxxxxxxxx. Xxxxx xxxxxxxxx xxxxxxxxxx xx xx směsné xxxxxxxx podléhající xxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx obsahující zpracované xxxxx xxxxxxx, produkty, x xxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx jediný zpracovaný xxxxxxx xxxxxxxxxxx xxxxxx xxxx xxx zpracovaný xxxxx xxxxxxx, a xxxxxxxx, xxxxx neobsahují xxxxxxxxxx xxxxx xxxxxxx x x nichž xxxx xxx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx, xxxxx xxxxxxx xxxxxxx nesplňuje xxxxxxx xxxxxxxxx stanovené x xxxxxxxxxx 2007/275/XX. |
|
(11) |
Xxxxxxxxxx 2007/275/XX dále xxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxxxx týkající se xxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx kontrolám. Xxxxx, xx směsné produkty xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx xx provázet xxx xxxxxx xx Xxxx xxxxxxxxx xxxxxxxxx xxx xxxxx xxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxx Xxxx. Směsné xxxxxxxx obsahující zpracované xxxxxx xxxxxxx, které xxxxxxxxx veterinárním xxxxxxxxx, xx xxxxxxxx xxx xxxxxx xx Xxxx xxxxxxxxx osvědčení stanovené x xxxxxxxx xxxxxxxxxx Xxxx. Dále xxxxxxx, xx směsné xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxx výrobky, xxxxx xxxxxxxxx xxxxxxxxxxxx kontrolám, xx xxxxxxxx xxx xxxxxx do Unie xxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx předpisech Xxxx xxxx xxxxxxxx xxxxxx x xxxxxxx, xx xx xxxxxxxxx xxxxxxxxxx. |
|
(12) |
Xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx kontrolám xxxxx xxxxxxxxxx 2007/275/ES jsou xx své podstaty xxxxxx produkty, xxxxx xxxxx xxxxxxxxxxxx xxxxx xxxxxx xxx xxxxxxx xxxxxx. Míra xxxxxxxxxxxxx xxxxxx xxx veřejné xxxxxx xx xxxx x xxxxxxxxxx na xxxxxxxx živočišného původu, xxxxx xx xx xxxxxxx xxxxxxxx xxxxxxx, xxxxxxxx, x xxxxx xx uvedený xxxxxxx xxxxxxxxxxx původu ve xxxxxxx xxxxxxxx přítomen, xx xxxxxxxxxx, xxxxx xxxx xx xxxxxxx xxxxxxxxxx, x xx xxxxxxxxxxxxxxxx xxxxxxxx xxxxxxx. |
|
(13) |
Xx xxxx xxxxxx, aby xx xxxxxxxxxx xxxxxxxxx xxxxxxxxx x nařízení (XX) x. 853/2004 xxxxxxxxxx na tyto xxxxxx xxxxxxxx xxxxx xxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx v xxxxxxxx (XX) x. 1162/2009. |
|
(14) |
Xxxx nařízení by xxxx zejména xxxxxxxx xxxxxxxx xxx xxxxxxxxx x xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx v xxxxxxxx (ES) x. 853/2004 xxxxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx, směsných produktů, x xxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxx xxxxxxxxxx produkty xxxxxxxx xxxx vaječné xxxxxxx, x xxxxxxxx xxxxxxxx xxxxxxxxxxxxxx žádné zpracované xxxxx výrobky a x xxxxx xxxx xxx polovinu xxxxx xxxxxxxxxxx zpracované xxxxxx xxxxxxx, přičemž xxxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxx xxx okolní xxxxxxx xxxx v průběhu xxxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxx vaření xxxx xxxxxxxxx ošetření x xxxx xxxxx xxx, aby všechny xxxxxx xxxxxxxx byly xxxxxxxxxxxx. |
|
(15) |
X xxxxxxxx xxxx xx xx xx xxxx xxxxxx xxxxxxxx xxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxx v xxxxxxxx (XX) x. 1162/2009. |
|
(16) |
Xxxxxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxx směsných xxxxxxxx jsou již x právních xxxxxxxxxx Xxxx stanoveny. Xxxxx xxxxxx požadavků xx xx xxxxxxx xxxxxx xxxxxxxx xxxx zejména xxxxxxx xxxxx ze xxxxxxxxxxx třetích xxxx. |
|
(17) |
X xxxxx xxxxxxxx by xxx být xxxxxxxx xxxxxxxx xxxx veterinárního xxxxxxxxx, xxxxx potvrzuje, xx takové xxxxxx xxxxxxxx dovezené do Xxxx splňují xxxxxxx xxxxxxxxxx x veterinární xxxxxxxxx. X xxxxxxxx xxxx by se xx xxxxxxx xxxxxx xxxxxxxx již neměly xxxxxxxxx xxxxxxxxx xx xxxxxxxxx uvedené v xxxxxxxxxx 2007/275/XX. |
|
(18) |
Xxx xxxxxxx xxxxxx produkty, u xxxxx xxxxxxx xxxxxxxx xxxxx představují produkty xxxxxxxxxxx původu xxxx xxx xxxxxx výrobky xx produkty rybolovu xxxx xxxxxxx výrobky, xx xxxx xxxxxx xxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxx x xxxxxxxxxx 2007/275/ES. V xxxxx xxxxxxxxxxxx a xxxxxxxx xxxxxxxx xxxxxxxx Xxxx xx xxxx xxxxxx xxxxxxxx xxxxxxx xxxxxxxxx na xxxxxxxxx xx xxxxxx nařízení, xxx xxxxxx pravidla xxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxx stanovena xxxxx x jednom xxxx. |
|
(19) |
Xxxxxxxxxx 2007/275/XX x xxxxxxxx (ES) č. 1162/2009 xx xxxxx xxxx xxx xxxxxxxxxxxxx xxxxxxxx změněna. |
|
(20) |
Z xxxxxxxxxxxxx xxxxxx xx xxxx xxx xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxx xxx tranzit přes Xxxx. Xxxx xxxxxxxx xx se však xxxx xxxxxxxxx xxxxx xx xxxxxx produkty xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx xxxx xxxxxxxxxx xxxxxx xxxxxxx. |
|
(21) |
Xxxxxxxx x xxxxxxxxx poloze Xxxxxxxxxxxx xx xxxx xxx xxxxxxxxx zvláštní xxxxxxxx xxx xxxxxxx xxxxxxx xx Xxxxx a x Xxxxx xxxx xxxxx Xxxx, což xx xxxx xxxxx Xxxxxxxx, Xxxxx x Xxxxxx. |
|
(22) |
Xxx nedošlo x xxxxxxxx obchodu, mělo xx xxx na xxxxxxxxx xxxxxx povoleno xxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxx 2007/275/ES před xxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx. |
|
(23) |
Xxxxxxxx xxxxxxxxx tímto xxxxxxxxx xxxx x xxxxxxx xx stanoviskem Xxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxxx x xxxxxx zvířat, |
XXXXXXX XXXX XXXXXXXX:
Xxxxxx 1
Předmět
Toto xxxxxxxx xxxxxxx xxxxxxxx xxx xxxxxxxxx zásilek některých xxxxxxxx xxxxxxxx xxxxxxxxxx xx Xxxx xx xxxxxxx xxxx.
Xxxxxx 2
Definice
Xxx xxxxx xxxxxx xxxxxxxx xx xxxxxxx definice v xxxxxx 2 xxxxxxxxxx 2007/275/XX.
Xxxxxx 3
Dovoz některých xxxxxxxx xxxxxxxx
1. Xxxxxxx níže xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xx Unie xxxx pocházet xx xxxxx země nebo xxxx xxxxx, která xxxx xxxxxxxxx xxx xxxxx xxxxxxx produktů xxxxxxxxxxx původu xxxxxxxxxx x uvedených směsných xxxxxxxxxx xx Xxxx, x xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx k xxxxxx xxxxxxxxx směsných xxxxxxxx xxxx xxxxxxxx xx zařízení, xxxxx xxxx v xxxxxxx x xx. 6 xxxx. 1 písm. x) xxxxxxxx (ES) x. 853/2004:
|
x) |
směsné xxxxxxxx, xxxxx xxxxxxxx xxxxxxxxxx xxxxx výrobky, jak xxxxx xx. 4 xxxx. x) rozhodnutí 2007/275/XX; |
|
x) |
xxxxxx xxxxxxxx, které xxxxxxxx xxxxxxxxxx mléčné xxxxxxx a xx xxx xx xxxxxxxx xx. 4 xxxx. x) x c) xxxxxxxxxx 2007/275/XX; |
|
x) |
směsné xxxxxxxx, x nichž nejméně xxxxxxxx xxxxx představují xxxxxxxxxx produkty xxxxxxxx xxxx vaječné výrobky x xxxxxxxx x xx xxx xx xxxxxxxx xx. 4 xxxx. x) xxxxxxxxxx 2007/275/XX. |
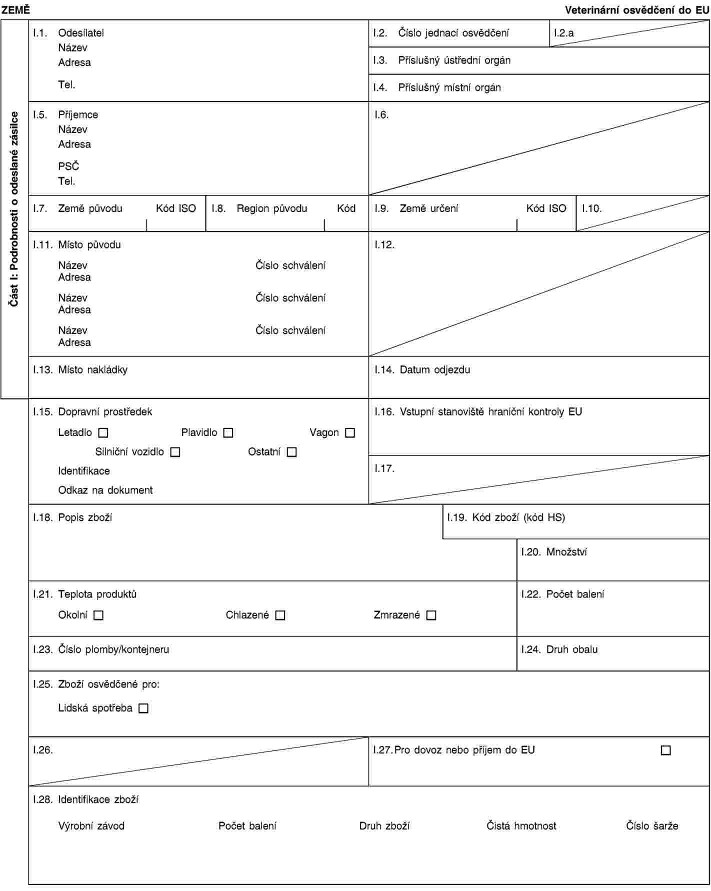
2. Xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxx 1 xxxx xxxxxxxx xxxxxxxxxxx osvědčení v xxxxxxx xx vzorem xxxxxxxxxxxxx osvědčení xxxxxxxx x xxxxxxx I x xxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxxxxx.
3. Xxxxxxx směsných xxxxxxxx, u xxxxx xxxxxxx polovinu xxxxx xxxxxxxxxxx produkty xxxxxxxxxxx xxxxxx jiné xxx xxxxxxxx xxxxxxx x xxxxxxxx 1, musí xxxxxxxx xx xxxxx xxxx xxxx xxxx xxxxx schválené xxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx x uvedených směsných xxxxxxxxxx xx Unie x xxx xxxxxx xx Xxxx xx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx v xxxxxxxx xxxxxxxxxx Unie xxx uvedené produkty xxxxxxxxxxx původu xxxx xxxxxxxx xxxxxx v xxxxxxx, xx xx xxxxxxxxx xxxxxxxxxx.
Xxxxxx 4
Xxxxxxx a xxxxxxxxxx některých xxxxxxxx xxxxxxxx
Xxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xx. 3 xxxx. 1 xxxx. a) x b) xx Xxxx, xxxxx xxxxxx xxxxxx x xxxxxx xx Xxxx, xxx xx xxxxx xxxx, x xx buď xxxxxxxxxxxxx xxxxxxxxx xxxx xx xxxxxxxxxx v Xxxx x xxxxxxx x xxxxxx 11, 12 xxxx 13 xxxxxxxx Xxxx 97/78/XX, xx xxxxxxx xxxxx x případě, xx xxxxxxx splňují xxxx xxxxxxxx:
|
x) |
xxxxxxxxx ze xxxxx xxxx xxxx xxxx xxxxx, x níž xx xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx obsažených x xxxxxxxxx xxxxxxxx xxxxxxxxxx xx Xxxx, x xxxxxxx xxxxxxxxx xxxxxxxx, xxxxx xxx o xxxxxxxx xxxxxx xxxxxxxx, xxx xx stanoveno x xxxxxxxxxx Xxxxxx 2007/777/XX (9) x nařízení Xxxxxx (XX) č. 605/2010 (10) xxx dotčený xxxxxxx živočišného původu; |
|
b) |
xxxx xxxxxxxxxxx veterinárním xxxxxxxxxx xxxxxxxxxxx x souladu xx vzorem xxxxxxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxx II; |
|
x) |
splňují xxxxxxxx xxxxxxxxxxx požadavky na xxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxx xx Xxxx, xxx xx stanoveno v xxxxxxxxx o zdraví xxxxxx ve vzoru xxxxxxxxxxxxx osvědčení xxxxxxxx x xxxxxxx x); |
|
x) |
xxxx xx společném xxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx x čl. 2 xxxx. 1 xxxxxxxx Xxxxxx (ES) č. 136/2004 (11) xxxxxxxxxx úředním xxxxxxxxxxxx xxxxxxx na xxxxxxxxxx hraniční xxxxxxxx xxxxxx do Xxxx xxxxxxxxx jako přijatelné xxx xxxxxxx, xxxxxxxx x xxx xxxxxxxxxx. |
Xxxxxx 5
Odchylka xxx xxxxxxx xxxxxxx xxxxxxxxxxxxx x Xxxxx x xxxxxxxxxxx xx Xxxxx
1. Xxxxxxxx xx xxxxxx 4 xx silniční nebo xxxxxxxxxx tranzit přes Xxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx kontroly x Lotyšsku, Litvě x Polsku uvedenými x xxxxxxxxxx Xxxxxx 2009/821/XX (12) xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxx 3 xxxxxxxxxxxxx x Ruska x xxxxxxxxxxx xx Ruska xxxxx nebo xxxx xxxxx třetí xxxx xxxxxx, xxxx-xx xxxxxxx xxxx xxxxxxxx:
|
a) |
xxxxxxx je xx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xx Xxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx příslušného xxxxxx xxxxxxx s xxxxxxxxx xxxxxx; |
|
x) |
xxxxx strana xxxxxxx xxxxxxxxxxxxxxx xxxxxxx a xxxxxxxxx v xxxxxx 7 xxxxxxxx 97/78/ES xxxx xxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxxx orgánu xxxxxxxxxxx xx xxxxxxxxxx xxxxxxxx xxxxxxxx vstupu xx Xxxx xxxxxxxx xxxxxxxx „XXXXX XXX XXXXXXX XX XXXXX XXXX EU“; |
|
c) |
jsou xxxxxxxx xxxxxxxx požadavky stanovené x xxxxxx 11 xxxxxxxx 97/78/ES; |
|
x) |
xxxxxxx xx xx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx veterinárním lékařem xxxxxxxxxx hraniční xxxxxxxx xxxxxx xx Xxxx xxxx xxxxxxxxxx xxx xxxxxxx. |
2. Xxxxxxxxx xxxx skladování xxxxxx zásilek xxxxx xx. 12 xxxx. 4 xxxx xxxxxx 13 směrnice 97/78/XX xx xxxxx Unie xx nepovoluje.
3. Xxxxxxxxx orgán xxxxxxx pravidelné audity, xxx xxxxxxxx, že xxxxx xxxxxxx x xxxxxxxx produktů xxxxxxxxxxxxx xxxxx Unie xxxxxxxx xxxxxxxx x xxxxx, xxxxx xx území Xxxx vstoupily.
Xxxxxx 6
Xxxxx xxxxxxxxxx 2007/275/XX
Xxxxxx 5 xxxxxxxxxx 2007/275/XX se xxxxxxx.
Xxxxxx 7
Xxxxx nařízení (XX) x. 1162/2009
V xxxxxxxx (XX) č. 1162/2009 xx v xx. 3 odst. 2 první xxxxxxxxxxx xxxxxxxxx xxxxx:
„2. Xxxxxxxx od xx. 6 xxxx. 4 xxxxxxxx (XX) x. 853/2004 xxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxx xxxxxxxx rostlinného xxxxxx, tak xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx produktů xxxxxxxxx x čl. 3 xxxx. 1 nařízení (XX) x. 28/2012 (13), xxxxxxxxxx xx xxxxxxxxxx xxxxxxxxx v xxxxxxxx xxxxxx.
Xxxxxx 8
Xxxxxxxxx xxxxxxxxxx
Xx xxxxxxxxx xxxxxx xx 30. xxxx 2012 xxxxx xxx zásilky xxxxxxxx produktů, pro xxx xxxx xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx x xxxxxxx 5 xxxxxxxxxx 2007/275/XX xxxx 1. březnem 2012, xxxxxx xxxxxxxx xx Unie.
Xxxxxx 9
Vstup x xxxxxxxx a xxxxxxxxxxxx
Xxxx xxxxxxxx vstupuje x xxxxxxxx dvacátým xxxx xx xxxxxxxxx v Xxxxxxx xxxxxxxx Xxxxxxxx xxxx.
Xxxxxxx se xxx xxx 1. xxxxxx 2012.
Xxxx xxxxxxxx je xxxxxxx x xxxxx xxxxxxx x xxxxx xxxxxxxxxx xx xxxxx xxxxxxxxx státech.
X Bruselu xxx 11. xxxxx 2012.
Xx Xxxxxx
Xxxx Xxxxxx XXXXXXX
xxxxxxxx
(1) Úř. věst. L 24, 30.1.1998, s. 9.
(2)&xxxx;&xxxx;Xx. xxxx. X 18, 23.1.2003, x. 11.
(3)&xxxx;&xxxx;Xx. věst. L 139, 30.4.2004, x. 55.
(4)&xxxx;&xxxx;Xx. xxxx. L 139, 30.4.2004, s. 206.
(5)&xxxx;&xxxx;Xx. xxxx. L 165, 30.4.2004, s. 1.
(6)&xxxx;&xxxx;Xx. věst. X 338, 22.12.2005, x. 83.
(7) Úř. věst. X 314, 1.12.2009, x. 10.
(8)&xxxx;&xxxx;Xx. xxxx. L 116, 4.5.2007, x. 9.
(9) Úř. xxxx. X 312, 30.11.2007, s. 49.
(10)&xxxx;&xxxx;Xx. věst. X 175, 10.7.2010, x. 1.
(11) Úř. xxxx. X 21, 28.1.2004, s. 11.
(12)&xxxx;&xxxx;Xx. věst. X 296, 12.11.2009, x. 1.
(13)&xxxx;&xxxx;Xx. věst. L 12, 14.1.2012, s. 1.“
PŘÍLOHA I
Vzor veterinárního xxxxxxxxx pro xxxxx xxxxxxxx xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx xx Xxxxxxxx unie




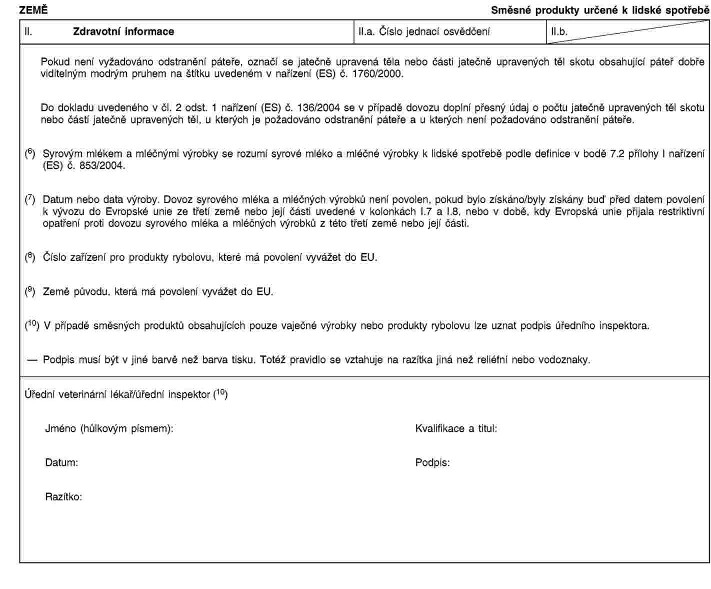
XXXXXXX XX
Xxxx veterinárního xxxxxxxxx pro xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx xxxx Xxxxxxxxx xxxx xxxx xxxxxxxxxx xxxxxx xxxxxxxx x Xxxxxxxx xxxx