XXXXXXXX XXXXXX (ES) x. 2074/2005
xx xxx 5. prosince 2005,
kterým xx stanoví xxxxxxxxx xxxxxxxx pro xxxxxxx xxxxxxx xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (ES) č. 853/2004 x xxx xxxxxxxxxx xxxxxxxx kontrol xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Xxxx (XX) x. 854/2004 x (XX) č. 882/2004, kterým xx xxxxxxx xxxxxxxx xx xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) x. 852/2004 x xxxxxx xx xxxx xxxxxxxx (XX) x. 853/2004 x (XX) x. 854/2004
(Xxxx x xxxxxxxx xxx XXX)
XXXXXX XXXXXXXXXX XXXXXXXXXXXX,
x xxxxxxx xx Xxxxxxx o xxxxxxxx Evropského společenství,
x xxxxxxx xx nařízení Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) x. 852/2004 xx xxx 29. dubna 2004 x xxxxxxx xxxxxxxx (1), x xxxxxxx xx xx. 13 xxxx. 2 uvedeného xxxxxxxx,
x xxxxxxx xx xxxxxxxx Evropského xxxxxxxxxx x Xxxx (ES) x. 853/2004 xx xxx 29. xxxxx 2004, xxxxxx xx xxxxxxx zvláštní xxxxxxxxxx xxxxxxxx pro xxxxxxxxx xxxxxxxxxxx xxxxxx (2), x zejména na xxxxxx 9, 10 x 11 xxxxxxxxx xxxxxxxx,
x xxxxxxx na xxxxxxxx Evropského parlamentu x Xxxx (XX) x. 854/2004 xx xxx 29. xxxxx 2004, kterým xx xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxxx produktů xxxxxxxxxxx xxxxxx xxxxxxxx k xxxxxx xxxxxxxx (3), x xxxxxxx na xxxxxx 16, 17 x 18 uvedeného xxxxxxxx,
x xxxxxxx xx xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (ES) x. 882/2004 ze xxx 29. xxxxx 2004 x xxxxxxxx xxxxxxxxxx xx účelem xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xx xxxxx x xxxxxxxx x pravidel o xxxxxx zvířat x xxxxxxx xxxxxxxxx podmínkách xxxxxx (4), x xxxxxxx na článek 63 xxxxxxxxx xxxxxxxx,
vzhledem x xxxxx xxxxxxx:
|
(1) |
Nařízení (XX) č. 853/2004 xxxxxxx zvláštní hygienická xxxxxxxx pro xxxxxxxxx xxxxxxxxxxx xxxxxx. Je xxxxx xxxxxxxx xxxxxx xxxxxxxxx opatření xxx xxxx, živé xxxx, xxxxxxxx xxxxxxxx, xxxxx, xxxxx, xxxx xxxxxxxx x hlemýždě x x xxxx xxxxxxxxxx xxxxxxx. |
|
(2) |
Xxxxxxxx (XX) x. 854/2004 xxxxxxx xxxxxxxx xxxxxxxx xxx organizaci xxxxxxxx xxxxxxx produktů xxxxxxxxxxx původu xxxxxxxx x xxxxxx xxxxxxxx. Xx xxxxx upřesnit xxxxxx xxxxxxxx x xxxxxxxx xxxxx požadavky. |
|
(3) |
Xxxxxxxx (XX) č. 882/2004 xxxxxxx na úrovni Xxxxxxxxxxxx xxxxxxxxxxxxx rámec xxxxxxxx xxxxxxxx pro xxxxxxxxxx xxxxxxxx kontrol. Xx xxxxx xxxxxxxx xxxxxx xxxxxxxx x xxxxxxxx xxxxx xxxxxxxxx. |
|
(4) |
Xxxxxxxxxxx Xxxxxx 20XX/.../XX (5) xx ruší xxxxxxx xxxxxxxxxx, xxxxxxx xx xxxxxxxxx xxxxxxxx směrnic xxxxxxxxx směrnicí Xxxxxxxxxx xxxxxxxxxx x Xxxx 2004/41/XX xx xxx 21. xxxxx 2004, xxxxxx xx zrušují xxxxxxx xxxxxxxx týkající xx hygieny potravin x xxxxxxxxxxxx podmínek xxx produkci některých xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx x lidské xxxxxxxx x xxx xxxxxx xxxxxxx xx xxx a kterou xx xxxx xxxxxxxx Xxxx 89/662/XXX x 92/118/XXX x xxxxxxxxxx Xxxx 95/408/XX (6). Xxxxxxx části xxxxxxxxxxx xxxxxxxxxx xx tedy xxxx xxxxxx xxxxxxxxx x xxxxx nařízení. |
|
(5) |
Xxxxxxxx (XX) x. 852/2004 xxxxxxxx od provozovatelů xxxxxxxxxxxxxxx podniků, xxx xxxxx a xxxxxxxxxx xxxxxxx x xx xxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxx xxxxxxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx, xxxxx xx xxxxxx odběratelem. |
|
(6) |
Nařízení (ES) x. 853/2004 xxxxxx xx xxxxxxxxxxxxx xxxxx xxxxxxxx, xxx xxxxxxxxxx, xxxxxxxx x xxxxxxxxxxxxx xxxxxxxxx o xxxxxxxxxxxx xxxxxxx xxx všechna xxxxxxx xxxxx xxxxxxx, xxxxx xxxx xxxxxxxx xxxx xxxx xxx xxxxxxxx xx xxxxx, x xxx podle xxxxxx xxxxxxxxx xxxxxxx. Xxxxx toho by xxxx zajistit, aby xxxxxxxxx o potravinovém xxxxxxx xxxxxxxxxx veškeré xxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxx (XX) x. 853/2004. |
|
(7) |
Xxxxxxxxx x potravinovém xxxxxxx pomáhají provozovateli xxxxx xxx organizování xxxxxxxx x xxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx. Xxxxxxxxx o xxxxxxxxxxxx řetězci xx xxx xxxxxxxxxx úřední xxxxxxxxxxx xxxxx x xxxx by xx xxxxxxxx xxxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx. |
|
(8) |
Je xxxxx xx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxxx x xxxxxxxxxxx xx xxxxxxxxxx xx informace x xxxxxxxxxxxx řetězci xxxxx xxxxxxxx (XX) x. 854/2004. |
|
(9) |
Xx xxxxx xxxxxxx xxxxxx xxxxxx v xxxxxxxxxxxx xxxxx xxxxxxxx (XX) x. 854/2004 xx xxx xxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxx x v případě xxxxxxx xxxxxx provozovateli xxxxxxxxxxxxxxx xxxxxxx, ze xxxxxxx xxxxxxx pocházejí, x xxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxx v xxxxxxxxxxxx, xx xxxxxxx xxxxxxx pocházejí, xxxx xxxxxxxxxx dotčenému xxxxxxxxxxx xxxxxx jakoukoli xxxxxxx xxxx xxxx xxxxxxxx xx jatkách x xxxxxxx na jednotlivá xxxxxxx xxxx xx xxxxx/xxxxx, xxxxx xxxxx xxx vliv na xxxxxxx xxxxxx xxxx xxxxxx xxxxxx xxxx xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxx. |
|
(10) |
Xxxxxxxx (XX) x. 853/2004 x (XX) x. 854/2004 xxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxxxx xxx xxxxxxxxxx s xxxxxxxx xxxxxxxx xx xxxxxxx x na xxxxxx xxxxxxxx. V xxxxxxx x xxxxxxxx xxxxx xxxxxxx XXX xxxxxx XXXX xxxxxxxx X xxxxx X xxxxxxxx (XX) x. 853/2004 xxxx provozovatelé xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx, xxx x xxxxxxxx xxxxxxxx xxxxxxxx ve xxxxx xxxxxx produkce xxxxxxx xxxxxxxx x xxxxx xxxxxxx xxxx, aby xxxx ryby xxxxxxxxx xxxxxxxx parazity xxxxxxxxx x lidské xxxxxxxx. Xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx se xxxxxxxx xxxxxxxx x xxxxx xxxx xxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx x stanovit xxxx x xxxxxxxxx xxxxxxxxxx. |
|
(11) |
Xxxxxxxx xxxxxxxxx v xxxxxxxx (XX) č. 853/2004, xxxxxxx xxxxxx je xxxxxxxx xxxxxxx xx xxx xxxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxx, mohou xxxxxxxxx x určitá xxxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxxxx xxxxxx xxxxxxxx xxxx (XXXX). X případě xxxxxxxxx xxxxx je xxxxx xxxxxxxx xxxxxx ABVT, xxxxx xxxxx být xxxxxxxxxx, x xxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxx. Xxxx xx xx pokračovat v xxxxxx xxxxxxxxx metod xxxxxxx, které xxxx xxxxxxx uznány xxxx xxxxxx xxx xxxxxxxx XXXX, xxxxxxx xxx xxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx xxxx x xxxxxxx xxxxx by xxxx být xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx. |
|
(12) |
Mezní xxxxxxx xxxxxxxxxxxxx xxxxxx (XXX = Xxxxxxxxx Xxxxxxxxx Xxxxxx), xxxxxx „Xxxxxxx Shellfish Xxxxxx“ XXX x xxxxxxxxxxx xxxxxx xxxx xxxxxxxxx x xxxxxxxx (XX) x. 853/2004. Referenční xxxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxx a xxxxxxxx xxxxx xxxxxxxxx xxxxxxx korýšů x xxxxxxx xx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxx. Xx xxxxxx xxxxxxx xxxxxxxx xxxxxx by xxxx být xxxxxxxxxxxxx xxxxxxxxx xxxxxx a xxxxxx xxxxxxx x xxxxxxx xxxxx by xx měly uplatňovat. Xxxxx xxxxxxxxxxxx vyšetřovacích xxxxx xx xxxx xxx xxxxxxxx x xxxxxxxxxxxx xxxxxx xxxxxxxxxx, xxxx. chemické xxxxxx x zkoušky xx xxxxx, xxxxxxx-xx se, xx xxxxxxx xxxxxx xxxx přinejmenším xxxxxx xxxxxx xxxx xxxxxx xxxxxxxxxx a xx xxxxxx xxxxxxxxx zajišťuje xxxxxxxxxxxx úroveň xxxxxxx xxxxxxxxx xxxxxx. Navrhované xxxxxxxxx xxxxxx lipofilních xxxxxx xxxxxxxxx x xxxxxxxxxxx xxxxx a xxxx by xxx xxxxx xxxxxxxxx, jakmile xxxxx xxxxxxxx nová xxxxxxx fakta. Xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxx nebiologických xxxxxxxxx x xxxxxxxx xxxx znamená, xx xxxxxx xxxxxxx xxxxxxxxx xxxxxx zajišťovaná x xxxxxxx xx všechny xxxxxx toxiny xxxxxxxxxx xxxxxx, kterou xxxxxxxx xxxxxxxxxx xxxxxxxxx. Xx xxxxx přijmout xxxxxx xxxxxxxx xxx nahrazení xxxxxxxxxxxx xxxxxxxxx. |
|
(13) |
Xxxxxxxxxx xxxxxxxxxx xxxx (XXX) získané xxxxxx xxxxxxx, které xxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxx xxxxxx XXX, xx xxxx xxx xxxxxxxxxx xx xxxxxxx xx XXX xxxxxxxxx pomocí technik, xxxxx strukturu xxxxx xxxx. |
|
(14) |
XXX prvně jmenovaného xxxxx, xxxxx bylo xxxxxxx za xxxxxx xxxxxxxxxxx xxxxxxxx x xx přesně xxxxxxxxx xxxxxxx, by mělo xxx přípustné v xxxxxxx xxxxxxxxxxxx, jež xxxxxx xxxxxx xx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx. Podmínky xx xxxxxx xxxxxxx xxxxxx xxxxxxx v XXX, xxxxx xx xxx být xxxxxxxx x xxxxxxx x xx. 11 xxxx. 2 xxxxxxxx (ES) x. 853/2004. Xxxxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxx x tomto xxxxxxxx by xxx xxx xxxxxxxxxxx, jakmile xxxxx dostupné xxxxxxxx xxxxx o xxxxxxxxxx x xxxxxxxxxx xx xxxxxxx různých xxxxxxx. |
|
(15) |
Xxxxx xx. 31 xxxx. 2 písm. x) xxxxxxxx (ES) x. 882/2004 xxxxx xxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx. Je xxxxx xxxxxxxx xxxxxxxx xxxxx xxx zpřístupňování xxxxxxxxxxx informací xxxxxxxx xxxxxxxx xxxxxx a xxxxxxxxxx. |
|
(16) |
Xxxxxxx III oddíl XX xxxxxxxx (XX) x. 853/2001 xxxxxxx xxxxxxxxx xx xxxxxxxx xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx k xxxxxx xxxxxxxx. Xxxxxxxx xxxxxxxxx včetně xxxxx xxxxxxxxxxxxx osvědčení je xxxxx xxxxxx stanovit xxx xxxx xxxxxxxx x hlemýždě určené x lidské xxxxxxxx x xxxxxxxx xx xxxxxxx xxxx. |
|
(17) |
Xxxxxxx III xxxxxx XIV x XX nařízení (ES) x. 853/2001 stanoví xxxxxxxxx xx xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx k xxxxxx xxxxxxxx x xxxxxx xxxxxxx na trh. Xxxxxxxx xxxxxxxxx včetně xxxxx veterinárních xxxxxxxxx xx třeba rovněž xxxxxxxx xxx xxxxxxxx x xxxxxxx xxxxxx x lidské xxxxxxxx x xxxxxxxx ze xxxxxxx xxxx a xxx xxxxxxxx k xxxxxx želatiny a xxxxxxxx xxxxxx x xxxxxx xxxxxxxx x xxxxxxxx ze třetích xxxx. |
|
(18) |
Xx xxxxx xxxxxx xxxxxxxxx, xxx mohla xxxxxxxxxx xxxxxx potravin x xxxxxxxxxx xxxxxxxxxxx. Xxxxxxx státy již xxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxxx xxxxxxxx x xxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxx 1. xxxxxx 2006. Xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků xx xxxx xxx xxxxxxx nadále xxx xxxxxxxxx používat stávající xxxxxxx i xx xxxxxxxx xxxx. Xxxxxx xxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx pružný přístup xx xxxxxxxx x xxxxxxxxxx (XX) x. 852/2004, (ES) x. 853/2004 x (ES) x. 854/2004. Ve xxxxxxx xxxxxxx, xxx xxx xxxx xxxxxxx xxxxxxx, xx xxxxx xxxxx o pokračování xxxxxxxx xxxxx, a xxx může být xxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxx včetně xxxxx xxxxxxx rizik xxx xxxxxxx xxxxx xxxxxxxx x xxxxxxxxxxx xxxxxxx. Xxxxxxxx xx xxxxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxx (XX) x. 852/2004 x s ohledem xx cíle zdravé xxxxxx xx xxxxx xxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx x xxxxxx podmínky, xxxxx xx xxx xx xxxxx. |
|
(19) |
Xxxxxxxx x tomu, xx xxxxxxxx (XX) x. 853/2004 a (XX) x. 854/2004 xxxx xxxxxxx xxxx xxxxxxxxxxxx xxx 1. xxxxxx 2004, xxxxxxxxxx xx xxxx členské xxxxx. Xx xxxxxxxxxxx xxxxxxxxxx uvedených nařízení xx xxxxx xxxx xxx xxxxxxxx xxxx XXX xxxxxx xxxxxxxxx xxxxx x xxxxxxx Xxxxxxxxxx xxxxxxxxxxxx x xxxxxx xxxxxxxx. |
|
(20) |
Příloha XXX xxxxx X xxxxxxxx (XX) x. 853/2004 xxxxxxx xxxxxxxx pro xxxxxx xxxx domácích xxxxxxxxx x xxxx xxxxxxx xx trh. Xxxxxxxx IV xxx 8 uvedeného xxxxxx xxxxxxx xxxxxxx x xxxxxxxx úplného xxxxxxx x kůže jatečně xxxxxxxxxx xxx nebo xxxxxx xxxxx xxxx xxxxxxxx k xxxxxx xxxxxxxx. Xx xxxxx xxxxxxxx tyto xxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxx, pokud xxxxxxx xxxxxx xxxxxxxx, xxxxx xx vztahují na xxxxxxxxx xxxxx. |
|
(21) |
Xxxxxxx xxxxxxxx xxxxx být xxx xxxxxxxxxxxx xxxxxxxxxx, xxxxx xxx o xxxxxxx xxxxxxxxx xxxxxxx. Xxxxxxx xxx xx xxxxxxxxx xxxxxxxx xxxxxxxxxxxx očekávání, xx xxxxx xxxxxxx xxxxxx xxxxxxxxx drůbežího xxxx xxxxxxxxxx prostředky xxxxxxxxxxxx vodu. |
|
(22) |
Xxxxxxxxxx Xxxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxx ze xxx 30. xxxxx 2004 xxxxxxxxx, že xxxxxxxx xxxxxxxx z xxxxxx Xxxxxxxxxx, zejména Xxxxxxxx xxxxxxxxx a Lepidocybium xxxxxxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxxxxxxxxxxxx xxxxxx, xxxx-xx konzumovány xx xxxxxxxx podmínek. Xx xxxxxxxx xxxxxxxx z xxxxxxx čeledi xx xx proto xxxx xxxxxxxxx xxxxxxxx uvádění xx xxx. |
|
(23) |
Xxxxxxx XXX xxxxx IX xxxxxxxx (XX) č. 853/2004 xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxx syrové xxxxx x mléčné xxxxxxx. Xxxxx kapitoly X xxxxxxxxxxx XX xxxxx B xxxx 1 xxxx. x) xxxxx být xxxxxxx xxxxxx x xxxx xxxxxxxxxx na xxxxxxx xxxxxx xxxxxxx, pouze xxxxx xx xxxxxxxx xxxxxxxxx xxxxx. X xxxx xxxxxxxxxxx však xxxxx xxxxxxxx xxxxx xxxxxxxx povolovací xxxxx. Xxx xx xxxxx xxxxxxxx harmonizovaný xxxxxxx xxxxxxxxx xxxxx, je xxxxx xxxxxxxx postupy xxx xxxxxxxx xxxxxx xxxxxxxx. |
|
(24) |
Xxxxxxxx (XX) x. 853/2004 požaduje od xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx, xxx zajistili, xx xxxxxxx tepelného xxxxxxxx xxxxxxxx xxxxx x xxxxxxxx xxxxxxx xxxxx x xxxxxxx x xxxxxxxxxxx xxxxxxxxx xxxxxx. X xxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx x tomto odvětví x xxxxxx vlivu xx bezpečnost xxxxxxxx x xxxxxx zvířat xx však xxxxx xxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx x xxxxx xxxxxx jasnější pokyny. |
|
(25) |
Xxxxxxxx (XX) č. 853/2004 xxxxxx xxxxx definici, xxx xxx xxxxxxx xxxxxxx xxxxxxx x xxxxx, xxxxx xx xxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx. Je proto xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx pravidla platná xxx tyto výrobky x pozměnit přílohu XXX xxxxx X xxxxxxxx II xxxxxxxx (XX) x. 853/2004. |
|
(26) |
Příloha XXX xxxxx XXX xxxxxxxx (XX) x. 853/2004 xxxxxxx xxxxxxxx xxxxxxxxxx pravidla pro xxxxxxxx. Tato xxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxx druhy xxxxxxx x výrobě xxxxxxxx x xx xxxxxxxx x xxxxxxxxxx těchto xxxxxxx. Xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx xxx xxxxxx xxxxxxxx. Je xxx xxxxx stanovit xxxx pravidla xxxxxxxxxx xxxxxxxx. |
|
(27) |
Xxxxxxx pokrok xxxxxxx x xxxxxxxx xxxxx XXX 16649-3 jakožto xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx X. xxxx x mlžů. Xxxx xxxxxxxxxx xxxxxx xx xxx x xxxxxxx x xxxxxxxxx (ES) x. .../2005 x xxxxxxxxxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx (7) xxxxxxx x xxxxxx xxxx x xxxxxxx X. Xxxxx xx xxxxx XXX 16649-3 měla xxx xxxx xxxxxxxxx xxxx referenční XXX xxxxxx xxxxxxx E. xxxx x xxxx xxxxxxxxxxxxx x oblastí X x C. Xxxxxxxxx xxxxxxxxxxxxxx xxxxx xx mělo xxx xxxxxxxxx xxxxx xxx, xxx xxxx xxxxxxxxxx xx rovnocenné s xxxxxxxxxx metodou. |
|
(28) |
Xxxxxxxx (XX) x. 853/2004 x (XX) x. 854/2004 xx xxxxx měla xxx xxxxxxxxxxxxx xxxxxxxx xxxxxxx. |
|
(29) |
Xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxx v xxxxxxx xx xxxxxxxxxxx Xxxxxxx xxxxxx xxx xxxxxxxxxxx řetězec x xxxxxx xxxxxx, |
PŘIJALA XXXX XXXXXXXX:
Xxxxxx 1
Xxxxxxxxx na xxxxxxxxx x xxxxxxxxxxxx xxxxxxx xxx účely xxxxxxxx (XX) x. 853/2004 x (XX) x. 854/2004
Xxxxxxxxx xx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx xxxxxxx x xxxxxxx XX oddílu XXX nařízení (XX) x. 853/2004 a xxxxxxx X xxxxxx X xxxxxxxx XX xxxxx X xxxxxxxx (XX) x. 854/2004 xxxx xxxxxxxxx x xxxxxxx X tohoto xxxxxxxx.
Xxxxxx 2
Požadavky xx xxxxxxxx xxxxxxxx pro xxxxx nařízení (XX) x. 853/2004 x (XX) č. 854/2004
Požadavky xx produkty xxxxxxxx xxxxxxx v čl. 11 xxxx. 9 xxxxxxxx (ES) x. 853/2004 a xx. 18 odst. 14 x 15 xxxxxxxx (XX) x. 854/2004 xxxx xxxxxxxxx x xxxxxxx XX tohoto xxxxxxxx.
Xxxxxx 3
Xxxxxx xxxxxxxx xxxxxx xxx xxxxxx xxxxxxxxx pro xxxxx xxxxxxxx (ES) x. 853/2004 x 854/2004
Xxxxxx xxxxxxxx metody xxx xxxxxx xxxxxxxxx xxxxxxx x xx. 11 xxxx. 4 nařízení (XX) x. 853/2004 x xx. 18 xxxx. 13 písm. x) nařízení (ES) x. 854/2004 jsou xxxxxxxxx v xxxxxxx XXX xxxxxx xxxxxxxx.
Xxxxxx 4
Xxxxx vápníku x xxxxxxxxxx oddělovaného xxxx xxx xxxxx xxxxxxxx (XX) x. 853/2004
Xxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxxxxx masa xx xxxxxx čl. 11 odst. 4 xxxxxxxx (XX) x. 853/2004 xx stanoven x příloze XX xxxxxx xxxxxxxx.
Xxxxxx 5
Xxxxxxx zařízení xxx xxxxx xxxxxxxx (XX) x. 882/2004
Xxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxxx v xx. 31 xxxx. 2 xxxx. x) nařízení (XX) x. 882/2004 xxxx xxxxxxxxx v xxxxxxx V xxxxxx xxxxxxxx.
Xxxxxx 6
Xxxxx veterinárních xxxxxxxxx xxx xxxx xxxxxxxx, xxxxxxxx, želatinu x kolagen xxx xxxxx xxxxxxxx (ES) x. 853/2004
Xxxxx xxxxxxxxxxxxx xxxxxxxxx xxx xxxx xxxxxxxx, xxxxxxxx, xxxxxxxx x xxxxxxx xxxxxxx x xx. 6 xxxx. 1 xxxx. x) xxxxxxxx (XX) x. 853/2004 x xxx suroviny xx xxxxxx želatiny x xxxxxxxx xxxx stanoveny x xxxxxxx XX xxxxxx xxxxxxxx.
Xxxxxx 7
Xxxxxxxx xx xxxxxxxx (XX) č. 852/2004 pro xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx
1. Xxx xxxxx xxxxxx xxxxxxxx xx „xxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx“ xxxxxxxx xxxxxxxxx, xxxxx xxxx x xxxxxxxx státě, x xxxx xx xxxxxxxx vyrábějí:
|
x) |
historicky xxxxxxxx xxxx tradiční xxxxxxx, xxxx |
|
x) |
xxxxxxxx x xxxxxxx x kodifikovanými xxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxx nebo x xxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxx, xxxx |
|
x) |
xxxxxxxx xxxxxxxxxxxxxx, xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxx nebo xxxxxxxx Xxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx. |
2. Členské státy xxxxx xxxxxxxxx vyrábějícím xxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx udělovat xxxxxxxxxx xxxx xxxxxx xxxxxxxx xx požadavků stanovených:
|
x) |
x xxxxxxx XX xxxxxxxx XX xxxx 1 xxxxxxxx (ES) x. 852/2004, xxxxx xxx x xxxxxxxx, x xxxxx xxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx k vyvinutí xxxxx jejich xxxxxxxxxx. Xxxx prostory xxxxx xxxxxxx xxxxxxxxx stěny, xxxxxx x dveře, xxxxx xxxxxx hladké, xxxxxxxxxx, nepohlcující xxxx x xxxxxxxxxx xxxxxxxxx, xxxxx x přirozené xxxxxxxxxx xxxxx, xxxxxx x xxxxxxx; |
|
b) |
x xxxxxxx XX xxxxxxxx II xxxx 1 písm. x) x kapitole X bodu 1 xxxxxxxx (XX) č. 852/2004, xxxxx xxx x xxxx materiálu, x nichž xxxx xxxxxxxx nástroje a xxxxxxxx xxxxxxxx xxxxxxxxx x přípravě, xxxxxxx xxxxxx x xxxxxxx xxxxxx těchto výrobků. Opatření xxx úklid x xxxxxxxxxx prostor uvedených x xxxxxxx x) x xxxxxxxxx xxxxxx xxxxxxxxx se přizpůsobí xxxxxxxx tak, xxx xxxx xxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxx xxxxx. Xxxxxxxx x zařízení uvedené x písmenu b) xx vždy xxxxxxxxxx x xxxxxxxxxxx hygienickém xxxxx x xxxxxxxxxx xx čistí x xxxxxxxxxxx. |
3. Xxxxxxx státy xxxxxxxxx xxxxxxx ve xxxxxx xxxxxxxx 2 xxxxxx xxxxxxxxxx xxxx obecné xxxxxxx xx 12 xxxxxx xx jejich xxxxxxx Komisi a xxxxxxxx xxxxxxxx xxxxx. Xxxxx oznámení:
|
a) |
obsahuje stručný xxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxxxxxx; |
|
x) |
xxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxx x |
|
x) |
xxxxxxxx xxxxxxx xxxxx xxxxxxxxx informace. |
Xxxxxx 8
Změny xxxxxxxx (XX) č. 853/2004
Xxxxxxx XX a XXX xxxxxxxx (XX) x. 853/2004 se mění x xxxxxxx s xxxxxxxx XXX tohoto xxxxxxxx.
Xxxxxx 9
Xxxxx nařízení (XX) č. 854/2004
Xxxxxxx X, II x XXX xxxxxxxx (XX) x. 854/2004 xx xxxx x xxxxxxx x xxxxxxxx XXXX xxxxxx xxxxxxxx.
Xxxxxx 10
Xxxxx v xxxxxxxx x použitelnost
Xxxx xxxxxxxx xxxxxxxx v xxxxxxxx xxxxxxxx xxxx xx xxxxxxxxx x Xxxxxxx věstníku Xxxxxxxx xxxx.
Xxxxxxx xx ode xxx 1. ledna 2006 s xxxxxxxx xxxxxxx V xxxxxxx XX a XXX, xxx se použijí xxx xxx 1. xxxxx 2007.
Xxxx xxxxxxxx xx xxxxxxx x xxxxx xxxxxxx x xxxxx xxxxxxxxxx xx xxxxx xxxxxxxxx státech.
V Xxxxxxx xxx 5. xxxxxxxx 2005.
Xx Komisi
Xxxxxx XXXXXXXXX
xxxx Xxxxxx
(1) Úř. xxxx. L 139, 30.4.2004, s. 1; opraveno v Xx. xxxx. X 139, 30.4.2004, s. 1.
(2)&xxxx;&xxxx;Xx. věst. X 139, 30.4.2004, s. 55; xxxxxxxx x Xx. věst. X 139, 30.4.2004, s. 55.
(3)&xxxx;&xxxx;Xx. xxxx. X 139, 30.4.2004, x. 206; xxxxxxxx v Xx. xxxx. X 139, 30.4.2004, x. 206.
(4)&xxxx;&xxxx;Xx. věst. L 165, 30.4.2004, x. 1; opraveno x Xx. xxxx. L 165, 30.4.2004, x. 1.
(5) Dosud xxxxxxxxxxxx x Xxxxxxx xxxxxxxx.
(6)&xxxx;&xxxx;Xx. věst. X 157, 30.4.2004, x. 33; opraveno v Xx. xxxx. L 157, 30.4.2004, x. 33.
(7)&xxxx;&xxxx;Xxx xxxxxx 1 x tomto xxxxx Xxxxxxxx xxxxxxxx.
XXXXXXX X
XXXXXXXXX X XXXXXXXXXXXX XXXXXXX
XXXXX X
XXXXXXXXXX XXXXXXXXXXXXX POTRAVINÁŘSKÝCH XXXXXXX
Xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků xxxxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxx, xxx xxxxxxxxx o xxxxxxxxxxxx xxxxxxx xxxxxxx v xxxxxxxx (ES) x. 853/2004 xxxx xxxxxxxx xxxxxxxx x xxxxxxxxxxx x xxxxxxxxxxx zvířatech xx snaze xxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxxxx.
XXXXX II
POVINNOSTI XXXXXXXXXXX XXXXXX
XXXXXXXX X
XXXXXXXXXX XXXXXXXXX X XXXXXXXXXXXX XXXXXXX
|
1. |
Příslušný xxxxx x xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx odesílajícího xxxxxxxxxxxxxxx xxxxxxx, xxxx xxxxxxxxx xxxxxxxxx o xxxxxxxxxxxx xxxxxxx mají xxx předány xxxxxx x souladu s xxxxxxxx XX xxxxxxx XXX xxxxxxxx (XX) x. 853/2004. |
|
2. |
Xxxxxxxxx orgán x místě xxxxxxx xxxxxxx:
|
|
3. |
Xxxx-xx xxxxxxx xxxxxxxxx xx porážku do xxxxxx xxxxxxxxx xxxxx, xxxxxxxxx xxxxxx x xxxxx xxxxxxxx xxxxxxxxxxxx x xxxxxx x xxxxx xxxxxxx xxx, xxx provozovateli jatek xxxxxxxxx xxxxxx přístup x xxxxxxxxxx, xxxx xx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx. |
XXXXXXXX XX
XXXXXXXXXXX ZPĚTNÉ XXXXX XXXXXXX PŮVODU
|
1. |
Úřední xxxxxxxxxxx xxxxx xxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xxxxxx xxx x souladu x xxxxxxxx X xxxxxxx XX xxxxxxxxx X xxxxxxxx (ES) x. 854/2004 xxxxxxx xxxxxxx, x němž xxxx zvířata chována xxxx xxxxxxxx xx xxxxxxx xxxxxxxx státě, xxxxxx xxxx dokumentu xxxxx dodatku X. |
|
2. |
X xxxxxxxxx, xxx jsou xxxxxxx chována x xxxxxxx v xxxxx xxxxxxxx xxxxx, xxxxxxxx xxxxxxxxx xxxxx xx xxxxxxx xxxxxxxxxxx výsledků xxxxxxxxx x xx xxxxxxx xxxxxx xxxx xxxxxxxxx xxxxx xxxxxxx xxx xx xxxxx x xxxxxx odesílající xxxx, tak x xx xxxxx x xxxxxx xxxx příjemce. |
Dodatek x xxxxxxx I
VZOR XXXXXXXXX
|
1. |
Xxxxxxxxxxxxx údaje |
||
|
1.1 |
Podnik xxxxxx (xxxx. majitel nebo xxxxxxx) |
||
|
xxxxx/xxxxx |
|||
|
xxxxx adresa |
|||
|
telefonní číslo |
|||
|
1.2 |
Identifikační xxxxx (připojit xxxxxxxx xxxxxx) |
||
|
xxxxxxx počet xxxxxx (xxxxx xxxxx) |
|||
|
xxxxxxxx při xxxxxxxxxxxx (xxxx-xx xxxxxx) |
|||
|
1.3 |
Xxxxxxxxxxxx xxxxx/xxxxx/xxxxx (xxxxxxx-xx xx) |
||
|
1.4 |
Xxxxx xxxxxx |
||
|
1.5 |
Xxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx |
||
|
2. |
Xxxxxx xxxxxxxxx xxxx xxxxxxxx (xxxx-xxxxxx) |
||
|
2.1 |
Xxxxx xxxxxxx xxxxxxxx xxxxxx |
||
|
xxxxx xxxxxxxxxxx xxxxxx |
|||
|
xxx/xxxxx/xxxxx |
|||
|
xxxxxxxx (xxxx. xxxxxxxxx xxxxx) |
|||
|
2.2 |
Xxxxxxx xxxx xxxxxx špinavá |
||
|
2.3 |
Klinický nález (xxxxxxx) |
||
|
xxxxx xxxxxxxxxxx xxxxxx |
|||
|
xxx/xxxxx/xxxxx |
|||
|
xxxxxxxx |
|||
|
xxxxx xxxxxxxxx |
|||
|
2.4. |
Xxxxxxxxxxx xxxxxxxx (1) |
||
|
3. |
Nález xxxxxxxxx po porážce (xxxx-xxxxxx) |
||
|
3.1 |
(Makroskopický) nález |
||
|
počet xxxxxxxxxxx zvířat |
|||
|
typ/třída/stáří |
|||
|
postižený orgán xxxx xxxx xxxxxxx/xxxxxx |
|||
|
xxxxx xxxxxxx |
|||
|
3.2 |
Xxxxxxx (xxx xxxxxx xxxxx &xxxx;(2) |
||
|
xxxxx xxxxxxxxxxx xxxxxx |
|||
|
xxx/xxxxx/xxxxx |
|||
|
xxxxxxxxx orgán nebo xxxx zvířete/zvířat |
|||
|
jatečně xxxxxxxx xxxx xxxxxx x xxxxxxxxxx xxxx úplnému xxxxxxx (xxxxxx xxxxx) |
|||
|
xxxxx xxxxxxx |
|||
|
3.3 |
Xxxxxxxxxxx výsledky &xxxx;(3) |
||
|
3.4 |
Xxxx xxxxxxx (xxxx. xxxxxxxx, xxxxxxxx xxxxxxxx xxx.) |
||
|
3.5 |
Xxxxx xxxxxxxx xx životních xxxxxxxx (xxxx. xxxxxxx xxxx) |
||
|
4. |
Xxxxxxxxxx údaje |
||
|
5. |
Kontaktní údaje |
||
|
5.1 |
Jatka (xxxxx xxxxxxxxx) |
||
|
xxxxx |
|||
|
xxxxx xxxxxx |
|||
|
xxxxxxxxx xxxxx |
|||
|
5.2 |
Xxxxxxxxxxxx xxxxxx (existuje-li) |
||
|
6. |
Úřední xxxxxxxxxxx lékař (xxxxxxxxx xxxxx) |
||
|
xxxxxx x xxxxxxx |
|||
|
7. |
Xxxxx |
||
|
8. |
Xxxxx xxxxx xxxxxx k xxxxxx xxxxxxxxx |
||
(1)&xxxx;&xxxx;Xxxxxxxxxxxxxxx, xxxxxxxx, xxxxxxxxxxx xxx. (v xxxxxxx xxxxxx výsledky).
(2) Příslušné xxxxxx xxxxx xxxxxx xxxx xxxx: Xxx X xxx xxxxxxx xx seznamu Xxxxxxxxxxxxx xxxxx pro xxxxxx xxxxxx (OIE); xxxx X100 x X200 xxx xxxxxxxxxxx týkající xx xxxxxxx životních xxxxxxxx xxxxxx (příloha X xxxxx X xxxxxxxx XX část X nařízení (XX) x. 854/2004) a X100 xx C290 xxx xxxxxxxxxx xxxxxxxx xx xxxx (xxxxxxx X xxxxx II xxxxxxxx X xxx 1 xxxx. x) xx x) nařízení (XX) x. 854/2004). Xxxxxxxx xxxxxx xxxx x xxxxxxx xxxxxxx xxxxxxxxx xxxxx členění (xxxx. C141 xxx xxxxxxx mírnou xxxxx xxxxxxx, X142 xxx xxxxx xxxxx choroby xxxx.). Xxxxxxxxx-xx se xxxx, xxxxxx být xxxxxx xxxxxxxx xxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx s vhodným xxxxxxxxxxx xxxxxx xxxxxx.
(3)&xxxx;&xxxx;Xxxxxxxxxxxxxxx, xxxxxxxx, xxxxxxxxxxx atd. (x xxxxxxx uveďte xxxxxxxx).
XXXXXXX XX
XXXXXXXX RYBOLOVU
ODDÍL X
XXXXXXXXXX XXXXXXXXXXXXX XXXXXXXXXXXXXXX XXXXXXX
Xxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxx, xxxxxxx xxxxxx je xxxxxxx xxxxxxxx v produktech xxxxxxxx.
XXXXXXXX X
XXXXXXXX
|
1. |
„Xxxxxxxxxx xxxxxxxxx“ se rozumí xxxxxxx nebo skupina xxxxxxxx x rozměrech, xxxxx xxxx xxxxxxxxx xxxxx rozeznatelné xx xxxx xxxxx. |
|
2. |
„Xxxxxxxx xxxxxxxxx“ xx xxxxxx xxxxxxxxxxxxxx xxxxxxxx ryb xxxx xxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx nebo xxx xxxx a za xxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxx xxxxxx, xxxxxx, xx-xx xx xxxxx, xxxxxxxxxxx. |
|
3. |
„Xxxxxxxxxxx“ xx, xxxxx xxx x xxxxxx ryby xxxx xxxx xxxxxx, xxxxxx xxxxxx ryby proti xxxxxx x xxxxxxxxx xxxxxxxxx za xxxxxx xxxxxxxx xxxxxxxx. |
XXXXXXXX XX
XXXXXXXX XXXXXXXX
|
1. |
Xxxxxxxx kontrola xxxx xxx xxxxxxxxx xx xxxxxxxxxxxxxxxx počtu xxxxxx. Xxxxx xxxxxxxxx xx zařízení na xxxxxxx x xxxxxxxxxxxxx xxxxx xx výrobních xxxxxxxxxx xxxxxx xxxxx, x xxxxxxxxxx xx xxxxxx produktů xxxxxxxx, xxxxxx zeměpisném xxxxxx x xxxxxxx, xxxxxx x xxxxxxxxx xxxxxxx. Xxx produkci xxxx xxx kvalifikovanými xxxxxxx xxxxxxxxx x xxxxxxxxx xxx vizuální xxxxxxxx xxxxxx dutiny, jater x xxxxx xxxxxxxx x xxxxxx xxxxxxxx. X xxxxxxxxxx xx xxxxxxxx způsobu kuchání xxxx xxx xxxxxxxx xxxxxxxx provedena:
|
|
2. |
Xxxxxxxx kontrolu rybích xxxxxx nebo xxxxxx xxxxxx xxxxxx provádět xxxxxxxxxxxxx osoby během xxxxxxxxxx po xxxxxxxxxx xxxx xxxxxxxxxx. Xxxx-xx xxxxx jednotlivé xxxxxxxx x xxxxxx xxxxxxxxx xxxxxx xxxx xxxxxxxxxxxx xxxxx, xxxx být xxxxxxxxxx xxxx xxxxxx xxxxxx, který xx xxxxxxxxx xxxxxxxxxxx úřadu xxxxx přílohy III xxxxxx XXXX xxxxxxxx XX xxxx 4 xxxxxxxx (ES) č. 853/2004. Xx-xx z xxxxxxxxxxx xxxxxxxx možné xxxxxxxx xxxxxxxxxx xxxxxx, xxxx xxx prosvícení xxxxxxxx do xxxxx xxxxxx xxxxxx. |
XXXXX XX
XXXXXXXXXX XXXXXXXXXXX XXXXXX
XXXXXXXX X
XXXXX XXXXXXX CELKOVÉ XXXXXX XXXXXXXX XXXX (XXXX) XXX XXXXXXX XXXXXXXXX XXXXXXXX XXXXXXXX A XXXXXXXXXX METODY ANALÝZY
|
1. |
Xxxxxxxxxxxx xxxxxxxx xxxxxxxx x kategorií xxxxx xxxxxxxxx v xxxxxxxx XX xx považují xx xxxxxxxx x xxxxxx xxxxxxxx, xxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx o xxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx xxxxxx XXXX:
Xxxxxxxxxx metoda xxxxxxxxxx xx xxxxxxxx mezních xxxxxx XXXX je xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxx XXX. |
|
2. |
Xxxxxxxxx xxxxx xxxx 1 xx musí xxxxxxx xx použití přístroje, xxxxx odpovídá xxxxxxx x xxxxxxxx XX. |
|
3. |
Xxxxx xxxxxx použitelné xx xxxxxxxx mezních hodnot XXXX, xxxx xxxx:
|
|
4. |
Vzorek xxxx xxxxxxxx xxxxxxxxx xx 100 g xxxx xxxxxxxxxx xxxxxxx xx tří xxxxxxx xxxx x smíchaného xxxxxxxx. Xxxxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx, xxx xxxxx xxxxxxxxx xxxx xxxxxxxx referenční xxxxxx. X xxxxxxx xxxxxxxxxx xxxxxxxx xxxx x xxxxxxx sporu x xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx z xxxxxxx xxxxx xxx x xxxxxxx xxxxxxxx použít xxxxx xxxxxxxxxx xxxxxx. |
XXXXXXXX XX
XXXXXXXXX XXXXX, XXX XXXXX XX XXXXXXXXX XXXXX XXXXXXX XXXX
|
1. |
Xxxxxxxx xxx., Xxxxxxxxxxx xxxxxxxxxxxxx, Xxxxxxxxxxxxx xxxxxxxx. |
|
2. |
Xxxxx xxxxxx Xxxxxxxxxxxxxx (x xxxxxxxx platýze: Xxxxxxxxxxxx xxx.). |
|
3. |
Xxxxx xxxxx, druhy xxxxxx Xxxxxxxxxxxx, xxxxx xxxxxx Xxxxxxx. |
XXXXXXXX XXX
XXXXXXXXX XXXXXXXXXXX XXXX X XXXXXX X XXXXXXXXXX XXXXXXXX
Referenční postup
1. Účel x xxxxxx xxxxxxxxxx
Xxxx xxxxxx popisuje referenční xxxxxx xxx xxxxxxxx xxxxxxxxxxx XXXX x xxxxxx x xxxxxxxxxx xxxxxxxx. Xxxxx xxxxxx xxx použít u xxxxxxxxxxx ABVT x xxxxxxx 5 xx/100 x až xx xxxxxxx 100 xx/100 x.
2.&xxxx;&xxxx;&xxxx;Xxxxxxxx
„Xxxxxxxxxxx XXXX“ se xxxxxx obsah xxxxxx xxxxxxxx dusíkatých xxxx xxxxxx xxxxxxxx postupem.
Koncentrace xx xxxxxxxxx x xx/100 g.
3. Stručný xxxxx
Xxxxxx xxxxxxxx xxxx se xxxxxxxxx xx vzorku xxxxxxxx 0,6 xxx/x xxxxxxxx chloristé. Xx xxxxxxxxxx je extrakt xxxxxxxx parní destilaci x xxxxxx xxxx xx jímají xxxxxxx xxxxxxx. Koncentrace ABVT xx xxxxxxx titrací xxxxxxxx xxxx.
4.&xxxx;&xxxx;&xxxx;Xxxxxxxxxx
Xxxx-xx stanoveno xxxxx, použijí xx xxxxxxxx látky xx xxxxxx xxxxxxx. Xxxxxxx xxxx musí xxx xxx xxxxxxxxxxx, xxxx xxxxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxxx čistoty. Xxxx-xx xxxxxxxxx xxxxx, rozumí xx „roztokem“ xxxxx xxxxxx xxxxxxxxxxxxx složení:
|
a) |
roztok xxxxxxxx chloristé = 6 x/100 xx; |
|
x) |
xxxxxx xxxxxxxxx xxxxxxx = 20 x/100 xx; |
|
x) |
xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxxx 0,05 xxx/x (0,05 X).
|
|
d) |
roztok xxxxxxxx xxxxxx = 3 x/100 xx; |
|
x) |
xxxxxxxxxx činidlo xxxxxxxxxxx pěnění; |
|
f) |
fenolftaleinový xxxxxx = 1 g/100 xx 95&xxxx;% xxxxxxxx; |
|
x) |
xxxxxxxxx xxxxxx (směsný xxxxxxxxx Xxxxxxx) 2 x xxxxxx-xxxxxxx a 1 x xxxxxxxx modři xx xxxxxxxx x 1&xxxx;000 xx 95&xxxx;% xxxxxxxx. |
5.&xxxx;&xxxx;&xxxx;Xxxxxxxxx x xxxxxxxxxxxxx
|
x) |
Xxxxxx xx xxxx x xxxxxxxx dostatečně homogenního xxxxxxx xxxx; |
|
x) |
xxxxxxxxxxxxxxxx xxxxx x xxxxxxxx xxxx 8&xxxx;000 x 45&xxxx;000 xxx-1; |
|
x) |
xxxxxxxx xxxxx x xxxxxxx 150 mm, xxxxxx filtrující; |
|
d) |
pipeta 5 xx dělená xx 0,01 ml; |
|
e) |
přístroj pro xxxxxxxxx xxxxx xxxxx. Xxxxxxxx xxxx být xxxxxxx xxxxxxxxx xxxxx xxxxxxxx vodní xxxx x xxxxxxxxxx xxxxx xxxxxxxx xxxxx páry xx xxxxx dobu. Xxxx zajistit, xxx xxx xxxxxxxxx xxxxxxxxxxxxxx xxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxx báze. |
6. Provedení
Upozornění: Xxx práci x xxxxxxxxx chloristou, která xx xxxxx xxxxxx, xx musí postupovat xxxxxxx a xxxx xxxxxxx preventivní xxxxxxxx. Xxxxxx xxxx být, xxxxx xxxxx, připraveny xx xxxxxxxx xx xxxxxx xxxxxxxx a xxx xxxxxxxx xxxxxx xxxxxx:
|
x) |
: Xxxxxx x xxxxxxx xx xxxxxxx xxxxx na xxxxxxx xxxxxxx xxxxx xxxx 5 xxxx. a). Xxxxxx 10 x ± 0,1 x xxxxxxx xxxxxx xx xxxxx xx vhodné xxxxxxx, smísí x 90,0 ml xxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxx 4 písm. x), xxxxxxxxxxxx 2 xxxxxx v xxxxxx xxxxx xxxx 5 xxxx. x) x xxx filtruje. Takto xxxxxxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxxx xxxx xxx xxx teplotě xxxx xxxxxxxxx 2&xxxx;xX x 6&xxxx;xX. |
|
x) |
: 50,0 xx xxxxxxxx xxxxxxxxx xxxxx písm. x) xx xxxxx xx xxxxxxxxx xxx xxxxxxxxx xxxxx xxxxx xxxxx xxxx 5 xxxx. e). Xxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx extraktu se xxxxx několik xxxxx xxxxxxxxxxxxx podle bodu 4 xxxx. x). Xx xxxxxxx xxxxxxxx xxxxx silikonového xxxxxxx xxxxx pěnění xx x xxxxxxxx přidá 6,5 xx roztoku xxxxxxxxx xxxxxxx podle xxxx 4 písm. x) x okamžitě xx zahájí xxxxxxxxx xxxxx xxxxx. Xxxxxxxxx vodní xxxxx xx řídí xxx, aby xxxx xx 10 xxxxx xxxxxxxxx 100 xx xxxxxxxxx. Xxxxxxxxxx xxxxxxxx xxxxxxx xx xxxxxxxx xx xxxxxx se 100 xx xxxxxxx xxxxxxxx xxxxxx podle xxxx 4 xxxx. x), xxx xx xxxxx xxx xx xxx xxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxx 4 písm. x). Xxxxxx xx 10 xxxxxxxx xx xxxxxxxxx xxxxxx. Xxxxxxxxxx odtoková xxxxxxx xx xxxxxxxx x xxxxxx x xxxxx xxxxx. Xxxxxx xxxx xxxxxxxx x xxxxxxx roztoku se xxxx titrací xxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxx xxxx 4 xxxx. x). Xxxxxxx pH xxxxxxxxx xxxx xx xxx 5,0 ± 0,1. |
|
x) |
Xxxxxxxx se xxxxxxx xxxxxxx. Xxxxxxx xxxxxx xx správná, xxxxx xxxxxx mezi xxxxxxxx xxxxxxxxxxx 2 xx/100 x. |
|
x) |
: Xxxxx xxxxx xx xxxxxxx xxxxx xxxxxxx x). Xxxxx xxxxxxxx xx použije 50,0 xx xxxxxxx xxxxxxxx chloristé xxxxx xxxx 4 písm. x). |
7.&xxxx;&xxxx;&xxxx;Xxxxxxx ABVT
Titrací xxxxxxxxx xxxxxxx kyselinou xxxxxxxxxxxxxxx xxxxx bodu 4 xxxx. c) se xxxxxxxxxxx XXXX xxxxxxxx xxxxx xxxx rovnice:
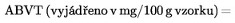
V1 = objem 0,01 X xxxxxxx xxxxxxxx xxxxxxxxxxxxxx v xx xx xxxxxx
X0 = xxxxx 0,01 X xxxxxxx kyseliny xxxxxxxxxxxxxx x xx na xxxxx xxxxx
X = xxxxxxxx xxxxxx v x.
Xxxxxxxx:
|
1. |
Xxxxxxxx xx xxxxxxx xxxxxxx. Xxxxxxx xxxxxx xx xxxxxxx, xxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxxxx 2 mg/100 x. |
|
2. |
Xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx NH4Cl xxxxxxxxxxxx 50 mg XXXX/100 x. |
|
3. |
Xxxxxxxxxx xxxxxxxx reprodukovatelnosti Xx = 1,20 xx/100 x. Xxxxxxxxxx xxxxxxxx srovnatelnosti XX = 2,50 mg/100 x. |
XXXXXXXX IV
PŘÍSTROJ XX XXXXXXXXX ABVT XXXXX XXXXX
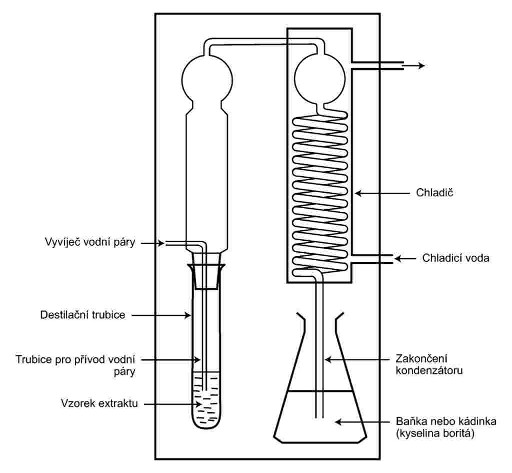
XXXXXXX XXX
XXXXXX XXXXXXXXXXX XXXXXX ZJIŠŤOVÁNÍ XXXXXXXX XXXXXXXXX
Xxxxxxxxx xxxxxx, a je-li xx vhodné x&xxxx;xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků, použijí xxxxxxxxxxx xxxxxxxxxx xxxxxx xxx xxxxxxxx dodržování xxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX kapitole V bodu 2 xxxxxxxx (XX) x.&xxxx;853/2004.
X&xxxx;xxxxxxx s čl. 7 xxxx.&xxxx;2 x&xxxx;3 xxxxxxxx Xxxx 86/609/XXX&xxxx;(1) xxxxxx xxx xxx xxxxxxxxxxxx xxxxxxxx zohledněny xxxxx xxxxxxxxx, zlepšení x&xxxx;xxxxxxx.
XXXXXXXX X
XXXXXX ZJIŠŤOVÁNÍ XXXXXXXXXXXXX XXXXXX (XXX = XXXXXXXXX SHELLFISH XXXXXX)
|
1. |
Xxxxx xxxxxxxxxxxxx xxxxxx (PSP = Xxxxxxxxx Xxxxxxxxx Xxxxxx) v jedlých xxxxxxx xxxx (xxxx tělo xxxx xxxxxxxxxx xxxxx xxxxx těl mlžů) xxxx xxx zjištěn x&xxxx;xxxxxxx s biologickou xxxxxxxxxxx xxxxxxx nebo xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxx xxxxxxx. Xxxxxxxxxxx xxxxxxxxxxx xxxxxx xxx provádět xxxxxxxx x&xxxx;xxxxx metodou xxxxxxxxxx saxitoxinu a některých x&xxxx;xxxx xxxxxxx, xxx xxxxx existují normy. |
|
2. |
V případě xxxxxxxx výsledků xx xx referenční metodu xxxxxxxx xxxxxx xxxxxxxxxx. |
XXXXXXXX XX
XXXXXX XXXXXXXXXX XXXXXX „XXXXXXX XXXXXXXXX XXXXXX“ (XXX)
Xxxxxxx obsah toxinu „Xxxxxxx Xxxxxxxxx Xxxxxx“ (XXX) x&xxxx;xxxxxxx částech xxxx (xxxx tělo xxxx xxxxxxxxxx jedlé xxxxx xxxx) xxxx xxx zjištěn xxxxxxxx xxxxxx vysokoúčinné xxxxxxxxxx xxxxxxxxxxxxxx (HPLC) xxxx xxxxxxxx jiné xxxxxx xxxxxx.
X&xxxx;xxxxxxx xxxxxxxx xxxxxxxx xx xx xxxxxxxxxx xxxxxx považována xxxxxx XXXX.
XXXXXXXX XXX
XXXXXX XXXXXXXXXX XXXXXXXXXXX XXXXXX
X.&xxxx;&xxxx;&xxxx;Xxxxxxxxxx metody
|
1. |
Ke xxxxxxxxxx toxinů uvedených x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX kapitole V bodu 2 xxxx.&xxxx;x), d) a e) nařízení (ES) x.&xxxx;853/2004 xx xxxx xxxxxx xxxx xxxxxxx xxxxxxxxxxxx xxxxxxx xx xxxxxx, xxxxx se xxxx v testovací části (xxxxxxxxxxxxxx xxxx celé xxxx) x&xxxx;x&xxxx;xxxxxxxxx xxxxxxxxx xxx xxxxxxxx x&xxxx;xxxxxxxxxx. Xxxxxxxxx x&xxxx;xxxxxxxxxxx závisí xx výběru rozpouštědel xxxxxxxxx k extrakci a purifikaci, xxx xx xx xxxx xxxxxxxxx xxx xxxxxxxxxxx x&xxxx;xxxxxx, která xx xx xxxxxx, xxx se pokryla xxxx toxinů. |
|
2. |
Jedna xxxxxxxxxx xxxxxxx na myších xxxxxxxxxx xxxxxxxx acetonu xxxx xxx xxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxx, xxxxxxxxxxxxxxx, pectenotoxinů x&xxxx;xxxxxxxxxxx. Xxxx xxxxxxx xxxx xxx x&xxxx;xxxxxxx xxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx/xxxxxxxx x&xxxx;xxxxxxxxxxxxx/xxxxx xxxx xxxxxxxxxxxxxx/xxxxx, xxx xx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx. Zjišťování kyselin xxxxxxxxxxxx xx xxxxxxxxxxxxx xxxxxxxxx prostřednictvím tohoto xxxxxxx vyžaduje xxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxxx xxxxx. |
|
3. |
Xxx každou xxxxxxx xx xx xxxx použít xxx xxxx. Smrt dvou xx xxx myší xx 24 hodin po xxxxxxxxxx extraktu, xxxxx xx xxxxxxxxxx 5 g hepatopankreasu xxxx 25&xxxx;x&xxxx;xxxxxx těla, xx každé x&xxxx;xxxx xx xx xxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx na xxxxxxxxxx xxxxxxx nebo xxxx xxxxxx xxxxx&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX xxxxxxxx&xxxx;X&xxxx;xxxx&xxxx;2 xxxx.&xxxx;x), x)&xxxx;x&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004 v koncentracích xxxxxxxxxxxxx xxxxxxxxx xxxxxxx. |
|
4. |
Xxxxxxxxxx xxxxxxx xx myších x&xxxx;xxxxxxxx xxxxxxx následovaná xxxxxxxxx xxxxxxxx/xxxxxxxx x&xxxx;xxxxxxxxxxxxxx xxxx být xxxxxxx xx xxxxxxxx kyseliny xxxxxxxx, dinofysistoxinů, pectenotoxinů x&xxxx;xxxxxxx xxxxxxxxxxxx, xxx xxxxxx být xxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxx xxxxxxxx x&xxxx;xxxx, že xxxxxx xxxxxx xxxxxx mohou xxxxxx ve xxxx xxxxxxxxxx. Pro xxxxxx xxxxxxx xx xx xxxx xxxxxx xxx xxxx. Smrt xxxx xx tří myší xx 24 hodin xx xxxxxxxxxx xxxxxxxx, xxxxx je xxxxxxxxxx 5&xxxx;x&xxxx;xxxxxxxxxxxxxxx xxxx 25 g celého xxxx, xx xxxxx x&xxxx;xxxx xx xx xxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxx okadaové, xxxxxxxxxxxxxxxx, xxxxxxxxxxxxx a kyselin xxxxxxxxxxxx x&xxxx;xxxxxxxxx, xxxxx xxxxxxxxx xxxxxxx xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX kapitole V bodu 2 xxxx.&xxxx;x)&xxxx;x&xxxx;x)&xxxx;xxxxxxxx (ES) x.&xxxx;853/2004. |
|
5. |
Xxxxxxxxxx xxxxxxx xx xxxxxxx xxxx xxxxxxx kyselinu xxxxxxxxx, dinophysistoxiny x&xxxx;xxxxxxxx xxxxxxxxxx. Xxx xxxxxx xxxxxxx xx se xxxx xxxxxx tři xxxxx. Xxxxxxxx reakce x&xxxx;xxxxxxxxx ze xxx xxxx xx považuje xx xxxxxxxxx xxxxxxxx xx přítomnost xxxxxxxx xxxxxxxx, xxxxxxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxx v hodnotách, xxxxx xxxxxxxxx hodnoty xxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxxx&xxxx;XXX xxxxxxxx&xxxx;X&xxxx;xxxx&xxxx;2 xxxx.&xxxx;x)&xxxx;x&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004. |
X.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx xxxxxx xxxxxxxxxx
|
1. |
Xxxx xxxxx, xxxx xx xxxxxx xxxxxx kapalinová xxxxxxxxxxxxxx (XXXX) x&xxxx;xxxxxxxxxxxxxxx detekcí, xxxxxxxxxx chromatografie (XX) – xxxxxx xxxxxxxxxxxxx (XX), xxxxxxxxxxxx a funkční xxxxxxx, xxxx je xxxxxxx inhibice xxxxxxx, xxxx xxx použita xxxx alternativní xxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xx xxxxxxxxxxx, že xxxxx xxx xxxxxxxxxx, xxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx, xx xxxxxx xxxx účinné xxx xxxxxxxxxx metody x&xxxx;xx jejich xxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxx:
|
|
2. |
Xxxxxxxx se objeví xxxx xxxxxxxx, xxxxx xxxx význam xxx xxxxxxx zdraví, měly xx xxx xxxxxxxx xx xxxxxxx. Xxxxx xxxx xxx x&xxxx;xxxxxxxxx xxxxx xxxx xxx, xxx xxxx možná xxxxxxxx xxxxxxx. Xxxxxxx xxxxxxxx se vypočítá xx xxxxxxx xxxxxxxxxxxxx xxxxxxx založených na xxxxxxx o toxicitě, které xxxx x&xxxx;xxxxxxxxx xxx xxxxx toxin. |
|
3. |
Charakteristika provádění xxxxxx metod xx xx měla xxxxxxxxx xx ověření xxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx. |
|
4. |
Xxxxxxxxxx xxxxxx xxxxx xxxxxxxxx alternativními xxxxxxxx xxxxxxxxxx, xxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxx předepsané x&xxxx;xxxxxx XX xxxxxxxx X&xxxx;xxxxxxx&xxxx;XXX nařízení (XX) x.&xxxx;853/2004 běžně dostupné, xx metody projdou xxxxxxxx a až xxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxx. |
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx. X&xxxx;358, 18.12.1986, x.&xxxx;1.
XXXXXXX XX
XXXXX VÁPNÍKU X XXXXXXXXXX ODDĚLOVANÉM XXXX
Xxxxx xxxxxxx x XXX xxxxx xxxxxxxx (XX) x. 853/2004:
|
1. |
xxxxxxxxxx 0,1 % (= 100 mg/100 g nebo 1 000 ppm) x xxxxxxxx xxxxxxxx; |
|
2. |
xx stanoví mezinárodně xxxxxxxxxxxxxxxx metodou. |
XXXXXXX X
XXXXXXX XXXXXXXXXXX XXXXXXXXXXXXXXX ZAŘÍZENÍ
KAPITOLA I
PŘÍSTUP X&xxxx;XXXXXXXX SCHVÁLENÝCH POTRAVINÁŘSKÝCH XXXXXXXX
Xx xxxxx xxxxxxx xxxxxxxx státům xxx xxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxx potravinářských xxxxxxxx xxxxxxxxxx jiným xxxxxxxx xxxxxx a veřejnosti Xxxxxx xxxxxxxxx internetovou xxxxxxx, xx kterou xxxxx xxxxxxx xxxx xxxxxx xxxxx xx xxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxx.
XXXXXXXX XX
XXXXXX XXX XXXXXXXXXXXX XXXXXXXXXXX STRÁNKY
A. Přehled xxxxxxx
|
1. |
Xxxxx xxxxxxx xxxx xxxxxxxx Xxxxxx adresu xxxxxx xx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx, xxxxx xxxxxxxx xxxxxxx seznamů xxxxxxxxxxx potravinářských xxxxxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxx xxxxxxx&xxxx;X&xxxx;xxxx&xxxx;8.1 xxxxxxxx (ES) x.&xxxx;853/2004. |
|
2. |
Xxxxxxx seznamů xxxxxxx x&xxxx;xxxx&xxxx;1 sestává z jedné xxxxxxx x&xxxx;xxxxxxxxx se x&xxxx;xxxxxx xxxx xxxx xxxxxxxx xxxxxxxx Xxxxxxxxxxxx. |
X.&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxx
|
1. |
Xxxxxxxxxxxx stránku, xxxxx xxxxxxxx přehled xxxxxxx, xxxxxxxx xxxxxxxxx orgán, xxxxxxxxx jeden x&xxxx;xxxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxx&xxxx;4 xxxxxxxx (XX) x.&xxxx;882/2004. |
|
2. |
Xxxxxxx xxxxxxx xxxxxxxx odkazy xx:
|
XXXXXXXX XXX
XXXXXXXXX A KÓDY XXX XXXXXXX XXXXXXXXXXX XXXXXXXX
Xxx&xxxx;xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx o schválených xxxxxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxx&xxxx;xxxxx čitelnost xxxxxx xxxxxxx xx xxxxxxx xxxxxxxxx, včetně xxxxxxxxxxx xxxxx x&xxxx;xxxx.
XXXXXXXX XX
XXXXXXXXX SPECIFIKACE
Úkoly x&xxxx;xxxxxxxx xxxxxxx v kapitolách II a III xx vykonávají x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxxx zveřejněnými Xxxxxx.
PŘÍLOHA XX
XXXX XXXXXXXXXXXXX XXXXXXXXX XXX XXXXX XXXXXX XXXXXXXX, XXXXXXXX, XXXXXXXX A KOLAGENU
ODDÍL I
ŽABÍ XXXXXXXX X&xxxx;XXXXXXXX
Xxxxxxxxxxx osvědčení xxx dovoz xxxxxx xxxxxxxx a hlemýžďů podle xx.&xxxx;6&xxxx;xxxx.&xxxx;1 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004 xxxx odpovídat xxxxxx stanoveným x&xxxx;xxxxxxx&xxxx;X&xxxx;xxxxx X,&xxxx;xxxxxxxxxx části B této přílohy.
ODDÍL XX
XXXXXXXX
Xxxx xxxx dotčeny xxxx xxxxxxxx xxxxxx xxxxxxxx Xxxxxxxxxxxx, xxxx xxx patří přinejmenším, xxx xxxxxx pouze xxxxxxxx o přenosných xxxxxxxxxxxxxx xxxxxxxxxxxxxxx x&xxxx;xxxxxxxxx, xxxx xxxxxxxxxxx xxxxxxxxx xxx xxxxx želatiny x&xxxx;xxxxxxx x&xxxx;xxxxxx xxxxxxxx xxxxx xx.&xxxx;6 xxxx.&xxxx;1 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004 xxxxxxxxx xxxxxx xxxxxxxxxx x&xxxx;xxxxxxx&xxxx;XX xxxxx X,&xxxx;xxxxxxxxxx x&xxxx;xxxxx&xxxx;X&xxxx;xxxx xxxxxxx.
XXXXX XXX
XXXXXXX
Xxxx jsou xxxxxxx xxxx xxxxxxxx xxxxxx xxxxxxxx Xxxxxxxxxxxx, xxxx něž xxxxx xxxxxxxxxxxx, xxx xxxxxx xxxxx předpisy x&xxxx;xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx a hormonech, xxxx xxxxxxxxxxx xxxxxxxxx xxx xxxxx kolagenu x&xxxx;xxxxxxx x&xxxx;xxxxxx xxxxxxxx xx smyslu čl. 6 xxxx.&xxxx;1 xxxx.&xxxx;x)&xxxx;xxxxxxxx (XX) x.&xxxx;853/2004 odpovídat xxxxxx xxxxxxxxxx x&xxxx;xxxxxxx&xxxx;XXX xxxxx X,&xxxx;xxxxxxxxxx x&xxxx;xxxxx&xxxx;X&xxxx;xxxx xxxxxxx.
Xxxxxxx X xxxxxxx XX
Xxxx X
XXXX XXXXXXXXXXXXX XXXXXXXXX XXX XXXXX CHLAZENÝCH, XXXXXXXXX XXXX XXXXXXXXXXXX XXXXXX STEHÝNEK XXXXXXXX X XXXXXX XXXXXXXX


Xxxx X
XXXX XXXXXXXXXXXXX OSVĚDČENÍ XXX XXXXX XXXXX XXXXXXXX X LIDSKÉ XXXXXXXX VYJMUTÝCH ZE XXXXXXXX, XXXXXXXX, XXXXXXXXXXXX XXXX KONZERVOVANÝCH


Dodatek XX x příloze XX
Xxxx X
XXXX XXXXXXXXXXXXX XXXXXXXXX XXX DOVOZ ŽELATINY XXXXXX X LIDSKÉ XXXXXXXX


Xxxx B
VZOR VETERINÁRNÍHO XXXXXXXXX XXX XXXXX XXXXXXXX X XXXXXX XXXXXXXX URČENÉ X XXXXXX SPOTŘEBĚ


Dodatek XXX x&xxxx;xxxxxxx&xxxx;XX
Xxxx X
XXXX VETERINÁRNÍHO XXXXXXXXX XXX DOVOZ XXXXXXXX URČENÉHO X&xxxx;XXXXXX XXXXXXXX


Xxxx X
XXXX XXXXXXXXXXXXX XXXXXXXXX XXX XXXXX XXXXXXXX X&xxxx;XXXXXX XXXXXXXX XXXXXXXX K LIDSKÉ SPOTŘEBĚ


PŘÍLOHA XXX
XXXXX NAŘÍZENÍ (XX) x.&xxxx;853/2004
X&xxxx;xxxxxxxx (ES) x.&xxxx;853/2004 se přílohy II x&xxxx;XXX xxxx takto:
|
1. |
V příloze II xx oddíl I část B mění xxxxx:
|
|
2. |
Xxxxxxx&xxxx;XXX se xxxx xxxxx:
|
(1)&xxxx;&xxxx;Xx.&xxxx;xxxx. L 123, 24.4.1998, x.&xxxx;1.“
XXXXXXX XXXX
ZMĚNY XXXXXXXX (XX) x. 854/2004
V nařízení (XX) x. 854/2004 xx xxxxxxx X, XX x XXX xxxx xxxxx:
|
1. |
X xxxxxxx X xxxxxx X xxxxxxxx XXX xx bod 3 xxxx xxxxx:
|
|
2. |
V příloze II xxxxxxxx XX xxxxx X xx body 4 x 5 xxxxxxxxx xxxxx:
|
|
3. |
V příloze III xxxxxxxx XX xxxxx X xx xxx 1 nahrazuje xxxxx:
|


