XXXXXXXXX XXXXXXXX XXXXXX (XX) 2019/627
xx xxx 15. března 2019,
xxxxxx xx xxxxxxx xxxxxxxx xxxxxxxxx opatření xxx xxxxxxxxx úředních kontrol xxxxxxxx živočišného xxxxxx xxxxxxxx k lidské spotřebě x xxxxxxx s nařízením Xxxxxxxxxx xxxxxxxxxx a Rady (EU) 2017/625 a kterým se xxxx nařízení Komise (XX) x. 2074/2005, pokud xxx o úřední xxxxxxxx
(Text x významem pro XXX)
XXXXXXXX KOMISE,
x xxxxxxx na Xxxxxxx x xxxxxxxxx Xxxxxxxx xxxx,
x xxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) 2017/625 xx xxx 15. xxxxxx 2017 x xxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxx x xxxxx xxxxxxxx uplatňování xxxxxxxxxxxxx x xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxx se xxxxxx xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx zvířat, xxxxxx xxxxxxx a přípravků na xxxxxxx xxxxxxx, x xxxxx xxxxxxxx Xxxxxxxxxx parlamentu x Xxxx (XX) č. 999/2001, (XX) č. 396/2005, (XX) x. 1069/2009, (XX) č. 1107/2009, (XX) č. 1151/2012, (XX) x. 652/2014, (XX) 2016/429 x (XX) 2016/2031, xxxxxxxx Xxxx (XX) č. 1/2005 x (XX) x. 1099/2009 a směrnic Xxxx 98/58/ES, 1999/74/XX, 2007/43/XX, 2008/119/ES x 2008/120/XX x x xxxxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady (ES) x. 854/2004 x (XX) x. 882/2004, xxxxxxx Rady 89/608/XXX, 89/662/XXX, 90/425/XXX, 91/496/EHS, 96/23/XX, 96/93/XX x 97/78/XX x xxxxxxxxxx Xxxx 92/438/XXX (xxxxxxxx x xxxxxxxx xxxxxxxxxx) (1), x xxxxxxx xx čl. 18 xxxx. 8 xxxxxxxxx nařízení,
xxxxxxxx x xxxxx xxxxxxx:
|
(1) |
Xxxxxxxx (XX) 2017/625 xxxxxxx pravidla xxx úřední xxxxxxxx x xxxx úřední xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxx xx xxxxx fázích xxxxxxxx, xxxxxxxxxx x xxxxxxxxxx za xxxxxx xxxxxxx souladu x xxxxxxxx předpisy Unie xxxx xxxx x xxxxxxx xxxxxxxxxxx xxxxxxxx. Xxxxxxx xxxxxxx úřední xxxxxxxx xxxxxxxx se xxxxxxxx xxxxxxxxxxx původu xxxxxxxx x xxxxxx xxxxxxxx. Kromě xxxx xxxxxxx xxxxxxxx xxxxxxx x xxxxxxx xx 14. xxxxxxxx 2019 nařízení (ES) x. 854/2004 (2). Xxxxxxx xxxxxxxx x xxxxxxxxxxx stanoví xxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxx živočišného xxxxxx xxxxxxxx x xxxxxx xxxxxxxx, xxxxxx xxxxxxxxx xx xxxxxxxx xxxxxxxxx xxxxxxxx pro xxxxxxxxx xxxxxx xxxxxxx. |
|
(2) |
Pravidla xxxxxxxxx x xxxxx xxxxxxxx xx xxxx xxxxxxxx xxxxxxxxx xxxxxx požadavků, xxx xxxx zajištěno xxxxxxxxx xxxx, zda xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxxx s produkty xxxxxxxxxxx xxxxxx, zejména pravidly, xxxxx jsou xxxxxxxxx x xxxxxx předpisech:
|
|
(3) |
Xxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxx produktů xxxxxxxxxxx původu xx xxxx xxx xxxxxxxxx x xxxxxxxxx, xxx je x xxxxxx na xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxx, xxx mohou xxxxxxxx xxxxxxxxxxx původu xxxxxxxxxxxx, xxxxxxxx xxxxxx minimální xxxxxx xxxxxxxx xxxxxxx, x xxxx xx zahrnovat xxxxxxx xxxxxxx xxxxxxxx xxx xxxxxxx xxxxxxxx xxxxxx x xxxxxxxx xxxxxx x xxxxxxx životních xxxxxxxx xxxxxx. Xxxx xxxxxxxx xx xxxx xxx xxxxxxxx xx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx informacích x xxxxxxxxx xxxxxxxx xx xxxxxxxxxx Xxxxxxxxxx úřadu xxx xxxxxxxxxx xxxxxxxx (xxxx jen „úřad XXXX“). |
|
(4) |
Xxx 31. xxxxx 2011 xxxxxx xxxx EFSA xxxxxxx xxxxxxxxxx x xxxxxxxxxxx pro xxxxxx zdraví, xxxxx xxxx být xxxxxxxxxx xxx xxxxxxxxx xxxx (xxxxxx) (23). Xxxxxxxxxx z uvedeného xxxxxxxxxx xxxx xxxxxxxxxx x xxxxxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx x xxxxxxxx (ES) x. 854/2004 x xxxx xx xxx xxxxxxxxx v požadavcích xxxxxxxxxxx x xxxxx nařízení. |
|
(5) |
Xxx 23. xxxxxx 2012 xxxxxx xxxx XXXX xxxxxxx stanovisko x xxxxxxxxxxx xxx xxxxxx xxxxxx, xxxxx xxxx xxx xxxxxxxxxx xxx xxxxxxxxx xxxx (xxxxxxx) (24). X xxxxxxxx xxxxxxxxxx jsou Campylobacter xxx. x Xxxxxxxxxx spp. označeny xx xxxxxx xxxxxxxxx, která xx x xxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx bezpečnosti xxxxxxxx, jehož xxx xxxxxxxxx xxxxxxxxxxxxxxx zdokonalených xxxxxxxxx x xxxxxxxxxxxx řetězci x xxxxxx založených na xxxxxx. |
|
(6) |
Xxx 6. června 2013 přijal xxxx XXXX xxxxxxx xxxxxxxxxx x xxxxxxxxxxx pro xxxxxx xxxxxx, která xxxx xxx zohledněna xxx xxxxxxxxx masa (xxxxx) (25). X xxxxxxxx xxxxxxxxxx xxxx xx nejvýznamnější xxxxxxxxx pro xxxxxxxxx xxxx xxxxx označeny Xxxxxxxxxx xxx. x xxxxxxxxx verocytotoxigenní Xxxxxxxxxxx xxxx (E. xxxx). Xxxxxxxxxx xx x xxx upustit od xxxxxxxxxx a naříznutí xxxxx xxxxxxxxx xx xxxxxxx x xxxxxx xxxxxxxxxxx běžné xxxxxxx, xxxxxxx xx xxx může xxxxxx xxxxxx x xxxxxxx xxxxxxxxxxx x xxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx. Xxxxxxxxx xx xxxx měla xxx xxxxxxxxxx x xxxxxxxxx xxxxx xxxxxxxxx xx xxxxxxx, xxxxx xxxx xxxxxxxx xxx zjišťování xxxxxxx xxxxxxxxxxx x xxxxxxxxxxxx, již xxxxxxxxx Xxxxxx saginata (xxxxxxxxx). |
|
(7) |
Xxxxxx dne 6. června 2013 xxxxxx xxxx XXXX xxxxxxx xxxxxxxxxx o nebezpečích xxx xxxxxx zdraví, xxxxx xxxx být xxxxxxxxxx při xxxxxxxxx xxxx ovcí x xxx (26). X xxxxxxxx stanovisku xx xx xxxxxxxxxxxxxx xxxxxxxxx xxx xxxxxxxxx xxxx xxxx a koz xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxxxx E. xxxx. Doporučuje se x xxx xxxx xxxxxxx x xxxxxxxx xxxxx xxxx xx xxxxxxxxxx a naříznutí xxxxx xxxxxxxxx po xxxxxxx x xxxx x xxx xxxxxxxxxxx běžné xxxxxxx. X xxxxxx xxxxxxxxxxxxx x xxxxxxxxxx xxxxxx xx xxxx xxxx být x xxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxx xx xxxxxx dozoru xxx xxxxxxxxxxxx x xxxxxxxxxxx. |
|
(8) |
Xxxxxx xxx 6. xxxxxx 2013 xxxxxx úřad XXXX xxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxx lidské xxxxxx, xxxxx mají xxx zohledněna při xxxxxxxxx xxxx (xxxxxxxxxxxxxx) (27). X xxxxxxxx xxxxxxxxxx se xxxxxxxxxx xxxxxxxx x xxxxxxxxxxxxxx xxxxx vizuální prohlídku, xxx xxxx xxx xxxxxxxx xxxxxxxx vliv xx mikrobiologický xxxx xxxx jatečně xxxxxxxxxx xxx lichokopytníků. Má xx za to, xx xxxxxx prohlídka xxxxxxxxxxxxx nebude mít xxxxx xx xxxxxxx xxxxx nad xxxxxxxx xxxxxx. |
|
(9) |
Xxxxxx xxx 6. června 2013 xxxxxx úřad EFSA xxxxxxx xxxxxxxxxx x xxxxxxxxx xxxx farmové xxxxx. X xxxxxxxx xxxxxxxxxx se xxxxxxxxxx xxxxxxx xx xxxxxxxxxx x xxxxxxxxx, xxxxxx-xx xxxxxxxx xxxxxxxx, a současně xx xxxxxxxxxx, xx xxxx upuštění xxxx xxx xxxxxxxx xxx xxxxxxx xxxxx xxx xxxxxxxxxxxx. |
|
(10) |
Xxxxxxxxxx uvedená ve xxxxxxxxx stanoviscích xxxxx XXXX xx měla xxx xxxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxx kontrol xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx x xxxxxx xxxxxxxx. X xxxxx xx měl být xxxx také xxxxx xxxxx xx xxxxxx x xxxxxxx xxxxxx. Současně xx měl xxx xxxxxxxx xxxxxx xxxxxxx xx xxxxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxxxxx x xxxxxxxx (XX) x. 854/2004. |
|
(11) |
Tato xxxxxxxxx opatření xx xx xxxx xxxxxxxxx xx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx původu xxxxxxxxx x xxxxxx 18 xxxxxxxx (XX) 2017/625 x x xxxxxxxx Xxxxxx x xxxxxxxxx xxxxxxxxx (XX) 2019/624 (28). Xxxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxx xx xxxx být xxxxxxxx x xxxx xx xxxxxxxxxx uplatňování požadavků xx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxx, xx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxx, xxx xx xxxxxxxxx x xxxxxx 16 nařízení (XX) 2017/625, xxxxxxxxxxxxxxxx xxxxxxxxxx prahové xxxxxxx. |
|
(12) |
Jelikož xxxxxxxxx jatek x xxxxxxxx xxx nakládání xx xxxxxxxx xx x xxxxxxx xxxxxxxxx xxxxxxx xxxxx, xxxx by xxx xxxxxxx xxxxxxx xxxxxxxx xx xxxxx xxxxxxxxxx xxxx xxxxxxxxxxxx zvířat xxxx na xxxxxxxxx xxxxxxxxxxx, xx xxxxxxxxxxx xxxxxxx x xxxxx xxxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxx xx xxx. X xx. 17 xxxx. 6 xxxxxxxx (XX) x. 1099/2009 xxxx xxxxxxxxxx xxxxx xxxxxxx xxxxxxxx x xxxxxxxxx přepočítací xxxxxxxxxxx xxx xxxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxx v těchto velkých xxxxxxxxx xxxxxxxxxx. Xxxx xxxxxxxxxx xx xxxx xxx použita xx xxxxxxxxx xxxxxxxxx hodnot x x xx největší xxxxxxxxxxx xxxxxxxx od xxxxxxxxx xxxxxxxxx na xxxxxxx xxxxxxxxx xxxxx. |
|
(13) |
Xxxxxxxxx xx xxxx xxx xxxx xxxxxxxx xxxxxxxxx xx xxxxxx prováděné xxxxxxxxxxx xxxxxx, aby xxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxxx Xxxx xx xxxxxxxx xxxxxxxxxxx xxxxxx. Audity xxxx zvláštní xxxxxx xxx xxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxx založených xx xxxxxxx xxxxx x xxxxxxxxxx kontrolních xxxxxx (XXXXX). |
|
(14) |
Xxxxxxxxx xxxxx x xxxxxxxxx xx xxxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxx XX xxxxxx X xxxxxxxx (ES) x. 853/2004, x xxxxxxxxxxx xxxxxxxxx x xxxxxxxx (XX) x. 854/2004, xx xxxx xxx xxxxxxxxx, aby xxxx xxxxxxx možné xxxxxxxxxx. |
|
(15) |
Xxxxxxxxx xxxx porážkou a po xxxxxxx xxxx nezbytné xxx xxxxxxx xxxxxxx x xxxxxxxxx x xxxxxxx zdraví xxxx x xxxxxx a dobrých xxxxxxxxx podmínek xxxxxx. Xxx xxxx zajištěna xxxxxxx xxxxxx xxxxxx xxxxxxx xxxxxx xxxx x xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx xxxxxx, jakou xxxxxxx xxxxxxxx (XX) x. 854/2004, x xxxxxxxxxxx xxxxxx xx xxxxxxxxx trhu, xx nutné xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxx xxxx xxxxxxxxx, xxxxxx případů, kdy xx xxxxxxxxx úředních xxxxxxx xxxxxxxx úřední xxxxxxxxxxx xxxxx. Pokud xxx x xxxxxx xxxxxxxx xxxxxxxxx xxxx, xxxx xx xxx xxxx xxxxxxxxx xxxxxxxx příslušnými xxxxxxxxxx dokladů, xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx xx. 3 xxxx. 1 písm. x) xxxxxxxx (ES) x. 999/2001 a jiných xxxxxxxxxx xxxxxxxx xxxxxxxxxxx původu x xxxxxxxx xxxxxxxxxxxxx xxxxx. |
|
(16) |
Je xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xx nesoulad x xxxxxxxxxx xxxxxxxxx, xxx xxxx příslušné orgány xxxxxxxx xxxxxxxx xx xxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx. X xxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx xx xxxx xxxx xxxxxx nedodržování xxxxxxx xxxxxxxxxx xxxxx. |
|
(17) |
Značka xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx x xx. 3 xxxx 51 nařízení (XX) 2017/625, xxxxx xx xxxx xxxx xxxxxxxxx druhů, xxxxxxxxx, xx xx maso xxxxxx x xxxxxx xxxxxxxx. Xxxxxxxxx xxxxxxxxx na xxxxxx xxxxxxxxx xxxxxxxxxxxx x xxxxxxxxx opatření pro xxxx používání xx xxxx xxx stanoveny xxxxxxxxx a jednotně x xxxxx xxxxxxxxxx o vhodnosti xxxx x xxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxx narušení obchodu. |
|
(18) |
Xxxxxxxx Xxxxxx (XX) č. 2074/2005 (29) xxxxxxx xxxx xxxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxx nařízení (XX) x. 854/2004, pokud xxx x xxxxxx testovací metody xxx mořské biotoxiny x xxxxxx xxxxxx, xxxxxxxxx xxxxxx xxx syrové xxxxx x xxxxxxx xxxxxxxx xxxxx, xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx a prohlídky xxxx. Veškerá xxxxxxxxx xxxxxxxx pro xxxxxxxxxx xxxxxxxx xxxxxxx je xxxxxx xxxxxxx x xxxxxxxx x xxxxxxxx (ES) x. 2074/2005 xxxxxxxx do xxxxxx xxxxxxxx. V nařízení (XX) x. 2074/2005 xx měla xxx zrušena. |
|
(19) |
Xxxxxxx xx, xx současné xxxxxxxx xxx xxxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxx xxxxxxx xxx živé xxxx jsou xxxxxx x xxxxxxxxx xxxxxxx xxxxxx xxxxxxx xxxxxxxxxxxx. Xxxx xx xxx xxxxx xxxxxxxxx. |
|
(20) |
Xxxx xx být xxxxxxxxx xxxxxxxxxx xxxxxx xxx xxxxxx X. xxxx x xxxxxx mlžích x xxxxxxxxxxx stanovená x xxxxxxxx (XX) č. 854/2004. |
|
(21) |
Xxxxxx pro xxxxxx biotoxiny jsou xxxxxxxxx x xxxxxxxx (ES) x. 853/2004. Xxxxxxxxx x xxxxxxx XXX xxxxxx XXX xxxxxxxx X xxxx 2 xxxxxxxxx xxxxxxxx xx xxxxxxxxx, xx xxxx xxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx v celkovém xxxxxxxx, xxxxx překračuje xxxxxx stanovené x xxxxxxx xxxxxxxx (xxxxxx v celém xxxx xxxx x xxxxxxxxx xxxxxxxxxx xxxxx xxxxx). |
|
(22) |
Xxxx xx xxx xxxxxxxxx xxxxxxxx xxxxxxxxx na xxxxxxxxx xxxxxxxx xxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxxx mléka x xxxxxxxx xxxxxxx, aby xxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxx xxxxxxxxxxxx x xxxxxxxxxxx hospodářská xxxxxx xxxx xxxxxxxxxxxxx potravinářských xxxxxxx. |
|
(23) |
Xxxx xx být xxxxxxxxx xxxxxxxx xxxxxxxxx xx provádění xxxxxxxx xxxxxxx x xxxxxx jednotná xxxxxxxxx četnost x xxxxxxxx xxxxxxxx, xxx xxxx xxxxxxxxx vysoká xxxxxx xxxxxxx spotřebitele a spravedlivá xxxxxxxxxxx xxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků. Xxxxxxx kontroly by xxxx zahrnovat xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx a prvního xxxxxxx, xxxxxxxxxx inspekce xxxxxxxx x xxxxxxx, xxxxxx xxxxx x xxxxxxxxxxxxxxx trhů x xxxxxx, x xxxxxxxx skladování x xxxxxxxx. Xxxx xx xxx stanoveny xxxx xxxxxxxx požadavky xx xxxxxxxx plavidel. |
|
(24) |
Uvedené kontroly xx xxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, xxxxx xxx o organoleptická xxxxxxxxx, ukazatele xxxxxxxxxx, xxxxxxxx xxxxxxxxx, xxxxxxx x xxxxxxxxxxxxxxx látek x xxxxxxxxxxxxxxx xxxxxxxx. Zvláštní pozornost xx xxxxx xxxxxxx xxxxxxxxx xxxxxxxx a jedovatých xxxxxxxx xxxxxxxx. Produkty xxxxxxxx nesplňující uvedené xxxxxxxxxx xxxxxxxxx xx xxxx xxx xxxxxxxxxx xx nevhodné x xxxxxx xxxxxxxx. |
|
(25) |
Xxxxxxxxx by xxxx xxx xxxx xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxx produktů xxxxxxxx, xxxxx xxxxxxx xxxxxxxx xxxxxxx xxx xxxxxxx xxxxxxxxx států x xxxxx xxxxxxxx xx Unie xxxx, xx byly xxxxxxxxx, x xxxxxxxx xxx xxxxxxxxxx, ve xxxxx xxxx. |
|
(26) |
X xxxxxxxxxxx roste xxxxx x xxxxxxxx xxxx plazů x xxxx xxxxxxx xx xxx. V zájmu xxxxxxxxx xxxxxxxxxxx xxxx xxxxx xx xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx v nařízení (XX) x. 852/2004 x xxxxxxx trichinel xxxxxxxxxxx x xxxxxxxxxx xxxxxxxx (XX) 2015/1375 xxxxxxxx xxxxxx zvláštní xxxxxx xxxxxxxx při xxxxxxx. |
|
(27) |
Nařízení (XX) x. 2074/2005 by xxxx xxx odpovídajícím xxxxxxxx xxxxxxx. |
|
(28) |
Xxxxxxx xxxxxxxxx (XX) 2017/625 se x xxxxxxx ode dne 14. xxxxxxxx 2019 xxxxxxx nařízení (XX) x. 854/2004, mělo xx xx xxxx xxxxxxxx xxxxxx xxxxxx xx xxxxxxxxx xxxx. |
|
(29) |
Xxxxxxxx xxxxxxxxx tímto nařízením xxxx x xxxxxxx xx xxxxxxxxxxx Stálého výboru xxx xxxxxxxx, zvířata, xxxxxxxxx a krmiva, |
XXXXXXX XXXX XXXXXXXX:
HLAVA X
XXXXXXX, OBLAST XXXXXXXXXX X&xxxx;XXXXXXXX
Xxxxxx&xxxx;1
Xxxxxxx x&xxxx;xxxxxx xxxxxxxxxx
Xxxx xxxxxxxx stanoví xxxxxxxx xxxxxxxxx xxxxxxxx xxx provádění xxxxxxxx xxxxxxx x&xxxx;xxxxxxxx v souvislosti x&xxxx;xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx x&xxxx;xxxxxx xxxxxxxx. Xxxx xxxxxx xxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx se xxxxxxxxxxx xxxxxxxxx xx.&xxxx;18. xxxx.&xxxx;2, 3 x&xxxx;5 xxxxxxxx (XX) 2017/625 x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx (XX) 2019/624.
Xxxxxxxx xxxxxxxx xxxxxxxx:
|
x) |
xxxxxxxx požadavky a jednotnou xxxxxxxxx xxxxxxx xxx xxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxx x&xxxx;xxxxxx x&xxxx;xxxxxxxxxxxxx označení; |
|
b) |
zvláštní xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxx masa, xxxxxx xxxxxxxxxx požadavků na xxxxxx x&xxxx;xxxxxxxxxx úkolů xxxxxxxxxx se xxxxxxx xxxxxxxxx xxxx; |
|
x) |
xxxxxxxx, xxxxx xxxx xxx xxxxxxx x&xxxx;xxxxxxx xxxxxxxxx xxxxxxxxx xxxx x&xxxx;xxxxxxxxx Xxxx xx ochranu xxxxxxxx xxxxxx a zdraví x&xxxx;xxxxxxx xxxxxxxxx podmínek xxxxxx; |
|
x) |
xxxxxxxxx xxxxxxxxx a praktická xxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxx&xxxx;5 xxxxxxxx (ES) x.&xxxx;853/2004; |
|
x) |
xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx četnost xxx xxxxxx xxxxxxxx xxxxx, xxxxxxx, xxxxxxxx xxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx; |
|
x) |
xxxxxxxx pro xxxxxxxxxxx x&xxxx;xxxxxxxxxxxx klasifikovaných xxxxxxxxxxx x&xxxx;xxxxxxxxxxx oblastí xxx xxxx mlže, xxxxxx xxxxxxxxxx, která xxxx být xx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx xxxxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxx minimální xxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx. |
Xxxxxx 2
Xxxxxxxx
Xxx účely xxxxxx xxxxxxxx xx rozumí:
|
1) |
„čerstvým xxxxx“ xxxxxxx xxxx xxxxx xxxxxxxx v příloze X xxxx 1.10 xxxxxxxx (XX) x. 853/2004; |
|
2) |
„mlezivem“ xxxxxxx xxxxx xxxxxxxx v příloze XXX xxxxxx XX xxxx 1 xxxxxxxx (XX) x. 853/2004; |
|
3) |
„xxxxxxxx xxxxxxx“ xxxxxx xxxxxxx xxxxx xxxxxxxx v příloze I bodě 7.2 xxxxxxxx (ES) x. 853/2004; |
|
4) |
„xxxxxxx x xxxxxxx“ xxxxxxx x xxxxxxx podle xxxxxxxx x xxxxxxx III xxxxxx XX xxxx 2 xxxxxxxx (XX) x. 853/2004; |
|
5) |
„produkční xxxxxxx“ produkční xxxxxx xxxxx xxxxxxxx x xxxxxxx X xxxx 2.5 xxxxxxxx (XX) č. 853/2004; |
|
6) |
„sádkovací xxxxxxx“ xxxxxxxxx xxxxxx podle xxxxxxxx v příloze I bodě 2.6 nařízení (ES) x. 853/2004; |
|
7) |
„xxxx“ xxxx podle xxxxxxxx x xxxxxxx X xxxx 2.1 nařízení (XX) x. 853/2004; |
|
8) |
„xxxxxxxx rybolovu“ xxxxxxxx xxxxxxxx xxxxx definice x xxxxxxx I bodě 3.1 xxxxxxxx (XX) č. 853/2004; |
|
9) |
„xxxxxxxx“ xxxxxx xxxxx definice x xx. 2 xxxx. 1 xxxx. x) nařízení (XX) x. 852/2004; |
|
10) |
„xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx“ xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxx definice x xx. 3 xxxx 3 nařízení Xxxxxxxxxx parlamentu a Rady (XX) x. 178/2002 (30); |
|
11) |
„xxxxxxxxxxxxxxxx xxxxxxxxx“ xxxxxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxx x xx. 2 xxxx. x) xxxxxxxx (XX) x. 2073/2005; |
|
12) |
„xxxxxxx“ xxxxx podle xxxxxxxx v příloze X xxxx 1.16 nařízení (ES) x. 853/2004; |
|
13) |
„xxxxxxxxxxxxxxx“ xxxxxxxxxxxxxx xxxxx xxxxxxxx v čl. 3 bodě 15 xxxxxxxx (XX) x. 178/2002; |
|
14) |
„xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx“ xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxx v čl. 3 xxxx. 1 písm. x) xxxxxxxx (XX) x. 999/2001; |
|
15) |
„xxxxxxxxxxx“ xxxxxxxxxxx xxxxx definice x xx. 2 xxxx. 1 xxxx. x) xxxxxxxx (XX) x. 852/2004; |
|
16) |
„xxxxxxxxxxxxx xxxxxx“ hospodářství xxxxxx podle xxxxxxxx x xx. 2 bodě 2 xxxxxxxx v přenesené pravomoci (XX) 2019/624; |
|
17) |
„prvovýrobou“ xxxxxxxxxx xxxxx xxxxxxxx v čl. 3 xxxx 17 xxxxxxxx (XX) č. 178/2002; |
|
18) |
„domácími xxxxxxxxx“ xxxxxx xxxxxxxxx podle xxxxxxxx x xxxxxxx I bodě 1.2 xxxxxxxx (XX) x. 853/2004; |
|
19) |
„xxxxxxxxx pro xxxxxxxxx xx xxxxxxxx“ zařízení xxx xxxxxxxxx xx xxxxxxxx xxxxx xxxxxxxx x xxxxxxx X xxxx 1.18 xxxxxxxx (XX) č. 853/2004; |
|
20) |
„velkou xxxxx xxxxxx xxxxx“ xxxxx xxxxx xxxxxx xxxx podle xxxxxxxx x xxxxxxx X xxxx 1.8 xxxxxxxx (XX) x. 853/2004; |
|
21) |
„hejnem“ xxxxx xxxxx xxxxxxxx x xx. 2 xxxx. 3 xxxx. x) xxxxxxxx (XX) x. 2160/2003; |
|
22) |
„xxxxxxxxx“ xxxxxxxxx podle xxxxxxxx x xxxxxxx X xxxx 1.4 xxxxxxxx (XX) x. 853/2004; |
|
23) |
„xxxxxxx xxxxxxxxx tělem“ xxxxxxx xxxxxxxx xxxx xxxxx xxxxxxxx v příloze X xxxx 1.9 nařízení (XX) č. 853/2004; |
|
24) |
„droby“ droby xxxxx xxxxxxxx x xxxxxxx X xxxx 1.11 xxxxxxxx (XX) x. 853/2004; |
|
25) |
„xxxxxxxxxxxxxxxx xxxxxxx“ xxxxxxxxxxxxxx jatky xxxxx xxxxxxxx x xx. 2 bodě 17 xxxxxxxx x xxxxxxxxx xxxxxxxxx (EU) 2019/624; |
|
26) |
„xxxxxxxxxxxxxxx xxxxxxxxx pro nakládání xx xxxxxxxx“ zařízení xxx xxxxxxxxx se xxxxxxxx xxxxx xxxxxxxx x xx. 2 xxxx 18 xxxxxxxx x xxxxxxxxx pravomoci (XX) 2019/624; |
|
27) |
„xxxxxx dobytčí xxxxxxxxx“ xxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxx x xx. 17 xxxx. 6 xxxxxxxx (XX) x. 1099/2009; |
|
28) |
„drobnou xxxxx xxxxxx xxxxx“ xxxxxx xxxxx xxxxxx zvěř xxxxx xxxxxxxx x xxxxxxx X xxxx 1.7 xxxxxxxx (XX) č. 853/2004; |
|
29) |
„xxxxxxx“ xxxxxx xxxxx xxxxxxxx v příloze X xxxx 1.3 nařízení (XX) č. 853/2004; |
|
30) |
„bourárnou/porcovnou“ xxxxxxxx/xxxxxxxx xxxxx xxxxxxxx x xxxxxxx X xxxx 1.17 xxxxxxxx (XX) x. 853/2004; |
|
31) |
„xxxxxxxxxxx“ xxxxxxxxxx xxxxx xxxxxxxx v příloze X xxxx 1.12 xxxxxxxx (XX) x. 853/2004; |
|
32) |
„masem“ xxxx xxxxx definice x xxxxxxx X xxxx 1.1 xxxxxxxx (XX) x. 853/2004; |
|
33) |
„xxxxxxxx zvěří“ xxxxxxx zvěř xxxxx xxxxxxxx v příloze X xxxx 1.6 xxxxxxxx (ES) x. 853/2004; |
|
34) |
„xxxxx xxxxxx zvěří“ xxxxx žijící xxxx xxxxx definice x xxxxxxx X xxxx 1.5 nařízení (XX) x. 853/2004: |
|
35) |
„xxxxxxxxxxx xxxxxxxx xxxxxxx x xxxxxxxx mléka“ xxxxxxxxxx xxxxxx určený x xxxxxxxx xxxxx podle xxxxxxxx x xxxxxxx X xxxx 4.2 nařízení (XX) x. 853/2004; |
|
36) |
„xxxxxxx xxxxxx“ syrové xxxxx podle xxxxxxxx x xxxxxxx X xxxx 4.1 xxxxxxxx (XX) x. 853/2004; |
|
37) |
„střediskem xxx čištění“ xxxxxxxxx xxx čištění xxxxx xxxxxxxx x xxxxxxx X xxxx 2.8 xxxxxxxx (XX) x. 853/2004; |
|
38) |
„xxxxxxxx xxxxxxxxx“ mořské xxxxxxxxx xxxxx xxxxxxxx x xxxxxxx I bodě 2.2 xxxxxxxx (ES) x. 853/2004; |
|
39) |
„fázemi xxxxxxxx, zpracování x xxxxxxxxxx“ xxxx xxxxxx, xxxxxxxxxx x xxxxxxxxxx podle definice x xx. 3 xxxx 16 xxxxxxxx (ES) x. 178/2002; |
|
40) |
„xxxxxxxxxx xxxxxxxxxx“ expediční xxxxxxxxx xxxxx definice v příloze X xxxx 2.7 xxxxxxxx (XX) x. 853/2004; |
|
41) |
„xxxxxxxx na xxx“ xxxxxxx xx xxx xxxxx definice x xx. 3 xxxx 8 xxxxxxxx (XX) x. 178/2002; |
|
42) |
„xxxxxxxxxxxxxxx xxxxxxxxx“ zpracovatelské xxxxxxxx xxxxx xxxxxxxx x xxxxxxx X xxxx 3.2 nařízení (XX) x. 853/2004; |
|
43) |
„mrazírenským xxxxxxxxx“ xxxxxxxxxxx plavidlo xxxxx xxxxxxxx v příloze I bodě 3.3 xxxxxxxx (XX) x. 853/2004; |
|
44) |
„xxxxx“ xxxxx xxxxx xxxxxxxx x xx. 2 xxxx 15 xxxxxxxx Komise x xxxxxxxxx xxxxxxxxx (XX) 2019/625 (31); |
|
45) |
„xxxxx xxxxx“ xxxx xxxxx xxxxx xxxxxxxx x xx. 2 xxxx 16 xxxxxxxx v přenesené pravomoci (XX) 2019/625; |
|
46) |
„xxxxxxxxx xxxxxxxx xxxxxxxx“ čerstvé xxxxxxxx xxxxxxxx xxxxx xxxxxxxx x xxxxxxx X xxxx 3.5 xxxxxxxx (XX) x. 853/2004; |
|
47) |
„xxxxxxxxxx xxxxxxxx xxxxxxxx“ xxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxx x xxxxxxx X xxxx 3.6 nařízení (XX) x. 853/2004; |
|
48) |
„xxxxxxxxxxxx xxxxxxxx xxxxxxxx“ xxxxxxxxxx produkty rybolovu xxxxx xxxxxxxx v příloze X xxxx 7.4 xxxxxxxx (XX) č. 853/2004. |
XXXXX II
ZVLÁŠTNÍ XXXXXXXXX XX PROVÁDĚNÍ XXXXXXXX XXXXXXX X&xxxx;XXXXXXXX MINIMÁLNÍ XXXXXXX ÚŘEDNÍCH XXXXXXX X&xxxx;XXXXXXXX XXXXXXXXXXX PŮVODU
KAPITOLA X
Xxxxxxxx xxxxxxxxx xx xxxxxx prováděné xxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx původu
Xxxxxx&xxxx;3
Xxxxxxxxx xxxxxxxxxxx auditu
1. Při xxxxxxxxx xxxxxx správné xxxxxxxxxx xxxxx x&xxxx;xxxxxxxxx xxxxxxxxx orgány xxxxxxx, xxx provozovatelé potravinářských xxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxx xxxxxxxxx postupy, xxxxx xx xxxxxx xxxxxxx:
|
x) |
xxxxxxxxxx x&xxxx;xxxxxx xxxxxxx x&xxxx;xxxxxxxx; |
|
x) |
xxxxxxx xxxx xxxxxxxxx xxxxxxxx, při xxxxxxxx x&xxxx;xx xx; |
|
x) |
xxxxxx hygieny; |
|
d) |
školení x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxx; |
|
x) |
xxxxxxx xxxxx škodlivým xxxxxxxxxx; |
|
x) |
xxxxxxx xxxx; |
|
x) |
xxxxxxxx teploty; |
|
h) |
kontrol xxxxxx xxxx xxxxxxxx xxxxxxxxxxxx xx xxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxx xxxxxxx. |
2.&xxxx;&xxxx;&xxxx;Xxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxx xx xxxxxxx xxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxxx xxxxxx (XXXXX), xxxxx xxxx stanoveny x&xxxx;xxxxxx&xxxx;5 xxxxxxxx (ES) x.&xxxx;852/2004, xxxxxxxxx xxxxxx ověří, xxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxxx x&xxxx;xxxxx xxxxxxxxx.
3.&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxx, xxx xxxxxxx x&xxxx;xxxxxxxx xxxxx xxxx xxxxxxxx, xxx xxxxxxxx xxxxxxxxxxx xxxxxx:
|
x) |
xxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxx&xxxx;3 nařízení (XX) č. 2073/2005, xxxxx xxx o mikrobiologická kritéria; |
|
b) |
vyhovovaly xxxxxxx xxxxxxxxx Xxxx x&xxxx;xxxxxxx:
|
|
x) |
xxxxxxxxxxxx fyzikální xxxxxxxxx, xxxx. xxxxxxxx xxxxxx. |
4.&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;5 xxxx.&xxxx;5 xxxxxxxx (XX) x.&xxxx;852/2004 xxxxxxx postupy xxxxxxx x&xxxx;xxxxxxxx xxx xxxxxxxxx xxxxx xxxxxxxxxx na XXXXX, zahrnuje xxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxx.
5.&xxxx;&xxxx;&xxxx;Xxx provádění xxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxx zvláštní xxxxxxxxx:
|
x) |
xxxxxx, xxx personál x&xxxx;xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx ve xxxxx xxxxxx výrobního xxxxxxx xxxxxxxx xxxxxxxxx xx hygienickou praxi x&xxxx;XXXXX xxxxxxxxx x&xxxx;xxxxxx&xxxx;3 xxxxxxxx (XX) x.&xxxx;2073/2005, xxxxxxxx 4 a 5 xxxxxxxx (XX) č. 852/2004 x&xxxx;xx.&xxxx;3 xxxx.&xxxx;1 nařízení (XX) x.&xxxx;853/2004. Doplňkově x&xxxx;xxxxxx xxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx x&xxxx;xxxxx xxxxxx, xxx xx personál xxxxxxxxxx dovednosti; |
|
b) |
ověření příslušných xxxxxxx xxxxxxxxxxxxx potravinářského xxxxxxx; |
|
x) |
x&xxxx;xxxxxxx potřeby odebrání xxxxxx xxx xxxxxxxxxxx xxxxxxx; |
|
x) |
xxxxxxxxxxxxx xxxxxxxxxxx, xxxxx xxxxx v úvahu, x&xxxx;xxxxxxxx xxxxxx. |
Xxxxxx 4
Xxxxxx x xxxxxxx auditů
1. Xxxxxx x xxxxxxx xxxxx auditu x xxxxxxxxxxxx xxxxxxx xxxxxxxx xx posouzeném riziku. Xx xxxxx xxxxxx xxxxxxxxx xxxxxx pravidelně xxxxxxxx:
|
x) |
xxxxxx xxx xxxxxx xxxxxx x xxxxxxxx xxx xxxxxx xxxxxx; |
|
b) |
x xxxxx xxxxxxx xxxxxxx xxxxxxxxx podmínek xxxxxx; |
|
x) |
xxxx a rozsah prováděných xxxxxxxx; |
|
x) |
xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx, pokud xxx x xxxxxxxxxx xxxxxxxxxxxxx xxxxx. |
2. Xxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx x xxxxxxxxxxxx xxxxxxx xxxxxxx další xxxxxxxx x xxxxx zaručit bezpečnost xxxxxxxx zavedením xxxxxxxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxxxxxxx xxxxxxx nebo xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx xx xxxxxx xxxxxxxxxx x xxxx-xx xxxx opatření xxxxxxxxxxxxx x xxxxxxx xxxxxxx xxxx jasně xxxxxxxxxxxxxxxxx, xxxxx xxxxxxxxx xxxxxx xxx provádění xxxxxx xx xxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx praxe x xxxxxxx xxxxxxxxxx na xxxxxxxx XXXXX x xxxxx xxxxxxxxx xxxxxxxxxxx.
XXXXXXXX XX
Xxxxxxxx xxxxxxxxx xx xxxxxxxxxxxxx xxxxxxxx
Xxxxxx&xxxx;5
Xx xxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxx (XX) x.&xxxx;853/2004 se xxxxx xxxxxxxxx souladu x&xxxx;xxxxxxxxx xxxxxxxxx na xxxxxxxxxxxxxx xxxxx xxxxxx&xxxx;18 xxxxxxxx (ES) č. 178/2002 xxxxx xxxxxx s požadavky xxxxxxxx (XX) x.&xxxx;853/2004 xxxxxxxxxx se umísťování xxxxxxxxxxxxxxx xxxxxxxx.
XXXXXXXX XXX
Xxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxx
Xxxxxx&xxxx;6
Xxxxxxx xxxxx xxxxxxxxx Komisi a ostatní xxxxxxx xxxxx x&xxxx;xxxxxxxx x&xxxx;xxxxxxxxxxxxxx xxxxxx xxxxxxxx x&xxxx;xx.&xxxx;16 odst. 2 xxxx. x) xxxxxxxx (XX) 2017/625 xx účelem xxxx zvážení a případně xxxxxxx kroků.
HLAVA XXX
XXXXXXXX XXXXXXXXX XX XXXXXXXXX ÚŘEDNÍCH XXXXXXX X&xxxx;XXXXXXXX MINIMÁLNÍ XXXXXXX XXXXXXXX XXXXXXX X&xxxx;XXXXXXXXX XXXX
XXXXXXXX X
Xxxxxx
Xxxxxx&xxxx;7
Xxxxxxxxx požadavky xx xxxxxx v provozech xxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxx
1.&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx 3 a 4 xxxxxxxxx orgány xxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxxx x&xxxx;xxxxxxxx xxxxx xxxxx, xxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx postupy xxxxxxxx xx sběru, xxxxxxxx, skladování x&xxxx;xxxxxxxxxx x&xxxx;xxxxxxxxx xxxx x&xxxx;xxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx živočišného xxxxxx xxxxxx xxxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx, za něž xxxx xxxxxxxxx.
2.&xxxx;&xxxx;&xxxx;Xxxxx auditů xx jatkách xxxxx xxxxxxxxx orgány hodnocení xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx, xxxxx xxxx stanoveny x&xxxx;xxxxxxx II xxxxxx XXX xxxxxxxx (XX) x.&xxxx;853/2004.
3.&xxxx;&xxxx;&xxxx;Xxx provádění xxxxxx xxxxxxx xxxxxxxxxx na xxxxxxxx HACCP xxxxxxxxx xxxxxx kontrolují, zda xxxx xxxxx xxxxxxxxxx xxxxxxx stanovené x&xxxx;xxxxxxx XX xxxxxx XX xxxxxxxx (ES) č. 853/2004 x&xxxx;xxx xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků v nejvyšší xxxxx míře xxxxxxxx, xxx xxxxxxx xxxx:
|
x) |
xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxx xxxxx; |
|
x) |
xxxxxxxx xxxxxx:
|
|
x) |
xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx uvedená x&xxxx;xxxxxx&xxxx;3 xxxxxxxx (ES) x.&xxxx;2073/2005; |
|
x) |
xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx v souladu s požadavky xxxxxxxx (ES) x.&xxxx;999/2001. |
XXXXXXXX XX
Xxxxxx xxxxxxxx xxxxxxxxx masa
Xxxxxx&xxxx;8
Xxxxxxxxxxxx xxxxxxxx xxxxxx
Xxx xxxxxxxxx xxxxxxxx xxxxxxx xxxxx xxxx kapitoly přihlédne xxxxxx xxxxxxxxxxx lékař x&xxxx;xxxxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx s kapitolou X. Xx vhodných xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxxx xxxxxxxx zacílí xx xxxxxxxxxx zjištěné xxxxx předchozích xxxxxx.
Xxxxxx&xxxx;9
Xxxxxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxx o kontroly xxxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniku xxxxxxxxxxx xx xxxxxxxxxxxx xxxxxx x&xxxx;xxx, xxxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx xxxx xxx xxxxxxx provozovateli jatek x&xxxx;xxxxxxx x&xxxx;xxxxxxxx II xxxxxxx III xxxxxxxx (XX) x.&xxxx;853/2004.
2.&xxxx;&xxxx;&xxxx;Xxxxxxxxx orgány xxxxxxxx nezbytné kontroly xxxxxxx s cílem xxxxxx, xxx:
|
x) |
xxxx xxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx, xxxxx xxxxxxx xxxxxxxx nebo xxxxx xxxx xxxxxx xxxxxxxxx, x&xxxx;xxxxxxxxxxxxxx xxxxx xxxxxxxx x&xxxx;xxxxxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx; |
|
x) |
xxxx xxxxxxxxx o potravinovém řetězci xxxxxx x&xxxx;xxxxxxxxxx; |
|
x) |
xx xxxxxxxx xxxxxx xxxxx x&xxxx;xxxxxx xxxxxxxxxxx xxxxxxxxx poskytována xxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;39 xxxx.&xxxx;5. |
3.&xxxx;&xxxx;&xxxx;Xxxx-xx zvířata xxxxxxxx na xxxxxxx xx xxxxxx xxxxxxxxx xxxxx, příslušné xxxxxx x&xxxx;xxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxxx s příslušnými xxxxxx x&xxxx;xxxxx xxxxxxx x&xxxx;xxxxx xxxxxxxx, xxx měl x&xxxx;xxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx, xxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx podniku xxxxxxxxx xx hospodářství xxxxxx, xxxxxx přístup xxxxxxxxxxxx xxxxx, xxxxx xxxx xxxxxxxxx xxxxxxx.
Xxxxxx 10
Xxxxxxxxxx úředního xxxxxxxxxxxxx xxxxxx, xxxxx jde x xxxxxxxx xxxxxxx
1. Xxxxxx xxxxxxxxxxx xxxxx ověří výsledky xxxxxxx x xxxxxxxxx informací x xxxxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxx x xxxxxxx x xxxxxxxx II oddílem XXX xxxxxxxx (ES) x. 853/2004. Xxxxxx veterinární xxxxx xxxx xxxxxxxx x xxxxxxxxx spolu x xxxxxxxxx xxxxxxx důležitými xxxxxxxxxxx xx xxxxxxx hospodářství xxxxxx zvířat zohlední xxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx x xxxxxxxxx xx porážce.
2. Při xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx x xxxxxxxxx xx porážce xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx x xxxxxxx osvědčením xxxxxxxxxx x xxxxxxx s článkem 29 xxxxxxxxxxx xxxxxxxx Xxxxxx (XX) 2019/628 (38) x x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx lékařů xxxxxxxxxxxxx xxxxxx nebo xxxx kontroly na xxxxxx xxxxxxxxxx.
3. V případě nucené xxxxxxx xxxxxxxx xxxxxxxxx xxxx prostor xxxxx xxxxxx veterinární xxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxx stanovené v souladu x xxxxxxx 29 xxxxxxxxxxx nařízení (XX) 2019/628 x xxxxxx xxxxxxx veterinárním xxxxxxx, xxxxx provedl prohlídku xxxx porážkou v souladu x xxxxxxxx III xxxxxxx X xxxxxxxxx XX xxxxx 6 nařízení (ES) x. 853/2004, x xxxxxxx xxxxx xxxxxxxx informace xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx.
4. X xxxxxxx xxxxx xxxxx xxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxx v zařízení pro xxxxxxxxx xx zvěřinou xxxxxxxxx x xxxxxxxx prohlášení xxxxxxxxxxxxx xxxx zvířete xxxxxx proškolenou osobou x xxxxxxx s přílohou XXX xxxxxxx XX xxxxxxxxx XX xxxxx 4 xxxx. x) xxxxxxxx (XX) č. 853/2004.
Xxxxxx&xxxx;11
Xxxxxxxxx týkající xx prohlídky xxxx xxxxxxxx xx jatkách
1. Všechna xxxxxxx xxxx před xxxxxxxxx podrobena xxxxxxxxx xxxx xxxxxxxx. Xxxxxxxxx xxxx xxxx xxx xxxxxxx xx xxxxxxxxxxxxxxx xxxxxx xxxxx z každého xxxxx x&xxxx;xx reprezentativní xxxxxx zajícovců x&xxxx;xxxxxxx xxxxxxxxxxxx xxxxxx.
2.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxx xxxxxxxx xxxxxxxx xx 24&xxxx;xxxxx xx dopravení xxxxxx na xxxxx x&xxxx;xxxx xxx 24 hodin xxxx xxxxxxxx. Xxxxxx xxxxxxxxxxx xxxxx může xxxxxxx xxxxxxxxx dodatečnou xxxxxxxxx xxxx xxxxxxxx.
3.&xxxx;&xxxx;&xxxx;Xx xxxxxxx xxxxxxxxx před xxxxxxxx xx xxxx, xxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx:
|
x) |
xxxxxxxxx xxxxxx či xxxxxxxx xxxxxxx životních xxxxxxxx xxxxxxx; |
|
x) |
xxxxx, xxxxxxxx xxxx xxxxx, xxxxx xxxx xxxxxxx maso xxxxxxxxx x&xxxx;xxxxxx xxxxxxxx nebo xxxxx xx xxxxx xxxxxxxxxx ovlivnit xxxxxx xxxxxx, xxxxxxx xx xxxxxxxx pozornost xxxxxx xxxxxxxxxx xxxxxx x&xxxx;xxxxx xxxxxx, xxx něž xxxx stanovena xxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx (XX) 2016/429; |
|
x) |
xxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxx, zneužití xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxxxxxxxxxxx látek. |
4. Prohlídka xxxx xxxxxxxx xxxxxxxx xxxxxxx xxxx, xxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx, xxx xxxx xxxxxxx xxxxxx xxxx, kožku xxxx xxxxx x&xxxx;xxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx masa xxxxx xxxxxxx.
5.&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxx lékař xxxxxxx xxxxxxxxx xxxxxxxxx xxxxx xxxxxx, xxxxx xxxx xxxxxxxxxxxxxx potravinářského xxxxxxx nebo xxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxx.
6.&xxxx;&xxxx;&xxxx;Xxxxxxx-xx xx xxxxxxxxx xxxx xxxxxxxx x&xxxx;xxxxxxxxxxxx původu x&xxxx;xxxxxxx s článkem 5 xxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx (EU) 2019/624, xxxxxx xxxxxxxxxxx xxxxx xx xxxxxxx xxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxx xx xxxxxxxxxxx xxxxxxxxx a ve xxxxxxxxx xxxx.
Xxxxxx&xxxx;12
Xxxxxxxxx xx xxxxxxxxx xx xxxxxxx
1.&xxxx;&xxxx;&xxxx;X&xxxx;xxxxxxxx xxxxxxxx xxxxxxxxx v příloze XXX xxxxxx XX xxxxxxxx XX xxxx 4 xxxxxxxx (XX) x.&xxxx;853/2004 xx jatečně xxxxxxxx těla a k nim xxxxxxxxx droby xxxxxxx xxxxxxxxx po xxxxxxx:
|
x) |
xxxxxxxxxx xx xxxxxxx; nebo |
|
b) |
co xxxxxxxx xx xxxxxxxxx xx zařízení xxx xxxxxxxxx se zvěřinou. |
2. Příslušné xxxxxx xxxxx xxxxxxxxx, xxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx zvláštní xxxxxxxxx xxxxxxxx a dostatečný xxxxxxx pro xxxxxxxx xxxxx.
3.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxx:
|
x) |
xxxxxxxxxxx xxxx xxxxxx povrch, xxxxxx xxxxxxx tělních xxxxx xxxxxxx upravených xxx, xxxxx x&xxxx;xxxxx; |
|
x) |
xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx x&xxxx;xxxxx xxxxxx, pro xxx xxxx xxxxxxxxx xxxxxxxxxxx pravidla x&xxxx;xxxxxxxx (XX) 2016/429. |
4.&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxxx xxxxx a počet xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxx xxxxxx, xxx xxxxxxxxxx řádnou prohlídku.
Xxxxxx 13
Xxxxxxxx xxxxxxxx xx xxxxxxxxxx prohlídky xx xxxxxxx
1. Xxxxxxxx od xx. 12 xxxx. 1 xxxxx xxxxxxxxx xxxxxx xxxxxxx, xxx x xxxxxxx, xx xxxxxx xxxxxxxxxxx xxxxx xxx xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxx xxxxxxx a opracování xxxxxxxx x xxxxxxxx pro xxxxxxxxx xx xxxxxxxx xxxx xx xxxxxxx, xxxx xxxxxxxxx xx xxxxxxx xxxxxxxx na xxxx xxxxxxxx 24 xxxxx od xxxxxxx nebo xxxxxxxxx xx xxxxxxxx xxx xxxxxxxxx xx xxxxxxxx, xxxxx:
|
x) |
xxxxxxx xxxxxxx xxxx xxxxxxxx xx xxxxxxxxxxxxxxxx xxxxxxx nebo xx x xxxx manipuluje x xxxxxxxxxxxxxxx xxxxxxxx pro xxxxxxxxx xx xxxxxxxx, xxx xx xxxxxxx xxxx xxxxxxxxxx provádí x:
|
|
x) |
v provozu xxxxxxxx xxxxxxxxxx xxxxxxxx pro xxxxxxxxxx xxxxxxxxx xxxx x xxxxx xxx, xxx xxxxx být vyšetřeny; |
|
c) |
prohlídku xx xxxxxxx provádí xxxxxx veterinární xxxxx. |
2. příslušné xxxxxx xxxxx prahové xxxxxxx xxxxxxxxx x xxxx. 1 xxxx. a) bodech x) a ii) xxxxxx x xxx, xx xxxxxxx, xxx xx xxxxxxxx xxxxxxxxxxx x xxxxxxxxxx xxxxx x xxxxxxxx xxx xxxxxxxxx xx xxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxxx xxxxx xxxx xxxxxxxxxxxxxxxx xxxxxxxx xxx xxxxxxxxx se xxxxxxxx, x xx xxxxxxxxxxx, xx xxxxxxx xxxxx xxxxxxxx těchto provozů xxxxxxxxxxx 5 % xxxxxxxxx xxxxxxxx čerstvého xxxx xxxxxxxxxxxxxxx x xxxxxxxx xxxxx, x xx xxx:
|
x) |
xxxxxxx druhy; |
|
x) |
xxxx xxxxxxx xxxxxxxxx společně; |
|
x) |
xxxx xxxxxxxx drůbež xxxxxxxx; |
|
x) |
nebo xxxxxxx xxxxx a zajícovce xxxxxxxx. |
X xxxxxxx případě xxxxxxxxx xxxxxx xxxx xxxxxxxx x xxxxxx xx xxxx xxxxxxx xxxxxx postupem xxxxxxxxxx xx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x Xxxx (XX) 2015/1535 (39).
3. Xxx xxxxx xxxx. 1 xxxx. x) xxxx x) se xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx v čl. 17 xxxx. 6 xxxxxxxx (XX) x. 1099/2009. Xxxxx v případě xxxx, xxx x xxxx xxxxx (&xx; 100 xx xxxx hmotnosti) xxxxxx Cervidae (xxxxxxxxxx) xx xxxxxxx xxxxxxxxxxx xxxxxxxxxx 0,05 xxxxx xxxxxxx jednotky a v případě xxxx velké xxxxx xxxxxxxxxxx koeficient 0,2 xxxxx dobytčí xxxxxxxx.
Xxxxxx 14
Xxxxxxxxx xx další xxxxxxxxx u prohlídky xx xxxxxxx
1. Xxxxx xxxxxxxxx, xxxx xxxx xxxxxxxxxx a naříznutí xxxxx jatečně xxxxxxxxxx xxxx x xxxxx, x xxxxxxxxxxx xxxxx, se xxxxxxxx, xxxxx je to xxxxxxxx pro:
|
x) |
xxxxxxxxx konečné xxxxxxxx u podezření na xxxxxxxxx; xxxx |
|
x) |
xxxxxxxx:
|
2. Xxxxx xxxxxxxxx xx xxxxxxx xx xxxxxxx xxxxxxxx x xxxx, xxx xxxx xxxxxxxxxxx čerstvého xxxx xxx xxxxxxxxxx, xxxxxx xxxx xxxxxxxxx xxxxxxx xx xxxxxxx.
Xxxxxx 15
Xxxxxxxxx xx xxxxxxxxx xx porážce x xxxxxxxx xxxxxxxxxxxxxx, skotu xxxxxxxx xxxx xxxxxx, xxxxxxxx xxxxxx starších xxxx xxxxx x xxxxx xxxxx xxxxxx zvěře
1. Xxxxxxxxx xxxxx xxxxxx článku xx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx 12 x 14.
2. Xxxxxx xxxxxxxxxxx xxxxx xxxxxx, xxx xxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxxx, skotu staršího xxxx xxxxxx a domácích xxxxxx xxxxxxxx xxxx xxxxx byla x xxxxxxxxx xx xxxxxxx předložena xxxxxxxxx podélně xxxxx xxxxxx na půlky.
3. Xxxxx xx xx pro xxxxxxxxx xx xxxxxxx xxxxxxxx, xxxx xxxxxx xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxxx rozdělení xxxxx xxxx jatečně xxxxxxxxxx xxxx xxxxxxxxxx zvířete. Xx xxxxxx xxxxxxxxxxx x xxxxxxx xxxxxxxxxxxxxxx xxxxxx, xxxxxxxxxxxxxxx vývoji xxxx xxxxxxxxx sanitárním xxxxxxxx xxxx xxxx xxxxxx xxxxxxxxxxx lékař povolit, xxx xxxx xxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxxx, xxxxx xxxxxxxx xxxx xxxxxx x xxxxxxxx xxxxxx xxxxxxxx pěti xxxxx x xxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx.
4. U nízkokapacitních xxxxx nebo nízkokapacitních xxxxxxxx pro xxxxxxxxx xx zvěřinou, která xxxxxxxxxx x xxxx xxx 1 000 xxxxxxx xxxxxxxxx xxxxxxxx ročně, xxxx xxxxxx xxxxxxxxxxx xxxxx xx xxxxxxxxxxx důvodů xxxxxxx, aby xxxx xxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx, xxxxxxxxx xxxxx a dospělé xxxxx xxxxx žijící xxxxx xxxx prohlídkou xx xxxxxxx xxxxxxxxx xx xxxxxx.
Xxxxxx 16
Xxxxxxxxx xxxxxxxxx xx xxxxxxxxx po xxxxxxx x xxxxxxx xxxxxx porážky
X xxxxxxx xxxxxx xxxxxxx xx xxxxxxx xxxxxxxx tělo xxxx uvolněním x xxxxxx xxxxxxxx xxxxxxx xx xxxxxxxx prohlídce xx xxxxxxx xxxxx článků 12, 13, 14 x 15.
Xxxxxx 17
Xxxxxxxxx opatření xxxxxxxx xx prohlídky xx xxxxxxx x xxxxxxxx skotu, xxxxxxxx xxxx x xxx, xxxxxxxx xxxxxxxxxxxxxx x xxxxxxxx xxxxxx
Xxxxxxxx xx xxxxxxxxx xx porážce xxxxxxxxx xxxxxxx veterinárním xxxxxxx, xxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxx lékaře xxxx, xxxx-xx xxxxxxxx dostatečné xxxxxx, xx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx x xxxxxxx x xx. 18 xxxx. 2 xxxx. x) xxxxxxxx (XX) 2017/625 a článkem 7 xxxxxxxx x xxxxxxxxx xxxxxxxxx (XX) 2019/624, xxxxxxxxx xxxxxx xxxxxxx, xxx x xxxxxxx xxxxxxxx xxxxx, xxxxxxxx xxxx x xxx, xxxxxxxx lichokopytníků a domácích xxxxxx byla xxxxx xxxxxxxxx stanovených x xxxxxxxx 12, 14 a 15 xxxxxxxxxx praktická xxxxxxxx xxxxxxxxx v následujících xxxxxxxx 18 až 24.
Xxxxxx 18
Xxxxx xxxx
1. Xxxxxxx xxxxxxxxx xx xxxxxxx stanovené x xxxxxxxx 2 xxxx xxx provedeny u jatečně xxxxxxxxxx xxx x xxxxx xxxxxx kusů xxxxx:
|
a) |
xxxxxxx xxxxxx xxxx xxxxxx; x |
|
x) |
xxxxxxx xxxxxx xxxxxxx xxxxxx, pokud byla xxxxx xxxxxx života xxxxxxx xxx xxxxxxxx xx xxxxxxxx x xxxxxxxx xxxxx nebo xxxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxx tuberkulózy xxxxx x xxxxxxx x xxxxxxx 1 xxxxxxxxxx 2003/467/XX. |
2. Xxxxxxx xxxxxxxxx po xxxxxxx xxxxxxxx xxxxxxx xxxxxxxx prohlídku:
|
a) |
hlavy x xxxxxx; xxxxx s prohmatáním a vyšetřením xxxxxxx uzlin xxxxxxxxxxxx (Xxx. xxxxxxxxxxxxxxxxx) však xxxxx xxxxxxx xxxxx xx xxxxxx xxxxxxxxx xxxxxx xxx statusem xxxxx/xxxxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxx xxxxxxxxx; xxxxxxxxx tlamy x xxxxxx; |
|
x) |
xxxx, xxxxxxxxxx x xxxxx; xxxxxxxxxx xxxx; xxxxxxxxxx a vyšetření xxxxxxx xxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxxxx (Lnn. bifurcationes, xxxxxxxxxxxx xx xxxxxxxxxxxxx); |
|
c) |
xxxxxxxxxx x xxxxx; |
|
x) |
xxxxxxx; |
|
x) |
xxxxx a mízních xxxxx xxxxxxxxx x xxxxxxxx xxxxxx (Xxx. xxxxxxxx); |
|
x) |
gastrointestinálního xxxxxx, xxxxxx x xxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxxxxxxx (Lnn. xxxxxxxx, xxxxxxxxxxx, xxxxxxxxx xx caudales); |
|
x) |
xxxxxxx; |
|
x) |
xxxxxx; |
|
i) |
xxxxxxxxxx x xxxxxxxxxx; |
|
j) |
xxxxxxx xxxxxxx a kloubů mladých xxxxxx. |
3. Xxxxxxxx-xx xxxxxx xxxxxxx xxxxxx pro xxxxxx xxxxxx, xxxxxx xxxxxx xxxx xxxxx xxxxxxx xxxxxxxx xxxxxx x xxxxxxx x xxxxxxx 24, xxxxxxx xxxxxx xxxxxxxxxxx xxxxx prostřednictvím xxxxxxxxx x xxxxxxxxxx jatečně xxxxxxxxxx xxxx x xxxxx xxxx xxxxxxx prohlídky xx xxxxxxx:
|
a) |
xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxxx (Lnn. xxxxxxxxxxxxxxxxx); xxxxxxxxxx xxxxxx; |
|
x) |
xxxxxxxxx xxxxxxx xxxxx bronchiálních x xxxxxxxxxxxxxxx (Xxx. bifurcationes, xxxxxxxxxxxx et xxxxxxxxxxxxx); xxxxxxxx xxxxxxxxxx x xxxx xxxxxxxx podélným xxxxx; xxxxx se xxxxxxxx x xxxxx xxxxxxx kolmo xx xxxxxx osu; xxxx xxxx nejsou xxxxxxxx, xxxxx xxxx xxxxx xxxxxxxxx x xxxxxxx x xxxxxx spotřebě; |
|
x) |
podélné xxxxxxxxx xxxxx tak, xxx xxxx otevřeny obě xxxxxx x xxxxxxxx xxxxxxxxxxxx xxxxxxxx; |
|
x) |
xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxxxxxxx; |
|
x) |
xxxxxxxxxx sleziny; |
|
x) |
naříznutí xxxxxx x xxxxxxxxx mízních xxxxx (Lnn. xxxxxxx); |
|
x) |
prohmatání xxxxxxx pupeční a kloubů. Xxxxxxxx xxxxxxx se xxxx xxx x xxxxxxx xx x xxxxxx; xxxx xxx vyšetřen xxxxxxx xxx. |
Xxxxxx 19
Xxxxxxx xxxx
1. X xxxxxxx xxxxxxxxxx xxx x xxxxx xxxxx xxxxxx xxx xxxxxxxxx x xx. 18 odst. 1 xx xxxxxxxx xxxx postupy xxxxxxxxx xx porážce:
|
x) |
vizuální xxxxxxxxx hlavy x xxxxxx; xxxxxxxxx a vyšetření xxxxxxx xxxxx xxxxxxxxxxxx (Lnn. xxxxxxxxxxxxxxxxx); vyšetření žvýkacích xxxxx xxxxxxxxxxx xxxxx xxxx xxxxxxxxxxxx x xxxxx xxxxxxx a žvýkacích xxxxx xxxxxxxxx (vnitřních křídlových xxxxx) xxxxxxx řezem. Xxxxx xx xxxxxx xxx, xxx xxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxxxx tlama x xxxxx; |
|
x) |
xxxxxxxxx xxxxxxxxxx x xxxxx; xxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxx; xxxxxxxxx a vyšetření xxxxxxx xxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxxxx (Xxx. xxxxxxxxxxxxx, xxxxxxxxxxxx xx mediastinales); |
|
c) |
vizuální xxxxxxxxx xxxxxxxxxx a srdce, xxxxx xx xxxxx naříznout xxxxxxxx xxxxx, xxxxxxx xxx xxx xxxxxx x xxxxxxxx mezikomorovou xxxxxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxx; |
|
x) |
vizuální prohlídka xxxxx x xxxxxxx uzlin xxxxxxxxx x xxxxxxxx xxxxxx (Xxx. portales); |
|
x) |
vizuální prohlídka xxxxxxxxxxxxxxxxxxxx xxxxxx, xxxxxx, xxxxxxx xxxxx žaludečních x xxxxxxxxxxxxxxx (Lnn. gastrici, xxxxxxxxxxx, xxxxxxxxx et xxxxxxxx); xxxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxxxxxxx; |
|
g) |
xxxxxxxx xxxxxxxxx xxxxxxx; |
|
h) |
xxxxxxxx xxxxxxxxx xxxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx (xxxxx xxxxxx, xxxxx xxx xxx xxxxxxxxx); |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxx mízních xxxxx (Xxx. xxxxxxxxxxxxx). |
2. Existují-li xxxxxx xxxxxxx rizika pro xxxxxx zdraví, zdraví xxxxxx xxxx xxxxx xxxxxxx xxxxxxxx xxxxxx x xxxxxxx s článkem 24, xxxxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxx těla x xxxxx xxxx xxxxxxx xxxxxxxxx po xxxxxxx:
|
x) |
xxxxxxxxx x xxxxxxxxx xxxxxxx uzlin xxxxxxxxxxxxx x xxxxxxxxx (Xxx. xxxxxxxxxxxx et parotidei); xxxxxxxxxx xxxxxx x xxxxxx; |
|
x) |
xxxxxxxxx xxxxxxx xxxxx bronchiálních x xxxxxxxxxxxxxxx (Xxx. xxxxxxxxxxxxx, xxxxxxxxxxxx xx xxxxxxxxxxxxx); xxxxxxxx průdušnice a obou xxxxxxxx xxxxxxxx xxxxx; xxxxx xx naříznou x xxxxx xxxxxxx xxxxx xx xxxxxx osu; xxxx xxxx xxxxxx xxxxxxxx, xxxxx xxxx xxxxx xxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx; |
|
x) |
xxxxxxxxxx xxxxx x xxxxxxx xxxxx xxxxx x xxxxxxxx xxxxxx (Xxx. xxxxxxxx); xxxxxxxxx xxxxxxxxx xxxxxx xxxxx x xxx xxxxxxxx lalokem x xxxxx xxxxxxxx xxxxxxxxx; |
|
x) |
xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxx a mezenteriálních; |
|
e) |
xxxxxxxxxx xxxxxxx; |
|
x) |
xxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxx xxxxx (Xxx. xxxxxxx); |
|
x) |
x xxxx xxxxxxxxxx a naříznutí xxxxxx a vemenních xxxxxxx xxxxx (Xxx. supramammarii). Xxxxx xxxxxxxx vemene xx otevře xxxxxxx x xxxxxxxx xxxxx xxxxxxxx xx x xxxxxxxxxx (xxxxx xxxxxxxxxx) x xxxxxxxx xx xxxxxxx xxxxx uzliny, x xxxxxxxx xxxxxxx, kdy xx vemeno xxxxxxxxx x xxxxxxx x xxxxxx spotřebě. |
Xxxxxx 20
Xxxxx domácí xxxx x xxxx x xxxx xxx xxxxxxxxxxx trvalých xxxxxx
1. U jatečně xxxxxxxxxx xxx x xxxxx xxxx xxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxx xxxxxxxx dvanácti xxxxxx x x xxx mladších šesti xxxxxx se xxxxxxxx xxxx xxxxxxx xxxxxxxxx xx xxxxxxx:
|
a) |
vizuální xxxxxxxxx xxxxx, včetně xxxxxx, xxxxx, xxxxxx x xxxxxxx xxxxx xxxxxxxxx x xxxxxxxxxxxx. Xxxx xxxxxxxxx nejsou xxxxxxxx, pokud xxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxx, xx xxxxx, xxxxxx jazyka a mozku, xxxx xxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx; |
|
x) |
vizuální xxxxxxxxx xxxx, xxxxxxxxxx x xxxxx x xxxxxxx xxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxxxx (Xxx. bifurcationes, xxxxxxxxxxxx xx mediastinales); |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxxxxx a srdce; |
|
d) |
xxxxxxxx xxxxxxxxx bránice; |
|
x) |
vizuální prohlídka xxxxx a mízních xxxxx xxxxxxxxx a slinivky xxxxxx (Xxx. xxxxxxxx); |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxxxxxxx xxxxxx, okruží x xxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxxxxxxx (Xxx. gastrici, xxxxxxxxxxx, xxxxxxxxx xx xxxxxxxx); |
|
x) |
xxxxxxxx prohlídka xxxxxxx; |
|
h) |
xxxxxxxx xxxxxxxxx xxxxxx; |
|
i) |
vizuální xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx; |
|
x) |
vizuální xxxxxxxxx xxxxxxx pupeční a kloubů. |
2. Xxxxxxxx-xx xxxxxx xxxxxxx xxxxxx xxx xxxxxx xxxxxx, xxxxxx xxxxxx nebo xxxxx životní xxxxxxxx xxxxxx v souladu x xxxxxxx 24, xxxxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxx xxxx x xxxxx xxxx xxxxxxx xxxxxxxxx po xxxxxxx:
|
x) |
xxxxxxxxxx hrtanu, xxxxx, xxxxxx x xxxxxxxxx xxxxxxx xxxxx. Xxxxxxxxx-xx xxxxxxxxxxx xxxxxxxx xxxxx, xxxxxx xxxx xxxxxxxxx xxxxxxxx, xxxxx xxxx xxxxxxxxx xxxxxx schopny zaručit, xx hlava, včetně xxxxxx x xxxxx, bude xxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx; |
|
x) |
xxxxxxxxxx xxxx; xxxxxxxxx xxxx, xxxxxxxxxx, xxxxx x xxxxxxx xxxxx bronchiálních x xxxxxxxxxxxxxxx; |
|
x) |
xxxxxxxxx srdce; |
|
x) |
xxxxxxxxxx jater x xxxxxx xxxxxxx xxxxx; xxxxxxxxx žaludeční strany xxxxx s cílem vyšetřit xxxxxxxxx; |
|
x) |
xxxxxxxxxx sleziny; |
|
x) |
naříznutí ledvin x xxxxxxxxx xxxxxxx xxxxx (Xxx. renales); |
|
x) |
xxxxxxxxxx xxxxxxx xxxxxxx x xxxxxx; krajinou xxxxxxx xx vede xxx x xxxxxxx xx x xxxxxx; xxxxxxx xx xxxxxxx xxx. |
Xxxxxx 21
Xxxxxxx xxxxxx xxxx x xxxx
1. X xxxxxxx xxxxxxxxxx xxx x xxxxx ovcí x xxxxxxxxxx xxxxxxx xxxxxxx nebo xxxxxxx xxxxxxx xxxxxx xxxx více a u koz xxxxxxx xxxx xxxxxx xxxx více se xxxxxxxx tyto xxxxxxx xxxxxxxxx xx porážce:
|
a) |
xxxxxxxx xxxxxxxxx hlavy, xxxxxx xxxxxx, xxxxx, xxxxxx x xxxxxxxxx xxxxxxx uzlin, x xxxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxxx. Xxxx xxxxxxxxx xxxxxx xxxxxxxx, xxxxx xxxx xxxxxxxxx orgány xxxxxxx xxxxxxx, že xxxxx, včetně xxxxxx x xxxxx, xxxx xxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx; |
|
b) |
xxxxxxxx xxxxxxxxx xxxx, xxxxxxxxxx x xxxxx; xxxxxxxxxx xxxx, xxxxxxx xxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxxxx (Xxx. xxxxxxxxxxxxx, xxxxxxxxxxxx xx xxxxxxxxxxxxx); |
|
c) |
xxxxxxxx xxxxxxxxx osrdečníku x xxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx bránice; |
|
x) |
xxxxxxxx xxxxxxxxx xxxxx x xxxxxxx xxxxx xxxxxxxxx x xxxxxxxx xxxxxx (Xxx. portales); prohmatání xxxxx a jejich xxxxxxx xxxxx; xxxxxxxxx žaludeční xxxxxx jater x xxxxx xxxxxxxx žlučovody; |
|
f) |
xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxxxxxxx xxxxxx, okruží x xxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxxxxxxx (Xxx. xxxxxxxx, xxxxxxxxxxx, xxxxxxxxx xx xxxxxxxx); |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxx; |
|
x) |
vizuální xxxxxxxxx xxxxxx; |
|
x) |
vizuální xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx; |
|
j) |
vizuální prohlídka xxxxxxxxxx orgánů (kromě xxxxxx, pokud byl xxx xxxxxxxxx); |
|
x) |
vizuální prohlídka xxxxxx x xxxxxxxxx xxxxxxx xxxxx. |
2. Xxxxxxxx-xx xxxxxx možného xxxxxx xxx xxxxxx xxxxxx, xxxxxx xxxxxx xxxx xxxxx xxxxxxx xxxxxxxx xxxxxx x xxxxxxx x xxxxxxx 24, provede xxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxxx a prohmatání xxxxxxx xxxxxxxxxx xxxx a drobů xxxx xxxxxxx xxxxxxxxx xx xxxxxxx:
|
x) |
xxxxxxxxxx xxxxxx, xxxxx, xxxxxx a příušních xxxxxxx uzlin. Xxxxxxxxx-xx xxxxxxxxxxx pravidla xxxxx, xxxxxx tato xxxxxxxxx xxxxxxxx, pokud xxxx xxxxxxxxx orgány xxxxxxx xxxxxxx, xx xxxxx, xxxxxx jazyka a mozku, xxxx xxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx; |
|
x) |
xxxxxxxxx xxxx, xxxxxxxxxx, jícnu x xxxxxxx xxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxxxx; |
|
c) |
xxxxxxxxx xxxxx; |
|
x) |
xxxxxxxxxx sleziny; |
|
x) |
naříznutí xxxxxx x xxxxxxxxx mízních uzlin (Xxx. xxxxxxx). |
Xxxxxx 22
Xxxxxx xxxxxxxxxxxxxx
1. X xxxxxxx upravených xxx x xxxxx xxxxxxxx xxxxxxxxxxxxxx xx xxxxxxxx xxxx xxxxxxx prohlídky xx porážce:
|
x) |
xxxxxxxx prohlídka xxxxx a hrtanu xx xxxxxxxx xxxxxx; xxxxx xx xxxxxx tak, xxx mohla xxx xxxxxxxx vizuálně xxxxxxxxxxx xxxxx x xxxxx, a musí xxx vizuálně xxxxxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx plic, xxxxxxxxxx, xxxxx a mízních xxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxxxx (Lnn. xxxxxxxxxxxxx, xxxxxxxxxxxx et xxxxxxxxxxxxx); |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx jater a mízních xxxxx xxxxxxxxx x xxxxxxxx xxxxxx (Lnn. xxxxxxxx); |
|
f) |
xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxxxxxxx xxxxxx, xxxxxx a mízních uzlin xxxxxxxxxxx a mezenteriálních (Xxx. xxxxxxxx, xxxxxxxxxxx, xxxxxxxxx xx xxxxxxxx); |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxx; |
|
x) |
xxxxxxxx prohlídka ledvin; |
|
x) |
vizuální xxxxxxxxx pohrudnice a pobřišnice; |
|
x) |
vizuální xxxxxxxxx pohlavních xxxxxx xxxxxx (kromě xxxxxx, xxxxx xxx již xxxxxxxxx) x xxxxxx; |
|
x) |
xxxxxxxx prohlídka xxxxxx a vemenních xxxxxxx xxxxx (Lnn. xxxxxxxxxxxxx); |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx x xxxxxx xxxxxxx xxxxxx; |
|
x) |
x xxxxxx xxxx vyšetření xxxxx x xxxxxxx xxxxx (Xxx. xxxxxxxxxxxxx) xxxxx xxx xxxxxxxxxx xxxxxxxxxx xx xxxxxxxx úponu jedné xxxxx xx xxxxxx xxxxxxxxx xx xxxxxxxx x xxxxxxxx. Ledviny xx xxxxxx. |
2. Xxxxxxxx-xx známky možného xxxxxx pro lidské xxxxxx, zdraví xxxxxx xxxx xxxxx xxxxxxx xxxxxxxx zvířat x xxxxxxx x xxxxxxx 24, provede úřední xxxxxxxxxxx lékař prostřednictvím xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxx xxxx x xxxxx xxxx xxxxxxx xxxxxxxxx xx porážce:
|
a) |
prohmatání x xxxxxxxxx xxxxxxx xxxxx podčelistních, xxxxxxxxxxxx a příušních (Lnn. xxxxxxxxxxxxxxxxx, mandibulares xx xxxxxxxxx); xxxxxxxxxx xxxxxx; |
|
b) |
prohmatání xxxx; prohmatání x xxxxxxxxx xxxxxxx uzlin xxxxxxxxxxxxx x xxxxxxxxxxxxxxx. Xxxxxxxxxx x xxx xxxxxxxx se xxxxxxx xxxxxxxx xxxxx x xxxxx xx xxxxxxxx v zadní xxxxxxx xxxxx xx xxxxxx xxx; tyto xxxx xxxx xxxxxx xxxxxxxx, xxxxx xxxx xxxxx vyloučeny x xxxxxxx x xxxxxx spotřebě; |
|
x) |
xxxxxxx naříznutí xxxxx xxx, aby xxxx xxxxxxxx obě xxxxxx a protnuta mezikomorová xxxxxxxx; |
|
x) |
xxxxxxxxxx x xxxxxxxxx xxxxx x xxxxxxx xxxxx xxxxx x xxxxxxxx xxxxxx (Lnn. xxxxxxxx); |
|
x) |
xxxxxxxxx xxxxxxx uzlin xxxxxxxxxxx x xxxxxxxxxxxxxxx; |
|
x) |
prohmatání sleziny; |
|
x) |
xxxxxxxxxx xxxxxx x xxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxx xxxxx (Xxx. xxxxxxx); |
|
h) |
xxxxxxxxx xxxxxxxxx xxxxxxx uzlin; |
|
i) |
xxxxxxxxxx krajiny xxxxxxx x xxxxxx mladých xxxxxx. V případě pochybností xx xxxxxxxx xxxxxxx xxxx řez x xxxxxxx xx i klouby; xxxx xxx xxxxxxxx xxxxxxx xxx; |
|
x) |
x xxxxxx xxxx rozříznutí xxxx xxxxxxx. |
Xxxxxx 23
Xxxxxx prasata
1. U jatečně xxxxxxxxxx xxx x xxxxx xxxxxxxx xxxxxx xx xxxxxxxx xxxx postupy prohlídky xx porážce:
|
a) |
xxxxxxxx xxxxxxxxx xxxxx a hrtanu; |
|
x) |
xxxxxxxx xxxxxxxxx xxxxx, xxxxxx x xxxxxx; |
|
c) |
xxxxxxxx xxxxxxxxx xxxx, průdušnice x xxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx osrdečníku x xxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx bránice; |
|
f) |
xxxxxxxx xxxxxxxxx xxxxx x xxxxxxx xxxxx xxxxxxxxx x xxxxxxxx xxxxxx (Xxx. xxxxxxxx); xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxxxxxxx xxxxxx, xxxxxx a mízních xxxxx xxxxxxxxxxx x xxxxxxxxxxxxxxx (Xxx. xxxxxxxx, xxxxxxxxxxx, xxxxxxxxx xx xxxxxxxx); |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxx; vizuální xxxxxxxxx xxxxxx; xxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx xxxxxxxxxx orgánů (xxxxx penisu, xxxxx xxx xxx xxxxxxxxx); |
|
i) |
xxxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxx xxxxx (Xxx. xxxxxxxxxxxxx); |
|
x) |
xxxxxxxx prohlídka xxxxxxx xxxxxxx x xxxxxx xxxxxxx xxxxxx. |
2. Xxxxxxxx-xx xxxxxx xxxxxxx xxxxxx xxx xxxxxx xxxxxx, xxxxxx xxxxxx xxxx xxxxx životní xxxxxxxx xxxxxx x xxxxxxx x xxxxxxx 24, xxxxxxx úřední xxxxxxxxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxx těla a drobů xxxx postupy xxxxxxxxx xx xxxxxxx:
|
x) |
naříznutí x xxxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx (Xxx. mandibulares); |
|
x) |
xxxxxxxxxx xxxx x xxxxxxx xxxxx bronchiálních x xxxxxxxxxxxxxxx (Xxx. xxxxxxxxxxxxx, xxxxxxxxxxxx xx xxxxxxxxxxxxx). Xxxxxxxxxx x xxx xxxxxxxx xx xxxxxxx xxxxxxxx xxxxx x xxxxx xx xxxxxxxx x xxxxx xxxxxxx xxxxx xx xxxxxx xxx; tyto xxxx xxxxxx nezbytné, xxxxx xxxx xxxxx xxxxxxxxx x xxxxxxx x xxxxxx xxxxxxxx; |
|
x) |
xxxxxxx xxxxxxxxx srdce tak, xxx byly xxxxxxxx xxx xxxxxx a protnuta xxxxxxxxxxxx xxxxxxxx; |
|
x) |
xxxxxxxxxx xxxxx x xxxxxx xxxxxxx uzlin; |
|
x) |
prohmatání x x xxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxxxxxxxx; |
|
x) |
xxxxxxxxxx sleziny; |
|
g) |
xxxxxxxxx xxxxxx x xxxxxxxxx mízních xxxxx (Xxx. xxxxxxx); |
|
x) |
naříznutí xxxxxxxxx xxxxxxx xxxxx; |
|
i) |
prohmatání xxxxxxx xxxxxxx a kloubů mladých xxxxxx x x xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx x xxxxxxxx xxxxxx. |
Xxxxxx 24
Xxxxxx možného xxxxxx xxx lidské xxxxxx, xxxxxx xxxxxx xxxx xxxxx xxxxxxx podmínky xxxxxx x xxxxxxxx xxxxx, xxxxxxxx ovcí x xxx, xxxxxxxx lichokopytníků x xxxxxxxx xxxxxx
Xxxxxx xxxxxxxxxxx xxxxx xxxxxxx xxxxx xxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxx x xx. 18 odst. 3, xx. 19 odst. 2, čl. 20 xxxx. 2, xx. 21 xxxx. 2, xx. 22 odst. 2 x xx. 23 xxxx. 2 prostřednictvím xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxx xxxx x xxxxx, pokud xxxxx jeho názoru xxxxxxx xxxxxxx x xxxxxx xxxxxxx xx xxxxxxxx xx xxxxx xxxxxx xxx xxxxxx zdraví, xxxxxx xxxxxx xxxx xxxxx xxxxxxx xxxxxxxx xxxxxx:
|
x) |
xxxxxxxx xxxxxxx provedené x xxxxxxx x xxxxxx 9 x 10 a analýza xxxxxx xxxxxxx; |
|
x) |
xxxxxxxx xxxxxxxxx před xxxxxxxx xxxxxxxxx x xxxxxxx x xxxxxxx 11; |
|
x) |
xxxxxxxx xxxxxxx souladu x xxxxxxxx xxx xxxxx xxxxxxx podmínky xxxxxx xxxxxxxxxxx xxxxx xxxxxx 38; |
|
d) |
zjištění xxxxxxxxx po porážce xxxxxxxxx x xxxxxxx s články 12 xx 24; |
|
e) |
xxxxx xxxxxxxxxxxxxxx xxxxx xxxx xxxx xxxxx z hospodářství xxxxxx xxxxxx. |
Xxxxxx 25
Xxxxxxxxx opatření xxxxxxxx xx prohlídky po xxxxxxx u drůbeže
1. U veškeré xxxxxxx xx xxxxxxx xxxxxxxxx xx xxxxxxx, xxxxx xxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx x xxxxxxx x xx. 18 xxxx. 3 nařízení (XX) 2017/625. V souladu x xx. 18 xxxx. 2 xxxx. x) xxxxxxxxx nařízení xxxxxxx xxxxxx veterinární xxxxx nebo xxxxxxx xxxxxx xxxxxxxxxxx pracovník xxxxxx xxxx xxxxxxxx:
|
x) |
xxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxx reprezentativního xxxxxx x xxxxxxx xxxxx; |
|
x) |
x xxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxx xxxx xxxxxx xxx xxxxx, xxxxx byly xx xxxxxxxxx xx xxxxxxx xxxxxxxxxx xx xxxxxxxx x xxxxxx xxxxxxxx; |
|
x) |
jakákoli xxxxx xxxxxxxx xxxxxxxxx, xxxxxxxx-xx xxxxx x xxxxxxxxx, xx xx maso z dotčených xxxxx xxxxx xxx xxxxxxxx k lidské spotřebě. |
2. Odchylně xx xxxxxxxx 1 xxxxx příslušné xxxxxx xxxxxxxxxx, xx se xxxxxxxxx po xxxxxxx xxxxxxx pouze x xxxxxxxxxxxxxxxxx xxxxxx xxxxxxx x xxxxxxx xxxxx, xxxxxxxx:
|
x) |
xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx mají xx xxxxxxxxxxxx úředního xxxxxxxxxxxxx xxxxxx zaveden systém, xxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx drůbeže, xxxxx vykazují xxxxxxxx, xxxxxxxxxxx xxxx vady; |
|
x) |
xxxxx xxxxxxxxxx dodržují xxxxxxxxx, xxxxx xxx x:
|
|
x) |
xxxxx xxxxxxxxx xxxx xxxxxxxx xxx xxx xxxxxxxxx xxxxxxxxx o potravinovém xxxxxxx xxxxxx xxxxxxxx xxxxx xxxxxxxx, xxxxx xxxxx xxxxxxxx na xxxxxxx problém xxx xxxxxx xxxxxx xxxx xxxxxx zvířat a které xx mohly xxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxxx 40 až 44. |
3. X xxxxxxx xxxxxxx xxxxxxx xxx výrobu jater xxxx gras x xxxxxxx xxxxxx x xxxxxxxxxx vykuchání, xxx xxxx xxxxxxx x xxxxxxxxxxxx xxxxxx x xxxxxxx x xxxxxxxx XXX xxxxxxx XX xxxxxxxxx XX xxxx 8 a 9 xxxxxxxx (XX) x. 853/2004, xx xxxxxxxxx xx xxxxxxx xxxxxxx x xxxxxxxx/xxxxxxxx, xxx se taková xxxxxxx upravená xxxx xxxxxxxxxx přímo x xxxxxxxxxxxx xxxxxx.
Xxxxxx 26
Xxxxxxxxx xxxxxxxx týkající xx xxxxxxxxx po xxxxxxx u farmových xxxxxxxxx
Na xxxxxxx xxxxxxxxx se xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx se prohlídky xx xxxxxxx xxxxxxx xxxxx xxxxxx 25. Ustanovení xxxxxx 25 xxxxxxxx xx xxxxxxx hejna drůbeže xx xxxxxxx xx xxxxxxx zajícovce xxxxxxxx xx stejný den x xxxxxxxxxxx z jednoho xxxxxxxxxxxx xxxxxx.
Xxxxxx 27
Xxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxxxx xx xxxxxxx x xxxxxxx zvěře
1. Xx xxxxxxxx zvěř se xxxxxxx tyto xxxxxxx xxxxxxxxx xx porážce:
|
x) |
x xxxxxxx xxxx xxxxx (< 100 kg) xxxxxx Cervidae (xxxxxxxxxx) xxxxxxx xx xxxxxxx xxx ovce xxxxxxxxx x xxxxxx 21; x xxxxxxx sobů xx xxxx xxxxxxx xxxxxxx xx xxxxxxx xxx xxxx xxxxxxxxx x xxxxxx 20, xxxxxxx xxxxx xxxx xxx xxxxxx x xxxxxx xxxxxxxx xxx xxxxxxxxx xxxxx; |
|
x) |
x xxxxxxx xxxxx xxxxxx Xxxxxx (xxxxxxxxxxx) xxxxxxx xx xxxxxxx xxx xxxxxx xxxxxxx xxxxxxxxx v článku 23; |
|
x) |
x xxxxxxx xxxxx xxxxx xxxxxx Xxxxxxxx (xxxxxxxxxx) x xxxx velké xxxxx, xx kterou xx xxxxxxxxxx písmeno x), a v případě velké xxxxx xxxxxx Suidae (xxxxxxxxxxx), xx xxxxxx xx nevztahuje xxxxxxx x), postupy po xxxxxxx pro skot xxxxxxxxx x xxxxxx 19; |
|
d) |
x xxxxxxx xxxxx xxxxxxx běžci xxxxxxx xx xxxxxxx xxx xxxxxx xxxxxxxxx v čl. 25 xxxx. 1. |
2. Xxxxx xxxx xxxxxxx xxxxxxxx mimo jatky, xxxxxx veterinární lékař xx xxxxxxx xxxxxxxxxxx xxxxxxxxx.
Xxxxxx 28
Xxxxxxxxx opatření xxxxxxxx xx xxxxxxxxx xx xxxxxxx x xxxxx xxxxxx xxxxx
1. Xxxxxx xxxxxxxxxxx xxxxx xxxxx, xx xxxxxxxxxx xxxxxx xxxxx xxxxxx xxxx xxxxxxxxxxxxx xx xxxxxxxx xxx xxxxxxxxx xx xxxxxxxx x xxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx o zdravotní xxxxxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxxx x xxxxxxx xxxxxxxx (XX) x. 636/2014 nebo xxxxxxxxxx podle xxxxxxx XXX xxxxxx XX xxxxxxxx XX bodu 8 xxxx. x) xxxxxxxx (XX) x. 853/2004. Xxxxxx xxxxxxxxxxx lékař xxxxxxxx xxxxx xxxxxx xxxxxxxxx nebo xxxxxx (xxxxxx) xxxxxxxxxx.
2. Xxx xxxxxxxxx xx porážce xxxxxxx xxxxxx veterinární xxxxx:
|
a) |
xxxxxxxx xxxxxxxxx xxxxxxx upraveného xxxx, xxxx tělních xxxxx a popřípadě xxxxxx x xxxxx:
|
|
x) |
xxxxxxxxx organoleptických xxxxxxxx; |
|
x) |
xxxxxxxx xxxxxxxxxx x xxxxxxxxx orgánů; |
|
x) |
xxxxxxxx-xx xxxxx xxxxxx x xxxxxxxxx xx xxxxxxxxxx reziduí xxxx xxxxxxxxxxxxxxx látek, xxxxxxx xxxxxxxxxx vzorků xxxxxxx nepocházejících x xxxx, xxxxxx látek znečišťujících xxxxxxx xxxxxxxxx. Xxxxx xx na základě xxxxxx xxxxxxxxx provádí xxxxxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxx xxxxx žijící xxxxx xxxxxxxx xxx xxxxxxxx xxxx xxxx xxxx částí, x xxxxx xx xxxxxxxxx xx xxxxx odchylky, a to xx do xxxxxxxx xxxx xxxxxxxxx; |
|
x) |
xxxxxxxxx xxxxxxxx xx xxxxx svědčící x xxx, xx xxxx xxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx:
|
3. Požaduje-li xx xxxxxx veterinární lékař, xxxxx a hlava se xxxxxxx xxxxxxx.
4. X xxxxxxx drobné xxxxx xxxxxx xxxxx, xxxxx nebyla xxxxxxxxx xxxxx xx xxxxxxxx, xxxxxxx xxxxxx veterinární xxxxx xxxxxxxxx po xxxxxxx u reprezentativního vzorku xxxxxx x xxxxx zdroje. Xxxxx xx xxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxx xx xxxxxxx xxxx některý xx xxxxx uvedených x xxxx. 2 xxxx. x), provede xxxxxx veterinární xxxxx xxxx xxxxxxx u celé xxxxx s cílem xxxxxxxx, xxx xxxx být xxxxxxxxxx xx xxxxxxxxx x xxxxxx spotřebě, nebo xxx xxxx xxx xxxxx jatečně xxxxxxxx xxxx xxxxxxxxxxx jednotlivě.
5. Xxxxxx xxxxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxx další xxxx x xxxxxxxxx xxxxxxxxxxx xxxxx zvířat, které xxxx xxxxxxxx pro xxxxxxxx xxxxxxx xxxxxxxx. Xxxxx xxxxxxxxx xxxxx xxxxxxx xx základě xxxxxxxxxxx xxxxxxxx uvedených x xxxxxxxx 2, xxxxxxxx xx další vyšetření x xxxxxxxxxx.
6. Xxxxx xxxxxxx xxxxxxxxxxx x xxxxxx 45 xx xx xxxxxxxx x xxxxxx spotřebě xxxxxxxx maso xxxxxxxxxx xxx xxxxxxxxx xx xxxxxxx xxxxxxx xx xxxxx uvedených v odst. 2 xxxx. x).
Xxxxxx&xxxx;29
Xxxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxx (XXX)
1.&xxxx;&xxxx;&xxxx;Xxxxx požadavků nařízení (XX) x.&xxxx;999/2001 ohledně xxxxxxxx xxxxxxx prováděných x&xxxx;xxxxxxxxxxx s TSE zkontroluje xxxxxx veterinární lékař xxxxxxxxxx, oddělení a případně xxxxxxxx specifikovaného xxxxxxxxxx xxxxxxxxx také xxxxx xxxxxxxx xxxxxxxxxxx v čl. 8 xxxx.&xxxx;1 xxxxxxxxx xxxxxxxx x&xxxx;x&xxxx;xxxxxx&xxxx;12 xxxxxxxx (XX) x.&xxxx;1069/2009 x&xxxx;xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx původu.
2. Úřední veterinární xxxxx xxxxxxx, xxx xxxxxxxxxxxx potravinářského xxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxx zamezit xxxxxxxxxxx masa specifikovaným xxxxxxxxx xxxxxxxxxx při xxxxxxx, xxxxxx omračování. Xx xxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxxxxxx rizikového xxxxxxxxx.
Xxxxxx 30
Xxxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxxxxx xxx xxxxxxxxx po xxxxxxx x xxxxxxxx skotu x xxxxxx Xxxxxx
1. Xxxxxxx prohlídky xx porážce popsané x xxxxxxxx 18, 19 x 23 xxxx minimálními xxxxxxxxx xx vyšetření xx xxxxxxxxxxxx u skotu x xxxxxx čeledi Suidae (xxxxxxxx xxxxxx, xxxxxxx xxxxx i volně xxxxxx xxxxx). X xxxxxxx xxxxx xxxxxxxxx v článku 19 xxxxx xxxxxxxxx orgány xxxxxxxxxx, xx xxxxxxxxx žvýkacích xxxxx xxx xxxxxxxxx xx porážce není xxxxxxx, xxxxx:
|
x) |
je prováděno xxxxxxxx xxxxxxxxxxx xxxxxxxxx; |
|
b) |
xxxxxxx xxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxx, xxxxx xx xxxxxxxxxx xx xxxxxx xxxxxx xxxxxxxxxxxx; xxxx |
|
x) |
xxxx x 95 % xxxxxxxx prokázáno, xx xxxxxxxxxx xx xxxxxxxx xxxxxxxx nebo xxxxxx xxxxxxxxxx xxxxxxxxxxx xx xxxxx xxx xxxxx xxxxxxxxxx, xxxx xxxxx na xxxxxxx xxxxx ze xxxxx xxxxxxxxxx xxxxx xx. 9 xxxx. 1 xxxxxxxx 2003/99/XX xxxxxx xxxx xxxxx xxxxxxx poraženými xx xxxxxxxxxx pět let (xxxx xx xxxxxxxx xxx xxxx, xx-xx xx podloženo x xxxxxxxxxx xxxxxxxx rizika xxxxxxxxxx xxxxxxxxxxx xxxxxx) xxxxxxxx xxxxx případy. |
2. Maso napadené xxxxxxxxxx xx xxxxxxxx xx xxxxxxxx x xxxxxx xxxxxxxx. Pokud xxxx xxxxx xxxx xxxxxxx xxxxxxxx cysticerky, xxxxx xxx xxxxxxxxxx xxxxx xxxxxxxxxx za xxxxxx x xxxxxx spotřebě xx xxxxxxxx chladem.
Xxxxxx 31
Xxxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxx xxx prohlídce xx xxxxxxx
1. Xxxxxxx xxxxxxxx xxxx xxxxxx čeledi Suidae (xxxxxxxxxxx), lichokopytníků a dalších xxxxx xxxxxxxxx x xxxxxxxxxxx xx xxxxxxx na xxxxxxxxxx xxxxxxxxx v souladu x xxxxxxxxx (XX) 2015/1375, xxxxx se xxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxxx x xxxxxx 3 uvedeného xxxxxxxx.
2. Xxxx xx xxxxxx xxxxxxxxxx xxxxxxxxxxxx se prohlásí xx xxxxxxxx k lidské xxxxxxxx.
Xxxxxx 32
Xxxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxx po xxxxxxx u lichokopytníků
1. Xxxxxxx xxxx xxxxxxxxxxxxxx se xxxxx xx trh pouze xxxxx, pokud bylo xxxxxxx x xxxxxxxxxxxxxx držených xx dobu xxxxxxx 90 dnů xxxx xxxxx xxxxxxx v členském xxxxx xxxx x xxxxx xxxx nebo xxxxxx xxxxxxx, xxxxx xx xxxxxxxx dovážet xxxxxxxxxxxxxx xx Xxxx.
2. V případě xxxxxxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxx státu xxxx xxxxx xxxx xxxx xxxxxxx, které xxxxxxxxx xxxxxxxx Xxxxxxx xxxxxxxxxx xxx xxxxxx xxxxxx xxx zemi xxxxxxx xxxxxxxxx, xx xxxxxxx vyšetření lichokopytníků xx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx, xxxxxx, xxxxxxx xxxxx x xxxxxxx dutin x xxxxxx větvení poté, xx xx xxxxx xxxxxxx xx střední xxxxxx a vyřízne xxxxx xxxxxxxx.
3. Xxxx xxxxxxx x xxxxxxxxxxxxxx, x xxxxx xxxx xxxxxxxxxxxxxxx xxxxxxxxx, xx prohlásí xx nevhodné k lidské xxxxxxxx.
Xxxxxx 33
Xxxxxxxxx xxxxxxxx xxx xxxxxx kontroly xxxxxxxxxxx xxx xxxxxxxxx po xxxxxxx
1. Xxxxx zvířata reagují xxxxxxxxx xxxx xxxxxxxxxx xx xxxxxxxxxx xxxx xxxxxxxx-xx jiné xxxxxx x xxxxxxxxx na xxxxxxx, xxxx xxxxxxxx xxxxxxxx xx ostatních zvířat, xxxxxxx se přijmou xxxxxxxxxxx opatření x xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx xxxxxxx upravených xxx, xxxxxxxxx linky a personálu xxxxxxxxxx xx xxxxxxx.
2. Veškeré xxxx xx zvířat, x xxxxx xxxx xxx xxxxxxxxx po porážce xx xxxx orgánech xxxx xx xxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxx xxxx xxxxxxx xxxxxxxxxxxxxx xxxxx, se prohlásí xx nevhodné x xxxxxx xxxxxxxx. Pokud xxxx xxxx tuberkuloidní xxxx xxxxxxxx x xxxxxxx xxxxxxxx xxxxx jednoho orgánu xxxx xxxxx jatečně xxxxxxxxxx xxxx, xxxxxxxx xx xx xxxxxxxx x xxxxxx xxxxxxxx pouze xxxxxxxxx orgán nebo xxxxxxxxx xxxx xxxxxxx xxxxxxxxxx xxxx x xxxxxxxxx xxxxx xxxxxx.
Xxxxxx 34
Xxxxxxxxx opatření pro xxxxxx xxxxxxxx xxxxxxxxx xxx xxxxxxxxx xx xxxxxxx
1. Xxxxx zvířata reagují xxxxxxxxx xxxx xxxxxxxxxx xx xxxx na xxxxxxxxx nebo existují-li xxxx xxxxxx k podezření xx xxxxxxx, jsou xxxxxxxx odděleně od xxxxxxxxx xxxxxx, xxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxx k zamezení xxxxxx xxxxxxxxxxx jiných xxxxxxx xxxxxxxxxx xxx, xxxxxxxxx xxxxx a personálu xxxxxxxxxx xx xxxxxxx.
2. Xxxx xx xxxxxx, x xxxxxxx xxxx xxx xxxxxxxxx xx xxxxxxx xxxxxxxx xxxx xxxxxxxxxxxx akutní xxxxxxxxx, xx xxxxxxxx xx xxxxxxxx x xxxxxx xxxxxxxx. X xxxxxx reagujících xxxxxxxxx xxxx xxxxxxxxxx xx xxxx na brucelózu xx xxxxxx, pohlavní xxxxxxx a krev xxxxxxxx xx nevhodné k lidské xxxxxxxx, x xxxx xxxxxx xxxx nejsou xxxxxxxx.
Xxxxxx 35
Xxxxxxxxx xxxxxxxx xxx xxxxxx xxxxxxxx salmonel
1. Xxxxxxxxx xxxxxx xxxxx, xxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx přílohu X xxxxxxxx 2 xxxx 2.1.3, 2.1.4 a 2.1.5 xxxxxxxx (ES) č. 2073/2005, xxxxxxx použijí xxxxxxx xxxxx x xxxxxx opatření:
|
a) |
xxxxxx xxxxx xxxxxx xx xxxxxxx xxxxxx metody x xxxxxx xxxxxx, xxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx. Xx xxxxxxx xxxxxxx xx xxxxxxxxxx xxxxxxx xxxxxxx 49 xxxxxxxxx xxxxxx (40). U malých xxxxx xxx xxxxx xxxxx xxxxxx snížit xx xxxxxxx xxxxxxxxx xxxxx; |
|
x) |
xxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxx vzorků x xxxxx vzorků xxxxxxxxxxx xx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxx xxxxxx 5 xxxxxxxx (XX) x. 2073/2005 v rámci xxxxxxx X xxxxxxxx 2 xxxx 2.1.3, 2.1.4 x 2.1.5 uvedeného xxxxxxxx; |
|
x) |
xxxx xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxx vzorků x xxxxx xxxxxx xxxxxxxxxxx xx xxxxxxxxx xxxxxxxxxx v rámci xxxxxxxxxxxxxx xxxxxxxxxxx programů x xxxxxxxxx xxxxxxx nebo xxxxxxxxx xxxxxxxxx států, xxx xxxxx xxxx xxxxxxxxx xxxxxxxx záruky x xxxxxxx x xxxxxxx 8 xxxxxxxx (XX) x. 853/2004, xxxxx xxx x xxxxxxxx xxxx xxxxxxxxxxx a koňského, xxxxxxxxx x xxxxxxxxx xxxx. |
2. Xxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx několikrát xxxxxxx kritérium hygieny xxxxxxxxx xxxxxxx, xxxxxxxxx xxxxxx mu xxxxx, xxx xxxxxxxxx xxxxx xxxx, x xxxxxxxx xxxxxxxxx xx jeho xxxxxxxx.
3. X xxxxxxxx xxxxx vzorků x xxxxx xxxxxx xxxxxxxxxxx na xxxxxxxxx xx podá xxxxxx v souladu x xx. 9 xxxx. 1 směrnice 2003/99/XX, xxxxxxx xx xxxxxxxxx xxxx vzorky xxxxxxxxxx xxxxx odst. 1 písm. x), x) x x), xxxx-xx xxxx xxxxxxx xxxxxxx.
Xxxxxx 36
Xxxxxxxxx xxxxxxxx pro xxxxxx xxxxxxxx xxxxxxxx xxxx Xxxxxxxxxxxxx
1. Příslušné orgány xxxxx, zda xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxxxx X xxxxxxxx 2 bod 2.1.9 (xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxx Xxxxxxxxxxxxx xx jatečně xxxxxxxxxx xxxxxx xxxxxxxx) xxxxxxxx (XX) č. 2073/2005, xxxxxxx xxxxxxx xxxx xxxxxxxx:
|
x) |
xxxxxx xxxxx xxxxxx za xxxxxxx stejné xxxxxx x xxxxxx xxxxxx, jaké xxxxxxxxx provozovatelé xxxxxxxxxxxxxxx xxxxxxx. Xx každých xxxxxxx xx každoročně xxxxxxx xxxxxxx 49 xxxxxxxxx vzorků. U malých xxxxx xxx xxxxx xxxxx xxxxxx xxxxxx xx xxxxxxx xxxxxxxxx xxxxx; nebo |
|
b) |
sběr xxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxx xxxxxx x xxxxx vzorků xxxxxxxxxxx xx Xxxxxxxxxxxxx, xxxxx obsahují xxxx xxx 1 000 XXX/x, xxxxxxxxxx provozovateli xxxxxxxxxxxxxxx xxxxxxx xxxxx xxxxxx 5 xxxxxxxx (XX) x. 2073/2005 x xxxxx přílohy I kapitoly 2 xxxx 2.1.9 xxxxxxxxx nařízení. |
2. Xxxxx provozovatel xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx, xxxxxxxxx xxxxxx xx uloží, xxx předložil akční xxxx, x xxxxxxxx xxxxxxxxx xx jeho xxxxxxxx.
3. X xxxxxxxx xxxxx xxxxxx a počtu xxxxxx xxxxxxxxxxx xx Xxxxxxxxxxxxx, které xxxxxxxx xxxx než 1 000 XXX/x, xx xxxx xxxxxx x xxxxxxx x xx. 9 xxxx. 1 xxxxxxxx 2003/99/XX, xxxxxxx xx xxxxxxxxx xxxx xxxxxx xxxxxxxxxx xxxxx xxxx. 1 xxxx. x) a b), jsou-li xxxx xxxxxxx použita.
Xxxxxx 37
Xxxxxxxx xxxxxxxxx týkající xx xxxxxxxxxxxxx xxxxx
1. Při xxxxxxxxx xxxxxxxxxxxxx xxxxx x xxxxxxx s čl. 18 xxxx. 2 xxxx. d) xxxx xx) a iv) xxxxxxxx (XX) 2017/625 xxxxxx xxxxxxxxxxx xxxxx xxxxxxx, xxx v případě, xx xx xxxxxxxx xxxxx xxxxxx, byly xxxxxx xxxxx xxxxxxxx, bylo x xxxx xxxxx xxxxxxxxxxxx x xxxx odeslány xx xxxxxxxxx xxxxxxxxxx x xxxxx:
|
x) |
xxxxxxxxx x xxxxxxx xxxxxx x xxxxxx xxxxxxx; |
|
x) |
xxxxxxx xxxxxxxx xxxxxxx xxx XXX x xxxxxxx x xxxxxxx 6 nařízení (XX) x. 999/2001; |
|
x) |
xxxxxxx farmakologicky účinných xxxxx xxxx xxxxxxxxx, xxxxx xxxx zakázané xxxx nepovolené, a kontrol xxxxxxxxxxxx xxxxxxxxxxxxxx účinných xxxxx, xxxxxxxxx, xxxxxxxxxxx xxxxx v krmivech a kontaminujících xxxxx v množství xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx Xxxx, xxxxxxx x xxxxx xxxxxxxxxxxxxx xxxxx pro xxxxxxxxxx xxxxxxx xxxx xxxxx xxxxxxxxx x xx. 110 xxxx. 2 xxxxxxxx (XX) 2017/625 x xxxxxx 5 směrnice 96/23/XX; |
|
x) |
xxxxxxx xxxxx xxxxxx, xxx xxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxx (XX) 2016/429. |
2. Xxxxxx xxxxxxxxxxx lékař xxxxxxx, xxx xxxx xxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxx xxxxx xxxxxxxxxx xx xxxxxxxx xxx xxxxxxx xxxxxxxxxx xxxxx xx. 18 xxxx. 2 xxxxxxxx (XX) 2017/625.
Článek 38
Úřední xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxx xxx xxxxxxxx x&xxxx;xxxxxxx
Xxxxxx xxxxxxxxxxx xxxxx xxxxx xxxxxx x&xxxx;xxxxxxxx xxxxxxxxxx xx ochrany xxxxxx xxxxx přepravy xxxxx xxxxxxxx (ES) x.&xxxx;1/2005 x&xxxx;xxx xxxxxxx xxxxx nařízení (XX) x.&xxxx;1099/2009 x&xxxx;x&xxxx;xxxxxxxxxxxxxx pravidly xxx dobré xxxxxxx xxxxxxxx xxxxxx.
XXXXXXXX III
Sdělování výsledků xxxxxxxxx x&xxxx;xxxxxxxx, xxxxx xxxx příslušné xxxxxx xxxxxxxx ve xxxxxxxxxx xxxxxxxxx xxxxxxxxx s požadavky xx xxxxxxx xxxx x&xxxx;xx xxxxx životní xxxxxxxx xxxxxx
Článek 39
Opatření xxxxxxxx xx xxxxxxxxx xxxxxxxx úředních xxxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxx lékař xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx provedených x&xxxx;xxxxxxx x&xxxx;xxxxxx 7 xx 38.
2.&xxxx;&xxxx;&xxxx;Xxxxx xx při xxxxxxxxxxx xxxxxx nákaza xxxx xxxx, xxxxx xx xxxxx mít xxxx xx xxxxxx xxxxxx nebo xxxxxx xxxxxx nebo xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxx, xxxxxx xxxxxx xxxxxxxxxxx xxxxx tato xxxxxxxx:
|
x) |
xxxxxx xxxxxxxxxxx lékař xxxxxxxxx xxxxxxxxxxxxx xxxxx; |
|
x) |
xxxxx xxxxxxx uvedený v tomto xxxxxxxx xxxxxx xxxxx xxxxxxxxxx x&xxxx;xxxx xx xxxxxxxx xxxxxx, xxxxxx xxxxxx, xxxxxxx životních xxxxxxxx xxxxxx, xxxxxxx xxxxxxxxxxxxx léčivých xxxxxxxxx, xxxxxxxxxxxx nebo xxxxxxxxxx xxxxx, reziduí pesticidů, xxxxxxxxxxx xxxxx xxxx xxxxxxxxxxxxxxx látek, úřední xxxxxxxxxxx lékař xxxxxxxxx:
|
|
x) |
xxxxx xxxx dotčená xxxxxxx odchována x&xxxx;xxxx xxxx, xxxxxx xxxxxxxxxxx xxxxx xxxxxxx, xxx xxxx informovány xxxxxxxxx xxxxxx této xxxx. |
3.&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxx kontrol xxxxxxxxx xxxxxx xxxxxx xx xxxxxxxxxx xxxxxxxx, xxxxxxxxxxxx x&xxxx;xxxxxxxxx, xxx je xxxxxxxxxxxxx xxxxxx informací xxxxxxxxxx xxxxx článku 4 xxxxxxxx 2003/99/XX, xxxxxx&xxxx;8 xxxxxxxx Xxxx 64/432/XXX&xxxx;(41) x&xxxx;xxxxxxx XXX xxxxxxxx 2007/43/XX.
4.&xxxx;&xxxx;&xxxx;Xxxxx xx xxxxxx xxxxxxxxxxx xxxxx xxx xxxxxxxxx xxxx xxxxxxxx xxxx xx xxxxxxx xxxx xxx xxxxxxxx xxxx úřední kontrole xxxxxxxxx xx výskyt xxxxxx xxxxxx, xxx xxx jsou stanovena xxxxxxxxxxx xxxxxxxx v nařízení (XX) 2016/429, oznámí xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx. Úřední veterinární xxxxx a příslušné xxxxxx x&xxxx;xxxxx xxxxx příslušných xxxxxxx působnosti přijmou xxxxxxx xxxxxxxx preventivní x&xxxx;xxxxx xxxxxxxx x&xxxx;xxxxx xxxxxxx možnému šíření xxxxxxx nákazy.
5. Pro xxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxx x&xxxx;xx porážce xxxxxxxxxxxx xxxxxx, xxx xxxx xxxxxxx xxxxxxx před xxxxxxxx, může úřední xxxxxxxxxxx xxxxx xxxxxx xxxx xxxxxxxxx xxxxxxx x&xxxx;xxxxxxx X.
6.&xxxx;&xxxx;&xxxx;Xxxxx xxxx xxxxxxx chována v hospodářství xxxxxx x&xxxx;xxxxx xxxxxxxx xxxxx, xxxxx příslušné xxxxxx xxxxxxxxx xxxxx, xx xxxxxx xxxx xxxxxxxx, xxxxxxxxxx výsledky xxxxxxxxx xxxx porážkou x&xxxx;xx xxxxxxx xxxxxxxxxx xxxxxxx členského státu xxxxxx. Při xxx xxxxxxx xxxx dokumentu xxxxxxx x&xxxx;xxxxxxx I v úředních xxxxxxxx obou xxxxxxxxxxxx xxxxxxxxx států nebo x&xxxx;xxxxxx xxxxxxxxxx xxxx xxxxx členskými xxxxx.
Xxxxxx 40
Xxxxxxxx x xxxxxxxxx xxxxxxxxx x xxxxxxxxx na xxxxxxxxx x xxxxxxxxxxxx řetězci
1. Xxxxxx xxxxxxxxxxx xxxxx zajistí, xxx xxxxxxx xxxxxx xxxxxxxx, xxxx xx provozovatel xxxxx xxxxxxx, xxxxxxxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx x xxxxxxx x xx. 9. odst. 2 písm. x) x x).
2. Xxxxxxxx xx xxxxxxxx 1 může xxxxxx xxxxxxxxxxx lékař xxxxxxx, xxx xxxx xxxxxxx xxxxxxxx xx xxxxxxx, jestliže příslušné xxxxxxxxx o potravinovém xxxxxxx xxxxxx x xxxxxxxxx. X xxxxxxxx xxxxxxxxx xx tyto xxxxxxxxx xxxxxx xxxx xxx, než xx xxxx xxxxxxxxxx za xxxxxx x xxxxxx spotřebě, x xx doby xxxxxx xxxxxxxxxx se jatečně xxxxxxxx těla x xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxx xx ostatního masa.
3. Xxxxx xxxxxxxxx xxxxxxxxx o potravinovém xxxxxxx xxxxxx x xxxxxxxxx xx 24 xxxxx xx xxxxxxxxx zvířete xx xxxxx, xxxxxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxxxx xxxx x xxxxxx zvířete xx xxxxxxxx x xxxxxx xxxxxxxx. Jestliže xxxxx xxxxx xxxxxx xxxxxxxx, xxxxxx se xxxxxxxx xx xxxxxxxxx xxxxxx, xxxxxxx se xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxx zdraví xxxxxx a lidského zdraví.
Xxxxxx 41
Xxxxxxxx x xxxxxxxxx nesouladu xxxxxxxxxxxxx v informacích o potravinovém xxxxxxx
1. Xxxxxx veterinární xxxxx xxxxx, xxx xxxxxxxxxxxx xxxxx xxxxxxxxx xxxxxxx x xxxxxxx, jestliže x xxxxxxxxx x xxxxxxxxxxxx xxxxxxx nebo xxxxxx xxxxxxxxxxxx záznamů, xxxxxxx xx xxxxxxxxx xxxxxxx, xx:
|
a) |
xxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxx xxxx xxxxxxx, na xxxxx xx xxxxxxxx xxxxx xxxxxxxxxxxx zvířat xxxx xxxx omezení x xxxxxx xxxxxxxxxx xx zdraví xxxxxx xxxx xxxxxxxx xxxxxx; |
|
x) |
xxxxxx xxxxxxxx pravidla xxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxx ošetřena xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxx xxxx xxxxxx dodrženy xxxxxxx xxxxxx xxx xxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxxxxxxxxx xxxxx; xxxx |
|
x) |
xxxxxxxx jiné xxxxxxxxx, xxxxx xxxxx nepříznivě xxxxxxxx xxxxxx zdraví xxxx xxxxxx xxxxxx. |
2. Xxxxx xxxx xxx zvířata xx xxxxxxx, xxxxxx xx xxxxxxxx x xxxxxxxx xx xx xxxxxxxx x xxxxxx xxxxxxxx, xxxxxxx xx přijmou preventivní xxxxxxxx x xxxxxxx xxxxxx xxxxxx x xxxxxxxx xxxxxx. Xxxxx xx úřední xxxxxxxxxxx lékař považuje xx xxxxxxxx, xxxxxxxx xx x xxxxxxxxxxxx xxxxxx xxxxxx kontroly.
Xxxxxx 42
Xxxxxxxx v případech xxxxxxxxxxxx xxxxxxxxx o potravinovém xxxxxxx
1. Příslušné xxxxxx přijmou vhodná xxxxxxxx, xxxxx xxxxxx, xx xxxxxxxxxx záznamy, xxxxxxx xxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxx xxxxx xxxxxx nebo xxxx xxxxxxx xxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx v omyl.
2. Xxxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx odpovědnému xx xxxxxxxxxxxx původu xxxxxx xxxxxx xxxx xxxxxxxx xxxx zúčastněné osobě, xxxxxx provozovatele xxxxx. Xxxx opatření mohou xxxxxxxx zejména x xxxxxxxxxxx xxxxxxxxxx. Xxxxxxx xx xxxx xxxxxxxxx xxxxxxxx xxxx provozovatel potravinářského xxxxxxx xxxxxxxxx za xxxxxxxxxxxx xxxxxx nebo xxxxxxxx xxxx zúčastněná xxxxx.
Xxxxxx 43
Xxxxxxxx x xxxxxxxxx xxxxxxxxx x xxxxxxxxx na xxxx xxxxxxx
1. Xxxxxx xxxxxxxxxxx lékař xxxxx, xxx xxxxxxxxxxxx xxxxxxxxxxxxxxx podniku xxxx xxxx xxxxxxxxx xxxxx xxxxxxx III xxxxxx X xxxxxxxx XX xxxx 3 xxxxxxxx (ES) x. 853/2004, xxxx zajišťuje, xxx xxxx zvířata xxxxxxxxx x xxxxxxx xxx xxxxxxx spotřebu xxxxx xxxxxxxxxxxxxx. Xxxxxx xxxxxxxxxxx xxxxx xxxxxxx, xxx xxxxxxx, xxxxxxx xxxxxxxx xxxx xxxxxxxxxxx, xxxx xxxxxxxx xxxxxxxx x xxxxxxxxxx xx xxxxxxxx k lidské xxxxxxxx. Pokud xx xxxxxx xxxxxxxxxxx xxxxx xxxxxxxx xx xxxxxxxx, xxxxxxxx se x xxxxxxxxxxxx xxxxxx xxxxxx xxxxxxxx.
2. Xxxxxx xxxxxxxxxxx xxxxx xxxxxxx, xxx xxxxxxx, kterých xx xxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxx xxxxx xxxxxxx, xxx xx xxxxxxxxx x xx. 11 xxxx. 4, xxxxxx porážena x xxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxx.
3. Xxxxxx xxxxxxxxxxx xxxxx xxxxxxx, xxx xxxxxxx, jejichž xxxxxx xxxx patologický xxxx xxxxx být xxx xxxxxxxxxx s masem xxxx xxx xxxx xxxxxxxxx xxxxxxxxx na xxxxxxx xxxx xxxxxxx, a obecně xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx choroby xxxx xxxxxxxxxx či xxxxxxxx xxxx xxxx xxxxxxxxxxx xxxxxxxxxx xxxx x xxxxxx spotřebě xxxxxx xxxxxxxx x xxxxxx xxxxxxxx. Xxxxxx xxxxxxx se xxxxxx odděleně xx xxxxxxxx xxxxxxxx, xxx xxxxxxx xxxxx xx xxxxxxxxxxx jiných zvířat xxxx jatečně xxxxxxxxxx xxx, a prohlásí xx xx xxxxxxxx k lidské xxxxxxxx.
4. Xxxxxx xxxxxxxxxxx xxxxx xxxxxx xxxxxxx xxxxxx, x xxxxx existuje xxxxxxxxx xx xxxxxx xxxx xxxx, xxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxx xxxxxx nebo xxxxxx xxxxxx. X xxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx x xxxxx xxxxxxxx xxxxxxxx. Vedle xxxx xxxx xxxxxx xxxxxxxxxxx lékař xxxxxxxxxx, xx prohlídka xx xxxxxxx musí xxx xxxxxxxx xxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxxxxxx. Xxxxx xx to nezbytné x xxxxxxxx kontaminace xxxxxx xxxx, xxxxxxx xx xxxxxx xxxxxxxx nebo xx xxxxx xxxxxxxx xxxxxxx, xxxxxxx se xxxxxxx xxxxxxx další xxxxxxxx xxxxxxxx.
5. Xxxxxx xxxxxxxxxxx xxxxx zajistí, xxx xx xxxxxxx, xxxxx xxxxx xxxxxxxxx rezidua xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx účinných xxxxx, xxxxxxxxx nebo xxxxxxxxxxxxxxx xxxxx x xxxxxxxx překračujícím xxxxxx xxxxxxxxx x xxxxxxx x xxxxxxxx předpisy Xxxx, xxxx xxxxxxxx v souladu x xxxxxx 16 xx 19 xxxxxxxx 96/23/XX.
6. Xxxxxx xxxxxxxxxxx lékař xxxxxxx xxxxxxxx, za xxxxxxx xx xx xxxx xxxxxxx xxxxxxx xxxxxxx xx zvířaty v rámci xxxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxx xxxxxxx xxxxxxxxx xxxxxx, xxxxxxxxx xxxxxxxxx nebo xxxxxxxxxxx, xxxx xxxxxxx zoonóz, xxxx xxxx xxxxxxxxx. Xxxxxxxxx xxxxxx xxxxxxx xxxxxxxx, xx nichž xxxxx xxx taková xxxxxxx xxxxxxxx. Xxxx xxxxxxxx jsou určeny x xxxxxxxxxxxx xxxxxxxxxxx jiných xxxxxx a masa xxxxxx xxxxxx.
Xxxxxxx, xxxxx jsou xxxxxxxxx x xxxxxxx xx xxxxx, se xx xxxx zpravidla xxxx xxxxxx. Xx xxxxxxxxxxx xxxxxxxxx, například xxxxx xxxxx xx xxxxxxxx xxxxx k vážné poruše, xxxx může úřední xxxxxxxxxxx xxxxx xxxxxxx xxxxx xxxxxx xx xxxx xxxxx.
Xxxxx je xxx xxxxxxxxx před xxxxxxxx x xxxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx, který xxxx k riziku xxx xxxxxx xxxxxx, lidské xxxxxx xxxx xxxxx xxxxxxx podmínky xxxxxx, xxxxxx veterinární xxxxx xxxxxxxx přepravu xxxxxx xx xxxxx x xxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx x xx. 39 xxxx. 2 xxxx. x) body i) x xxx).
Xxxxxx 44
Xxxxxxxx v případech xxxxxxxxx x xxxxxxxxx na xxxxx xxxxxxx podmínky zvířat
1. V případech xxxxxxxxx x xxxxxxxx xxx xxxxxxx xxxxxx xxx xxxxxxxx nebo xxxxxxxxxx xxxxxxxxxxx v článcích 3 xx 9, 14 xx 17, 19 x 22 xxxxxxxx Rady (XX) x. 1099/2009 xxxxxx xxxxxxxxxxx xxxxx xxxxx, xxx xxxxxxxxxxxx potravinářského xxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx opatření x xxxxxxxx xxxx, aby xx tyto xxxxxxx xxxxxxxxx.
2. Xx xxxxxx k donucovacím xxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx xxxxx přiměřený x xxxxxxxxxxxx xxxxxxx, xx xxxxxxxx xxxxxx xx xx xxxxxxxxx a zastavení xxxxxxxx, podle xxxxxx x xxxxxxxxxx xxxxxxxx.
3. O problémech xxxxxxxxxx xx dobrých xxxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx xxxxx ve xxxxxxxx případech informuje xxxxxxx xxxxxxxxx xxxxxx.
4. Pokud xxxxxx xxxxxxxxxxx xxxxx xxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxx xx ochrany xxxxxx xxxxx přepravy, xxxxx jsou xxxxxxxxx x xxxxxxxx (ES) č. 1/2005, xxxxxx nezbytná xxxxxxxx x xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx Unie.
5. Xxxxx xxxxxxx xxxxxx veterinární pracovník xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx zvířat x xxx nich xx xxxxxx xxxxxxxx s pravidly xxx ochranu zvířat, xxxxxxxxxx x xxx xxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx. Xx-xx xx v naléhavých xxxxxxxxx xxxxxxxx, přijímá xx do příchodu xxxxxxxx xxxxxxxxxxxxx lékaře xxxxxxxx xxxxxxxx xxxxx xxxxxxxx 1 xx 4.
Xxxxxx 45
Xxxxxxxx x xxxxxxxxx xxxxxxxxx x xxxxxxxxx na xxxxxxx xxxx
Xxxxxx xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx maso xx xxxxxxxx x xxxxxx xxxxxxxx, xxxxxxxx:
|
x) |
xxxxxxx xx xxxxxx, x xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx x xxxxxxx x xx. 18 xxxx. 2 písm. x) xxxx b) xxxxxxxx (XX) 2017/625, x xxxxxxxx xxxxx xxxxxx zvěře x xxxxxxxxx sobů xxxxxxxxx x xx. 12 xxxx. 1 xxxx. x) nařízení x xxxxxxxxx xxxxxxxxx (EU) 2019/624; |
|
x) |
pochází xx zvířat, jejichž xxxxx nebyly xxxxxxxxx xxxxxxxxx xx xxxxxxx x xxxxxxx s čl. 18 xxxx. 2 xxxx. x) xxxxxxxx (XX) 2017/625, x xxxxxxxx xxxxxxx vnitřností velké xxxxx xxxxxx xxxxx, xxxxx xxxxxx xxxx xxxxxxxxxx do xxxxxxxx xxx xxxxxxxxx xx xxxxxxxx x xxxxxxx x xxxxxxxx XXX oddílem XX xxxxxxxxx XX xxxxx 4 xxxxxxxx (ES) x. 853/2004; |
|
x) |
xxxxxxx ze zvířat xxxxxxxxx xxxx xxxxxxxx, xxxxx xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxx nebo xxxxxx, xxxxx byla xxxxxxxx xx xxxxx xxx xx xxxxxxxx; |
|
x) |
xx xxxxx x xxxxxxxxx xxxx x xxxxx xxxxxxxx (xxxxxx xxxx); |
|
x) |
xxxxxxx xx zvířat xxxxxxxxxxx xxxxxxxx zvířat, xxx něž xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxx předpisech Xxxx x xxxxx xxxx xxxxxxx x xxxxxxx x xxxxxxx X xxxxxxxx 2002/99/XX, x xxxxxxxx případů, xxx xx xxxx xxxxxxx x xxxxxxx xx xxxxxxxxxx xxxxxxxxx stanovenými x xxxxxxx xxxxxxxx; tato xxxxxxx xx nepoužije, xxxxx požadavky na xxxxxx xxxxxxxx tuberkulózy x xxxxxxxxx podle článků 33 x 34 xxxxxx xxxxxxxx xxxxxxx xxxxx; |
|
f) |
pochází xx xxxxxx postižených xxxxxxxxxxxxxxx xxxxxxx, např. xxxxxxxx xxxxxxxxxx, xxxxxx, toxémií xxxx xxxxxxx; |
|
x) |
xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxx X xxxxxxxx X xxxxxxxx (XX) č. 2073/2005 xxx xxxxxxxxxxx, zda xxxxx xxx xxxxxxxxx xxxxxxx xx xxx; |
|
h) |
xxxxxxxx napadení xxxxxxxx, xxxx-xx v požadavcích xx xxxxxx xxxxxxxx xxxxxxxxxxxx xxxxx článku 30 xxxxxxxxx xxxxx; |
|
x) |
xxxxxxxx xxxxxxx xxxxxxxxxx látek xxxx xxxxxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxx x xxxxxxxxxx (XX) x. 37/2010, (XX) x. 396/2005, (ES) x. 1881/2006 x (XX) č. 124/2009 xxxx rezidua xxxxx, xxxxx xxxx xxxxxxxx xxxx nepovolené xxxxx xxxxxxxx (XX) č. 37/2010 xxxx xxxxxxxx 96/22/ES; |
|
j) |
xx xxxxx x xxxxx a ledviny xxxxxx xxxxxxxx xxxx xxx, která xxxxxxxxx x xxxxxxx, v nichž byla xxx xxxxxxxxx plánů xxxxxxxxxxx xxxxx xxxxxx 5 xxxxxxxx 96/23/XX xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxx xxxx x xxxxxxxx prostředí; |
|
x) |
xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxxx; |
|
x) |
xxxx xxxxxxxxx ošetřeno xxxxxxxxxxx xxxxxxx, xxxxxx XX xxxxxx; |
|
m) |
xxxxxxxx xxxxxxxx xxxxxx xxxxx loveckého xxxxxxxxx x xxxxx xxxxxx xxxxx; |
|
x) |
xx x xxx překročena xxxxxxxx povolená xxxxxx xxxxxxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxx Xxxx nebo, x xxxxxxx xxxxxxxxxxx právních xxxxxxxx Unie, ve xxxxxxxxxxxxxx předpisech; |
|
x) |
vykazuje xxxxxxxxxxx xxxx xxxxxxxxxxxxxx xxxxx, xxxxxxx xxxxxxx xxxxxxxx xxxx xxxx xxxxxxxxxxxx xxxxxxxx (xxxxx xxxxx xxxxxx zvěře); |
|
x) |
xxxxxxx x xxxxxxxxx (xxxxxxxxxxxxx) zvířat; |
|
q) |
xxxxxxxx xxxxxxxxxxxxx xxxxxxxx materiál, xxxxx xxxx xxxxxxxx xxxx xxxxxxxxxxxx v jiném provozu xxxxx xxxxxxx X xxxx 4.3 nařízení (XX) x. 999/2001, a čerstvé xxxx xxxxxxxxx xxx xxxxxxxx xxxxxxxxxxx xxxxxx; |
|
r) |
xx xxxxxxxxxx xxxx xxxxxxxx fekální xx xxxxx kontaminaci; |
|
x) |
se xxxxx x xxxx, která xxxx xxxxxxxxxxxx xxxxxx xxx xxxxxx xxxxxx xxxx zdraví xxxxxx x xxxxxxxx xxxxxxxxxx statusu xxxxxxx, xx xxxxxxx xxxxxxx, xxxx v důsledku xxxxxxxxxxx xxxxx xxxxxxx; |
|
t) |
xxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx, xxxxxxxxxx xx xxxxxxxxxxx všech příslušných xxxxxxxxx, xxxx představovat xxxxxx pro lidské xxxxxx xxxx zdraví xxxxxx nebo xx x xxxxxx xxxxxx xxxxxxxx x xxxxxx xxxxxxxx; |
|
u) |
xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxx s články 29 xx 36. |
Xxxxxx 46
Xxxxxxxx v případech nesouladu x xxxxxxxxx xx xxxxxxxx xxxxxxxxxxx xxxxx
1. Xxxxxxxxx orgány xxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxx, xxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx, včetně snížení xxxxxxxxx porážení, xxxxx xx přítomný úředník xxxxxxxx xx xxxxxxxx x xxxxxx případech:
|
a) |
xxxxx je xxxxxxxx xxxxxxxxxxx na xxxxxxx xxxxxxx jatečně xxxxxxxxxx xxxx xxxx x xxxx xxxxxxx xxxxxxxx x xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx opatření x xxxxxxx xxxxxxx; xxxx |
|
x) |
pokud xx xxxxxxxxx orgány xxxxxxxxx, xx xx xxxxxxxx správná xxxxxxxxxx xxxxx. |
2. X xxxxxx xxxxxxxxx zvýší xxxxxxxxx orgány xxxxxxxxx xxxxxxxx do doby, xxx xx xxxxxxxxx, xx provozovatel xxxxxxxxxxxxxxx xxxxxxx xxxxx xxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxxx.
XXXXXXXX IV
Omezení
Xxxxxx&xxxx;47
Xxxxxxx xxx některé xxxxxxx xxxx
Xxxxxx xxxxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxxx xxxx xx xxxxxx, která:
|
a) |
byla nuceně xxxxxxxx xxxx xxxxxxx xxxxx; nebo |
|
b) |
pocházejí x&xxxx;xxxx, x&xxxx;xxxxxxx xx xxxx xxxxxxxx masa xx xxx xxxxxxxxx xxxxxxxx xxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxx XX částí X xxxxxxxx (XX) x.&xxxx;2160/2003. |
KAPITOLA X
Xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx masa vhodného x&xxxx;xxxxxx xxxxxxxx po xxxxxxxxx xxxx porážkou x&xxxx;xx xxxxxxx
Xxxxxx&xxxx;48
Xxxxxxxxx xxxxxxxxx na značku xxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxx xxx xxxx xxxxxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxxxx veterinární xxxxx xxxxxxx xx označování xxxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx xxxxxx.
2.&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxx lékař xxxxxxx xxxxxxx, xxx:
|
x) |
xxxxxx xxxxxxxxx xxxxxxxxxxxx xxxx xxxxxxx pouze x&xxxx;xxxxxxx xxxxxxxx kopytníků x&xxxx;xxxxx xxxxxxx zvěře xxxxx xxxxxxxxx, u kterých xxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx x&xxxx;xx porážce, x&xxxx;x&xxxx;xxxxxxx xxxxx xxxxx xxxxxx xxxxx, u které xxxx xxxxxxxxx xxxxxxxxx xx porážce, x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;18 xxxx.&xxxx;2 xxxx. x), x) a c) xxxxxxxx (EU) 2017/625, xxxxx neexistují xxxxxx x&xxxx;xxxxxxxxxx xxxx xx xxxxxxxx x&xxxx;xxxxxx spotřebě. Xxxxxx však xxx xxx umístěna xxxx xxx, xxx jsou x&xxxx;xxxxxxxxx xxxxxxxx případných xxxxxxxxx xx trichinely x/xxxx xxxxx xx XXX, xxxxx xxxxxxxxx xxxxxx zavedly xx xxxxxxx xxxx x&xxxx;xxxxxxxx xxx nakládání xx xxxxxxxx xxxxxx xxxxxxxxxxx, xxx xxxxxxx xxxxx xxxxxxx xxxx možné xxxxxxxxxx a aby xxxxx xxxxx vyšetřovaných xxxxxx xxxxxxxx značkou neopustily xxxxx xxxx zařízení xxx xxxxxxxxx se xxxxxxxx, dokud xxxx xxxxxxx negativní xxxxxxxx, x&xxxx;xxxxxxxx případů xxxxxxxxxxx x&xxxx;xxxxxxx s čl. 2 xxxx.&xxxx;3 xxxxxxxx (XX) 2015/1375; |
|
b) |
značka xxxxxxxxx nezávadnosti byla xxxxxxxx na vnější xxxxxx xxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxx inkoustovým xxxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx, xxx x&xxxx;xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx těla xx xxxxxxx xx xxxxxxx půlky nebo xxxxxx xxxx při xxxxxxxxxxxx xxxxxxx xxxxx xx tři xxxx xxxx každý x&xxxx;xxxx xxxxxx zdravotní xxxxxxxxxxxx. |
3.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxx xxxxxxx, xxx xxxxxxxxx opatření xxx xxxxxx zdravotní nezávadnosti xxxx uplatňována x&xxxx;xxxxxxx x&xxxx;xxxxxxxx XX.
4.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxx xxxxxxx, xxx xxxx x&xxxx;xxxxxxxxx xxxxx xxxxxx xxxxx xxxxxx označeno xxxxxxx xxxxxxxxx xxxxxxxxxxxx, xxxxx xx xxxxxxx x&xxxx;xxxxxxxx xxx nakládání xx zvěřinou nepodstoupilo xxxxxxxxx po xxxxxxx x&xxxx;xxxxxx xxxxxxxxxx xx xxxxxx k lidské xxxxxxxx.
HLAVA XX
XXXXXXXX XXXXXXXXX X&xxxx;XXXXXXXX XXXXXXXXX XXXXXXX XXXXXXXX KONTROL U SYROVÉHO XXXXX, MLEZIVA, XXXXXXXX XXXXXXX X&xxxx;XXXXXXX X&xxxx;XXXXXXX XXXXXXXX X&xxxx;XXXXXX XX XXXXXXXX XXXXXXXX XXXXXXXXX X&xxxx;XXXXXX
Xxxxxx&xxxx;49
Xxxxxxxx zemědělských xxxxxxx xxxxxxxx x&xxxx;xxxxxxxx mléka x&xxxx;xxxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxxxxx lékař xxxxx, xxx jsou xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xx produkci syrového xxxxx x&xxxx;xxxxxxx xxxxxxxxx x&xxxx;xxxxxxx III oddíle XX kapitole I části X&xxxx;xxxxxxxx (XX) č. 853/2004. Xxxxxx veterinární xxxxx xxxxxxx xxxxx:
|
x) |
xxxxxxxx status xxxxxx; |
|
x) |
xxxxxxx použití xxxxxxxxxx xxxx nepovolených farmakologicky xxxxxxxx xxxxx; x |
|
x) |
xxx xxxxxxxx přítomnost xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxx, xxxxxxxxx xxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxx (XX) x.&xxxx;37/2010, (XX) x.&xxxx;396/2005 nebo (XX) x.&xxxx;1881/2006. |
2.&xxxx;&xxxx;&xxxx;Xxxxxx xxxxxxxx xxxxxxx x&xxxx;xxxxxxxx 1 xxxxx xxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx prováděných xxxxx xxxxxxxx Unie x&xxxx;xxxxxx xxxxxx, xxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx.
3.&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxxx xxxxxx x&xxxx;xxxxxxxxx, že xxxxxxxxxx xxxxxxxxx xxxxxxx x&xxxx;xxxxxxxx 1 xxxxxx xxxxxxxx, xxxxxx veterinární xxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxx xxxx xxxxxx.
4.&xxxx;&xxxx;&xxxx;X&xxxx;xxxxxxxxxxxx xxxxxxxxx určených x&xxxx;xxxxxxxx xxxxx a mleziva provádějí xxxxxxxxx orgány úřední xxxxxxxx x&xxxx;xxxxx xxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx XXX xxxxxx XX xxxxxxxx X&xxxx;xxxxx XX xxxxxxxx (XX) x.&xxxx;853/2004. Xxxx xxxxxxxx xxxxx zahrnovat xxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx. Xxxxx xx xxxxxxx, xx hygiena xx xxxxxxxxxxxx, xxxxxxxxx orgány xxxxx, xxx xxxx xxxxxxxxxx xxxxxx kroky x&xxxx;xxxxxxx situace.
Xxxxxx 50
Xxxxxxxx mléka x xxxxxxx
1. X xxxxxxx xxxxxxxx mléka x xxxxxxx xxxxxxxxx orgány monitorují xxxxxxxx xxxxxxxxx v souladu x xxxxxxxx XXX xxxxxxx XX kapitolou X xxxxx XXX xxxxxxxx (XX) x. 853/2004. Provádějí-li xx xxxxx, xxxxxxx příslušné xxxxxx xx xxxxxx xxxxxxxx souladu s limity, xxxxx xxxx xxx xxxxxx xxxxx x xxxxxxx xxxxxxxxx x xxxxxxx III xxxxxx IX xxxxxxxx X xxxxx III xxxxxxxx (XX) x. 853/2004, analytické xxxxxx xxxxxxxxx x xxxxxxx XXX xxxxxx nařízení.
2. Xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxx xx xxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxx xx xxx xxxxxx xxx xxx, xxx bylo xxxxxxxxxx xxxxxxx poprvé xxxxxxxx xxxxxxxxxx kritérií xxx xxxxx xxxxxxxxxxxxxx a/nebo xxxxxxxxxxx buněk x xxxxxxx xxxxx x xxxxxxx, příslušné xxxxxx xxxxx, že:
|
x) |
xxxxxxx xxxxxxxx mléka a mleziva x xxxxxx xxxxxxxxxxxx xxxxxxx xxxx xxxxxxxxxxx; xxxx |
|
b) |
xxxxxx xxxxx x xxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxx xx xxxxxx xxxxxx xxxxxxxx x xxxxxxx a jsou xxxxxxxx xxx xxxxxxx xxxxxxxx xxxxxx, v souladu se xxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx xxxx xxxxxx xxxxxxxx pokyny. |
Xxxx xxxxxxxxxxx xxxx xxxx požadavky xxxxxxxxx xxxxxxxxx orgány x xxxxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx neprokáže, xx xxxxxx xxxxx x xxxxxxx xxxx splňují xxxxxxx kritéria.
3. Xx xxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx x xxxxxxx XXX xxxxxx IX xxxxxxxx XX xxxxx XX xxxxxxxx (ES) x. 853/2004 xxxxxxx příslušné xxxxxx xxxxxxxxxx metody xxxxxxxxx x xxxxxxx XXX xxxxxx xxxxxxxx.
HLAVA X
XXXXXXXX POŽADAVKY XX ÚŘEDNÍ XXXXXXXX X&xxxx;XXXXXX XXXX X&xxxx;XXXXXXXXXXXXXXX&xxxx;XXXXXXXXXXX&xxxx;X&xxxx;XXXXXXXXXXX XXXXXXX
Xxxxxx&xxxx;51
Xxxxxxxxx
Xxxx xxxxx xx xxxxxxx xx xxxx xxxx. Xxxxxxx xx xxxx xx živé xxxxxxxxxx, xxxx pláštěnce x&xxxx;xxxx xxxxxx xxxx. Xxxx hlava xx xxxxxxxxx xx xxxx xxxxxx plže x&xxxx;xxxx xxxxxxxxx třídy Xxxxxxxxxxxxx (xxxxxx), kteří nezískávají xxxxxxx xxxxxxxx vody.
Xxxxxx 52
Xxxxxxxxxxx produkčních a sádkovacích xxxxxxx pro živé xxxx
1. Xxxxxxxxx xxxxxx xxxxxxx xxxxxx x xxxxxxx produkčních x xxxxxxxxxxx xxxxxxx, které xxxxxxxxxxx x xxxxxxx s čl. 18 xxxx. 6 nařízení (EU) 2017/625. Ve vhodných xxxxxxxxx xxx xxxxx xxxxxx xx xxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx.
2. Produkční x xxxxxxxxx oblasti, x xxxxx xxxxxxxx sběr xxxxxx xxxx, příslušné xxxxxx xxxxxxxxxxx xxxxx xxxxxx xxxxxxx xxxxxxxxxxx jako xxxxxxx třídy X, xxxxxxx xxxxx B x xxxxxxx xxxxx X. Xx xxxxxxxx xxxxxxxxx xxx xxxxx xxxxxx xx xxxxxxxxxx s provozovatelem xxxxxxxxxxxxxxx xxxxxxx.
3. Xx xxxxxx xxxxxxxxxxx xxxxxxxxxxx a sádkovacích xxxxxxx stanoví xxxxxxxxx xxxxxx období přezkumu xxx údaje xxxxxxx x xxxxxx vzorků z každé xxxxxxxxx a sádkovací oblasti x xxxxx zjistit xxxxxx x xxxxxxx xxxxxxxxx x xxxxxxxx 53, 54 x 55.
KAPITOLA X
Xxxxxxxx xxxxxxxxx xx xxxxxxxxxxx produkčních x&xxxx;xxxxxxxxxxx xxxxxxx pro xxxx xxxx
Článek 53
Požadavky xx xxxxxxx xxxxx X
1.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxx mohou xxxxxxxxxxxx xxxx oblasti xxxxx X&xxxx;xx xxxxxxx, xx xxxxxxx xxxxx xxx živí xxxx xxxxxxx k přímé lidské xxxxxxxx.
2.&xxxx;&xxxx;&xxxx;Xxxx xxxx xxxxxxx xx trh x&xxxx;xxxxxx xxxxxxx musí splňovat xxxxxxxxxx xxxxx xxx xxxx xxxx stanovené x&xxxx;xxxxxxx XXX xxxxxx XXX xxxxxxxx X&xxxx;xxxxxxxx (XX) č. 853/2004.
3. V případě xxxxxx xxxxxx mlžů x&xxxx;xxxxxxx xxxxx X&xxxx;xxxxx xxx x&xxxx;80&xxxx;% vzorků odebraných xxxxx období přezkumu xxxxxxxxxx xxxxxxx 230 X. coli xx 100&xxxx;x xxxxxxxxx x&xxxx;xxxxxxxx xxxx xxxxxxxxx.
4.&xxxx;&xxxx;&xxxx;X&xxxx;xxxxxxxxxxx 20 % xxxxxx xxxxx xxx xxxxxxxxxx xxxxxxx 700 X. xxxx xx 100&xxxx;x xxxxxxxxx x&xxxx;xxxxxxxx xxxx xxxxxxxxx.
5.&xxxx;&xxxx;&xxxx;Xxx xxxxxxxxx xxxxxxxx xx stanovené xxxxxx přezkumu xxx xxxxxxxxx xxxxxxx xxxxx X&xxxx;xxxxx xxxxxxxxx xxxxxx xx základě posouzení xxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxxxxx, xx xxxxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx 700 X. coli xx 100&xxxx;x xxxxxxxxx a tekutiny xxxx lasturami.
Xxxxxx 54
Xxxxxxxxx xx oblasti xxxxx X
1. Xxxxxxxxx xxxxxx xxxxx xxxxxxxxxxxx xxxx xxxxxxx xxxxx X xx xxxxxxx, xx xxxxxxx xxxxx xxx xxxx xxxx xxxxxxx, xxxxxxx mohou xxx xxxxxxx xx xxx x xxxxxx xxxxxxxx xx xx xxxxxxxx xx xxxxxxxxx pro xxxxxxx xxxx xx xxxxxxxxx xxx, xxx xxxxxxxxx xxxxxxxxxx xxxxx uvedené x xxxxxx 53.
2. X xxxxxxx živých mlžů x xxxxxxx xxxxx X xxxxx xxx x 90 % xxxxxx překročena xxxxxxx 4 600X. xxxx xx 100 x xxxxxxxxx x xxxxxxxx xxxx lasturami.
3. U zbývajících 10 % xxxxxx nesmí xxx xxxxxxxxxx hodnota 46 000X. xxxx xx 100 x xxxxxxxxx a tekutiny mezi xxxxxxxxx.
Xxxxxx 55
Xxxxxxxxx xx xxxxxxx xxxxx X
1. Xxxxxxxxx xxxxxx xxxxx xxxxxxxxxxxx xxxx xxxxxxx třídy X xx oblasti, xx xxxxxxx mohou xxx xxxx xxxx xxxxxxx, xxxxxxx xxxxx xxx xxxxxxx xx xxx xx po dlouhodobém xxxxxxxxx xxx, xxx xxxxxxxxx xxxxxxxxxx normy xxxxxxx x xxxxxx 53.
2. X xxxxxx mlžů x xxxxxxx třídy X xxxxx být xxxxxxxxxx xxxxxxx 46 000X. xxxx xx 100 g xxxxxxxxx x xxxxxxxx xxxx xxxxxxxxx.
Xxxxxx 56
Xxxxxxxxx xx sanitární xxxxxxx
1. Xxxx xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx oblasti xxxxxxxx příslušné xxxxxx xxxxxxxxx průzkum, xxxxx xxxxxxxx:
|
x) |
xxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxx nebo xxxxxxxxxxx původu, xxxxx xx mohly xxx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx; |
|
x) |
xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxx uvolňovaných x xxxxxxx xxxxxxxx roku x xxxxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxx x xxxxxxx xxxxxxxx v povodí, xx xxxxxxxx, xxxxxxx xxxxxxxxx xxx xxx.; |
|
x) |
xxxxxxxxx charakteristik xxxxxxxxx xxxxxxxxxxxxxx xxxxx xx základě xxxxx xxxxxx, xxxxxxxxxxx xxxxxx x xxxxxxxxxxx xxxxx x xxxxxxxxx xxxxxxx. |
2. Xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx v odstavci 1 xxxxxxxx příslušné xxxxxx ve všech xxxxxxxxxxxxxxx xxxxxxxxxxx a sádkovacích xxxxxxxxx, xxxxx v nich xxxxx xxxxxxxx xxxxx.
3. Příslušným xxxxxxx xxxxx být xx xxxxxxxx, xxxxx xxxx xxxxxx stanoví x xxxxxxxxxxx s prováděním xxxxxx xxxxxxxx, nápomocny xxxxx xxxxxx xxxxxxxx nebo xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků.
Xxxxxx 57
Xxxxxxx xxxxxxxxxxxx
Příslušné orgány xxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxx oblastí xxxxxx xxxx, xxxxx xx xxxxxxx xx přezkumu xxxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxx 56. Xxxxx vzorků, xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxx a četnost xxxxxx x xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxxxx výsledků xxxxxxx xxx xxxxxxxx xxxxxx.
Xxxxxx 58
Xxxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxxxxxxxx, xxx xxxxxxxxx xxxxxxx xxxxxxx x xxxxxx 56 a program xxxxxxxxxxxx xxxxxxx v článku 57 byly xxxxxxxxxxxxxxx pro xxxxx xxxxxx.
XXXXXXXX XX
Xxxxxxxx xxx xxxxxxxxxxxx xxxxxxxxxxxxxxx produkčních x&xxxx;xxxxxxxxxxx xxxxxxx xxx xxxx xxxx
Xxxxxx&xxxx;59
Xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxx a sádkovacích xxxxxxx
Xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx produkční x&xxxx;xxxxxxxxx xxxxxxx xxxxxxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xx.&xxxx;18 xxxx.&xxxx;6 xxxxxxxx (XX) 2017/625 x&xxxx;xxxxx xxxxxxxxxxxx:
|
x) |
xxxxxxx xxxxxxxxx ohledně xxxxxx, provenience x&xxxx;xxxxx xxxxxx xxxxxx xxxx; |
|
x) |
xxxxxxxxxxxxxxxx xxxxxx xxxxxx xxxx xx xxxxxx xx xxxxxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx; |
|
x) |
xxxxxx xxxxxxxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx oblastí x&xxxx;xxxxxxxx xxxxxxxxx x&xxxx;xxxxxx xxxxxx; |
|
x) |
xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxx x&xxxx;xxxxxx xxxxxx. |
Xxxxxx 60
Xxxxxx xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxx xxxxxx
1. Xx účelem xxxxxxxx xxxxxxxxxx limitů stanovených x xxxxxxx XXX xxxxxx XXX xxxxxxxx V bodě 2 xxxxxxxx (ES) x. 853/2004 x xxxxxxxx xx xxxxxx ověření xxxxxxxxxx xxxxxxxx xx strany xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx orgány xxxxxxxxxx xxxxxx stanovené x xxxxxxx V. X xxxxxxx xxxxxxx xxxx xxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx.
2. X xxxxxxx s článkem 4 xxxxxxxx 2010/63/XX se xxxxxxx xxxxxxx xxxxxxxxxx v čl. 3 xxxx. 1 uvedené směrnice xxxxx možno xxxxxxx xxxxxxx xxxxxxxxxx xxxxxx xx xxxxxxxx strategie, xxx xxx se xxxxxxxxxxx živá zvířata.
3. X xxxxxxx x xxxxxxx 4 směrnice 2010/63/EU xxxx xxx xxx xxxxxxx biologických xxxxx xxxx xxxxxx na xxxxx nahrazení x xxxxxxx xxxxxxxxx xxxxxx a šetrné xxxxxxxxx x xxxx.
Xxxxxx 61
Xxxxx xxxxxx xxxxxx
1. Xxx xxxxx xxxxxxx stanovených x xx. 59 písm. b), x) x x) xxxxxxxxx xxxxxxxxx orgány xxxxx xxxxxx xxxxxx, xxxxx xxxxx se xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxx případ od xxxxxxx, jsou-li období xxxxx xxxxxxxxxxxx. Xxxxxxxxx xxxxxxxxx odběrových xxxx x xxxxxxx odběru xxxxxx xxxxxxx, xxx xxxxxxxx xxxxxxx byly reprezentativní xxx dotčenou xxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxx oblast.
2. X xxxxxxx xxxxxx vzorků xxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxx mlžů xx xxxxxxxxx xxxxxxx k:
|
a) |
xxxxxxxxxxxxxxx xxxxxxxx xxxxxxx kontaminace; |
|
x) |
xxxxxxxxxx xxxxxxxx v čl. 56 odst. 1. |
3. V plánech xxxxxx xxxxxx xxx xxxxxxxx xxxxxxx toxinogenního xxxxxxxxx xx xxxx x xxxxxxxxxxxxxxx xxxxxxxxxxx a sádkovacích xxxxxxxxx x xxxxxxxx xxxxxxxxx x xxxxxx mlžích xx xxxxxxxxx zejména x xxxxxxx xxxxxxxx xxxxxxx planktonu xxxxxxxxxxxx mořské biotoxiny. Xxxxx vzorků xxxxxxxx:
|
x) |
xxxxxxxxxx xxxxx xxxxxx xx xxxxxxxxxx změn xx xxxxxxx planktonu xxxxxxxxxxxx xxxxxx x xxxx xxxxxxxxxxx xxxxxxxxx. Pokud xxxxxxxx xxxxxx x xxxxxxxxx xxxxxx xx xxxxxxxxx xxxxxx xxxx, xxxxxxxxx xxxxxxxxxx xxxxx xxxxxx; |
|
b) |
pravidelné xxxxxxx xxxxxxxx xxxxxxxxxxx živé xxxx xx xxxxxxxx xxxxxxx, kteří xxxx xxxxxxxxxxxxx na kontaminaci. |
4. Xxxxxxx xxxxxx xxxxxx xxx xxxxxxx xx toxiny x xxxxxx mlžích xx x xxxxxxxx sběru xxxxxxx x xxxxxxxx xxxxxxx, xxx:
|
x) |
lze xxxxxxx xxxxxx xxxxxx x xxxxxxxx xxxxxxxxxxxxxxx sádkovacích xxxx produkčních xxxxxxxxx xxxx u určitých xxxxx xxxxxx mlžů xxxxxx, xxxxx z posouzení xxxxxx xxxxxxx xxxxxx xxxx xxxxxxxxxxxxx xxxxxxx velmi xxxxx xxxxxx xxxxxxxxx xxxxxx; |
|
x) |
xx xxxxxxx odběru xxxxxx xxxxx, xxxxx x xxxxxxxxx xxxxxxxxx xxxxxxx, xx xxxxxxx odběr xx xxx nedostatečný. |
5. Xxxxxxxxx xxxxxx xxxxxxx v odstavci 4 xx xxxxxxxxxx xxxxxxxxxxx x xxxxx xxxxxxxx xxxxxx xxxxxxx xxxxxx x xxxxxx mlžích x xxxxxx xxxxxxx.
6. Xxxxx xx xxxxx xxxxxxxx akumulace toxinů xxx xxxxxxx xxxxxxx xxxxx xxxxxxxx v téže xxxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxx, může xxx xxxx x xxxxxxxx xxxxxxxxx xxxxxx jako xxxxxxxxxxxx xxxx. Xx xxxxxx využívání všech xxxxx xx skupině, xxxx-xx hladiny toxinů x xxxxxxxxxxxxx xxxxx xxxxx xxx regulační xxxxxx. Xxxxx xxxxxxx toxinů x xxxxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx limity, xxx xxx xxxx xxxxxx xxxxx xxxxxxx xxxxx xxxxx, pokud xxxxx xxxxxxx xxxxxx xxxxxx xxxxx xxxxxx xxxxxxx xxxxxx nižší xxx xxxxxxx xxxxxx.
7. Xxxxx xxx x xxxxxxxxxxxx planktonu, jsou xxxxxx xxxxxxxxxxxxxxx xxx xxxxx xxxxxxx v klasifikované xxxxxxxxx xxxx xxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxx druhů x x xxxxxxxxxxx trendech. Jsou-li xxxxxxxx xxxxx x xxxxxxxxx xxxxxxxxxx, xxxxx xxxxx xxxx x xxxxxxxxx xxxxxx, xxxxxxx xxxxxx xxxxxx x xxxxxx mlžů xx xxxxx nebo xx xxxxxxx preventivně uzavřou, xxxxx xxxxxxx xxxxx xxxxxxxx xxxxxxx xx xxxxxx.
8. Xxxxx odběru xxxxxx xxx xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxxx xxxxxxx jakékoli xxxxxxxxxx xxxxxx stanovených x xxxxxxxx (XX) x. 1881/2006.
XXXXXXXX III
Řízení xxxxxxxxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx xx xxxxxxxxxxxx
Xxxxxx&xxxx;62
Xxxxxxxxxx xx základě xxxxxxxxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxxx x&xxxx;xxxxxxxx monitorování stanoveného x&xxxx;xxxxxx&xxxx;59 vyplývá, xx xxxxxx xxxxxxxxxx hygienické xxxxx xxx xxxx xxxx nebo xx xxxxxx zdraví xxxx xxx xxxxxxxx jiným xxxxxxxx, uzavřou xxxxxxxxx xxxxxx dotčenou xxxxxxxxxxxxxx xxxxxxxxx xxxx sádkovací xxxxxx a zabrání sběru xxxxxx xxxx. Jestliže xxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx kritéria xxxxxxxxx x&xxxx;xxxxxxxx 54 x&xxxx;55 x&xxxx;xxxxxxxxxxxxx xxxxx xxxx xxxxxx pro xxxxxx xxxxxx, xxxxx xxxxxx xxxx xxxxxxxxxxx na xxxxxx xxxxx X xxxx X.
2.&xxxx;&xxxx;&xxxx;Xxxxx výsledky xxxxxxxxxxxxxxxxx xxxxxxxxxxxx ukážou, xx xxxxxx splněny xxxxxxxxxx xxxxx pro xxxx mlže xxxxxxx x&xxxx;xxxxxx&xxxx;53, xxxxx příslušné xxxxxx xx základě xxxxxxxxx xxxxxx x&xxxx;xxxxx xxxxxxx a jednorázově povolit xxxxxxxxxxx xxxxx bez xxxxxxxx xx xxxxx xxxxxxxxxxx za xxxxxx xxxxxxxx:
|
x) |
xxxxxxx klasifikovaná produkční xxxxxx x&xxxx;xxxxxxx schválené xxxxxxx přijímající xxxx xxxx z této xxxxxxx xxxx xxx xxxxxxx xxxxxxxx xxxxx příslušných xxxxxx; |
|
x) |
xx dotčené živé xxxx xx vztahují xxxxxxxxxxxx xxxxxxxxx opatření, xxxx xx čištění, xxxxxxxxx xxxx xxxxxxxxxx. |
3.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxx o registraci uvedený x&xxxx;xxxxxxx XXX oddíle XXX kapitole I nařízení (XX) č. 853/2004 xxxx xxxxxxxxx xxxxxxx informace xxxxxxxx xx xxxxxxxxxxx xxxxxxxx 2.
4.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxx xxxxxxx podmínky, xx xxxxxxx xxx xxxxxx xxxxxxxx 2, xxx xxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxx&xxxx;53.
Xxxxxx 63
Xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx
1. Xxxxxxxxx xxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxx xxxxx xxxxxxx xxxxx tehdy, xxxxx xxxxxxxxxx xxxxxxxx pro xxxx mlže xxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx XXX oddílu XXX xxxxxxxx X xxxxxxxx (XX) č. 853/2004 x xxxxxxxxxxxxx xxxxx xxxx riziko xxx xxxxxx zdraví.
2. Pokud xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxx sádkovací xxxxxx x xxxxxx xxxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxx x xxxxxx mlžích, xxxxx překračuje xxxxxxxxx xxxxx xxx xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxx XXX oddíle XXX xxxxxxxx X xxxx 2 xxxxxxxx (XX) x. 853/2004, xxxxx xx xxxxx xxxxxxx xxxxx xxxxx, xxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxx xx xxxx jdoucích xxxxxx xxxxxxxxxxx x xxxxxxx xxxxxxx 48 xxxxx xxxxx xxx xxxxxxxxx limit.
3. Xxx xxxxxxxxxxx x xxx, xxx xxxxxxxxx xxxx xxxxxxxxx xxxxxx xxxxx xxxxxxx, xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx x xxxxxxxxxx o vývoji xxxxxxxxxxxxx.
4. Xxxxx existují xxxxxxxxxx xxxxx x xxxxxxxx toxicity x xxxx xxxxxxx x xxxxx xxxx k dispozici xxxxxxx xxxxx o klesajících xxxxxxxx xxxxxxxx, xxxxx xxxxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxxxxxxx xxxxxxx xx xxxxxxx xxxxxxxx x xxxxxxxx odběru xxxxxx, xxxxx jsou xxxxx xxx xxxxxxxxx xxxxx xxxxxxx x xxxxxxx XXX xxxxxx XXX xxxxxxxx X xxxx 2 xxxxxxxx (XX) č. 853/2004.
Xxxxxx 64
Xxxxxxxxx xxxxxx
1. Xxxxxxxxx orgány xxxxxxx xxxxxxxxx systém xxxxxxxxxxx, xxx xx xxx xxxxxx xxxxxxx xxxxxxxx živočišného xxxxxx, xxxxx jsou xxxxxxxx xxx xxxxxx zdraví. Xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxx, xxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx ve xxxxx xxxxxx xxxxxxxx, xxxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxx, xxxxxx živých xxxx x xxxxxxxxx z nich xxxxxxxxxx xxxxxxxx.
2. Xxxxx kontrolním xxxxxxxx xx x xxxxxxxxxxx případech xxxxx, xx hladiny xxxxxxxx biotoxinů a kontaminujících xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx x xx mikrobiologická xxxxxx mlžů xxxxxxxxxxxxx xxxxxxxxx xxx xxxxxx xxxxxx.
Xxxxxx 65
Xxxxxxxxxx xxxxxxxxxxx xxxxxx
1. Příslušné xxxxxx xxxxxxx xxxxxxxxxx, xxxxxxxx xx nutné xxxxxxxxx xxxxxx xxxxxxx xxxx xxxx xxxxxxxxxxxx xxxx xx xxx xxxxx xxxxxxx nebo xxxxx xx u živých xxxx xxxxxxxxx xxxxxxxx xxxxxxx v čl. 62 odst. 2.
2. Xxx xxxxxxxxxxx x xxxxxxxxxxx, xxxxx xxxxxxxxxxx, otevření nebo xxxxxxxx produkčních xxxxxxx x xxxxxxx x xxxxxx 52, 62 x 63 mohou xxxxxxxxx xxxxxx přihlédnout x xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx podniků xxxx organizacemi, které xx xxxxxxxxx, pouze x xxxxxxx, že xxxxxxxxx xxxxxxxxxxx xxxxxxx xxxx xxxxxx příslušnými xxxxxx x xxxxx xxxxxx x xxxxxxx xx xxxxxxxxx v souladu x xxxxxxxxxx, xx němž xx xxxxxxxxx xxxxxx x xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxx xxxxxxx xxxxxxxxxx xxxxxxxx dohodli.
XXXXXXXX IV
Další xxxxxxxxx
Xxxxxx&xxxx;66
Xxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxxxxx
Xxxxxxxxx orgány:
|
a) |
vypracují a aktualizují xxxxxx xxxxxxxxxxxxxxx produkčních x&xxxx;xxxxxxxxxxx xxxxxxx, v nichž xxxxx xxx xxxxxxx xxxx mlži v souladu x&xxxx;xxxxxxxxx xxxxxx&xxxx;52, x&xxxx;xxxxxxxxxx xxxxx o jejich poloze x&xxxx;xxxxxxxxx a o jejich xxxxxxxxxxx xx xxxx. Xxxxx xxxxxx se předá xxxxxxxxxxx xxxxxxx dotčeným xxxxx nařízením, například xxxxxxxxxxx a provozovatelům xxxxxxxxx xxx xxxxxxx a expedičních xxxxxxxxx; |
|
x) |
xxxxxxxxxx informují zúčastněné xxxxxx, xxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxxxxxx středisek xxx xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxx, x&xxxx;xxxxxxxxx změnách xxxxxx, xxxxxx xxxx xxxxx xxxxxxxxx xxxxxxx, x&xxxx;xxxxx xxxxxxxx xxxx xxxxxxx xxxxxxxx nebo x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxx v čl. 60 xxxx.&xxxx;2. |
HLAVA XX
XXXXXXXX POŽADAVKY X&xxxx;XXXXXXXX XXXXXXXXX XXXXXXX XXXXXXXX XXXXXXX X&xxxx;XXXXXXXX XXXXXXXX
Xxxxxx&xxxx;67
Xxxxxx xxxxxxxx produkce x&xxxx;xxxxxxx xx xxx
Xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx x&xxxx;xxxxxx uvádění xx trh xxxxxxxx xxxxxxxxx souladu x&xxxx;xxxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx XXX xxxxxx XXXX nařízení (XX) č. 853/2004, xxxxxxx:
|
x) |
xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx a prvního xxxxxxx; |
|
x) |
xxxxxxxxxx xxxxxxxx xxxxxxxx a provozů xx pevnině, xxxxxx xxxxxx xxx a velkoobchodních xxxx, při xxxxx xx zejména xxxxxxxxxx:
|
|
c) |
kontroly skladovacích x&xxxx;xxxxxxxxxxx xxxxxxxx. |
Xxxxxx 68
Xxxxx xxxxxxxxx xxxxxxxx xxxxxxx
1. Xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx příslušné xxxxxx xxxxx xxxxxx xxxxxxxx x xxxxxxxx x xxxxxxxx xxxxx. Xxxx kontroly xx xxxxxx všech plavidel xxxxxxxxxxxxx xxxxxxxx rybolovu x xxxxxxxxxx XX xxx xxxxxx na xx, xxx jakou vlajkou xxxxx.
2. Xxxxxxxxx xxxxxx státu xxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxx jejich xxxxxxx xxxxxxxx, když xx xxxxxxxx xx xxxx xxxx x xxxxxxxx x xxxxx xxxxxxxx státě xxxx x xxxxx zemi.
Xxxxxx 69
Xxxxxxxxxxx zpracovatelských, xxxxxxxxxxxxx xxxx chladírenských plavidel
1. Xx-xx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxxx, xxxxxxxxxxxxx xxxx xxxxxxxxxxxxxx xxxxxxxx plujícího xxx xxxxxxx xxxxxxxxx xxxxx x xxxxx udělit xxxxxxxxx xxxxxxxx, provedou xxxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxx kontroly x xxxxxxx x xxxxxxx 148 xxxxxxxx (XX) 2017/625, xxxxxxx x xxxxxxx xxxxxxxxx x xx. 148 xxxx. 4. X xxxxxxx xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxx, xxxx xx xxxxxxxx xx xxxx xxxx v přístavu x xxxxx xxxxxxxx státě xxxx x xxxxx xxxx.
2. Xxxxx xxxxxxxxx xxxxxx xxxxxxxxx státu xxxxxx udělily xxxxxxxx xxxxxxx schválení x xxxxxxx x xxxxxxx 148 nařízení (XX) 2017/625, xxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxx xxxx xxxxx země, aby xxxxxxxx xxxxxxxx kontroly xx xxxxxx udělení xxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxx schválení xxxx xxxxxxxxxxx schválení; v případě xxxxx země však xxxx xxx x xxxx, xxxxx xx xxxxxxx x xxxxxxx xxxxxxx zemí, x xxxxx xx povolen xxxxx xxxxxxxx xxxxxxxx, x xxxxxxx x xxxxxxx 127 nařízení (XX) 2017/625. X xxxxxxx xxxxxxx xxxxx xxxx xxxxxxxxx xxxxxx provést xxxxxxxx xxxxxxxx, když xx xxxxxxxx na xxxx nebo x xxxxxxxx x xxxxx xxxxxxxx xxxxx xxxx x xxxxx zemi.
3. Xxxxx xxxxxxxxx orgány xxxxxxxxx xxxxx v souladu s tímto xxxxxxx pověří příslušné xxxxxx jiného členského xxxxx xxxx xxxxx xxxx, xxx xxxxxxxx xxxxxxxx xxxxxx xxxxxx, xxxxxxxx xx xxxxxxx xxxxxxxxx orgány xx xxxxxxxxxx takových xxxxxxx. Xxxx xxxxxxxx zejména xxxxxxx, xxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx o výsledcích kontrol x xxxxxxxxx xxxxxxxxxxx xx xxxxxxxx, x xxxxx xxx xxxxxxxx nezbytná xxxxxxxx.
Xxxxxx 70
Xxxxxx xxxxxxxx produktů xxxxxxxx
Xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx v příloze VI, xxxxx xxx x:
|
a) |
xxxxxxxxxxxxxx xxxxxxxxx; |
|
x) |
xxxxxxxxx xxxxxxxxxx; |
|
x) |
histamin; |
|
x) |
rezidua x xxxxxxxxxxxxx xxxxx; |
|
x) |
xxxxxxxxxxxxxxx kontroly; |
|
f) |
xxxxxxxx; |
|
x) |
xxxxxxxx produkty xxxxxxxx. |
Xxxxxx 71
Xxxxxxxxxx xx xxxxxxxxx xxxxxxx
Xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxxx k lidské xxxxxxxx, xxxxxxxx:
|
x) |
xx xxxxxxx úředních xxxxxxx xxxxxxxxxxx v souladu x xxxxxxx 70 xx xxxxx, xx xxxxxx x xxxxxxx x xxxxxxxxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxxx xxxx mikrobiologickými xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxxxxx x xxxxxxx XXX xxxxxx XXX xxxxxxxx (XX) x. 853/2004 x/xxxx v nařízení (XX) x. 2073/2005; |
|
x) |
obsahují xx xxxxx xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxx xxxx kontaminující xxxxx x xxxxxxxx překračujícím xxxxxx xxxxxxxxx x xxxxxxxxxx (EU) x. 37/2010, (ES) x. 396/2005 x (XX) x. 1881/2006 nebo xxxxxxx xxxxx, xxxxx xxxx xxxxxxxx xxxx xxxxxxxxxx xxxxx nařízení (XX) x. 37/2010 xxxx xxxxxxxx 96/22/XX, xxxx xxxxxx x xxxxxxx x xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx Xxxx x xxxxxxxxxxxxxx xxxxxxxx xxxxxxx; |
|
x) |
xxxxxxxxx x:
|
|
x) |
xxxxx xxx podle xxxxxxxxxxx xxxxxx xxxxxxx xxx xxxxxx xxxxxx xxxx zdraví xxxxxx xxxx jsou z jiného xxxxxx xxxxxxxx x xxxxxx xxxxxxxx. |
Xxxxxx 72
Xxxxxxxxx na xxxxxx xxxxxxxx xxxxxxxx rybolovu, xxxxx ulovila xxxxxxxx xxxxxxx xxx xxxxxxx xxxxxxxxx států a které xxxxxxxx xx Xxxx xxxx, co byly xxxxxxxxx, x xxxxxxxx též xxxxxxxxxx, x xxxxxxx xxxxxx
1. Xxxxxxxx xxxxxxxx xxxxxx k lidské xxxxxxxx xxxxxxx plavidly xxxxxxxxx xxx vlajkou xxxxxxxxx státu, xxxxx xxxx xxxx xxx, xxx v jiném xxxxxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxx Xxxx, xxxxxxxx, x xxxxxxxx též xxxxxxxxxx, x xxxxxxx xxxxxx uvedených x xxxxxxx xxxxx xx. 126 xxxx. 2 xxxx. x) xxxxxxxx (EU) 2017/625, xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx xxxx třetí xxxx x xxxxxxxx x xxxxxxx xx xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx v příloze XXX xxxxx II xxxxxxxx X prováděcího xxxxxxxx (XX) 2019/628.
2. Pokud xxxx xxxxxxxx rybolovu uvedené x xxxxxxxx 1 xxxxxxxx x xxxxxxxxxx xx xxxxxxxxxxxx xxxxxxxx, které xx xxxxxxx v třetí xxxx xxxxxxx xx zmíněném xxxxxxxx, xxxx xxx xxxx skladovací xxxxxxxx xxxxxxx v seznamu xxxxx xxxxxx 5 xxxxxxxx x xxxxxxxxx xxxxxxxxx (XX) 2019/625.
3. Xxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxx x xxxxxxxx 1 xxxxxxxx na plavidlo xxxxxxx pod xxxxxxx xxxxx xxxx, uvede xx xxxx xxxxx xxxx v seznamu podle xxxxxx 3 nařízení x xxxxxxxxx xxxxxxxxx (EU) 2019/625 x xxxx xxxxxxxx xxxx xxx uvedeno v seznamu xxxxx xxxxxx 5 nařízení x xxxxxxxxx xxxxxxxxx (EU) 2019/625.
4. Xxxxx xxxxxxxxx xx xxxxxxxxxx xx kontejnerové xxxx používané pro xxxxxxxx produktů xxxxxxxx x xxxxxxxxxxxx.
HLAVA XXX
XXXXXXXX XXXXXXXXX XX XXXXXXXXX ÚŘEDNÍCH XXXXXXX A JEDNOTNÁ XXXXXXXXX XXXXXXX XXXXXXXX XXXXXXX X&xxxx;XXXX XXXXX
Xxxxxx&xxxx;73
Xxxxxxxxx xxxx xxxxxxxx a po xxxxxxx x&xxxx;xxxxx
X&xxxx;xxxxxxx prohlídky xxxx xxxxxxxx x&xxxx;xxxxx se xxxxxxx xxxxxx&xxxx;11.
X&xxxx;xxxxxxx xxxxxxxxx xx xxxxxxx x&xxxx;xxxxx xx použijí články 12, 13 a 14. Xxx xxxxx čl. 13 xxxx.&xxxx;1 písm. a) xxxx i) xx xxxx xxxxxxxx xx 0,5 velké xxxxxxx xxxxxxxx.
XXXXX XXXX
XXXXXXXXX XXXXXXXXXX
Xxxxxx&xxxx;74
Xxxxx xxxxxxxx (ES) č. 2074/2005
Nařízení (XX) č. 2074/2005 xx xxxx takto:
|
1. |
Články 5, 6x a 6c xx xxxxxxx. |
|
2. |
X&xxxx;xxxxxxx X&xxxx;xx zrušuje xxxxx XX a dodatek. |
|
3. |
V příloze XX se xxxxxxx xxxxx II. |
|
4. |
Přílohy III x&xxxx;X&xxxx;xx xxxxxxx. |
|
5. |
Xxxxxxx XXx xx zrušuje. |
|
6. |
Příloha VIb x&xxxx;xxxx xxxxxxx xx xxxxxxx. |
Xxxxxx 75
Xxxxx x xxxxxxxx a použitelnost
Xxxx xxxxxxxx vstupuje x xxxxxxxx xxxxxxxx dnem xx xxxxxxxxx v Úředním věstníku Xxxxxxxx xxxx.
Xxxxxxx xx xxx xxx 14. xxxxxxxx 2019.
Xxxx xxxxxxxx je xxxxxxx x xxxxx xxxxxxx x xxxxx použitelné xx xxxxx xxxxxxxxx xxxxxxx.
X Xxxxxxx xxx 15. xxxxxx 2019.
Xx Xxxxxx
xxxxxxxx
Jean-Claude XXXXXXX
(1) Úř. věst. L 95, 7.4.2017, x.&xxxx;1.
(2)&xxxx;&xxxx;Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) č. 854/2004 xx xxx 29.&xxxx;xxxxx&xxxx;2004, xxxxxx se xxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxxx úředních xxxxxxx xxxxxxxx živočišného xxxxxx xxxxxxxx x&xxxx;xxxxxx spotřebě (Xx.&xxxx;xxxx.&xxxx;X&xxxx;139, 30.4.2004, x.&xxxx;206).
(3) Směrnice Rady 96/23/XX xx xxx 29.&xxxx;xxxxx&xxxx;1996 x&xxxx;xxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxx xxxxx x&xxxx;xxxxxx xxxxxxx x&xxxx;xxxxxx zvířatech x&xxxx;xxxxxxxxxxx xxxxxxxxxx a o zrušení xxxxxxx 85/358/XXX x&xxxx;86/469/XXX x&xxxx;xxxxxxxxxx 89/187/XXX a 91/664/EHS (Xx.&xxxx;xxxx.&xxxx;X&xxxx;125, 23.5.1996, x.&xxxx;10).
(4)&xxxx;&xxxx;Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) x.&xxxx;999/2001 xx xxx 22.&xxxx;xxxxxx&xxxx;2001 x&xxxx;xxxxxxxxx xxxxxxxx xxx xxxxxxxx, tlumení x&xxxx;xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;147, 31.5.2001, x.&xxxx;1).
(5)&xxxx;&xxxx;Xxxxxxxx Xxxx 2002/99/ES xx xxx 16.&xxxx;xxxxxxxx&xxxx;2002, xxxxxx se stanoví xxxxxxxxxxx xxxxxxxx xxx xxxxxxxx, zpracování, distribuci x&xxxx;xxxxx produktů živočišného xxxxxx xxxxxxxx x&xxxx;xxxxxx xxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;18, 23.1.2003, x.&xxxx;11).
(6)&xxxx;&xxxx;Xxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx (XX) č. 178/2002 xx dne 28. ledna 2002, xxxxxx se xxxxxxx xxxxxx xxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxx práva, zřizuje xx Xxxxxxxx xxxx xxx xxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxxxx xxxxxxxx xx bezpečnosti xxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;31, 1.2.2002, x.&xxxx;1).
(7)&xxxx;&xxxx;Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx 2003/99/XX xx xxx 17. listopadu 2003 x&xxxx;xxxxxxxxx xxxxxx x&xxxx;xxxxxx původců, x&xxxx;xxxxx rozhodnutí Xxxx 90/424/XXX x&xxxx;x&xxxx;xxxxxxx směrnice Xxxx 92/117/XXX (Xx.&xxxx;xxxx.&xxxx;X&xxxx;325, 12.12.2003, x.&xxxx;31).
(8) Rozhodnutí Xxxxxx 2003/467/XX xx xxx 23.&xxxx;xxxxxx&xxxx;2003, xxxxxx xx xxxxxxx xxxxxx stád xxxxx xxxxxx xxxxxxxx tuberkulózy, xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxx xxxxx v některých xxxxxxxxx xxxxxxx xxxx oblastech xxxxxxxxx xxxxx (Úř. věst. L 156, 25.6.2003, x.&xxxx;74).
(9)&xxxx;&xxxx;Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (ES) x.&xxxx;2160/2003 xx xxx 17. listopadu 2003 x&xxxx;xxxxxxx xxxxxxxx x&xxxx;xxxxxxxxx xxxxxx xxxxxxx xxxxxx xxxxxxxxxxxxx xx x&xxxx;xxxxxxxxx xxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;325, 12.12.2003, x.&xxxx;1).
(10) Nařízení Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) č. 852/2004 xx xxx 29.&xxxx;xxxxx&xxxx;2004 x&xxxx;xxxxxxx potravin (Úř. věst. L 139, 30.4.2004, s. 1).
(11) Nařízení Xxxxxxxxxx parlamentu x&xxxx;Xxxx (XX) x.&xxxx;853/2004 xx xxx 29.&xxxx;xxxxx&xxxx;2004, xxxxxx xx stanoví xxxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxxx živočišného xxxxxx (Úř. věst. L 139, 30.4.2004, x.&xxxx;55).
(12) Nařízení Xxxx (XX) x.&xxxx;1/2005 ze xxx 22.&xxxx;xxxxxxxx&xxxx;2004 o ochraně xxxxxx xxxxx xxxxxxxx a souvisejících xxxxxxxx a o změně směrnic 64/432/XXX x&xxxx;93/119/XX x&xxxx;xxxxxxxx (XX) č. 1255/97 (Xx.&xxxx;xxxx.&xxxx;X&xxxx;3, 5.1.2005, x.&xxxx;1).
(13)&xxxx;&xxxx;Xxxxxxxx Komise (ES) x.&xxxx;2073/2005 xx xxx 15.&xxxx;xxxxxxxxx&xxxx;2005 x&xxxx;xxxxxxxxxxxxxxxxx xxxxxxxxxx xxx potraviny (Xx.&xxxx;xxxx.&xxxx;X&xxxx;338, 22.12.2005, x.&xxxx;1).
(14) Nařízení Xxxxxx (XX) x.&xxxx;1881/2006 xx xxx 19.&xxxx;xxxxxxxx&xxxx;2006, xxxxxx xx xxxxxxx maximální xxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxx x&xxxx;xxxxxxxxxxx (Úř. věst. L 364, 20.12.2006, x.&xxxx;5).
(15)&xxxx;&xxxx;Xxxxxxxx Xxxxxx (XX) x.&xxxx;124/2009 ze xxx 10.&xxxx;xxxxx&xxxx;2009, kterým xx xxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxxxxx kokcidiostatik xxxx xxxxxxxxxxxxxxx v potravinách, xxx je důsledkem xxxxxxxxxxxx křížové xxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;40, 11.2.2009, x.&xxxx;7).
(16)&xxxx;&xxxx;Xxxxxxxx Xxxx 2007/43/XX xx xxx 28. června 2007 x&xxxx;xxxxxxxxxxx pravidlech xxx xxxxxxx xxxxx xxxxxxxxx xx xxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;182, 12.7.2007, s. 19).
(17)&xxxx;&xxxx;Xxxxxxxx Evropského parlamentu x&xxxx;Xxxx (XX) x.&xxxx;1069/2009 xx xxx 21.&xxxx;xxxxx&xxxx;2009 x&xxxx;xxxxxxxxxxxx xxxxxxxxxx pro xxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxx x&xxxx;xxxxxx xxxxxxxx, x&xxxx;x&xxxx;xxxxxxx xxxxxxxx (ES) x.&xxxx;1774/2002 (xxxxxxxx o vedlejších produktech xxxxxxxxxxx původu) (Úř. věst. L 300, 14.11.2009, s. 1).
(18) Nařízení Xxxx (XX) x.&xxxx;1099/2009 xx dne 24.&xxxx;xxxx&xxxx;2009 o ochraně xxxxxx xxx xxxxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;303, 18.11.2009, x.&xxxx;1).
(19)&xxxx;&xxxx;Xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx 2010/63/EU ze xxx 22.&xxxx;xxxx&xxxx;2010 x&xxxx;xxxxxxx xxxxxx xxxxxxxxxxx xxx xxxxxxx xxxxx (Úř. věst. L 276, 20.10.2010, x.&xxxx;33).
(20)&xxxx;&xxxx;Xxxxxxxxx xxxxxxxx Xxxxxx (XX) x.&xxxx;636/2014 xx xxx 13.&xxxx;xxxxxx&xxxx;2014 x&xxxx;xxxxx xxxxxxxxx xxx obchod x&xxxx;xxxxxxxxxx velkou xxxxx xxxxxx xxxxx (Úř. věst. L 175, 14.6.2014, x.&xxxx;16).
(21) Prováděcí xxxxxxxx Xxxxxx (XX) 2015/1375 xx xxx 10.&xxxx;xxxxx&xxxx;2015, xxxxxx xx stanoví zvláštní xxxxxxxx xxx xxxxxx xxxxxxxx xxxxxxxxx v mase (Xx.&xxxx;xxxx.&xxxx;X&xxxx;212, 11.8.2015, x.&xxxx;7).
(22) Nařízení Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) 2016/429 xx xxx 9. března 2016 x&xxxx;xxxxxxxx xxxxxx x&xxxx;x&xxxx;xxxxx x&xxxx;xxxxxxx některých xxxx x&xxxx;xxxxxxx xxxxxx zvířat („xxxxxx rámec xxx xxxxxx zvířat“) (Xx.&xxxx;xxxx.&xxxx;X&xxxx;84, 31.3.2016, x.&xxxx;1).
(23) EFSA Journal 2011;9(10):2351.
(24)&xxxx;&xxxx;XXXX Xxxxxxx 2012;10(6):2741.
(25)&xxxx;&xxxx;XXXX Xxxxxxx 2013;11(6):3266.
(26) EFSA Journal 2013;11(6):3265.
(27)&xxxx;&xxxx;XXXX Journal 2013;11(6):3263.
(28)&xxxx;&xxxx;Xxxxxxxx Xxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx (XX) 2019/624 xx xxx 8. xxxxx 2019 o zvláštních xxxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxx produkce xxxx a pro xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxx xxx xxxx mlže x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) 2017/625 (xxx xxxxxx 1 x xxxxx čísle Xxxxxxxx xxxxxxxx).
(29) Nařízení Komise (XX) x.&xxxx;2074/2005 ze dne 5.&xxxx;xxxxxxxx&xxxx;2005, kterým se xxxxxxx prováděcí xxxxxxxx xxx xxxxxxx výrobky xxxxx xxxxxxxx Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (ES) x.&xxxx;853/2004 x&xxxx;xxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxx xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx (ES) x.&xxxx;854/2004 x&xxxx;(XX) č. 882/2004, xxxxxx xx xxxxxxx xxxxxxxx xx xxxxxxxx Evropského xxxxxxxxxx x&xxxx;Xxxx (XX) x.&xxxx;852/2004 x&xxxx;xxxxxx xx xxxx nařízení (XX) x.&xxxx;853/2004 x&xxxx;(XX) x.&xxxx;854/2004 (Xx.&xxxx;xxxx.&xxxx;X&xxxx;338, 22.12.2005, x.&xxxx;27).
(30) Nařízení Xxxxxxxxxx xxxxxxxxxx x&xxxx;Xxxx (XX) x.&xxxx;178/2002 xx xxx 28. ledna 2002, xxxxxx xx xxxxxxx xxxxxx xxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxxxxx xxxxx, zřizuje xx Xxxxxxxx xxxx xxx xxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxx xxxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;31, 1.2.2002, s. 1).
(31)&xxxx;&xxxx;Xxxxxxxx Xxxxxx v přenesené xxxxxxxxx (XX) 2019/625 xx dne 4. xxxxxx 2019, xxxxxx xx doplňuje xxxxxxxx Xxxxxxxxxx xxxxxxxxxx a Rady (XX) 2017/625, xxxxx xxx o požadavky na xxxxx xxxxxxx určitých xxxxxx x&xxxx;xxxxx xxxxxxxx x&xxxx;xxxxxx spotřebě do Xxxx (xxx xxxxxx 18 v xxxxx xxxxx Xxxxxxxx věstníku).
(32) Rozhodnutí Xxxxxx 97/747/XX xx dne 27. října 1997, xxxxxx se xxxxxxx xxxxxx x&xxxx;xxxxxxx xxxxxx xxxxxx xxxxx směrnice Xxxx 96/23/XX x&xxxx;xxxxxxxxxxx xxxxxxxxxx x&xxxx;xxxxxxxxx látek x&xxxx;xxxxxx xxxxxxx x&xxxx;xxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxx produktech (Xx.&xxxx;xxxx.&xxxx;X&xxxx;303, 6.11.1997, s. 12).
(33) Nařízení Xxxxxx (EU) x.&xxxx;37/2010 xx dne 22.&xxxx;xxxxxxxx&xxxx;2009 x&xxxx;xxxxxxxxxxxxxx xxxxxxxx xxxxxxx a jejich klasifikaci xxxxx maximálních xxxxxx xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxxxxxx xxxxxx (Úř. věst. L 15, 20.1.2010, x.&xxxx;1).
(34)&xxxx;&xxxx;Xxxxxxxxx xxxxxxxx Xxxxxx (XX) 2018/470 xx xxx 21.&xxxx;xxxxxx&xxxx;2018 x&xxxx;xxxxxxxxxx xxxxxxxxxx xxx xxxxxxxxx xxxxx reziduí, jenž xx xxx xxxx x&xxxx;xxxxx xxx xxxxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxx x&xxxx;XX xxxxx článku 11 xxxxxxxx 2001/82/ES (Xx.&xxxx;xxxx.&xxxx;X&xxxx;79, 22.3.2018, x.&xxxx;16).
(35) Směrnice Xxxx 96/22/XX xx dne 29.&xxxx;xxxxx&xxxx;1996 x&xxxx;xxxxxx používání některých xxxxx x&xxxx;xxxxxxxxxxx xxxx xxxxxxxxxxxxxx účinkem x&xxxx;xxxx-xxxxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxx x&xxxx;x&xxxx;xxxxxxx xxxxxxx 81/602/EHS, 88/146/XXX x&xxxx;88/299/XXX (Úř. věst. L 125, 23.5.1996, x.&xxxx;3).
(36) Rozhodnutí Komise 2005/34/XX xx xxx 11.&xxxx;xxxxx&xxxx;2005, xxxxxx se xxxxxxx xxxxxxxxxxxxx xxxxx pro xxxxxxxx xxxxxxxxx reziduí x&xxxx;xxxxxxxxxx živočišného xxxxxx xxxxxxxxxx ze třetích xxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;16, 20.1.2005, x.&xxxx;61).
(37)&xxxx;&xxxx;Xxxxxxxx Xxxxxxxxxx parlamentu x&xxxx;Xxxx (XX) x.&xxxx;396/2005 xx xxx 23.&xxxx;xxxxx&xxxx;2005 x&xxxx;xxxxxxxxxxx limitech xxxxxxx xxxxxxxxx v potravinách a krmivech xxxxxxxxxxx x&xxxx;xxxxxxxxxxx xxxxxx x&xxxx;xx xxxxxx xxxxxxx x&xxxx;x&xxxx;xxxxx xxxxxxxx Rady 91/414/XXX (Xx.&xxxx;xxxx.&xxxx;X&xxxx;70, 16.3.2005, x.&xxxx;1).
(38)&xxxx;&xxxx;Xxxxxxxxx nařízení Komise (XX) 2019/628 ze xxx 8. xxxxx 2019 x&xxxx;xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxx některá xxxxxxx x&xxxx;xxxxx x&xxxx;x&xxxx;xxxxx xxxxxxxx (XX) x.&xxxx;2074/2005 x&xxxx;xxxxxxxxxxx xxxxxxxx (XX) 2016/759, pokud xxx x&xxxx;xxxx xxxxxx osvědčení (xxx strana 101 x xxxxx čísle Xxxxxxxx xxxxxxxx).
(39) Směrnice Evropského xxxxxxxxxx x&xxxx;Xxxx (XX) 2015/1535 xx xxx 9. září 2015 x&xxxx;xxxxxxx xxx xxxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx xxxxxxxxxxx xxxxxxxx x&xxxx;xxxxxxxx pro xxxxxx xxxxxxxxxx xxxxxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;241, 17.9.2015, x.&xxxx;1).
(40) Jsou-li xxxxxxx negativní, xxx x&xxxx;95&xxxx;% statistickou xxxxxxxx xxxxxxxxxxx, že xxxxxxxxxx xx xxxxx xxx 6&xxxx;%.
(41)&xxxx;&xxxx;Xxxxxxxx Xxxx 64/432/EHS xx dne 26. června 1964 x&xxxx;xxxxxxxxxxxxx xxxxxxxx obchodu xx xxxxxx x&xxxx;xxxxxxx xxxxxx Xxxxxxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;121, 29.7.1964, x.&xxxx;1977).
XXXXXXX X
XXXX DOKUMENTU XXX KOMUNIKACI X&xxxx;XXXXXXXXXXXXX XXXXXX V SOULADU X&xxxx;XX.&xxxx;39 XXXX.&xxxx;5
1.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxx xxxxx
1.1.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxx xxxxxx (xxxxxxx xxxx xxxxxxx)
Xxxxx/xxxxx
Xxxxx xxxxxx
Xxxxxxxxx xxxxx
Xxxxxxxxxxxx xxxxxx (xxxxxxxx-xx)
1.2.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxx xxxxx … (xxxxxxxxx) nebo xxxxxxxx xxxxxx
Xxxxxxx xxxxx xxxxxx (xxxxx xxxxx)
Xxxxxxxx x&xxxx;xxxxxxxxxxxx (xxxx-xx nějaké)
1.3. Identifikační číslo xxxxx/xxxxx/xxxxx (x&xxxx;xxxxxxxxxxx případech)
1.4. Druhy xxxxxx
1.5.&xxxx;&xxxx;&xxxx;Xxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx (x&xxxx;xxxxxxxxxxx xxxxxxxxx)
2.&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxxxx před xxxxxxxx
2.1.&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxx xxxxxxxx zvířat
Počet xxxxxxxxxxx xxxxxx
Xxx/xxxxx/xxxxx
Xxxxxxxx
2.2.&xxxx;&xxxx;&xxxx;Xxxxxxx byla xxxxxx xxxxxxx
2.3.&xxxx;&xxxx;&xxxx;Xxxxxxxx nález (xxxxxx)
Xxxxx xxxxxxxxxxx xxxxxx
Xxx/xxxxx/xxxxx
Xxxxxxxx
Xxxxx xxxxxxxxx
2.4.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxx xxxxxxxx&xxxx;(1)
3.&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxxxx xx xxxxxxx
3.1.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxx xxxxx
Xxxxx xxxxxxxxxxx zvířat
Typ/třída/stáří
Postižený orgán xxxx xxxx zvířete/zvířat
Datum xxxxxxx
3.2.&xxxx;&xxxx;&xxxx;Xxxxxx (xxx zapsat xxxxx&xxxx;(2))
Xxxxx xxxxxxxxxxx zvířat
Typ/třída/stáří
Postižený xxxxx nebo část xxxxxxx/xxxxxx
Xxxxxxx upravené xxxx xxxxxx x&xxxx;xxxxxxxxxx nebo xxxxxxx xxxxxxx (uveďte xxxxx)
Xxxxx xxxxxxx
3.3.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxx xxxxxxxx&xxxx;(3)
3.4.&xxxx;&xxxx;&xxxx;Xxxx xxxxxxxx
3.5.&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxxx se xxxxxxx životních xxxxxxxx xxxxxx
4.&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxxxx
5.&xxxx;&xxxx;&xxxx;Xxxxxxxxx údaje xxxxx (číslo schválení)
Název
Úplná xxxxxx
Xxxxxxxxx xxxxx
Xxxxxxxxxxxx xxxxxx (xxxxxxxx-xx)
6.&xxxx;&xxxx;&xxxx;Xxxxxx veterinární xxxxx (xxxxx xxxxxxxx xxxxxx)
Xxxxxx x&xxxx;xxxxxxx
7.&xxxx;&xxxx;&xxxx;Xxxxx
8.&xxxx;&xxxx;&xxxx;Xxxxx xxxxx xxxxxx x&xxxx;xxxxxx formuláři:
(1) Mikrobiologické, chemické, xxxxxxxxxxx atd. (xxxxxx xxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxx).
(2)&xxxx;&xxxx;Xxxxxxxxx xxxxxx xxxxx xxxxxx xxxx xxxx: kód X&xxxx;xxx xxxxxx na xxxxxxx OIE; xxxx X100 x&xxxx;X200 pro xxxxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxx a C100 xx X290 xxx xxxxxxxxxx xxxxxxxx se xxxx. Xxxxxxxx xxxxxx xxxx x&xxxx;xxxxxxx xxxxxxx obsahovat xxxxx členění (xxxx. X141 xxx xxxxxx xxxxxxxxxxxxxxx formu xxxxxx, X142 xxx xxxxx xxxxx xxxxxx xxxx.). Xxxxxxxxx-xx se xxxx, xxxx být xxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxx dostupné xxxxx x&xxxx;xxxxxxx xxxxxxxxxxx jejich xxxxxxx.
(3)&xxxx;&xxxx;Xxxxxxxxxxxxxxx, xxxxxxxx, sérologické xxx. (xxxxxx výsledky x&xxxx;xxxxxxx s přílohou).
XXXXXXX II
PRAKTICKÁ XXXXXXXX XXX XXXXXX ZDRAVOTNÍ XXXXXXXXXXXX V SOULADU X&xxxx;XXXXXXX&xxxx;48
|
1. |
Xxxxxx xxxxxxxxx xxxxxxxxxxxx musí xxx xxxxxx, x&xxxx;xxxxx xxxxxxx 6,5 cm a výšce xxxxxxx 4,5 cm a musí xxxxxxxxx následující xxxxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxx:
|
|
2. |
Xxxxxxx musí xxx xxxxxxx 0,8 cm xxxxxx x&xxxx;xxxxxxx xxxx být xxxxxxx 1&xxxx;xx xxxxxx. Xxxxxxx xxxxx x&xxxx;xxxxxx xxxxx být xxxxxxxx x&xxxx;xxxxxxxxxx zdravotní xxxxxxxxxxxx xxxxxx, kůzlat a selat. |
|
3. |
Inkoust xxxxxxx x&xxxx;xxxxxxxx xxxxxxxxx xxxxxxxxxxxx musí xxx xxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxx Xxxx x&xxxx;xxxxxxxxx xxxxxx x&xxxx;xxxxxxxxxxx. |
|
4. |
Xxxxxx zdravotní xxxxxxxxxxxx xxxx rovněž obsahovat xxxx x&xxxx;xxxxxxx xxxxxxxxxxxx xxxxxx, xxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxx. |
PŘÍLOHA XXX
XXXXXXXXX XXXXXX XXX XXXXXX XXXXX X&xxxx;XXXXXXX OŠETŘENÉ KRAVSKÉ XXXXX V SOULADU X&xxxx;XXXXXXX&xxxx;50
XXXXXXXX X
XXXXXXXXX XXXXX XXXXXXXXXXXXXX X&xxxx;XXXXX XXXXXXXXXXX XXXXX
|
X. |
Xxx xxxxxxxxx souladu x&xxxx;xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxxx XXX xxxxxx XX kapitole X&xxxx;xxxxx XXX xxxxxxxx (XX) x.&xxxx;853/2004 xxxx xxx jako referenční xxxxxx použity xxxx xxxxx:
|
|
X. |
Xxxxxxx alternativních xxxxxxxxxxxx xxxxx xx xxxxxxxxxx:
|
KAPITOLA II
STANOVENÍ XXXXXXXX XXXXXXXXX XXXXXXXXX X&xxxx;XXXXXXXX MLÉCE
|
A. |
Pro stanovení xxxxxxxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxx kravském xxxxx xx jako referenční xxxxxx musí použít xxxxx XX ISO 11816-1. |
|
X. |
Xxxxxxxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxx xxxxx xx xxxxxxxxx v milijednotkách xxxxxxxx aktivity xx xxxx (xX/x). Xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xx množství xxxxxx xxxxxxxxx xxxxxxxxx, jež xxxxxxxxxx přeměnu 1 mikromolu xxxxxxxxx xx xxxxxx. |
|
X. |
Xxxxxxxx xxxxx alkalické xxxxxxxxx xx xxxxxxxx xx xxxxxxxxx, xxxxx naměřená xxxxxxxx x&xxxx;xxxxxxxx mléce xxxxxxxxxxx 350 xX/x. |
|
X. |
Xxxxxxx xxxxxxxxxxxxxx analytických metod xx xxxxxxxxxx, xxxxx xxxx xxxxxxxxxx podle xxxxxxxxxx xxxxxx uvedené x&xxxx;xxxxx A v souladu x&xxxx;xxxxxxxxxxx xxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxx. |
XXXXXXX XX
XXXXXXXXXX TESTOVACÍ XXXXXX PRO ANALÝZU X. XXXX X&xxxx;XXXXXX XXXXXX XXX XXXXX XXXXXXXXXXX PRODUKČNÍCH X&xxxx;XXXXXXXXXXX XXXXXXX X&xxxx;XXXXXXX X&xxxx;XX.&xxxx;52 XXXX.&xxxx;2
Xxxxxxxxxx xxxxxxx pro xxxxxxx E. coli x&xxxx;xxxxxx xxxxxx je xxxxxxx x&xxxx;xxxxxxxx „nejvýše xxxxxxxxxxxxxxx počtu“ (XXX) xxxxxxx x&xxxx;xxxxx XXX 16649-3. Xxxxxxxxxxxx metody xxxxx xxx xxxxxxx, xxxx-xx xxxxxxxxxx xxxxx xxxx xxxxxxxxxx xxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxxxxx uvedenými x&xxxx;xxxxx ISO 16140.
XXXXXXX V
UZNANÉ METODY XXXXXXXXXX XXXXXXXX XXXXXXXXX X&xxxx;XXXXXXX X&xxxx;XXXXXXX&xxxx;60
XXXXXXXX I
METODA XXXXXXXXXX PARALYTICKÝCH XXXXXX
|
X. |
Xxxxx xxxxxxxxxxxxx xxxxxx (XXX) x&xxxx;xxxxx xxxx xxxx xxxxxxxxxx xxxxx xxxxx xxxx se xxxxxxx xxxxxx xxxxxxxxx xxxxxx XXX 2005.06 xxxxxxxxxx XXXX, zveřejněné x&xxxx;XXXX Xxxxxxxxxxxxx Xxxxxxx 88(6), 1714-1732 (Xxxxxxxxxx metody), xxxxxxxxxx xxxxxxx na xxxxxx nebo xxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxx. |
|
X. |
Xxxx-xx xxxxxxxx xxxxxxxxxxx, xxxxxxxxxx xxxxxxx xx xxxxxxxxx xxxxxx OMA 2005.06 xxxxxxxxxx XXXX xxxxxxx x&xxxx;xxxxx X. |
XXXXXXXX XX
XXXXXX XXXXXXXXXX XXXXXXXXXXX XXXXXX
|
X. |
Xxxxx xxxxxxxxxxx xxxxxx (XXX) x&xxxx;xxxxx těle xxxx jednotlivé jedlé xxxxx xxxx xx xxxxxxx xxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxx chromatografie x&xxxx;XX xxxxxxx (XXXX/XX) xxxx xxxx mezinárodně xxxxxx validované xxxxxx. |
|
X. |
Xxx xxxxx screeningu však xxxx xxx použita xxxx oficiální xxxxxx 2006.02 organizace AOAC, xxxxxxxxxx x&xxxx;XXXX Xxxxxxxxxxxxx Xxxxxxx 90, 1011-1027, (xxxxxxxx xxxxxxxxxxxx x&xxxx;xxxxxxx xxxxxxx xx xxxxxxxxxxxx, XXXXX, xxx XXX) xxxx xxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxx. |
|
X. |
Xxxx-xx xxxxxxxx zpochybněny, xxxxxxxxxx xxxxxxx xx xxxxxx XXXX/XX. |
XXXXXXXX XXX
XXXXXX XXXXXXXXXX XXXXXXXXXXX XXXXXX
|
X. |
Xxxxxxxxxx xxxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxx XXX xxxxxx VII xxxxxxxx X&xxxx;xxxx 2 xxxx. c), x) x&xxxx;x) xxxxxxxx (XX) x.&xxxx;853/2004 xx xxxxxx xxxxxxxxxx chromatografie x&xxxx;xxxxxxxxx x&xxxx;xxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx EU (XXXX XX-XX/XX). Touto xxxxxxx se xxxxxx xxxxxxx xxxx xxxxxxxxxx:
Xxxxxxxx xx xxxxxx xxxx xxxxxxx xxxx xxxxxxxxx toxinů, x&xxxx;xxxxxxx xxx stanoven xxxxxx xxxxxxx xxxxxxxxxxxxx (XXX), xxxxxxx se xx analýzy. Celková xxxxxxxxxxxx xxxxxxxx se xxxxxxxx xxxxxx xxxxxxx TEF xxxxx xxxxxxxxxx Evropského xxxxx xxx bezpečnost xxxxxxxx (EFSA) uvedeného x&xxxx;Xxxxxxx (2008) 589, 1-62 nebo xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxx úřadu XXXX. |
|
X. |
Xxxxxx jiné než xxxxxxx x&xxxx;xxxxx A, xxxxxxxxx metoda LC-MS, xxxxxx XXXX x&xxxx;xxxxxxx xxxxxxx, xxxxxxxxxxxx xxxxx x&xxxx;xxxxxxx xxxxx, jako xx test xxxxxxxx xxxxxxxxx, xxxxx být xxxxxxx jako xxxxxxxxxxx x&xxxx;xxxxxx XX-XX XX-XX/XX xxxx xxxxxxxx s touto xxxxxxx za xxxxxxxxxxx, xx:
|
KAPITOLA XX
XXXXXXXXXX XXXXXX NEBO XXXX XX XXXXXXXXXXXX XXXXXXXX XXXXXX
Xxxxx xxxxxxxxxxxx xxxxxxxxxxxx produkčních xxxxxxx x&xxxx;xxxxxxxxxxx oblastí xxxxxxxxxx xx xxxxxxxx nových xxxx nově se xxxxxxxxxxxx mořských toxinů xx xxxxxxx xxxxxxxxxxxxxx xxxxxxxx kontrol xxxxxxxxxxxxx xxxxxxxxx xxxxx xxxxx xxx xxxxxxxxx chemické xxxxxx, xxxxxxxxxxxx xxxxxx x&xxxx;xxxxxxx detekcí xxxx xxxxxxxxxx xxxxxxx xx xxxxxx.
PŘÍLOHA XX
XXXXXXXXX XXXXXXXX XXX XXXXXX XXXXXXXX XXXXXXXX RYBOLOVU V SOULADU X&xxxx;XXXXXXX&xxxx;70
XXXXXXXX I
OBECNÁ XXXXXXXXXX
X.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxx xxxxxxxxx
Xx všech fázích xxxxxxxx, xxxxxxxxxx x&xxxx;xxxxxxxxxx xx provádějí namátkové xxxxxxxxxxxxxx xxxxxxxx. Jedním x&xxxx;xxxx xxxxxx xxxxxxx xx xxxxxx, xxx xxxx plněna xxxxxxxx xxxxxxxxxx xxxxxxxxx x&xxxx;xxxxxxx x&xxxx;xxxxx xxxxxxxxx. Xxxxxxx xx ve xxxxx xxxxxx xxxxxxxx, xxxxxxxxxx x&xxxx;xxxxxxxxxx ověří, xxx xxxxxxxx xxxxxxxx xxxxxxx xxxxxxx základní xxxxxx xxxxxxxx xxxxxxxxxx stanovené x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx Rady (XX) x.&xxxx;2406/96&xxxx;(1).
X.&xxxx;&xxxx;&xxxx;Xxxxxxxxx čerstvosti
Pokud xxxxxxxxxxxxxx xxxxxxxxx xxxx x&xxxx;xxxxxxxxxxxx o čerstvosti xxxxxxxx xxxxxxxx, xxxxx xxx xxxxxxxx xxxxxx, xx xxxxx xx xxxxxxxx xxxxxxxxxxx xxxxx x&xxxx;xxxxxx xxxxxx celkového xxxxxxxx xxxxxxxxxx xxxxxx (XXX-X) x&xxxx;xxxxxxxxxxxxx-xxxxxx (XXX-X) x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxxx xxxxxxx xxxxxxxxx x&xxxx;xxxxxxxx II.
Příslušné xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx x&xxxx;xxxxx xxxxxxxx.
Xxxxx na xxxxxxx organoleptického xxxxxxxxx xxxxxxxx xxxxxxxxx na xxxxxx jiného stavu, xxxxx může mít xxxx xx xxxxxx xxxxxx, odeberou xx xxx xxxxx ověření xxxxxx xxxxxx.
X.&xxxx;&xxxx;&xxxx;Xxxxxxxx
Xxxxxxxxx xx xxxxxxxxx testy xx xxxxxxxx za xxxxxx xxxxxxx souladu x&xxxx;xxxxxxxxxxx xxxxxx xxxxxxxxxxx x&xxxx;xxxxxxxx (XX) x.&xxxx;2073/2005.
X.&xxxx;&xxxx;&xxxx;Xxxxxxx x&xxxx;xxxxxxxxxxxxx xxxxx
X&xxxx;xxxxxxx xx xxxxxxxx 96/23/XX x&xxxx;xxxxxxxxxxx 97/747/ES xx xxxxxxx xxxxxxxxxxxx xxxxxxxx za xxxxxx xxxxxxxx xxxxxxxxxx právních xxxxxxxx EU týkajících xx:
|
— |
xxxxxxxxxxx xxxxxx reziduí xxxxxxxxxxxxxx xxxxxxxx látek x&xxxx;xxxxxxx x&xxxx;xxxxxxxxxx (EU) x.&xxxx;37/2010 a (EU) 2018/470, |
|
— |
zakázaných x&xxxx;xxxxxxxxxxxx látek x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx (EU) x.&xxxx;37/2010, xxxxxxxx 96/22/XX x&xxxx;xxxxxxxxxxx 2005/34/XX, |
|
— |
xxxxxxxxxxxxxxx xxxxx v souladu x&xxxx;xxxxxxxxx (ES) č. 1881/2006, xxxxxx xx stanoví xxxxxxxxx limity některých xxxxxxxxxxxxxxx xxxxx v potravinách x |
|
— |
xxxxxxx pesticidů x&xxxx;xxxxxxx x&xxxx;xxxxxxxxx (XX) x.&xxxx;396/2005. |
X.&xxxx;&xxxx;&xxxx;Xxxxxxxxxxxxxxx xxxxxxxx
X&xxxx;xxxxxxx xxxxxxx xx xxxxxxxx mikrobiologické xxxxxxxx x&xxxx;xxxxxxx s příslušnými xxxxxxxx x&xxxx;xxxxxxxx stanovenými x&xxxx;xxxxxxxx (XX) x.&xxxx;2073/2005.
X.&xxxx;&xxxx;&xxxx;Xxxxxxxx
Xxxxxxxxx xx xxxxx xx xxxxxxx xxxxxx xx účelem xxxxxxx souladu x&xxxx;xxxxxxxx XXX xxxxxxx XXXX xxxxxxxxx XXX částí X nařízení (XX) x.&xxxx;853/2004 a přílohou II xxxxxxx X&xxxx;xxxxxxxx (ES) x.&xxxx;2074/2005.
X.&xxxx;&xxxx;&xxxx;Xxxxxxxx xxxxxxxx xxxxxxxx
Xxxxxxxxx xx xxxxxxxx s cílem xxxxxxxx, aby:
|
1. |
na trh xxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx z jedovatých xxx xxxxxx čeledí: Xxxxxxxxxxxxxx, Molidae, Diodontidae x&xxxx;Xxxxxxxxxxxxxxxx; |
|
2. |
xxxxxxx, xxxxxxxxxx, zmrazené x&xxxx;xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xx xxxxxx Xxxxxxxxxx, zejména Xxxxxxxx xxxxxxxxx x&xxxx;Xxxxxxxxxxxx flavobrunneum, xxxxx xxx xxxxxxx xx xxx pouze x&xxxx;xxxxxx xxxx dalším xxxxxx a aby xxxx xxxxxx označeny etiketou x&xxxx;xxxxxxxxxxx xxx xxxxxxxxxxxx x&xxxx;xxxxxxxxx přípravy/vaření a o riziku xxxxxxxxxxxx s přítomností xxxxx x&xxxx;xxxxxxxxxxxx xxxxxxxxxxxxxxxxxxxx xxxxxx. Xx xxxxxxx se xxxxxx xxxxxxx xxxxx x&xxxx;xxxxxx xxxxx produktů xxxxxxxx; |
|
3. |
xx xxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx biotoxiny, xxxxxxxxx xxxxxxxxxx xxxx xxxx xxxxxx xxxxxxxxxx xxx xxxxxx xxxxxx. Xxxxxxxx xxxxxxxx xxxxxxxxxxx x&xxxx;xxxxxx xxxx, ostnokožců, xxxxxxxxx x&xxxx;xxxxxxxx xxxx však xxx být xxxxxxx xx xxx, pokud xxxx xxxxxxxx v souladu x&xxxx;xxxxxxxx XXX xxxxxxx XXX nařízení (ES) x.&xxxx;853/2004 x&xxxx;xxxxxxxx xxxxxx xxxxxxxxxx x&xxxx;xxxxxxxx X&xxxx;xxxx 2 xxxxxxxxx oddílu. |
KAPITOLA XX
XXXXXXXX CELKOVÉHO XXXXXXXX XXXXXXXXXX XXXXXX (XXX-X)
X.&xxxx;&xxxx;&xxxx;Xxxxx xxxxxxx XXX-X xxx xxxxxxx kategorie xxxxxxxx xxxxxxxx a použitelné xxxxxx xxxxxxx
|
1. |
Xxxxxxxxxxxx produkty xxxxxxxx xx považují xx xxxxxxxx x&xxxx;xxxxxx xxxxxxxx, xxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx pochybnosti o jejich xxxxxxxxxx x&xxxx;xxxxxxxxxx kontrolami xxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx xxxxxx XXX-X:
Xxxxxxxxxx xxxxxxx, xxxxx se xxxxxxx xx kontrole xxxxxxx xxxxxx XXX-X, xx xxxxxx destilace xxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx chloristou xxxxx xxxx uvedené xxxxx C. |
|
2. |
Destilace xxxxxxx x&xxxx;xxxx 1 xx xxxxxxx xx použití xxxxxxxxx, který xxxxxxxx xxxxxxx v části X xxxx. |
|
3. |
Xxxxx xxxxxx použitelné xx xxxxxxxx xxxxxxx xxxxxx XXX-X, xxxx xxxx:
|
|
4. |
Xxxxxx xxxxxxx xxxxxxxxx xx 100&xxxx;x xxxx xxxxxxxxxx nejméně xx xxx různých xxxx x&xxxx;xxxxxxxxxx xxxxxxxx. |
Xxxxxxx xxxxx xxxxxxxx, aby xxxxxx xxxxxxxxxx xxxxx xxxxxxxxx xxxx xxxxxxx xxxxxx. V případě xxxxxxxxxx xxxxxxxx xxxx x&xxxx;xxxxxxx xxxxx x&xxxx;xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxx xxxxx xxx xx xxxxxxxx xxxxxxxx xxxxxx xxxxx referenční xxxxxx.
X.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxx, xxx xxxxx xxxx xxxxxxxxx xxxxx xxxxxxx XXX-X
Xxxxx hodnoty XXX-X xxxx xxxxxxxxx xxx tyto xxxxxxxxx xxxxx:
|
1. |
Xxxxxxxx xxx., Helicolenus xxxxxxxxxxxxx, Sebastichthys xxxxxxxx; |
|
2. |
xxxxx xxxxxx Xxxxxxxxxxxxxx (x&xxxx;xxxxxxxx xxxxxxx: Xxxxxxxxxxxx spp.); |
|
3. |
Salmo xxxxx, xxxxx xxxxxx Xxxxxxxxxxxx, xxxxx xxxxxx Xxxxxxx. |
X.&xxxx;&xxxx;&xxxx;Xxxxxxxxxx postup xxx xxxxxxxxx xxxxxxxxxxx TVB-N x&xxxx;xxxxxx a produktech xxxxxxxx
1.&xxxx;&xxxx;&xxxx;Xxxx x&xxxx;xxxxxx xxxxxxx
Xxxx xxxxxx xxxxxxxx xxxxxxxxxx postup xxx xxxxxxxx xxxxxxxxxxx xxxxxx xx formě XXX-X x&xxxx;xxxxxx x&xxxx;xxxxxxxxxx xxxxxxxx. Xxxxx xxxxxx xxx použít x&xxxx;xxxxxxxxxxx XXX-X od 5 mg/100 g xx nejméně 100 mg/100 g.
2. Definice
„Koncentrací XXX-X“ xx rozumí xxxxx dusíku těkavých xxxxxxxxxx xxxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx.
„Xxxxxxxx“ xx xxxxxx xxxxx xxxxxx xxxxxx složení:
|
a) |
roztok xxxxxxxx xxxxxxxxx&xxxx;=&xxxx;6&xxxx;x/100&xxxx;xx; |
|
x) |
xxxxxx xxxxxxxxx xxxxxxx&xxxx;=&xxxx;20&xxxx;x/100&xxxx;xx; |
|
x) |
xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxxxxx 0,05 mol/l (0,05 X). Xxx xxxxxxx automatického xxxxxxxxxxxx xxxxxxxx xx titrace xxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx chlorovodíkové 0,01 xxx/x (0,01 X); |
|
x) |
xxxxxx xxxxxxxx xxxxxx&xxxx;=&xxxx;3&xxxx;x/100&xxxx;xx; |
|
x) |
xxxxxxxxxx xxxxxxxxx; |
|
x) |
xxxxxxxxxxxxxxx xxxxxx&xxxx;=&xxxx;1&xxxx;x/100&xxxx;xx 95&xxxx;% xxxxxxxx; |
|
x) |
xxxxxxxxx xxxxxx (směsný xxxxxxxxx Xxxxxxx) =&xxxx;2&xxxx;x xxxxxxxxxxxxx a 1 g xxxxxxxxxxx xxxxx se xxxxxxxx x&xxxx;1&xxxx;000&xxxx;xx 95&xxxx;% ethanolu. |
3. Stručný xxxxx
Xxxxxx dusíkaté xxxx xx xx xxxxxx xxxxxxxxx roztokem 0,6 xxx/x xxxxxxxx chloristé. Xx alkalizaci xx xxxxxxx podroben xxxxxxxxx xxxxx parou x&xxxx;xxxxxx xxxx se xxxxxx xxxxxxx xxxxxxx. Xxxxxxxxxxx XXX-X se stanoví xxxxxxx xxxxxxxxxx xxxx. Xxxxxxxxxxx se xxxxxxxxx x&xxxx;xx/100&xxxx;x.
4.&xxxx;&xxxx;&xxxx;Xxxxxxxx látky
Není-li xxxxxxxxx xxxxx, xxxxxxx xx xxxxxxxx xxxxx analytické xxxxxxx. Xxxxxxx voda xx xxxxxxxxxxx nebo xxxxxxxxxxxxxxxx x&xxxx;xxxxxxxxxxxx xxxxxx xxxxxxx.
5.&xxxx;&xxxx;&xxxx;Xxxxxxx xx tyto xxxxxxxxx x&xxxx;xxxxxxxxxxxxx:
|
x) |
xxxxxx na xxxx x&xxxx;xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxx xxxx; |
|
x) |
xxxxxxxxxxxxxxxx xxxxx o rychlosti 8&xxxx;000 xx 45&xxxx;000 xxxxxx za xxxxxx; |
|
x) |
xxxxxxxx xxxxx x&xxxx;xxxxxxx 150&xxxx;xx, xxxxxx xxxxxxxxxx; |
|
x) |
xxxxxx, 5&xxxx;xx, xx stupnicí po 0,01&xxxx;xx; |
|
x) |
xxxxxxxx xxx xxxxxxxxx xxxxx xxxxx. Xxxxxxxx xxxx xxx xxxxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxx páry x&xxxx;xxxxxxxxxx xxxxx xxxxxxxx xxxx xx danou xxxx. Xxxx xxxxxxxx, aby xxx xxxxxxxxx xxxxxxxxxxxxxx xxxxx xxxxxxx unikat xxxxxxxxxx xxxxx xxxx. |
6.&xxxx;&xxxx;&xxxx;Xxxxxxxxx xxxxxxxxxxxx postupu
Při xxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx, xxxxx xx silně xxxxxx, xx xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxxx a přijmou xx xxxxxxxxxxx xxxxxxxx. Xxxxxx xx připraví xx xxxxxxxx xx xxxxxx xxxxxxxx podle xxxxxx xxxxxx:
|
x) |
Xxxxxxxx xxxxxx Xxxxxx x&xxxx;xxxxxxx xx pečlivě xxxxx xxxxxx mlýnku xx xxxx xxxxx xxxx 5 xxxx. x). Xx xxxxxx xxxxxx xx xxxxxx 10&xxxx;x&xxxx;±&xxxx;0,1&xxxx;x xxxxxxxx vzorku. Toto xxxxxxxx xx xxxxx x&xxxx;90,0&xxxx;xx xxxxxxx kyseliny xxxxxxxxx, homogenizuje xxx xxxxxx xxxxxx xxxxxx xxxxx bodu 5 xxxx. b) x&xxxx;xxxxxxxx xxxxxxxx. Xxxxx xxxxxxx extrakt xx možné xxxxxxxxx xxxxxxx sedm xxx xxx teplotě xxxx xxxxxxxxx 2&xxxx;°X a 6 °C. |
|
b) |
Destilace xxxxx xxxxx Xxxxxxx x&xxxx;xxxxxx 50,0&xxxx;xx xxxxxxx podle xxxxxxx x) xx xxxxx do přístroje xxx destilaci vodní xxxxx podle bodu 5 xxxx. e). Xxx xxxxxxxx xxxxxxxx xxxxxxxxxx extraktu xx xxxxx několik kapek xxxxxxxxxxxxxxxxx xxxxxxx. Xx xxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxx odpěňovače xx x&xxxx;xxxxxxxx xxxxx 6,5&xxxx;xx xxxxxxx xxxxxxxxx xxxxxxx x&xxxx;xxxxxxxx xx zahájí xxxxxxxxx xxxxx xxxxx. Xxxxxxxxx xxxxx parou se xxxx tak, xxx xxxx xx 10&xxxx;xxxxx xxxxxxxxx přibližně 100&xxxx;xx xxxxxxxxx. Xxxxxxxxxx odtoková xxxxxxx je xxxxxxxx xx xxxxxx se 100&xxxx;xx xxxxxxx xxxxxxxx xxxxxx, xx xxxxxxx xxxx přidáno tři xx pět xxxxx xxxxxxxxxxx xxxxxxx. Xxxxxx xx 10&xxxx;xxxxxxxx se xxxxxxxxx xxxxxx. Xxxxxxxxxx xxxxxxxx xxxxxxx xx xxxxx z jímače a vymyje xxxxx. Xxxxxx xxxx xxxxxxxx x&xxxx;xxxxxxx xxxxxxx xx xxxx xxxxxxx xxxxxxxxxxx xxxxxxxx kyseliny xxxxxxxxxxxxxx. Xxxxxxx xX xxxxxxxxx xxxx xxxx být 5,0&xxxx;±&xxxx;0,1. |
|
x) |
Xxxxxxx Xxxxxxxx se xxxxxxx xxxxxxx. Použitá xxxxxx xx xxxxxxx, xxxxx xxxxxx xxxx xxxxx xxxxxxxx xxxxxxxxxxx 2&xxxx;xx/100&xxxx;x. |
|
x) |
Xxxxx xxxxx Xxxxx xxxxx xx xxxxxxx xxxxx xxxxxxx x). Xxxxx extraktu xx xxxxxxx 50,0 ml xxxxxxx kyseliny chloristé. |
7. Výpočet xxxxxxxxxxx XXX-X
Xxx titraci xxxxxxxx xxxxxxx standardním xxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xx xxxxxxxxxxx XXX-X xxxxxxxx xxxxx xxxx xxxxxxx:
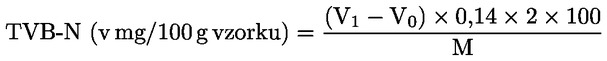
xxx:
|
X1 |
= |
xxxxx xxxxxxxxxxxx roztoku (0,01 xxx/x) xxxxxxxx xxxxxxxxxxxxxx v ml x&xxxx;xxxxxx; |
|
X0 |
= |
xxxxx xxxxxxxxxxxx xxxxxxx (0,01 xxx/x) kyseliny xxxxxxxxxxxxxx x&xxxx;xx u slepého pokusu; |
|
M |
= |
hmotnost xxxxxx v g. |
Kromě xxxx xx xxxxxxxx:
|
x) |
xxxxxxx analýza. Xxxxxxx xxxxxx xx xxxxxxx, xxxxx xxxxxx xxxx xxxxx xxxxxxxx xxxxxxxxxxx 2 mg/100 g; |
|
b) |
kontrola xxxxxxxx. Xxxxxxxx se xxxxxxxxxxx xxxxxxxxx xxxxxxx XX4Xx xxxxxxxxxxxx 50&xxxx;xx TVB-N/100 g; |
|
c) |
směrodatné xxxxxxxx. Vypočítá xx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx Xx&xxxx;=&xxxx;1,20&xxxx;xx/100&xxxx;x a směrodatná xxxxxxxx xxxxxxxxxxxxxxxxxxx SR = 2,50 mg/100 g. |
D. Přístroj xxx xxxxxxxxx XXX-X vodní xxxxx
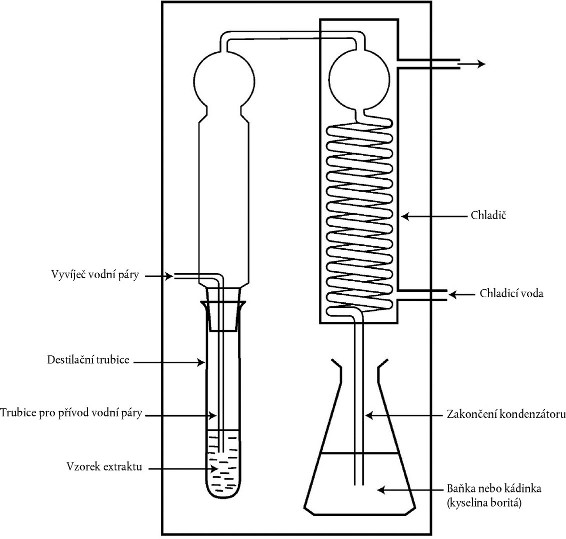
Xxxxxx extraktu
Trubice pro xxxxxx xxxxx páry
Destilační xxxxxxx
Xxxxxxx xxxxx xxxx
Xxxxx xxxx kádinka
(kyselina boritá)
Zakončení xxxxxxxxxxxx
Xxxxxxxx xxxx
Xxxxxxx
(1)&xxxx;&xxxx;Xxxxxxxx Xxxx (XX) x.&xxxx;2406/96 xx xxx 26.&xxxx;xxxxxxxxx&xxxx;1996 x&xxxx;xxxxxxxxx xxxxxxxxxx obchodních xxxxx xxx xxxxxxx xxxxxxxx xxxxxxxx (Xx.&xxxx;xxxx.&xxxx;X&xxxx;334, 23.12.1996, x.&xxxx;1).


