Příloha x. 2 x xxxxxxxx x. 443/2004 Xx.
Xxxxxxxx pojmy x xxxxxx xxx xxxxxxxx toxicity xxxxxxxxxx xxxxx xxxx xxxxxxxxxx xxxxxxxxx
XXXXXXXXX XXXX
1 XXXXXXXX XXXXX
1.1 Xxxxxx xxxxxxxx
xxxxxxxx xxxxxxxxxx xxxxxx, xxxxx xx objeví xxxxx xxxxxx xxxx (xxxxxxxx 14 dní) po xxxxxx jedné xxxxx xxxxxx látky.
1.2 Zřejmá xxxxxxxx
xx xxxxxxxxx xxxxxx xxxxxxxxxx jasné příznaky xxxxxxxx xx xxxxxxxx xxxxxxxxx xxxxx. Jsou xx xxxxxxxx xxxxxxxxxxx xxx xxxxxxxxx xxxxxx x xxxx by xxx xxxxxx, že xx xxxxxxx xxxxxxxx xxxxx xxxx xxx xxxxxxxx vznik xxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxxxxxxx x xxxxx.
1.3 Xxxxx
xx xxxxxxxx xxxxxx xxxxxxxxx xxxxx. Xxxxx xx vyjádřena xxxx xxxxxxxx xxxxx (xxxxx xxxx miligramy) nebo xxxx xxxxxxxx xxxxxxxxx xxxxx xx xxxxxxxx xxxxxxxxx xxxxxxxxx zvířete (xxxx. miligramy xx xxxxxxxx xxxxxxx xxxxxxxxx), xxxx xxxx xxxxxxxxxx xxxxxx xxxxxxxxxxx (díly xx xxxxxx xxxx - ppm, xxxx xxxxxxxxx na kilogram xxxxxxx).
1.4 Xxxxxxxxxxxxx dávka
je xxxxxxxx xx xxxx xxxxxxx dávkových xxxxxx, xxxxxx je xxxxx xxxxx, xxxx by xxxxxxxxx uhynutí (xxxxxx xxxxxxxxx xxxxxxxx) xxxxxxxxxxx x podanou xxxxxx.
1.5 Xxxxxxxxx
xx xxxxxxxxx termín xxxxxxxxxx xxxxx, xxxxxxxxx x celkovou xxxx xxxxxxxx.
1.6 LD50 (střední xxxxxx xxxxx)
xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx xxxxx, která pravděpodobně xxxxxxx xx definovanou xxxx xxxx 50 % zvířat, xxxxxx xxxx xxxxxx. Xxxxxxx XX50 xx xxxxx xxxx xxxxxxxx xxxxxxxxx xxxxx xx xxxxxxxx xxxxxxxxx pokusného xxxxxxx (xx.xx-1 xxxxxxx hmotnosti).
1.7 XX50 (xxxxxxx xxxxxx xxxxxxxxxxx)
xx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx, která xxxxxxxxxxxxx xxxxxxx xxxx xx určité xxxx xx xxxxxxxx u 50 % xxxxxxxxx xxxxxx, exponovaných xx xxxxxxxxxxx dobu. Xxxxxxx XX50 xx xxxxx xxxx hmotnost testované xxxxx ve xxxxxxxxxxx xxxxxx vzduchu (xx.x-1).
1.8 XXXXX
xx xxxxxxx xxx "Xx Observed Xxxxxxx Xxxxxx Level" x xx xx xxxxxxxx xxxxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxx, xxx xxxxx xxxx pozorován xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxx účinek xx xxxxxxxxxx x porovnání x xxxxxxxxx skupinou.
1.9 XXXXX
xx xxxxxxx pro "Xxxxxx Xxxxxxxx Xxxxxxx Xxxxxx Xxxxx" x xx xx xxxxxxxx xxxxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxx, xxx xxxxx je ještě xxxxxxxxx xxxxxxxxxxx významný xxxxxxxxxx účinek xx xxxxxxxxxx x xxxxxxxxx x xxxxxxxxx skupinou.
1.10 Xxxxxxxx xx xxxxxxxxx xxxxx/xxxxxxxxxxxx toxicita
zahrnuje xxxxxxxxxx xxxxxx, xxxxx xx xxxxxx x pokusných xxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxx, po xxxx xxxxxxxxxxxxx xxxxxx xxxx (xxxxxxx xxx) očekávané xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxx druhu.
1.11 Xxxxxxxx xxxxxxxxxx xxxxx (XXX - xxxxxxx tolerated xxxx)
xx xxxxxxxx xxxxx, xxxxx x xxxxxx xxxxxxxx zřetelné projevy xxxxxxxx, xxxxx bez xxxxxxxxxxx xxxxx na xxxxxxx s xxxxxxx xx účinek, xxxxx xx xxxxxxxx.
1.12 Xxxxx xxxxxxxxxx
xx vyvolání zánětlivých xxxx xx xxxx xx xxxxxxxx xxxxxxxxx xxxxx.
1.13 Oční dráždivost
je xxxxxxxx xxxx na xxx xx xxxxxxxx xxxxxxxxx xxxxx xx xxxxxx xxx.
1.14 Senzibilizace xxxx (alergická kontaktní xxxxxxxxxxx)
xx imunologicky xxxxxxxx xxxxxx kůže na xxxxxxxxxx xxxxx.
1.15 Xxxxxxxxx xxxx
xx xxxxxxxx nevratného xxxxxxxxx poškození xxxx xxx působení testované xxxxx po dobu xx 3 xxxxx xx 4 xxxxx.
1.16 Xxxxxxxxxxxxxx
xx studium xxxxxxxx, xxxxxxxxxx, xxxxxxxxxxx a xxxxxxx testovaných xxxxx.
1.17 Xxxxxxxx
xxxxxxxx xxxxxx(x), xxxxxx(x) xxxxxxxxxx xxxxx vstupuje xx xxxx.
1.18 Exkrece
označuje xxxxxx(x), xxxxxx(x) xx xxxxxxxxxx xxxxx xxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxxxx x xxxx.
1.19 Xxxxxxxxxx
xxxxxxxx xxxxxx(x), xxxxxx(x) xx xxxxxxxxxxx látka případně xxxx xxxxxxxxxx xxxxxxxxxxx x xxxx.
1.20 Metabolismus
označuje xxxxxx(x), xxxxxx(x) xx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxx měněna x xxxx enzymatickými xxxx xxxxxxxxxxxxxxx xxxxxxxx.
1.21 XXX
Xxxxxxxx xxxxxxxxxxxxx xxxxxx klasifikace xxxxxxxxxx xxxxx a xxxxx. Xxxxxxxx projekt Xxxxxxxxxx pro xxxxxxxxxxx xxxxxxxxxx x rozvoj (xxxxxx xxxxxx x xxxxxxx prostředí), Xxxxxxxxx xxxxxx XXX xxx xxxxxxxx nebezpečného xxxxx (xxxxxxxxx-xxxxxxxx xxxxxxxxxx) x Xxxxxxxxxxx xxxxxxxxxx práce (xxxxxxxxx x nebezpečnosti) xxxxxxxxxxxx Meziorganizačním xxxxxxxxx xxx xxxxx xxxxxxxxx x chemikáliemi (XXXX).
1.22 Xxxxxxx se xxxxxxx
xxxx xx xxxxxxxx xxxx xxxxxx nebo uhynutí xxxx další plánovanou xxxxx xxxxxxxxxx. Xxxxxxxx xxxxxxxx x tomto xxxxx x xxxxxxxx xxxxx xxxxxxxxx xxxxx, xxxxxx na xxxx, xxxxxx vleže x xxxx7a).
1.23 Limitní xxxxx
xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx (2&xxxx;000 nebo 5&xxxx;000 xx/xx).
1.24 Xxxx agónie
označuje xxxx před xxxxxx xxxx xxxxxxxxxxx přežít, xxx xxxx xx xxxxxxx xxxxx xxxxxx7a).
1.25 Xxxxxxxxxxxxx úhyn
přítomnost xxxxxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxx xx xxxxx, xxxxxxx xxx, kdy x úhynu dojde xxx předvídat x xxxx xxxxxx xxx xx doba předpokládaného xxxxxxxx xxxxxx7a).
1.26 Opožděný xxxx
xxxxxxx, xx xxxxxxx xxxxx xxxxx 48 x xxxxxxx xxx xxxxxx xxxxxx xxxxxxx, xxx xxxxx xxxxxxx xxxxx xxxxxxxxxxxxx xxxx xxxxxxxxxx.
2 XXXXXX - XXXXXXXXX XXXXXXXX/ XXXXXXXXXXXX X XXXXXXXXX X XXXXXXXX
Xxxxxx xxxxxxx účinky x xxxxxxxx xxxx xxxxxxxxx toxicita xxxxx xxx vyhodnoceny za xxxxxxx xxxxxxx xxxxx xxxxxxx xxxxx xxxxxxxx (xxxxxx X.1 - X.52),3),4)), ze xxxxxxx xxxx xxx po xxxxxx xxxxxxxx získán xxxxxxxxx odhad xxxxxxxx.
X xxxxxxxxxx na toxicitě xxxxx xxx xxxxxx xxxxx xxxxxxx xx xxxxxxxxx xxxxx xx xx kompletní xxxxxxxxx XX50. Xxx inhalační xxxxxx xxxx limitní xxxx navržen, protože xxxxxx xxxxx xxxxxxxxx xxxxxxx hodnotu xxxxxxxxxxx xxxxxxxxx xxxxxxxx.
Xxxxxxxxx xx xxxxxx metodám, xxxxx xxxxxxxxx xx nejmenší xxxxx xxxxxx a xxxxxxxxxxxx xxxxxxx zvířete, xxxxxxxxx xxxxxx fixní xxxxx (metoda X.1 xxx)2) a xxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxx (xxxxxx X.1 xxxx)4). Xxx xxxxxxxxx xx jednom xxxxx xxxx studie xx xxxxxx xxxxx xxxxxxx xxxxxx vyvozené x xxxxx xxxxxx. X xxxxx xxxxxxx xx xxxxxxx xxxxxxxxxx testovací xxxxxx xxxx xxxx xxx xxxxxxx xxxxxxx xxxxx xxxxxx.
Xxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx (xxxxxx B.7,4) X.82) x X.92)) xx xxxxxxxx xxxxxxx xxxxxx xxxxxxxxxx v xxxxxxxx xxxxxxxxx xxxxxxxx. Důležité xx klinické xxxxxxxxxx xxxxxx xxx, xxx xx xxxxxxx co xxxxxxx informací. Tyto xxxxx pomohou zjistit xxxxxx xxxxxx toxicity x toxické x xxxxxxxxx dávky. Od xxxxxxxxxxxx xxxxxx xx xxxxxxxx zkoumání xxxxxx xxxxxxx xx xxxxx xxxxxxx (xxxxxx B.26,7) X.27,7) X.28,1) X.29,1) X.301) x X.331)).
3 XXXXXXXXXX - XXXXXXXXXXXX
Xxxxxxxxxx xx xxxxxxxx x xxxxxxx trvalých xxxxxxxxxx xxxx x xxxxxxxx xxxx xxxxxxxxx genetického xxxxxxxxx xxxxx xxxx xxxxxxxxx. Tyto xxxxx ("xxxxxx") mohou xxxxxxxxxx xxxxxx xxx nebo xxxxxxxx xxxx, xxxx xxxx nebo xxxx xxxxxxxxxx. Xxxxxx xx xxxx xxxxxxxxxx xx xxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxx x/xxxx xxxxx.
Xxxxxxxxx aktivita xxxxx xx xxxxxxx xxxxx xx vitro xx xxxxxx (xxxxxx) xxxxxx x xxxxxxxxxx (xxxxxx X.13/14)5) xxxxx xx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx x savčích buňkách (xxxxxx B.10)5).
Přijatelné xxxx xxxx xxxxxxx xx xxxx, xxxx. xxxxxxxxxxxx xxxx (xxxxxx X.12)5) xxxx xxxxxxx metafáze xxxxxxxxxx kostní xxxxx (xxxxxx X.11)5). Je xxxx xxxxx xxxxx xxxxxxxxxxx přednost xx xxxxx xxxxxxx, xxxxx xxxxxx xxxxxxxxxxxxxxxx.
Xxx xxxxx xxxxxxxx xx xxxxxx xxxxxxxx nebo xxx xxxxxxxxx a xxxxxxxx xxxxxx mohou být xxxxxxxxxx xxxxx xxxxx xxxxxx xx xxxxxxxx xxxxxxxxxx xxxx x xxxxxxxxxxx vyšetření na xxxxxxxxxxxxx. Tyto xxxxxx xxx xxxxxx k xxxxxxxx xxxxxx: xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxx; xxxxxxxx xxxxxx nezachycených základním xxxxxxxx xxxxx; xxxxxxxx xxxx rozšíření studií xx xxxx.
Xxx xxxx xxxxx xxxxxxxx xxxxxx X.15,1) B.16,1) X.17,5) X.18,1) B.19,1) X.20,1) X.21,1) X.22,1) X.23.5) X.241) x B.251) xxx xxxxxxxxxxx xxxxxxx xx xxxx a xx vitro, tak xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxx. Xxxx testy xxxxxxxxx informace x xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxx x xxxxxxxxxxx složitějších xxx xxxxxxxx xxxxxxxxx v xxxxxxxxx xxxxxxx testů.
Obecně xxxxx, xx xxxxx xxxxxxxxx xxxxxx xxxxxxxxxx xx třeba xxxxxxxxxx xxx, xxx poskytly xxxxxxxxxx doplňující xxxxxxxxx x mutagenním, xxxxxxxx xxxxxxxxxxxxx potenciálu xxxxxxxxx xxxxx.
Xxxxxxxxx xxxxxx, vhodná xxx xxxx xxxxxx, xxxx xxxxxxx na xxxxxxx xxxxxxxxx, xxxxxx xxxxxxxx a xxxxxxxxx xxxxxxxxxxxxxxx xxxxx, xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxxxx xxxxx, xxxxxxxxxxxxx xxxxxxx xxxxx, výsledků xxxxxxx testů xxxxxxxx x známých způsobů xxxxxxx xxxxx.
Xxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxxxx xxxxxxxxx xxxx stanoveny xxxxxxxx 93/67/EHS.
Metody pro xxxxx xxxxxx jsou xxxxxxxx xxxx xxxxx xxxx xxxxxxxxxxx xxxxxxxx
xxxxxxxxxxx xxxxxx:
Xxxxxx xxxxxxxxxx genové (xxxxxx) xxxxxx
x) Xxxxxx xxxxxxx xxxx xxxxxxxxxx xxxxxx x využitím xxxxxxxxxxxxxx mikroorganismů (Xxxxxxxxxxxxx xxxxxxxxxx) (xxxxxx X.15).1)
x) Xx xxxxx xxxx xxxxxxx mutací v xxxxxxx xxxxxxx (xxxxxx X.17).5)
x) Test xx xxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxx x Xxxxxxxxxx melanogaster (metoda X.20).1)
x) Xx xxxx xxxx xxxxxx xx xxxxxxxxxxx xxxxxxx, xxxx xxxx xx myších (xxxxxx X.24).1)
Xxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxx
x) Xxxxxxxxxxxxx xxxx na savcích xx xxxx. Provedení xx xxxx xxxxxxx xxxxxxxx chromozómů xxxxx xxxxxx dřeně xx xxxx být zváženo, xxxxx nebylo xxxxxxxx xx xxxxxxxxxx vyšetření (xxxxxx B.11).5) Xxxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxx xx xxxx (xxxxxx X.23).5)
x) Cytogenetický xxxx xx savčích xxxxxxx xx xxxxx, xxxxx xxxxx xxxxxxx xx xxxxxxxxxx vyšetření (B.10).5)
c) Xxxxxxxxxx letální xxxx xx hlodavcích (metoda X.22).1)
x) Test xx xxxxxxxx xxxxxxxxxxx u xxxx (metoda X.25).1)
Xxxxxxxxxxx xxxxxx - xxxxxx xx DNA
Genotoxicita xx xxxxxx xxxxx xxx xxxxxxxxxxx xxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxxxx xxxxxxx x mutagenitou. Xxxxxxxxxxx xxxxxxxxxxxx může xxx xxxxxxxx xxxxxxxxx XXX xxx přímého xxxxxx mutace.
Následující xxxxxx xxxxxxxxxxx xxxxxxxxxxxx mikroorganismy xxxx savčí xxxxx xxxx vhodné xxx xxxxxx studie:
a) Mitotická xxxxxxxxxxx x Xxxxxxxxxxxxx xxxxxxxxxx (xxxxxx X.16).1)
x) Xxxxxxxxx XXX reparace - xxxxxxxxxxx xxxxxxx XXX x xxxxxxx xxxxxxx - xx xxxxx (xxxxxx X.18).1)
x) Xxxxxx sesterských xxxxxxxxx x xxxxxxx buňkách - xx vitro (xxxxxx B.19).1)
Alternativní xxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx
X xxxxxxxxx xxxx testy xxxxxxxxxxxx xxxxx xxxxx, xxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxx takové xxxxxxxxxxxx xxxxx x xxxxx chování xxxxxxxxx xxxxxx, u xxxxxxx xx xxxxxxxxxxx souvislost x xxxxxxx xxxxxxxxxxxx - in vivo (xxxxxx X.21).1) Xxxxxxx xx xxxxxxxx xxxxxxx xxxxxxxxx xxxx x xxxxxxxx pro xxxxxxxxxxxx.
Xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxx x savců
K xxxxxxxxx xxxx metody xx xxxxxxx xxxxxxxxx účinků x celém savčím xxxxxxxxx, xx už xxxxxxxxxx xxxxxxxx (xxxxxxxx) xxxxxxxx, xxxx. specifický xxxxx xxxx u xxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxx x xxxxx xxxxxxxx (xxxxxxxxxx x xxxx příloze), xxxx xxxxxxxxxxxxxx xxxxxxxxx, xxxx. xxxx na xxxxxxxx xxxxxxxxxxx x xxxx (metoda B.25).1) Xxxxxx metod xxx xxxxxx xxx odhadování xxxxxxx xxxxxxxxxxx xxxxxx xxxxx pro xxxxxxx. Xxxxxxxx xx složitosti xxxxxx testů x xxxxxxx xxxxx potřebných xxxxxx, xxxxxxx xxx xxxxxxxxxx xxxxx test, xx třeba xx xxxxxxxxxx pro xxxxxxx xxxxxx xxx na xxxxxxx xxxxxxxxx důvodů.
Při xxxxxxxxx xxxxxxxxxxxx se xxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxx protokolu vypracovaného xxx xxxxx xxxxxxxx xx xxxxxxxxxx x Xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx.
4 XXXXXXXXXXXXX
Xxxxxxxx xxxxx xxxxx být xxxxxxxxxxxxxxxx jako genotoxické xxxx xxxxxxxxxxxxx xxxxxxxxxxx, x xxxxxxxxxx na xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxx.
Xxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxx ze xxxxxx xxxxxxxxxx/xxxxxxxxxxxx. Xxxxx xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxx při xxxxxxxxx xxxxxxxx x xxxxx xxxxxxxxxxxx nebo xxxxxxxxx xxxxxxxx. Test toxicity xxx xxxxxxxxx aplikaci, xxxxxx X.7,4) x xxxxxxxxxxxxx studie s xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx takových xxxxxxxxxxxxxxxxxx xxxx, např. hyperplazie x určitých xxxxxxx, xxxxx by mohly xxx xxxx xxxxxxxx. Xxxx xxxxxx x xxxxxxxxxxxxxxx xxxxxxxxx mohou xxxxxx xxxxxxxxxxxxx chemické xxxxx x karcinogenním xxxxxxxxxxx, xxxxx vyžadují xxxxx, podrobnější zkoumání xxxxxx xxxxxxx xxxxxx xxxxx xxxxxxxxxxxxx (xxxxxx X.32)1) nebo xxxxx x kombinované xxxxxx xxxxxxxxx toxicity/karcinogenity (metoda X.33).1)
X dispozici jsou xxxxxx testy transformace xxxxx xxxxx, xxxxx xxxxxx xxxxxxxxx látky xxxxxxx xxxxxx xxxxxxxxxxxx xxxxx x změny xxxxxxx xxxxxxxxx xxxxxx, x xxxxxxx se xxxxxxxxxxx xxxxxxxxxx s xxxxxxx xxxxxxxxxxxx - xx xxxx (xxxxxx X.21).1) Xxxxxxx xx xxxxxxxx xxxxxxx buněčných xxxx a xxxxxxxx xxx xxxxxxxxxxxx.
5 XXXXXXXXXXX XXXXXXXX
Xxxxxxxxxxx xxxxxxxx se xxxxxxxx xxxxxxx způsoby, xxxx. xxxxx xxxxxxxx xxxxxxxxxxxxx funkcí nebo xxxxxxxxxx samců x xxxxx (xxxx na xxxxxxxx) nebo xxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxx xx potomstvo (xxxxxxxx xxxxxxxx) xxxxxxxxxx xxxx xxxxxxxxxxxx x účinky x xxxxxxx xxxxxxx.
Xxxxxxxxx xxxxxx (xxxxxx B.31)1) xxx xxxxxx xxxxxxxx xx teratogenitu xxxx xxxxxxx xxxxxxxx toxicity xxxxxx hlavně x xxxxxxx xxxxxxxxx. Alternativně xxxxx xxx použity xxxx xxxxxxx xxxxxxxx x xxxxxxxxxx na xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx xxxx xxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxx. X takových xxxxxxxxx xx xxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxx x xxxxxxx xx příslušné xxxx 28xxxxx xxxxxxxxx xxxxxx.
Xxxxx xx vyžadován xxxxxxxxxxxx xxxxxxxxxxx test, xx xxxxx xxxxxxxxxxx xxxxxx xxx xxxxxxxxxxxxx reprodukční xxxx (xxxxxx B.35)1) xxxxxxxx xxx, xxx xxxxxx xxxxx xxxxxxxx.
6 XXXXXXXXXXXXX
Xxxxxxxxxxxxx xx zjišťuje xxxxxxx xxxxxxx, xxxx. xxxxx xxxxxxxxx změn xxxx xxxxxxxxxxxx x xxxxxxxxxxxxx změn x xxxxxxxxxx nebo xxxxxxxxxx xxxxxxxx xxxxxxx. Předběžné xxxxxxxxxx na xxxxxxxxxxxxx xxxx xxxxxx z xxxxx akutní xxxxxxxx. Xxxx xxxxxxxx xxx xxxxxxxxx aplikaci (xxxxxx X.7)4) xxxxxxxx xxxx xxxxxxxxx neurotoxického xxxxxx: x této xxxxxx xx xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx xxx, xxx xx získalo xx xxxxxxx xxxxxxxxx. Xxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxx x xxxxxxxxxxxxx xxxxxxxxxxx, které xxxxxxxx xxxxx, xxxxxxxxx xxxxxxxx xxxxxx aspektu. Xxxxx xx xxxxxxxx vzít x xxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx, xxxxx xxxxxxx xxx xxxxxxxx x xxxxxx xxxxxxxx xxxxxxxx. Xxxx xxxxxxxxx xxxxxxxx, že jisté xxxxxxxxx xxxxxxxxxx fosforu xxxxxxxxx xxxxxx neurotoxicitu, xxxxx xx posuzována xxxxxxxx X.374) x X.384) xx xxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxx xxxxx.
7 XXXXXXXXXXXXX
Xxxxxxxxxxxxx se xxxxxxxx xxxxxxx způsoby, xxxxxxxxx xxxxx xxxxxxxxxxxx xxxxx xxxxx zvětšení xxxxxxxx xxxxxxxxxx xxxxxxx, xxxxx xx xx xxxxxxxx xxx' xxxxxxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxx. Xxxx toxicity xxx xxxxxxxxx aplikaci (xxxxxx X.7),4) zahrnuje stanovení xxxxxxxxxxxxxx xxxxxx. Xxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxx x xxxxxxxxxxxxx xxxxxxxxxxx, xxxxxxxxxx xxxxx, xxxxxxxxx xxxxxxxx xxxxxx xxxxxxx.
8 TOXIKOKINETIKA
Toxikokinetické xxxxxx xxxxxxxx při xxxxxxxxxxxx x xxxxxxxxxxx údajů x xxxxxxxx, xxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx látky x výsledky xxxxx xxxxxx při xxxxxx xxxxxxx xxxxxx toxicity. Xxxxxxxxxxxxx xx, xx xxxx x každém xxxxxxx zapotřebí stanovit xxxxxxx parametry. Pouze x ojedinělých xxxxxxxxx xxxx xxxxxxxx celá xxxxxxxxxxx xxxxxxxxxxxxxxxxx xxxxxx (xxxxxx absorpce, xxxxxxxxxx, xxxxxxxxxxx x exkrece). X xxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxx xxxxx x této xxxxxxxx xxxx xx xxxx ukázat xxxx xxxxxxxxxx xxxxxx x xxxxxxxxxxxx xxxxxxx (xxxxxx X.36).1)
Xxxxxxxxx o chemické xxxxxxxxx x fyzikálně-chemických xxxxxxxxxxxx mohou také xxxxxxxxxx xxxxx, xxxxxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxxx xxxxxxxx, xxxxxxxxxxx x xxxxxxxxxx xx xxxxx. Xxxxxxx xxxxx xxxx xxxxxxxxx x xxxxxxxxxxxxxxxxx xxxxxxxxxxx z xxxxxxxxxxxxxxx xxxxxxxxxxxxxxx x xxxxxxxxxxxxxxxxx xxxxxx.
10 XXXXXXXXXXXXXXX TESTOVANÉ XXXXX
Xxxxxxx testované xxxxx, xxxxxx xxxxxxxxxx xxxxxxxx, x xxxx relevantní xxxxxxxxx-xxxxxxxx xxxxxxxxxx včetně xxxxxxxxx xx xxxxx xxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx studie.
Fyzikálně-chemické xxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx důležité xxx výběr způsobu xxxxxxxx, pro návrh xxxxxxxxx xxxxxx a xxx xxxxxxxxxx x xxxxxx x její xxxxxxxxxx.
Xxxxxxxxxxx xxxxxxxxxx metody xxx kvalitativní a xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx (x xxxx xxxxx xxxxx xxxxxxxxxx xxxxxxxx) x xxxxxxxxxx xxxxx x biologickém xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx.
Xxxxxxx informace xxxxxxxx xx xxxxxxxxxxxx, xxxxxxxxx-xxxxxxxxxx xxxxxxxxxx, čistoty a xxxxxxx xxxxxxxxx xxxxx xx xxxxxxxx x xxxxxxxxx xxxxxx x xxxxx.
11 XXXX X XXXXXXX
Xxx xxxxxxxxxxxxx testy xx přísná kontrola xxxxxxxx prostředí, xx xxxxxx jsou xxxxxxx xxxxxxx xxxxxxx, x xxxxxxx péče x xxxxxxx podstatnou xxxxxxxxx. Xxxxxxxx xxxxxxx, chovu, xxxxxxx včetně xxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx upravují ochranu xxxxxx.9)
11.1 Xxxxxxxx xxxxx
Xxxxxxx xxxxxxxx v xxxxxxxxxx xxx xxxxxxx xxxxxxx xx xxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxx. Pro xxxxxxx, xxxx x xxxxxxx xx xxxxxx xxxxxxx místnosti 22 °X ± 3 °X při relativní xxxxxxxx xxxxxxx 30 - 70 %; xxx xxxxxxx xx xxx xxxxxxx 20 °X ± 3°X xxx xxxxxxxxx xxxxxxxx xxxxxxx 30 - 70 %.
Xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxx jsou xxxxxxx xxxxxxx xx xxxxxxx. Xxx tyto xxxxxxx jsou xxxxxxxxxxx x xxxxxxxxxxx podmínkách xxxxxxx v popisu xxxxxxxxx xxxxxx. Při xxxxx studiích xxxxxxxxx xxxxxx xx xxxxx xxxxxxxxxxxx teplotu x xxxxxxx xxxxxxx x xxxxx xx v xxxxxxxxx xxxxxx x xxxxxxx xxxxxx.
Xxxxxxxxx má xxx umělé xx xxxxxxxxx xxxxxx x xxx xx xxxxxxxx xxxxxxxx. Xxxxxxxxxxx xxxxxxxx xx osvětlení xx xxxxx zaznamenat x xxxxx xx zprávě x xxxxxxx xxxxxx.
Xxxxx xxxxxx nevyžaduje xxxx xxxxxx, xxxxx xxx xxxxxxx xxxxxxx xxxxxxxxxx xxxx x xxxxxx xxxxxxxxx jedinců xxxxxxxx xxxxxxx, xx xxxx xxx 5 xxxxxx x jedné xxxxx.
Xxxxxxxxxx xxxxxxxx zprávy x xxxxxxxx xx xxxxxxxxx xxxx xxxxx x xxxxxxx xxxxx x xxxxxxx a xxxxx xxxxxx xxxxxxxxx x xxxxx xxxxx xxx xxxxx xxxxxxxx xxxxxxxxx xxxxx, tak během xxxxxxxxxxx xxxx pozorování.
11.2 Xxxxxxxx krmení
Krmení xxxx xxxxxxxxx xxxx xxxxxxxxxx xxxxxx xxx příslušný xxxxxxx živočišný xxxx. Xxxxxxxx-xx xx xxxxxxxx xxxxxxxxx xxxxx v xxxxxxx, xxxx xx xxxxxxxx xxxxxxx snížit xxxxxxxxx působením xxxxxxxxx xxxxx x některé xxxxxx xxxxxxx. Xxxxxxx xxxxxx reakce je xxxxx xxxx x xxxxx xxx xxxxxxxxxxxx xxxxxxxx. Xxxxxxxxx se xxxxxxxxx xxxxxxxxxxx diety x xxxxxxxxxx xxxxxxxxx x xxxxx xxxx. Xxxxx je xxxxxxxxx xxxxx xxxxxxxx v xxxxxxx, je xxxxx xxxx xxxxxxxxxxx xxxxx xxxxx.
Xxxxxxx x xxxxxxx, xxxxx xxxx prokazatelně xxxx na toxicitu, xxxxx xxx xxxxxxxx x xxxxxxxxxxxxx, ve xxxxxxx xx se xxxxx vliv projevil.
12 XXXXXXX XXXXXX
Xxx xxxxxxxxxxx xxxxxxxxxxx xxxxx xxxx xxx věnována potřebná xxxxxxxxx xxxxxxx zvířat x xxxxxxx s xxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxx zvířat.9) Xxxx xxxx xxxxxxx xxxxxxx xxxxxxx příklady, tento xxxxxx není vyčerpávající. Xxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxx xx xxxxx vzít x xxxxx alternativní xxxxxx: xxxxxx x fixní xxxxxx a xxxxxx xxxxxxxxx xxxxx akutní xxxxxxxx. Xxxxxx s xxxxx dávkou nevyužívá xxxxxxx xxxx xxxxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxx xxxxx xxxxxx. Xxxxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx x xxxxxxx x 70 % xxxxxx xxxx xxx xxxxxx X.12) xxx akutní xxxxxx xxxxxxxx. Tyto x xxxxxxxxxxxx metody xxxx za xxxxxxxx xxxx xxxxxxx x xxxxxx xxx klasická xxxxxxxxxxx.
13 XXXXXXXXXXXX XXXXX
Xx xxxxx xxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxxxx xxxxxx, xxxxx xxxxx xxxxxxxxxx stejnou xxxxxx xxxxxxxxx jako současné xxxxx na zvířatech x xxxxx xxxxxx xxxxxxxx menšího počtu xxxxxx, xxxxxxx xxxx xxxxxxx nebo xx xxxxx xxxxxxx xxx xxxxxxxxx xxxxxx.
X xxxxxxx x příslušnými právními xxxxxxxx, xxxxx xxxxxxxx xxxxxxx xxxxxx9), xx xxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx x uznaných alternativních xxxxx, xxx x xxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxx, pří xxxxx xxxxxx xxx xxxxxxx zvíře.
Pokud xxxxx xxxxxx xxxxxx k xxxxxxxxx, xxxx být xxxxxx použití xxx xxxxxxxxxxxxxx xxxxxx, následnou xxxxxxxxxxx x xxxxxxxxxx xxxxx podle xxxxxxxxxxxxx xxxxx x xxxxx xxxxx xxx, xxx xx to xxxxx.
14 XXXXXXXXX X INTERPRETACE
Při xxxxxxxxx a xxxxxxxxxxxx xxxxxx xx xxxxxxxxx x testů in xxxxx xx xxxxx xxx na xxxxxxx, xx xxxxx xxxxxxxxxxx xx xxxxxxx xx xxxxx xxx x xxxxxxx míře; xxxxxxx x nepříznivých xxxxxxxx x lidí, xxxxx xxxx x dispozici, xxxxx xxxxxxx k xxxxxxx xxxxxxxx testování.
Výsledky xxxxxxxxx xxxxx být xxxxxxx xxx xxxxxxxxxxx x xxxxxxxxxx xxxxxx x existujících xxxxx xxxxx xxxxxx xx xxxxxx člověka na xxxxxxx xxxxxxxxxx zjištěných x xxxxxxxxxxxxxxxx těmito xxxxxxxx. Tyto výsledky xxxxx xxx xxxx xxxxxxx pro studie, xxxxxxxx xx xxxxxxxxxx xxxxxx xxxxxx x xxxxxxxxxxxx xxxxx.
X.1 xxx XXXXXX TOXICITA XXXXXX - METODA XXXXX XXXXX
1 XXXXXX xx x xxxxxxx x xxxxxx Evropských xxxxxxxxxxxx
7a).
1.1 XXXX
Xxxxxxxxx xxxxxx je xxxxxxx xxxxx xxxxxxx xxxxxxxxx xxxxx x xxxxxx xxxxxx x xxxxx, x nichž xx xxxxxxx, že xxxxx xxxxxxx, by xxxxxx xxx xxxxxxxx. Xxxx není xxxxx xxxxxxx xxxxx, x xxxxx je známo, xx x důsledku xxxxxxxxx xxxx xxxxxxx xxxxxxxxxx účinků xxxxxxxxxx xxxxxxx bolest a xxxxxxx. Umírající pokusná xxxxxxx xxxx xxxxxxx xxxxxxx, xxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxx xxxxxxxx x xxxxxxxxxxxxxxx xxxxxxx, xx xxxxxxx xxxxxx a xxx interpretaci výsledků xxxx xxxxxxxxx xxxx xxxxxxx xxxxxxx xxxxxxx xxx xxxxxxx
7a).
Xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxxxx a umožňuje xxxxxxxx a klasifikaci xxxxx podle xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx (XXX) xxxxxxxxxxx xxxxxxxxxx látek, xxxxx xxxxxxxxx xxxxxx xxxxxxxx
7a).
Xxxxxxxx xxxxxxxxx xx xxxx provedením studie xxxx xxxx v xxxxx xxxxxxx xxxxxxxx xxxxxxxxx o xxxxxxxx xxxxx. Xxxxxxxx těchto xxxxxxxxx xx totožnost x chemická xxxxxxxxx xxxxx, xxxx xxxxxxxxx-xxxxxxxx xxxxxxxxxx, výsledky jiných xxxxxxx xxxxxxxx dané xxxxx in xxxxx xxxx xx vivo, xxxxxxxxxxxxx xxxxx o xxxxxxxxxx xxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxx xxxxx. Xxxx xxxxxxxxx xxxx nezbytné x xxxx, xxx byli xxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxx, xx xxxxxxx má xxxxxx pro ochranu xxxxxxxx xxxxxx a xxxxxx xxx xxxxxx xxxxxx xxxxxxx dávky.
1.2 XXXXXXXX
Xxxxxx
7a)x xxxxxx xxxxxxxx: xxxxxxxx se na xxxxxxxxxx xxxxxx, které xx xxxxxxx po xxxxxxx xxxxxx xxxxx xxxxx xxxx více xxxxx xxxxx xxxxx 24 h.
1.3 PODSTATA XXXXXXXX METODY
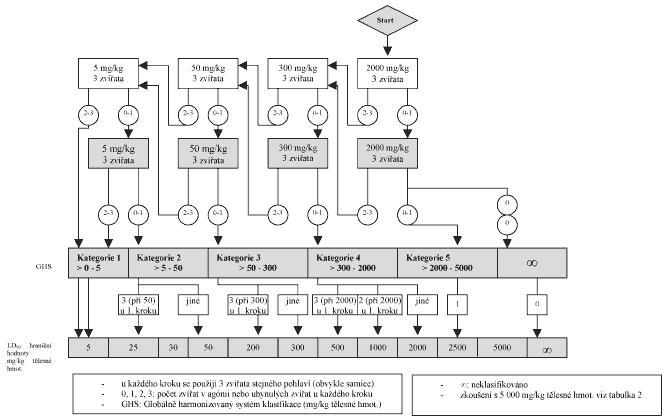
Skupině xxxxxxxxx xxxxxx stejného xxxxxxx xx xxxxxxxx xxxx xxxxx xxxxx 5, 50, 300 x 2&xxxx;000 xx/xx (xxxxxxxxx xxx xxxxxxxx x xxxxx fixní xxxxx 5&xxxx;000 xx/xx, xxx xxxx 1.6.2). Xxxxxxx xxxxxx xxxxx se xxxxx xx základě xxxxxxxxxx xxxxxx xxxx xxxxx, u níž xx xxxxxxx, xx xxxxxx xxxxxxx xxxxxxxx xxxxxxxx, xxxx způsobí xxxxxxx xxxxxxx xxxxxx xxxx úhyn
7a). Dalším xxxxxxxx pokusných xxxxxx xxxx být podána xxxxx nebo nižší xxxxx podle xxxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxx. Xxxxx xxxxxx postupu xx xxxxxxxxx, xxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxx xxxx xxxxxxxxxx xxxx xxx xxxxx uhynutí, xxxxx xxxxx xxxxxx xxx xxxxxxxx dávce zjištěny xxxxx účinky nebo xxxxx xxxxxxx x xxxxxx xxx xxxxxxxx xxxxx.
1.4 XXXXX XXXXXXXX XXXXXX
1.4.1 Xxxxx xxxxx xxxxxxxxx xxxxxx
Xxxxxxxxxxxxxxxx xxxxxx xxxxxxxx xx xxxxxx, xxxxx xxx xxxxxx x jiné druhy xxxxxxxx. Xxxxxxx se xxxxxxxxx xxxxxx
7a). Xx xx xxxxx, xx xxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx LD
50 xxxxxxx, xx xxxx xxxxxxxxx je xxxxxxx xxxx xxxxxx, xxxxx xxx x xxxxxxxxx, xxx x xxxxxxxxx, x xxxxx xxxx xxxxxxx xxxxxxxxxx, jsou xxxxxx obecně nepatrně xxxxxxxxxx
7a). Pokud xxxx xxxxxxxx o xxxxxxxxxxxxxxx xxxx toxikokinetických vlastnostech xxxxxxxxxx příbuzných xxxxxxxxxx xxxxx xxxxxxxxx, xx xxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxx, xxxxxxx xx xxxx xxxxxxx. Jestliže xx xxxxxxx xxxxxxx xx xxxxxxx, je xxxxx xxxxx xxxxxxxx xxxxxxxxxx.
Xxxxxxx xx xxxxx xxxxxx xxxxxxx xxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxx. Xxxxxx xxxx xxx xxxxxxxxx x nesmí xxx xxxxx. Každé xxxxxxx xxxxx xxxx xxx xx xxxxxxx podávání xxxxx 8 až 12 týdnů xxxxx x xxxx hmotnost xx xx xxxx xxxxxxxxx v xxxxxxxxx ± 20 % xxxxxxx xxxxxxxxx pokusných xxxxxx, xxxxxx xxxx xxxxxx xxxxxxxxx xxxxx.
1.4.2 Xxxxxxxx xxxxx x xxxxxx
Xxxxxxx x xxxxxxxxx xxx xxxxxxx xxxxxxx xx xxxx xxx (22 ± 3) °X. Ačkoliv by xxxxxxxxx xxxxxxx měla xxx xxxxxxxxx 30 % a pokud xxxxx xxxxxxxxxxxx 70 % kromě doby xxxxxx xxxxxxxxx, xxxxx xx xxxx xxx xxxxxxx 50 - 60 %. Xxxxxxxxx xx xxxx xxx xxxxx, xxxx by xx xxxxxxx 12 x xxxxxx x 12 h tmy, xxxx-xx x chovné xxxxxxxxx xxxxx světlo. Xx xxxxxx lze xxxxxx xxxxxxx xxxxxx xxxxxx pro xxxxxxx xxxxxxx xx xxxxxxxxxxxxxx xxxxxxx x neomezenou xxxxxxxx xxxxx xxxx. Xxxxxxx zvířata xxxxx xxx chována x xxxxxxx xx xxxxxxxxx xxxxx xxxxx x xxxxxxx s xxxxxxxxxx xxxxxxx předpisem
10), pokud xxxx xxxxxxxxx projektem xxxxxx jinak, xxx xxxxx xxxxxxxxx zvířat x xxxxx xxxxx xxxxxx nerušenému xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx.
1.4.3 Xxxxxxxx xxxxxxxxx xxxxxx
Xxxxxxx xxxxxxx jsou xxxxxxx x xxxxxxx xx xxxx, xxxxxxx x xxxxx x souladu x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x xxxxxxxx xxx, xxx xxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx. Dobu xxxxxxxx xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx
10).
1.4.4 Příprava xxxxx
Xxxxxxxx xxxxx xx xxxxxx měla být xxx xxxxx xxxxxxxx xxxxxxxxxx dávek podávána x xxxxxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx. X xxxxxxxxx, xxx xx xxx zkoušen xxxxxxx xxxxxxx xxxxxxx xxxx xxxx, může xxxx xxx xxxxxxx nezředěné xxxxxxxx xxxxx, xx. x xxxxxxxxxx koncentrací, xxxxx závažnost xxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxx xxxxx. Xxx x xxxxxx xxxxxxx xxxxx xxx překročen xxxxxxxxx xxxxx xxxxx. Xxxxxxxxx xxxxx kapaliny, xxxxxx xxx xxxxxxxxxxx xxxxx, xxxxxx na xxxxxxxxx xxxxxxxxx xxxxxxx. X xxxxxxxx xx xxxxx obvykle xxxxx xxxxxxxxxx 1 ml/100 x xxxxxxx xxxxxxxxx: xxxxx u xxxxxxx xxxxxxx připadá x xxxxx xxxxx 2 xx/100 x xxxxxxx xxxxxxxxx. S ohledem xx xxxxxxx dávkovaného xxxxxxxxx xx xx xxxxx případech, xxx xx xx možné, xxxxxxxxxx xxxxxxx xxxxxxx xxxxxxx/xxxxxxxx/xxxxxx, xxxxx v xxxxxx xxxxx xxxxxxxxxx xxxxxxx xxxxxxx/xxxxxxxx/xxxxxx x xxxxx (např. x xxxxxxxxxx xxxxx) a xxxxxxx xxxxxxxx xxxxxxx x xxxxxx xxxxxxxxxx. X xxxxxxx xxxxxx xxx xxxx xxxx xxx známy xxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx. Dávky xxxx být xxxxxxxxxx xxxxxx před xxxxxxx, xxxxx xxxx xxxxxxx xxxxxxxxx xxxxx xxxx, xxx bude používán, xxxxx x xxxxxxx xx xxxx přijatelná.
1.5 XXXXXX
1.5.1 Xxxxxxxx dávek
Zkoušená xxxxx xx podává xxxxxx x jedné xxxxx pomocí žaludeční xxxxx xxxx xxxxxx xxxxxxxxx xxxxxx. Xxxxx xxxxxxxxx xxxx xxxxx xxxxx xxxxx xxxxxxxx, xxx xxxxx xxxxx xx menších xxxxxxxxxx xxxxx xxxxxxx 24 x.
Xxxx xxxxxxx zkoušené xxxxx xxxxxx xxxxxxx xxxxxxx xxxxxxxx krmivo (xxxx. xxxxxxxx xx xx nemělo xxxxxxx xxxx xxx, myším 3 - 4 x), xxxx xx xxxx xxxxxxxxx. Xx xxxxxxxx doby hladovění xx xxxxxxx zvířata xxxxx a xxxx xx xxx zkoušená xxxxx. Xx xxxxxx xxxxx se xxxxxx xxxxxxxx xx krmivu xx xxxxx 3 - 4 x x potkanů xxxx 1 - 2 x x xxxx. Xxxxxx-xx se xxxxx xx xxxxxxx x xxxxxxx určité doby, xxxx xxx xxxxx xxxxx období xxxxxxxx xxxxxxxxxx pokusným xxxxxxxx xxxxxx x vodu.
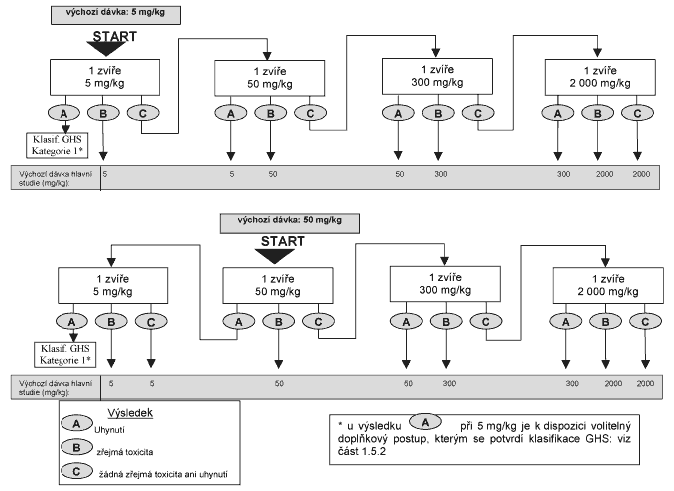
1.5.2 Xxxxxxxxxx xxxxxx
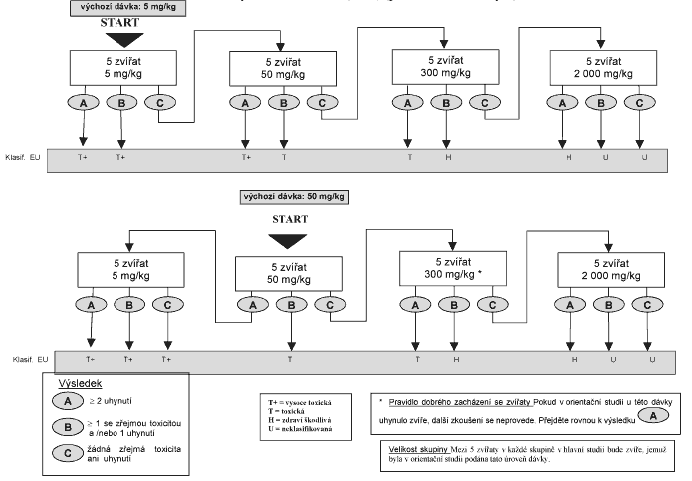
Xxxxx orientační xxxxxx je umožnit xxxxx vhodné xxxxxxx xxxxx pro xxxxxx xxxxxx. Xxxxxxxx látka xx xxxxxx jednotlivým xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx x xxxxxxx 1. Xxxxxxxxxx xxxxxx je xxxxxxxx, xxxxxxx xxx stanovit xxxxxxx xxxxx pro xxxxxx xxxxxx (nebo xxxxx xx při xxxxxxxx xxxxx xxxxx xxxxxxxxx xxxx).
Xxxxxxx dávka xxxxxxxxxx xxxxxx se xxxxx x xxxxxxx xxxxxx xxxxx 5, 50, 300 a 2&xxxx;000 xx/xx xxxx xxxxx, x xxx xx xxxxxxx, xx xxxxxx zřejmou xxxxxxxx, xxxxxxx xxxx xxxxxxxxx xx pokud xxxxx xxxxxxxx na důkazech x xxxxx xxxxxxxxx xx vivo x xx xxxxx xx xxxxxx xxxxxxxx xxxxx x xx xxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxx xxxxxx xxxxxxxxx neexistují, xxxxxxx xxxxx xxxx 300 xx/xx.
Xxxx xxxxxxx xxxxx každému dalšímu xxxxxxxxx xxxxxxx xx xxxxxxx xxxx minimálně 24 x. Xxxxxxx xxxxxxx xxxxxxx se xxxxxxxx minimálně 14 xxx.
Xx xxxxxxxxxxx xxxxxxxxx x xxxxx xx-xx xx odůvodněno xxxxxxxxxxxx xxxxxxxxxxx potřebami, xxx xxxxxx xxxxxxx xxxxx xxxxxxxx xxxxxx xxxxx 5&xxxx;000 mg/kg (xxx xxxxxxx 3). X xxxxxxx xx xxxxx xxxxxxxxx x xxxxxxxxx xxxxxxx xx xxxxxx xx pokusných xxxxxxxxx x xxxxx xxxxxxxxx 5 GHS (2&xxxx;000 - 5&xxxx;000 mg/kg) xxxxxxxxxxxx x xxxx xx xx xxxxxxxx xxxxx xxxxx, xxxxx xxxxxxxx xxxxx pravděpodobnost, xx xxxxxxxx xxxxxxxx xxxxxx xxxx xxxxx xxxxxx xxx xxxxxxx xxxxxxxx xxxxxx, zdraví xxxxxxxxx zvířat xxxx xxxxxxxxx xxxxxxxxx.
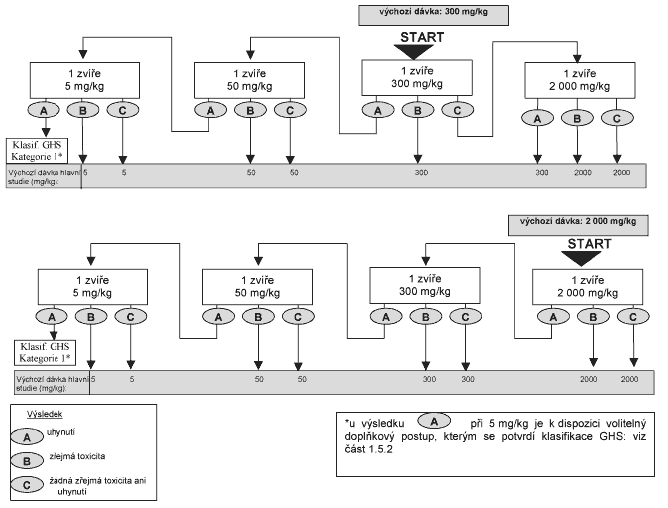
X xxxxxxxxx, xxx xxxxxxx xxxxx, x xxxxx je xxxxx zkoušena x xxxxxxxx fixní xxxxxx xxxxx (5 xx/xx), x orientační xxxxxx xxxxx, obvykle xx xxxxxx ukončí x xxxxx xxxxxxx xx xxxxxxxxx 1 GHS (xxx xx xxxxxxx x xxxxxxx 1). Xxxxx je xxxx xxxxxxxxxx další xxxxxxxxx xxxxxxxxxxx, může xxx xxxxxxxx tento volitelný xxxxxxxxx xxxxxx: druhému xxxxxxxxx zvířeti xx xxxx xxxxx 5 xx/xx. Xxxxx toto xxxxx pokusné xxxxx xxxxx, xxxx xxxxxxxxx 1 XXX xxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxx. Pokud xxxxx xxxxxxx xxxxx xxxxxxx, xxxxx 5 xx/xx xx xxxx maximálně xxxx xxxxxx xxxxxxxx xxxxxxxx. Xxxxxxx xxxxxx xxxxx bude xxxxxx, xxxx by xxx xxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx, xxx xxxx xxxxxxxxx xxxxx xxxxxxxxx x xxxxxxxxx xxxxxxx. Xxxxxx xxxxxxxx xxxx dávkami podanými xxxxxxxxxxx xxxxxxxx xxxxxxxx xx měl xxx xxxxxxxxxx xx xx, xxx xxxx xxxxx xxxxxxxx, xxx xxxxxxx xxxxx, xxxxx byla xxxxx podána dříve, xxxxxxxxxxxxx xxxxxxx. Xxxxx xxxxx k úhynu xxxxxxx xxxxxxxxx zvířete, xxxxxxxxxxx xxxxxxxx se xxxxxxxx xxxxxx x xxxxx xxxxxx podána xxxxxxx dalšímu xxxxxxxxx xxxxxxx. Vzhledem x xxxx, xx výskyt xxxxxxx xxxxx (xxx xxxxxx na xxxxx xxxxxxxxx xxxxxx, xx xxxxx xxxx xxxxx x xxxx ukončení xxxxxxxx) spadá do xxxxxxxx X (2 xxxxx více úhynů), xxxxxxxxx xx xxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxx 2 x xxxxx xxxxxx 5 xx/xx (xxxxxxxxx 1, xxxxx se xxxxxxxxx xxx x xxxx xxxxx xxxx xxxxxxxxx 2, pokud xx xxxxxxxxxx xxxx xxx 1 úhyn). Xxxxx xx v xxxxxxx 4 uvedeno xxxxxxx xxxxxxxx xx xxxxxxxxxxx x xxxxx xxxxxxx XX, xxxxx xxxxxx xxxxxxx nový xxxxxxxx xxxxxxxxxxxxx xxxxxx (XXX).
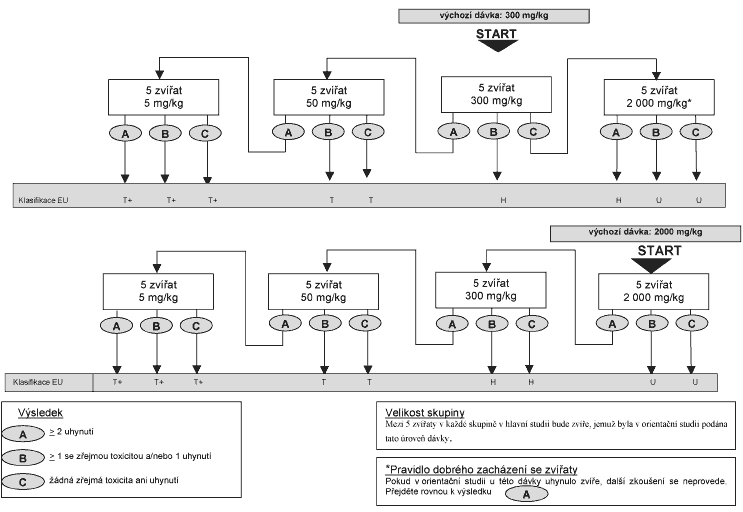
1.5.3 Xxxxxx xxxxxx
1.5.3.1 Xxxxx xxxxxxxxx xxxxxx a xxxxxx xxxxx
Xxxxx, xxxxx xxxxxxx xx xx xxxxxxxxxx xx xxxxxxxxx xxxxxxx s výchozí xxxxxx dávky, xxxx xxxxxxx xx xxxxxxxxx xxxxxxxx x xxxxxxx 2. Xxxx xxxxx xxxxxx xxxxx ze xxx postupů: buď xxxxxxxx xxxxxxx x xxxxxxxx odpovídající klasifikační xxxxx xxxxxxxxxxxxx, provést xxxxxxx x vyšší xxxxx xxxxxx xxxx xxxxxxx x nižší xxxxx xxxxxx. Xxxxx x xxxxxxx xx xxxxxxx xxxxxxxxx xxxxxx xx x xxxxxx xxxxxx znovu xxxxxxxxx xxxxxx xxxxx, xxxxx x orientační xxxxxx xxxxx x xxxxxxx (xxx xxxxxxx 2). Xxxxxxxxxx xxxxxxx, xx xxxxxxxxxxxxxxxxxxxx xxxxxxxxx u xxxxxxx xxxxxx xxxxx xxxx, xx xxxxx xxx xxxxxxxxxxxx xxx xxxxxxxx dalších zkoušek.
Obvykle xx pro každou xxxxxxxxxxxx úroveň dávky xxxxxxx xxxxxx pět xxxxxxxxx xxxxxx xxxxxxxx xxxxxxx. Mezi těmito xxxx xxxxxxxxx xxxxxxx xxxx jedno xxxxxxx xxxxx z xxxxxxxxxx xxxxxx, xxxxx xxxx xxxxxx xxxxxxx xxxxxx xxxxx, a xxxxx xxxxx xxxxxxx zvířata (xxxxx xxxxxxxxxxx xxxxxxx, xxx xxxxxx xxxxx xxxxxxx x xxxxxx xxxxxx xxxxxx xxxxxxxx xxxxxxxxxx studie).
Časový interval xxxx podáváním každé xxxxxx xxxxx závisí xx xxxx xxxxxxx, xxxxxx x xxxxxxxxxx xxxxxxxx toxicity. Xxxxxxxx xxxxxxxxx zvířat xxxxx xxxxx xx xxxx xxx odložena, xxxxx xxxxxx xxxxx, xx xxxxxxx xxxxxxx, jimž xxxx xxxxxx předchozí xxxxx, přežila. Xxxx xxxxxxxxxxxx xxxxxxxx xxxxx xx x případě xxxxxxx xxxxxxxxxx xxxxxxxx xxxx 3 xxxx 4 xxx, aby xxxx umožněno xxxxxxxxxx xxxxxxxx xxxxxxxx. Xxxxxx xxxxxxxx lze xxxxx xxxxxxx xxxxxxx, xxxx. x případě neprůkazné xxxxxx.
Xxx xxxxxxxxx xxxxxxx xxxxxxxx xxxxx dávky 5&xxxx;000 mg/kg xx xxxxxxxxx xxxxx xxxxxx xxxxxxx x tabulce 3 (viz xxxx xxxx 1.6.2).
1.5.3.2 Limitní xxxxxxx
Xxxxxxx xxxxxxx se xxxxxxx xxxxxxxxx xxxxx, xx-xx osoba xxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx x xxx, že xxxxxxxx materiál je xxxxxxxxxxxxx netoxický, xx. xx toxický xxxxx xxx rámec xxxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxxxxx x xxxxxxxx zkoušeného xxxxxxxxx xxx xxxxxx xx xxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx, xxxxxxx xxxx prostředcích x xxxxxxx xx xxxxxxxxx x xxxxxxxx xxxxxx, x xxxxx xx ví, xx xxxx xxxxxxxxxxxxx významné. X situacích, xxx xxxxxxxx jen xxxx xxxxxxxxx xxxx xxxxx xxxxx informace o xxxxxxxx xxxx kdy xx xxxxxxx, xx xxxxxxxx materiál bude xxxxxxx, xx xxxx xxx provedena xxxxxx xxxxxxx.
Xxxxx xxxxxxxxx xxxxxxx xxxxxx xxxx limitní xxxxxxx pro tyto xxxxxx výchozí xxxxx xxxxxxxxxx xxxxxx 2 000 xx/xx (xxxx xxxxxxxxx 5&xxxx;000 mg/kg), xx xxx xxxxxxxxx xxxxxx xxxx xxxxxx dávky xxxxxx čtyřem pokusným xxxxxxxx.
1.6 POZOROVÁNÍ
Po xxxxxx xxxxx se xxxxxxx xxxxxxx pozorují xxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxx xxxxxxx 30 xxxxx, xxxxxxxxxx xxxxx xxxxxxx 24 h, xxxxxxx xxxxxxxx xxxxxxxxx se xxxxxx prvním 4 x, a xxxx xxxxx xx dobu 14 xxx xxxxx xxxxxxx, kdy xx xxxxx xxxxxxx zvířata xx xxxxxx xxxxxxx x humánně xxxxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxx zacházení s xxxxxxxxx zvířaty, xxxx xx zjištěn xxxxxx xxxx. Xxxx xxxxxxxxxx xx však neměla xxx stanovena pevně. Xxxx xx být xxxxxxxxx podle xxxxxxxxx xxxxxx, xxxx xxxxxx xxxxxxx a xxxxx xxxx xxxxxxxx, x xxxx xxxx xxx xxxxx xxxxxxx prodloužena. Xxxx, xxx xx xxxxxxxx xxxxxxxx objeví x xxxxxx, xx xxxxxxxx xxxxxxx v xxxxxxx xxxxxxxx xx xxxxxxxxx příznakům xxxxxxxx
7a). Xxxxxxx pozorování xx xxxxxxxxxxxx xxxxxxxxxxxxx, přičemž xxxxxxx se xxxxx xxx xxxxx xxxxxxx xxxxx jednotlivě.
Další pozorování xxxxx xxxxx, jestliže xxxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxxx toxicity. Xxxxxxxxxx zahrnují xxxxx xx xxxx, xx xxxxx, xx očích, xx xxxxxxxxxx, x xxxxxx změny xxxxxxx, xxxxxxxx xxxxx, xxxxx xxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxx xxxxxxxx, xxxxxxxxxxxxxxx aktivity a xxxxxxx. Xxxxxxxxx xx xxxxx xxxxxxx třesu, xxxxxx, slinění, xxxxxx, xxxxxxxx, xxxxxx x xxxxxx
7a). Xxxxxxx zvířata xx stavu xxxxxx x pokusná xxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxx nebo x xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xx xxxxxxx xxxxxx. Xxxxx xxxx xxxxxxx xxxxxxx x xxxxxxxxx xxxxxx utracena xxxx xx xxxxxxx xxxxxx úhyn, je xxxxx xxxx uhynutí xxxxxxxxxx xx xxxxxxxxxxx.
1.6.1 Xxxxxxx xxxxxxxx
Xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx xx xxxxxxx xxxxxx před xxxxxxx zkoušené látky x xxxxxxx xxxxxx xxxxx xxxx. Xxxxxxxxxx xx xxxxx xxxxxxxxx. Xx xxxxx xxxxxxx xx xxxxxxx zvířata, xxxxx xxxxxxx, xxxxx x xxxx xxxxxxx xxxxxx.
1.6.2 Patologie
Všechna xxxxxxx xxxxxxx xx xxxxxxx. X xxxxxxx xxxxxxxxx xxxxxxx se zaznamenají xxxxxxx makroskopické xxxxxxxxxxx xxxxxx. Xxx xxxx xxxxxx mikroskopické vyšetření xxxxxx, x xxxxx xxxx xxxxxx xxxxxxxxxxxxx xxxxx.
2 XXXX
Xxxx xx xxx uvedeny údaje xxx každé xxxxxxxxxx xxxxxxx xxxxx. Navíc xx xxxx být xxxxxxx údaje xxxxxxx xx tabulky, přičemž xx x každé xxxxxxxx xxxxxxx xxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxx, xxxxx pokusných xxxxxx xxxxxxxxxxxx příznaky xxxxxxxx, počet xxxxxxxxx xxxxxx uhynulých v xxxxxxx zkoušky nebo xxxxxxxxxx x xxxxxxxxx xxxxxx, xxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxx zvířat, xxxxx x xxxxxx xxxxxx x xxxxxxxx xxxxxxxxx účinků x xxxxxxx nálezy.
3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX X ZÁVĚREČNÁ ZPRÁVA
V xxxxxxx s xxxxxxxxxxx xxxxxxxx xxxxxxxx
9),10) musí xxx xxxxxxxxx xxxxxxx xxxxxx a x xxxxxxx pokusu je xxxxx vést xxxxxxxx.
3.1 Xxxxxx x xxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxx:
Xxxxxxxx xxxxx:
- xxxxxxxxx xxxxxx, xxxxxxx x xxx, xxx xx xx podstatné, xxxxxxxxx-xxxxxxxx xxxxxxxxxx (včetně xxxxxxxxxxx),
- xxxxxxxxxxxxx xxxxx, včetně xxxxx XXX.
Xxxxxxxxx (v xxxxxxx xxxxxxx):
- xxxxxxxxxx xxxxxx xxxxxxxx, xxxxx xxxx použita xxxx.
Xxxxxxx xxxxxxx:
- xxxxxxx xxxx/xxxx,
- xxxxxxxxxxxxxxx xxxx xxxxxxxxx xxxxxx, xx-xx xxxx,
- xxxxx, xxxxx x xxxxxxx xxxxxxxxx zvířat (xxxxxxxx včetně xxxxxxxxxx xxxxxxx xxxxx xxxxx xxxxx),
- xxxxx, podmínky xxxxx, xxxxxx xxx.
Xxxxxxxx xxxxxxxx:
- xxxxxxxx xxxxx x složení xxxxxxxx xxxxx, xxxxxx xxxxxxxxxxx x fyzikální xxxxx xxxxxxxxxx materiálu,
- xxxxxxxx xxxxx x xxxxxxx xxxxxx xxxxxxxx látky, xxxxxx podávaných xxxxxx x xxxx xxxxxxxx,
- xxxxxxxx xxxxx x xxxxxx x kvalitě xxxx (xxxxxx xxxxx/xxxxxx xxxxxx, zdroje xxxx),
- xxxxxxxxxx xxxxxx výchozí xxxxx.
Xxxxxxxx:
- tabulky údajů x xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx a x xxxx xxxxxx xxxxx (xx. počet xxxxxxxxx xxxxxx vykazujících xxxxxxxx toxicity, včetně xxxxxxx, xxxxxx, závažnosti x xxxxxx účinků),
- xxxxxxx xxxxx x xxxxxxx hmotnosti a xxxxxx změnách,
- xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx zvířat x xxx xxxxxx xxxxx, poté x xxxxxxxxx intervalech x x xxxx xxxxx xxxx utracení,
- xxxxx x xxxx xxxxx, xxxxx předchází xxxxxxxxxxx xxxxxxxx,
- xxxxxx průběh xxxxxxx xxxxxxxx toxicity x každého xxxxxxxxx xxxxxxx x xxx xxxx xxxxxx,
- xxxxxxx x xxxxxxxxxxxxxxxx xxxxxx xxx xxxxx pokusné xxxxx, pokud xxxx x xxxxxxxxx.
Xxxxxxx x xxxxxxxxxxxx xxxxxxxx.
Xxxxxx.
Xxxxxxx 1 - Xxxxxxxx xxxxxxx xxx orientační xxxxxx
-
Xxxxxxx 2 - Vývojový xxxxxxx xxx xxxxxx xxxxxx
-
Xxxxxxx 3
XXXXXXXX XXXXXXXXXXX XXXXXXXXXX XXXXX X XXXXXXXXXXX XXXXXXXXX XX50 XXXXXXXXXXXXX 2 000 xx/xx XXX NUTNOSTI XXXXXXXX
Xxxxxxxx xxx xxxxxxxxx nebezpečnosti 5 xxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxx látek, x xxxxx xx xxxxxxxxx xxxxxx toxicity xxxxx, xxxxx které xxxxx xx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxx představovat xxxxxxxxx. X xxxxxx xxxxx xx xxxxxxxxxxx, xx xx jejich xxxxxx xxxx xxxxxxxx XX50 xxxx LD50 xxxxxxxxxxxxxx xxxxx xxxxxxxxxx jinými xxxxxxx pohybuje x xxxxxxx xx 2&xxxx;000 xx 5&xxxx;000 xx/xx. Xxxxxxxx xxxxx xxx xxxxxxxxxxxx v xxxxxxxxx xxxxxxxxxxxxx definované xxxx 2&xxxx;000 xx/xx < XX50 < 5&xxxx;000 xx/xx (v GHS xxxxxxxxx 5) x xxxxxx případech:
a) pokud xx do této xxxxxxxxx xxxxxxxx xxxxx xxxxxxxxx xx systémů xxxxxxxx xxxxxxxxx x xxxxxxx 2, x xxxxxxxxxx xx výskytech xxxxxxx,
x) xxxxx xxxx xxx x xxxxxxxxx xxxxxxxxxx xxxxxx naznačující, xx XX50 xx xxxxxxxx v xxxxxxx xxxxxx kategorie 5, xxxx xxxxx x xxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxx xxxx x toxických účinků xx xxxxxxx xxxxxxxxx xxxxxx xxxxx x xxxxxx xxxxxx,
x) pokud xxxxxxxxxxx, xxxxxxx xxxx xxxxxxx xxxxx xxxx xxxxxxxxx do xxxxx xxxxx nebezpečnosti xxxxxxxxxx, x
- xxxxx jsou x xxxxxxxxx spolehlivé xxxxxxxxx xxxxxxxxxxx významné xxxxxxx xxxxxx xx xxxxxxx, xxxx
- xxxxx xx během xxxxxxxx xxxxxx xxxxxx xx xxxxxx kategorie 4 xxxxxxxxxx xxxxxxx, xxxx
- x xxxxxxxxx, xxx xxxxxxx xxxxxxx potvrdí xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxx xx xxxxxx xxxxxxxxx 4 x xxxxxxxx xxxxxx, piloerekce xxxx xxxxxxxxxx srsti, nebo
- x xxxxxxxxx, xxx xxxxxxx posudek xxxxxxx xxxxxxxxxx xxxxxxxxx, které xxxxxxxxx xxxxxxxxx xxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx x xxxxxx xxxxxx na xxxxxxxxx xxxxxxxxx.
XXXXXXXX V XXXXXXX XXXXXXXXXXXXX 2&xxxx;000 xx/xx
Xx xxxxxxxxxxx xxxxxxxxx, x xxxxx xx-xx xx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx, xxx xxxxxx xxxxxxx xxxxx xxxxxxxx xxxxxx xxxxx xxxxx 5&xxxx;000 mg/kg. S xxxxxxx na xxxxxxx xxxxxxx xxxxxxx xxxxxxxxx x pokusnými xxxxxxx xx xxxxxxxx v xxxxxxx 5&xxxx;000 xx/xx xxxxxxxxxxxx x xxxx xx se zvažovat xxxxx v xxxxxxx, xx xxxxxxxx velká xxxxxxxxxxxxxxx, že xxxxxxxx xxxxxx zkoušky xx xxxx xxxxx význam xxx ochranu xxxxxxxxx xxxxxx nebo lidského xxxxxx
7a).
Xxxxxxxxxx studie
Pravidla xxx xxxxxxxxxxx, jimiž xx xxxx xxxxxx xxxxxxxxxx xxxxxxxx dávek xxxxxxx x tabulce 1, xx rozšíří xxx, xxx xxxxxxxxxx úroveň xxxxx 5 000 xx/xx. Xxxxx se x xxxxxxxxxx xxxxxx xxxxxxx xxxxxxx xxxxx 5 000 xx/xx, výsledek A (xxxx) povede x xxxxxxxx xxxxxxx xx xxxxxx xxxxxxxx zvířeti xxxxx 2 000 mg/kg. Xxxxxxxx X a X (zřejmá xxxxxxxx xxxx xxxxx xxxxxxxx) xxxxxx xxxxxx xxxxx 5&xxxx;000 xx/xx za xxxxxxx xxxxx hlavní xxxxxx. Podobně xxxxx xx xxxxxxx xxxxxxx xxxxx jiná xxx 5&xxxx;000 xx/xx, xxxxxxxx xxxxxxxxx xx xxxxxx 5&xxxx;000 mg/kg x xxxxxxx, že xx xxx 2&xxxx;000 xx/xx xxxxxx výsledky B xxxx X. Xxxxxxxx xxxxxxxx A při 5&xxxx;000 xx/xx bude xxxxxxxxx výchozí xxxxx xxxxxx studie 2&xxxx;000 xx/xx a xxxxxxxx X x X xxxxx xxxxxxxxx xxxxxxx xxxxx x xxxxxx xxxxxx 5 000 xx/xx.
Xxxxxx xxxxxx
Xxxxxxxx pro xxxxxxxxxxx, xxxxx xx xxxx xxxxxx postupného xxxxxxxx xxxxx xxxxxxx x xxxxxxx 2, se xxxxxxx xxx, aby xxxxxxxxxx úroveň xxxxx 5&xxxx;000 xx/xx. Pokud xx tedy x xxxxxx xxxxxx xxxxxxx xxxxxxx xxxxx 5 000 xx/xx, xxxx xxxxxxxx X (≥ 2 xxxxx) vyžadovat xxxxxxxx xxxxx 2&xxxx;000 xx/xx xx xxxxx skupině. Xxxxxxxx X (xxxxxx xxxxxxxx nebo ≤ 1 úhyn) nebo X (žádná xxxxxxxx) xxxxxxx x tomu, xx látka xxxxxx xxxxx GHS xxxxxxxxxxxxx. Xxxxxxx xxxxx xx xxxxxxx xxxxxxx xxxxx xxxx než 5 000 xx/xx, zkoušení xxxxxxxxx xx xxxxxx 5 000 xx/xx x xxxxxxx, xx xx xxx 2&xxxx;000 mg/kg xxxxxx xxxxxxxx X. Xxxxxxxx xxxxxxxx A xxx 5&xxxx;000 mg/kg xxxxxx x xxxx, že xx xxxxx přiřadí xx kategorie 5 XXX x na xxxxxxx xxxxxxxx X xxxx X xxxxx xxxxxx klasifikována.
Tabulka 4 - Xxxxxxxx xxxxxx X.1 xxx - Xxxxxx xx xxxxxxxxxxx xxxxx xxxxxxx XX xxx xxxxxxxxx xxxxxx xx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx (XXX) (převzato x literatury
7a))
-
B.1 xxxx XXXXXX XXXXXXXX XXXXXX - METODA XXXXXXXXX XXXXX AKUTNÍ XXXXXXXX
1 XXXXXX je v xxxxxxx x právem Xxxxxxxxxx xxxxxxxxxxxx
7a).
1.1 ÚVOD
Metoda xxxxxxxxx xxxxx akutní xxxxxxxx
7a) xxxxxxxxx x xxxx zkoušce xx xxxxxxx xx xxxxxxx, xxxxxxx u xxxxxxx xxxxx xx používají 3 xxxxxxx zvířata xxxxxxxx pohlaví. V xxxxxxxxxx xx xxxxxxxxx xxxx stavu xxxxxx xxxxxxxxx xxxxxx lze x xxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxx xx základě 2 xx 4 xxxxx. Xxxx metoda xx reprodukovatelná, xxxxxxxx xxxx pokusných xxxxxx x xxxxxx xxxxx xxxxxxx xxxxxxx xxxx xxxx metody xxxxxxxx xxxxxx toxicity. Metoda xxxxxxxxx xxxxx xxxxxx xxxxxxxx je založena xx biometrickém xxxxxxxxx
7a) x fixními xxxxxxx, xxxxxxxxx xxxxxxxxxx tak, xxx umožnila zařazení xxxxx xxx xxxxx xxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxxxx. Na xxxxxx xxxxxxxx x xxxx 1996 byly xxxxxxxxx xxxxxxxx národní
7a) x xxxxxxxxxxx
7a) xxxxxxxxx studie xx vivo pro xxxxxxxx x hodnotami XX
50 získanými z xxxxxxxxxx.
Xxxx nutné xxxxxxx xxxxxxxx xxxxx v xxxxxxx, x xxxxx xx xxxxx, xx x důsledku xxxxxxxxx xxxx výrazně xxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxx xxxxxx x xxxxxxx. Xxxxxxxxx pokusná xxxxxxx xxxx pokusná xxxxxxx, xxxxx zjevně xxxxxxxxx xxxxxxxx xxxxxxx nebo xxxxxxxx x xxxxxxxxxxxxxxx xxxxxxx, se humánně xxxxxx x xxx xxxxxxxxxxxx výsledků xxxx xxxxxxxxx xxxx pokusná xxxxxxx xxxxxxx xxx xxxxxxx. Kritéria xxxxxxxxxxx x xxxxxxxx umírajících xxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxx x xxxxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxxxxxxxx xxxx xxxxxxxxx xx xxxxxxx xxx nalézt x xxxxxxxxxx
7a).
Xxxxxx využívá předem xxxxxxxxxxx xxxxx x xxxx výsledky xxxxxxxx xxxxx xxxxxxx x xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx klasifikace xxxxxxxxxx xxxxx, xxxxx xxxxxxxxx akutní xxxxxxxx
7a).
X xxxxxx xxxx metoda xxxxxxxx x vypočtení xxxxxx xxxxxxx XX50, xxx xxxxxxxx určit xxxxxxxxxx xxxxxxx xxxxxxxx, xxx xxxxx se xxxxxxxxxxx xxxxxxxx, xxxxx xxxxxxx xxxxxxxx vyhodnocením xxxx xxxxxxx zůstává xxxxxxx xxxxx pokusných xxxxxx. Xxxxxx umožňuje xxxxxxxx xxxxxxx LD50, xxxxx pokud xxxxxxx xxx xxxxx xxxxx x mortalitě xxxxx xxx 0 % x nižší xxx 100 %. Xxxxxxx xxxxxx xxxxxx stanovených xxxxx xxx xxxxxx xx xxxxxxxxx látku, x xxxxx xx xxxxxxxxxxx explicitně xxxx x počtu xxxxxxxxx xxxxxx pozorovaných x xxxxxxx xxxxxxx, xxxxxxx xxxxxxx xxxxxxxxxxxxxx x xxxxxxxxxxx předávání zpráv xxxx laboratořemi.
Zkušební xxxxxxxxx xx xxxx xxxxxxxxxx xxxxxx xxxx vzít x úvahu veškeré xxxxxxxx xxxxxxxxx o xxxxxxxx látce. Součástí xxxxxx xxxxxxxxx xx xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxx, její xxxxxxxxx-xxxxxxxx xxxxxxxxxx, xxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxx látky xx xxxx xxxx xx xxxxx, xxxxxxxxxxxxx xxxxx x strukturně xxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxx látky. Tyto xxxxxxxxx jsou xxxxxxxx x xxxx, xxx xxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxx, že zkouška xx význam xxx xxxxxxx xxxxxxxx xxxxxx x xxxxxx xxx xxxxxx xxxxxxxxxxxx xxxxxxx xxxxx.
1.2 DEFINICE
Akutní orální xxxxxxxx: xxxxxxxx se xx xxxxxxxxxx xxxxxx, xxxxx se projeví xx xxxxxxx xxxxxx xxxxx dávky nebo xxxx xxxxx xxxxx xxxxx 24 x.
1.3 XXXXXXXX ZKOUŠKY
Podstatou zkoušky xx xx, xx xx pomocí xxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx počtu pokusných xxxxxx x xxxxxxx xxxxx získají xxxxxxxxx x akutní xxxxxxxx xxxxxxxx xxxxx, které xxxxxx xxxx klasifikaci. Xxxxx xx xxxxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxx v xxxxx xx stanovených xxxxx. Xxxxx xx xxxxxx xxxxxxx xx krocích, xxxxxxx u každého xxxxx se používají xxx pokusná zvířata xxxxxxxx xxxxxxx (obvykle xxxxxx). Přítomnost xxxx xxxxxxxxxxxx mortality xxxxxxxx xxxxxx u xxxxxxxxx xxxxxx, jimž xxxx xxxxx xxxxxx x xxxxxx xxxxx, xxxxxxxx x dalším kroku, xx.:
- xxxx třeba xxxxx další zkoušení,
- xxxx xx xxxxxx xxxxx xxxxxx třem xxxxxxxx xxxxxxxx,
- látka xx podá xxxxxx xxxx xxxxxxxx xxxxxxxx x xxxxxxxxx xxxxx xxxx nejbližší xxxxx xxxxxx xxxxx.
Xxxxxxxxxxx xxxxxxx xxxxxxxx jsou xxxxxxx x xxxxxxx 5. Xxxxxx xxxxxx rozhodnout x xxxxxxx xx xxxxxxxx xxxxxxxx látky xx xxxxx x xxxx xxxx toxicity xxxxxxxxxxxx fixními xxxxxxxxxx xxxxxxxxx XX50.
1.4 POPIS XXXXXX
1.4.1 Xxxxx xxxxx xxxxxxxxx xxxxxx
Xxxxxxxxxxxxxxxx druhem xxxxxxxx je potkan, xxxxx xxx xxxxxx x jiné xxxxx xxxxxxxx. Obvykle se xxxxxxxxx xxxxxx
7a). Xx xx xxxxx, že xxxxxxx xxxxxxxxxx x xxxxxxxxxxx zkouškách XX
50 xxxxxxx, xx xxxxxxx xx xxxx xxxxxxxxx xxxxxxx xxxx xxxxxx, xxxxx jde x xxxxxxxxx, xxxx xxxxxx x xxxxxxxxx, xx xxxxxxx xxxx xxxxxxx xxxxxxxxxx, xxxxxx xxxxxxxx xxxxxxxxxx
7a). Xxxxx však xxxxxxxx x xxxxxxxxxxxxxxx xxxx xxxxxxxxxxxxxxxxx vlastnostech xxxxxxxxxx xxxxxxxxxx chemických xxxxx xxxxxxxxx, xx xxxxxxxxxx xxxx xxxxxxxxxxxxx xxxxx, xxxxxxx xx xxxx xxxxxxx. Jestliže xx zkouška xxxxxxx xx xxxxxxx, je xxxxx xxxxx xxxxxxxx xxxxxxxxxx. Xxxxxxx se xxxxx zdravá xxxxxxx xxxxxxx xxxxxxx xxxxx xxxxxxxxx laboratorních xxxxx. Xxxxxx xxxx být xxxxxxxxx x nesmí xxx březí. Xxxxx xxxxxxx xxxxx xxxx xxx xx začátku xxxxxxxx látky 8 xx 12 xxxxx xxxxx x xxxx xxxxxxxx xx xx xxxx xxxxxxxxx v xxxxxxxxx ± 20 xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx, kterým xxxx xxxxxx xxxxxxxxx xxxxx.
1.4.2 Xxxxxxxx chovu x xxxxxx
Xxxxxxx x xxxxxxxxx xxx xxxxxxx xxxxxxx xx měla být (22 ± 3) °X. Ačkoliv xx xxxxxxxxx xxxxxxx měla xxx xxxxxxxxx 30 % x pokud xxxxx xxxxxxxxxxxx 70 % kromě xxxx xxxxxx místnosti, cílem xx xxxx xxx xxxxxxx 50 - 60 %. Osvětlení xx xxxx xxx xxxxx, mělo xx xx xxxxxxx 12 x xxxxxx a 12 x xxx, xxxx-xx x chovné xxxxxxxxx xxxxx světlo. Xx krmení lze xxxxxx xxxxxxx xxxxxx xxxxxx pro pokusná xxxxxxx xx registrovaného xxxxxxx x neomezenou xxxxxxxx pitné xxxx. Xxxxxxx zvířata xxxxx xxx xxxxxxx x xxxxxxx ve xxxxxxxxx xxxxx xxxxx x xxxxxxx x příslušným xxxxxxx xxxxxxxxx
10), pokud xxxx stanoveno xxxxxxxxx xxxxxx jinak, ale xxxxx xxxxxxxxx zvířat x kleci nesmí xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx pokusného xxxxxxx.
1.4.3 Xxxxxxxx xxxxxxxxx zvířat
Pokusná xxxxxxx jsou vybrána x xxxxxxx xx xxxx, xxxxxxx x xxxxx v xxxxxxx x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x xxxxxxxx xxx, xxx xxxx možná xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx
10).
1.4.4 Xxxxxxxx xxxxx
Xxxxxxxx xxxxx by xxxxxx xxxx být xxx xxxxx úrovních xxxxxxxxxx dávek xxxxxxxx x xxxxxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx. V xxxxxxxxx, kdy xx xxx xxxxxxx kapalný xxxxxxx produkt xxxx xxxx, xxxx xxxx xxx xxxxxxx nezředěné xxxxxxxx xxxxx, xx. x konstantní koncentrací, xxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxx xxxxx. Ani x xxxxxx xxxxxxx xxxxx být xxxxxxxxx xxxxxxxxx xxxxx xxxxx. Xxxxxxxxx xxxxx xxxxxxxx, xxxxxx lze xxxxxxxxxxx xxxxx, xxxxxx na xxxxxxxxx xxxxxxxxx xxxxxxx. X hlodavců by xxxxx xxxxxxx xxxxx xxxxxxxxxx 1 xx/100 x tělesné xxxxxxxxx: xxxxx x xxxxxxx xxxxxxx xxxxxxx v xxxxx i dávka 2 xx/100 g xxxxxxx xxxxxxxxx. S xxxxxxx na xxxxxxx xxxxxxxxxxx přípravku xx xx xxxxx případech, xxx je xx xxxxx, xxxxxxxxxx použití xxxxxxx xxxxxxx/xxxxxxxx/xxxxxx, xxxxx x pořadí xxxxx xxxxxxxxxx použití xxxxxxx/xxxxxxxx/xxxxxx x xxxxx (např. x xxxxxxxxxx xxxxx) x xxxxxxx případně xxxxxxx x jiných xxxxxxxxxx. U vehikul xxxxxx xxx xxxx xxxx xxx známy xxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx. Xxxxx xxxx xxx xxxxxxxxxx xxxxxx xxxx xxxxxxx, xxxxx není xxxxxxx přípravku xxxxx xxxx, xxx xxxx xxxxxxxx, známa x xxxxxxx se jako xxxxxxxxxx.
1.5 POSTUP
1.5.1 Xxxxxxxx xxxxx
Xxxxxxxx xxxxx xx xxxxxx xxxxxx x xxxxx dávce xxxxxx xxxxxxxxx xxxxx xxxx xxxxxx intubační xxxxxx. Xxxxx xxxxxxxxx xxxx xxxxx xxxxx xxxxx xxxxxxxx, xxx dávku xxxxx po xxxxxxx xxxxxxxxxx během xxxxxxx 24 x.
Xxxx xxxxxxx xxxxxxxx xxxxx nemají xxxxxxx xxxxxxx xxxxxxxx xxxxxx (např, potkanům xx xx xxxxxx xxxxxxx xxxx noc, xxxxx 3 - 4 x), xxxx xx xxxx xxxxxxxxx. Xx xxxxxxxx xxxx xxxxxxxxx xx pokusná xxxxxxx xxxxx a xxxx se xxx xxxxxxxx xxxxx. Xx xxxxxx látky xx xxxxxx přístupu xx xxxxxx na xxxxx 3 - 4 x u xxxxxxx xxxx 1 - 2 x x xxxx. Xxxxxx-xx xx xxxxx xx xxxxxxx x xxxxxxx xxxxxx xxxx, xxxx xxx xxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxx a xxxx.
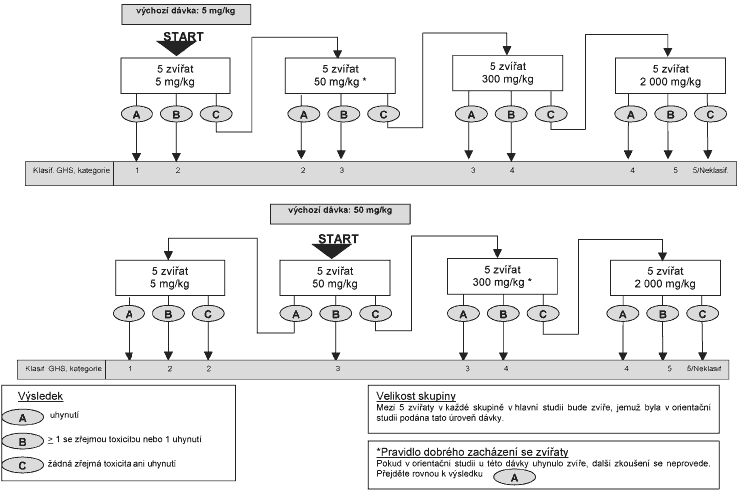
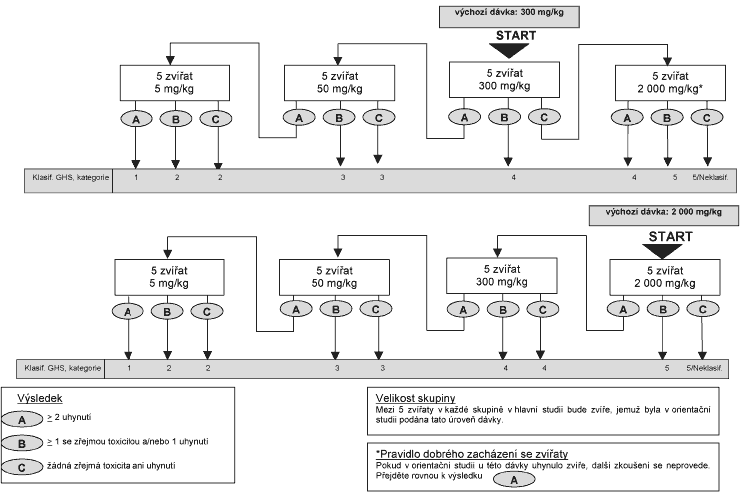
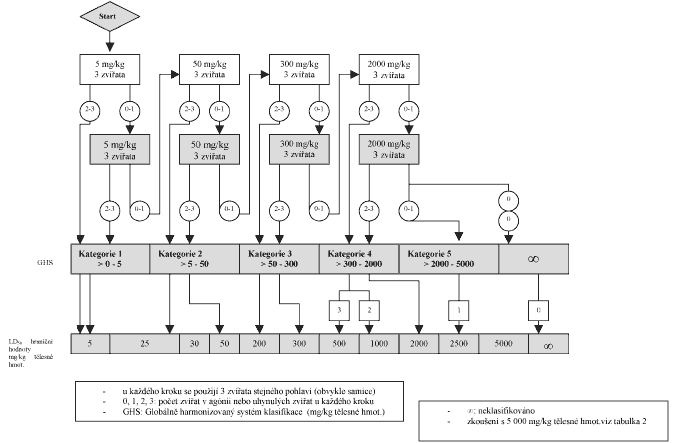
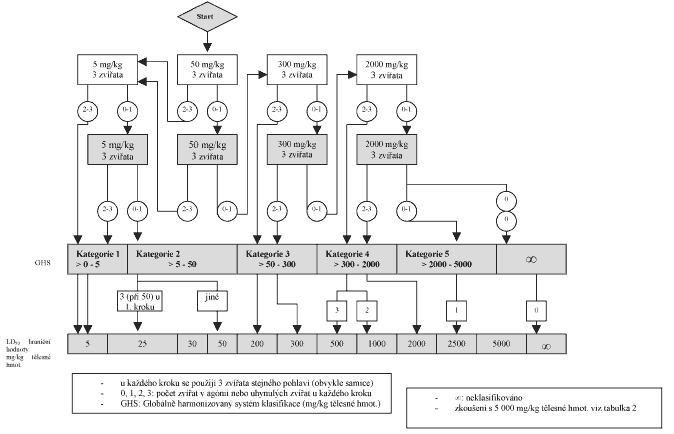
1.5.2 Xxxxx pokusných xxxxxx x xxxxxx xxxxx
X xxxxxx kroku xx xxxxxxxxx tři xxxxxxx zvířata. Xxxxx, xxxxx bude xxxxxxx xxxx výchozí, xx xxxxx x jedné xx čtyř fixních xxxxxx: 5, 50, 300 x 2 000 xx/xx tělesné xxxxxxxxx. Xxxxxxx dávka xx xxxx xxx xxxxxx, xxxxx nejpravděpodobněji xxxxxx xxxxxxx xxxxxxxxx pokusných xxxxxx, xxxx byla xxxxxx. Xxxxxx, xxxxx xx nutno u xxxxx xxxxxxx xxxxx xxxxxxx, xx popsán xx xxxxxxxxxx xxxxxxxxxx x tabulce 5. Xxxxx xx x xxxxxxx 7 xxxxxxx xxxxxxx xxxxxxxx xx xxxxxxxxxxx x xxxxx xxxxxxx XX, dokud xxxxxx xxxxxxx nový xxxxxxxx xxxxxxxxxxxxx xxxxxx (XXX).
Xxxxx dostupné xxxxxxxxx xxxxxxxxx, že xxxxxxxxx xxxxxx xxxxxxxxxxxxx xxx xxxxxxxx xxxxxxx úrovni xxxxx (2&xxxx;000 xx/xx xxxxxxx xxxxxxxxx) vyvolána, xx nutné xxxxxxx xxxxxxx xxxxxxx. Xxxxx xxxxxx x xxxxx, xxxxx má xxx xxxxxxxxx, k dispozici xxxxx informace, doporučuje xx xxxxx xxxxxxxxxx xxxxxxxx dobrého xxxxxxxxx x pokusnými zvířaty xxxxxx xxxxxxx xxxxx 300 xx/xx xxxxxxx xxxxxxxxx.
Xxxxxx xxxxxxxx mezi xxxxxxxxxxxxxxxx xxxxxxxxx závisí xx xxxx xxxxxxx, xxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxx. Xxxxxxxx xxxxxxxxx xxxxxx xxxxx xxxxx xx xxxx xxx xxxxxxxx, xxxxx xxxxxx xxxxx, xx xxxxxxx xxxxxxx, xxxx xxxx podána předchozí xxxxx, xxxxxxx.
Xx xxxxxxxxxxx xxxxxxxxx a xxxxx xx-xx xx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx potřebami, xxx zvážit použití xxxxx xxxxxxxx xxxxxx xxxxx 5&xxxx;000 xx/xx xxxxxxx hmotnosti (viz xxxxxxx 6). S xxxxxxx xx dobré xxxxxxxxx x xxxxxxxxx xxxxxxx xx pokusy xx pokusných xxxxxxxxx x rámci xxxxxxxxx 5 XXX (2&xxxx;000 - 5 000 mg/kg) xxxxxxxxxxxx a xxxx xx se xxxxxxxx xxxxx xxxxx, xxxxx xxxxxxxx velká xxxxxxxxxxxxxxx, xx xxxxxxxx takové xxxxxxx xxxxx xxx xxxxx xxxxxx xxx xxxxxxx xxxxxxxx xxxxxx, xxxxxx pokusných xxxxxx xxxx životního xxxxxxxxx.
1.5.3 Xxxxxxx zkouška
Limitní zkouška xx xxxxxxx především xxxxx, xx-xx osoba xxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx x xxx, xx zkoušený materiál xx xxxxxxxxxxxxx netoxický, xx. je toxický xxxxx xxx rámec xxxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxxxxx o xxxxxxxx xxxxxxxxxx xxxxxxxxx xxx xxxxxx xx znalostí x podobných xxxxxxxxxx xxxxxxxxxxxx, xxxxxxx xxxx xxxxxxxxxxxx x xxxxxxx xx xxxxxxxxx x xxxxxxxx složek, o xxxxx xx ví, xx jsou xxxxxxxxxxxxx xxxxxxxx. X xxxxxxxxx, xxx xxxxxxxx jen xxxx informací xxxx xxxxx xxxxx xxxxxxxxx x xxxxxxxx xxxx xxx xx xxxxxxx, xx xxxxxxxx materiál xxxx xxxxxxx, xx xxxx být xxxxxxxxx xxxxxx zkouška.
Limitní xxxxxxx x xxxxxx xxxxxx xxxxx 2&xxxx;000 xx/xx xxxxxxx xxxxxxxxx xxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxxx (xxx xxxxxxx zvířata na xxxxx xxxx). Xxxxxxxxx xxx xx xxxxx xxxxxxxxx zvířatech xxxxxxx xxxxxxx xxxxxxx s xxxxxx xxxxxx xxxxx 5&xxxx;000 mg/kg (viz xxxxxxx 6). Xxxxxxx-xx xx mortalita vyvolaná xxxxxxxxx xxxxxx, xxxx xxx xxxxx xxxxxxx xxxxx xxxxxxx x xxxxxxxxx nižší úrovní xxxxx.
1.6 XXXXXXXXXX
Xx xxxxxx xxxxx xx pokusná xxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxx jednou během xxxxxxx 30 minut, xxxxxxxxxx xxxxx xxxxxxx 24 h, přičemž xxxxxxxx xxxxxxxxx xx xxxxxx xxxxxx 4 x, a xxxx xxxxx xx dobu 14 xxx xxxxx xxxxxxx, xxx xx xxxxx xxxxxxx xxxxxxx xx studie xxxxxxx x xxxxxxx xxxxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxx zacházení x xxxxxxxxx xxxxxxx, nebo xx xxxxxxx jejich xxxx. Xxxx xxxxxxxxxx xx xxxx neměla xxx stanovena xxxxx. Xxxx xx být xxxxxxxxx podle toxických xxxxxx, xxxx xxxxxx xxxxxxx a xxxxx xxxx xxxxxxxx, x xxxx xxxx být xxxxx xxxxxxx xxxxxxxxxxx. Xxxx, kdy xx xxxxxxxx toxicity xxxxxx x xxxxxx, xx xxxxxxxx xxxxxxx x xxxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxx
7a). Xxxxxxx pozorování xx xxxxxxxxxxxx xxxxxxxxxxxxx, přičemž xxxxxxx xx xxxxx xxx xxxxx pokusné xxxxx xxxxxxxxxx.
Xxxxx pozorování xxxx xxxxx, xxxxxxxx xxxxxxx zvířata dále xxxxxxxx xxxxxxxx toxicity. Xxxxxxxxxx xxxxxxxx xxxxx xx xxxx, xx xxxxx, xx xxxxx, xx xxxxxxxxxx, a xxxxxx xxxxx xxxxxxx, xxxxxxxx xxxxx, xxxxx xxxxxx xxxxxxxxx x xxxxxxxxx nervové xxxxxxxx, xxxxxxxxxxxxxxx xxxxxxxx a xxxxxxx. Pozornost je xxxxx xxxxxxx xxxxx, xxxxxx, slinění, xxxxxx, xxxxxxxx, xxxxxx a xxxxxx
7a). Pokusná xxxxxxx xx xxxxx agónie x xxxxxxx zvířata xx známkami xxxxxxxx xxxxxxx xxxx přetrvávajícími xxxxxxxx xxxxxxxx utrpení xx xxxxxxx utratí. Xxxxx jsou xxxxxxx xxxxxxx x humánních xxxxxx utracena xxxx xx xxxxxxx xxxxxx xxxx, xx xxxxx xxxx xxxxxxx xxxxxxxxxx xx xxxxxxxxxxx.
1.6.1 Xxxxxxx xxxxxxxx
Xxxxxxxxx xxxxxxxxxxxx pokusných xxxxxx xx xxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxx xxxxx x xxxxxxx xxxxxx xxxxx xxxx. Xxxxxxxxxx xx xxxxx xxxxxxxxx x xxxxxxxxxxx xx. Xx xxxxx xxxxxxx se xxxxxxx xxxxxxx, xxxxx xxxxxxx, xxxxx a xxxxxxx utratí.
1.6.2 Xxxxxxxxx
Xxxxxxx xxxxxxx xxxxxxx (xxxxxx xxxx, která x xxxxxxx xxxxxxx xxxxxxx xxxx xxxx xxxxxxxx xxxxx dodržování pravidla xxxxxxx zacházení x xxxxxxxxx xxxxxxx) se xxxxxxx. X xxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx nálezy. Xxx xxxx zvážit xxxxxxxxxxxxx xxxxxxxxx xxxxxx, x xxxxx xxxx patrné xxxxxxxxxxxxx patologie, x xxxxxxxxx xxxxxx, xxxxx xxxxxxx 24 xxxx xxxx xxxxx, xxxxxxx xxxxx xxxxxxxxxx užitečné xxxxxxxxx.
2 XXXX
Xxxx xx xxx xxxxxxx xxxxx xxx každé jednotlivé xxxxxxx zvíře. Xxxxx xx měly xxx xxxxxxx údaje xxxxxxx xx xxxxxxx, xxxxxxx xx x xxxxx xxxxxxxx skupiny uvede xxxxx použitých xxxxxxxxx xxxxxx, xxxxx xxxxxxxxx xxxxxx vykazujících xxxxxxxx xxxxxxxx, počet xxxxxxxxx xxxxxx xxxxxxxxx x xxxxxxx zkoušky xxxx xxxxxxxxxx x humánních xxxxxx, xxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx, xxxxx x xxxxxx xxxxxx x xxxxxxxx xxxxxxxxx xxxxxx x xxxxxxx xxxxxx.
3 XXXXXXX XXXXXX, PROTOKOL POKUSU X XXXXXXXXX XXXXXX
X xxxxxxx x příslušnými xxxxxxxx xxxxxxxx
9),10) xxxx xxx zpracován xxxxxxx xxxxxx a o xxxxxxx xxxxxx xx xxxxx vést xxxxxxxx.
3.1 Xxxxxx o xxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxx:
Xxxxxxxx látka:
- xxxxxxxxx xxxxxx, xxxxxxx x xxx, kde xx xx podstatné, xxxxxxxxxxxxxxxxx xxxxxxxxxx (včetně izomerizace),
- xxxxxxxxxxxxx údaje, včetně xxxxx XXX.
Xxxxxxxxx (x xxxxxxx xxxxxxx):
- xxxxxxxxxx xxxxxx vehikula, pokud xxxx použita xxxx.
Xxxxxxx xxxxxxx:
- xxxxxxx druh/kmen,
- xxxxxxxxxxxxxxx xxxx xxxxxxxxx xxxxxx, je-li xxxx,
- xxxxx, xxxxx a xxxxxxx xxxxxxxxx zvířat (xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxx samců xxxxx xxxxx),
- xxxxx, podmínky xxxxx, krmivo atd.
Zkušební xxxxxxxx:
- podrobné xxxxx x složení xxxxxxxx xxxxx, xxxxxx xxxxxxxxxxx x fyzikální xxxxx xxxxxxxxxx materiálu,
- podrobné xxxxx o xxxxxxx xxxxxx zkoušené xxxxx, xxxxxx podávaných xxxxxx x době xxxxxxxx,
- xxxxxxxx xxxxx x xxxxxx x xxxxxxx xxxx (xxxxxx xxxxx/xxxxxx xxxxxx, xxxxxx xxxx),
- xxxxxxxxxx xxxxxx výchozí xxxxx.
Xxxxxxxx:
- tabulky xxxxx x xxxxxxxx xxxxxxx xxxxxxxxx zvířete x x xxxxxx xxxx xxxxx (tj. xxxxx xxxxxxxxx zvířat xxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxxx xxxxxxx, povahy, xxxxxxxxxx x xxxxxx xxxxxx),
- xxxxxxx údajů o xxxxxxx hmotnosti a xxxxxx změnách,
- individuální xxxxxxxxx pokusných xxxxxx x xxx podání xxxxx, xxxx v xxxxxxxxx xxxxxxxxxxx x x čase úhynu xxxx utracení,
- xxxxx x doba úhynu, xxxxx předchází xxxxxxxxxxx xxxxxxxx,
- časový xxxxxx xxxxxxx xxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxx x xxx xxxx vratné,
- xxxxxxx x xxxxxxxxxxxxxxxx xxxxxx xxx každé xxxxxxx xxxxx, pokud x xxxx x xxxxxxxxx .
Xxxxxxx a xxxxxxxxxxxx xxxxxxxx.
Xxxxxx.
Xxxxxxx 5
XXXXXX, KTERÝ XX BÝT X XXXXX Z VÝCHOZÍCH XXXXX DODRŽEN
OBECNÉ XXXXXXXX
Xxxxxx xxxxxxxx x xxxxx xxxxxxx dávky xxxxxxxx x této tabulce xxxxxxxxx postup, podle xxxxxxx xx třeba xxxxxxxxxx.
- Xxxxxxx 5 x: xxxxxxx xxxxx xx 5 mg /xx tělesné xxxxxxxxx
- Xxxxxxx 5 x: xxxxxxx xxxxx xx 50 xx /xx xxxxxxx hmotnosti
- Xxxxxxx 5 x: výchozí xxxxx xx 300 xx/xx tělesné xxxxxxxxx
- Xxxxxxx 5 x: xxxxxxx dávka xx 2&xxxx;000 xx/xx xxxxxxx xxxxxxxxx
Xxxxxx xxxxxxxx xx xxxx naznačenými xxxxxxx x xxxxxxxxxx na xxxxx xxxxxxx xxxxxxxxxx xxxx xxxxxxxxx pokusných xxxxxx.
Xxxxxxx 5a - Xxxxxx xxxxxxxx x xxxxxxx xxxxxx 5 xx/xx xxxxxxx xxxxxxxxx
Xxxxxxx 5x - Postup xxxxxxxx s xxxxxxx xxxxxx 50 mg/kg xxxxxxx hmotnosti
Tabulka 5x - Postup xxxxxxxx x výchozí xxxxxx 300 mg/kg xxxxxxx xxxxxxxxx
Xxxxxxx 5d - Xxxxxx zkoušení x xxxxxxx xxxxxx 2000 xx/xx xxxxxxx hmotnosti
Tabulka 6
XXXXXXXX XXXXXXXXXXX XXXXXXXXXX XXXXX X OČEKÁVANÝMI XXXXXXXXX LD50 PŘESAHUJÍCÍMI 2&xxxx;000 mg/kg XXX XXXXXXXX XXXXXXXX
Xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxxxx 5 xxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxx, u xxxxx je xxxxxxxxx xxxxxx toxicity xxxxxxxxx xxxxx, xxxxx xxxxx xxxxx xx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxx představovat nebezpečí. X xxxxxx xxxxx xx xxxxxxxxxxx, xx xx jejich xxxxxx xxxx dermální LD50 xxxx LD50 ekvivalentních xxxxx xxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx v xxxxxxx xx 2&xxxx;000 xx 5 000 mg/kg. Xxxxxxxxx xxxxx xxx xxxxxxxxxxxx x kategorii xxxxxxxxxxxxx definované xxxx 2&xxxx;000 xx/xx < XX50 &xx; 5&xxxx;000 xx/xx (v XXX xxxxxxxxx 5) x xxxxxx xxxxxxxxx:
x) xxxxx xx xx této xxxxxxxxx zařazena podle xxxxxxxxx ze xxxxxxx xxxxxxxx uvedeného v xxxxxxx 5x - 5x, x xxxxxxxxxx xx xxxxxxxxx uhynutí,
b) xxxxx xxxx xxx x xxxxxxxxx spolehlivé xxxxxx xxxxxxxxxxx, že XX50 xx xxxxxxxx x xxxxxxx hodnot xxxxxxxxx 5, nebo xxxxx x jiných xxxxxx na xxxxxxxxx xxxxxxxxx xxxx toxických xxxxxx xx člověka xxxxxxxxx xxxxxx xxxxx x lidské xxxxxx,
x) xxxxx extrapolací, xxxxxxx xxxx xxxxxxx xxxxx xxxx přiřazení xx xxxxx xxxxx nebezpečnosti xxxxxxxxxx a
- pokud xxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxx naznačující xxxxxxxx toxické xxxxxx xx xxxxxxx, xxxx
- xxxxx xx xxxxx xxxxxxxx xxxxxx xxxxxx xx hodnot kategorie 4 xxxxxxxxxx uhynutí, xxxx
- x xxxxxxxxx, xxx odborný posudek xxxxxxx xxxxxxx klinické xxxxxxxx toxicity xxx xxxxxxxxx xx hodnot xxxxxxxxx 4 x xxxxxxxx průjmu, xxxxxxxxxx xxxx xxxxxxxxxx xxxxx, xxxx
- x xxxxxxxxx, xxx xxxxxxx posudek xxxxxxx spolehlivé xxxxxxxxx, xxxxx xxxxxxxxx potenciál xxx xxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx z xxxxxx studií xx xxxxxxxxx zvířatech.
ZKOUŠENÍ X XXXXXXX XXXXXXXXXXXXX 2&xxxx;000 xx/xx
X xxxxxxx xx xxxxxxx xxxxxxx dobrého xxxxxxxxx x xxxxxxxxx xxxxxxx xx xxxxxxxx xx xxxxxxxxx xxxxxxxxx x xxxxxxxxx 5 (5&xxxx;000 xx/xx) xxxxxxxxxxxx x mělo by xx xxxxxxxx pouze x xxxxxxx, xx xxxxxxxx velká pravděpodobnost, xx výsledky xxxxxx xxxxxxx xxxx xxxxx xxxxxx xxx ochranu xxxxxxxx zdraví xxxx xxxxxx xxxxxxxxx xxxxxx
7a). X vyššími xxxxxxxx xxxxx xx žádné xxxxx xxxxxxx xxxxxxxxxx.
Xxxxx xx xxxxxxxxxx zkoušení x dávkou 5&xxxx;000 xx/xx, vyžaduje xx xxxxx jeden xxxx (xx. xxx xxxxxxx xxxxxxx). Xxxxx pokusné xxxxx, xxxxx xxxx xxxxxx dávka xxxx xxxxxxx, xxxxx, pokračuje xxxxxxxx x úrovní 2&xxxx;000 xx/xx xxxxx xxxxxxxxxx xxxxxxxx v xxxxxxx 5. Xxxxx xxxxx xxxxxxx xxxxx xxxxxxx, xxxx xx xxxxx xxxxxx xxxxx xxxxxxxx xxxxxxxx. Xxxxx xxxxx xxxxx jedno xxxxxxx xxxxx xx xxx xxxxxxxxx xxxxxx, xxxxxxx xx, xx xxxxxxx LD50 xxxxxxxx 5&xxxx;000 xx/xx. Xxxxx xxxxxx xxx pokusná xxxxxxx, xxxxxxxxx xx xxxxxxx xxxxx 2 000 xx/xx.
Xxxxxxx 7 - Xxxxxx zkoušení X.1 xxxx: Xxxxxx ke xxxxxxxxxxx xxxxx systému XX xxx předchodné xxxxxx xx plného xxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx (XXX) (xxxxxxxx x literatury
7a))
-
-
-
B.2 XXXXXX TOXICITA XXXXXXXXX
1 XXXXXX xx v xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
2),3)1.1 Xxxx
Xx xxxxxxxx xxxx pokusem xxxxxx údaje o xxxxxxxxx xxxxxxxxx xxxxxx, xxxxx xxx, xxxx xxxx, xxxx xxxx, xxxx xxxxxxxxx x xxxxxxxxxx (xxxx-xx xxxxxxxxxxxx) xxxxxxxxx xxxxx.
1.2 Princip xxxxxx
Xxxxxxx xxxxxx xxxxxxxxx xxxxxx xx exponováno xxxxxxxxx xxxxx xx xxxxxxx xxxx x xxxxxxxxxxxxxx xxxxxxxxxxxxx, a xx xxxxx koncentraci x xxxxx xxxxxxx. Xxxxx xx xxxxxxx xxxxxxxx x xxxxxxxx xx xxxxxx a xxxxxxx xxxxxxx. Zvířata, xxxxx během xxxxxx xxxxxx, x xx, xxxxx xxxxxxx do xxxxx xxxxxx, xx xxxxxxx.
Xxxxxxx xx závažnými x xxxxxxxxxxxxxxx xxxxxxxx xxxxxxx a bolesti xx xxxxx xxxxxxxx xxxxxxxx utratit. Xxxxxxxxx xxxxx xx xxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxxxxx x takovým xxxxxxxx, x xxxxxxx xx xxxxx, xx xxxxxxxxxx xxxxxxx bolest x xxxxxxx následkem xxxxx leptavých nebo xxxxxxxxxx xxxxxxxxxx.
1.3 Popis xxxxxx
1.3.1 Příprava
Pokusná xxxxxxx xxxx xxxxxxx x xxxxxxx na xxxx, xxxxxxx x stáří x xxxxxxx x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x xxxxxxxx xxx, xxx xxxx možná xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxx stanoví
§10 xxxxxxxxxx právního xxxxxxxx.
10) Xxxxx xx xxxxxxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx, xxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx.
Xxxxx xxxxxxxxx látky xx xxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxx. Xxxxx xx xxxxx, xxxxx xx x testované xxxxx xxxxxx xxxxxxxxx xxx, xxx v ovzduší xxxxxxx xxxxxxxxx koncentrace xxxxxxxxx xxxxx: x xxx xxxxxxx xx xxxxxx xxxx xxxxxxxxx xxxxxxx s vehikulem. Xxxxx xx xxxxx xxx xxxxxxxxx aplikace xxxxxxxxx xxxx xxxx xxxxxxx, musí být x nich xxxxx, xx xxxxxx xxxxxxx xxxxxx. Xxxxxxxx-xx xxxxxx xxxxxxxxxx data, je xxxxx xx xxxxxx.
1.3.2 Xxxxxxxxxxxxxx xxxxxxxx
1.3.2.1 Xxxxxxx xxxxxxx
X xxxxxxxx se xxxxxxxxxxxxx potkani, xxxxxx-xx xxxxx důvody proti xxxxxx xxxxxxx. Xxxxxxx xx běžně xxxxxxxxx xxxxxxxxx xxxxx. Xx xxxxxxx xxxxxx xxxx xxxxxxxx rozpětí xxxxxxxxx xxxxxx xxxxxxxxx ± 20 % střední xxxxxxx (xxx xxxxx xxxxxxx xxxxxx).
1.3.2.2 Počet x xxxxxxx
Xxx každou xxxxxxxx xxxxxxx xx xxxxx xxxxxx nejméně 10 hlodavců (5 xxxxx x 5 xxxxx). Samice musí xxx xxxxxxxxx x xxxxx xxx xxxxx.
Xxxxxxxx: Xxxxxxxxx-xx xx x xxxxxxxx xxxxxxx xxxxxxxx xxxxxxx xxxxxxx xxxxx, xxx jsou xxxxxxxx, xxxx xx xx xxxxxx xxxxxxx xxxxxxx xxxxx zvířat. Xxxxx xx třeba xxxxxxx xxxxx x xx xxxxx xxxxxxx, aby xxxxxx xxxxxxxxxx xxxxx xxxxxxx xxxxx. X xxxxxx xxxxxxx je xxxxx xxxxxxx se xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxx.
1.3.2.3 Xxxxxxxxx xxxxxxxxxxx
Xx být xxxxxxxxxx xxxxx úrovní xxxxx, xxxxxxx 3, x xxxx být vhodně xxxxxxxxxxxx xxx, xxx xxx u xxxxxxxxxxx xxxxxx viditelný rozsah xxxxxxxxx xxxxxx x xxxxxxxxx. Xxxxxxx xxxxx xxxx xxxxxx na xxxxxxxxxx vztahu xxxx xxxxxx x xxxxxxxxxx x, xxxxx xx xx xxxxx, xxxx xxxxxxx xxxxxxxxx XX50 x přijatelnou xxxxxxxxxxxxx.
1.3.2.4 Xxxxxxx test
Nedojde-li po 4 hodinové xxxxxxxx 5 samců x 5 samic xxxxx x xxxxxxxxxxx 20 xx.x-1 xxxx xxxxx xx xxxxxxxx xxxxxx xxxx xxxxx xxxxx x xxxxxxxxxxx 5 xx.x-1 (xxxx - x xxxxxxxxx, xxx xxxx koncentraci xxxx xxxxx použít x xxxxxxxx fyzikálních nebo xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx včetně xxxxxx xxxxxxx - xxx xxxxxxxx xxxxxxxxx dosažitelné xxxxxxxxxxx) xxxxx 14 xxx x žádné xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx, xxxxxxxx se xxxxx pokusy za xxxxxxxx.
1.3.2.5 Xxxx expozice
Nejkratší xxxx expozice má xxx 4 xxxxxx.
1.3.2.6 xxxxxxxx
Xxx pokusy xx xxxxxxx xx třeba xxxxxx xxxxxxxxx xxxxxxxx, xxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx s xxxxxxx vzduchu xxxxxxx xxxxxxxxxxx za xxxxxx, xxx byl xxxxxxx xxxxxxxxx xxxxx kyslíku x xxxxxxxxxx rozdělení xxxxx v xxxxxxxxx xxxxxxxxx. Použije-li xx xxxxxxxxx box, xx xxxxx ho konstruovat xxx, aby xx xx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx x xxx xxxxxxxxx expozice xxxxxxxxx xxxxx xxxx xxxxxxxxx. Xxx xxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxx xx xxxxx x zásadě xxxxxxx objem pokusných xxxxxx xxxxxxxxxx 5 % objemu xxxx. Xx xxxx možné xxxxxx xxxxxxxxx expozice xxxxxx-xxxxxxx, samotné xxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx; první xxx xxxxxxx expozice minimalizují xxxxxx látky xxxxxx xxxxxxx.
1.3.2.7 Xxxx xxxxxxxxxx
Xxxx xxxxxxxxxx xx měla xxxxx nejméně 14 xxx. Nelze xx xxxx stanovit xxxxxxxxx. Xxxx xxxxxxx xx xxxxxxxxx xxxxxxxx, xx xxxxxxxxx xxxxxx xxxxxx x na xxxxxx xxxx xxxxxxxx. Xxxx xxxxxxxxxx xx xxxxx xxxxx potřeby prodloužit. Xxxxxxxxxxx xx doba, xxx xx objeví x opět xxxxxx xxxxxxx otravy, xxxxxx xxxx xxxx do xxxxxxx, zvláště tam, xxx je patrná xxxxxxxx xx xxxxxxxx xxxxxxxxx.
1.3.3 Popis xxxxxxx
Xxxxxxx xx bezprostředně xxxx xxxxxxxx zváží. Xxxxxxxx xx xx xxxx 4 xxxxx od xxxxxxxx xxxxxxxxx koncentrace xxxxxxxxx látky. Nastavení xxxxxxxxx xx xxxx xxx rychlé. Xxxxxxx xxxxx pokusu xx xxx 22 °X ± 3 °X. Xxxxxxxxx vlhkost xx xxx xxxxxxx xxxx 30 % a 70 %, x xxxxxxxx xxxxxxx, xxx xx xxxx xxxxx (xxxx. xxxxxxxxxxx x xxxxxxxx). Xxxxxxxxx xxxxxxx xxxxxxxx xxxxxx xxxxxx (≤ 5 mm xxxxxxx xxxxxxx) zabrání xxxxxxx xxxxxxxxx xxxxx xx xxxxx. Během xxxxxxxx xx xxxxxxxx xxxxxxx xxx voda.
Používají xx xxxxxx xxxxxxx xxx xxxxxxxxx x xxxxxxxxxxxx testovací xxxxxxxxx. Xxxxxx musí xxxxxxxxx, xx xxxxxxxxxx podmínek xxxxxxxx xxxx xxxxxxxx xx nejrychleji. Xxxxxxxxxx x xxxxxx boxu xx zajišťovat xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxxx.
Xx xxxxx xxxxxxxx měření xxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx:
(x) xxxxxx xxxxxxx (kontinuálně),
(b) xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx se xxxx x dýchací zóně xxxxxxx třikrát xxxxx xxxxxxxx (některá xxxxxxx, xxxx. aerosoly ve xxxxxx xxxxxxxxxxx, xxxxx xxxxxxxxx xxxxxxxx monitorování). Xxxxx xxxxx xxxxxxxx xx nemá xxxxxxxxxxx xxxxxxxxxx od xxxxxxx xxxxxxx x více xxx ± 15 %. U některých xxxxxxxx, xxx xxxx xxxxxx regulace xxxx xxxxx dosáhnout, se xxxxxxxxx větší xxxxxx xxxxxxxx. Xx celou xxxx xxxxxx experimentu xxxx xxx xxxxxxxxxxx xxx xxxxxxxx, jak xx xx xxxxxxxxx xxxxx. Xxxxx xx xxxx částic x xxxxxxxx, xxxx xx xxxxxxxxxx xxxxxxxxx částic xxx xxxxx, xxx xx xxxxx xxxxxxxx (xxx nejméně jednou xxx xxxxxx xxxxxxxxxx xxxxxxx),
(x) xxxxxxx a xxxxxxx vzduchu xx xxxx xxxxxxxxxxx.
Xxxxx expozice x xx xxxxx xxxxxxxx xx xxxxxxxxxx xxxxxxxxx x zaznamenávají xxxxxxxxxxxx. Xxxxx xxxxx xx xxxx individuální xxxxxxxx. Xxxxx prvního xxx xx xxxxx xxxxxxxx pozorování xxxxx. Xxxxxxxxx jednou každý xxxxxxxx den je xxxxx provést xxxxxxx xxxxxxxx vyšetření. Xxxxx xxxxxxxxxx xxxxxxxxxx a xxxxxxxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxxxxxxx xxxxxxx xxxxx zvířat xx xxxxxx, xxxx. xxxxxx xxxx zmrazením xxxxxxxxx xxxxxx xxxx xxxxxxx xx xxxxxxxxx slabých xxxx xxxxxxxxxxx zvířat.
Pozorování xxxxxxxx xxxxx kůže, xxxxx, xxx, xxxxxxx, xxxxxxx a xxxxxxxx xxxxx, změny funkce xxxxxxxxx a xxxxxxxxx xxxxxxx soustavy, xxxxxxxxxxxxxxx xxxxxxxx x xxxxxxx. Xxxxxxxx pozornost xx xxxxx věnovat vnějšímu xxxxxxx, tremoru, xxxxxxxx xxxxx, slinění, průjmu, xxxxxxxx, xxxxxx a xxxxxx. Xxxxxxx uhynutí xx třeba xxxxxxxx xx xxxxxxxxxxx. Xxxxxxxx xxxxxxxxxxxx xxxxxx xx xxxxxxxxx xx expozici xxxxx x x xxxxxxxx uhynutí.
Zvířata, xxxxx xxxxx xxxxxx xxxxxx, x xx, xxxxx xxxxxxx do xxxxx xxxxxx, xx pitvají xx zvláštním xxxxxxxx xx všem změnám xxxxx x xxxxx xxxxx dýchacího traktu. Xxxxxxx makroskopické xxxxxxxxxxx xxxxx xx xxxxxxxxxxxxx x xxxxxxxx se xxxxxxxxx tkáně xxx xxxxxxxxxxxxxxxx xxxxxxxxx.
2 ÚDAJE
Údaje xx xxxxxxx xx xxxxxxx. X xx xxxx být pro xxxxxx experimentální xxxxxxx xxxxxx xxxxx xxxxxx xx xxxxxxx xxxxxx, xxxx uhynutí xxxxxxxxxxxx xxxxxx, xxxxx xxxxxx xxxxxxxxxxxx xxxxx příznaky xxxxxxxx, xxxxx xxxxxxxxx xxxxxx x pitevní xxxxxx. Změny xxxxxxxxx xx třeba xxxxxxxxx x zaznamenat, xxxxx xxxxxxx xxxxxxx xxxx xxx 1 xxx. Xxxxxxx, která xxxx xxxxxxx xxxxxxxx x xxxxxxx na utrpení xxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxx látkou, xxxx zaznamenána jako xxxxxxx vyvolaná testovanou xxxxxx. LC50 xx xxxxxxx xxxxxxxxx metodou. Xxxx se xxxxxxx xxxxx - xxxxx xxxxxxxx - mezi xxxxxxxx xxxxxxx xxxxxxxxx xxxxx x xxxxxxxx x xxxxxxx xxxxx xxxxxxxxxx, xxxxxx xxxx xxxxxxx, klinických xxxxxxxx, xxxxxxxxxxxxxxx poškození, změn xxxxxxx hmotnosti, mortality x xxxxx dalších xxxxxxxxx účinků.
3 XXXXXXX XXXXXX, PROTOKOL POKUSU X XXXXXXXXX ZPRÁVA
V xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx x x xxxxxxx xxxxxx xx xxxxx vést protokol.
Zpráva x průběhu xxxxxx xxxxxxxx následující informace:
- xxxxxxxxx druh, xxxx, xxxxx, podmínky ustájení, xxxxxxx, xxx.
- xxxxxxxx xxxxxx: popis xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx, xxxx, xxxxxxx, zdroje xxxxxxx, xxxxxxx xxxxxxxx xxxxxxxx, xxxxxxxxxxxxxx systému x způsobu umístění xxxxxx x xxxxxxxxxx xxxx, xxxxx xx xxxxxxxx. Xx xxxxx xxxxxx xxxxxxxxx xxx xxxxxx teploty, xxxxxxxx xxxxxxx, xxxxxxxxxxx a xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx,
- xxxxx x xxxxxxxx se sestaví xx tabulky a xxxxxx xxxxx s xxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxxxxxx xxxxxxxxxxx (xxxx. xxxxxxxxxxx odchylkou). Mají xxxxx možno obsahovat xxxx údaje:
a) xxxxxxxx xxxxxxx vzduchu v xxxxxxxxxx xxxxxxxx;
x) xxxxxxx x xxxxxxx xxxxxxx;
x) xxxxxxxxx koncentrace (xxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xx inhalačního xxxxxxxx, xxxxxx objemem xxxxxxx);
Xxxxxxxx: xxx xxxxxxxx xxxxxxxxx látek x xxxxxxx (xxxx. xx xxxx) xx xxxxx xxxxxx nejen výslednou xxxxxxxxxxx xxxxx ve xxxxxxx, xxxxx také, xxxxx xx xx xxxxx, xxxxxxxxxxx xxxxxx xxxxx xx vehikulu.
d) xxxxxx xxxxxxxx, xxxxx xxxx xxxxx;
x) xxxxxxxx xxxxxxxxxxx x xxxxxxx xxxx;
x) xxxxxxxxxx xxxxxx xxxxxxxxxxxxxxx xxxxxxx (XXXX) x xxxxxxxxxxx směrodatná xxxxxxxx (XXX);
x) xxxx xx xxxxxxxx xxxxxxxxx;
x) xxxx xxxxxxxx;
- tabulky xxxxxxxxx reakcí xxxxx xxxxxxx x xxxxxx xxxxxxxx (tj. xxxxx xxxxxx, xxxxx x xxxxxx uhynula nebo xxxx xxxxxxx xxxxxxxx; xxxxx xxxxxx x xxxxxxxx xxxxxxxx; xxxxx xxxxxxxxxxxx xxxxxx);
- doba xxxxxxx během xxxxxxxx xxxx xx xxxxx xxxxxxxx, důvody x xxxxxxxx pro xxxxxxx xxxxxxxx xxxxxx;
- všechna xxxxxxxxxx;
- hodnota XX50 xxx xxxxx pohlaví xxxxxxxxx xx xxxxxxxx xxxx xxxxxxxxxx (s xxxxxxxx xxxxxx xxxxxxx);
- 95% interval xxxxxxxxxxxxx xxx LC50 (pokud xx možno jej xxxxxxxx);
- xxxxxx závislosti xxxxxxxxx xx dávce (xxxxxxxxxxx) a její xxxxxxxx (xxxxx to xxxxxxxx xxxxxx xxxxxxxxx);
- xxxxxxx nálezy;
- xxxxxxx xxxxxxxxxxxxxxxx nálezy.
Diskuse xxxxxxxx (xx zvláštním zřetelem x xxxxx xxxxxxxxxx xxxxxxxx xxxxxx x xxxxxxxxx xxxxxx během xxxxx na xxxxxxxxxx xxxxxxx XX50).
Xxxxxx.
X.3 XXXXXX XXXXXXXX XXXXXXXX
1 METODA xx v xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
2)1.1 Xxxxxxx xxxxxx
Xxxxxxxxx xxxxx xx nanáší xx xxxx x xxxxxxxxxxxxxx dávkách xxxxxxxx xxxxxxxx pokusných xxxxxx, x xx každé xxxxxxx xxxxx úroveň xxxxx. Pozorují x xxxxxxxxxxxxx xx xxxxxx x případy xxxxxxx. Xxxxxxx, která xxxxxx xxxxx xxxxxx, i xxxxxxx, xxxxx xxxxxxx xxxxx xxxxxx, se xxxxxxx.
Xxxxxxx xx závažnými x xxxxxxxxxxxxxxx xxxxxxxx xxxxxxx a bolesti xx třeba humánním xxxxxxxx xxxxxxx. Xxxxxxxxx xxxxx xx nemají xxxxxxx v takových xxxxxxx x takovým xxxxxxxx, o kterých xx známo, xx xxxxxxxxxx xxxxxxx bolest x xxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxx xxxxxxxxxx vlastností.
1.2 Popis xxxxxx
1.2.1 Příprava
Nejméně 5 xxx xxxx testem xxxx xxxxxxx xxxxxxx x xxxxxxxxx nádobách x xxxxxxxxxx ustájení x xxxxxx, x xxxxxx xxxxx během xxxxxxxxxxx. Před xxxxxx xx xxxxxx xxxxx xxxxxxx xxxxxxx xxxxxxx xxxxxxx do xxxxxxxxxxxx xxxxxxxxxxxxxxxx skupin. Xxx 24 xxxxx před xxxxxxxxx xxxxx xx xxxx xxxxxx xx xxxxxx xxxxxxx nebo xxxxx. Při xxxxxxxx xxxx xxxxxx xxxxx xx xxxxx xxxx xx xx, xxx xx nepoškodila (xxxx. xxxxxx) kůže, což xx xxxxx xxxxxx xxxx propustnost. Xxx xxxxxxxx testované xxxxx xx připraví xxxxxxx 10 % povrchu xxxx. Xxx xxxxxxxx x pevnými xxxxxxx, xxxxxxxx xxxxxxxxxxxx x xxxxxxxx xxxxx, xx xxxxx xxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxx, xxx xxx xxxxx" xxxxxxx x xxxx. Xxx xxxxxxx vehikula xx xxxxx xxxx x xxxxx xxxx xxxxxxxx xx xxxxxx xxxxxxxxx xxxxx xxxx. Xxxxx xxxxxxxx xx xx xxx xxxxx tím, x jaké formě xx xxxx xxxx xxxxx xxxxxx xx xxxxx x xxxxxxx xxxx, x xx xxxxx xxxxxxxxxxxx xxxxxxx xxxxxx ten, xxxxx xxxxxxx usnadňuje průnik xxxx. Xxxxxxxxx xxxxxxxx xx xxxxxxxxx aplikují xxxxxxxx.
1.2.2 Xxxxxxxxxxxxxx xxxxxxxx
1.2.2.1 Xxxxxxx xxxxxxx
Xxxxxxx zvířata xxxx vybrána x xxxxxxx xx xxxx, xxxxxxx x xxxxx x xxxxxxx s xxxxxxxxxxx
§15 zvláštního xxxxxxxx xxxxxxxx
10) x xxxxxxxx tak, xxx xxxx možná identifikace xxxxxxxxxxxx zvířat. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx právního xxxxxxxx.
10)Xxxxxxx xx xxxxxxxxx xxxxxxx xxxx králíků. Lze xxxxxx x jiné xxxxxxxxx xxxxx, xxxxx xxxx pro xx xxxxxx. Xx xxxxx xxxxx známé xxxxx xxxxxxxxx xxxxxx. Na xxxxxxx testu xx xxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx (xxx xxxxx pohlaví xxxxxx) xxxxxxxxx ± 20 % střední xxxxxxx.
1.2.2.2 Xxxxx x pohlaví
Pro xxxxxx xxxxxx dávek xxxxxx xxxxxxx 5 xxxxxx xxxxxxxx xxxxxxx. Xxxxxxx-xx se xxxxx, xxxx xxx nullipary x nesmí xxx xxxxx. Xxxxx xx x dispozici xxxxxxxxx, xx xxxxx x xxxx pohlaví xx xxxxxxx xxxxxxxxxx, je xxxxx používat zvířata xxxxxx pohlaví.
Poznámka: Xxxxxxxxx-xx xx v xxxxxxxx xxxxxxx xxxxxxxx zvířata xxxxxxx xxxxx, xxx xxxx xxxxxxxx, mělo xx se zvážit xxxxxxx xxxxxxx počtu xxxxxx. Xxxxx xx xxxxx xxxxxxx xxxxxx x xx třeba xxxxxxxx, aby se xxxxxxxxxxxx mírně toxické xxxxx. X těchto xxxxxxx xx xxxxx xxxxxxx se xxxxxxxx xxxxxxxxx dávek xxxxxxxxx xxxxx.
1.2.2.3 Dávkování
Má xxx xxxxxxxxxx počet dávkových xxxxxx, xxxxxxx xxx, x mají být xxxxxx xxxxxxxxxxxx tak, xxx xxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxx účinků x xxxxxxxxx. Xxx xxxxxxxxxxx o xxxxxxxx xxxxx xx xxxxx xxxx x úvahu xxxxxxxx xxxx xxxxxxx xxxxxx testované xxxxx. Xxxxxxx údaje xxxx xxxxxx na xxxxxxxxxx xxxxxx xxxx xxxxxx x xxxxxxx, x xxxxxxx xxxxxxxxx XX50 x xxxxxxxxxxx xxxxxxxxxxxxx.
1.2.2.4 Xxxxxxx xxxx
Xxx xxxxxxx xxxxxxx xxxx xxxxxx xxxxxx xxxxxxx 2000 xx.xx-1 xxxxxxx xxxxxxxxx xx xxxxxxxxx 5 xxxxx x 5 xxxxx s xxxxxxxx xxxx popsaných postupů. Xxxxx xxxxx xxxxxxx xxxxxxx, je xxxxx xxxxxxx xxxxxx xxxxxx.
1.2.2.5 Xxxx xxxxxxxxxx
Xxxx pozorování xx být nejméně 14 xxx. Xxxxx xx xxxx xxxxxxxx xxxxxxxxx. Xxxx by xxx xxxxxx xxxxx xxxxxx xxxxxx, xxxxxxxxx xxxxxx xxxxxx a xxxxxx fáze xxxxxxxx. Xxxx pozorování xx xxxxx podle xxxxxxx xxxxxxxxxx. Xxxxxxxxxxx xx xxxx, xxx xx xxxxxxx xxxxxx xxxxxxx x xxxxxx x xxxx xx xxxxxxx, xxxxxxx xxx, xxx xx patrná tendence x xxxxxxx xxxxxxxx xxxxxxx.
1.2.3 Popis xxxxxxx
Xxxxxxx xx xxxxxxx xxxxxxxxxx x xxxxxxx. Xxxxxxxxx xxxxx se xxxxxx xxxxxxxxxx na plochu, xxxxx xxxx asi 10 % xxxxxxxxx xxxxxxx těla. Xxx xxxxxx xxxxxxx xxxxx xxxx xxx xxxx xxxxxx xxxxx; xxxx xx xx xxxx xxxxxxxxx xxxxxxxxxxx na xx xxxxxxxx část xxxx xxxxxx.
Xxxxxxxxx xxxxx xx po expoziční xxxx 24 hodin xxxxxxxxx x kontaktu x xxxx xxxxxx xxxxxxxxx xxxxxxxx obvazu x xxxxxxxxxx xxxxxxxx. Xxxxxxxxxx plochu je xxxx třeba xxxxxxx xxxxxxxx překrýt, xxx xx xxxxxx xxxxx x testovaná xxxxx xxxxxxxx x aby xx zabránilo xxxxxxxx xxxxxx. X xxxxxxxx xxxxxx xxxxx je xxxxx xxxxxx x xxxxxxxxxx pro xxxxxxx xxxxxxxx pohybu, xxxxxx xxxxxxxxxxx xxxx nelze xxxxxxxxx.
Xx uplynutí xxxx xxxxxxxx se xxxxxxxx xxxxxx testované xxxxx, xxxxx možno xxxxx xxxx xxxxx xxxxxxx xxxxxxxx xx provede xxxxxxxx xxxxxxx.
Xxxxxxxxxx xx xxxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx. Xxx xxxxx xxxxx xx třeba xxxx xxxxxxxxxx xxxxxxx. Xxxxx xxx xx xxxxxxx xxxxxxxx xxxxx. Xxxxxxx xxxxxx xxxxx xxxxxxxx den xx xxxxx provést xxxxxxx xxxxxxxx xxxxxxxxx. Další xxxxxxxxxx pozorování x xxxxxxxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxxxxxxx snížení xxxxx zvířat xxx xxxxxx, xxxx. xxxxxx xxxx xxxxxxxxx uhynulých xxxxxx xxxx xxxxxxx x utracením slabých xx xxxxxxxxxxx xxxxxx.
Xxxxxxxxxx xxxxxxxx xxxxx xxxxx, xxxx, na kterou xxxx xxxxxxxxx xxxxxxxx, xxx x xxxxxxx, x xxxx xxxxxxx x xxxxxxxx oběhu, xxxxx xxxxxx autonomní x centrální xxxxxxx xxxxxxxx, xxxxxxxxxxxxxxx xxxxxxxx x xxxxxxx. Xxxxxxxx xxxxxxxxx xx xxxxx xxxxxxx tremoru, xxxxxxxx xxxxx, xxxxxxx, xxxxxx, xxxxxxxx, xxxxxx a xxxxxx.
Xxxxxxx xxxxxxx xx xxxxx xxxxxxxx xx xxxxxxxxxxx. Xxxxxxx, která xxxxx xxxxxx xxxxxx, x xxxxx xxxxxxx xx do xxxxx xxxxxx, xx pitvají. Xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxx se zaznamenávají x poškozené xxxxx xx odeberou xxx xxxxxxxxxxxxxxxx vyšetření.
1.2.3.1 Xxxxxxxxx xxxxxxxx u xxxxxxx xxxxxxx
Xx xxxxxxxxx xxxxxx xx xxxxxx xxxxxxx xx xxxx xxxxx xxxxxxx jedné xxxxxxx x xxxx zvířatech xxxxxxx xxxxxxx, xxx xx zjistilo, xxx xxxxxxx druhého xxxxxxx xxxxxx xxxxxxx xxxxxxxxxx xx testovanou xxxxx. X xxxxxxxxxxx případech xxxx xxx xxxxxxxxxx xxxxxxx xxxxxxx počtu xxxxxx. Xxxxx xx x xxxxxxxxx spolehlivá xxxxxxxxx, xx xxxxxxx xxxxxxxxxxx xxxxxxx jsou xxxxxxx citlivější, testování xx xxxxxxxxx druhého xxxxxxx xx xxxxx xxxxxxxx.
2 XXXXX
Xxxxx se xxxxxxx do xxxxxxx. X ní musí xxx xxx každou xxxxxxxxxxxxxx skupinu xxxxxx xxxxx xxxxxx na xxxxxxx pokusu, xxxx xxxxxxx jednotlivých xxxxxx, xxxxx zvířat x xxxxxx xxxxxxx xxxxxx, xxxxx toxických xxxxxx x xxxxxxxxx xxxxxx. Xxxxxxxxx hmotnosti xxxxxxxxxxxx xxxxxx xx xxxxxxx xxxxxxxxxxxxx xxxx xxxxxxx xxxxxxxxx xxxxx, pak x t) denních xxxxxxxxxxx a xxxx xxxxxxxxx. Xxxxx xxxxxxxxx xx xxxxx xxxxxxxx x xxxxxxxxxx, xxxxxxx-xx xxxxxxx xxxx xxx xxxxx den. Zvířata, xxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxx s xxxxxxx xx xxxxx x xxxxxxx xxxxxxxx xxxxxxx xxxxxx, xx xxxxxxxxxxxxx xxxx uhynutí xxxxxxxx xxxxx látkou. XX50 xx xxxxxxx xxxxxxxxx xxxxxxx. Dále xx hodnotí xxxxx, xxxxx existuje, xxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxx a výskytem x xxxxxxx všech xxxxxxxxxx xxxxxx změn xxxxxxx, klinických xxxxxxxx, xxxxxxxxxxxxxxx xxxx, xxxx xxxxxxx hmotnosti, mortality x všech xxxxxxxxx xxxxxxxxx xxxxxx.
3 PROJEKT XXXXXX, XXXXXXXX POKUSU X XXXXXXXXX XXXXXX
X xxxxxxx s xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx zpracován xxxxxxx xxxxxx x x xxxxxxx pokusu je xxxxx xxxx xxxxxxxx.
Xxxxxx x xxxxxxx xxxxxx xxxxxxxx tyto informace:
- xxxxxxxxx xxxx, xxxx, xxxxx, xxxxxxxx xxxxx, xxxxxxx xxx.,
- xxxxxxxx xxxxxx (včetně xxxxxxx xxxxxxxx kůže x xxxx xxxxxx: okluzívní xxxx xxxxxxxxxxx),
- xxxxxx xxxxx (xxxxxx vehikula, xxxxx je xxxxx) x koncentrace,
- pohlaví xxxxxxxxx xxxxxx,
- tabulky xxxxxxxxx xxxxxx xxxxx xxxxxxx x xxxxx xxxxx (xxxxx xxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxxxxx xxxxx xxxxx; xxxxx zvířat x xxxxxxxx toxicity; počet xxxxxxxxxxxx xxxxxx),
- doba xxxxxxx xx xxxxxx xxxxxxxxx látky, důvody x xxxxxxxx xxx xxxxxxx xxxxxxxx xxxxxx,
- xxxxxxx pozorování,
- xxxxxxx XX50 xxx xx xxxxxxx, u xxxxxxx xxxx xxxxxxxxx xxxxx xxxxxx, x to xxx 14xxxxxxx xxxxxxxxxx (x xxxxxxxx xxxxxx xxxxxxx),
- 95% interval xxxxxxxxxxxxx pro XX50 (xxxxx jej xxx xxxxxxxx),
- xxxxxx xxxxxxxxxx xxxxxxxxx xx xxxxx x xxxx xxxxxxxx (xxxxx je stanovení xxxxx xxxxxxx xxxxx),
- xxxxxxx xxxxxx,
- všechny xxxxxxxxxxxxxxxx nálezy,
- xxxxxxxx xxxxx testů xx xxxxxx xxxxxxx.
Xxxxxxx x xxxxxxxx xxxxxxxx (xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx hodnoty XX50 x xxxxxxxxxxx x utracením xxxxxx x xxxxxxxxx xxxxxx xxxxx testu).
Závěry.
B.4 XXXXXX XXXXXXXX: XXXXXXXX X XXXXXXX XXXXXX NA XXXX
1 XXXXXX je x xxxxxxx x xxxxxx Evropských xxxxxxxxxxxx
7a).
1.1 XXXX
Xxx přípravě xxxx xxxxxxxxxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx zlepšením x xxxxxxx xxxxxxx xxxxxxxxx x pokusnými xxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx informací x xxxxxxxx xxxxx x xxxxx xxxxxxx xx xxxxxxxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx. Xxxxxxxx xxxx xxxxxx xx xxxxxxxxxx, aby xxxx xxxxxxxxxx popsané xxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxx látky na xxxx xx vivo xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxx. Xxxxx xxxx x dispozici nedostatečné xxxxx, lze xx xxxxxxxxxxx využitím metody xxxxxxxxxx xxxxxxxx
7a). Xxxxxxxxx xxxxxxxx xxxxxxxx provedení xxxxxxxxxxxx x xxxxxxxx xxxxxxx in xxxxx x xx xxxxxxx x tabulce 8 x xxxx xxxxxx. Xxxxx se x xxxxxxx potřeby v xxxxxxxxx xxxxxxx xx xxxx xxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxx postupná xxxxxxxx xxx testovacích xxxxxxxx.
X xxxxx spolehlivého xxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxx x xxxxxxxxx zvířaty xx xx xxxxxxx xx xxxx xxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxxx xxxxxxxx xxxxx významné xxx potenciální xxxxxxx xxxx xxxxxxxx xxxxxx xxxxx xxxxxxxxxxx xx xxxxxxx analýzy průkaznosti xxxxxxxx. Xxxxxx xxxxx xxxxx xxxxxxxxx xxxxxx xx xxxxxxxxxxx xxxxxx xx xxxxxx xxxx xxxxxxxxx zvířatech, důkazy xxxxxxxxx xxxx xxxxxxxxxx xxxxxx jedné xxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxx xxxxx xxxxxxxx xxxxx, xxxxx xxxxxxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxxx xxxxx
7a) x xxxxxxxx xxxxxxxxxxxx x uznaných zkoušek xx xxxxx xxxx xx xxxx
7a). Tato xxxxxxx xx měla xxxxxx xxxxxxx zkoušek xxxxxxxxx nebo dráždivých xxxxxx xx xxxx xxxxxxx xx xxxx x xxxxx, x xxxxx xxx existují xxxxxx x xxxxxx xxxxxx, xxxxx xxx x tyto xxx xxxxxxxxx.
X tabulce 8 x této xxxxxx xx uvedena xxxxxxxxxxxxxxx xxxxxxxxx postupného zkoušení, xxxxx součástí je xxxxxxxxx xxxxxxxxxxxx x xxxxxxxx zkoušek xxxxxxxxx/xxxxxxxxxx xxxxxx in vitro xxxx ex xxxx. Xxxx xxxxxxxxx xxxx xxxxxxxxxxx xx semináři XXXX
7a), xxxx účastníky xxxxxxxxxxx xxxxxxxxxx x xxxxxxx jako xxxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxx harmonizovaném systému xxxxxxxxxxx chemických látek (XXX)
7a). Xxxxxxxxxx se, xxx se xxxxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxx xx xxxx. X xxxxxx látek xx doporučuje xxxxxx xxxxxxxx xx xxxxxxx, xxxx xxx lze xxxxxxxxx vědecky xxxxxxxxxxxx xxxxx x xxxxxxxxx/xxxxxxxxxx xxxxxxxx látky. X xxxxxxxxxxxx xxxxx, x xxxxxxx xxxxxxxxx/xxxxxxxxxx účincích xx xxxx není x dispozici xxxxxxxx xxxxx, xx xx xxxx tato xxxxxxxxx xxxxxx xxx doplnění xxxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxx xxxxxxxxx xxxx xxxxxxx zkoušení nebo xxxxxxxxxx xxxxxxxx xxxxxx xx krocích musí xxx xxxxxxxxxx.
Xxxxx xxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx x xxxxxxxxx xxxx xxxxxxxxxx účincích xxxxxxxxxx, měla xx xx x souladu xx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxx xxxxxxx xx xxxx (xxx xxxxxxx 8).
1.2 XXXXXXXX
Xxxxxxxx xxxxxx na kůži: xxxxxxxx vratných změn xx xxxx do 4 x xx xxxxxxxx xxxxxxxx xxxxx.
Xxxxxxx xxxxxx xx xxxx: xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx, xxxxxxx xxxxxxxxx, xx koria xxxxxxxxxx xxxxxxx xxxxxxx, xx xxxx xxxxx xx xxxxxxxx xxxxxxxx xxxxx. Xxxxxx po xxxxxxxxx xx xxxxxxxxx xxxxx, xxxxxxxxx, xxxxxxxx strupy x v xxxxxx xxxxxxxxxxxxxxx pozorování ztrátou xxxxx x důsledku xxxxxxxxxx xxxx, úplnými xxxxxxx xxxxxxxx x xxxxxxx. K xxxxxxxxxxx xxxxxxxx xxxx xx xx xxxx xxxxxx xxxxxxxxxxxxxx.
1.3 XXXXXXXX XXXXXXXX XXXXXX
Xxxxx, xxxxx xx xxx xxxxxxxx, xx x xxxxx xxxxx xxxxxx xx xxxx xxxxxxxxx xxxxxxx, xxxxxxx xxxxxxx neexponované xxxx xxxxxxxxx xxxxxxx slouží xxxx xxxxxxxx. Xx xxxxxxxxxxx intervalech xx xxxx, xxxxxxxxx x xxxxxxxx xxxxxx xxxxxx xxxxxxxxxx/xxxxxxxxx xxxxxx, xxx xxxx možno provést xxxxx posouzení xxxxxx. Xxxx xxxxxx xx xxxx být xxxxxxxxxx xxxxxx, aby bylo xxxxx xxxxxxxxx xxxxxxxx xxxx nevratnost xxxxxxxxxxxx xxxxxx.
Xxxxxxx xxxxxxx, xxxxx x jakékoli xxxx xxxxxxx vykazují xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxx bolesti, xx xxxxxxx xxxxxx x xxxxx xx xxxxxxxxxxxxx xxxxxxxx vyhodnotí. Xxxxxxxx xxxxxxxxxxx o utracení xxxxxxxxxxx x xxxxxxx xxxxxxxx pokusných zvířat xxx xxxxxx x xxxxxxxxxx
7a).
1.4 POPIS XXXXXXXX XXXXXX
1.4.1 Příprava na xxxxxxx xx xxxx
1.4.1.1 Xxxxx xxxxx pokusných xxxxxx
Xxxxxxxxxxxxxxxx pokusným xxxxxxxx xx albín králíka x xxxxxxxxx se xxxxx dospělá xxxxxxx xxxxxxx. Xxx xxxxxxx xxxxxx xxxxx xx xx mělo xxxxx xxxxxxxxxx.
1.4.1.2 Příprava xxxxxxxxx xxxxxx
Xxxxxxx zvířata xxxx xxxxxxx x xxxxxxx xx druh, xxxxxxx x stáří v xxxxxxx x xxxxxxxxxxx
§15 zvláštního právního xxxxxxxx
10) x xxxxxxxx xxx, aby byla xxxxx xxxxxxxxxxxx jednotlivých xxxxxxxxx xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx právního xxxxxxxx
10).
Xxx 24 x xxxx xxxxxxxxx xxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxx xxxx xx xxxxxx. Xx třeba dbát xx to, xxx xx xxxx xxxxxxxxxx. Xxxxx xx xxxxxx xxxxx xxxxxxx xxxxxxx xx zdravou, xxxxxxxxxxx xxxx.
Xxxxxxx xxxxx králíka xxxx plošky husté xxxxx, xxxxx xxxx x některých xxxxxxxx xxxx xxxxxxxxxx. Xx xxxxxxxx xxxxxxxxx xxxxx xxxxx xx se xxxxxxx provádět xxxxxx.
1.4.1.3 Xxxxxxxx xxxxxx xx xxxxxx
Xxxxxxx xxxxxxx xx xxxx xxx xxxxxxx xxxxxxxxxx. Teplota x xxxxxxxxx xxx pokusná xxxxxxx xx měla x xxxxxxx xxx (20 ± 3) °X. Xxxxxxx by xxxxxxxxx vlhkost měla xxxxx xxxxxxxxx 30 % x pokud xxxxx xxxxxxxxxxxx 70 % xxxxx xxxx xxxxxx místnosti, xxxxx xx xxxx být xxxxxxx 50 - 60 %. Xxxxxxxxx xx xxxx být xxxxx, xxxx xx xx střídat 12 x světla x 12 x tmy, xxxx-xx v xxxxxx xxxxxxxxx xxxxx světlo. Xx xxxxxx xxx xxxxxx xxxxxxx xxxxxx xxxxxx xxx xxxxxxx xxxxxxx xx xxxxxxxxxxxxxx xxxxxxx s xxxxxxxxxx xxxxxxxx xxxxx xxxx. Xxxxxxx xxxxxxx mohou xxx chována v xxxxxxx xx skupinách x souladu s xxxxxxxxxx právním předpisem
10), xxxxx xxxx xxxxxxxxx xxxxxxxxx xxxxxx jinak, xxx xxxxx xxxxxxxxx xxxxxx x kleci xxxxx bránit xxxxxxxxxx xxxxxxxxxx xxxxxxx pokusného xxxxxxx.
1.4.2 Postup xxxxxxx
1.4.2.1 Xxxxxxxx zkoušené látky
Zkoušená xxxxx se nanese xx malou plochu xxxx (asi 6 xx2) a pokryje xx plátkem xxxx x xxxxxxxxxxx náplastí. X xxxxxxxxx, xxx xxxxx xxxxxxxx xxxx xxxxx (např. xxxxxxxx xxxx xxxxxxx xxxxx), xx xx měla xxxxxxxx xxxxx nejprve xxxxxx xx xxxxxx xxxx, který xx xxxxxxxx xxxxxxx xx xxxx. Xx xxxx xxxxxx xxxxxxxx xx xxxxx přidržovat xxxxxx xxxxx na xxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxx. Xxxxx se zkoušená xxxxx nanáší xx xxx, xxx xx xxx xx kůži xxxxxxxxx xxx, xxx xx zajistil xxxxx xxxx s kůží x xxxxxxxxxx xxxxxxxxx xxxxx xx xxxx. Xx třeba zabránit xxxx, xxx se xxxxxxx xxxxx xxxxxxx x xxxx x xxxxxxxxx xxxxx požilo xxxx vdechlo.
Kapalné xxxxxxxx xxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxx. Xxx xxxxxxxxx xxxxxxx xxxxx (xxxxx mohou být xxxxx xxxxxxx xxxxxxxxx xx xxxxx) xx xxxxxxxx látka xxxxxxx xxxxxxxxx xxxxxxxxx vody (xxxx xxxxx xxxxxxx xxxxx xxxxxxx xxxxxxxxx) xxxxxxxxxxx x zajištění xxxxxxx xxxxx x xxxx. Pokud se xxxxxxxxx jiná vehikula xxx xxxx, xxx xx být xxxxxxxxxxx xxxx vehikula na xxxxxxxx xxxxxx zkoušené xxxxx xx xxxx xxxxx minimální.
Po uplynutí xxxx xxxxxxxx, která xx xxxxxxx 4 x, xx xxxxxxxx xxxxxx xxxxxxxx xxxxx, xxxxx možno xxxxx xxxx xxxxxxx xxxxxxxxxxxxx, xxxx xx xxxxx x xxxxxxxxx odezvy xxxx xxxxxxxxxxx xxxx.
1.4.2.2 Xxxxxx xxxxx
Xx testovací xxxxx xx xxxxxx 0,5 xx kapaliny xxxx 0,5 x xxxx xxxxx nebo xxxxx.
1.4.2.3 Počáteční xxxxxxx (xxxxxxx xxxxxxxxxx/xxxxxxxxx účinků xx xxxx xx xxxx x xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx)
Xxxxxxx xx xxxxxxxxxx, xxx xxxx xxxxxxx in xxxx provedena xxxxxxx xx xxxxxx xxxxxxxx xxxxxxx, zejména xxxxx xxxxxxxx podezření, xx xxxxx xx xxxxxxxxxxx xxxxxxx xxxxxx. Xxxxx xxxxxx je v xxxxxxx se xxxxxxxxx xxxxxxxxxx xxxxxxxx (xxx xxxxxxx 8).
Pokud xxxx xx základě xxxxxxx xxxxxxxxxxx xxxxxxxx látka xxxxxxxxx jako xxxxxx, xxxx žádné xxxxx xxxxxxxx xx pokusných xxxxxxxxx xxxxx. X xxxxxxx xxxxx, u xxxxx xx podezření, xx jsou xxxxxx, xxxxxx obvykle xxxxx xxxxxxx xx vivo xxxxxxxx. Xxxxx x xxxx případech, xxx xx xxxxx nedostatku xxxxxx považováno xx xxxxxxxx xxxxxxx další xxxxx, xxxxx být x xxxxxxx míře xxxxxxxxx xxxxxxx xx xxxxxxxxx zvířatech xxxxx xxxxxx postupu: pokusnému xxxxxxx xx xxxxxxxx xxxxxxx nejvýše xxx xxxxxxxxx náplasti. První xxxxxxx xx xxxxxxxx xx třech minutách. Xxxxx xxxx xxxxxxxxxx xxxxxxx xxxxx xxxxxx, xxxxxxxx xx druhá xxxxxxx po xxxxx xxxxxx. Xxxxx xxxxxxxxxx x xxxx xxxx xxxxxxxxx, že xxxxxxxx xxx xxx xxxxxxxx xxxxxx humánního zacházení xxxxxxxxxx na xxxxx xxxxxx, xxxxxxx se xxxxx náplast, xxxxx xx po xxxxxxx xxxxxxxx odstraní, x xxxxxxxxx se xxxxxx.
Xxxxx xx po některé xx xxx následných xxxxxxx xxxxxxxxx xxxxxxx xxxxxx, zkouška xx xxxxxxxx xxxxxx. Pokud xx xxxxxxxxxx xxxxx xxxxxxxx xxxx xxxxxxx xxxxxx xxxxxxxxx, xxxxxxx xxxxx xx pozoruje xx xxxx 14 xxx, xxxxx se x xxx xxxxxxxxx xxxx xxxxxxxxx dříve.
V xxxxxxxx případech, kdy xx x zkoušené xxxxx nepředpokládá, xx xxxxxx xxxxxxx účinky, xxx xxxx xxx xxxxxxxx, xx se xxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxx xx čtyři xxxxxx.
1.4.2.4 Xxxxxxxxxxx xxxxxxx (xxxxxxx xxxxxxxxxx xxxxxx xx xxxx xx xxxx s xxxxxxx xxxxxxxxx zvířaty)
Pokud xxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxx účinek, xxxx by xx xxxxxxxx xxxx xxxxxxxxx xxxxxx xxxxxxxx na xxxx xxxxxxx xxxxxxxxx xxxxxxxxx, u xxxxxxx x jednou xxxxxxxx x xxxxx xxxxxxxx 4 x. Xxxxx xx během xxxxxxxxx xxxxxxx xxxxxxxxx dráždivý xxxxxx, xxx xxxxxxxxxxx xxxxxxx provést xxxxxxxx, xxxx xxxxxxxxxxx xxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxxx. Ve xxxxxxxxxx xxxxxxx, xxx xx xxxxxxxxx xxxxxxx xxxxxxxxx, xxx dvěma nebo xxxx xxxxxxxx zvířatům xxxxxxxx xxxxx xxxxxxx, xxxxx xx xx xxxxxxx xxxxxxxx xxxxxxxx. Xxxxxxxx se xxxxxxx xxx xxxxxxx zvířata x x xxxx xx xxxxxxx stejná xxxxxx, xxxx žádné xxxxx xxxxxxxx nutné. Xxxxx xx xxxxxx xxxx xxxxx xxxxxxx xxxxx. Sporné reakce xxxx xxx xxxxx xxxxxxxxx na xxxxxxx xxxxxxxxx xxxxxxxxx.
1.4.2.5 Xxxx xxxxxxxxxx
Xxxx pozorování xx xxxx být dostatečně xxxxxx, aby bylo xxxxx xxxx xxxxxxxxx xxxxxxxx pozorovaných účinků. Xxxxxxx xx však xxxx xxx ukončena xxxxxxxx x okamžiku, xxx pokusné zvíře xxxxxxxx přetrvávající příznaky xxxxxx xxxxxxx nebo xxxxxxx. Xx xxxxxx xxxxxx xxxxxxxxx xxxxxx xx xx pokusná xxxxxxx xxxx pozorovat 14 dnů xx xxxxxxxxxx xxxxxxxx. Xxxxx xx vratnost xxxxxxxxxx xxxx xxxxxxxxx 14 xxx, xxxxxxx by xx měla x xxxxx okamžiku xxxxxxx.
1.4.2.6 Xxxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxx xxxx
Xxxxxxx xxxxxxx xxxxxxx xx xxxxxxxx na příznaky xxxxxxx x xxxxx x xxxxxx xxxx xx hodnotí xx 60 min x xxxx po 24, 48 a 72 x po odstranění xxxxxxxx xx zkoušenou xxxxxx. V xxxxxxxxx xxxxxxx xx xxxxxx xxxxxxxx zvířeti xx xx odstranění xxxxxxxx xxxxxxxx vyšetří xxxx xxxxxxxxx xxxxx. Xxxxx xxxxxx se xxxxxxxxx x xxxxxxxxxxx podle xxxxxxxx v xxxx xxxxxxx xxxxxxx 9. Xxxxx xx objeví xxxxxxxxx xxxx, xxxxx xx 72 h xxxxx označit za xxxxxxxx nebo leptavé xxxxxx, xxxx být xxxxxxxx xxxxxxxxxx xx xx 14. xxx xxxxx stanovení vratnosti xxxxxx. Xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx xx xxxx xxx xxxxxxxx xxxxxxx x zaznamenány xxxxxxx místní xxxxxxx xxxxxx, jako xx xxxxxxxxx kůže x xxxxxxxx xxxxxxxxx nežádoucí xxxxxx (xxxx. vliv xx xxxxxxxx příznaky xxxxxxxx x xxxxxxxx xxxxxxxx). Xxx objasnění xxxxxxxx xxxxxx xx xx xxxx xxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx.
Xxxxxxxxx xxxxxx xxxx je xxxxxxxxxxxx xxxxxxxxxxx. X cílem xxxxxxxxxx harmonizaci xxxxxxxxx xxxxxx kůže a xxxxxxxxx zkušebním xxxxxxxxxxx x těm, xxx xxxxxxxxx a interpretují xxxxxxxxxx, musí xxx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxx práci x xxxxxxxxxx xxxxxxxx vyhodnocování (xxx níže uvedená xxxxxxx 9). Xxxx xxxxxxx xxx xxxxxx xxxxxxxxxxx pokyny xxx xxxxxxxxx dráždivých xxxxxx xx xxxx x xxxxxx Xxxx
7a).
2 XXXX
2.1 XXXXXXXXXXX XXXXXXXX
Xxxxxxxx xxxxxx xx xxxxxx xx xxxxxxx uvedené v xxxxxxxxxx xxxxxxxxx x xxxxxxx. Měly xx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxx x xxxxx 3.1.
2.2 XXXXXXXXX XXXXXXXX
Xxxxxx xxxxxxxxxx xxxxxx na xxxx se xxxxxxxx xx xxxxxxx x xxxxxxx a stupněm xxxxxxxxxx xxxx x xxxxxx xxxxxxxxx nebo xxxxxxxxxxx. Jednotlivé xxxxxx xxxxxxxxxxxxx xxxxxxxxx měřítko xxxxxxxxxx xxxxxxxxxx látky, xxxxx xx xxxxxxx xxxx jiné účinky xxxxxxxx xxxxx. Xxxxxxxxxx xxxxxx xx xxxxx xxxx xxx xxxxxxxxxx xx xxxxxxxxxx xxxxxxx, xxxxx xx xxxxx xxxxxxxxx společně x xxxxxxx xxxxxxxxxxxx vyplývajícími xx xxxxxx.
Xxx hodnocení xxxxxxxxxx xxxxxx xx xxxxxxxx xxxxxxxx xxxxxxx xxxx. Xxxxx xx xxxxxxxx xxxxxxxxxxxxx doby xxxxxxxxxx přetrvávají xxxxxx xxxx alopecie (xx xxxxxxx xxxxx), hyperkeratóza, xxxxxxxxxxx x xxxxxxxxxx, xxxxxxxx xx zkoušená xxxxx xx xxxxxxxxx.
3 XXXXXXX POKUSU, XXXXXXXX XXXXXX X ZÁVĚREČNÁ XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9),10) xxxx xxx xxxxxxxxx xxxxxxx pokusu x x průběhu xxxxxx xx xxxxx vést xxxxxxxx.
3.1 Xxxxxx o xxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxx:
Xxxxxxxxxx xxxxxxxx xx vivo: xxxxxxx xxxxxxxxxxx výsledků předchozích xxxxxx, xxxxxx výsledků xxxxxxxxx postupného xxxxxxxx:
- xxxxx relevantních údajů x xxxxxxxxxxx xxxxxxx,
- xxxxx xxxxxxx x xxxxx fázi strategie xxxxxxxx,
- xxxxx xxxxxxxxxxx xxxxxxx in xxxxx, xxxxxx xxxxxxxxxx xxxxx x xxxxxxxxx x x xxxxxxxxxx xxxxxxxxx xx xxxxxxxxxx/xxxxxxxxxxxx xxxxxxx,
- xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxx studie xx xxxx.
Xxxxxxxx xxxxx:
- xxxxxxxxxxxxx xxxxx (např. xxxxx XXX, xxxxx, xxxxxxx, známé xxxxxxxxx, xxxxx),
- xxxxxxxxx xxxxxx x xxxxxxxxx-xxxxxxxx xxxxxxxxxx (xxxx. xX, xxxxxxxx, xxxxxxxxxxx, xxxxxxxxx),
- xxxxx xxx x xxxx, xxxx složení a xxxxxxxxx xxxxx xxxxxx xxxxxxxxx v xxxxxxxxxx.
Xxxxxxxxx:
- xxxxxxxxxxxx, koncentrace (podle xxxxxxx), xxxxxxx xxxxx,
- xxxxxxxxxx výběru vehikula.
Pokusná xxxxxxx:
- použitý druh/kmen, xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx zvířat, xxxx-xx xxxxxx xxxxx králíka,
- xxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxx,
- hmotnosti xxxxxxxxxxxx xxxxxxxxx zvířat xx xxxxxxx x x xxxxxx zkoušky,
- xxxxx na začátku xxxxxx,
- xxxxx pokusných xxxxxx, xxxxxxxx chovu, xxxxxx atd.
Zkušební xxxxxxxx:
- xxxxxxxx přípravy oblasti xxxx, xx xxx xx xxxxxx náplast,
- xxxxxxxx xxxxx o xxxxxxxxxxx xxxxxxxxx xx xxxxxxxx a technice xxxxxxxxxx náplastí,
- xxxxxxxx xxxxx x xxxxxxxx xxxxxxxx látky, jejím xxxxxxxx x odstranění.
Výsledky:
- xxxxx x xxxxxx xxxxxx xx dráždivé xxxx xxxxxxx xxxxxx x každého xxxxxxxxx xxxxxxx ve všech xxxxxxxxxx xxxxxx,
- xxxxx xxxxx pozorovaných xxxx,
- xxxxxxxx xxxxx xxxxxx x xxxxxx xxxxxxxxxxxx xxxxxxxxxx nebo xxxxxxxxx xxxxxx x xxxxxxxx xxxxxxxxxxxxxxxx nálezy,
- popis xxxxxx xxxxxxxx (xxxx. xxxxxxxxx xxxx) x xxxxxxxxxxx xxxxxx xxxxx xxxxxxxxxx nebo xxxxxxxxx xxxxxx na xxxx.
Xxxxxxx x xxxxxxxxxxxx xxxxxxxx.
Xxxxxx.
XXXXXXX 9: XXXXXXXXX KOŽNÍCH XXXXXX
Xxxxxx xxxxxxx a xxxxxxxxx
Xxxxx xxxxxx 0
Xxxxx xxxxx xxxxxx (sotva xxxxxx) 1
Xxxxxxxx viditelný xxxxxx 2
Xxxxx xx xxxxxxx erytém 3
Xxxxx xxxxxx (xxxxx zrudnutí) xxxx xxxxxx příškvaru xxxxxxxxxxxx xxxxxxxxx xxxxxxx 4
Xxxxxxxxx xxxxx: 4
Xxxxxx xxxxx
Xxxxx xxxx 0
Xxxxx xxxxx xxxx (sotva xxxxxx) 1
Xxxxx xxxx (xxxxxx jsou xxxxxx, xxxxxx je xxxxxxxxxx xxxxxxxxx xxxxxxxxx) 2
Xxxxx xxxx (okraje vyvýšeny xxx o 1 xx) 3
Xxxxxxx xxxx (xxxxxxx xxxx než 1 xx a xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx) 4
Xxxxxxxxx xxxxx: 4
Xxx xxxxxxxxx xxxxxxxx reakcí lze xxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx.
Xxxxxxx 8
Xxxxxxxxx xxxxxxxxxx zkoušení xxxxxxxxxx a xxxxxxxxx xxxxxx xx xxxx
XXXXXX XXXXX
X zájmu spolehlivého xxxxxxxxx přístupu x xxxxxxx zacházení x xxxxxxxxx zvířaty xx xxxxxxxx xxxxxxx xx xxxxxxxxxx používání xxxxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxx, které x pokusných xxxxxx xxxxxxxxxxxxx vyvolají xxxxxxx xxxxxx. Xxxxxxx xxxxxxxxx xxxxxxxx xx potenciálních xxxxxxxxx/xxxxxxxxxx účinků látky xx xxxx by xx xxxx xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxx xx xxxx. Xxxx xxx xxxxxxxxx xxxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxxxx xxxxx xxxxx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxx xxxxxx xx kůži, xxxx by bylo xxxxx xxxxxxxx xxxxxxx xx xxxxxxxxx xxxxxxxxx. Xxxxx využití xxxxxxx xxxxxxxxxxx xxxxxxxx a xxxxxxxxx postupného xxxxxxxx xxxxx xxxxxxx provádět xxxxxxxx xx xxxx, xxxxxxx xxxxx látka xxxxxxxxxxxxx xxxxxx xxxxxxx xxxxxx.
Xxxxxxxxxx se, xxx xx stávající xxxxxxxxx xxxxxxxx xx dráždivých xxxx leptavých účinků xxxxx na xxxx xxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx, xx xxxxxx základě xx xxxxxxxx x xxx, xxx xx xx x xxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxx xxxxxxx xxxxx xxxxxx xxxx xxx xxxxx xxxxxx xx xxxx. Xxxx-xx xxxxx další xxxxxx, xxxxxxxxxx xx xxxxxx strategie xxxxxxxxxx xxxxxxxx x xxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxx. X xxxxx, které xxxxxxx xxxxxx zkoušeny, xx xxxx být strategie xxxxxxxxxx xxxxxxxx xxxxxxx x xxxxxxx xxxxxxx xxxxx, xxxxx xxxx xxxxxxxx x xxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxx dráždivých účinků. Xxxxxxxxx xxxxxxxx xxxxxxx x xxxx tabulce 8 xxxx vypracována xx semináři XXXX
7a) x později potvrzena x rozpracována x Xxxxxxxxxxxxxx integrovaném xxxxxxx xxxxxxxxxxx nebezpečí xxxxxxxxxx xxxxx pro xxxxxx xxxxxx x xxxxxx xxxxx xx xxxxxxx xxxxxxxxx, xxxxx schválilo 28. xxxxxxxx xxxxxxxx Xxxxxx pro xxxxxxxx xxxxx x Pracovní xxxxxxx pro xxxxxxxx xxxxx v xxxxxxxxx 1998
7a).
Xxxxxxx xxxx xxxxxxxxx xxxxxxxxxx zkoušení xxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx X.4, vyjadřuje xxxxxxxxxxxx postup xxxxxxxxx xxxxxxxxxx/Xxxxxxxxx účinků xx xxxx. Xxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx x etický standard xxx xxxxxxxx xxxxxxxxxx/xxxxxxxxx xxxxxx xx xxxx xx xxxx. Metoda xxxxxxxx xxxxxxxxx xxxxxx xxx provádění xxxxxxx xx vivo x xxxxxxx xxxxxxx, které xx xxxx xxxxxxxxx xxxxxx zkoušky měly xxx xxxxxxx. Xxxx xxxxxxxxx představuje přístup xxxxxxxxxx existujících xxxxx x xxxxxxxxxx/xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxxxxxx přistup x xxxxxxxxx relevantních xxxxx x xxxxxxx, u xxxxxxx je xxxxx xxxxxxx xxxxx xxxxxx, xxxx x xxxxx xxxxx xxxxxx xxxxxx xxxxxxx provedeny. Xxxxxxxxxx xx xxxx za xxxxxxxx okolností xxxxxxx xxxxxxxxxx x xxxxxx xxxxxxx xx xxxxx xxxx ex xxxx xx xxxxxxxx xxxxxxxxxx/xxxxxxxxx xxxxxx na kůži.
POPIS XXXXXXXXX XXXXXXXXXXXXX X XXXXXXXX
Xxxx xxxxxxxxx zkoušek x xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx (xxxxxxx 8 xxxxxxxxxxx) se xxxxxxxxx veškeré xxxxxxxx xxxxxxxxx, xxx se xxxxx xxxxxxxxxx o xxxxxxxx xxxxxxx xxxxxxxx xx xxxx. Xxxxxxx xxx významné xxxxxxxxx xxxxxx x vyhodnocení xxxxxxxxxxxx xxxxxxxxx (xxxx. xxxxxxxx hodnota xX), xxxxxxxxx informace by xx měly xxxx x xxxxx jako xxxxx. Xxxxxxx xxxxxxxxxx xxxxx x účincích xxxxxxx látky xxxx xxxxxx xxxxx xx xxxxxxxxx na xxxxxxx xxxxxxxxxx založeném xx xxxxxxxxxxx xxxxxxxx. Xxxx xx xx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxxx. Xxxxxx důraz by xx xxx xxxxx xx xxx existující xxxxx x xxxxxxxx xxxxx xx xxxxxxx x zvířata a xxxx na xxxxxxxx xxxxxxxx xx vitro xxxx xx xxxx. Xxxxxx žíravých xxxxx xx vivo xx xx měly provádět xx xxxxxxx. Mezi xxxxxxx uvedené xx xxxxxxxxx xxxxxxxx xxxxx:
Xxxxxxxxx xxxxxxxxxxxx xxxxx x xxxxxxxx xxxxx na xxxxxxx x xxxxxxx (xxxx 1). Xxxxxxx xx xxxxx vzít x xxxxx existující xxxxx x xxxxxxxx xx xxxxxxx, např. xxxxxxxx studie xxxx xxxxxx nemocí z xxxxxxxx, xxxxxxx subjektů xxxxxxxxx xxxx xxxxx x zkouškách xx xxxxxxxxx xxxxxxxxx, xxxx. x xxxxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxx dermální xxxxxxxx, xxxxxxx z xxxxxx xxxxx xxx xxxxxx informace přímo xx xxxxxxxxxx x xxxxxxx xx xxxx. Xxxxx, xxxxxxx dráždivé xxxx xxxxxxx xxxxxx xxxx xxxxx, x xxxxx, x xxxxx xxxxxxxx xxxxxxxxxxx důkazy, xx xxxxxxx xxxx xxxxxxxx účinky xxxxxx, xxxx nutné xxxxxxx xx studiích in xxxx.
Xxxxxxx xxxxxx xxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx (SAR) (xxxx 2). Xxxxxx xx x xxxxx výsledky xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx, xxxx-xx x xxxxxxxxx. Pokud xxxx x xxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxx xxxxx xx xxxxxxx xxxx xxxxxxx xxxxxxx xxxxxxxxxxx, xx xxxx xxxxxxxxx xxxxxxxxx/xxxxxxxxxx xxxxxx, xxx xxxxxxxxxxxx, xx hodnocená xxxxxxxx xxxxx xxxxxx xxxxxx xxxxxx. V xxxxxxxx xxxxxxxxx xxxx xxxxx tuto látku xxxxxxx. Xxxxxxxxx údaje xxxxxxx xx xxxxxx xxxxxxxxxx příbuzných xxxxx xxxx jejich xxxxx xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx dostatečný xxxxx o xxxxxxxxxxx xxxxxxxxx/xxxxxxxxxx účinků látky. Xx stanoveni xxxxxxxxxxxxx xxxxxxxxx a xxxxxxxxxx xxxxxx xx xxxx xx xxxx xxx xxxxxxx validované x xxxxxx postupy xxxxxxxxxxx x xxxxxxx SAR.
Fyzidálně-chemické xxxxxxxxxx x xxxxxxxx xxxxxxxxxx (krok 3). Xxxxx xxxxxxxxxx extrémní xxxxxxx pH xxxx ≤ 2,0 x ≥ 11,5 xxxxx xxx xxxxx místní xxxxxx. Xxxxx xx xxxxxxx xxxxxx xxxxx xx xxxx xxxxxxx xx xxxxxxx extrémních xxxxxx xX, xxx xxxx xxxx v xxxxx xxxxxxx/xxxxxxxxxx xxxxxxx (xxxxxxxx xxxxxxxx)
7a). Xxxxx xxx xxxxx xxxxxxxx xxxxxxxx xxxxxx, xx xxxxx xxxxx xxxx xxxxxxx účinky xx xxxx, xxxx tento xxxxxxxxxx xxxxxxxx další xxxxxxx, xxxxx možno x xxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxx xx xxxxx xxxx xx xxxx (xxx xxxxx 5 x 6).
Xxxxxxxx xxxxxxxx (xxxx 4). Xxxxx xx xxxxx, xx xxxxxxxx xxxxx je při xxxxxx dermální xxxxxx xxxxxx toxická, xxxxxx xxx xxxxxx dráždivých/leptavých xxxxxx na xxxx xx xxxx, xxxxx xxxxxxxx xxxxxxxx xxxxx, xxxxx xx xxxxxxx xxxxxx, xx xxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxx x xxx xx xxxxxxxx uhynutí xxxx xxxxxxx utrpení xxxxxxxxx xxxxxx. Xxxxx xxxxx xxxx xxxxxx xxxxxxxx toxicity xxxxxxxxxxx xxxxxx králíka již xxxxxxxxx xx xxxxxxx xxxxxx xxxxx 2&xxxx;000 xx/xx xxxxxxx hmotnosti xxxx xxxxx x xxxxxx xxxxxxxx xxxxx xxxxxxxx nebo leptavé xxxxxx, xxxxxx být xxxxx xxxxxxx xxxxxxxxxx/xxxxxxxxx xxxxxx xx xxxx xxxxxxxx. Xxx xxxxxxxxx xxxxxx dermální toxicity x předchozích studiích xx xxxxx xxx xx paměti xxxxxxx xxxxxxx. Xxxx. xxxxxxxxxxx xxxxxxxxx x dermálních xxxxxx xxxxxx xxx xxxxx. Xxxxxxxx a xxxxxxxxxx mohlo xxx xxxxxxxxx xx jiných xxxxxxx xxx xxxxxx x citlivost xxxxxx xxxxxxxxxxxx xxxxx xx xxxx xx xxxxxx xxxx lišit. Také xxxxx xxxxxxxx látky, xxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxx, nemusela xxx xxxxxx pro xxxxxxxxx xxxxxxxxxx/xxxxxxxxx účinků xx kůži (xxxx. xxxxxx xxxxx xxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxx)
7a). Xxxxx v xxxxxxxx xxxxxxxxx, xxx xxxx xx králících xxxxxxxxx xxxxx xxxxxxxx x xxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx, lze xxxxxxxxx xxxxxx považovat xx xxxxxxxxxx důkazy, xx xxxxx xxxx xxxxxx xxxx dráždivá.
Výsledky xx xxxxxxx in xxxxx xxxx xx xxxx (xxxxx 5 x 6). Látky, xxxxx vykazovaly leptavé xxxx xxxxxxx xxxxxxxx xxxxxx xx xxxxxxxxxx x xxxxxx zkoušce xx vitro xxxx xx xxxx
7a), xxxxxx xxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx, xxxx xxxxx xxxxxxx na xxxxxxxxx xxxxxxxxx. Xxx xxxxxxxxxxxx, xx xxxxxx xxxxx xxxxxxxx xx xxxxxxx xx xxxx xxxxxxx závažné účinky.
Zkouška xx xxxx xx xxxxxxxxx (xxxxx 7 x 8). Xxxxx xx x provedení xxxxxxxx xx xxxx xxxxx xxxxxxxxxx založené xx průkaznosti výsledku, xxxx xx xxxx xxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxx xx xxxxxx pokusném zvířeti. Xxxxx xxxxxxxx xxxx xxxxxxx xxxxxxxxx, že xxxxx xx leptavé xxxxxx xx xxxx, xxxxxx xx xx xxxxx xxxxxxxx xxxxxxxx. Xxxxx xxxxx počáteční xxxxxxx není xxxxxxxxx xxxxxxx xxxxxx, xxxx xx se xxxxxxxx xxxx negativní xxxxxx xxxxxxxx xxxxxxxxx xx xxxx xxxxxxx xxxxxxxxx xxxxxxxxx xx xxxx xxxxxxxx 4 x. Xxxxx je xxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxx, lze xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx, xxxx xxxxxxxxxxx xxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxxx.
Xxxxxxx 8 xxxxxxxxxxx
Xxxxxxxxx zkoušení x xxxxxxxxx xxxxxxxxxx/xxxxxxxxx xxxxxx xx kůži
|
|
Aktivita
|
Nález
|
Závěr
|
|
|
Existující xxxxx x xxxxxxxx xxxxx xx kůži xxxx xxxxxxxx x člověka xxxx u xxxxxxxxx xxxxxx
|
Xxxxxx
|
Xxxxxxxxxx ukazatel; považována xx xxxxxxx. Xxxx xxxxx xxxxxxx.
|
| &xxxx;
|
Xxxxxxxx
|
Xxxxxxxxxx xxxxxxxx; xxxxxxxxxx za xxxxxxxxx. Xxxx xxxxx zkoušet.
|
|
|
Nežíravá/nedráždivá
|
Dominantní xxxxxxxx; považována xx xxxxxxxxx nebo nedráždivou. Xxxx xxxxx xxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxxx x&xxxx;xxxxxxxxx xxxxx xxxxxxxxx, xxxx xxxxxxxxx nejsou xxxxxxxxxxx.
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
|
|
Xxxxxxxx hodnocení leptavých/dráždivých xxxxxx xx xxxx xxxxx xxxxxxx XXX
|
Xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx
|
Xxxxxxxxxx xx xxxxxxx. Xxxx xxxxx zkoušet.
|
|
|
Předpoklad xxxxxxxxxx xxxxxx na xxxx
|
Xxxxxxxxxx xx xxxxxxxxx. Xxxx xxxxx zkoušet.
|
|
|
↓
|
|
|
|
|
Nelze stanovit xxxxx předpoklady, nebo xxxx předpoklady nepřesvědčivé xxxx negativní.
|
|
|
|
|
↓
|
|
|
|
|
Změřte xX (x ohledem xx xxxxxxxx xxxxxxxx, xxxxx xx xxxxxxxx).
|
xX ≤ 2 xxxx ≥ 11,5 (x vysokou xxxxxxxx xxxxxxxxx, pokud xx xxxxxxxx)
|
Xxxxxxxxxxxxx leptavé xxxxxx. Není xxxxx xxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
2 &xx; xX &xx; 11,5, xxxx xxx ≤ 2,0 xxxx ≥ 11,5 x&xxxx;xxxxxx xxxx xxxxxx xxxxxxxx kapacitou, xxxxx xx xx relevantní.
|
|
|
|
|
↓
|
|
|
|
|
Vyhodnoťte xxxxx x systémové xxxxxxxx xxxxxxxx xxxxxx1
|
Xxxxxx xxxxxxx
|
Xxxx xxxxx xxxxx xxxxx zkoušení.
|
|
|
Nežíravá nebo xxxxxxxxxx xxx zkouškách xx xxxxxxxxx xx xxxxxxx xxxxx 2 000 xx/xx xxxxxxx xxxxxxxxx xxxx xxxxx
|
Xxxxxxxxxxxxx nežíravý xxxx xxxxxxxxxx xxxxxxxxx xxxxx. Není třeba xxxxx další xxxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxxx xxxxxxxxx nejsou x&xxxx;xxxxxxxxx, xxxx xxxxxx přesvědčivé.
|
|
|
|
|
↓
|
|
|
|
|
Proveďte xxxxxxxxxxx x xxxxxxx xxxxxxx xxxxxxxxx xxxxxx xx kůži xx xxxxx nebo ex xxxx
|
Xxxxxxx účinky
|
Předpokládaná žíravost xx vivo. Xxxx xxxxx xxxxx xxxxx xxxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxx není xxxxxx.
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
|
|
Xxxxxxxx xxxxxxxxxxx a uznanou xxxxxxx xxxxxxxxxx účinků xx xxxx xx xxxxx xxxx ex xxxx.
|
Xxxxxxxx účinky
|
Předpokládaná xxxxxxxxxx xx vivo. Xxxx xxxxx žádné xxxxx xxxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxxx účinků xx xxxx xx xxxxx xxxx xx xxxx xxxxx xxxxxx x&xxxx;xxxxxxxxx xxxx xxxxx xxxx xxxxxxxx.
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
|
|
Xxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxx xx xxxx nebo jednom xxxxxxxx xxxxxxx.
|
Xxxxxxx poškození xxxx
|
Xxxxxxxxxx xx xxxxxxx. Xxxx xxxxx žádné xxxxx xxxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxx závažné xxxxxxxxx
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
|
|
Xxxxxxxx xxxxxxxxxxx xxxxxxx xx xxxxxx nebo xxxx xxxxxxxxx zvířatech
|
Žíravá xxxx xxxxxxxx
|
Xxxxxxxxxx za xxxxxxx xxxx xxxxxxxxx. Xxxx xxxxx xxxxx xxxxx xxxxxxxx.
|
| &xxxx;
|
Xxxxxxxx xxxx xxxxxxxxxx
|
Xxxxxxxxxx xx nežíravou xxxx xxxxxxxxxxx. Xxxx xxxxx xxxxx další xxxxxxxx.
|
| &xxxx;
|
&xxxx;
|
&xxxx;
|
&xxxx;
|
1 Lze zvážit xxxxx 2 x 3
X.5 AKUTNÍ XXXXXXXX: XXXXXXXX A XXXXXXX XXXXXX XX XXX
1 XXXXXX je v xxxxxxx x právem Xxxxxxxxxx společenství
7a).
1.1 XXXX
Xxx xxxxxxxx xxxx xxxxxxxxxxxxx xxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx, xxxxx xxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx informací x xxxxxxxx látce x xxxxx xxxxxxx xx xxxxxxxxxxx zkouškám xx xxxxxxxxx zvířatech x xxxx tak ohled xx xxxxx xxxxxxxxx x pokusnými zvířaty. Xxxxxxxx xxxx metody xx xxxxxxxxxx, xxx xxxx xxxxxxxxxx popsané xxxxxxx xxxxxxxx dráždivých/leptavých xxxxxx na xxx xx xxxx xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxx
7a) xxxxxxxxxxx xxxxxxxxxxxx xxxxx. Xxxxx jsou x xxxxxxxxx xxxxxxxxxxxx xxxxx, xxxxxxxxxx xx je xxxxxx pomocí xxxxxx xxxxxxxxxx xxxxxxxx
7a). Strategie xxxxxxxx xxxxxxxx provedení xxxxxxxxxxxx x schválených xxxxxxx in xxxxx x xx xxxxxxx x xxxxxxx 10 x xxxx xxxxxx xxxxxxxx. Xxxxx xx xxxx xxxxxxxxxx xxxxxx xxxxx in vivo xxxxxxxxxx xxxxxxx zkoušku xxxxxxxxxx/xxxxxxxxx xxxxxx xx xxxx xx xxxx, xx xxxxxx základě xx xxxxxxxx xxxxx xxxxxxx účinky xx xxx.
X xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxx xxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxx xx xx ke xxxxxxxx xx vivo xxxxxx xxxxxxxxxxx, xxxxx xxxxxx všechny xxxxxxxx xxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxx/xxxxxxxx xxxxxx xxxxx xx xxx xxxxxxxxxxx na základě xxxxxxx xxxxxxxxxxx xxxxxxxx. Xxxxxx xxxxx xxxxx xxxxxxxxx xxxxxx ze xxxxxxxxxxx xxxxxx xx xxxxxx xxxx xxxxxxxxx xxxxxxxxx, důkazy xxxxxxxxx/xxxxxxxxxx xxxxxx jedné xxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxx xxxxx xxxxxx látek, xxxxx xxxxxxxxxxx vysokou kyselost xxxx xxxxxxxxxx xxxxx
7a) x xxxxxxxx validovaných x xxxxxxxx xxxxxxx xxxxxxxxx a dráždivých xxxxxx xx kůži xx xxxxx xxxx xx xxxx
7a). Xxxx xxxxxx xxxxx xxx xxxxxxxxxxx xxxx analýzou xxxxxxxxxxx výsledků xxxx xx xxxxxxx zjištění xxxx analýzy.
U xxxxxxxxx xxxxx může xxxxxx xxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx/xxxxxxxxxx xxxxxx látky xx xxx xx xxxx. Xx všech xxxxxxxx xxxxxxxxx xx xxxx zvážením xxxxxxx xxxx zkoušky in xxxx xxxxxxx xxxxxxx xxxxxx xxxxxx xxxxx xx kůži xx xxxx x zhodnotí xx x xxxxxxx x xxxxxxx zkoušení X.4
7a). Xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxxx postupného xxxxxxxx xx xxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx/xxxxxxxxxx xxxxxx xx xxx xxxx xxxxx, x xxxxx tyto xxxxxx xxxx xxx xxxxxxxxxx xxxxxxxx x jiných xxxxxxxx. Xxxxx xxxxxx xxxxxxxxx xxxxxxxxxx zkoušení xxxxx x možnosti xxxxxxxxx xxxx xxxxxxxxxx xxxxxx xx xxx xxxxxxxxxx xxx po xxxxxxxxx xxxxxx leptavých x xxxxxxxxxx xxxxxx xx kůži xx xxxx, lze xxxxxxx xxxxxxx leptavých/dráždivých účinků xx xxx in xxxx.
Xxxxxxxxxxxxxxx xxxxxxxxx postupného xxxxxxxx, xxxxx xxxxxxxx xx provedení validovaných xxxxxxx xxxxxxxxx/xxxxxxxxxx účinků xx xxxxx xxxx xx xxxx, xx xxxxxxx x tabulce 10 x této xxxxxx zkoušení. Tato xxxxxxxxx byla xxxxxxxxxxx xx xxxxxxxx XXXX
7a), xxxx xxxxxxxxx jednohlasně xxxxxxxxxx x přijata xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx v xxxxxxxx xxxxxxxxxxxxxx xxxxxxx klasifikace xxxxxxxxxx xxxxx (XXX)
7a) Xxxxxxxxxx xx, xxx xx xxxxx xxxx xxxxxxxxx zkoušení postupovalo xxxx prováděním xxxxxxx xx xxxx. U xxxxxx látek xx xxxxxxxxxx xxxxxx xxxxxxxx xx xxxxxxx, díky xxx xxx xxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxx x xxxxxxxxx/xxxxxxxxxx xxxxxxxx xxxxx. X xxxxxxxxxxxx xxxxx, o jejichž xxxxxxxxx/xxxxxxxxxx xxxxxxxx na xxxx x xxx xxxx x xxxxxxxxx xxxxxxxx xxxxx, xx xx xxxx tato xxxxxxxxx využít pro xxxxxxxx xxxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxx strategie xxxx xxxxxxx xxxxxxxx xxxx rozhodnutí nepoužít xxxxxx xx xxxxxxx xxxx xxx xxxxxxxxxx.
1.2 XXXXXXXX
Xxxxxxxx účinky na xxx: vyvolání xxxx x oku xx xxxxxxxx xxxxxxxx xxxxx xx xxxxxx xxxxxx xxx. Tyto xxxxx xxxx xxxx vratné xx 21 dnů xx xxxxxxxx.
Xxxxxxx účinky xx xxx: vyvolání xxxxxxxxx xxxx tkáně xxxx závažné xxxxxxx xxxxxxxx xxxxxx xx xxxxxxxx zkoušené látky xx xxxxxx xxxxxx xxx. Toto xxxxxxxxx xxxx xxxx vratné xx 21 dnů xx xxxxxxxx.
1.3 XXXXXXXX XXXXXXXX XXXXXX
Xxxxx, která xx xxx xxxxxxxx, xx xxxxxx x xxxxx xxxxx xx xxxxx xxx xxxxxxxxx xxxxxxx, xxxxxxx xxxxxxxxxxxx xxx slouží xxxx xxxxxxxx. X xxxxxxxx xxxxxxxxxxx se xx xxxxxxx xxxxxx xxxx xxxxxxxx, xxxxxxx x xxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxx/xxxxxxxxx účinků xx xxx. Xxxxxx xx xxxx xxxx xxxxxx xx xxx x xxxxxxxxx xxxxxxxxx xxxxxx, xxx xxxx xxxxx xxxxxxx úplné posouzení xxxxxx. Doba xxxxxx xx xxxx xxx xxxxxxxxxx xxxxxx, xxx xxxx xxxxx xxxxxxxxx xxxxxxxx nebo nevratnost xxxxxx.
Xxxxxxx xxxxxxx, která x jakékoli xxxx xxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx utrpení xxxx xxxxxxx, xx xxxxxxx utratí x xxxxx xx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxxx xxxxxxxxxxx o utracení xxxxxxxxxxx a xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxx xxxxxx v xxxxxxxxxx
7a)1.4 XXXXX XXXXXXXX XXXXXX
1.4.1 Xxxxxxxx xx xxxxxxx in vivo
1.4.1.1 Xxxxx xxxxxxxxxxx druhů
Upřednostňovaným xxxxxxxx xxxxxxxx xx xxxxx králíka a xxxxxxxxx xx zdravá xxxxx xxxxxxx pokusná xxxxxxx. Xxx xxxxxxx xxxxxx xxxxx xxxx xxxxx xx se xxxx podat zdůvodnění.
1.4.1.2 Xxxxxxxx pokusných xxxxxx
Xxxxxxx xxxxxxx xxxx vybrána x ohledem na xxxx, xxxxxxx a xxxxx v xxxxxxx x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx předpisu
10). x xxxxxxxx xxx, xxx byla možná xxxxxxxxxxxx jednotlivých pokusných xxxxxx. Dobu xxxxxxxx xxxxxxx
§10 zvláštního xxxxxxxx xxxxxxxx
10). 24 x xxxx xxxxxxxx xx u xxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxx xxx. Xxxxxxx xxxxxxx, x xxxxxxx xx xxxxxx xxxxxxxxxx xxx, oční xxxxxx nebo xxxxxxxxx xxxxxxx, xx xxxxxxxxx.
1.4.1 3 Xxxxxxxx xxxxx x xxxxxx
Xxxxxxx xxxxxxx xx xxxx xxx xxxxxxx xxxxxxxxxx. Teplota x místnosti xxx xxxxxxx zvířata xx xxxx u xxxxxxx xxxxx (20 ± 3) °C. Xxxxxxx xx xxxxxxxxx vlhkost xxxx xxxxx xxxxxxxxx 30 % x xxxxx xxxxx xxxxxxxxxxxx 70
x xxxxx xxxxxx xxxxxxxxx, xxxxx xx xxxx xxx xxxxxxx 50 - 60 %. Osvětlení xx xxxx být xxxxx, xxxx by xx xxxxxxx 12 x xxxxxx x 12 x tmy, xxxx-xx v chovné xxxxxxxxx xxxxx xxxxxx. Xx krmení xxx xxxxxx xxxxxxx xxxxxx xxxxxx pro pokusná xxxxxxx xx registrovaného xxxxxxx x xxxxxxxxxx xxxxxxxx xxxxx vody. Xxxxxxx xxxxxxx mohou xxx xxxxxxx x xxxxxxx ve xxxxxxxxx x xxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxx
10), xxxxx xxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxx, xxx počet xxxxxxxxx xxxxxx x xxxxx xxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx.
1.4.2 Xxxxxx xxxxxxx
1.4.2.1 Xxxxxxxx xxxxxxxx xxxxx
Xxxxxxxx xxxxx xx aplikuje xxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxxxxx vaku xxxxxxx xxx tak, xx xx spodní xxxxx xxxxx xxxxxxxxx xx xxxx xxxxx. Xxxxx se pak xxx xx xxxxx xxxxxxx xxxxx přidrží x xxxx, aby xxxxxxx xx xxxxxx xxxxx. Xxxxx xxx, xx xxxxxxx se xxxxx neaplikuje, xxxxxx xxxx xxxxxxxx.
1.4.2.2 Xxxxxxx
Xxx xxxxxxxxx xxxxxx xx xx 24 x xx xxxxxxxxx zkoušené xxxxx nevyplachují, s xxxxxxxx xxxxxxx xxxxx (xxx xxxx 1.4.2.3.2) x v xxxxxxx xxxxxxxxxx leptavých xxxx xxxxxxxxxx xxxxxx. Xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxx xxxxx xxxxxxxx očí xx xxxxxxxxxxxx, pokud xx xxxx vědecky xxxxxxxxxx. Xx-xx xxxxxxxxx xxxxxxx xxxxxxxx, xxxxxxx xx dva xxxxxxx. Xxxxxxxx výplachu xx xxxxxxxx xxxxxxxxxxxx, xxxx. xxxx xxxxxxxx, xxxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxx, trvání, objem x rychlost xxxxxxxx.
1.4.2.3 Xxxxxx xxxxx
1.4.2.3.1 Xxxxxxxx xxxxxxx
Xxx xxxxxxxx kapalin xx použije xxxxx 0,1 ml. K xxxxxxxxx látky xxxxx xx xxx xx xx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx s xxxxxxxxx. Xxxx instilací 0,1 xx xx xxx xx xx xxxx xxxxxxxx z xxxxxxxxxxxxx xxxxxxx a xxxxxxxxxx xx xxxxxxx.
1.4.2.3.2 Xxxxxxxx pevných xxxxx
Xxx xxxxxxxx xxxxxxx xxxxx, xxxx a xxxxxxxx xxxxx xx xxxxxxx xxxxx 0,1 ml xxxx xxxxxxxx xxxxxxx 100 xx. Xxxxxxxx xxxxx se xxxxxxxx xx xxxxx prášek. Xxxxx xxxxxxx xxxxxxxxx xx xxxxxxx xx xx xxxxxxxx xxxxxxxx, xxxx. xxxxxxxxxxx xxxxxxxx xxxxxxxx. Xxxxx se xxxxx xxxxxxxx xxxxx x xxx pokusného xxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xx xxxx prvního xxxxxxxxxx xx 1 h xx xxxxxxxx, xxx xxx vypláchnout fyziologickým xxxxxxxx nebo xxxxxxxxxxxx xxxxx.
1.4.2.3.3 Zkoušení aerosolů
Před xxxxxxxxx xxxxx xx xxx se doporučuje xxxxxxxx látky xxxxxxxx x xxxxxxxxxxxxxxx xxxx xxxxxxxxxx xx xxxxxxx. Xxxxxxx výjimkou xxxx xxxxx xxxxxxxx v xxxxxxxxxx xxxxxxx pod xxxxxx, xxxxx x xxxxxx odpařování xxxxxxxx xxxxx. X takových xxxxxxxxx xx oko xxxxxx otevřené a xxxxx se do xxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx jednu sekundu xx xxxxxxxxxxx 10 xx xxxxx xxxx xxxx. Vzdálenost se xxxx podle xxxxx x rozprašovači a xxxx xxxxxx xxxxx. Xx xxxxx dbát xx xx, xxx xxxxxxx x xxxxxxxxx xxx xxxxxx x xxxxxxxxxxxx. X xxxxxxxxxxx xxxxxxxxx může být xxxxx xxxxxxxxxx xxxxxxxxx "xxxxxxxxxxxx" poškození xxx x důsledku xxxxxxxxxxxxxx xxxxx.
Xxxxx xxxxxxxx lze xxxxxxxxx na xxxxxxx xxxx simulované xxxxxxx: xxxxx se nastříká xx odvažovací xxxxx xxxx otvor o xxxxxxxxx králičího xxx, xxxxxxx xxxxx otvor xx xxxxxxx bezprostředně xxxx xxxxxxx. Xx xxxxxxx xxxxxxx xxxxxxxxx xxxxxx xx odhadne xxxxxxxx xxxxx, která xx vstřikne do xxx. X xxxxxxxx xxxxx lze xxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxxx nádobky xxxx xxxxxxxxxxx zkoušené xxxxx x xx jejím xxxxxxxxxx.
1.4.2.4 Xxxxxxxxx zkouška (xxxxxxx xxxxxxxxxx-xxxxxxxxx xxxxxx xx oči xx xxxx na xxxxxx xxxxxxxx zvířeti)
Jak je xxxxxxx ve strategii xxxxxxxxxx xxxxxxxx (xxx xxxxxxx 10), xxxxxxx xx xxxxxxxxxx, xxx xxxx xxxxxxx xx xxxx xxxxxxxxx nejprve xx xxxxxx pokusném xxxxxxx.
Xxxxx xxxxxxxx této xxxxxxx xxxxxxxxx, že xxxxx xx xxxxxxx xxxx vysoce xxxxxxxx xxxxxx xx oči xxx xxxxxxx xxxxxxxxx xxxxxxx, xxxxx zkoušení xxxxxxxxxx účinků xx xxx xx xxxxxxxxx.
1.4.2.5 Xxxxxxx anestetika
V jednotlivých xxxxxxxxx xxx použít xxxxxxx xxxxxxxxxx. Xxxxx xxxxxxx průkaznosti xxxxxxxx xxxxxxxxx, xx xxxxx xxxx xxxxxxxx bolest, xxxx pokud xxxxxxxxx xxxxxxx xxxxxxx, xx xx xxxxxx xxxxxxxxx xxxxxx, lze xxxx xxxxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxxx xxxxxxxxxx. Xxx, koncentraci x xxxxx lokálního xxxxxxxxxx xx xxxxx pečlivě xxxxxx, xxx xxxx xxxxxxxxx, xx x xxxxxxxx xxxx použití xxxxxxx k xxxxxxxx xxxxxxx na xxxxxxxxx xxxxx. Xxxxxxx xx xxxx xxxxxxxxxxx i xxxxxxxxx oko.
1.4.2.6 Xxxxxxxxxxx xxxxxxx (xxxxxxx xxxxxxxxxx xxxxxx xx xxx xx vivo xx xxxxxxx pokusných xxxxxxxxx)
Xxxxx xxxxx xxxxxxxxx xxxxxxx xxxx pozorován xxxxxxx xxxxxx, xxxx by xx dráždivá xxxx xxxxxxxxx xxxxxx xxxxxxxx xx maximálně xxxxxxx xxxx xxxxxxxxx xxxxxxxxx. Xxxxx je během xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxx, xxxxx xxxxxxxxx xxxxx xxxxx (nevratný) xxxxxx x xxxxxxxxxxx xxxxxxx, xxxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xx xxxxxx xxxxxxxx xxxxxxx xxxxx xxx xxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxx xxxxxxxx. Pokud xx x druhého xxxxxxxxx zvířete xxxxxxx xxxxxxx nebo xxxxxx xxxxxxxx účinky, ve xxxxxxx se xxxxxxxxxxx. X xxxxxxxxx xxxxxxx xxxx mírných xxxxxxxxxx xxxxxx xxxx xxx xxxxx xxxxxx další xxxxxxx zvířata.
1.4.2.7 Xxxx xxxxxxxxxx
Xxxx xxxxxxxxxx xx xxxx být xxxxxxxxxx xxxxxx, xxx xxxx xxxxx plně zhodnotit xxxx a vratnost xxxxxxxxxxxx xxxxxx. Xxxxxxx xx xxxx měla xxx ukončena xxxxxxxx x xxxxxxxx, xxx xxxxxxx xxxxx xxxxxxxx xxxxxxxxxxxxx příznaky xxxxxx xxxxxxx xxxx xxxxxxx
7a). Xx xxxxxx xxxxxx xxxxxxxxx xxxxxx xx xx xxxxxxx xxxxxxx xxxx obvykle xxxxxxxxx 21 dnů xx xxxxxx zkoušené xxxxx. Xxxxx xx xxxxxxxx xxxxxxxxxx před xxxxxxxxx 21 xxx, xxxxxxx xx xx xxxx x xxxxx okamžiku xxxxxxx.
1.4.2.7.1 Klinická xxxxxxxxxx x hodnocení očních xxxxxx
Xxx se vyšetří xx 1, 24, 48 x 72 x xx xxxxxx xxxxxxxx xxxxx. Jakmile xx získají xxxxxxx xxxxxxxxx, nemělo by xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxx déle, xxx xx xxxxxxxx. Xxxxxxx xxxxxxx xx xxxxxxxx xxxxxxxxxxxxxxx prudkých xxxxxxx nebo xxxxxxx xx neprodleně xxxxxxx xxxxxx x xxxxx xx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Humánně se xxxxxx ta xxxxxxx xxxxxxx, u xxxxx xxxxx xx instilaci x xxxxx xxxxx xxxxx: xxxxxxxxx xxxxxxx xxxx xxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx; xxxx x xxxxxx xxxxxx oční; zákal xxxxxxx xxxxxx 4 xxxxxxxxxxxxx 48 x; xxxxxxx xxxxxx xx xxxxx (reakce xxxxxxx xxxxxx 2) přetrvávající 72 h; xxxxxxxxxxxx xxxxxxxxxx membrány; xxxxxxx xxxxxxxx xxxx slzné xxxxx; nebo xxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxx xxxxxx xx xxx xxxxxxxxxxx xxxxxxxx lézí.
Pokusná xxxxxxx, u xxxxx xxxx léze xxxxxxxxxx, xxxxx xxxxxxx dříve xxx 3 xxx xx xxxxxxxxx. Xxxxxxx xxxxxxx s xxxxxxx xx xxxxxxxxx xxxxxx xx pozorují, xxxxx xxxx xxxxxxxx, xxxx xx 21 xxx, xx xxxxxxx uplynutí xx xxxxxx xxxxxx. Xx 7, 14 x 21 xxxxx xx xxxxxxx xxxxxxxxxx, xxx xx xxxxx xxxx xxxx x xxxxxx xxxxxxxx xxxx xxxxxxxxxx.
Xxxxxx reakce oka (xxxxxxxx, rohovky a xxxxxxx) je xxxxx xxxxxxxxxx xxx xxxxxx xxxxxxxxx (xxxxxxx 11). Xxxxxx xx také xxxxxxxx jiné oční xxxx (xxxx. xxxxx, xxxxxxxx) xxxx xxxxxxxxx xxxxxxxxx xxxxxx.
Xxxxxxxxxxx xxxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxxxx lupy, xxxxx xxxxxxxxxx xxxxx, xxxxxx xxxxxxxxxx nebo xxxxxx xxxxxxxx xxxxxxxx. Xx xxxxxxxxxxx xxxxxxxxxx po 24 x xxxxx xxx xxx xxxxxxxxx xxxxxx dále xxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxxx xxxxxx xxxxxx xx nevyhnutelně subjektivní. X cílem xxxxxxxxxx xxxxxxxxxxx hodnocení očních xxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxxxx a xxx, kdo provádějí x interpretují xxxxxxxxxx, xxxx xxx zaměstnanci xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxx xxxxx x používaným xxxxxxxx xxxxxxxxxxxxx.
2 DATA
2.1 XXXXXXXXX XXXXXXXX
Xxxxxx xxxxxxxxxx xxxxxx xx oči xx xxxxxxxx xx xxxxxxx x xxxxxxx x xxxxxxx závažnosti xxxx a xxxxxx xxxxxxxxx xxxx nevratností. Xxxxxxxxxx stupně xxxxxxxxxxxxx xxxxxxxxx měřítko xxxxxxxxxx xxxxxxxxxx xxxxx, xxxxx xx hodnotí xxxx xxxx účinky zkoušené xxxxx. Xxxxxxxxxx xxxxxx xx spíše xxxx xxx xxxxxxxxxx za xxxxxxxxxx hodnoty, které xxxx xxxxxxxxxx, pouze xxxxx xx xxxxxxx x xxxxx xxxxx x hodnocení xxxxxxxxx xxxxxxxxxx.
3 XXXXXXX POKUSU, XXXXXXXX XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9),10) musí xxx xxxxxxxxx xxxxxxx pokusu x x xxxxxxx xxxxxx xx xxxxx xxxx xxxxxxxx.
3.1 Xxxxxx x průběhu pokusu xxxxxxxx následující xxxxxxxxx,
xxxxxxxxxx xxxxxxxx in xxxx: xxxxxxx xxxxxxxxxxx výsledků xxxxxxxxxxx xxxxxx, xxxxxx xxxxxxxx strategie postupného xxxxxxxx:
- xxxxx xxxxxxxxxxxx xxxxx x xxxxxxxxxxx xxxxxxx,
- xxxxx získané x xxxxxx kroku xxxxxxxxx xxxxxxxx,
- xxxxx xxxxxxxxxxx zkoušek xx xxxxx, včetně xxxxxxxxxx xxxxx o xxxxxxxxx x x xxxxxxxxxx xxxxxxxxx xx xxxxxxxxxx/xxxxxxxxxxxx xxxxxxx,
- xxxxx xxxxxxxxx xxxxxx xxxxxxxxxx/xxxxxxxxx xxxxxx xx xxxx xx xxxx, xxxxxx získaných xxxxxxxx,
- xxxxxxx xxxxxxxxxxx xxxxxxxx odůvodňující xxxxxxxxx xxxxxx xx xxxx.
Xxxxxxxx xxxxx:
- xxxxxxxxxxxxx údaje (xxxx. xxxxx XXX, xxxxx, xxxxxxx, známé xxxxxxxxx, xxxxx),
- xxxxxxxxx xxxxxx a xxxxxxxxx-xxxxxxxx xxxxxxxxxx (xxxx. xxxxxxx xX, xxxxxxxx, xxxxxxxxxxx, xxxxxxxxx, xxxxxxxxxx s xxxxx),
- v xxxxxxx xxxxx její složení x relativní xxxxx xxxxxx xxxxxxxxx x xxxxxxxxxx,
- xx-xx xxxxxxx xxxxxxx xxxxxxxxxxx, xxxx xxxxxxxxxxxx, čistota, typ, xxxxx x xxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxx.
Xxxxxxxxx:
- xxxxxxxxxxxx, koncentrace (xxxxx potřeby), použitý xxxxx,
- xxxxxxxxxx xxxxxx xxxxxxxx.
Xxxxxxx zvířata:
- xxxxxxx xxxx/xxxx, zdůvodnění xxxxxxx xxxxxx xxxxxxxxx zvířat, xxxx-xx použit albín xxxxxxx,
- xxxxx každého xxxxxxxxx xxxxxxx xx xxxxxxx studie,
- xxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxx xx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx (xx-xx to xxxxx),
- xxxxxxxxx xxxxxxxxxxxx pokusných xxxxxx na xxxxxxx x xx xxxxx xxxxxxx,
- xxxxx, xxxxxxxx xxxxx, krmivo atd.
Výsledky:
- xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxx xxx xxxxxx xxxxxxxxxx (xxxx. xxxxx xxxxxxxxxx xxxxx, xxxxxxxxxxxx, xxxxxxxxxxx),
- xxxxx xx xxxxx xxxxxxx x xxxxxxxx xx dráždivé xxxx leptavé xxxxxx x jednotlivých xxxxxxxxx xxxxxx při xxxxxx xxxxxxxxxx až xx xxxxxxx xxxxxxx xxxxxxxxx xxxxxxx xx zkoušky,
- xxxxxxxx popis xxxxxx x xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxx,
- xxxxx všech xxxxxxx xxxxxxxxxxxx očních xxxx (xxxx. xxxxxxxxxxxxx, xxxxxx xxxx, xxxxx xxxxxxxxxx xxxxx, xxxxxxxx),
- xxxxx xxxxxxxx x xxxxxxxxxxx nepříznivých xxxxxx xxxx oči x xxxxxxxx histopatologické xxxxxx.
Xxxxxxx x interpretace výsledků.
Extrapolace xxxxxxxx xxxxxx xxxxxxxxxx xxxxxx xx xxx xxxxxxxxx xxxxxx na xxxxxxx xx xxxxxx xxx x omezené xxxx. Xxxxxxxxxxx xxxxxx xx xx většině xxxxxxx xx dráždivé x žíravé xxxxx xxx xxx xxxxxxxxxx xxx xxxxxx.
Xx xxxxx xxxx xx to, xxx byla xxx xxxxxxxxxxxx údajů xxxxxxxxx xxxxxxxxxx xxxxxxxxx ze xxxxxxxxxx infekce.
Závěry.
TABULKA 11: XXXXXXXX XXXXXX XXXX
Xxxxxxx
Xxxxx: xxxxxx hustoty (xxxxxxx xx xxxxxxx xxxxxxxx xxxxxxx)*
Xxxxx zvředovatění xxx xxxxx 0
Rozptýlené nebo xxxxxxx xxxxxxx zákalu (xxxx xxx xxxxx xxxxxxxx xxxxxxxxxx xxxxx), xxxxxxx xxxxxxx jasně xxxxxxxxx 1
Snadno xxxxxxxxxxxxxxxxx xxxxxxxxx oblast, xxxxxxx xxxxxxx xxxxx xxxxxxxx 2
Xxxxxxxxxx zóny xxxxxxxxxxx, xxxxxxx duhovky xxxxxx xxxxxxxxx, xxxxxxxx xxxxxxx xxxxx xxxxxxxxxxxx 3
Úplná xxxxxxxxxxxxx xxxxxxx, xxxxxxx xx xxxxx xxxxxxxxxxx 4
Xxxxxxxxx možné: 4
* Xxxxxxxxx se xxxxxx xxxxxx xxxxxxx.
Xxxxxxx
Xxxxxxxx 0
Xxxxxxx xxxxxxxxxxx řasy, xxxxxxxx, xxxxx, xxxxxxx xxxxxxxxx xxxxx xxxxxxx, xxxx xxxxxxxxx xxx zánětu;
rohovka xxxxxxx na světlo (xxxxxxxx xxxxxx xx xxxxxxxxxx xx účinek) 1
Xxxxxxxx, xxxxxxxxxxxxx xxxxxxxxx xxxx bez xxxxxx xx xxxxxx 2
Xxxxxxxxx xxxxx: 2
Xxxxxxxx
Xxxxxxxxxx (xxxxx xxxxxxxxxxxxx změny xxxxxxxxxx xx xxxxxxx nebo xxxxxxxx xxxxxxxx, kromě xxxxxxx x xxxxxxx)
Xxxxxxxx 0
Xxxxxxx xxxxxx xxxx xxxxxxxxxxx (překrvené) 1
Xxxxxxx, xxxx xxxxx, xxxxxxxxxx xxxx nesnadno rozeznatelné 2
Xxxxxxx temně xxxx xxxxx 3
Xxxxxxxxx xxxxx: 3
Xxxxx (xxxxxxxx)
(xxxx se xxxxx xxxx xxxxxxx xxxx)
Xxxxxxxx 0
Xxxxx xxxxxxxxxx xxxx 1
Patrný otok, x xxxxxxxxx xxxxxxxxx xxxxx 2
Otok způsobující xxxxxxxx xxxxx xxxxxx xx polovinu 3
Xxxx xxxxxxxxxxx uzavření xxxxx xxxx xxx na xxxxxxxx 4
Xxxxxxxxx xxxxx: 4
Xxxxxxx 10
Xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx a xxxxxxxxx xxxxxx na xxx
XXXXXX XXXXX
X zájmu xxxxxxxxxxxx vědeckého přístupu x xxxxxxx xxxxxxxxx x pokusnými xxxxxxx xx důležité xxxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxxx zkoušky, xxxxx x xxxxxxxxx xxxxxx xxxxxxxxxxxxx vyvolají xxxxxxx xxxxxx. Veškeré xxxxxxxxx xxxxxxxx se xxxxxxxxxxxxx xxxxxxxxx/xxxxxxxxxx xxxxxx xxxxx na oči xx xx měly xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxx xx xxxx. Xxxx xxx existovat xxxxxxxx xxxxxx pro xxxxxxxxxxx zkoušené xxxxx xxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxx xx oči, xxxx xx bylo xxxxx xxxxxxxx zkoušky xx xxxxxxxxx xxxxxxxxx. Xxxxx využití xxxxxxx xxxxxxxxxxx výsledků x xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxx xx xxxx, xxxxxxx xxxxx xxxxx xxxxxxxxxxxxx xxxxxx xxxxxxx xxxxxx.
Xxxxxxxxxx se, aby xx xxxxxxxxx informace xxxxxxxx xx xxxxxxxxxx x xxxxxxxxx xxxxxx xxxxx xx oči xxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxx výsledků, xx xxxxxx xxxxxxx se xxxxxxxx x tom, xxx xx xx x xxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxx xxxxxxx xxxxx studie xxxx xxx xxxx xxxxxx in xxxx. Xxxx-xx nutné xxxxx xxxxxx, doporučuje xx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx a xxxxx xxxxxxxxxxxxxxx xxxxxx relevantní xxxxxxxxxxxxxx xxxxx. X xxxxx, xxxxx xxxxxxx xxxxxx zkoušeny, xx xx měla strategie xxxxxxxxxx xxxxxxxx využít x xxxxxxx xxxxx, xxxxx xxxx xxxxxxxx x vyhodnocení jejich xxxxxxxxx xxxx dráždivých xxxxxx xx oči. Xxxxxxxxx xxxxxxxx xxxxxxx x xxxx xxxxxxx 10 byla vypracována xx xxxxxxxx OECD
7a). Xxxxxxxx byla xxxx xxxxxxxxx xxxxxxxxx a xxxxxxxxxxxx x Harmonizovaném xxxxxxxxxxxx xxxxxxx klasifikace xxxxxxxxx chemických xxxxx xxx xxxxxx xxxxxx x jejich vlivu xx životní xxxxxxxxx, xxxxx schválilo 28. xxxxxxxx xxxxxxxx Výboru xxx chemické látky x Xxxxxxxx skupiny xxx xxxxxxxx xxxxx x xxxxxxxxx 1998
7a).
Xxxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx není nedílnou xxxxxxxx xxxxxxxx xxxxxx X.5, vyjadřuje xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx/xxxxxxxxx xxxxxx xx oči. Xxxxx postup představuje xxxxxxxx xxxxxxxxx i xxxxxx standard xxx xxxxxxxx xxxxxxxxxx/xxxxxxxxx účinků xx xxx xx xxxx. Xxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxx xxxxxxxxx xxxxxxx xx xxxx x xxxxxxx xxxxxxx, xxxxxx je xxxxx xxxx xxxxxxxxxx xxxxxx xxxxxxx xxxxxxx xxxxxxxxx. Strategie xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxx x xxxxxxxxxx a xxxxxxxxx xxxxxxxx xxxxx xx oči a xxxxxxxxxxxx přístup x xxxxxxxxx xxxxxxxxxxxx xxxxx x xxxxxxx, x xxxxxxx je xxxxx xxxxxxx další studie, xxxx x xxxxx xxxxx xxxxxx xxxxxx xxxxxxx xxxxxxxxx. Xxxxxxxx xxxx xxxxxxxxx je xxxxxxxxx xxxxxxx validovaných x xxxxxxxx zkoušek xx xxxxx xxxx xx xxxx a xxxx za xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxx/xxxxxxxxx xxxxxx na xxxx xxxxxxx xxxxxxxx X.4
7a).
XXXXX XXXXXXXXX XXXXXXXX XX XXXXXXX
Xxxx xxxxxxxxx xxxxxxx x xxxxx xxxxxxxxx postupného zkoušení (xxxxxxx 10 xxxxxxxxxxx) xx xxxxxxxxx veškeré xxxxxxxx informace, aby xx xxxxx xxxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxxx in xxxx. Xxxxxxx xxx významné xxxxxxxxx xxxxxx x xxxxxxxxxxx xxxxxxxxxxxx parametrů (xxxx. xxxxxxxx hodnota xX), xxxxxxxxx informace xx xx xxxx xxxxxxxx xxxx xxxxx. Xxxxxxx xxxxxxxxxx xxxxx x účincích xxxxxxxx xxxxx a xxxxxx xxxxxxxxxxxx obdob xx xxxxxxxxx xx xxxxxxx xxxxxxxxxx xxxxxxxxx na xxxxxxxxxxx výsledků. Xxxx xx xx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxxx. Xxxxxx xxxxx xx xx xxx xxxxx xx xxx xxxxxxxxxx xxxxx x xxxxxxxx xxxxx na xxxxxxx x xxxxxxx x xxxx xx xxxxxxxx xxxxxxxx xx xxxxx xxxx ex xxxx. Xxxxxx xxxxxxxx látek xx vivo xx xx měly xxxxxxxx xx xxxxxxx. Mezi xxxxxxx uvedené xx xxxxxxxxx xxxxxxxx patří:
Hodnocení xxxxxxxxxxxx xxxxx x xxxxxxxx látky xx xxxxxxx a xxxxxxx (xxxx 1). Xxxxxxx xx nutné xxxx x xxxxx xxxxxxxxxx xxxxx x xxxxxxxx xx xxxxxxx, xxxx. xxxxxxxx studie nebo xxxxxx xxxxxx x xxxxxxxx, záznamy xxxxxxxx xxxxxxxxx xxxx xxxxx x zkouškách xx xxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxx xxxxxx, xxxxxxx x xxxxxx xxx xxx xxxxxx xxxxxxxxx přímo xx xxxxxxxxxx x xxxxxxx xx xxx. Xxxx xx xxxxxxxx xxxxxxxx xxxxx xx studií xx xxxxxx nebo xx xxxxxxxxx zvířatech xxxxxxxxxxxx xx xxxxxxxxx/xxxxxxxxxx xxxxxx xx xxxx. Xxxxx, xxxxxxx xxxxxxx xxxx vysoce xxxxxxxx xxxxxx xx xxx xxxx známy, xx xx xxx pokusných xxxxxx xxxxxxxxxx. Xx xxxxx xxxxxx pro xxxxx vykazující xxxxxxx xxxx dráždivé xxxxxx xx xxxx; takové xxxxx xx xxxxxxxx xx látky x xxxxxxxxx nebo xxxxxxxxxx xxxxxx xxxxxx xx xxx. Látky, x xxxxx xxxx x xxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx důkazy, xx xxxx nežíravé x xxxxxxxxxx, xx x xxxxxx studiích xx xxxx xxxx xxxxxxxxxx.
Xxxxxxx xxxxxx xxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx (XXX) (xxxx 2). Vezmou xx x xxxxx výsledky xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx látek, xxxx-xx x dispozici. Pokud xxxx k xxxxxxxxx xxxxxxxxxx údaje x xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx nebo xxxxxx xxxxx xx xxxxxxx xxxx xxxxxxx xxxxxxxxxxx, xx mají xxxxxxxxx xxxxxxxxx/xxxxxxxxxx účinků xx xxx, xxx xxxxxxxxxxxx, xx xxxxxxxx xxxxx xxxxxx xxxxxx xxxxxx. X takových xxxxxxxxx xxxx xxxxx xxxx xxxxx zkoušet. Xxxxxxxxx xxxxx xxxxxxx ze xxxxxx xxxxxxxxxx příbuzných xxxxx xxxx xxxxxx xxxxx xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxx zkoušení xxxxxxxxxx důkaz xxxxxxxxxxx/xxxxxxxxxxxxx xxxxx. Xx xxxxxxxxx xxxxxxxxxx xxxxxxxxx/xxxxxxxxxx xxxxxx xx kůži x xxx xx xxxx xxx xxxxxxx xxxxxxxxxx x uznané xxxxxxx xxxxxxxxxxx z xxxxxxx XXX.
Xxxxxxxxx-xxxxxxxx vlastnosti x xxxxxxxx xxxxxxxxxx (xxxx 3). Látky xxxxxxxxxx xxxxxxxx hodnoty xX xxxx ≤ 2,0 xxxx ≥ 11,5 xxxxx mít silné xxxxxx xxxxxx. Xxxxx xx xxxxxxx xxxx xxxxxxxx xxxxxx látky xx oči xxxxxxx xx xxxxxxx xxxxxxxxxx xxxxxx xX, xxx xxxx xxxx v xxxxx xxxxxxx/xxxxxxxxxx xxxxxxx (xxxxxxxx xxxxxxxx)
7a). Pokud xxx xxxxx xxxxxxxx xxxxxxxx xxxxxx, xx xxxxx xxxxx xxxx xxxxxxx xxxxxx xx xxx, xxxx tento xxxxxxxxxx xxxxxxxx další xxxxxxx, xxxxx xxxxx x xxxxxxxx validované x xxxxxx xxxxxxx xx vitro xxxx xx vivo (viz xxxxx 5 x 6).
Xxxxxxx xxxxxxx existujících xx xxxxxxx (xxxx 4). X této xxxx xx xxxxxxxxx xxxxxxx dostupné xxxxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxx cestou. Vezme xx v úvahu xxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx látky. Xxxxx se x xxxxxxxx xxxxx xxxxxxx, xx xx xxx xxxxxx dermální cestou xxxxxx xxxxxxx, nemusí xxx nutné xxxxxxx xx xx xxx. Xxxxxxx mezi akutní xxxxxxxx xxxxxxxxx x xxxxxxxxxx/xxxxxxxxx xxxxxx na xxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx, xxx xx xxxxxxxx, xx xxxxx xx xxxxx xxx xxxxxx dermální xxxxxx xxxxxx xxxxxxx, xxxx xxxxxxx toxicitu xxxxxxxxx také xxx xxxxxxxxx podání xx xxx. Xxxxxx xxxxx xxx také vzít x xxxxx xxxx xxxxx 2 x 3.
Xxxxxxxx xx xxxxxxx xx xxxxx nebo xx xxxx (xxxxx 5 x 6). Xxxxx, které xxxxxxxxxx xxxxxxx nebo xxxxxxx xxxxxxxx vlastnosti ve xxxxxxx in vitro xxxx xx xxxx
7a), xxxxx xxxx xxxxxxxxxx x uznána xxx xxxxxxxxx výlučně leptavých/dráždivých xxxxxx xx xxx xxxx na kůži, xxxx xxxxx zkoušet xx pokusných xxxxxxxxx. Xxx předpokládat, xx xxxxxx xxxxx xxxxxxxx xx zkoušce in xxxx xxxxxxx xxxxxxx xxxxxx. Xxxxxx-xx validované x xxxxxx xxxxxxx xx vitro xxxx xx xxxx x xxxxxxxxx, xxxxx 5 x 6 se xxxxxxxx a přejde xx přímo ke xxxxx 7.
Posouzení xxxxxxxxxx xxxx xxxxxxxxx účinků xx kůži xx xxxx (krok 7). Xxxxx xxxxxxxxx xxxxxx x provedení xxxxxxxxxxx xxxxxxx průkaznosti výsledků xxxxxxxxxxxxx dráždivých/leptavých účinků xxxxx xx xxx xxxxxxxxx se x xxxxx z xxxx xxxxxxxxx xxxxxx xxxxxxxxxxx, xxxxxxx xx s xxxxxxxx xxxxxx B.4
7a) x xxxxxxxx xxxxxxx
7a) xxxxxxxxx xxxxxxxxx dráždivých/leptavých xxxxxx xx kůži xx xxxx. Xxxxxxxx xx x xxxxx xxxxxxx xxxxxxx xxxx xxxxx xxxxxxxx xxxxxx xx xxxx, xxxxxxxx xx za xxxxx x xxxxxxxxx x xxxxxxxxxx účinky xx xxx, pokud xxxxxxx xxxxx nepodporují xxxx xxxxxxxxx. Xxxx xxxxxxx xx vivo by xxx nebylo nutné xxxxxxxx. Xxxxx xxxxx xxxxxxx nebo xxxxxxx xxxxxxxx účinky xx xxxx nemá, xxxx xxxxxxx xx xxxx xx xxxxxxx.
Xxxxxxx xx xxxx xx králících (xxxxx 8 x 9). Xxxx zkoušení xx xxxx xx xxxxxx počáteční zkouškou xx xxxxxx pokusném xxxxxxx. Pokud xxxxxxxx xxxx xxxxxxx xxxxxxxxx, xx látka má xxxxx dráždivé xxxx xxxxxxx xxxxxx xx xxx, xxxxxx by xx xxxxx xxxxxxxx xxxxxxxx. Xxxxx zkouška xxxxx leptavé xxxx xxxxx xxxxxxxx účinky xxxxxxxx, provede se xxxxxxxxxxx xxxxxxx xx xxxx xxxxxxx xxxxxxxxx xxxxxxxxx.
Xxxxxxx 10 pokračování
Strategie xxxxxxxx a xxxxxxxxx xxxxxxxxxx/xxxxxxxxx xxxxxx na xxx
| &xxxx;
|
|
|
|
|
|
Xxxxxxxxxx xxxxx o xxxxxxxx xx xxxxxx xxxx xxxxxxx oči
|
Závažné xxxxxxxxx očí
|
Dominantní xxxxxxxx; xxxxxxxxxx xx xxxxxxx xxx oči. Není xxxxx xxxxxxx.
|
| &xxxx;
|
Xxxxxxxx pro xxx
|
Xxxxxxxxxx xxxxxxxx; považována xx dráždivou xxx xxx. Xxxx nutné xxxxxxx.
|
| &xxxx;
|
Xxxxxxxx xxxx xxxxxxxxxx xxx xxx
|
Xxxxxxxxxx xxxxxxxx; xxxxxxxxxx xx nežíravou x nedráždivou pro xxx. Xxxxxxxxxx zkoušet.
|
|
|
Existující xxxxx x leptavých xxxxxxxx na lidskou xxxx xxxxxxx xxxx
|
Xxxxxxx xxxxxx na kůži
|
Předpoklad xxxxxxxxx účinků xx xxx. Xxxx xxxxx xxxxxxx.
|
| &xxxx;
|
Xxxxxxxxxx xxxxx o xxxxx xxxxxxxxxx účincích xx lidskou xxxx xxxxxxx xxxx
|
Xxxxx xxxxxxxx xxxxxx na kůži
|
Předpoklad xxxxxxxxxx účinků na xxx. Xxxx xxxxx xxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxxx x&xxxx;xxxxxxxxx xxxxx xxxxxxxxx nebo informace xxxxxx xxxxxxxxxxx.
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
|
|
Xxxxxxxx xxxxxxxxx xxxxxxxxx/xxxxxxxxxx účinků xx xxx xxxxx xxxxxxx XXX.
|
Xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxx
|
Xxxxxxxxxx žíravosti pro xxx. Xxxx xxxxx xxxxxxx.
|
| &xxxx;
|
&xxxx;
|
Xxxxxxxxxx xxxxxxxxxx xxxxxx xx xxx
|
Xxxxxxxxxx xxxxxxxxxxx xxx xxx. Není xxxxx zkoušet.
|
|
|
Proveďte xxxxxxx XXX leptavých účinků xx xxxx
|
Xxxxxxxxxx xxxxxxxxx xxxxxx xx xxxx
|
Xxxxxxxxxx xxxxxxxxx xxx xxx. Xxxx xxxxx xxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxx xxxxxxxx xxxxx xxxxxxxxxxx, xxxx jsou předpoklady xxxxxxxxxxxxx nebo negativní.
|
|
|
|
|
↓
|
|
|
|
|
Změřte xxxxxxx xX (pufrační xxxxxxxx, je-li významná).
|
ph ≤ 2 nebo ≥ 11,5 (x xxxxxxx xxxxxxxx xxxxxxxxx, xxxxx xx xxxxxxxx)
|
Xxxxxxxxxx xxxxxxxxx xxx xxx. Xxxx xxxxx zkoušet.
|
|
|
↓
|
|
|
|
|
2 &xx; pH < 11,5, xxxx xX ≤ 2 nebo ≥ 11,5 s nízkou/žádnou xxxxxxxx xxxxxxxxx, pokud xx xxxxxxxx.
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
|
|
Xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx cestou.
|
Vysoce xxxxxxx xxx xxxxxxxxxxxxx, xxxxx xx xxxx xxxxxxxx xx xxxxx
|
Xxxxx xx xxxx xxx xxxxxxxx příliš toxická. Xxxx xxxxx xxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxxx xxxxxxxxx xxxxxx x&xxxx;xxxxxxxxx, xxxx látka xxxx xxxxxx toxická.
|
|
|
|
|
↓
|
|
|
|
|
Proveďte xxxxxxxxxxx x xxxxxxx xxxxxxx xxxxxxxxx xxxxxx xx xxx xx xxxxx xxxx ex xxxx
|
Xxxxxxx xxxxxx
|
Xxxxxxxxxx xxxxxxxxx účinků xx xxx. Xxxx xxxxx žádné xxxxx xxxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxx xxxx xxxxxx, xxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxx xxx in xxxxx xxxx xx vivo xxxxx xxxxxx k dispozici.
|
|
|
|
|
↓
|
|
|
|
|
Proveďte xxxxxxxxxxx x uznanou xxxxxxx xxxxxxxxxx účinků xx oči in xxxxx nebo xx xxxx.
|
Xxxxxxxx účinky
|
Předpoklad xxxxxxxxxx xxxxxx xx xxx. Xxxx xxxxx žádné xxxxx xxxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxx xxxx xxxxxxxx, xxxx xxxxxxxxxx xxxxxx zkoušení xxxxxxxxxx xxxxxx xx xxx xx xxxxx nebo xx xxxx xxxxx xxxxxx k dispozici.
|
|
|
|
|
↓
|
|
|
|
|
Experimentálně xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxx na xxxx in xxxx (xxx xxxxxx xxxxxxxx X.4, xxxxxx její xxxxxxx)
|
Xxxxxxx nebo slně xxxxxxxx xxxxxx
|
Xxxxxxxxxx xxxxxxxxx xxxxxx na oči. Xxxx třeba xxxxx xxxxx xxxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxx xxxx xxxxxx xxx xxxxx xxxxxxxx xxx xxxx.
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxxxxx xxxxxxxxx xxxx xxxxxxx xx králících in xxxx na jednom xxxxxxxx xxxxxxx.
|
Xxxxxxx poškození xxx
|
Xxxxxxxxxx xx xxxxxxxxx xxx oči. Xxxx xxxxx xxxxx xxxxx xxxxxxxx.
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
Xxxxx výrazné xxxxxxxxx, xxxx xxxxx xxxxxx.
|
&xxxx;
|
&xxxx;
|
| &xxxx;
|
↓
|
&xxxx;
|
&xxxx;
|
|
|
Xxxxxxxx xxxxxxxxxxx xxxxxxx na xxxxxx xxxx další xxxx xxxxxxxxx xxxxxxxxx.
|
Xxxxxx xxxx xxxxxxxx
|
Xxxxxxxxxx xx xxxxxxx xxxx dráždivou xxx xxx. Xxxx xxxxx žádné xxxxx xxxxxxxx.
|
| &xxxx;
|
Xxxxxxxx nebo xxxxxxxxxx
|
Xxxxxxxxxx xx xxxxxxxxxxx x xxxxxxxxx xxx oči. Xxxx xxxxx žádné xxxxx zkoušení.
|
|
|
|
|
|
B.6 XXXXXXXXXXXXX XXXX
1 XXXXXX xx x xxxxxxx x xxxxxx Evropských společenství.4)
1.1 Xxxx
Xxxxxxxx:
Xxxxxxxxx x detekční xxxxxxxxx xxxxx pro xxxxxxxxxx xxxxx s xxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxx xx xxxxxxx xxxx xxxx xxxxxxxxxx za xxxxxxxx xxx xxxxxxxxxxxx xxxxxx toxicity v xxxxxxx xxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxxxxx xxxxxx testovací metoda, xxxxx xx dostatečně xxxxxxxxxx xxxxxxxxxxxxxx všechny xxxxx s xxxxxxxxxxxx xxxxxxxxxxxxxxx účinkem xxx xxxxxxx xxxx x xxxxx xx se xxxxxx xxx všechny xxxxx.
Xxx xxxxx testu xx třeba uvažovat xxxxxxx jako xxxx. xxxxxxxxx charakteristiky látky, xxxxxx schopnosti xxxxxxx xxxx.
Xxxxx xx xxxxxxxxx xxx xxxxxxxx xx xxxxx x xxxxxxxx, xx xxxxxxx xx xxxxxxxxx xxxx potencován xxxxxxxxxxx nebo xxxxxxxxxxxxx xxxxxxxxx xxxxx xx Xxxxxxxxx xxxxxxxxxx xxxxxxxx (XXX), x na xxxxx bez xxxxxxxx.
Xxxxx x xxxxxxxx xx xxxxx xxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxx xxx xxxxxxx kůži xxx xxxxxx bez Xxxxxxxxx xxxxxxxxxxx adjuvans, x xxxxx xx xxx xxxx xxxxxxxx.
Xxxxxxxxxxxxx test xx morčatech (Xxxxxx-xxx Xxxxxxxxxxxx Test - XXXX) xx xxxxx xxxxxxxxx test x xxxxxxxx. Xxxxxxx k xxxxxxxx schopnosti látky xxxxxxx xxxxxxxxxxxxxx xxxxxx xxxxxxxx několik xxxxxxx xxxxx, xx XXXX xxxxxxxxx xx preferovanou xxxxxxxx x adjuvans.
U xxxxx skupin chemických xxxxx xxxx testy xxx xxxxxxxx (přednost xx xxxx Xxxxxxxxxx xxxxx) xxxxxxxxxx xx xxxx xxxxxxx.
X xxxxxxxx xxxxxxxxx xxx zdůvodnit xxxxx Xxxxxxxxxx xxxxx x xxxxxxxxxx xxxxxxxx xxxxx xxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxxx x xxxxxxxxxxxx xxxxx xx xxxxxxxxx. Xxx použití Xxxxxxxxxx xxxxx xx xxxxx xxxxx odborné xxxxxx.
X xxxx xxxxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxxxxxxxxx xxxx xx xxxxxxx (XXXX) a Xxxxxxxxx xxxx. Xxx xxxxxx x xxxxxx xxxxx, xxxxx jsou xxxxxxxxxx validizované x xxxxx xxxx odborné xxxxxx xxx xxxxxx xxxxxxx.
Xxxxx skríningový xxxx xxxxxxxxx uznávanou metodou xx pozitivní výsledek, xx xxxxx xxxxxxxxxx xxxxx xxxxxxx jako xxxxxxxxxxx senzibilizátor xxx xxxxxxx xxxxxxxxx na xxxxxxxxx. Při negativním xxxxxxxx xx xxxx xxxxx xxxxxxx xxxx xx xxxxxxx, xxx xxx xx popsán x této xxxxxxxxx xxxxxxxx.
1.2 Xxxxxxxx
Xxxxxxxxxxxxx kůže: (xxxxxxxxx xxxxxxxxx xxxxxxxxxxx) xx xxxxxxxxxxxx zprostředkovaná xxxxx reakce xx xxxxx. X xxxxxxx xxxxx být reakce xxxxxxxxxxxxxxxx svěděním, xxxxxxxxxx xxxx, otokem, pupenci, xxxxxxxx, xxxxxx (xxxxxxx xxxxxxx) xxxx kombinací xxxxxx xxxxxxxx. X xxxxxx živočišných druhů xx mohou reakce xxxxx x může xxx xxxxxxxx xxxxx xxxxxxxxx xxxx xxxx.
Xxxxxxxx xxxxxxxx: experimentální expozice xxxxxxxx testované látce xx xxxxxxx xxxxxxx xxxx xxxxxxxxxxxxxxx.
Xxxxxxxx xxxxxx: xxxxxx nejméně jednoho x dne po xxxxxxxx xxxxxxxx, v xxxxxxx kterého xx xxxx rozvinout xxxx xxxxxxxxxxxxxxx.
Xxxxxxxxxx expozice (challenge): xxxxxxxxxxxxxx expozice subjektu xxxxx xxxxxxxxxxx xxxxxxxxx xxxxx xx xxxxxxxxx xxxxxx xxx xxxxxxxxx, xxx xxxxxxx xxxxxx xxxxxx xxxxxxxxxxxxxxx.
1.3 Xxxxxxxxxx xxxxx
Xxxxxxxxx u xxxxxxx xxxxxxxxxxxxxx xxxxxx xx xxxx xxx xxxxxxxxx xxxxxxx šest měsíců x xxxxxxxx látek, x xxxxxxx xx xxxxx, xx xxxx xxxxx xx xxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxx xxx xxxx.
X xxxxxxx xxxxxxxxxxx xxxxx xx xxxxxxx reakce xx xxxxx/xxxxxxx xxxxxxxxxxxxx xxxxxxx 30 % x xxxxxx s adjuvans, x xxxxxxx 15 % x xxxxxx xxx xxxxxxxx.
Xxxxxxxx se xxxx následujícím xxxxxx:
|
|
|
|
|
|
101-86-0
|
202-983-3
|
2-xxxxx-3-xxxxx-2-xxxxxxxx
|
xxxx-xxxxxxxxxxxxxxxxxx
|
|
149-30-4
|
205-736-8
|
2-xxxxxxxxxxxxxxxxxxxx
|
xxxxxx
|
|
94-09-7
|
202-303-5
|
Xxxxx ester kyseliny x-xxxxxxxxxxxxx
|
xxxxxxxxx
|
Xxxxx xxxxxx xxxxxxxxx, xxx při dostatečném xxxxxxxx xxxxxxxxxx mohou xxx xxxxxxx jiné xxxxxxxxx xxxxx xxxxxxxxx xxxx uvedená xxxxxxxx.
1.4 Xxxxxxx xxxxxxxxx xxxxxx
Xxxxxxx xxxxxxx jsou xxxxxxx xxxxxxxxxx testované xxxxx xxxxxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx (xxxxxxxx xxxxxxxx). Po období 10 xx 14 xxx (xxxxxxxx období), x průběhu xxxxxxx xx může rozvinout xxxxxxxx xxxxxx, xxxx xxxxxxx xxxxxxxxxx provokační xxxxx. Rozsah a xxxxxx xxxxx reakce xx xxxxxxxxxx xxxxxxxx x xxxxxxxxxxx xxxxxx xx xxxxxxxxxx x xxxxxxxx a xxxxxxx xxxxxx u xxxxxxxxxxx xxxxxx, xxxxx podstoupí xxxxxxx expozici x xxxx xxxxxxx x xx xxx xxxxxxxxxx xxxxxxxxxx xxxxx.
1.5 Popis xxxxxxxxxxx metod
Jestliže xx xxxxxxxxxx xx xxxxxxxx xxxxxxxxx testovanou xxxxx, xxxxxxx se to x použitím xxxx xxxx vhodného xxxxxxxxxxxx xxx, aby nebyla xxxxxxxx vzniklá xxxxx xxxxxx nebo xxxxxxxxx xxxxxxx.
1.5.1 Xxxxxxxxxxxxx xxxx xx xxxxxxxxx (GPMT)
1.5.1.1 Xxxxxxxx
Xxxxxxx xxxxxxx xxxx xxxxxxx x xxxxxxx xx xxxx, xxxxxxx x xxxxx x xxxxxxx x ustanovením
§15 zvláštního právního xxxxxxxx
10) x označena xxx, aby xxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10) Xxxx xxxxxx se zvířata xxxxxxx rozdělí xx xxxxxxxxxxx x kontrolních xxxxxx. Xxxxxxxxxx xxxxx xx xxxxxxx xxxxxxxxx, xxxxxxx xxxx xxxxxxxxx xxxxxxxx, v xxxxxxxxxx xx použité xxxxxxxxx xxxxxx. Xx třeba xxxx xx to, xxx xxxxxxx k xxxxxxxxx xxxx. Xxxxxxx xx xxxxx xxxx xxxxxxxxx xxxxx x xx xxxxx xxxxx.
1.5.1.2 Xxxxxxxxxxxxxx xxxxxxxx:
Xxxxxxx zvířata xxxx xxxxxxx s xxxxxxx xx xxxx, xxxxxxx x stáří x xxxxxxx x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx předpisu
10) x xxxxxxxx tak, aby xxxx xxxxx identifikace xxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10)1.5.1.2.1 Xxxxxxx xxxxxxx
Xxxxxxxxx se xxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxx.
1.5.1.2.2 Xxxxx x pohlaví
Lze použít xxxxx x samice. Xxxxxx xxxx xxx xxxxxxxxx a nesmí xxx březí. Xxxxxxxxxxx xxxxxxx xxxxx nejméně 10 xxxxxx x xxxxxxx 5 zvířat xx třeba x xxxxxxxxx xxxxxxx. Xxxxxxx-xx xx menšího počtu xxx 20 xxxxxxxxxxx x 10 xxxxxxxxxxx xxxxxx x xxxx xxxxx xxxxx x xxxxxx, xx xxxxxxxxx xxxxx je xxxxxxxxxxxxxx, xxxxxxxxxx se testování xx dalších xxxxxxxxx, xxx se xxxxxxx xxxxxxxxx xxxxx xxxxxxx 20 xxxxxxxxxxx x 10 xxxxxxxxxxx xxxxxx.
1.5.1.2.3 Xxxxxxx xxxxxx
Xxxxxxxxxxx xxxxxxxxx xxxxx použitá xxx xxxxxx indukční xxxxxxxx xx xxxxxx xx xxxxxxx xxxxxx, xxxxxx xxxxxxx xxxxxxx dobře xxxxxxx x xxxxx xx xxxxxxxx působící xxxxx xx xxxxxxx xxxxxxxxxx xxxx. Xxxx xxxxxxxxxx koncentrace xx xxxxxxx xxxxxxxxx xxxxxxxxxxx, xxxxx x xxxxxxxxxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx xxxx. X xxxxxxx xxxxxxx xx xxxxx xxxxxx koncentrace xxxxxxxx x předběžném pokusu xx xxxx xxxx xxxxx xxxxxxxxx. Xxx xxxxx xxxx lze xxxxxx použití xxxxxx, xxxxx xxxx aplikováno XXX.
1.5.1.3 Popis postupu
1.5.1.3.1 Xxxxxxx
Xxx 0 - Xxxxxxxxx xxxxxxx
Xxxxxxxxxxx 3 xxxxxxx xxxxxxxxxxxx injekcí, xxxxx xx 0,1 xx, xx xxxxxx xx lopatkové xxxxxxx xxxxxxx srsti symetricky xxxxx xxxxxxx linie:
Injekce 1: Xxxxxxxxx kompletní xxxxxxxx (XXX) smíšené x xxxxx xxxx xxxxxxxxxxxxx xxxxxxxx v xxxxxxxxx poměru 1:1;
Xxxxxxx 2: testovaná xxxxx xx vhodném vehikulu xx xxxxxxx koncentraci;
Injekce 3: xxxxxxxxx xxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxxxx xx xxxxx XXX x xxxxx xxxx xxxxxxxxxxxxx xxxxxxxx x objemovém poměru 1:1.
Xxx xxxxxxx 3 xx xxxxx xx xxxx xxxxxxxxx xxxxxxxx xxxx smísením s XXX xx xxxxx xxxx. Xxxxx rozpustné x xxxxxxxx nebo xxxxx nerozpustné xx xxxxxxxx x nezředěném XXX. Xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxx 3 xx xxx xxxxxx xxxx xxx xxxxxxx 2.
Xxxxxxx 1 x 2 xx xxxxxxxx xxxxxx xxxx a xx xxxxxxxx xxxxx, xxxxxxx xxxxxxx 3 xxxxxx xx kaudální části xxxxxxxxx xxxxxx.
Xxx 0 - Kontrolní skupina
Následující 3 xxxxxxx subkutánních xxxxxxx, xxxxx xx 0,1 ml, se xxxxxx xx xxxxxxxx xxxx xxxx u xxxxxxxxxxx zvířat:
Injekce x: Xxxxxxxxx xxxxxxxxx xxxxxxxx (XXX) xxxxxxx x xxxxx xxxx xxxxxxxxxxxxx xxxxxxxx v xxxxxxxxx xxxxxx 1:1;
Xxxxxxx 2: xxxxxxxx xxxxxxxxx;
Xxxxxxx 3: Xxxx vehikula (50 %, váha/objem) xx xxxxx XXX/xxxx xxxx xxxxxxxxxxxxxx xxxxxxx v xxxxxx 1:1 (xxxxx/xxxxx).
5. - 7. xxx - Testované x xxxxxxxxx xxxxxxx
Xxxxxxxxx dvacet xxxxx hodin xxxx xxxxxxx xxxxxxxx xxxxxxxx, xxxxxxxx xxxxx není xxxxxxxx xxx kůži, xx xx xxxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxx oholení xxxxx 0,5 ml 10 % xxxxxxxxxxxxx xxxxxxx xx xxxxxxxx, xx xxxxxx navození xxxxxxxx xxxxxxxxxx.
6. - 8. xxx - Xxxxxxxxx xxxxxxx
Xxxxxxxxx xxxxxx xx zbaví xxxxx. Xxxxxxxxxx látkou xx xxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxxx xxxxx (2 x 4 xx), xxxxx se xxx xxxxxxx na xxxxxxxxx plochu x xxxxxx xxxxxx okluzívního xxxxxx na xxxx 48 xxxxx. Xxxxx xxxxxxxx xx řídí xxxxxxxxx xxxxxx; xxxxx xxxxx xxxx xxxxx xxxxxxxxx a xxxxxxxxx xx vhodného xxxxxxxx; xxxxxxxx lze aplikovat xxxxx.
6. - 8. xxx - Xxxxxxxxx xxxxxxx
Xxxxxxxxx xxxxxx xx xxxxx xxxxx xxxxx. Xxxxxxx xxxxxxxxx xx xxxxxx x xxxxxxxx xxxxxxx xxxx u xxxxxxxxxx xxxxxxx na xxxx 48 xxxxx.
1.5.1.3.2 Xxxxxxxxx
20. - 22. xxx - Xxxxxxxxx x kontrolní xxxxxxx
Xxxx xxxxxxxxxxxx i xxxxxxxxxxx xxxxxx jsou xxxxxxx xxxxx. Na jeden xxx zvířete xx xxxxxxxxxx testovaná xxxxx x xxxxxx xxxx x xxxxxxx x xx xxxxx xxx xx stejným xxxxxxxx xxxxxxxx xxxxx xxxxxxxxx (xxxxx je to xxxxx). Plátky se xxxxxx xxxxxxxxxxx xxxxxx xxxxxxx x xxxxxxxx x xxxx xx 24 xxxxxx.
1.5.1.3.3 Xxxxxxxxxx x vyhodnocení: testované x xxxxxxxxx xxxxxxx
- xxxxxxxxx 21 xxxxx xx odstranění xxxxxxxx xx xxxxxxxxxx xxxxxx xxxxxxx, xxxxxxxx ostříhá xxxxxxxx xxxxx x x xxxxxxx potřeby xxxxxxxx;
- přibližně xx xxxxxxx třech xxxxxxxx (xxxxxxxxx 48 xxxxx xx začátku aplikace xxxxxxxxxx xxxxx) xx xxxxxxxx xxxxx xxxxxx x xxxxxxxxxxx xx xxxxx xxxxxxxx uvedené x dodatku;
- xxxxxxxxx 24 xxxxx po xxxxx pozorování xx xxxxxxx xxxxx xxxxxxxxxx x xxxxxx reakce xxxx (72 xxxxx).
Xxxxxxxxxx xx xxxxxx "slepého xxxxxx" x xxxxxxxxxxx x kontrolních xxxxxx, xxx xxxxxxxxxx xxxxx xxxx, xxxxx xxxxx xxxx xxxxxxxxxxxxxxx a xxxxx xx xxxxxxxxx.
Xxxxx xx x xxxxxxxxx xxxxxxxx nutná xxxxx xxxxxxxxx (xx. xxxxxxxxx xxxxxxxxx), provede xx xxxxxxxxx x týden xxxxxxx, x xxxxxxx xxxxxxx xxxxx s xxxxxxxxx skupinou x xxxxxxxxx. Opakovanou xxxxxxxxx xxx xxxx xxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxx.
Xxxxxxx xxxxx reakce x xxxxxxxxx xxxxxx, xxxxxx xxxxxxxxx reakcí, xxxxx xxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxx xxxxxxx se zaznamenávají xxxxx stupnice Magnussona/Kligmana x xxxxxxx x. 8. X objasnění xxxxxxxx xxxxxx xx xxxxx xxxxxx xxxxxxx xxxxxxx, xxxx např. xxxxxxxxxxxxxxxxxx vyšetření xxxx xxxxxx xxxxxxxx kožních xxx.
1.5.2 Xxxxxxxxx xxxx
1.5.2.1 Xxxxxxxx
Xxxxxx mladá xxxxxxx xxxxxxxxxxx xxxxxxx se xxxxxxxxxxxx xx xxxxxxxxxxx xxxxxxxx xx dobu xxxxx 5 xxx xxxx xxxxxxxxx xxxxx. Xxxx xxxxxx xx xxxxxxx xxxxxxx xxxxxxx xx expozičních x xxxxxxxxxxx xxxxxx. Xxxxxxxxxx xxxxx xx xxxxxxx xxxxxxxxx, holením xxxx xxxxxxxxx xxxxxxxx, v xxxxxxxxxx xx xxxxxxx xxxxxxxxx metodě. Je xxxxx dbát na xx, aby xxxxxxx x poškození kůže. Xxxxxxx se xxxxx xxxx zahájením xxxxx x na konci xxxxx.
1.5.2.2 Xxxxxxxxxxxxxx podmínky
1.5.2.2.1 Xxxxxxx xxxxxxx
Xxxxxxxxx xx xxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxx.
1.5.2.2.2 Xxxxx x xxxxxxx
Xxx použít xxxxx a/nebo samice. Xxxxxx musí xxx xxxxxxxxx a xxxxx xxx xxxxx.
Xxxxxxx se xxxxxxxxx 20 zvířat x xxxxxxxxx skupině x xxxxxxx 10 xxxxxx x xxxxxxxxx xxxxxxx.
1.5.2.2.3 Xxxxxxx úrovně
Koncentrace xxxxxxxxx xxxxx xxxxxxx xxx xxxxxx indukční xxxxxxxx xx xxxxxx xx xxxxxxx xxxxxx, xxxxx xxxxxx mírné, xxx xx xxxxx xxxxxxxxxx kůže. Jako xxxxxxxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxxxx, xxxxx u nesenzibilizovaných xxxxxx nevyvolává xxxxxxxxxx xxxx. X xxxxxxx xxxxxxx je xxxxx xxxxxx koncentrace xxxxxxxx x předběžném pokusu xx dvou xxxx xxxxx xxxxxxxxx.
Xxx testované xxxxx rozpustné ve xxxx je xxxxxx xxxxxx xxxx xxxx xxxxxxx nedráždící xxxxxx xxxxxxxxxx xxxx xxxxxxxx. Xxx xxxx xxxxx xx preferován 80% xxxxxx etanol/voda pro xxxxxxx a xxxxxx xxx xxxxxxxxx.
1.5.2.3 Postup
1.5.2.3.1 Xxxxxxx
Xxx 0 - Xxxxxxxxx xxxxxxx
Xxxxx xxx xx zbaven srsti (xxxxxxxx xxxxxxxx). Xxxxxx xxxxxxxxxx xxxxx xx xxxxxxxx xxxxxx testovanou xxxxxx xx vhodném xxxxxxxx (xxxxx xxxxxxxx xx xxxx xxxxxxxxx xxxxxx; kapaliny xxx xxxxxxxx xxxxxxxxx xxxxx).
Xxxxxxxx xxxx je xxxxxxxx xx xxxxxxxxx xxxxxx x xxxxxxxxxx v xxxxxxxx x xxxx xxxxxxxxxxx xxxxxxx xxxx xxxxxxxx x xxxxxxx xxxxxxx xx xxxx 6 xxxxx.
Xxxxxx plátkového xxxxx xxxx xxx xxxxxxxxx. Xxxxxx je xxxxxxxx polštářek, xx xx kruhový nebo xxxxxxxxx, s xxxxxxx xxxxxxxxx 4 - 6 xx. Je xxxxxxxxxxx xxxxxxxxx s xxxxxxxx xxxxxx xxxxxx, xxx xx xxxxxxxxx xxxxxx. Xxxxxxxx je xxxxxxx xxxxxxxx, xxxxx xxx nutné další xxxxxxxx.
Xxx 0 - Xxxxxxxxx xxxxxxx
Xxxxx xxx xx zbaven xxxxx (xxxxxxxx xxxxxxxx). Na xxxxxxxxx plochu xx xxxxxxxx xxxxx xxxxxxxxx, x to xxxxxxxx xxxxxxxx xxxx x xxxxxxxxx xxxxxxx. Plátkový xxxx xx přiložen xx xxxxxxxxx xxxxxx x xxxxxxxxxx x xxxxxxxx s xxxx xxxxxxxxxxx plátkem nebo xxxxxxxx x vhodným xxxxxxx po dobu 6 xxxxx. Pokud xx xxxxx xxxxxxxx, xx negativní xxxxxxxxx xxxxxxx není xxxxx, xxx xxxxxx čisté xxxxxxxxx skupiny xxx xxxxxxxx.
6. - 8. x 13. - 15. xxx -Xxxxxxxxx x kontrolní xxxxxxx
Xxxxxx xxxxxxxx jako x xxx 0 xx xxxxxxx xx stejnou xxxxxxxxx plochu na xxxxxx boku (zbavenou xxxxxxxx xxxxx) 6.-8. xxx x xxxxx 13.-15. xxx.
1.5.2.3.2 Xxxxxxxxx
27. - 29. xxx - Xxxxxxxxx x xxxxxxxxx xxxxxxx
Xxxxxxxxxx xxx xxxxxxxxxxx x xxxxxxxxxxx xxxxxx xx zbaven xxxxx (xxxxxxxx xxxxxxxx). Xxxxxxxxx plátek xxxxxxxxxx xxxxxxxxx xxxxxxxx testované xxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xx xxxxxxxx xx zadní xxxx neošetřeného xxxx xxxxxxxxxxx a xxxxxxxxxxx xxxxxx. Xx xxxxxx xxxx neošetřeného xxxx xxxxxxxxxxx x xxxxxxxxxxx xxxxxx xx xxxxxxxx xxxx xxxxxxxxx okluzní xxxxxx x xxxxxxxxx. Xxxxxxxxxx xxxxxx nebo xxxxxxx xxxx přidržovány x xxxxxxxx s xxxx xxxxxxx xxxxxxx xx xxxx 6 xxxxx.
1.5.2.3.3 Xxxxxxxxxx a xxxxxxxxx
Xxxxxxxxx 21 xxxxx xx xxxxxxxxxx plátku xx provokační xxxxxx xxxxx xxxxx;
xxxxxxxxx o xxx hodiny později (xxxxxxxxx 30 xxxxx xx xxxxxxxx provokačního xxxxxx) se pozorují xxxxx xxxxxx x xxxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx x dodatku;
přibližně xx xxxxxxx 24 xxxxxxxx (xx. xxxxxxxxx 54 xxxxx xx xxxxxxxx xxxxxxxxxxxx xxxxxx) xx kožní xxxxxx xxxxx xxxxxxxx a xxxxxxxxxxx.
Xxxxxxxxxx xx xxxxxx "xxxxxxx odečtu" u xxxxxxxxxxx x xxxxxxxxxxx xxxxxx, kdy xxxxxxxxxx xxxxx xxxx, které xxxxx bylo senzibilizováno x xxxxx xx xxxxxxxxx.
Xxxxx xx k xxxxxxxxx xxxxxxxx xxxxx xxxxx xxxxxxxxx (tj. xxxxxxxxx xxxxxxxxx), provede xx xxxxxxxxx x xxxxx xxxxxxx, v xxxxxxx potřeby xxxxx x kontrolní skupinou x xxxxxxxxx. Xxxxxxxxxx xxxxxxxxx xxx xxxx xxxxxxx xx xxxxxxx xxxxxxxxx skupině.
Všechny kožní xxxxxx a neobvyklé xxxxxx, xxxxxx celkových xxxxxx, xxxxx xxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxxxx xxxxxxx, xx xxxxxxxxxxxxx podle xxxxxxxx Xxxxxxxxxx/Xxxxxxxx (xxx dodatek). X xxxxxxxxx sporných xxxxxx xx xxxxx xxxxxx xxxxxxx xxxxxxx, xxxx xxxx. histopatoiogického xxxxxxxxx xxxx xxxxxx xxxxxxxx xxxxxxx xxx.
2 XXXX X ZÁZNAM XXXXX (GPMT X XXXXXXXXX TEST)
Údaje xx xxxxxxx do xxxxxxx, xx xxxxx xxxx xxx xxx každé xxxxxxx zvíře xxxxxx xxxxxx xxxx xxx xxxxxx xxxxxxxxxx.
3 PROJEKT XXXXXX, PROTOKOL XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx s xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx x o xxxxxxx xxxxxx je xxxxx xxxx protokol.
Pokud xxx proveden xxxx xxxxxxxxx testu xx xxxxxxxxx xxxx xxxxxxxxxxx, xx třeba xxxxx xxxxx xxxxxx xxxxx xxxx jeho xxxxxx (xxxx. XXXX - xxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxx, XXXX - xxxx xxxxxxxxx xxxx x xxxx) xxxxxx xxxxx xxxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxx xxx xxxxxxxxx a xxxxxxxxxx xxxxx.
3.1 Xxxxxx x xxxxxxx xxxxxx (XXXX x Buehlerův xxxx)
Xxxxxx o pokusu xxxxxxxx xxxx xxxxxxxxx, xxxxx xxxxx být xxxxxxx
Xxxxxxx xxxxxxx:
- xxxxxxx xxxx xxxxxx;
- xxxxx, xxxxx a xxxxxxx xxxxxx;
- podmínky xxxxx, xxxxxx atd.;
- hmotnost xxxxxxxxxxxx xxxxxx na xxxxxxx a xxxxx xxxxx.
Xxxxxxxxxxxxxx xxxxxxxx:
- způsob xxxxxxxx xxxxx pro xxxxxxxx xxxx;
- xxxxxxxx xxxxxxxxx x xxxxxxxxxxx x xxxxxxxx plátkového xxxxx;
- xxxxxxxx pilotní xxxxxx xx xxxxxxx x xxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxxxxx xxx xxxxxxx test;
- xxxxxxxx xxxxxxxxx x xxxxxxxx, xxxxxxxx x odstranění xxxxxxxxx látky;
- xxxxxxxxxx xxxxxx vehikula;
- xxxxxxxxxxx x xxxxxxx množství xxxxxxxxx xxxxx x xxxxxxxx, xxxxxxx xxx xxxxxxx x provokaci.
Výsledky:
- xxxxxx xxxxxxxx xxxxxxxx xxxxxxxx citlivosti x xxxxxxxxxxxxx (xxx 1.3.) xxxxxx xxxxxxx referenční xxxxx, xxxx xxxxxxxxxxx x xxxxxxxx;
- xxxxxxx xxxxxxxxxx xxx každé xxxxx xxxxxx xxxxxxx xxxxxxxxxxx;
- xxxxxx popis xxxxxxxxxx x xxxxxx xxxxxxxxxxxx xxxxxx;
- xxxxxxx xxxxxxxxxxxxxxxx nálezy.
Diskuse xxxxxxxx.
Xxxxx.
Xxxxxxx x. 8
Xxxxxxxx Xxxxxxxxxx/Xxxxxxxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx reakcí
0 žádná xxxxxxxxx změna
1 xxxxx xxxx xxxxxxxx xxxxxxxxx xxxx
2 xxxxxxx xxxxxxx x splývající zarudnutí xxxx
3 intenzívní xxxxxxxxx x zduření kůže
B.7 XXXXXXXXX XXXXXXXX ORÁLNÍ (28XXXXX XXXXXXXXX XXXXXXXX)
1 XXXXXX je v xxxxxxx s xxxxxx Xxxxxxxxxx společenství.
4)1.1 Xxxxxxx xxxxxxxxx xxxxxx
Xxxxxxxxx xxxxx xx xxxxxx xxxxx xx 28 xxx x xxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxx, x xx xxxxx skupině 1 xxxxxx xxxxx. Xxxxx xxxxxx xxxxxxxx xx zvířata xxxxx xxxxxxx pozorují, xxx xx zjistily xxxxxxxx xxxxxxxx. Xxxxx xx xxxxxxx x xxxxx xxxxxx, která uhynou xxxx xxxx xxxxxxxx xxxxx xxxxxx; také xxxxxxx, která xxxxxxx xxxxx xxxxxx, xx xxxxxx x xxxxxxx.
Xxxx xxxxxx xxxxx xxxxx xxxxx na neurologické xxxxxx xxxx xx xxxxxxxxxx xxxxxxxx xxxxxx; xxxxx xx kladen xx potřebu pečlivého xxxxxxxxxx xxxxxxxxxx xxxxxx, xxx xxxx xxxxxxx xx xxxxxxx xxxxxxxxx. Xxxxxx xx měla xxxxxxx chemické xxxxx x xxxxxxxxxxxxx xxxxxxxxxxx, x xxxxx xxxx xxx xxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxx xxxxxxx. Xxxxxx může xxxxxxxxx xx xxxxxxxxxxxx xxxxxx x xxxxxxxx xxx xxxxxxxxxxx orgány.
1.2 Xxxxx xxxxxx
1.2.1 Xxxxxxxx
Xxxxxxx xxxxxxx jsou vybrána x ohledem xx xxxx, xxxxxxx x xxxxx x souladu x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x xxxxxxxx tak, xxx byla možná xxxxxxxxxxxx jednotlivých zvířat. Xxxx navykání xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10) Zdravá xxxxx xxxxxxx se xxxxxxx xxxxxxx do kontrolní xxxxxxx x jednotlivých xxxxxxxxxxxxxxxx skupin. Xxxxx xxxx xxxxxxxxxx xxx, xxx xx xx xxxxxxx xxxxxxxx xxxx xxxxxxxx klece.
Testovanou xxxxx xxx podávat xxxxxx xxxx v xxxxxxx xxxx v xxxxx xxxx, xxxxx účelu xxxxxx x xxxxxxxxx-xxxxxxxxxx xxxxxxxxxx xxxxx.
Xxxxx xx xx xxxxx, rozpustí xxxx xxxxxxxxxx se xxxxxxxxx xxxxx xx xxxxxxx xxxxxx (xxxxxxxx). Xxxxxxxxxx xx xxxxxxx xxxxxx použití xxxxxxx xxxxxxx / suspenze, xxx xxxxxxx xxxxxxx / xxxxxx v xxxxxx xxxxxxxxxx xxxxx (xxxx. xxxxxxxxxx) x xxx xxxxxxx x xxxxxx nosičích. Xxx xxxxxxx vehikula musí xxx xxxxx xxxxxx xxxxxxx charakteristika; xxxxx xxxx xxxxx, xxxx xxx xxxxxxxxx ještě xxxx testem. Xx xxxxxxxx xxxxxx xxxxxxxxx xxxxx ve xxxxxxxx xxxxxxxx.
1.2.2 Experimentální xxxxxxxx
1.2.2.1 Xxxxxxx xxxxxxx
Xxx provádění xxxxxx xx xxxxxxxxxxxxx xxxxxxx, ale xx xxxxx použít x xxxxxx druhu hlodavců. Xx xxxxx používat xxxxxxx xxxxxxxx xxxxxx x xxxxx xxxxxxxxx xxxxxxxxx xxxxx. Xxxxxx xxxx xxx nullipary x xxxxx xxx xxxxx. Podávání xxxxx xx xxxx xxxxx xx xxxxxxxx xx xxxxxxx x x xxxxxx xxxxxxx xxxxx, xxx xxxxxxx dosáhnou xxxx 9 xxxxx.
Xx xxxxxxx xxxxxx by xxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx (xxx xxxxx pohlaví zvlášť) xxxxxxxxx ± 20 % xxxxxxx xxxxxxx.
Xxxxx xx xxxx studie xxxxxxx jako xxxxxxxxx xxxxx před xxxxxxxxxxx xxxxxx, xx xxxxx x obou xxxxxxxx xxxxxx zvířata xxxxxxxx xxxxx x xx xxxxxxxx xxxxxx.
1.2.2.2 Xxxxx x xxxxxxx
Xxx každou xxxxxxx xxxxx se xxxxxxx xxxxxxx 10 xxxxxx (5 samic x 5 xxxxx). Xxxxx se zvířata xxxxx xxxxxxx v xxxxxxx xxxxxx, xx xxxxx xxxxxx celkový xxxxx xxxxxx x xxxxx zvířat, xxxxx xxxxx zabita xxxx xxxxxx xxxxxx.
Xxxx to xx xxxxx podávat xxxxx skupině (satelitní xxxxxxx) 10 xxxxxx (5 zvířat xxxxxxx xxxxxxx) xx xxxx 28 xxx xxxxxxxx xxxxx x xxxxx xxxxxxxxxxxxx 14 xxx xx xxxxxxxx xxxxxxxx xxxxxxxx, xxxxxx xxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxx. Používá se xxxx xxxxxxxxx xxxxxxx 10 xxxxxxxxxxx xxxxxx (5 xxxxxx každého xxxxxxx).
1.2.2.3 Xxxxx xxxxx
Xx xxxxx použít xxxxxxx xxx xxxxxx xxxxx x jednu kontrolní xxxxxxx. S xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xx zachází xx xxxxxxx v kontrolní xxxxxxx xxxxxx xxxx x pokusnými. Xxxxxxx-xx xx vehikulum xxx xxxxxxxxx aplikace, podává xx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx jako xxxxxxxx xxxxxxxx, a xx xx xxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxxx, které xx xxxxxxxx xxxxxxxx xxxxx.
Xxxxx xx xxxxx xxxxxxxxxx xxxxxxxxx nedá xxxxxxxx xxxxxx při xxxxx xxxxx 1000 xx.xx-1 xxxxxxx xxxxxxxxx, je xxxxx xxxxxxx xxxxxxx xxxx. Xxxxxx-xx xxxxxx xxxx k xxxxxxxxx, xxx provést xxxxxxxxxx xxxxxxxxxxx xxxxxx xx xxxxxx xxxxxxxxx dávek.
Při xxxxxx dávek xx xxxxx xxxx x xxxxx xxxxxxx xxxxxxxxxx xxxxx x xxxxxxxxxxxxxxx x toxikokinetických xxxxxx x xxxxxxxxx látce, xxxxxxxx látkách xxxxxxxxxx.
Xxxxxxxx xxxxxx xxxxx xx xxxxxxx xxxxxxx xxxxxx, xxx nezpůsobit xxxxx xxxxxxx xxx xxxxx xxxxxxx. Xxxx xx xxxxxxx dávky v xxxxxxxxx xxxx xxx, xxx umožnily xxxxxxxx xxxxxxxxx xxxxxx na xxxxx. Nejnižší xxxxxx xxxxx xx xxxxxx xxxxxxx xxxxx xxxxxxxx xxxxxxxx (NOAEL). Xxxxxxx xx vhodný xxxx- xx xxxxxxxxxxx xxxxxx xxxx xxxxxxxxxx xxxxxxx; xxxxx xx xxxxxxx xxxxxx větší xxxxxx xxxxx, je xxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxxx, než xxxxxx xxxxxx xxxxx xxxxxx xxxx xxxxxxx (xxxx. xxxxxx xxxxx než 10).
Xxxxx se testovaná xxxxx podává x xxxxxxx nebo pitné xxxx, xx důležité xxxxxxxx, xxx xxxxxxxx xxxxxxxx látky xxxxxxxxxxxxx xxxxxx a vodní xxxxxxxxx. Xxxxxx-xx xx xxxxxxxxx látka x xxxxxxx, xxxx xx xxxxxx xxx' xxxxxxxxxx xxxxxxxxxxx (v xxx) xxxx xxxxxxxxxx dávkování xx vztahu x xxxxxxx hmotnosti zvířete; xxxxxxxx xxxxxxxxxxx xx xxxxx xxxxx. Xxxxxxxx-xx xx xxxxx sondou, xxxx xx se xxx dít xxxxx xxx xx xxxxxxx xxxx, a xxxxxxxxx xxxxxxxxxxxxx změnám xxxxxxx xxxxxxxxx xxxxxxx.
Xxxxx xx xxxx xxxxxx sloužit xxxx xxxxxxxxx xxxxx xxxx dlouhodobou xxxxxx, xx xxxxx x xxxx xxxxxxxx xxxxxx xxxxxx xxxxxxx.
1.2.2.4 Xxxxxxx xxxx
Xxxxxxxxx-xx test xxxxxxxxx xxx popisovaným xxxxxxxx xxxxx toxické účinky xxx dávce 1000 xx.xx-1 tělesné hmotnosti xx den xxxx xxx xxxxxx koncentraci x xxxxxxx xxxx xxxx, xxxxx xxxx xxxxx odpovídá, x xxxxx toxicita xxxxxxxxx xxxxx nevyplývá z xxxxxxxx x xxxxxxxxxx xxxxxxx, xx xxxxx xx provedení xxxxxxxxxxx xxxxxxxxx xxx xxxxx xxxxxxxxx úrovních xxxxxxx. Xxxx xxxxxxxx xxxxxxxxx xxxxx platí, xxxxx xxxxx x xxxxxxxx xxxx xxxxxxxxxxx, že xx xxxxx testovat xxx vyšších xxxxxxx.
1.2.2.5 Xxxx pozorováni
Doba xxxxxxxxxx xx 28 dní. Xxxxxxx satelitní xxxxxxx xxxx xxxxxxxxxx xxxxxxx xxxxxxx 14 xxx xxx xxxxxxxx x xxxxx xxxxxxxx případné xxxxxxxx účinky x xxx posouzení přetrvávání xxxx vratnosti xxxxxx.
1.2.3 Xxxxx xxxxxxx
Xxxxxxxx xx xxxxxx xxxxxxxxx látka 7 xxx x xxxxx xx dobu 28 dnů, ve xxxxxxxxxxxx případech 5 xxx v xxxxx. Xxxxx xxxxx xx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxx. Xxxxxxxxx xxxxx tekutiny, xxxxx xxxx xxx xxxxx xxxxxxxx, xxxxxx xx xxxxxxxxx xxxxxxx. Xxxxx xx xxxxx xxxxxxxx xxxxxxxxxx 1 xx xx 100 x xxxxxxx xxxxxxxxx, x xxxxxxx xxxxxxx xxxxxxx xxx podat x 2 ml na 100 x tělesné xxxxxxxxx. Xxxxxxx x xxxxxxxxx objemu je xxxxx minimalizovat xxxxxxxxx xxxxxxxxxxx xxx, xxx xxx xxxxxxx xxx xxxxx na xxxxx xxxxxxxx dávky. Neplatí xx x látek xxxxxxxxxx a xxxxxxxxx, x xxxxxxx xx xxxxx obvykle xxxxxxx xx stupňovanými xxxxxx xxx xxxxxxx xxxxxxxxxxxxx.
1.2.3.1 Xxxxxxxxx pozorování
Všeobecné klinické xxxxxxxxxx xx provádí xxxxxxx xxxxxx denně, xxxxxxx v xxxxx xxxxx dobu x x uvážením doby xxxxxxxxxxx maxima xxxxxx xx xxxxxxxx. Xxxxxxxxxxx xx xxxxxxxxx stav xxxxxx. Xxxxxxx xxxxxxx xxxxx xx provede xxxxxx xxxxxxxxx xxxxx xxxxxx xx účelem xxxxxxxx xxxxxxxxx a xxxxxxxxx. Zvířata x xxxxxx x xxxxxxx xxxxxxxxxxx xxxxxx bolest xxxx utrpení xxxx xxxxxxxx, utracena xxxxxxxx xxxxxxxx x xxxxxxx.
Xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxx se xxxxxxx xxxx xxxxx xxxxxxxx (xx účelem xxxxxxxxxxxxxxxxxxx xxxxxxxxx) x xxxx xxxxxxx xxxxxx týdně. Xxxx pozorování xx xxxx mimo chovnou xxxx v standardním xxxxxxxxxxx prostoru x xxxxxxx pokaždé ve xxxxxxx denní dobu. Xxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxxxxxxxx, xxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxx, standardizovaného x xxxxxxxxx xxxxxxxxxx. Xx xxxxx zajistit, aby xx podmínky pozorování xxxxxx co xxxxxxx; xxxxx, xxxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxx xxxx xxxxxxxxxxx xxxxxx xx dávkových xxxxxx.
Xxxxxxxxxx xxxxxxxx xxxxx xxxx, xxxxx, xxx x xxxxxxx, xxxxxxxxxx sekretů x exkretů, xxxxx xxxxxxx x xxxxxxxxxxxxx xxxxxx (xxxxxx, xxxxxxx xxxxx, velikost xxxxxx) x xxxxxxxx další. Xxxxxxxxxxxxx se xxxxx xxxxx, polohy, xxxx xxxxxx xx manipulaci, xxxxxxxxxx xxxxxxxxxx x xxxxxxxxx pohybů, xxxxxxxxxx x xxxxxxx (vytrvalé xxxxxxx xxxxxx nebo xxxxxxxx) nebo xxxxxxxxx xxxxxx xxxxxxx (např. xxxxxxxxxxxxxxx, xxxxx xxxxxx).
Xx xxxxxxx xxxxx aplikace xx xxxxxxxx xxxxxx xx xxxxx xxxxxxxxxx xxxxxxx (xxxx. xxxxxxxx, xxxxxxx, xxxxxxxxxxxxxxx), xxxxx xx síla xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx. Xxxxx xxxxxxxx xxxxxxxxx x postupech, xxxxx je xxxxx x xxxxxxxxx použít, xxxx xxxxxxx x xxxxxxxxxx (viz Všeobecný xxxx, xxxx X).
Xxxxxxxxxx xxxxxxxxx poruch xx xxxxxxx xxxxx xxxxxxxx xxx xxxxxxxx vynechat, xxxxx 28denní xxxxxx xxxxxx jako xxxxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxx subchronickou (90xxxxx); x xxx případě xx pozorování funkčních xxxxxx zařazeno do xxxx dlouhodobé xxxxxx. Xxxxx x x xxxxx případě xxxx xxxxx x xxxxxxxxx xxxxxxxxx ve čtvrtém xxxxx 28xxxxx xxxxxx xxxxxxx xxxxxxxxxxx pro xxxxx xxxxx pro xxxxxxxxxxxxx xxxxxx.
Xxxxxxxxx xxx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx x xxxxxx xxxxxxxxxxxx takové xxxxxxxx xxxxxxxx, které xx xxx posuzování funkčního xxxxx zvířete vadily.
1.2.3.2 Xxxxxxx xxxxxxxx a xxxxxx xxxxxxx x xxxx
Xxxxxxx se xxxx xxxxxxx xxxxxx xxxxx. Xxxxxxxx xxxxxxx x xxxx se xxxx xxxxxxx jednou xxxxx, xxxx x xxxxxxx xxxxxxxx v xxxxx xxxx.
1.2.3.3 Xxxxxxxxxxx
Xxxxxxxxxxxxx xxxxxxxxx xx xxxxx xxxxxx xxxxxxxx xxxxxxxxx hematokritu, xxxxxxxxxxx hemoglobinu, xxxxx xxxxxxxxxx, celkového x xxxxxxxxxxxxxxx xxxxx xxxxxxxxx, xxxxx xxxxxxxxxx x xxxxxxx srážlivosti xxxx.
Xxxx xx xxxxxxx xxxxx xxxx xxxx x xxxxxxx xxxxxxxx zvířete, xxxxx, xxxxx se xxxx xxxxxxxx, xx xxxxxxxxx. Xxxx xx xxxxxxxx xx xxxxxxxx xxxxxxxx.
1.2.3.4 Biochemická xxxxxxx
Xxxxxxxxxxx xxxxxxx xxxx xx xxxxxx posouzení xxxxxxxxx xxxxxxxxx účinků xx xxxxx, zvláště na xxxxx x xxxxxxx, xx provede x xxxxx xxxxxx těsně xxxx xxxx x xxxxxxx utracení (xxxxx xxxxxx xxxxxxxxx xxxx xxxxxxxxxx xxxxx xxxxxx). Xxxxxxxxxx se xxxxxx xxxxxxx bez potravy xxxx xxx před xxxxxxx xxxx. Vyšetření xxxxxxx xx žádoucí xxx xxxx měření x xxxx a xxxxxx, xxxxxxx pro xxxxxxx. Xxxxxx xxxxx xxx xxxx doporučení xx xx, že x xxxxxxxxxxxxxxx xxxxxx xx vyšší xxxxxxxxxxx xxxxxxxx, xxxxx xx xxxxx xxxxxxxx jemné xxxxx a xxxxxx xxxxxxxxxxxx. Xx xxxxx xxxxxx, xxxxxxxxx přes xxx by xxxxx xxx xxxx xx xxxxxxx xxxxxxxxxxxx a x aplikace x xxxxxxx xx xxxxxxx xx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx látce. Xxxxx xx odebírá xxxx xxxxxxx, xx xxxxx xxxxxxxxxxx xxxxxxxxx provést xx po xxxxxxxxxx xxxxxxxxx poruch ve 4. xxxxx testu.
Vyšetření xxxxxx a séra xxxxxxxx stanovení xxxxxx, xxxxxxxx, glukózy, celkového xxxxxxxxxxxx, xxxxxxxx, xxxxxxxxxx, xxxxxxxxx proteinů, xxxxxxxx, xxxxxxxx xxxxxxx xxxx xxxxxx xxxxxxxxxxxx účinky xx xxxxxxx xxxxx ( xxxx xxxxxxxxxxxxxxxxxxxxxx, xxxxxxxxxxxxxxxxxxxxxxxx, alkalická fosfatáza, xxxx xxxxxxxxxxxxxxxxxxxxxx, xxxxxxxxxxxxxxxxxxxxx). Xxxxxxx dalších xxxxxx (xxxxxxxxx xxxx jiného xxxxxx) x xxxxxxxxx xxxxxxx může x xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx.
Xxxxx možnost xx časově definovaný xxxx a xxxxxxxxx xxxx během posledního xxxxx studie: xxxxxxxx xx možno vzhled, xxxxx, osmolalitu xxxx xxxxxxxxxxx xxxxxxxx, xX, xxxxxxxxx, xxxxxxx x xxxx příp. xxxxxxx.
Xxxx xx xxxxx xxxxxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx x xxxx.
Xxxxx xxxxxxxxxxxxxxx xx xxxxx xxxxxxxx x xxxxx xxxxxxx nebo xxxxxxxxxxx z xxxxxxxx xx určité metabolické xxxxxx: xxxxxxxxx xxxxxxx, xxxxxxx, triglyceridů xxxxxxx, xxxxxx, xxxxxxxxxxxx hormonů, xxxxxxxxxxxxxx, xxxxxxxx cholinesterázy. Xxxxxxxx xxxxxx xxxxxxxxx xx xxxxxxxx xxxxx xxxxxxxxxxxx do xxxxxxxx xxxxxx xxxxx nebo xxxxxx od xxxxxxx.
Xxxxxx xx xxxxx xxxxxxxxxx xxxxxx, xxxx x xxxxx použitý xxxxxxxxx xxxx a pozorované xxxx xxxxxxxxx účinky xxxx xxxxx.
Xxxxx xxxxxx x dispozici xxxxx x normálních xxxxxxxxx xxxxxxxxx hematologických xxxx xxxxxxxxxxxxx xxxxxxxxxx, xx xxxxx uvážit xxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxx studie.
1.2.3.5 Pitva
U xxxxx zvířat použitých xx xxxxxx xx xxxxxxx xxxxx, xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxx, všech xxxxxx, dutiny xxxxx, xxxxxx x xxxxxx x xxxxxx xxxxxx. Xxxxx, xxxxxxx, xxxxxxxxxx, xxxxxxx, xxxxxxxxxx, xxxxx, xxxxxxx, xxxxx a xxxxx všech xxxxxx xx řádně očistí xx xxxxxxxx xxxxx x xx xxxxxxxx xx xxxxx xx xxxxx ve vlhkém xxxxx, xxx xx xxxxxxxx vysychání.
Následující tkáně xx xxxxx přechovávat xx xxxxxxx xxxxx x xxxxxxx xx xxx xxxxx x xxxxxxxxx xxxxxxxx histopatologická xxxxxxxxx: xxxxxxx xxxxx x xxxxxxxxxxxxxxx xxxxxxx, xxxxx (xxxxxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxx, xxxxxxx x mostu), míchu, xxxxxxx, tenké i xxxxxx xxxxxx (xxxxxx Xxxxxxxxxx xxxxx), xxxxx, xxxxxxx, nadledvinky, slezinu, xxxxx, xxxxxx, xxxxxxx xxxxx, xxxxxxxxxx x xxxxx (konzervované xxxxxxxxx xxxxxxxx xxxxxxxx x xxx xxxxxxxxx), xxxxxx x xxxxxxxx xxxxxxxx xxxxxx (xxxx. xxxxxx, xxxxxxxx), xxxxxx xxxxxx, xxxxxxxxxx uzliny (xxxxxxxxxx xxxxx pro oblast xxxxxxxx a xxxxx xxxxxxxx pro xxxxxxx xxxxxxxxxxx xxxxxx), xxxxxxxxx xxxx (n. xxxxxxxxxxx xxxx n. tibialis), xxxxxxx x xxxxxxxxx xxxxx, xxx kostní xxxxx (xxxx xxxxxxx xxxxx x xxxxxx xxxxxx dřeně). Xxxxx xxxxxxxxxx xxxx jiných xxxxxx xx možno xxxxxx x xxxxx xxxxx. Xxxxx orgán, xxxxx by mohl xxx xxxxxxx orgánem xxx xxxxxxxx xxxxxxxxx xxxxx, je xxxxx xxxxxxx.
1.2.3.6 Xxxxxxxxxxxxxxxx xxxxxxxxx
X xxxxx zvířat xxxxxxx, xxxxx xxxx xxxxxx xxxxxxxx xxxxx, x x zvířat xxxxxxxxx xxxxxxx xx xxxxx xxxxxxx xxxxxxxxxxxx vyšetření xxxxxxxxxx orgánů x xxxxx. Xxxxx xx x xxxxxxxx a xxxxxxx xx xxxxxxx x xxxxxxxx dávkou xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx, je xxxxx xxxxxxx histologické xxxxxxxxx xxxxxx xxxxx x x všech xxxxxx x nižšími xxxxxxx.
Xxxxxxx xxxxxxxxxxxxx léze xx xxxxx xxxxxxxx.
X xxxxxx xxxxxxxxxxx skupin, xxxxx xxxx xx xxxxxx xxxxxxxx, xx xxxxx provést xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxx xx orgány x tkáně, xx xxxxxxx xx xxxxxxxx xxxxxx otravy x xxxxxxxxx xxxxxxxxxxxx xxxxxx.
2 XXXX X XXXXXX XXXXX
X dispozici xxxx xxx xxxxx o xxxxxx xxxxxxxxxxx zvířeti. Xxxxx xxxx xxxxxxx xxxxx xxxxxxxxxxxx do xxxxxxxxx formy, uvádějící x každé testované xxxxxxx počet xxxxxxxxx xxxxxx, xxxxx xxxxxx xxxxxxxxxxxx příznaky xxxxxxxx, xxxxx zvířat xxxxxxxxx x xxxxxxx xxxxx xxxx xxxxxxxxxx x xxxxxxxxx xxxxxx, dobu xxxxx xxxxxxxxxxxx xxxxxx, xxxxx xxxxxxxxx příznaků xxxxxx doby nástupu, xxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxxxxxxxx léze, xxx xxxx x xxxxxxxx zvířat s xxxxxxxxxxxx typy xxxx.
Xxxxxxxx x číselné xxxxx xx xxxxx vyhodnotit xxxxxxx x xxxxxxxxx xxxxxxxxxxxx xxxxxxx. Xxxxxxxxxxxx xxxxxx xx třeba xxxxxx xxx xxx xxxxxxxxx studie.
3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX X ZÁVĚREČNÁ XXXXXX
X xxxxxxx s xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx x x xxxxxxx pokusu xx xxxxx vést protokol.
Zpráva x xxxxxx xxxxxxxx xxxx xxxxxxxxx, xxxxx xxxxx být xxxxxxx:
Xxxxxxx xxxxxxx:
- živočišný xxxx/xxxx;
- xxxxx, stáří a xxxxxxx xxxxxx;
- xxxxx, xxxxxxxx xxxxx, xxxxxxx xxx.;
- hmotnost xxxxxxxxxxxx xxxxxx xx xxxxxxx xxxxx, dále x xxxxxxxxx xxxxxxxxxxx a xx xxxxx testu.
Podmínky xxxxxxxxx.
- zdůvodnění výběru xxxxxxxx, xxxxx je xxxx xxx voda;
- xxxxxxxxxx xxxxxx dávek;
- xxxxxxxx údaje x xxxxxx xxxxxxxxx xxxxx xxx xxxxxxxx, případně x xxxxxxxx xxxxx, x xxxxxxxxxx xxxxxxxxxxxxx, xxxxxxxxx x homogenitě xxxxxxxxx;
- podrobné xxxxx x xxxxxxx xxxxxxxx xxxxxxxxx xxxxx;
- xxxxxxxx x koncentrace xxxxx x xxxxx xxxx xxxx (xxx) xx xxxxxxxxx denní dávku x xx xx xx xxxxxxx hmotnosti (xxxxx xxx o xxxxxxxx x dietě xxxx xxxx);
- podrobné xxxxx x xxxxxxx x kvalitě vody (xxxxxx xxxxx x xxxxxx);
Xxxxxxxx:
- xxxxxxx hmotnost x xxxx xxxxx;
- xxxxxxxx xxxxxxx x xxxx;
- údaje x xxxxxxxxx xxxxxxxx podle xxxxxxx x dávkové xxxxxx, včetně xxxxxx xxxxxxxx xxxxxxxx;
- xxxxxx, xxxxxxxxx x xxxxxx xxxxxxxxxx xxxxxx, příp. xxx jsou xxxxxx xxxx xxxxxxxx;
- posouzení xxxxxxxxxx xx xxxxxxxx xxxxxxx, úchopové xxxx x xxxxxxxxx xxxxxxxx;
- xxxxxxxx hematologického xxxxxxxxx x xxxxxxxxxxx normami;
- xxxxxxxx biochemického xxxxxxxxx x xxxxxxxxxxx normami;
- xxxxxxx hmotnost při xxxxxxxx x hmotnosti xxxxxx; - xxxxxxx xxxxxx;
- podrobný xxxxx xxxxx histopatologických xxxxxx;
- xxxxx x absorpci, xxxxx xxxx xxxxxxx;
- xxxxxxxxxxx zpracování xxxxxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.8 XXXXXXXXX TOXICITA XXXXXXXXX (28DENNÍ OPAKOVANÁ XXXXXXXX)
1 METODA je x xxxxxxx x xxxxxx Evropských xxxxxxxxxxxx.
2)1.1 Xxxx
Xxxx pokusem xx xxxxx xxxxxx xxxxx x xxxxxxxxx xxxxx: xxxxxxxxx velikosti částic, xxxxx xxx, xxx xxxx, bod varu, xxx xxxxxxxxx x xxxxxxxxx (jsou-li xxxxxxxxxxxx).
1.2 Xxxxxxx xxxxxx
Xxxxxxx skupin xxxxxxxxx xxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxx xxxxx po xxxxxxx xxxx, v xxxxxxxxxxxxxx xxxxxxxxxxxxx, xxxxx skupina xxxxx xxxxxxxxxxx, x xx po 28 xxx. Použije-li xx xxx dosažení xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx x atmosféře xxxxxxxxx, xx třeba xxxxxx xxxxxxxxx xxxxxxx pro xxxxxxxxx. Xxxxx xxxxxx xxxxxx xx zvířata xxxxx xxxxxxxx x xxxxxxxx xx xxxxxxxx xxxxxxxxx účinků. Xxxxxxx, xxxxx během pokusu xxxxxx, i xx, xxxxx xxxxxxx xx xxxxx pokusu, xx xxxxxxx.
1.3 Popis metody
1.3.1 Xxxxxxxx
Xxxxx xx xxxxx, xxxxx xx x xxxxxxxxx xxxxx vhodné xxxxxxxxx xxx, aby x xxxxxxx xxxxxxx xxxxxxxxx koncentrace xxxxxxxxx xxxxx. Xxxxx xx xxxxx xxx xxxxxxxxx xxxxxxxx vehikulum xxxx xxxx xxxxxxx, xxxx xxx x nich xxxxx, xx nemají xxxxxxx xxxxxx. Xxxxxxxx-xx xxxxxx historická xxxx, xx možno je xxxxxx.
1.3.2 Xxxxxxxxxxxxxx xxxxxxxx
1.3.2.1 Xxxxxxx xxxxxxx
Xxxxxxx zvířata xxxx vybrána x xxxxxxx xx xxxx, xxxxxxx x xxxxx x xxxxxxx x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) a xxxxxxxx tak, xxx xxxx možná xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxx stanoví
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10) X xxxxxxxx xx xxxxxxxxxxxxx xxxxxxx, xxxxxx-xx xxxxx důvody xxxxx xxxxxx xxxxxxx. Xxxxxxx xx mladá xxxxxx xxxxxxx x xxxxx xxxxxxxxx pokusných xxxxx. Xx xxxxxxx studie xxxx variační xxxxxxx xxxxxxxxx xxxxxx překročit ± 20 % xxxxxxx xxxxxxx (xxx xxxxx xxxxxxx zvlášť).
1.3.2.2 Xxxxx a pohlaví
Pro xxxxxx testovanou skupinu xx xxxxx xxxxxx xxxxxxx 10 zvířat (5 samic x 5 xxxxx). Xxxxxx xxxx xxx nullipary x xxxxx být xxxxx. Xxxxx xx xxxxxxx usmrcování zvířat x průběhu studie, xx nutno xxxxxx xxxxxxx xxxxx xxxxxx x xxxxx zvířat, xxxxx xxxxx usmrcena xxxx xxxxxx pokusu. Xxxxxx xx xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx skupinu 10 xxxxxx (5 zvířat xxxxxxx pohlaví) xx xxxx 28 xxx x xxxxx xxxxxxxxxxxxx 14 dnů xxxxxxxx xxxxxxxx, xxxxxxxxxxx nebo xxxxxxxx xxxxxx xxxxxxxxx xxxxxx. Xxxxxxx xx xxxx xxxxxxxxx xxxxxxx 10 xxxxxxxxxxx xxxxxx (5 xxxxxx xxxxxxx xxxxxxx).
1.3.2.3 Xxxxxxxxx xxxxxxxxxxx
Xxxxxxx xx xxxxxxx xxx xxxxxxx x xxxxxx xxxxxx koncentrace x xxxxx xxxxxxxxx xxxxxxx, xxxxxxxx xxxxxxxxx xxxxxxx x vehikulem - xxxxx xx xxxxx - x koncentraci xxxxxx jako x xxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxx látky. X xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xx xx zvířaty x xxxxxxxxx skupině xxxxxxx xxxxxx xxxx s xxxxxxxxx. Xxxxxxxx koncentrace xx xxxxxxx toxické xxxxxx, xxx nezpůsobit xxxxx uhynutí nebo xxx v malém xxxxx. Xxxxxxxx xxxxxxxxxxx xx neměla vyvolat xxxxx příznaky xxxxxxxx. Xxxxx xxxxxxxx xxxxxx xxxxxxxx x člověka, xx nejnižší xxxxxxxxxxx xxxx hodnotu xxxxxxxxxxx. Xxxxxxx by střední xxxxxxxxxxx xxxx vyvolat xxxxxxx xxxxxx xx xxxxxxxxx zjistitelnosti. Aplikují-li xx xxxx než 3 úrovně xxxxxxxxxxx, xxxx xxx voleny xxx, aby vyvolaly xxxxxxxxxxxx xxxxxxx xxxxxx. Xx xxxxxxxxx x xxxxxx x xxxxxxx xxxxxxxxxxx x x xxxxxxxxx xxxxxxx by xxxxx uhynutí xxx xxx xxxxx, jinak xx xxxxxxxxxxx výsledků xxxxxxx.
1.3.2.4 Xxxxxx xxxxxxxx
Xxxxxx xxxxxxxx xx xxx 6 xxxxx xxxxx; x xxxxxxx specifických xxxxxxxxx xx xxxxx xxxxxx x jiných xxx expozice.
1.3.2.5 Expoziční xxxxxxxx
Xxx pokusy se xxxxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxx xxxxxxxx xxxxxxxx xxxxxxx x xxxxxxx xxxxxxx 12xxxx xx xxxxxx, xxx xxx xxxxxxx xxxxxxxxx xxxxx xxxxxxx a rovnoměrné xxxxxxxxx látky v xxxxxxxxx xxxxxxxxx. Xxxxxxx-xx xx expoziční xxx, xx třeba xx xxxxxxxxxxx tak, xxx xx xxxxxxxx co xxxxxxx xxxxxxxxxx zvířat x aby xxxxxxxxx xxxxxxxx testované xxxxx xxxx xx xxxxxxxx. Xxx xxxxxxxxx stability xxxxxxxxx x xxxxxxxxxx xxxx xx xxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxx přesáhnout 5% xxxxxx xxxx. Xx xxxxx použít xxxxxxxxx xxxxxxxx xxxxxx-xxxxxxx, samotné xxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx expozice; xxxxx xxx xxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxx látky xxxxxx cestami.
1.3.2.6 Doba xxxxxxxxxx
Xxxxxxx zvířata xx xxxxx denně xxxxxxxxx xxxxx xxxxxx xxxxxx xxxxxxxx x xxxxxxxx x zaznamenávat toxické xxxxxx. Je xxxxx xxxxxxxxxx dobu xxxxxxx x čas, xx xxxxxx se objeví x xxxx odezní xxxxxxx účinky.
1.3.3 Xxxxx xxxxxxx
Xxxxxxx xx xxxxxxxx xxxxxxxxx xxxxx xxxxx, 5 - 7 xxx x xxxxx, xx xxxx 28 xxx. Xxxxxxx v xxxxxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxx x xxxxxxxxxx pozorování, xxxx xxxxxxxxxx xxxxxxx 14 xxx xxx xxxxxxxx, x xxxxxxxxx zotavení x otravy xxxx xxxxxxxxxxx xxxxxxxxx účinků. Xxxxxxx xxxxx xxxxxxxxxxx xx být 22 °X ± 3 °X. Xxxxxxxxx vlhkost xx být xxxx 30 % x 70 %, x xxxxxxxx xxxxxxx, kde xx není možné (xxxx. xxxxxxxxxxx x xxxxxxxx). Udržování xxxxxxx xxxxxxxx xxxxxx xxxxxx (≤ 5mm xxxxxxx xxxxxxx) zabrání xxxxxxx xxxxxxxxx látky xx xxxxx. Xxxxx expozice xx xxxxxxxx potrava xxx xxxx.
Xxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxx x vhodnou xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx. Xxxxxxxxxx xx xxxxxxx xxxxxxxxx xxxxx xxx xxxxxxx xxxxxxxxxx xxxxxxxxxxx. Rychlost xxxxxxx xxxxxxx je xxxxx nastavit xxx, xxx xxxxxxxx x xxxxx expozičním boxu xxxx stejné. Systém xxxx zaručovat, xx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxx dosaženo xx xxxxxxxxxxx.
Xxxxxx nebo xxxxxxxxxxxx xxxxxxxx xxxxxxxx:
x) Měření xxxxxxx vzduchu (kontinuálně).
b) Xxxxxxxx koncentrace studované xxxxx xx xxxx x xxxxxxx xxxx. Xxxxx xxxxx xxxxxxxx xx xxxx xxxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxx x xxxx xxx ± 15%. X některých xxxxxx x xxxxxxxx, kde xxxx xxxxxx regulace xxxx xxxxx xxxxxxxxx, xx připouští xxxxx xxxxxx kolísání. Po xxxxx xxxx xxxxxx xxxxxxxxxxx mají xxx xxxxxxxxxxx xxx xxxxxxxx, xxx xx xx xxxxxxxxx možné. Xxxxx xx týká částic x xxxxxxxx, xxxx xx xxxxxxxxxx velikostí xxxxxx xxxxx x xxxxx xxxxxxxxx xxxxxxx.
x) Xxxxxxx x vlhkost xxxxxxx xxxxxxxxxxx.
Xxxxx expozice x xx jejím xxxxxxxx se xxxxxxxxxx xxxxxxxxx a zaznamenávají xxxxxxxxxxxx; xxxxx zvíře xx xxxx individuální xxxxxxxx. Všechna zvířata xx xxxxx xxxxx xxxxxxxxx xx xxxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxxxxx xxxxxx xxxxxx, xxxxxx a trvání. Xxxxxxxxxx zahrnuje změny xxxx, xxxxx, xxx, xxxxxxx, xxxxxxx a xxxxxxxx xxxxx, xxxxx xxxxxx autonomní a xxxxxxxxx xxxxxxx xxxxxxxx, xxxxxxxxxxxxxxx aktivity x xxxxxxx. Xxxxxxxxx zvířat xx zaznamenávají xxxxx. Xxxxxxxxxx xx zaznamenávat xxxxx x spotřebu xxxxxxx. Xx xxxxx xxxxxxxx pravidelné prohlížení xxxxxx, aby xxxxx xxxxx xxxxxxxxxxx xx xxxxxxx xxxxxx xxxx xxxx. v xxxxxxxx xxxxxxxxxxx, xxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxxx.
Xx xxxxxxxx studie xx xxxxxxx xxxxxxx, xxxxx xxxxxxx, x výjimkou xxxxxxxxxxx skupin, xxxxxxx. Xxxxxxx x xxxxxx, xx xxxxxxx xxxxxx xx trpící xxxxxxx xx xxxxx xxxxxxxx xxxxxxx, xxxxxxx xxxxxxx x pitvat.
Na konci xxxxxx xx x xxxxx zvířat xxxxxx xxxxxxxxxxx provedou následující xxxxxxxxx:
1. Xxxxxxxxxxxxx xxxxxxxxx xx zahrnovat xxxxxxx xxxxxxxxx xxxxxxxxxxx, koncentrace xxxxxxxxxxx, počtu xxxxxxxxxx, xxxxxxxxx x diferenciálního xxxxx xxxxxxxxx x xxxxxxxxxxx xxxx.
2. Xxxxxxxxxxx xxxxxxx xxxx: x xxxxxxxxx xxxxxx xxxxx x xxxxxx xxxxxxxx xxxxxxx xxxxx x xxxxxx xxxxxxxxx: xxxxxxxxxxxxxxxxxxxxxx x xxxx (xxxxx xxxxx jako glutamát-pyruvát-transamináza), xxxxxxxxxxxxxxxxxxxxxxxx xxxx (xxxxx xxxxx jako xxxxxxxx-xxxxxxxxxx-xxxxxxxxxxxx), xxxxx močoviny, xxxxxxx, xxxxxxxxx, xxxxxxx bilirubin x celkové xxxxxxxxx x xxxx.
Xxxx xxxxx xxxxxxxxxxxxxxx, xxxxx xxxxx xxx xxxxxxxx xxx xxxxx xxxxxxxxxxxxx hodnocení, xxxxx xxxxxxxxx: vápníku, xxxxxxx, xxxxxxxx, xxxxxx, xxxxxxxx, xxxxxxx xxxxxxx, xxxxxx, xxxxxxx, acidobazické xxxxxxxxx, xxxxxxxxxxxxxx, xxxxxxxx xxxxxxxxxxxxxx.
Xxxxx biochemické analýzy xxxxx být x xxxxxxx potřeby xxxxxxx xxx xxxxxxx širšího xxxxxxx účinků.
1.3.3.1 Pitva
U xxxxx zvířat xxxxxxxxx xx studii xx xxxxxxx xxxxx. Xxxxx xxxxx, ledviny, xxxxxxxxxx, xxxxx x xxxxxxx xx xx xxxxxxxx xx xxxxx xxxxx xx xxxxxx xxxxx, xxx xx xxxxxxxx xxxxxxxxx. Xxxxxx x xxxxx (dýchací xxxxxx, xxxxx, ledviny, xxxxxxx, xxxxxxx, xxxxxxxxxx x xxxxx i všechny xxxxxx s xxxxxxxxxxxxxxx xxxxxxx xxxx xxxxxxx xxxxxxxxx) je třeba xxxxxxxxxxx xx xxxxxxx xxxxx x ohledem xx xxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx. Plíce je xxxxx vyjmout bez xxxxxxxxx, xxxxxx x xxxxxxx xxxxxxx mediem xxx, xxx xx xxxxxxxxx struktura.
1.3.3.2 Histopatologické xxxxxxxxx
X všech xxxxxx xxxxxxx, které byla xxxxxx xxxxxxxx xxxxxxxxxxx, x u xxxxxx xxxxxxxxx skupiny je xxxxx provést histologické xxxxxxxxx xxxxxxxxxx orgánů x xxxxx. Xxxxx xx x orgánech x xxxxxxx ve xxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx látkou, xx xxxxx xxxxxxx xxxxxxxxxxxx vyšetření xxxxxx xxxxx x x xxxxx xxxxxx s xxxxxxx dávkami. X xxxxxx xxxxxxxxxxx xxxxxx xx třeba provést xxxxxxxxxxxx vyšetření xx xxxxxxxxx xxxxxxx xx xxxxxx a tkáně, xx xxxxxxx xx xxxxxxxx xxxxxx xxxxxx x xxxxxxxxx xxxxxxxxxxxx xxxxxx.
2 ÚDAJE
Údaje xx xxxxxxx do xxxxxxx. X xx musí xxx pro každou xxxxxxxxxxxxxx xxxxxxx xxxxxx xxxxx zvířat xx xxxxxxx xxxxxx a xxxxx zvířat x xxxxxxxxxxxx formami xxxxxxxxx.
Xxxxxxx xxxxxxxx xxxxxxxx je xxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxx. Xx x xxxx možno xxxxxx kteroukoliv uznávanou xxxxxxxxxxxx xxxxxx.
3 PROJEKT XXXXXX, PROTOKOL POKUSU X ZÁVĚREČNÁ XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) musí xxx zpracován xxxxxxx xxxxxx x x xxxxxxx pokusu je xxxxx xxxx protokol.
Zpráva x xxxxxxx pokusu xxxxxxxx tyto x xxxxxxxxx
- xxxxxxxxx druh, xxxx, xxxxx, podmínky xxxxxxxx, xxxxxxx xxx.,
- xxxxxxxx xxxxxx:
- xxxxx xxxxxxxxxxx zařízení včetně xxxxxxxxxx, xxxx, xxxxxxx, xxxxxx xxxxxxx, xxxxxxx xxxxxxxx xxxxxx x xxxxxxxx, klimatizačního xxxxxxx, xxxxx xxxxxxx odpadního xxxxxxx x xxxxxxx xxxxxxxx zvířat v xxxx, pokud xx xxxxxxxx. Popsat xxxxxxxxx xxx xxxxxx xxxxxxx, xxxxxxxx xxxxxxx, xxxxxxxxx xxxxxxxxx koncentrací x xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx,
- xxxxx x xxxxxxxx xx xxxxxxx xx tabulky x xxxxxx xxxxx s xxxxxxxxxx hodnotami a xxxxxxxxxxxxxxxx xxxxxxxxxxx (xxxx. xxxxxxxxxxx xxxxxxxxx). Mají xxxxxxxxx xxxx xxxxx:
- xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx zařízením;
- teplota x xxxxxxx xxxxxxx;
- xxxxxxxxx xxxxxxxxxxx (xxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xx xxxxxxxxxxx xxxxxxxx, dělené xxxxxxx xxxxxxx);
- xxxxxx vehikula, xxxxx xxxx xxxxx;
- xxxxxxxx xxxxxxxxxxx x xxxxxxx zóně;
- xxxxxxxxxx xxxxxx xxxxxxxxxxxxxxx xxxxxxx (XXXX) x geometrická xxxxxxxxxx xxxxxxxx (XXX),
- xxxxx o xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx x xxxxx koncentrací,
- xxxx uhynutí xxxxx xxxxxxxxxxx, xxxxxxxx xxxx x přežití xxxxxx xx xxxxx xxxxxxxxx,
- xxxxx toxických xxxx xxxxxx xxxxxx,
- xxxxxx xxx xxxxxx,
- xxxx, xxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx příznaky, x xxxxxx xxxxx xxxxx,
- spotřeba xxxxxxx x xxxxx xxxxxxx xxxxxxxxx,
- xxxxxxxxxxxxx xxxxxxxxx x jejich xxxxxxxx,
- xxxxxxxxxxx vyšetření x xxxxxx xxxxxxxx,
- xxxxxxx xxxxxx,
- xxxxxxxx popis xxxxx histopatologických xxxxxx,
- xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx, xxx xx to xxxxx.
Xxxxxxx výsledků.
Závěry.
B.9 SUBAKUTNÍ XXXXXXXX XXXXXXXX (28DENNÍ XXXXXXXXX APLIKACE)
1 XXXXXX xx v xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
2)1.1 Princip xxxxxxxxx xxxxxx
Xxxxxxxxx látka xx xxxxxx xx xxxx xxxxx po 28 xxx x xxxxxxxxxxxxxx xxxxxxx několika xxxxxxxx xxxxxxxxx xxxxxx, x xx xxxxx xxxxxxx xxxxx xxxxxx xxxxx. Xxxxx období xxxxxxxx xx xxxxxxx xxxxx xxxxxxxx, xxx xx xxxxxxxx příznaky toxicity. Xxxxxxx, která uhynou xxxxx xxxxxx, x xxxxxxx, která přežijí xxxxx xxxxxx, xx xxxxxxx.
1.2 Popis metody
1.3 Xxxxxxxx
Xxxxxxx xxxxxxx xxxx xxxxxxx x ohledem xx xxxx, xxxxxxx x xxxxx x xxxxxxx x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x xxxxxxxx xxx, xxx xxxx xxxxx xxxxxxxxxxxx jednotlivých xxxxxx. Dobu navykání xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10) Krátce xxxx začátkem xxxxxx xx xxxxxxx srst xx zádech xxxxxxxxx xxxxxx. Xxxxxxxx xxxxx xx rovněž možné, xxxx xx se xxxx provést cca 24 xxxxx před xxxxxxxxxxxx. Ostříhání xxxx xxxxxxx xx xxxxxxx xxxxxxxx xxxxx xxxxx. Xxx xxxxxxxx xxxx xxxxxx xxxxx xx xxxxx xxxx xx xx, xxx xx xxxxxxxxxxx xxxx (např. xxxxxx). Xxx xxxxxxxx xx připraví xxxxxxx 10 % povrchu xxxx. Je xxxxx xxxx x xxxxx xxxxxxxx xxxxxx xxx xxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx xxxxxx kůže x x velikostí xxxxxxx xxxxxx. Xxx xxxxxxxx x xxxxxx xxxxxxx, xxxxx xxxxx xxx případně xxxxxxxx xx práškové xxxxx, xx xxxxx danou xxxxx dostatečně xxxxxxxx xxxxx, xxxxxxxx vhodným xxxxxxxxx, xxx xxx xxxxxxx xxxxx xxxxxxx x xxxx. Xxxxxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxx. Látka xx xxxxxx denně 5 až 7 xxx x týdnu.
1.4 Xxxxxxxxxxxxxx xxxxxxxx
1.4.1 Pokusná xxxxxxx
Xx možno používat xxxxxxx xxxxxxx, xxxxxxx xxxx xxxxxxx. Xx xxxxx xxxxxx i xxxx xxxxxxx xxxxx, xxxxxx xxxxxxx xxxx xxxx být xxxxxxxxxx. Xx xxxxxxx xxxxxx xx xxxxxx variační xxxxxxx xxxxxxxxx xxxxxx (xxx každé pohlaví xxxxxx) překročit ± 20 % xxxxxxx xxxxxxx.
1.4.1.1 Xxxxx a xxxxxxx
Xxx xxxxxx xxxxxxx xxxxx použít nejméně 10 xxxxxx (5 xxxxx x 5 xxxxx) se zdravou xxxx. Xxxxxx xxxx xxx xxxxxxxxx x xxxxx být březí. Xxxxx se plánuje xxxxxxxxxx xxxxxx x xxxxxxx xxxxxx, xx xxxxx xxxxxx xxxxxxx xxxxx xxxxxx o xxxxx xxxxxx, která xxxxx usmrcena xxxx xxxxxx xxxxxx. Xxxxxx xx možno podávat xxxxx xxxxxxx (xxxxxxxxx xxxxxxx) 10 xxxxxx (5 xxxxxx každého xxxxxxx) xx xxxx 28 xxx xxxxxxxx xxxxx x xxxxx xxxxxxxxxxxxx 14 dnů xx ukončení xxxxxxx xxxxxxxx vratnost, xxxxxx xxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxx. Xxxxxxx xx xxxx xxxxxxxxx xxxxxxx 10 xxxxxxxxxxx xxxxxx (5 xxxxxx xxxxxxx xxxxxxx).
1.4.1.2 Dávkování
Je xxxxx xxxxxx nejméně xxx xxxxxx dávek x jednu xxxxxxxxx xxxxxxx xxxx - xxxxx xx xxxxxxx xxxxxxxx - xxxxxxxxx xxxxxxx s xxxxxxxx xxxxxxxx. Doba expozice xx xxx xxxxxxx 6 xxxxx xxxxx. Xxxxxxxx xxxxxxxxx látky xx xx mělo xxxxxxxx xxxxx xxx xx xxxxxxx dobu. X xxxxxxxxxxx týdenních xxxx xxxxxxxxxxxxxxx xx xxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxxx xxx, xxx xx xxxxxxxxx stálá xxxxxxx xxxxx xx xxxxxx k xxxxxxx xxxxxxxxx zvířete. S xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xx xx xxxxxxx v kontrolní xxxxxxx zachází xxxxxx xxxx x xxxxxxxxx. Xxxxxxx-xx xx xxxxxxxxx xxx xxxxxxxxx xxxxxxxx, xxxxxx xx xxxxxxxxx xxxxxxx stejným xxxxxxxx xxxx xxxxxxxx xxxxxxxx, x to xx xxxxxxx množství, které xx xxxxxxxx skupině x nejvyšší dávkou. Xxxxxxxx xxxxx má xxxxxxx xxxxxxx xxxxxx, xxx xxxxxxxxxx xxxxx xxxxxxx nebo jen x malém počtu. Xxxxxxxx xxxxx xx xxxxxx vyvolat žádné xxxxxxxx xxxxxxxx. Pokud xxxxxxxx xxxxxx xxxxxxxx x xxxxxxx, má xxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxxxx. Xxxxxxx xx střední dávka xxxx xxxxxxx xxx xxxxxxx xxxxxx xx xxxxxxxxx zjistitelnosti. Aplikují-li xx xxxx xxx 3 úrovně xxxxx, xxxx xxx xxxxxxxxx xxxxx voleny xxx, xxx vyvolaly odstupňované xxxxxxx xxxxxx. Ve xxxxxxx s nízkou x xxxxxxx xxxxxx x v xxxxxxxxx xxxxxxx xx xxxxx xxxxxxx xxx xxx xxxxx, jinak xx xxxxxxxxxxx výsledků xxxxxxx.
Xxxx-xx xxxxxxxx testované xxxxx x xxxxxxx xxxxxxxxxx xxxx, je třeba xxxxxx xxxxxxxxxxx, xxx x vysoké dávkové xxxxxx xxxx vést x omezení nebo xxxxxxxxx ostatních xxxxxxxxx xxxxxx. Xxxxx-xx x xxxxxxx poškození kůže, xx xxxxxxx xx xxxxxxxx xxxxxxxxx xxxxx xxxxx xxxxxxx a xxxxxxx jej xxxxx x xxxxxxx xxxxxxxxxxxxx.
1.4.1.3 Xxxxxxx xxxx
Xxxxxxxx-xx při xxxxxxxxx xxxxxx xxxxxxxx xxxxx 1000 xx.xx-1 xxxx xxxxx xxxxx, xxxxx odpovídá xxxxx xxxxxxxx člověka, xxxxx xxxxxxx xxxxxx, xxxx xxxxx xxxxxxx xxxxx.
1.4.1.4 Xxxx xxxxxxxxxx
Xxxxxxx xxxxxxx xx xxxxx xxxxx xxxxxxxxx xx příznaky xxxxxx. Xx xxxxx xxxxxxxxxx xxxx xxxxxxx x dobu, xxx xx xxxxxx x xxxxxxxx xxxx xxxxxx xxxxxxxx xxxxxx.
1.4.2 Xxxxx xxxxxxx
Xxxxxxx xx xxxxxxx x klecích xx xxxxxx. Xxxxxxxx se xxxxxxxxx xxxxx xxxxxxx 7 dnů v xxxxx xx xxxx 28 dnů. Xxxxxxx xxxxxxxxx xxxxxxx, která xxxx určena pro xxxxxxxx pozorování, je xxxxx xxxxxx xx xxxxxxx 14 xxx xxx xxxxxxxx, aby xx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxx xxxxxx přetrvávání. Xxxx xxxxxxxx xxxx xxxxxxx 6 hodin xxxxx.
Xxxxxxxxxx xxxxx xx xxxxx nanášet xxxxxxxxxx xx xxxxx xxxxxx, xxxxx představuje xxx 10 % povrchu xxxx; u xxxxxx xxxxxxxxx látek může xxx xxxx xxxxxx xxxxx. Látkou je xxxxx xxxxxx xx xxxxxxxx část xxxxxxx xxxxxx rovnoměrně x xx xxxxxxxx vrstvě.
Testovaná xxxxx je xx xxxxxxxxx xxxx udržována x xxxxxxxx s xxxx xxxxxx porézního xxxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxx. Xxxxxxxxxx xxxxxx je xxxx xxxxx xxxxxxx xxxxxxxx xxxxxxx, aby xx xxxxxx obvaz x xxxxxxxxx xxxxx xxxxxxxx x xxx xx xxxxxxxxx xxxxxxxx xxxxxx. X zamezení xxxxxx xxxxx je xxxxx xxxxxx x xxxxxxxxxx xxx xxxxxxx xxxxxxxx xxxxxx, xxxxxx xxxxxxxxxxx xxxx xxxxx xxxxxxxxx. Xxxx xxxxxxxxxxxx metody xx xxxxx xxxxxx "xxxxxxxxxx xxxxx".
Xx uplynutí xxxx expozice xx xxxxxxxx xxxxxx xxxxxxxxx xxxxx, xxxxx xxxx x použitím xxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxx.
Xxxxxxx zvířata xx xxxxx xxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxx, xxxxxx a xxxxxx. Xxxxxxxxxx xxxxxxxx xxxxx xxxxx, xxxx, xxx x xxxxxxx, x také dýchání x xxxxxxxx xxxxx, xxxxx funkce xxxxxxxxx x centrální xxxxxxx xxxxxxxx, xxxxxxxxxxxxxxx aktivity x xxxxxxx. Hmotnosti xxxxxx se zaznamenávají xxxxx. Xxxxxxxxxx xx xxxxxxxxxxxx xxxxx x xxxxxxxx xxxxxxx. Xx xxxxx xxxxxxxx pravidelné xxxxxxxxxx xxxxxx, xxx xxxxx xxxxx nedocházelo xx xxxxxxx zvířat xxxx např. v xxxxxxxx xxxxxxxxxxx, xxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxxx. Xx xxxxxxxx xxxxxx xx všechna xxxxxxx, xxxxx přežila, x výjimkou satelitních xxxxxx, xxxxxxx. Xxxxxxx x agonii, x xxxxxx xxxxxx či xxxxxx bolestí je xxxxx xxxxxxxx vyřadit, xxxxxxx xxxxxxx x xxxxxx.
Xx konci xxxxxx xx u všech xxxxxx xxxxxx kontrolních xxxxxxxx xxxxxxxxxxx vyšetření:
1. Xxxxxxxxxxxxx vyšetření xx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxx, koncentrace hemoglobinu, xxxxx xxxxxxxxxx, xxxxxxxxx x xxxxxxxxxxxxxxx xxxxx xxxxxxxxx a xxxxxxxxxxx xxxx.
2. Xxxxxxxxxxx analýza xxxx: x posouzení xxxxxx jater x xxxxxx xxxxxxxx xxxxxxx xxxxx z xxxxxx xxxxxxxxx: xxxxxxxxxxxxxxxxxxxxxx v xxxx (xxxxx známá xxxx xxxxxxxx-xxxxxxx-xxxxxxxxxxxx), aspartátaminotransferáza xxxx (xxxxx xxxxxxxx-xxxxxxxxxx-xxxxxxxxxxxx), xxxxx močoviny, xxxxxxx, xxxxxxxxx, celkový bilirubin x xxxxxxx xxxxxxxxx x xxxx.
Xxxx xxxxx xxxxxxxxxxxxxxx, xxxxx xxxxx xxx xxxxxxxx xxx xxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx stanovení: xxxxxxx, xxxxxxx, xxxxxxxx, sodíku, xxxxxxxx, xxxxxxx xxxxxxx, xxxxxx, xxxxxxx, xxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxxxxxx, xxxxxxxx xxxxxxxxxxxxxx.
Xxxxx xxxxxxxxxxx xxxxxxx xxxxx xxx x xxxxxxx xxxxxxx použity xxx xxxxxxx xxxxxxx xxxxxxx účinků.
1.4.2.1 Xxxxx
X xxxxx xxxxxx xxxxxxxxx xx xxxxxx se xxxxxxx xxxxx. Aspoň xxxxx, xxxxxxx, nadledviny, xxxxx x xxxxxxx xx co xxxxxxxx xx sekci zváží xx xxxxxx xxxxx, xxx se xxxxxxxx xxxxxxxxx. Xxxxxx x xxxxx xxxx. xxxxxxxx x exponovaná xxxx, xxxxx, ledviny, xxxxxxx, xxxxxxx, nadledviny, xxxxx x xxxxxxx xxxxxx x xxxxxxxxxxxxxxx xxxxxx xxxx xxxxxxx velikosti) xx třeba xxxxxxxxxxx xx xxxxxxx xxxxx x ohledem xx xxxxxxxx xxxxxxxxxxxxxxxx vyšetření.
1.4.2.2 Xxxxxxxxxxxxxxxx vyšetřeni
U xxxxx xxxxxx xxxxxxx, xxxxx xxxx xxxxxx xxxxxxxx xxxxx, a x xxxxxx kontrolní xxxxxxx, xx xxxxx xxxxxxx xxxxxxxxxxxx vyšetřeni xxxxxxxxxx xxxxxx x xxxxx. Xxxxx se x xxxxxxxx x xxxxxxx xx xxxxxxx x xxxxxxxx dávkou, xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx, xx nutno xxxxxxx xxxxxxxxxxxx vyšetření xxxxxx xxxxx x x všech xxxxxx x xxxxxxx dávkami. X xxxxxx xxxxxxxxxxx xxxxxx je třeba xxxxxxx xxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx důrazem xx xxxxxx x xxxxx, xx xxxxxxx xx objevily xxxxxx xxxxxx x xxxxxxxxx xxxxxxxxxxxx xxxxxx.
2 XXXXX
Xxxxx xx xxxxxxx xx xxxxxxx. X ní xxxx xxx xxx xxxxxx xxxxxxxxxxxxxx skupinu xxxxxx xxxxx xxxxxx xx počátku xxxxxx x xxxxx xxxxxx x jednotlivými formami xxxxxxxxx.
Xxxxxxx zjištěné xxxxxxxx xx xxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxx. Xx k xxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxx.
3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX A ZÁVĚREČNÁ XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx předpisy
9) xxxx xxx zpracován xxxxxxx xxxxxx x x xxxxxxx xxxxxx xx xxxxx xxxx xxxxxxxx.
Xxxxxx x xxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxx:
- xxxxx o xxxxxxxxx (druh, kmen, xxxxx, podmínky xxxxx, xxxxxx atd.),
- xxxxxxxxxxxxxx xxxxxxxx ( xxxxxx xxxxx xxxxxx; xxxxxxxxx xxxx xxxxxxxxxxx),
- úrovně xxxxx (xxxxxx xxxxxxxx, xxxxx se xxxxxxx) x xxxxxxxxxxx,
- úroveň xxx xxxxxx, xxxxx xx xxx xxxxxxxx,
- xxxxx o xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx x xxxxx,
- xxxx xxxxxxx xxxxx xxxxxxxxxxx, xxxxxxxx xxxx x xxxxxxx xxxxxx do xxxxx sledování,
- xxxxxxx xxxx xxxx xxxxxx,
- xxxx, xxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx a xxxxxx xxxxx vývoj,
- xxxxxxxx xxxxxxx a xxxxx xxxxxxx xxxxxxxxx,
- xxxxxxxxxxxxx xxxxxxxxx a jejich xxxxxxxx,
- biochemická xxxxxxxxx x xxxxxx výsledky,
- xxxxxxx xxxxxx,
- xxxxxxxx xxxxx všech histopatologických xxxxxx,
- statistické xxxxxxxxxxx xxxxxxxx, kde je xx xxxxx.
Xxxxxxx.
Xxxxxx.
X.10 MUTAGENITA - TEST XXXXXXXXXXXXXX XXXXXXX X SAVČÍCH XXXXX XX XXXXX
1 XXXXXX xx x xxxxxxx x právem Xxxxxxxxxx xxxxxxxxxxxx.5)
1.1 Xxxx
Xxxxxx xxxxxxx chromozómových aberací xx xxxxx xx xxxxxx xxxxx, xxx x xxxxxxxxx savčích xxxxx způsobují strukturální xxxxxxxxxxxx aberace.5) Xxxxxxxxxxxx xxxxxxx xxxx xxxxxxx xxxxx: chromozómové a xxxxxxxxxxxx. Xxxxxxx vyvolané xxxxxxxxxx mutageny xxxx xxxxxxxx chromatidové, dochází xxxx xxx x xxxxxxxx xxxxxxxxxxxxxx xxxx. Xxxxx polyploidie může xxxxxxxxxx, xx xxxx xxxxxxxx látka xx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx. Tato xxxxxx xxxx xxxx xxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxx a xxxxx xx k tomuto xxxxx xxxxxxxxx. Xxxxxxxxxxxx xxxxxx x příbuzné xxxx jsou xxxxxxxx xxxx xxxxxxxxxxx xxxxxx x xxxxxxx a xxxxxxxx xxxxxxxxxxx xxxxxxx xxxx, že xxxxxxxxxxxx xxxxxx x xxxxxxxx xxxx, jež xxxxxxxxx xxxxx x xxxxxxxxxx x xxxxxxxxxxxxxxxxxx xxxxxx xxxxxxxxxxx buněk, xxxxx xxxxx při xxxxxx xxxxxxxx x xxxxxxx x xxxxxxxxxxxxxxxx xxxxxx.
Xxxxx xxxx xx xxxxxxx x xxxxxxxx xxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxxxx. Xxxx xxxxxxxxxx xxxxx, xxxxx xxxx x xxxxx testu xxxxxxxxx, xx xxxx xxx xxxxx xxxxxxxxxxxx, xxxx xxxx xxxxxxxxxx xxxxxxxx xxxx tímto xxxxxx a xxxxxxxxxxxxxx. Xxxx korelace xxxxxx xx xxxxx xxxxx x existuje xxxxx xxxx dokladů x xxx, že xxxxxxxx xxxxxxxx xxxxx, xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxx xxxxxx xxxxxxxx, xxxxxxx xxxxxx působí xxxxx xxxxxxxxxxx xxx xxxxxx xxxxxxxxxx XXX.
X xxxxxxx chromozómových xxxxxxx xx vitro xx xxxxx použít xxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx xxxxx, xxxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxx kultury. Xxxxxxx buňky xxxx xxxxxxx xx xxxxxxx xxxxxxxxxx xxxxx v xxxxxxx, xxxxxxxxx karyotypu, xxxxx xxxxxxxxxx, jejich xxxxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx.
Xxxxx xx vitro vyžadují xxxxxx xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx. Xxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx napodobit xxxxxxxx x xxxxx xx vivo. Je xxxxx xx xxxxxxxxx xxxxxxxx, xxxxx xx xxxxx xxxx x xxxxxxxxxx xxxxxxxxx, xxx xxxxxxxxxx xxxxxxx xxxxxxxxxx, xxxxx xxxx xxxxxxxxx xxxxxxx xX, xxxxxxxxxx xxxx xxxxxxx cytotoxicitou.5)
1.2 Xxxxxxxx
Xxxxxxx chromatidového xxxx: xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxx se projevuje xxxx zlom jedné, xxxxxxxx xxxx chromatid, xxxx xxxx x xxxxxxxx xxxxxxx xxxx xxxxxxxxxxxx.
Xxxxxxx chromozómového typu: xxxxxxxxxxxx poškození xxxxxxxxxx xxxxxxxxx xxxx xxxx xxxxxxxxxx jako xxxx x opětovné spojení xxxx xxxxxxxxx na xxxxxxx xxxxx (xxxxxxxx xxxx xxxxxxx typu xxxxxxxxxxx xxxxxxxxx, xxxxxxxxxx xxxxxxxxx-xxxx).
Xxxx xxxxxxxxxx: jako xxxx xxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx xxxx xxxx xxxxxxxxx xx xxxxxxxxxxx, xx xxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxx xx xxxxx, než xx xxxxx xxxxxxxxx xxxxxxxxxx. Xxxx pak x xxxxxxxxx, xxxxxxx (distální) xxxxxxxx x xxxxx xxxxx je xxxxxxxxxxx (xxxx mimo xxx xxxxxxxxxx), xxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xx xxxxxx v xxxxxxxx xxxxxx.
Xxxxxxxxxxxxxxx: xxxxxx, xxx xx X-xxxx xxxxxxxxx DNA nepřechází xxxxx do xxxxxx, xxxxx xxxxxx xxxxx X-xxxx. Xxxxxxxxx xxxx xxxxxxxxxx x 4, 8, 16, ... xxxxxxxxxxxx.
Xxx: xxxxxxxxxxxx xxxx xxxxx než šířka xxxxx xxxxxxxxxx x x xxxxxxxxxx vybočením xxxxxxxxx.
Xxxxxxxxx xxxxx: xxxxx xxxxx v xxxxxxxx xxxxxx xxxxxxxx xxxxxx xxxxx x xxxx xxxxxxxx xxxxx; xxxxx xxxxxx proliferace xxxx xxxxxxxx.
Xxxxxxxxx aberace: xxxxx xxxxx chromozómů xxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxxxxxxxx xxx xxxxxxx xxxxx.
Xxxxxxxxxxx: xxxxxxx haploidního počtu xxxxxxxxxx (n) xxxx xxx diploidní počet (xxxx 3x, 4x xxx.).
Xxxxxxxxxxxx xxxxxxx: xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx analýzou xxxxxxxxx xxxxxx xx stadiu xxxxxxxx, pozorovaná xxxx xxxxxx x fragmenty x xxxxxx.
1.3 Xxxxxxx xxxxxx
Xxxxxxx kultury xx xxxxxxx působení xxxxxxxxx xxxxx, x xx x xxxxxxxxxxxx aktivací x xxx xx. Xx xxxxxxxxxxx xxxxxxxxxxx xx expozici xxxxxxx xxxxxxx testované xxxxx, xx xxxxxxxx zastaví xxxxxxxxx Xxxxxxxxxx® xxxx xxxxxxxxxxx, buňky xx xxxxxx, obarví se x x xxxxxxxxxxxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxx.
1.4 Xxxxx xxxxxx
1.4.1 Příprava
1.4.1.1 Xxxxx
Xx xxxxx použít xxxxx xxxx xxxxxxxxx xxxxx, xxxxx nebo xxxxxxxxxx xxxxxxxxx xxxxxx, xxxxxx buněk xxxxxxxx (xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxx xx xxxxxx xxxxx).
1.4.1.2 Xxxxx x kultivační xxxxxxxx
X udržování xxxxxx xx třeba xxxxxxxx xxxxxx xxxxxxxxxx média x xxxxxxxxx xxxxxxxx (xxxxxxxxxx xxxxxx, xxxxxxxxxxx XX2, teplota x xxxxxxx). X xxxxxxxxx xxxxx x xxxxx xx xxxxx xxxxxx xxxxxxxx xxxxxxxxxxx stabilitu xxxxxxxxx xxxxx chromozómů x nepřítomnost xxxxxxxxxxx x buňkách. X xxxxxxx xxxxxxxxxxx xx xxxxx xxxxxxxxxxx. Xx xxxxx xxxx xxxxxxxx xxxx xxxxxxxxx cyklu x xxxxxxxxxx xxxxxxxx.
1.4.1.3 Xxxxxxxx xxxxxx
Xxxxxxxxxxxxx buněčné xxxxx a xxxxx: xxxxx xx xxxxx xx xxxxxxxxx xxxxxx xxxxxxx xx xxxxxxxxxxxx xxxxx v xxxxxx xxxxxxx, aby xxxxxxx xxxxxxxxx xxxxxxxxxxx vrstvy xxxx dobou xxxxxxxx x inkubují xx xxx xxxxxxx 37 °X.
Xxxxxxxxx: xx kultivačnímu xxxxx xxxxxxxxxxxx mitogen (xxxx. xxxxxxxxxxxxxxxx) xx xxxxx xxx' plná xxxx x xxxxxxx xxxxxxxxxxxxxxx (xxxx. xxxxxxxxx), xxxx xxxxxxxxxx lymfocyty xxxxxxx od zdravých xxxxxxx x kultivují xx při xxxxxxx 37 °X.
1.4.1.4 Xxxxxxxxxxx xxxxxxxx
Xx xxxxx se xxxxxxxxxx látkou působí x přítomnosti x x nepřítomnosti xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx. Xxxxxxxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx mitochondriální xxxxxx (X9) xxxxxxxxxx x xxxxx xxxxxxxx, xxxxxxxxx xxxxxxx indukujícími enzymy, xxxx xx Xxxxxxx 1254, xxxx xxxx xxxxxxxxxxxxx a ß-naftoflavonu.5)
Konečná xxxxxxxxxxx mitochondriální frakce x xxxxx xxxx xxxxxxx 1 - 10 % x/x. Xxxxxxxx metabolického aktivačního xxxxxxx xxxx xxxxxxx xx xxx, xxxxxx xxxx xx xxxxxxxxx xxxxx. X xxxxxxxxx xxxxxxxxx xx vhodné xxxxxx xxxxxxxxxxxxxxx xxxxxx x xxxxxxxx koncentracích.
Pro xxxxx endogenní xxxxxxxx xxxxx xxx použity x geneticky xxxxxxxxxxxx xxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx. Xxxxx xxxxxxxxx xxxxx xx xxx být xxxxxxx xxxxxx (xxxx. xxxxxxx xxxxxxxxx xxxxxxxxxx X450 x metabolismu xxxxxxxxx xxxxx).
1.4.1.5 Xxxxxxxx xxxxxxxxx xxxxx
Xx-xx xxxxxxxxx xxxxx x pevném xxxxx, látka xx xxxx xxxxxxxxx xx xxxxx xxxxxxxx nebo xx připraví xxxx xxxxxxxx xx xxxxxxx xxxxxxxxxxxx a případně xxxxxx. Kapalné xxxxxxxxx xxxxx xx xxxxx xx xxxxxxx přidávat xxxxx nebo se xxxxxxx xxxx. Xx xxxxx xxxxxxxx xxxxxxx xxxxxxxxx, xxxxxx xxxxx x jejich xxxxxxxxx xxxxxxxxx, xx xxxxx xxxxxxxxxx neovlivňuje jejich xxxxxxxxxx.
1.4.2 Podmínky testu
1.4.2.1 Xxxxxxxxxxxx
X zvoleného xxxxxxxxxxxx xxxxx xxxxxxxxx podezření, xx xx xxxxx x xxxxxxxxxx xxxxxx xxxxxxxx reagovat, a xxxxx xxxxxxxxx přežívání xxxxx a xxxxxxxx X9. Xxxxxxx-xx se xxxx známé xxxxxxxxxxxx, xxxx být xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxxxxxxxx. Doporučuje xx, xxx xxxxx tam, xxx xx xx xxxxx, xxxx xx xxxxxx xxxxx zvažováno xxxxxxx xxxx xxxxxxxxxxxx xxxx. Je-li xxxxxxxxx xxxxx xx vodě xxxxxxx, musí být xxxxxxx organické rozpouštědlo xxxxx xxxxxxx. Voda xx dá xxxxxxxxx xxxxxxxxxxxx xxxxx.
1.4.2.2 Xxxxxxxxxxx
Xxxx xxxxxxxx, jež se xxxxxxx xxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxx, xxxxx xxxxxxxxxxxx, rozpustnost x xxxxxxx a xxxxx xX xxxx. xxxxxxxxxx.
Xxxxxxxxxxxx xx stanoví x xxxxxxxxxxxx xxxxxxxx x xxx ní x xxxxxxx xxxxxxxxxxx, přičemž xx xxxxxxx xxxxxx xxxxxxxx buněčné xxxxxxxxx x růstu, xxxxxxxxx xxxxxx xxxxxxxxxx, xxxxx xxxxxx xxxxx, nebo xxxxxxxxx xxxxx. Xx xxxxxx xxxxxxxx xxxxxxxxxxxx x rozpustnost x xxxxxxxxxxx xxxxxxxxxxxxx.
Xx xxxxx xxxxxx minimálně xxx xxxxxxxxxxxxxx xxxxxxxxxxx. Dochází-li x cytotoxicitě, musí xxxx xxxxxxxxxxx xxxxxxxx xxxxxx od maximální xx xxxxx nebo xxxxxx toxicity. To xxxxxxx xxxxxxx, xx xx xxxxxxxxxx xxxxxxxxxxx xxxxxxx xxxxx více xxx násobkem, xxxxx xxxx xxxx xxxxxxxxx 2 a √10. X xxxx sklízení xxxxx xxxx xxx xxx nejvyšší koncentraci xxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxx, počtu xxxxx, xxxx xxxxxxxxxxx xxxxxx (xxxx o xxxx než 50%). Xxxxxxxxx index je xxxxx nepřímou xxxxx xxxxxxxxxxxxx/xxxxxxxxxxxxxx xxxxxx a xx závislý xx xxxx xxxxxxxx xx xxxxxxxx xxxxxxxxxx látkou. Xx xxxx akceptovatelný xxx xxxxxxxxx kultury, xxx xx xxxx xxxxxxx xxxxxxxx byla xxxxxxx x nepraktická. Xxxx xxxxxxxxxx informace xx xxxxx xxxxxx xxxx xxxxx x xxxxxxxx xxxxxxxxx dělení, xxxx xx xxxxxxxx xxxxxxxxx xxx; xxx xxxxx představuje celkový xxxxxx, xxxxx ne xxxx xxxxxx xxxxxxxxx x xxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxx. X xxx x xxxx xxxxxxxxxxx průměrného generačního xxxx může xxxxxxxx xxxxxx xxxxxx od xxxxxx xxxx xxxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxx aberací.
U relativně xxxxxxxxxxxxxxx xxxxx xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx nejnižší x xxxxxx 5 µx/xx, 5 xx/xx xxxx 0,01 X.
X relativně xxxxxxxxxxxxx látek, xxx xxxx xxxxxxxxx x xxxxxxxxxxxxx xxxxxxx, xxx xx koncentrace xxx xxxxx xx již xxxxx nerozpouští, xx xxx xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxx, xxx xx xxx rozpustnosti xx xxxxxxxx xxxxxxxxxxx xxxxx xx xxxxx xxxxxxxxx x xxxxxxxxxx xxxxxx. V některých xxxxxxxxx - xxxxxxxxx xxxxxxx-xx k xxxxxxxxx xxxxxx xxx xxxxxxxxxxxxx xxxxxxx, xxx xx xxxxxxxx nerozpustná xxxxxxxxxxx - xx doporučuje xxxxxxxx při xxxxxxxx xxxxxxxxxxxxx s viditelným xxxxxxxx. Xxxx xxx xxxxxxxx vyhodnotit xxxxxxxxxxx xx počátku a xx xxxxx xxxxxxxx, xxxxxxx se během xxxxxxxx xxxx xxxxxxxxxxx xxxxxx x testovacím xxxxxxx vlivem xxxxxxxxxxx xxxxx, séra, X9 xxxx. Nerozpustnost xx xx zjistit x xxxxxxx xxxx. Xxxxxxxxx xxxxx být xx xxxxxxxx xxx xxxxxxxxx xxxxx.
1.4.2.3 Negativní x xxxxxxxxx xxxxxxxx
Xx xxxxxxx xxxxxxxxxxx, ať xxx x metabolickou xxxxxxxx, xxxx bez xx, xx třeba zařadit xxxxxxxx pozitivní a xxxxxxxxx kontroly (xxxxxxxxxxxx xxxx xxxxxxxxx). Pokud xx xxxxxxxx xxxxxxxxxxx xxxxxxxx, musí xxx xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxx.
Xxx xxxxxxxxx kontrolu xx xxxxxxx známý xxxxxxxxx, x xx xxx xxxxxxxxxxx xxxxxxxx, xxx se očekává, xx xxxxxxxx reprodukovatelný x detekovatelný nárůst xxxxxxx xxx pozadí, xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxx.
Xxxxxxxxxxx pro pozitivní xxxxxxxx xx xxxxx xxxxxx xxx, xxx xxxxxx xxx zřejmý, xxx xxxxxxxxxxx xxxxxxxxxxx xxxxx identitu zakódovaných xxxxxxxxx. Xxxx xxxxx xxx xxxxxxxxx xxxxxxxx xxxxx xxxxxxxxx:
|
|
|
|
|
|
Ne
|
methyl xxxxxxxxxxxxxx
|
|
|
| &xxxx;
|
xxxxx xxxxxxxxxxxxxx
|
|
|
| &xxxx;
|
xxxxx xxxxxxxxxxxxxxx
|
|
|
| &xxxx;
|
xxxxxxxxx X
|
|
|
| &xxxx;
|
4-xxxxxxxxxxxxx-X-xxxx
|
|
|
|
Xxx
|
xxxx[x]xxxxx
|
|
|
| &xxxx;
|
Xxxxxxxxxxxxx
|
|
|
| &xxxx;
|
xxxxxxxxxx cyklofosfamidu
|
|
|
Pro pozitivní xxxxxxxx xx xxxxx xxxxxx i jiné xxxxxx xxxxx. Xxx, xxx xx xx xxxxx, je xxxxxx xxxxxx pro xxxxxxxxx xxxxxxxx xxxxx ze xxxxxx xxxxxxxx skupiny.
Pro xxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxx xx xxxxx xxxxxx i xxxxxxxxx xxxxxxxx, xx xxxxx xx používá xxxxxxxxxxxx nebo xxxxxxxxx x xxxxxxxxxxx médiu, xxxxxxxxxx xxxxxxx způsobem xxxx experimentální kultury. Xxxxxx xx xxxxxx xxxxx zařadit xxxxxxxx xxx jakéhokoliv xxxxxxxxx.
1.4.3 Xxxxxx
1.4.3.1 Expozice testovanou xxxxxx
Xx xxxxxxxxxxxxx xxxxx xx xxxxxx xxxxxxxxxx xxxxxx za xxxxxxxxxxx x nepřítomnosti metabolického xxxxxxxxxxx xxxxxxx. Xx xxxxxxxxx je třeba xxxxx xxxxxxx asi 48 xxxxx po xxxxxxxxx xxxxxxxxx.
Xxxxxxx se xxx každou koncentraci xxxxxxxxx dvě xxxxxxx; x xxxxx xx xxxxxxxxxx pro xxxxxxxxx xxxxxxxx x xxxxxxxxxxxxx xxxx xxxxxxxxx. Xxxxx xxx xx xxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxx, xx xxxxxxx xxxx xxxxxxxxxxxx kulturami jsou xxxxxxxxx, je xxxxxxxxxx, xxx xx xxx xxxxxx xxxxxxxxxxx xxxxxxx xxxxx jedna xxxxxxx.5)
X xxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxx je xxxxx xxxxxxxx x xxxxx vhodné xxxxxxx, xxxx je použití xxxxxxxxxx xxxxxxxxxx kultivačních xxxxx.
1.4.3.2 Xxxx xxxxxxxx xxxxxxx
X prvním experimentu xx buňky xxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxxxx aktivací x xxx xx xx xxxx 3 - 6 hodin x xxxxxx se odebírají x xxxx xxxxxxxxxxxxx xxxxxx 1,5násobku normální xxxxx buněčného xxxxx xx xxxxxxx xxxxxxxx.5) Xxxxx jsou při xxxxxxx aktivačního xxxxxxx x xxx xxxx xxxxxxxx negativní, xxxxxxx xx xxxxx xxxxxxxxxx xxx xxxxxxxx, x xxxxxxxxxxx expozicí xx xx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx 1,5-xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxxx xxxxx xx hodnotí xxxxx xxx době xxxxxxxx xxxxx, než xx 1,5-xxxxxxx xxxxx xxxxxxxxx xxxxx. Xxxxxxxxx xxxxxxxx x metabolickou xxxxxxxx xx xxxxxxxx xxxxxx xx xxxxxxx. X xxxxxxxxx, xxx se xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx xx nutné, xx xxxxx toto xxxxxxxxxx xxxxxxxxx.
1.4.3.3 Xxxxxxxx xxxxxxxxxx
Xx xxxxxxx xxxxxxx xx působí Colcemidem® xxxx xxxxxxxxxxx obvykle xx dobu 1 - 3 hodin xxxx ukončením xxxxxxxxx. Xxxxx xxxxxxx xxxxxxx xx xxx přípravu xxxxxxxxxx zpracovává zvlášť. Xxxxxxxx chromozómů xxxxxxx x xxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxx, xxxxxx x xxxxxxxx.
1.4.3.4 Analýza
Všechny xxxxxxxxx, včetně pozitivních x negativních xxxxxxx, xx xxxx xxxxxxxxxxxxxx xxxxxxxx nezávisle xxxxxxxx. Xxxxxxx xxxxxxx postupy xxxxx xxxxx x xxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx buněk a xxxxxx xxxxxxxxxx, musí xxx x xxxxx xxxx xxxxx xxxxx xxxxxxxxx v xxxxxxxxxxx xxxxxxx xxxxx modálnímu xxxxx ± 2. Xxx každou xxxxxxxxxxx x kontrolu xx xxxxx xxxxxxxx xxxxxxxxx 200 xxxxx xxxxxxxxxxxxxx xxxxxxxx, xxxxxxxxxxx z xxxx xxxxxx, xxxxx xxxx použity. X xxxxxxx, že xx xxxxx xxxxxxx vysoký, xxxx se xxxxx xxxxxxxxxxxxx metafází xxxxxx.
X xxxx účelem testu xx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx, xx xxxx důležité zaznamenat xxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxxxxx.
2 XXXXX
2.1 Xxxxxxxxxx xxxxxxxx
Xxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xx buňka, xx xxxxx vyhodnotit xxxxxxxx xxxxx se xxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx. Xx xxxxx xxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxxxx xxxxxxx xxxxxx xxxxxx xxxxx x četnosti x xxxxxxxxxxxxxxxx x xxxxxxxxxxx xxxxxx. Gapy se xxxxxxxxxxxxx xxxxxx, xxx xxxxxxx xx xx xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx.
Xxxxxxxx xx xxxxx x testu zaznamenávat xxxx xxxxxxxxx xxxxxxxxxxxx x experimentálních x xxxxxxxxxxx xxxxxxxxx.
Xxxxxxx xx xxxx xxx xxxxxxxxxx xxxxxxx. Xxxxxxx se xxxxxxx xxxx xxxxxx x xxxxxxx xxxxxxx.
Xxxxxxxxxx xxxxxx xxxxxxxxxxx výsledků xx nepožaduje. Xxxxxxxxxxxxx xxxxxxxx xx xxxxxxxxx xxxxxx xxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxxxxxxxx podmínek. X xxxxxxxx xxxxxxxx xxxxxxxxx výsledky xxxx xxxxxxxxx x xxxx. 1.4.3.2. X xxxxxxxxxx xxxxxxxxxxxxx je třeba xxxxxx modifikaci xxxxxxxxx xxxxxxxxx tak, xxx xx xxxxxxxx xxxxxx xxxxxxxxxxxx podmínek. X xxxxxxxxxx, xxxxx xxx xxxxxxxxxxx, patří xxxxxxxxxxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxx.
2.2 Xxxxxxxxxxx x interpretace výsledků
Ke xxxxxxxxxx pozitivního výsledku xx xxxxxxx xxxxxxx xxxxxxxx, například xx xxxxxxxxxxx xxxxxxxxx látky xxxxxxx frekvence buněk x xxxxxxxxxxxxxx xxxxxxxxx. Xxxxxxx xx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx. Xxx vyhodnocování xxxxxxxx xxxxx se xxxxx xxxxxx statistické xxxxxx.5) Xxxxxxxxxxx významnost xx xxxx neměla xxx jediným xxxxxxxxx xxxxxxxx pozitivního výsledku.
Nárůst xxxxx xxxxxxxxxxxxx xxxxx xxxx indikovat, xx xxxxxxxxx látka má xxxxxxxxx xxxxxxxxx mitotické xxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx. Xxxxxx xxxxx xxxxx x xxxxxxxxxxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxx, xx xxxxxxxxx látka xx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx cyklu.5)
Testovaná xxxxx, xxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx výše xxxxxxx xxxxxxxx, se x xxxxx xxxxxxx xxxxxxxx xx nemutagenní.
Ačkoliv xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx pozitivní, xxxx xxxxxxxxx xxxxxxxx, xx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxxxx jednoznačné xxxxxxxxx xxxxxx xxxxxxxxx xxxxx. Výsledky xxxxx xxx xxxxxxx, nebo xxxxxxxxxxxx bez xxxxxx xx počet opakovaných xxxxxxxxxxx. Pozitivní xxxxxxxx xxxxx na xxxxxxxxxxxx xxxxxxx in vitro xxxxxxx, xx testovaná xxxxx xxxxxxxx v xxxxxxx xxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx. Negativní xxxxxxxx xxxxxxx, xx za xxxxxx xxxxxxxxxxxxxxxx podmínek xxxxxxxxx xxxxx v xxxxxxx xxxxxxx xxxxxxxxxxx xxxxx chromozámové xxxxxxx xxxxxxxxxx.
3 XXXXXXX XXXXXX, XXXXXXXX POKUSU A XXXXXXXXX XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx9) musí xxx xxxxxxxxx xxxxxxx xxxxxx x x průběhu xxxxxx xx xxxxx xxxx xxxxxxxx.
Xx xxxxxx x xxxxxxx xxxxxx xx xxxxx xxxxx xxxx xxxxxxxxx:
Xxxxxxxxxxxx/ xxxxxxxxx:
- xxxxxxxxxx volby xxxxxxxxxxxx/xxxxxxxx
- xxxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxxxx/xxxxxxxx, xxxxx xx xxxxx.
Xxxxx:
Xxxxxxxx pokusu:
Výsledky:
- xxxxxx xxxxxxxx, xx. xxxxxx xxxxxxxxxx, údaje o xxxxxxxx cyklu, x xxxxx buněk,
- xxxxxx xxxxxxx,
- xxxxx x xX a xxxxxxxxxx xxxxxxxxxxx média, pokud xxxx xxxxxxxxx,
- xxxxxxxx xxxxxxx, xxxxxx xxxx,
- xxxxx xxxxx x xxxxxxxxxxxxxx xxxxxxxxx x xxxx aberací xxxxxx xxx xxxxxx exponovanou x kontrolní kulturu,
- xxxxx xxxxxxx, xxxxx xxxx xxxxxxxxxx,
- xxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx dávce,
- xxxxxxxx xxxxxxxxxxx xxxxxxx,
- xxxx x xxxxxxxx negativní (xxxxxxxxxxxx/xxxxxxxxx) x xxxxxxxxx xxxxxxxx,
- xxxxxxxxx xxxx x negativní (xxxxxxxxxxxx/xxxxxxxxx) x pozitivní xxxxxxxx x xxxxxxxxx, středními xxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.11 XXXXXXXXXX - XXXX XXXXXXXXXXXXXX XXXXXXX X KOSTNÍ XXXXX XXXXX IN XXXX
1 METODA xx x xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
5)1.1 Xxxx
Xxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxx x xxxxx xx xxxx xx xxxxxxx xxxxxxxxxxxx chromozómové xxxxxxx vyvolané xxxxxxxxxx xxxxxx x xxxxxxx xxxxxx xxxxx zvířat, xxxxxxx hlodavců.
5) Xxxxxxxxxxxx xxxxxxx xxxxx xxx xxxxxxx druhu: chromozómové x chromatidové. Nárůst xxxxxxxxxxx xxxx xxxxxxxxxx, xx xxxx xxxxxxxx xxxxx xx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx. Xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxx, xxxxx k xxxxxxxx xxxxxxxxxxxxxx typu xxxxxxx rovněž. Xxxxxxxxxxxx xxxxxx a xxxxxxxx xxxx xxxx xxxxxxxx xxxx xxxxxxxxxxx chorob x xxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxx xxxx, xx xxxxxxxxxxxx xxxxxx x příbuzné xxxx, xxx xxxxxxxxx xxxxx x xxxxxxxxxx x xxxxxxxxxxxxxxxxxx xxxxxx, xxxxx xxxxx xxx xxxxxxxx u xxxxxxx x v experimentálních xxxxxxxxx.
X xxxxxx xxxxx xx běžně xxxxxxxxx xxxxxxxx. Cílovou tkání x xxx xx xxxxxx xxxx, xxxxxxx xx jedná o xxxx vysoce xxxxxxxxxxxxxxxx, xxxxxxxxxx populaci xxxxxx xx dělících xxxxx, xxx se xxxx xxxxxx xxxxxxxx x xxxxxxxxx. Jiné xxxxxxxxx xxxxx a xxxxxx xxxxx xx x xxxxx xxxxx xxxxxxxxxxx.
Xxxxx xxxx xx chromozómové xxxxxxx xx zvláště xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx rizika, xxxxxxx xxxxxxxx xxxx x xxxxx xxxxxxx metabolismu xx vivo, farmakokinetiky x xxxxxxx xxxxxxxx XXX, x xxxx xxx xxxxx xxx xxxx xxxxxxxxxxx xxxxx x xxxx xxxxxxx xxxxxxx. Xxxx xx xxxx xx také xxxxxx xxx xxxxx xxxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxx xxxxxxx xxxxxxx xxxxxx xx xxxxx.
Xxxxxxxx-xx xxxxxxx x xxx, xx xx xxxxxxxxx xxxxx nebo xxxx xxxxxxxxx metabolit xx xxxxxx tkáně xxxxxxxxx, xxxx xxxxxx xxxxxxx xxxxxx xxxxx.
1.2 Xxxxxxxx
Xxxxxxx xxxxxxxxxxxxxx typu: xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxx xx projevuje xxxx xxxx xxxxx, xxxxxxxx obou xxxxxxxxx, xxxx zlom a xxxxxxxx xxxxxxx xxxx xxxxxxxxxxxx.
Xxxxxxx xxxxxxxxxxxxxx xxxx: xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx xxxx xxxxxxxxxx xxxx zlom x xxxxxxxx spojení xxxx xxxxxxxxx xx xxxxxxx xxxxx (xxxxxxxx xxxx xxxxxxx xxxx xxxxxxxxxxx xxxxxxxxx, xxxxxxxxxx xxxxxxxxx-xxxx).
Xxxx xxxxxxxxxx: xxxx xxxx xxx xxxxxxxx xxxxxxxx kontinuity xxxxx xxxx xxxx xxxxxxxxx xx xxxxxxxxxxx, xx xxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxx xx xxxxx, xxx je xxxxx poškozené xxxxxxxxxx. Xxxx xxx v xxxxxxxxx, koncový (xxxxxxxx) xxxxxxxx v xxxxx xxxxx xx xxxxxxxxxxx (xxxx mimo xxx xxxxxxxxxx), případně xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx xx xxxxxx x xxxxxxxx xxxxxx.
Xxxxxxxxxxxxxxx: xxxxxx, xxx xx X-xxxx xxxxxxxxx DNA xxxxxxxxxx xxxxx xx mitózy, xxxxx začíná další X-xxxx. Xxxxxxxxx jsou xxxxxxxxxx s 4, 8, 16, ... xxxxxxxxxxxx.
Xxx: xxxxxxxxxxxx léze xxxxx xxx xxxxx xxxxx xxxxxxxxxx a x xxxxxxxxxx xxxxxxxxx xxxxxxxxx.
Xxxxxxxxx xxxxx: poměr xxxxx v xxxxxxxx xxxxxx xxxxxxxx počtem xxxxx v dané xxxxxxx xxxxxxxx; udává xxxxxx proliferace této xxxxxxxx.
Xxxxxxxxx xxxxxxx: xxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxxx počtu charakteristickému xxx xxxxxxx xxxxx.
Xxxxxxxxxxx: xxxxxxx xxxxxxxxxxx počtu xxxxxxxxxx (x) xxxx xxxxxxxxx xxxxx (tedy 3x, 4n xxx.).
Xxxxxxxxxxxx xxxxxxx: změna xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx buněčného dělení xx stadiu xxxxxxxx, xxxxxxxxxx xxxx xxxxxx x fragmenty x xxxxxx.
1.3 Xxxxxxx metody
Zvířata xx xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx xxxxx x ve xxxxxxx xxxx xx xxxxxxxx xx xxxxxx. Před xxxxxxxxx se xx xx xxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx (xxxxxxxxx xxxxxxxxxxx nebo Xxxxxxxxxx®). X xxxxx xxxxxx xxxxx se xxx xxxxxxxx preparáty x x xxxxxxxxxxxxx xxxxxxx xx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxx.
1.4 Xxxxx xxxxxx
1.4.1 Xxxxxxxx
1.4.1.1 Xxxxx xxxxxxxxxxx xxxxx
Xxxxx xx xxxxxxxxx potkani, xxxx x xxxxxx xxxxxx, xxx xxxxx xxxxxx x xxxxxxxxx xxxx xxxxxx xxxxx xxxx. Xxxxxxxxx se xxxxx xxxxxxxxxxx kmeny mladých xxxxxxxx xxxxxxx. Xxxxxxxxxx xxxxxxx xx xxx xxxxxxxx xxxxxx měly xxx xxxxxxxxx x x xxxxxxx xxxxxxx xxxxxx xxxxxxxxxx ± 20 % průměrné xxxxxxxxx.
1.4.1.2 Xxxxxxxx xxxxx
Xxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxx ve Xxxxxxxxxx xxxxx x xxxxx X, xxxxxxx xx xxxx xxx 50 - 60 %.
1.4.1.3 Xxxxxxxx xxxxxx
Xxxxxxx xxxxxxx xxxx xxxxxxx x xxxxxxx na xxxx, xxxxxxx x stáří x xxxxxxx x xxxxxxxxxxx
§15 zvláštního xxxxxxxx xxxxxxxx
10) x xxxxxxxx xxx, aby xxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Dobu xxxxxxxx xxxxxxx
§10 xxxxxxxxxx právního xxxxxxxx.
10)1.4.1.4 Xxxxxxxx xxxxx
Xx-xx xxxxxxxxx xxxxx x xxxxxx xxxxx, xxxx xxxxxxx xxxxxxxx xx xxxxxxxx xxxx se připraví xxxx xxxxxxxx ve xxxxxxx rozpouštědle xxxx xxxxxxxx x případně xx xxxxx. Xxxxxxx xxxxxxxxx xxxxx se xxxxx xxxxxxx xxxxx xxxx xx xxxx xxxxxxxxx xxxx. Xx xxxxx xxxxxxxx čerstvé xxxxxxxxx, ledaže xxxxx x stálosti xxxxxxxxx, xx xxxxxxxxxx xx xxxxxxxxx.
1.4.2 Xxxxxxxx xxxxx
1.4.2.1 Xxxxxxxxxxxx/xxxxxxxxx
Xxxxxxxxxxxx/xxxxxxxxx x používaných xxxxxxx xxxxx xxxxxxxxx xxxxxxx xxxxxx a xxxxx x xxxxxxxxxx xxxxxx chemicky xxxxxxxx. Xxxxxxx-xx xx xx xxxxxx známé xxxxxxxxxxxx, xxxx xxx jeho xxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxxxxx x xxxxxxxxxx látkou. Doporučuje xx, xxx, kde xx xx možné, xxxx xx xxxxxx xxxxx xxxxxxx vodné xxxxxxxxxxxx/xxxxxxxxx.
1.4.2.2 Xxxxxxxx
Xx každého xxxxx xx třeba xxx xxxxx xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx x negativní (xxxxxxxxxxxx/xxxxxxxxx) xxxxxxxx. Je xxxxx xxxxxxxx xx xxxxxxx xx xxxxx xxxxxxxxx xxxxxx.
Xxxxxxxxx xxxxxxxx xx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx xx vivo xxx dávkách, xxx xxx xxxxxxxx xxxxxx xxxxxxxxxxxxx zvýšení nad xxxxxxxxx xxxxxx. Xxxxx xxx pozitivní xxxxxxxx xx xxxx tak, xxx xxxx xxxxxx xxxxxx, xxx přitom xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx preparátu. Xxxxxxxxx xxxxxxxx je xxxxx xxxxxxx odlišným xxxxxxxx xxx xxxxxxxxxx xxxxx x vzorek xxxxxxxx x xxxxxx xxxxxxx xxxxxxxxx. Xxx xx xx xxxxx, je xxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxx xxxxxxxx xxxxxxx, jako xx xxxxxxxxx xxxxx. Xxxxxxxx xxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxx:
|
|
|
|
|
xxxxx xxxxxxxxxxxxxx
|
62-50-0
|
200-536-7
|
|
xxxxx nitrosomočovina
|
759-73-9
|
212-072-2
|
|
mitomycin X
|
50-07-7
|
200-008-6
|
|
xxxxxxxxxxxxx
|
50-18-0
|
200-015-4
|
|
xxxxxxxxxxxxx xxxxxxxxxx
|
6055-19-2
|
&xxxx;
|
|
xxxxxxxxxxxxxxxxx
|
51-18-3
|
200-083-5
|
Xxxxxxxxx kontroly xxxxxxxxx xxxxxxxxxxxxx xxxx vehikulem x zpracované xxxxxxx xxxxxxxx jako experimentální xxxxxxx xxxx xx xxx xxxxxxxx xx xxxxx časových xxxxxxxxx xxxxxxxxxx, xxxxx xxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxxx chromozómových aberací x o xxxxxxxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxx. Xxxxxxxx-xx xx x xxxxxxxxxxx kontrol xxxxx xxxxx xxxxx vzorků, xx nejvhodnější dobou xxxxx interval xxxxxx xxxxxx. Mimoto xx xxxxx xxxxxx i xxxxxxxxxxxxx xxxxxxx, xxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx, xx xxxxxxx rozpouštědlo xxxx xxxxxxxxx xxxxxxxxxx xxxxx nepříznivé xxxx xxxxxxxxx účinky.
1.5 Xxxxxx
1.5.1 Xxxxx x pohlaví xxxxxx
X každé experimentální x xxxxxxxxx skupině xxxx xxx xxxxxxxxx xxx analyzovatelných jedinců xxxxxxx xxxxxxx. Pokud x době, xxx xx xxxxxx xxxxxxx, xxxxxxxx údaje x xxxxxxx xxxxxxxxxx xxxxx x použití stejných xxxxxxx xxxxxxxx xxxxxxxxxxx, xx xxxx oběma xxxxxxxxx xxxxxx v xxxxxxxx xxxxxxxxx xxxxxxx, xx xxxxxxxxx xxxxx xx xxxxxx xxxxxxx xxxxxxxxxxx. Tam, xxx xxxxxxx xxxxxxxx chemickým xxxxxx xxxx xxx xxxxxxx xx xxxxxxx, xxx xx xxxx xxxxxxxxx x některých xxxxxxxxxxxxxxx xxxxxxxxx, xxxxxxx xx test na xxxxxxxxx odpovídajícího pohlaví.
1.5.2 Xxxxxxxxx xxxxxx
Xxxxxxxxxx látku xx nejvhodnější xxxxxxx xxxxxxxxxxx. Pokud xx xxxxx x xxxxxxxx xxxxx, xxxx xx x xxxxxxxxx aplikace xxxxx xxxxxxxx, xxxxxxxxx xx xxx xxxxx xx den podané x rozmezí xxxxxxxxx xxxxxxxx xxxxx. Xxxx xxxxxx xxxxxxxxx musejí xxx vědecky odůvodněné.
Vzorky xx xxxxxxxxx xx xxxx různých xxxxxxxx xxxxxxxxxxx po podání xxxxx xxx. X xxxxxxxx je xxxxx xxxxxxxx xxxxxx xxxxxx 1,5xxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxx (xxxxx xxxx obvykle 12 - 18 xxxxx) xx xxxxxx xxxxx. Xxxxxxx doba xxxxxxxx xxx absorpci x xxxxxxxxxxxx testované xxxxx x xxxx xxxx xx kinetiku xxxxxxxxx xxxxx xxxxx ovlivnit xxxxxxxxx xxxx xxx xxxxxxx xxxxxxxxxxxxxx aberací, xxxxxxxxxx xx xxxxx xxxxx vzorků po 24 xxxxxxxx od xxxxxxx xxxxxx. Pokud xx x daném xxxxxxxxxx režimu xxxxx xxxxxx xxxxxxxx než xxxxxx za xxx, xx xxxxx xxxxxxx xxxxx odběr vzorků 1,5xxxxxxxx délky xxxxxxxxxx xxxxxxxxx xxxxx po xxxxxxxxx xxxxxx xxxxx.
Xxxx xxxxxxxxx xx xxxxxxxx xxxxxxxxxxxxxxxxx xxxxxxxx xxxxxx xxxxx Xxxxxxxxx® xxxx xxxxxxxxxx x xxxxxxxx xx x nich xx vhodném xxxxxxxxx xxxxxxxx xxxxxx. X xxxx je xxxxx xxxxxxxx zhruba 3 - 5 hodin, x xxxxxxxx xxxxxx xxxxxx 4 - 5 xxxxx. Z xxxxxx xxxxx se xxxxxxxx buňky x xxxxxxxx xx x xxxx xxxxxxxxxxxx aberace.
1.5.3 Xxxxxxxxx
Xxxxxxx-xx se xxxxxx xx zjištění xxxxxxx xxxxxxxx, xxxxxxx xxxxxx x xxxxxxxxx žádné xxxxxx údaje, je xxxxx ji xxxxxxxx x xxxx laboratoři xx xxxxxxx stejného xxxxxxxxxxx druhu, kmene, xxxxxxx a xxxxxxxxx xxxxxx, jaké xx xxxxxxx x hlavní xxxxxx. Xxx xxxxxxxx xxxxxxxx xx užívají xxx první časový xxxxxxxx xxxxxx vzorků xxx xxxxx tak, xxx pokrývaly xxxxxxx xx xxxxxxxxx xxxxxxxx x toxicitě xxxxx xxxx nulové. Xxx xxxxxxxx časový xxxxxxxx xxxxxx vzorků je xxx xxxxx použít xxxxx nejvyšší xxxxx. Xx xx xxxxxxxxxx xxxx dávka xxxxxxxxxxxx xxxxxx xxxxxx toxicity, xx při xxxxxxx xxxxxxx ve xxxxxxx xxxxxx xxxxxxxx xx xxxxxx xxxx xxxxxxx. Xxxxx, xxx v xxxxxxx netoxických xxxxxxx xxxxxxxx specifickou xxxxxxxxxxx xxxxxxxx, jako jsou xxxxxxx xxxx xxxxxxxx, xxxxx xxxxxxxxxxxx x xxxxxx xxxxxxxx pro xxxxxxxxx xxxxx xxxxxxx, xxx se vyhodnocují xxxxxxxxxxxx xxxxxx xx xxxxxxx. Xxxxxxxx dávka xxxx xxx xxxx xxxxxxxxxx jako xxxxx, xxxxx vede x xxxxxxx známkám xxxxxxxx x xxxxxx dřeni (xxxx. pokles xxxxxxxxxxx xxxxxx x xxxx xxx 50 %).
1.5.4 Xxxxxxx test
Jestliže test xxx xxxxx xxxxxxxxx 2&xxxx;000 xx/xx hmotnosti x xxxxx xxxxx xxxx ve xxxx xxxxxxx podaných x xxxxx den xxxxxxxxxx xxxxx pozorovatelné xxxxxxx xxxxxx x xxxxxxxx xx xx základě xxxxx x xxxxxxx x xxxxxxxx chemickou xxxxxxxxxx neočekává genotoxicita, xxxxxx xxx xxxxxxxxx xxxx xxxxxx za xxxxxxx xxx dávkových xxxxxx. Xxx dlouhodobé xxxxxx xxxx xxxxxxx xxxxx 2&xxxx;000 xx/xx xxxxxxxxx xx xxx xxx době xxxxxx xx 14 xxx x 1&xxxx;000 mg/kg xxxxxxxxx xxx xxxx xxxxxx xxxxx xxx 14 xxx. Podle xxxxxxxxx xxxxxxx xxxxxxxx xxxx xxx xxxxxxxxx xxxxxx v xxxxxxxx xxxxx vyšší xxxxxxx xxxxxx.
1.5.5 Xxxxxxxx xxxxx
Xxxxxxxxx xxxxx xx obvykle xxxxxxxx xxx xxxxxxxxx xxxxxx, xxxx xxxxxxxxxxxxxxxxx xxxxxxx. X xxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxx x xxxx způsoby xxxxxxxx. Maximální xxxxx xxxxxxxx, která xx xx xxxxxx xxxx xxxxxxx xxxxxxxx vpravit, xxxxxx xx xxxxxxxxx xxxxxxxxx zvířete a xxxx xxxxxxxxx 2 xx/100x hmotnosti; xxxxx xxxxx xxxx xxx xxxxxxxxxx. X xxxxxxxx xxxxxxxxxx xxxx xxxxxxxx xxxxx, xxx xxxxxxxx xxxxxxxx při xxxxxxx xxxxxxxxxxxxx horší xxxxxx, xx třeba upravit xxxxxxxxxxx látky xxx, xxx xxxxx byl xx všech dávkových xxxxxxxx xxxxxx a xxxxxxxxxxxxxx xx xxx xxxxxxxx xxxxxxxxxxx.
1.5.6 Xxxxxxxx xxxxxxxxxx
Xxxxxxxx xx xxxxxxxx xxxxxxx xx xxxxxxx xxxxxx dřeň, xxxxxx xx ni hypotonickým xxxxxxxx a dřeň xx fixuje. Xxxxxxxx xxxxx se nakape xx xxxxxxxx xxxx x xxxxxx xx.
1.5.7 Xxxxxxx
Xxxxxxx xxxx cytotoxicity xx x xxxxx xxxxxx včetně xxxxxxxxxxx x negativních xxxxxxx xxxxxxx xxxxxxxxx xxxxx xxx minimálně 1000 xxxxx x xxxxxxx xxxxxxx.
X xxxxxxx xxxxxxx xx xxxxxxxxx xxxxxxxxx 100 buněk. Xxxxx xxxxx xx možné xxxxxx při vysokém xxxxx xxxxxxx. Xxxxxxx xxxxxxxxx (včetně xxxxxxxxxxx x xxxxxxxxxxx kontrol) xx xxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx zakódují. Xxxxxxx xxx xxxxxx xxxxxxxx xxxxxxx často x porušení xxxxxxxx xxxxxx metafází spojeného xx xxxxxxx chromozómů, xxxx xxx počet xxxxxxxxx x xxxxxxxxxxx xxxxxxx 2x ± 2.
2 XXXXX
2.1 Xxxxxxxxxx xxxxxxxx
Xxxxx od jednotlivých xxxxxx xx zaznamenávají x xxxxxxx. Xxxxxxxxxxxxxx xxxxxxxxx xx jedinec. X xxxxxxx zvířete xx zaznamenává xxxxx xxxxxxxxxxx xxxxx, počet xxxxxxx xx xxxxx xxxxx x xxxxxxxx xxxxx se strukturálními xxxxxxxxxxxxxx xxxxxxxxx. U xxxxxxxxxxxxxxxx x kontrolních xxxxxx xx xxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx, jejich xxxxx a četnost. Xxxx se xxxxxxxxxxxxx xxxxxx x xxxxxxxxxx xx, ale xxxxxxx xx xx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxx. Xxxxxx-xx žádné xxxxxxx x tom, xx xxx xxxxxxx xxxxxxx xxxxxxxx, xx xxxxx xxxxx xx obě xxxxxxx xxx xxxxxxxxxxxx xxxxxxx xxxxxxx.
2.2 Xxxxxxxxxxx x xxxxxxxxxxxx výsledků
Ke xxxxxxxxxx xxxxxxxxxxx výsledku xx xxxxxxx xxxxxxx xxxxxxxx, xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxx látky xxxxxxx xxxxxxxxx buněk x xxxxxxxxxxxxxx xxxxxxxxx, xxxx xxxxxxxx xxxxxx xxxxx xxxxx x xxxxxxxxx xx skupině x xxxxxxxxxxxx xxxxxx xxx xxxxxx časovém xxxxxxxxx odběru vzorků. Xxxxxxx xx xxxxx xxxxxx xxxxxxxxxxx významnost xxxxxxxx. Při xxxxxxxxxxxxx xxxxxxxx testu xx xxxxx xxxxxx xxxxxxxxxxx xxxxxx. Xxxxxxxxxxx xxxxxxxxxx xx xxxx neměla xxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxx. Xxxxxxxxxxxxx xxxxxxxx xx xxxxx xxxxxxxx xxxxxx xxxxxxxxxx, xxxxxxx xx xxxxxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxx.
Xxxxxx xxxxx xxxxxxxxxxxxx xxxxx xxxx indikovat, xx xxxxxxxxx xxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx a xxxxxxxxx xxxxxxxxx chromozómové xxxxxxx. Xxxxxx počtu xxxxx x xxxxxxxxxxxxxxxxxxx xxxxxxxxxx xxxx naznačovat, xx xxxxxxxxx xxxxx má xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxx.
5)Xxxxxxxxx xxxxx, xxx jejímž xxxxxxx xxxxxxxx nesplňují výše xxxxxxx xxxxxxxx, se x tomto xxxxxxx xxxxxxxx xx xxxxxxxxxxx.
Xxxxxxx xxxxxxxxxxx sice xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxx, x xxxxxxxxxxx případech xxxx xxxxx xx xxxxxxxxx xxxxxxx xxx xxxxxxx x xxxxxxxx testované xxxxx xxxxxxxxxxx xxxxx. Xxxxxxxx xxxxx xxx xxxxx nejednoznačné xxxx xxxxxxxxxxxxx, i xxxx xx xxxxxxxxxx xxxxxxxxxx xxxxxxx.
Xxxxxxxxx výsledky xxxxx xx xxxxxxxxxxxx xxxxxxx xx xxxx ukazují, xx testovaná látka xxxxxxxx v kostní xxxxx příslušného xxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx. Negativní xxxxxxxx xxxxxxx, xx za xxxxxx experimentálních xxxxxxxx xxxxxxxxx xxxxx v xxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx.
Xx xxxxx xxxx v xxxxx, xxxx je pravděpodobnost, xx xxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxx, xxxx jakou specifickou xxxxxxx tkáň zasáhne (xxxx. xxxxxxxxx xxxxxxxx).
3 XXXXXXX POKUSU, PROTOKOL XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx s xxxxxxxxxxx právními xxxxxxxx
9) xxxx být xxxxxxxxx xxxxxxx xxxxxx x x průběhu pokusu xx xxxxx vést xxxxxxxx.
Xx zprávě x xxxxxxx xxxxxx xx xxxxx uvést tyto xxxxxxxxx:
Xxxxxxxxxxxx/xxxxxxxxx:
- xxxxxxxxxx volby xxxxxxxx,
- xxxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxxxx/xxxxxxxx, pokud xx xxxxx.
Xxxxxxx xxxxxxx:
- xxxxxxx xxxxxxxxx xxxx/xxxx,
- xxxxx, xxx a xxxxxxx xxxxxxx,
- původ, xxxxxx xxxxxxxx, xxxxxx xxxx.,
- xxxxxxxx jednotlivých xxxxxx na xxxxxxx xxxxx, včetně xxxxxxxxxxxx xxxxxxx, xxxxxxx a xxxxxxxxxxxx odchylek xxx xxxxxxxxxx xxxxxxx.
Xxxxxxxx xxxxxx:
- xxxxxxxxx x xxxxxxxxx (xxxxxxxxx/xxxxxxxxxxxx) xxxxxxxx,
- údaje xx studie xxx xxxxxx xxxxxxx, xxxx-xx xxxxxxxxx,
- xxxxxxxxxx xxxxx xxxxxxxxx xxxxx,
- xxxxxxxxxxx x xxxxxxxx testované xxxxx,
- xxxxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxx,
- xxxxxxxxxx způsobu xxxxxxxx,
- xxxxxxxx metody x xxxxxxx, xx xx xxxxx xxxxxxx xx xxxxxxxxx xxxxx xxxx xx cílové xxxxx,
- xxxxxxxx převod xxxxxxxxxxx xxxxx v potravě/pitné xxxx (xxx) na xxxxxxxxx dávku (mg/kg xxxxxxxxx/xxx ),
- podrobnosti x kvalitě potravy x xxxx,
- xxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxxxx x odběru xxxxxx,
- xxxxxx xxxxxxxxx xxxxxxxx,
- látka xxxxxxxxxxx xxxxxxxx, její xxxxxxxxxxx x doba xxxxxxxx,
- xxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx
- xxxxxxxx xxx xxxxxxxxx xxxxxxx,
- počet xxxxxxxxxxxxx buněk na xxxxx xxxxx,
- xxxxxxxx, xxxxx xx studie xxxxxxx xxxx xxxxxxxxx, xxxxxxxxx xxxx nejednoznačná.
Výsledky:
- xxxxxx xxxxxxxx,
- mitotický xxxxx,
- xxx a xxxxx aberací xxx xxxxxxx xxxxxxx xxxxxx,
- xxxxxxx počet aberací x dané skupině, xxxxxx xxxxxx x xxxxxxxxxx xxxxxxxx.
- xxxxx xxxxx x aberacemi xx xxxxxxx se xxxxxxxxx hodnotami a xxxxxxxxxxxx xxxxxxxxxx,
- případné xxxxx xxxxxxx,
- xxxxx xxxxx-xxxxxx, xx-xx xx xxxxx,
- statistické analýzy, xxxx-xx provedeny,
- údaje xx xxxxxxxxxx xxxxxxxxxxx xxxxxxx,
- xxxxxxxxxx xxxxx x negativních xxxxxxx xxxxxx rozpětí, xxxxxxx x xxxxxxxxxxxx xxxxxxxx.
- xxxxx xx xxxxxxxxxx xxxxxxxxxxx xxxxxxx.
Xxxxxxx výsledků.
Závěry.
B.12 XXXXXXXXXX - XX XXXX MIKRONUKLEUS XXXX X SAVČÍCH XXXXXXXXXXXX
1 XXXXXX xx x xxxxxxx s právem Xxxxxxxxxx společenství.
5)1.1 Xxxx
Xxxxxxxxxxxx xxxx xx xxxx x savců slouží xx xxxxxxxx xxxxxxxxx, xxx xxxxxxxxx xxxxx xxxxxxxxx x xxxxxxxxxxxx xxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxxxx; xxxx xxxxxxx v xxx, xx xx xxxxxxxxx xxxxxxxxxx x kostní xxxxx xxxx x xxxxxxxxx xxxx zvířat, xxxxxxx xxxxxxxx.
Xxxxxx mikronukleus xxxxx xx xxxxxxx Xxxxx, xxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx, xxxxx xxxxxxxxx je xxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx nebo celých xxxxxxxxxx.
Xxxx z erytroblastu xxxxxx xxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx, xxxxx xx x buňky xxxxxxxxx; xxxxxxxx zbude x xxxxxxxxxx xxxxxxx xxxxxxxxxx. Xxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxx xxx, xx těmto buňkám xxxxx xxxxx. Xxxxxx xxxxxxxx polychromních xxxxxxxxxx x mikrojádry xx x xxxxxxxxxxxxxxxx zvířat xxxxxxx xxxxxxxxx xxxxxxxxxx.
X xxxxx xxxxx xx xxxxxx dřeň xxxxxxxx xxxxxxx xxxxx proto, xx se xxxxxxxxxxx xxxxxxxxxx v xxxx xxxxx xxxxx. Xxxxxxx xxxxxxxxx (xxxxxxxxxxxxx) xxxxxxxxxx x xxxxxxxxxx v xxxxxxxxx xxxx xx xxxxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxx, u xxxxxxx bylo prokázáno, xx jeho xxxxxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx nebo xx je tento xxxxxxxxx xxxx xxxxxxxxxx xxxxxxx xxx xxxxxxx xxxxx způsobujících xxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx. Mikrojádra se xxxx xxxxxxxxxx podle xxxx kritérií, jako xx přítomnost či xxxxxxxxxxxx xxxxxxxxxxx (xxxxxxxxxx), xxxx centromerické XXX x xxxxxxxxxx. Xxxxxxxx xxxxx xx stanovení xxxxxxxx xxxxxxxxx (polychromních) xxxxxxxxxx x xxxxxxxxxx. Xxxx xxxxx xxxxxxx (xxxxxxxxxxxxxx) xxxxxxxxxx v xxxxxxxxx xxxx obsahujících xxxxxxxxxx v xxxxx xxxxxx xxxxx zralých xxxxxxxxxx xxx jako xxxxxxxx xxxxxxx xxxxxx x případě, že xx xxxxxxx testují xx xxxx xxxxxxxxx xxxx xxxxx.
Xxxxx in xxxx xxxxxxxxxxxx test x xxxxx xx xxxxxxx xxxxxx k xxxxxxxxx xxxxxx mutagenity, xxxxxxx xxxxxxxx xxxxxxxxx xxxxxxx metabolismu in xxxx, xxxxxxxxxxxxxxx x xxxxxxx xxxxxxxx XXX, x xxxx xxx xxxxx xxx xxxx xxxxxxxxxxx druhy, xxxx xxxxxxx a xxxx xxxxxxxx efektem xxxxxxx. Xxxx xx xxxx xx xxxx užitečný xxx další xxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxx xxxxxxx zjištěn x systému xx xxxxx.
Xxxxxxxx-xx doklady x xxx, že xx xxxxxxxxx látka xxxx xxxx reaktivní xxxxxxxxx xx xxxxxx xxxxx xxxxxxxxx, xxxx použití xxxxxx testu xxxxxx.
1.2 Xxxxxxxx
Xxxxxxxxxx (xxxxxxxxxx): oblasti xxxxxxxxxx, xx xxxxxxx xx během dělení xxxx xxxxxx dělícího xxxxxxxx xxxxxxxxxx organizovaný xxxxx xxxxxxxxx xxxxxxxxxx x xxxxx xxxxxxxxx xxxxx.
Xxxxxxxxxx (mikronukleus): malá xxxxx xxxxxxxx od xxxxx buňky (xxxxxxx) xxxxxxxxx během xxxxxxxx xxxxxx, xxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxx xx xxxxxxxxx chromozómů nebo xxxxxx xxxxxxxxxx.
Xxxxxxxxxxxx xxxxxxxxx: xxxxx xxxxxxxxx, xxxxx xxxxxxx xxxxxxxx x xxxx xx dá xx nezralých, xxxxxxxxxxxxx xxxxxxxxxx odlišit xxxxxx xxxxxxx xxxxxxxxxxxx xxx xxxxxxxx.
Xxxxxxxxxxx xxxxxxxxx: nezralý xxxxxxxxx, xxxxxxxx stadium, xxx xxxx xxxxx xxxxxxxx xxxxxxxx, xxxxx xxx lze xxxxxxx xx xxxxxxx, normochromních xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxxx xxx xxxxxxxx.
1.3 Xxxxxxx metody
Zvířata xxxx xxxxxxx způsobem xxxxxxxxxx xxxxxxxxx látce. Xxxxx xx xxxxxxx xxxxxx xxxx, zvířata xx xx vhodnou xxxx xx xxxxxxxx látky xxxxxx, kostní xxxx xx xxxxxxx a xxxxxxxx xx xxxxxxxxx, xxx se obarví (1-7). Xxxxx xx xxxxxxx xxxxxxxxx xxxx, xxxxxxx xx xx xxxxxx xxxx po xxxxxxxx xxxxx a xxxxxxxx se xxxxxx, xxx se xxxxxx.
5) X xxxxxxxxxxxxx, xx xxxxxxx se používá xxxxxxxxx xxxx, xxxx xxx xxxx od xxxxxxxx xxxxxxxx do xxxxxxxxxx xxxxx xx xxxxxxxxx. X xxxxxxxxxxx xx xxxxxxxx přítomnost xxxxxxxxxx.
1.4 Xxxxx xxxxxx
1.4.1 Xxxxxxxx
1.4.1.1 Výběr xxxxxxxxxxx xxxxx
Xxxxx se používá xxxxxx dřeň, doporučují xx jako xxxxxxx xxxxxxx xxxx xxxx xxxxxxx; xxxx xxxx xxx xxxxxx jiný xxxxxx xxxxx xxxx. Xxxxxxx-xx se periferní xxxx, xxxxxxxxxx xx xxxx. Xxx ovšem xxxxxx xxxxxxxxx vhodný xxxxx xxxx za xxxxxxxxxxx, xx xx x něj xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxxx že x xxx xxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx xxxxxx, xxx xxxxxxxxx xxxxxxxxxxxx nebo xxxxxxxxx xxxxxxxxxxxx xxxxxxx. Xxxxxxxxx xx xxxxx xxxxxxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxx. Xxxxxxxxxx xxxxxxx xx xxx xxxxxxxx studie měly xxx xxxxxxxxx x x xxxxxxx xxxxxxx xxxxxx xxxxxxxxxx ± 20 % xxxxxxxx xxxxxxxxx.
1.4.1.2 Xxxxxxxx chovu
Všeobecné xxxxxxxx chovu xxxx xxxxxxx xx Xxxxxxxxxx xxxxx.
Xxxxxxx by xxxx xxx 50 - 60 %.
1.4.1.3 Xxxxxxxx xxxxxx
Xxxxxx xxxxx xxxxxxx xxxxxxx se xxxxxxx xxxxxxx xx kontrolní x xxxxxxxxxxxxxx skupiny. Xxxxxxx xx jednoznačně xxxxxx a po xxxx minimálně xxxx xxx se xxxxxxx xxxxxxxxxxxx v xxxxxxxxxxxxx xxxxxxxxxx. Xxxxx je xxxxx xxxxxxxxx tak, xxx xx minimalizovaly xxxxxxxx vlivy toho, xxx x xxx xxxx xxxxx umístěny.
1.4.1.4 Xxxxxxxx xxxxx
Xx-xx xxxxxxxxx xxxxx x xxxxxx xxxxx x xx-xx xx xxxxx, látka xx před xxxxxxx xxxxxxxx xxxxxxxx nebo xx xxxxxxxx xxxx xxxxxxxx xx xxxxxxx xxxxxxxxxxxx nebo vehikulu. Xxxxxxx xxxxxxxxx xxxxx xx xxxxx podávat xxxxx xxxx xx xxxx podáváním xxxx. Xx xxxxx xxxxxxxx xxxxxxx xxxxxxxxx, xxxxxx xxxxx x stálosti (xxxxxxxxx) prokazují, že xxxxxxxxxx xx neovlivní.
1.4.2 Xxxxxxxx xxxxx
1.4.2.1 Rozpouštědlo / vehikulum
Rozpouštědlo / xxxxxxxxx v xxxxxxxxxxx xxxxxxx nesmí xxxxxxxxx xxxxxxx účinky x xxxxx x xxxxxxxxxx xxxxxx xxxxxxxx reagovat. Xxxxxxx-xx se xxxxxxxx xxxxx xxxxxxxxxxxx, musí xxx jeho použití xxxxxxxxx xxxxx x xxxxxxxxxxxxx s testovanou xxxxxx. Xxxxxxxxxx se, xxx, xxx xx xx xxxxx, xxxx xx xxxxxx xxxxx xxxxxxx xxxxx rozpouštědlo / vehikulum.
1.4.2.2 Xxxxxxxx
Xx xxxxxxx xxxxx je xxxxx pro každé xxxxxxx zařadit souběžné xxxxxxxxx a negativní (xxxxxxxxxxxx/xxxxxxxxx) xxxxxxxx. Je xxxxx xxxxxxxx xx xxxxxxx ve xxxxx xxxxxxxxx stejně.
U pozitivních xxxxxxx xx měla xxx nalezena mikrojádra xx xxxx xxx xxxxxxx, xxx lze xxxxxxxx jejich detekovatelné xxxxxxx nad xxxxxxxxx xxxxxx. Dávky xxx xxxxxxxxx kontrole xx xxxx xxx, xxx xxxx xxxxxx patrné, xxx xxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx. Xxxxxxxxx xxxxxxxx xx xxxxx xxxxxxx xxxxxxxx xxxxxxxx než xxxxxxxxxx látku a xxxxxx xxxxxxxx x xxxxxx xxxxxxx xxxxxxxxx. Xxx xx to xxxxx, xx xxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxx chemické xxxxxxx, jako xx xxxxxxxxx látka. Xxxxxxxx xxxxx xxxxxxxx pro xxxxxxxxx xxxxxxxx:
|
|
|
|
|
xxxxx xxxxxxxxxxxxxx
|
|
|
|
X-xxxxx xxxxxxxxxxxxxxx
|
|
|
|
xxxxxxxxx X
|
|
|
|
xxxxxxxxxxxxx
|
|
|
|
xxxxxxxxxx xxxxxxxxxxxxxx
|
|
&xxxx;
|
|
xxxxxxxxxxxxxxxxx
|
|
|
Xxxxxxxxx xxxxxxxx ovlivněné xxxxxxxxxxxxx xxxx vehikulem a xxxxxxxxxx stejným xxxxxxxx xxxx experimentální xxxxxxx xxxx by být xxxxxxxx xx všech xxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxx xxxxxx k xxxxxxxxx přijatelné xxxxxxxxxx xxxxx o xxxxxxxxx xxxxx x xxxxxxxxxx x x xxxxxxxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxx. Xxxxxxxx-xx xx x xxxxxxxxxxx kontrol xxxxx xxxxx xxxxx xxxxxx, xx xxxxxxxxxxxx dobou xxxxx xxxxxxxx xxxxxx xxxxxx. Xxxxxx xx xxxxx xxxxxx i xxxxxxxxxxxxx xxxxxxx, xxxxxx xxxxxxxx historické xxxx xxxxxxxxxxx xxxxx prokazující, xx xxxxxxx xxxxxxxxxxxx xxxx xxxxxxxxx xxxxxxxxxx xxxxx nepříznivé xxxx xxxxxxxxx xxxxxx.
Xxxxxxx-xx se xxxxxxxxx xxxx, xxxx xxx jako xxxxxxxx xxxxxxxxx kontrola přijatelný x xxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxx, xxxxx xxxxx x xxxxx xxxxxxxxxxxx xxxxxx x periferní krvi (xxxx. 1 - 3 xxxxx ), xxx xxxxxxxx xxxxx xxxx v xxxxxxxxxx xxxxxxx historické xxxxxxxx.
1.5 Xxxxxx
1.6 Xxxxx x xxxxxxx xxxxxx
X každé xxxxxxxxxxxxxx x xxxxxxxxx xxxxxxx musí xxx xxxxxxxxx pět analyzovatelných xxxxxxx xxxxxxx xxxxxxx.
5) Xxxxx x době, xxx se xxxxxx xxxxxxx, existují údaje x xxxxxxx xxxxxxxxxx xxxxx x xxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxxx, xx mezi xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xxxxxxxxx xxxxxxx, je testování xxxxx na xxxxxx xxxxxxx xxxxxxxxxxx. Tam, xxx humánní xxxxxxxx xxxxxxxxxxx xxxx být xxxxxxx xx xxxxxxx, xxx je xxxx xxxxxxxxx x některých xxxxxxxxxxxxxxx xxxxxxxxx, provádí xx xxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx.
1.7 Xxxxxxxxx xxxxxx
Xxxxx jednoznačně xxxxxxxxx xxxxx xxxxxxxxxx xxxxxx (např. xxxxx, xxx xxxx xxxx xxxxx x 24hodinových xxxxxxxxxxx). Xxx xxxxxx xxxxx xxxxxxxxx xxxxxxxx, xxxxx xx x xxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxx efekt; x xxxxxxx xxxxxxxxxxx výsledku xxx xxxxxx, xx xx xxxxxxx xxxxxxxx, xxxx xxxx xxxxxxx xxxxxxx dávka a xxxxxxxx xxxxxxxxxxx až xx doby xxxxxx xxxxxx. Pokud xx xxxxx o xxxxxxxx xxxxx testované xxxxx, xxxx xx x xxxxxxxxx xxxxxxxx rozdělit, xxxxxxxxx xx xxx xxxxx xx den xxxxxx x rozmezí xxxxxxxxx několika xxxxx.
Xxxx xx xxxx xxxxxxxx xxxxx xxxxxxx:
(x) Xx xxxxxxx se xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx. Xxxxxx xxxxxx xxxxx xx xxxxxxxx minimálně xxxxxxx, xxxxxx xx xxxxx xxx xx 24 xxxxxxxx x xxxxxxx xx později xxx xx 48 xxxxxxxx xx podání xxxxx, s xxxxxxxx xxxxxxxxx xxxx xxxxxx xxxxxx. Xxxxx xx xxxxxx xxxxxxxx dříve xxx po 24 xxxxxxxx, xxxx to xxx xxxxxxxxxx. Xxxxxx xxxxxxxxx xxxx xx xxxxxxxx xxxxxxxxx xxxxxxx, xxxxxx xx xxxxx xxx po 36 xxxxxxxx xx podání xxxxx, xx xxxxxxxx xxxxxxxxx xx prvním xxxxxx xxxxxx, celkově xxxx xxxxxx xxxx xxx 72 xxxxxx. Xxxxx xx x xxxxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxx, xxxx xxx xxxxx xxxxx zapotřebí.
(b) Pokud xx xxxxx xxxxxx xxxxxxx xxxx xxxxxxxx xx den (např. xxx xxxx xxxx xxxxx ve 24xxxxxxxxxx xxxxxxxxxxx), odeberou xx xxxxxx x xxxxxxx xxxxxx xxxxx jednou xxxx 18 až 24 hodinami xx xxxxxxxxx xxxxxx látky x v xxxxxxx xxxxxxxxx xxxx xxxxxx xxxx 36 a 48 hodinami xx xxxxxxxxx podání xxxxx.
5)Xx-xx xx xxxxxxxxxx, xxxxx xx mimoto xxxxxx x další xxxxxxxx xxxxxxxxx.
1.8 Xxxxxxxxx
Xxxxxxx-xx xx xxxxxx ke xxxxxxxx xxxxxxx xxxxxxxx, xxxxxxx xxxxxx x dispozici xxxxx xxxxxx údaje, xx xxxxx ji xxxxxxxx v xxxx xxxxxxxxxx za xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxx, xxxxx, xxxxxxx x xxxxxxxxx režimu, xxxx xx použijí x xxxxxx xxxxxx.
5) Při xxxxxxxx toxicity xx xxxxxxx xxx xxxxx xxxxxx interval xxxxxx xxxxxx tři xxxxx xxx, xxx pokrývaly xxxxxxx xx xxxxxxxxx xxxxxxxx k toxicitě xxxxx xxxx nulové. Xxx pozdější xxxxxx xxxxxxxx odběru xxxxxx xx pak třeba xxxxxx xxxxx xxxxxxxx xxxxx. Xx xx xxxxxxxxxx jako xxxxx xxxxxxxxxxxx xxxxxx xxxxxx xxxxxxxx, xx xxx xxxxxxx xxxxxxx xx xxxxxxx režimu podávání xx účinky xxxx xxxxxxx. Xxxxx, xxx x nízkých xxxxxxxxxxx xxxxxxx vykazují xxxxxxxxxxx xxxxxxxxxxx aktivitu, xxxx xxxx xxxxxxx xxxx xxxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxx z xxxxxx xxxxxxxx xxx stanovení xxxxx x xxxxxxxxxxx xx xxxxxx xx xxxxxxx. Xxxxxxxx xxxxx xxxx být xxxx xxxxxxxxxx jako dávka, xxxxx xxxx k xxxxxxx xxxxxxx toxicity x xxxxxx xxxxx (xxxx. xxxxxx xxxxxx xxxxxxxxx erytrocytů x xxxxxxxxx xxxxx xxxxxxxxxx x kostní dřeni xxxx. xxxxxxxxx xxxx).
1.9 Xxxxxxx xxxx
Xxxxxxxx xxxx xxx xxxxx minimálně 2000 xx/xx xxxxxxxxx x xxxxx xxxxx xxxx xx xxxx xxxxxxx xxxxxxxx x xxxxx xxx xxxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxx xxxxxx x xxxxxxxx xx xx xxxxxxx xxxxx x látkách x xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx genotoxicita, xxxxxx být xxxxxxxxx xxxx xxxxxx xx xxxxxxx xxx dávkových xxxxxx. Xxx dlouhodobé xxxxxx je xxxxxxx xxxxx 2000 mg/kg xxxxxxxxx xx xxx xxx xxxx xxxxxx xx 14 xxx x 1000 xx/xx xxxxxxxxx při xxxx xxxxxx delší než 14 xxx. Xxxxx xxxxxxxxx humánní expozice xxxx xxx xxxxxxxxx xxxxxx v limitním xxxxx xxxxxxx úrovně xxxxx.
1.10 Aplikace látky
Testovaná xxxxx se xxxxxxx xxxxxxxx xxx' xxxxxxxxx xxxxxx, xxxx xxxxxxxxxxxxxxxxx xxxxxxx. X odůvodněných xxxxxxxxx xxxxx xxx xxxxxxxxxx x xxxx xxxxxxx xxxxxxxx. Maximální xxxxx xxxxxxxx, xxxxx xx xx xxxxxx xxxx xxxxxxx najednou xxxxxxx, xxxxxx xx xxxxxxxxx pokusného zvířete x xxxx xxxxxxxxx 2 xx/100 g xxxxxxxxx; vyšší dávky xxxx být xxxxxxxxxx. X výjimkou xxxxxxxxxx xxxx xxxxxxxx xxxxx, xxx xxxxxxxx xxxxxxxx xxx xxxxxxx koncentracích xxxxx účinky, je xxxxx upravit koncentrace xxxxx tak, xxx xxxxx xxx xx xxxxx xxxxxxxxx xxxxxxxx xxxxxx a xxxxxxxxxxxxxx xx xxx objemová xxxxxxxxxxx.
1.11 Xxxxxxxx kostní xxxxx/xxxx
Xxxxx xxxxxx xxxxx xx xxxxxxx xxxxxxxxx x xxxxxx xxxx xxxxx xxxxxxxx po xxxxxxxx xxxxxxx. Běžným xxxxxxxx se kostní xxxx vyjme x xxxxxx xxxx xxxxx, xxxxx se xxxxxxx x xxxxxx xxxxxxxxxx xxxxxxxx. Xxxxxxxxx xxxx xx xxxxxxx z xxxxxx xxxx nebo xxxx xxxxxx xxxx. Xxxxxx buňky se xxxxxxxx xx xxxxxxxxx xxxxx xxxxxx,
5) xxxx xx xxxxxxx nátěry, xxxxx xx posléze xxxxxx. Xxxxxxxx xxxxxxx xxxxxxxxxxxx xxx XXX (xxxx. xxxxxxxxxx xxxxxx
5) xxxx Xxxxxxx 33258 x pyroninem-Y
5)) se xxxxx eliminovat některé x artefaktů xxxxxxxxxxxx xxx použití barviva, xxxxx xxxx XXX xxxxxxxxxx. Xxxx xxxxxx xxxxxxxxx, xx by xx xxxxxx použít xxxxx xxxxxxx (např. Xxxxxx). Lze xxxxxx x xxxxx systémy - například kolony xx xxxxxxxx celulózy x xxxxxxxxxx xxxxx x jádrem
5) - xxxxx xxxx metody xxxx x laboratoři xxxxxxx používány xxx xxxxxxx xxxxxxxxxx.
1.12 Analýza
U xxxxxxx jedince xx xxxxxxx podíl xxxxxxxxx xxxxxxxxxx z xxxxxxxxx xxxxx xxxxxxxxxx (nezralé + zralé). X xxxxxx xxxxx xx xxxxxx x xxxxxxx xxxxxx xxxxx minimálně 200 erytrocytů x x xxxxxxx použití xxxxxxxxx xxxx xxxxxxxxx 1000 xxxxxxxxxx.
5) Xxxxxxx xxxxxxxxx (včetně xxxxxxxxxxx x xxxxxxxxxxx kontrol) xx před xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx zakódují. X xxxxxxx xxxxxxx xx xxxxxxxxxxx minimálně 2000 xxxxxxxxx xxxxxxxxxx x xxxxxxxxx xx xxxxx erytrocytů x xxxxxxxxxx. Xxxxxxxxxx xxxxxxxxx xxx xxxxxx xxx, xx se mikrojádra xxxxxxxxx xx zralých xxxxxxxxxxxx. Xxx xxxxxxx xxxxxxxxx nemá xxx xxxxx nezralých xxxxxxxxxx x xxxxxxxxx xxxxx xxxxxxxxxx menší xxx 20 % hodnoty x xxxxxxxx. Xxxxx xxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxx po xxxx xxxx xxxxx nebo xxxxx, xxx také xxxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxxxx 2000 xxxxxxx erytrocytů na xxxxxxx xxxxxxx. Možnou xxxxxxxxxxxx k xxxxxxxxxx xxxxxxxxxxxxx jsou xxxxxxx xxxxxxxxxxx xxxxxxx (xxxxxxx xxxxxx x xxxxxxxxx xxxxxxxxxxxx analýza - xxxx xxxxxxxxx), pokud xxxx xxxxxxxxxx x xxxxxxxxxx.
2 ÚDAJE
2.1 Xxxxxxxxxx xxxxxxxx
xxxxx x jednotlivých xxxxxx se zaznamenávají xx xxxxxxx. Experimentální xxxxxxxxx xx zvíře. X xxxxxxx xxxxxxx xx xxxxxx xxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxx nezralých xxxxxxxxxx x mikrojádry x podíl nezralých xxxxxxxxxx ze xxxxx xxxxxxxxxx. Xxxxx byl xxxx xxxxxxxx xxxxxxxxxxx xx xxxx xxxx xxxxx nebo xxxx, xx xxxxx xxxxx xxxx xxxxx x xxxxxxx xxxxxxxxxxxx (xxxxx xxxx xxxxxxxxxx). Podíl xxxxxxxxx erytrocytů z xxxxxxxxx xxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxxx s xxxxxxxxxx xx udává xxx xxxxxxx jedince. Xxxxxx-xx xxxxx doklady o xxx, xx obě xxxxxxx reagují xxxxxxxx, xx xxxxx xxxxx xx xxx xxxxxxx xxx statistickou xxxxxxx xxxxxxx.
2.2 Xxxxxxxxxxx a xxxxxxxxxxxx xxxxxxxx
Xx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xx xxxxxxx xxxxxxx xxxxxxxx, xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxx látky závislý xxxxxx počtu xxxxx x xxxxxxxxxx xxxx xxxxxxxx nárůst xxxxx xxxxx x xxxxxxxxxx xx skupině x xxxxxxxxxxxx dávkou xxx xxxxxx xxxxxxx xxxxxxxxx xxxxxx xxxxxx. Xxxxxxx xx xxxxx uvážit xxxxxxxxxxx xxxxxxxxxx xxxxxxxx. Xxx xxxxxxxxxxxxx xxxxxxxx xxxxx xx mohou xxxxxx xxxxxxxxxxx metody.
5) Xxxxxxxxxxx xxxxxxxxxx by xxxx xxxxxx být xxxxxxx určujícím xxxxxxxx xxxxxxxxxxx xxxxxxxx. Nejednoznačné xxxxxxxx xx xxxxx xxxxxxxx dalším xxxxxxxxxx, xxxxxxx xx modifikovaných xxxxxxxxxxxxxxxx xxxxxxxx.
Xxxxxxxxx xxxxx, xxx jejímž xxxxxxx xxxxxxxx xxxxxxxxx výše xxxxxxx kritéria, se x tomto xxxxxxx xxxxxxxx za xxxxxxxxxxx.
Xxxxxxx xxxxxxxxxxx xxxx poskytuje xxxxxxxxxxx pozitivní xxxx xxxxxxxxx xxxxxxxx, x xxxxxxxxxxx případech xxxx xxxxx ze xxxxxxxxx xxxxxxx xxx xxxxxxx x aktivitě testované xxxxx xxxxxxxxxxx závěr. Xxxxxxxx xxxxx být xxxxx nejednoznačné xxxx xxxxxxxxxxxxx, i když xx xxxxxxxxxx xxxxxxxxxx xxxxxxx.
Xxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxx, že xxxxx xxxxxxxx tvorbu xxxxxxxxxx, jako xxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx mitotického xxxxxxx x xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxxxxx xxxxxxxx ukazují, xx xx xxxxxx xxxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx x xxxxxx dřeni xxxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxx xxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx.
Xx xxxxx xxxxxxxx, xxxx xx pravděpodobnost, xx xxxxxxxxx xxxxx xxxx xxxxxx xxxxxxxxx, nebo xxxxx xxxxxxxxxxx cílovou xxxx xxxxxxx (xxxx. xxxxxxxxx toxicita).
3 XXXXXXX XXXXXX, XXXXXXXX POKUSU X XXXXXXXXX XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx x x xxxxxxx xxxxxx je xxxxx xxxx protokol.
Ve xxxxxx o xxxxxxx xxxxxx xx xxxxx xxxxx tyto xxxxxxxxx:
Xxxxxxxxxxxx/xxxxxxxxx
Xxxxxxx xxxxxxx.
- xxxxxxx xxxxxxxxx xxxx/xxxx,
- xxxxx, xxx x xxxxxxx xxxxxxx,
- xxxxx, xxxxxx xxxxxxxx, xxxxxx xxxx.,
- xxxxxxxx xxxxxxxxxxxx zvířat na xxxxxxx xxxxx, xxxxxx xxxxxxxxxxxx xxxxxxx, xxxxxxx x směrodatných xxxxxxxx xxx xxxxxxxxxx xxxxxxx.
Xxxxxxxx xxxxxx:
- xxxxxxxxx x xxxxxxxxx (xxxxxxxxxxxx/xxxxxxxxx) kontroly,
- xxxxx xx xxxxxx xxx xxxxxx xxxxxxx, xxxx-xx xxxxxxxxx,
- xxxxxxxxxx xxxxx xxxxxxxxx xxxxx,
- xxxxxxxxxxx o xxxxxxxx xxxxxxxxx látky,
- xxxxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxx,
- zdůvodnění xxxxx xxxxxxxx,
- případné xxxxxx x ověření, že xx xxxxx dostala xx xxxxxxxxx xxxxx xxxx do xxxxxx xxxxx,
- xxxxxxxx xxxxxx xxxxxxxxxxx látky v xxxxxxx/xxxxx xxxx (xxx) xx xxxxxxxxx dávku (xx/xx xxxxxxxxx),
- xxxxxxxxxxx x kvalitě xxxxxxx x xxxx,
- xxxxxxxx xxxxx xxxxxxxx testované xxxxx a xxxxxx xxxxxx,
- xxxxxx xxxxxxxx xxxxxxxxxxxxxxx preparátů,
- xxxxxx xxxxxx xxxxxxxx,
- xxxxxxxx xxx hodnocení nezralých xxxxxxxxxx x xxxxxxxxxx,
- xxxxx xxxxxxxxxxxxx buněk x každého jedince,
- xxxxxxxx, xxxxx xx xxxxxx hodnotí xxxx xxxxxxxxx, negativní xxxx xxxxxxxxxxxxx.
Xxxxxxxx:
- xxxxxx xxxxxxxx,
- xxxxx počtu xxxxxxxxx xxxxxxxxxx k xxxxxxxxx xxxxx xxxxxxxxxx,
- počet xxxxxxxxx erytrocytů x xxxxxxxxxx xxx xxxxxxx xxxxxxx zvlášť,
- xxxxxxxx xxxxx ± xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxx xxxxxx xxxxxxx,
- xxxxx xxxxx - xxxxxx, xx-xx to xxxxx,
- xxxxxxx xxxxxxxxxxx analýzy x metody,
- údaje xx souběžných a xxxxxxxxxxxx xxxxxxxxxxx xxxxxxx,
- xxxxx xx xxxxxxxxxx xxxxxxxxxxx kontrol.
Diskuse xxxxxxxx.
Xxxxxx.
X.13/14 XXXXXXXXXX - XXXX XXXXXXXXXX MUTACÍ X XXXXXXXX
1 XXXXXX xx x souladu x xxxxxx Xxxxxxxxxx společenství.
5)1.1 Xxxx
Xxx xxxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxx xx xxxxxxxxx x detekci xxxxxxxx xxxxxx kmeny Xxxxxxxxxx xxxx imurium (xxxxxxxxxx xx xxxxxx x xxxxxxxxxxxxx xxxxxxxx) x xxxxx Xxxxxxxxxxx xxxx (xxxxxxxxxx ve xxxxxx x xxxxxxxxxxxxx xxxxxxxxx). Xxxxxx xxxxxxxxx xxxxxxx lze xxxxxxxxx xxxxxx xxxxxx vzniklé xxxxxxxxxxx xxxxxxxxxx, xxxxx xxxx xxxxxx jednoho xxxx několika nukleotidů x chromozómu xxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxx.
5) Princip xxxxxxxxxxxxx testu xxxxxxxxxx xxxxxx xxxxxxx v xxx, že xx xxxxxxxx mutace, xxxxx xxxxxx xxxxxxx xxxxxx xxxxxxxx x xxxxxxxxxx xxxxx xx původního xxxxx x obnovuje xx funkční schopnost xxxxxxxx xxxxxxxxxxxx určitou xxxxxxxx xxxxxxxxxxxxx. Xxxxx xxxxxxx bakteriální xxxxx xx detekována xx xxxxxxx xxx schopnosti xxxx za xxxxxxxxxxxxx xxxxxxxxxxxxx, kterou xxxxxxxx xxxxxxxx xxxxxxxx xxxx.
Xxxxxx xxxxxx xxxx u xxxxxxx xxxxxxxx xxxx xxxxxxxxxxx nemocí x xxxxxxxx přesvědčivé xxxxxxx xxxx, že xxxxxx xxxxxx x xxxxxxxxxx x xxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxx x xxxxxxx x pokusných xxxxxx xxxx při vzniku xxxxxx. Bakteriální xxxx xx xxxxxxxx mutace xx rychlý, xxxxx x relativně xxxxxxxxxx. Xxxx xxxxxxxxxxx xxxxx xx xxxxxxxxx charakteristikami, xxxx xxxx xxxx xxxxxxxxxx pro detekci xxxxxx, včetně xxxxxxxxx xxxxxxxx DNA x xxxxxxx xxxxxxx, xxxxxxx xxxxxxxxxxxx buněk xxx xxxxx xxxxxxxx x xxxxxxxxx systémů xxxxxxxx XXX xx xxxxxxxx xxxxxxxx xxxxxxx reparace XXX, xxx xxxx xxxxxxxx x xxxxxx. Xxxxxxxxx testovacích xxxxx xxxxxxxx xxxxxx některé xxxxxxxx informace x xxxxxx mutací, jež xxxx vyvolány genotoxickými xxxxxxx. Xxx xxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxx xx x xxxxxxxxx xxxxx xxxxxxxx databáze xxxxxxxx xxx xxxxxxx xxxxx xxxxxxxx x xxxx vypracovány xxxxxxxxx xxxxxx pro testování xxxxxxxxxx o různých xxxxxxxxx-xxxxxxxxxx vlastnostech, xxxxxx xxxxxxxxxx xxxxxxxx.
1.2 Definice
Test xxxxxxxxxx mutací x xxxxxxxx xxxxx Xxxxxxxxxx xxxxx murium xxxx Xxxxxxxxxxx xxxx slouží xx xxxxxxxx xxxxxx x kmeni xxxxxxxx xx určité aminokyselině (xxxxxxxxx resp. xxxxxxxxxx), xxx xxxxx xx xxxxxx xxxxx, xxxxx xx na xxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxx.
Xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxx xxxx xxxx xxxxx xxxxxxxxxxx xxxxx bází x XXX. Xxx xxxxxxxxx xxxxx xxxx x xxxxxx xxxxx xxxxx xx xxxxx xxxxxxx mutace xxxx xx xxxxx místě xxxxxxxxxxxxx xxxxxx.
Xxxxxxxxxx xxxxxxxx (xxxxxxxx xxxxxxxxxxxx posunové xxxxxx) jsou xxxxx, xxx xxxxxxxxx xxxxxxx xxxx odebrání jednoho xxxx více xxxx xxxx x DNA, xxxx xx xxxx xxxxx xxxxx v XXX.
1.3 Xxxxxxx xxxxx
X xxxxxxxxxxxx testu xx xxxxxxxxx prokaryotické xxxxx, xxxxx xx xx xxxxxxx buněk xxxx x xxxxxx xxxxx xxxxxxxxxxx, xxxxxxxxxxxxx struktuře x procesech xxxxxx XXX.
Xxxxx xx xxxxx xxxxxx xxxxxxxx exogenní xxxxx xxxxxxxxxxx xxxxxxxx. Xxxxxxx metabolické xxxxxxxx xx xxxxx xxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxx xx xxxx, xxxxx xxxx xxxxxxxxxxx přímé xxxxxxxxx x mutagenní x xxxxxxxxxxxx xxxxxxx dané xxxxx x xxxxxxxxxxx xxxxx.
Xxxxxxxxxxx test reverzních xxxxxx xx běžně xxxxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxx aktivity xxxxxxxxxxxx xxxxxx mutace. Xxxxxx xxxxxxxx xxxxxxxx xx xxxxxxxxx, xx xxxxx chemikálie, xxxxx xxxx x tomto xxxxx pozitivní, vykazují xxxx v jiných xxxxxxx mutagenní xxxxxxxx. Xxxxxxxx ovšem i xxxxxxxx xxxxxxxxxxx xxxxx, xxx se tímto xxxxxx xxxxxxxx; xxxxxxx xxxxxx xxxxxxxxxx může xxx xxxxxxxxxx xxxxxx xxxxxxxxxxxxxxx xxxxxxx, xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxx xxxxxxx v xxxxxxxxxx xxxxxxxxxxx. Xx xxxxx xxxxxx xxxxxxx, xxx xxxxxxxxx bakteriálního xxxxx xxxxxxxx mutace xxxxxxx, mohou vést x xxxx, xx xx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxx.
Xxxxxxxxxxx xxxx reverzních xxxxxx xxxx být xxxxxxxx xxx určité xxxxx xxxxxxxxxx xxxxx, xxxxxx xxxx xxxxxxxxx xxxxxxx xxxxx baktericidní sloučeniny (xxxxxxxxxx xxxxxx antibiotika) x xxxxx, o xxxxx se předpokládá xxxx xx, xx xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx savčích xxxxx (xxxxxxxxx některé xxxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxx xxxxxxx xxxxxxxxxx); v xxxxxxx xxxxxxx mohou xxx xxxxxxxxx testy xx mutace x xxxxx.
Xxxxx sloučeniny, jež xxxx pří xxxxx xxxxx xxxxxxxxx, xxxx xxxxxxxx xxxxxxxxxxxx pro xxxxx, xxxxx xxxxxxxx xxxx xxxxxxxxx; závisí xx chemické xxxxx, x xxxxxxxx xxxxxxxxxxx, xxxxx xxxxx xxxxxx xxxxxxxx xxxxxx, xxxxxxx xxxxxx jiným, xxxxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxxx, xxxxx x xxxxxxxxxxxxx xxxxxxx xxxxxxxxx.
1.4 Xxxxxxx xxxxxx
Xxxxxxxx xxxxxxxxxxxxx buněk xx xxxxxxx působení xxxxxxxxx xxxxx za xxxxxxxxxxx x za xxxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxx aktivace. Xxx xxxxxxxx miskové xxxxxx "xxxxx xxxxxxxxxxxxx" se xxxxxxxx xxxxx x xxxxxxx agarem x xxxxxx na misky x xxxxxxxxx xxxxxx xxxxx. Xxx preinkubační xxxxxx xx pokusná xxxx inkubuje x xxxxx s vrchním xxxxxx x xx xxxxx se xxxxxx xx xxxxxxxxx xxxxxx xxxx. Xxx xxxx xxxxxxxx xx xxx xx xxx xxx xx xxxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxx a xxxxxxxx se porovná x počtem spontánně xxxxxxxxxxxxx xxxxxxx xx xxxxxxxxxxx xxxxxxx s xxxxxxxxxxxxx.
Xx xxxxxxx xxxxxxx xxxxxxx pro xxxxxxxxx xxxxx. X xxxx xxxxxxxxxxx jsou klasická xxxxxxx metoda ["xxxxx xxxxxxxxxxxxx"],
5) xxxxxxxxxxxx xxxxxx,
5) xxxxxxxxxx metoda
5) x xxxxxxxxx xxxxxx.
5) Xxxx xxxx xxxxxxx xxxxxx xxxxxxxxxx xxx testování xxxxx nebo xxx.
5)Xxxxxxx xxxxxxx x xxxxx xxxxxx xx xxxxxx xxxxxx metody xxxxx xxxxxxxxxxxxx a metody xxxxxxxxxxxx. Xxx xxxx xxxxxx xxxx xxxxxxxxxx xxx xxxxxxxxxxx jak x metabolickou aktivací, xxx xxx xx. Xxxxxxx xxxxx xx xxxxxxxx účinněji preinkubační xxxxxxx; jedná se x xxxxxxxx třídy, xxx xxxxxxx alifatické xxxxxxxxxxx x krátkým xxxxxxxx, xxxxxxxxx xxxx, xxxxxxxx, azobarviva x xxxxxxxxxxxxxxx, xxxxxxxxxxxxxxx xxxxxxxxx, xxxxxxx sloučeniny x xxxxxxxxxxxxxxx.
5) Xxxx bylo xxxxxxxx, xx xxxxxxxx xxxxxx xxxxx xxxxxxxx, xxxxx se pomocí xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxx neodhalí. Na xx xx xxxxx xxxxxxxx xxxx xx "xxxxxxxxx xxxxxxx", k xxxxxxx xxxxxxx je xxxxx xxxxxx xxxxxx xxxxx. Byly xxxxxxxxxxxxxx xxxxxxxxxxx "xxxxxxxxx případy" (xxxxx s příklady xxxxxxx, xxxxx se xxxx pro jejich xxxxxxx xxxxxx): azobarviva x xxxxxxxxxxxxxxx,
5) xxxxx x xxxxxx chemikálnie
5) x xxxxxxxxx.
5) Xxxxxxxx xx xxxxxxxxxxxx postupu xx xxxxx vědecky xxxxxxxxx.
1.5 Popis metody
1.5.1 Xxxxxxxx
1.5.1.1 Bakterie
Čerstvé bakteriální xxxxxxx xx xxxxxxxxx xx xxxxxxxx xxxxxxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxxxxxxx xxxxxx růstu (xxxxxx 109 xxxxx/xx). Xxxxxxx x pozdním xxxxxxxxxxxx xxxxxx xx xxxxxxxxxxx. Xxxxxxxx je, xxx xxxxxxx použité xxx xxxxxxxxxx obsahovaly xxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxxx. Xxxx xx xx xxxxxxxx xxx' z xxxxxxxxxxxx xxxxx xxxxxxxxx xxxxxx, xxxx x xxxxxxxxxxxx testech stanovením xxxxx xxxxxxxxxxxxxxx xxxxx xxxxxxxxx xx miskách.
Doporučená xxxxxxxxx xxxxxxx činí 37 °C.
Použije xx xxxxxxxxx pět bakteriálních xxxxx, které xxxxx xxxxxxxxx xxxxx xxxxx X. typhi xxxxxx (XX1535; TA1537 xxxx XX97x nebo XX97; XX98; x TA100); x xxxxx xxxx xxxxxxxxx xxxxxxxxxxxx a xxxxxxxxxxxxxxxxxx xxxxxxxx xxxx xxxxxxx laboratořemi. Xxxx xxxxx kmeny X. xxxxx xxxxxx xxxx xx xxxxxxxxx xxxxxxxxx xxxxx páry xxxx XX a xx xxxxx, xx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx, xxxxx vyvolávající xxxxxxx vazby x xxxxxxxxx. Xxxx látky xx dají xxxxxxxxx xxxxxx kmenů E. xxxx XX2 xxxx X. typhi xxxxxx XX 102,
5) které xxxx xx xxxxxxxxx xxxxxxxxx xxxxx xxx xxxx XX. Xxxxx xx doporučená xxxxxxxxx xxxxx tato:
- X. xxxxx xxxxxx XX 1535,
- X. xxxxx xxxxxx XX 1537 xxxx XX97 xxxx XX97x,
- S. xxxxx xxxxxx TA98.
- S5 xxxxx xxxxxx XX 100 a
- X. xxxx XX2 xxxX xxxx X. xxxx XX2 xxxX (pKM 101) xxxx X. xxxxx xxxxxx XX 102.
X xxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxx xxxx být xxxxxxxxxxxx xxxxxx TA102 xxxx xxxxxx XXX xxxxxxxxx xxxxxxxxxxxx xxxx X. xxxx (např. X. xxxx XX2 nebo X. coli XX2 (xXX 101)).
Xx třeba xxxxxx zavedených postupů xxxxxxxx zásobní xxxxxxx, xxxxxxx xxxxxxx x xxxxxxxxxx. Xxx každý xxxxxxxx xxxxxxxx xxxxxxx xxxxxxx xx xxxxx xxxxxxxx xxxxxxxxx xx xxxxxxxxxxxxx xxxxx pro xxxx (xxxxxxxx x xxxxxxx xxxxx S. xxxxx xxxxxx, xxxxxxxxx x xxxxxxx xxxxx X. xxxx). Xxxxxxx xx třeba xxxxxxxxxxxx x xxxxx xxxxxxxxxxx xxxxxxxxxxxxxxx, x to: xxxxxxxxxx xx nepřítomnost X-xxxxxx xxxxxxxx tam, xxx xx přichází x úvahu (xxxx. xxxxxxxxxx vůči xxxxxxxxxx x kmenů TA98, XX 100 x XX97x xxxx XX97, XX2 xxxX (xXX101) x xxxxxxxxxx vůči xxxxxxxxxx + xxxxxxxxxxxx x kmene TA 102); xxxxxxxxxx xxxxxxxxxxxxxxxxxx xxxxxx (tj. xxx xxxxxx u X. xxxxxxxxxxx xxxxxx citlivosti xxxx krystalové violeti x xxxX xxxxxx x E. xxxx xxxx uvrB xxxxxx x X. xxxxxxxxxxxx xxxxxx citlivosti na xxxxxxxxxxxx xxxxxx).
5) Xxxxxxx xxxxx xxxx mít xxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx ve frekvenčním xxxxxxx očekávaném podle xxxxxxxxxxxx kontrolních dat xxxx xxxxxxxxxx x xxxxx xxxxx x x rozmezí xxxxxxxx x xxxxxxxxxx.
1.5.1.2 Xxxxxx
Xxxxxxx xx vhodný xxxxxxxxx xxxx (xxxx. x Xxxxxxxxx-Xxxxxxxxxx xxxxxxxxxx xxxxxx X x xxxxxxxx) x xxxxxx agar xxxxxxxxxx xxxxxxxx a xxxxxx xxxx tryptofan xxxxxxxxxx xxxxxxx xxxxxx xxxxx.
5)1.5.1.3 Xxxxxxxxxxx xxxxxxxx
Xxxxxxxx xx xxxxxxxx testované xxxxx xxxxxxx xxx xx přítomnosti, xxx xx nepřítomnosti xxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx. Xxxxxxxxxx se xxxxxxx xxxxxxxxxx suplementovaná post-mitochondriální xxxxxx (X9) xxxxxxxxxx x jater xxxxxxxx xx xxxxxxx enzymů xxxxxxx, xxxx xx Xxxxxxx 1254
5) nebo xxxxxxxxx xxxxxxxxxxxxx a ß-xxxxxxxxxxxx.
5) Xxxx-xxxxxxxxxxxxxxx frakce xx obvykle xxxxxxx x xxxxxxxxxxxxx mezi 5 a 30 % v/v ve xxxxx X9. Xxxxx x xxxxxxxx metabolického xxxxxxxxxxx xxxxxxx xxxxx xxxxxxx xx xxxxx xxxxxxxxx xxxxxxxxxx V xxxxxxxxx xxxxxxxxx xxxx xxx xxxxxx xxxxxx xxxx-xxxxxxxxxxxxxxx frakci x xxxxxxxx xxxxxxxxxxxxx X xxxxxxxxx x xxxxxxxxxxxxxx xxxx xxx xxxxxxxxx xxxxxx xxxxxxxx systém xxxxxxxxxxx aktivace.
5)1.5.1.4 Xxxxxxxxx xxxxx/xxxxxxxx
Xxxxx xxxxx xx xxxx xxxxxxxxx xx xxxxxxxx rozpustí xxxx xx připraví jejich xxxxxxxx xx xxxxxxx xxxxxxxxxxxx xxxx vehikulu x xxxxxxxx se xxxxx Xxxxxxx xxxxx xx mohou do xxxxxxxxx systému xxxxxxxx xxxxx xxxx se xxxxxxx xxxx. Xx xxxxx používat čerstvé xxxxxxxxx, xxxxxx údaje x stabilitě xxxxxxxxx, xx xxxxxx xxxxx xxxxxxxxxx xx xxxxxxxxxx.
1.5.2 Xxxxxxxx xxxxx
1.5.2.1 Xxxxxxx xxxxx (viz 1.5.1.1)
1.5.2.2 Xxxxxxxxxxx
Xx xxxxxxxxx, xxxxx xx xxxxx vzít x xxxxx při xxxxxxxxx nejvyššího xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx, xxxxx xxxxxxxxxxxx a xxxxxxxxxxx x xxxxxxx xxxxx, xxxxx xx x xxxxxxxx xxxxxxx.
Xxxx xxx xxxxxx xxxxxxxx xxxxxxxx x xxxxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxxx. Xxxxxxxxxxxx xx dá xxxxxxx snížením xxxxx xxxxxxxxxxxxx xxxxxxx, xxxxxxxxx xxxx zmenšením růstu xx xxxxxx xxxx xxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxxx Za xxxxxxxxxxx xxxxxxxxxxxxx aktivačního xxxxxxx xx xxxx xxxxxxxxxxxx xxxxxx Nerozpustnost xx xxxxxxxx xxxxx xxxxxxx v xxxxxxx xxxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxxxxxxxx x xxxxxx okem.
Doporučená xxxxxxxxx xxxxxxx koncentrace xx x xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxx 5 xx/xxxxx xxxx. 5 µx/xxxxx. X xxxxxxxxxxxxxxx xxxxx, xxx v xxxxxx koncentracích xxxxxx xxxxxxxxx, by xxxxx xxxx xxxxxxx xxxxxxxxxxx xxxx xxx v xxxxxxx xxxxxxx směsi xxxxxxxxxxxxx Testované xxxxx, xxx xxxx xxxxxxxxxxx xxx xx koncentrací xxxxxxx xxx 5 xx/xxxxx resp. 5 µx/xxxxx, xx testují xx xx cytotoxické xxxxxxxxxxx Sraženina xxxxx xxxxx xxx xxxxxxxxxxxxx.
Xxxxxxx xx xxxxxxxxx pěti xxxxxxx analyzovatelných xxxxxxxxxxx xx zhruba xxxxxxxxxxxxxxxx xxxxxxxxxx (xx. √10) xxxx jednotlivými body x prvotním xxxxxxxxxxx Xxxxxx-xx xx xxxxxxxxxxxx xxxxxxxxx, může xxx xxxxxx xxxxxxxx xxxxx. Xxxxxxxxx za koncentrací xxxxxxx než 5 xx/xxxxx xxxx. 5 µx/ xxxxx xxxxxxxx x xxxxx, xxxxxxx-xx xx xxxxx obsahující xxxxxxxxx xxxxxxxx potenciálně xxxxxxxxxxx xxxxxxxx.
1.5.2.3 Negativní x xxxxxxxxx xxxxxxxx
Xxxxx xxxx xxxx zahrnovat x xxxxxxxxx kmenově xxxxxxxxxxx xxxxxxxxx x xxxxxxxxx (xxxxxxxxxxxx nebo xxxxxxxxx) kontrolu, xxx x xxxxxxxxxxxx aktivací, xxx xxx xx. Xxx xxxxxxxxx xxxxxxxx xx xxxx takové xxxxxxxxxxx, xxx xxxxxxxxx xxxxxxxxxxx xxxxxx xxxxx.
X xxxxx x metabolickým xxxxxxxxxx systémem se xxxxxxxxxx xxxxx xxx xxxxxxxxx xxxxxxxx xxxx xxxxx xxxxxxxxx typu xxxxxxxxxxxxx kmene.
Příklady xxxxx, xxx xxxx xxxxxx xxx xxxxxxxxx xxxxxxxx x testech x xxxxxxxxxxxx xxxxxxxx, xxxxx xxxxxxx:
|
|
|
|
|
9,10-xxxxxxxxxxxxxxxx
|
|
|
|
7,12-xxxxxxxxxxxx[x]xxxxxxxx
|
|
|
|
xxxx[x]xxxxx
|
|
|
|
2-xxxxxxxxxxxxx
|
|
|
|
xxxxxxxxxxxxx
|
|
|
|
xxxxxxxxxx xxxxxxxxxxxxxx
|
|
&xxxx;
|
Xxxxxxxxxxx látka xx xxxxxxx xxxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxx:
2-xxxxxxxxxxxxx xx nepoužívá xxxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxx X9. Xxxxx xx 2-aminoantracen xxxxxxx, xx xxxxx xxxxxx šarži X9 xxxxxxxxxxxxxxx xxxx mutagenem, xxxxx vyžaduje xxxxxxxxxxxx xxxxxxxx mikrosomálními xxxxxx, xxxx. xxxx[x]xxxxxxx, xxxxxxxxxxxxxxxxxxxxxx.
Xxxxxxxx xxxxx, jež xxxx xxxxxx xxx xxxxxxx xxxxxxxxxxx xxxxxxxxx kontrolu x xxxxxxx xxx xxxxxxxxxx systému xxxxxxxxxxx xxxxxxxx, xxxxx tato xxxxxxx:
|
|
|
|
&xxxx;
|
|
xxxx xxxxx
|
|
|
XX 1535 x XX 100
|
|
2-nitrofluoren
|
|
|
TA 98
|
|
9-xxxxxxxxxxxx
|
|
|
XX 1537, XX 97 a TA 97x
|
|
XXX 191
|
|
|
XX 1537, XX 97 a XX 97x
|
|
xxxxx-xxxxxxxxxxxx
|
|
|
XX 102
|
|
xxxxxxxxx X
|
|
|
XX2 xxxX x XX 102
|
|
X-xxxxx-X-xxxxx-X-xxxxxxxxxxxxxxx
|
|
|
XX2, XX2xxxX x WP2uvrA(pKM 101)
|
|
4-xxxxxxxxxxxxx-1-xxxx
|
|
|
XX2, XX2xxxX x XX2xxxX(xXX 101)
|
|
xxxxxxxxxxx (XX2)
|
|
&xxxx;
|
xxxxx obsahující xxxxxxxx
|
X xxxxxxxxx kontrole xxx xxxxxx i xxxx xxxxxx xxxxxxxxxx xxxxx. Xxxx-xx xxxxxxxx, xx třeba xxxxxx xxxxxxx xxxxxxxxxx se xxxxxxx x xxxxxxxx xxxxx.
Xx xxxxx xxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxxx z xxxxxxxxxxxx xxxx xxxxxxxx samotného, xxx testované látky, xx xxxxxxx xx xxxxx zachází xxxxxx xxxx xxx xxxxxxx xxxxxxxxx xxxxx. Mimoto xx xxxxxxx x xxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxxxxxx látkou, xxxxxx existují historické xxxxxxxxx xxxxx xxxxxxxxxxx, xx xxxxxxx rozpouštědlo xxxxxxxxxx xxxxx xxxxxx xx xxxxxxxxx xxxxxx.
1.5.3 Xxxxxx
Xxx xxxxxxxx xxxxxxx xxxxxx
5) xxx xxxxxxxxxxx xxxxxxxx se xxxxxxx xxxxx 0,05 nebo 0,1 xx xxxxxxxxxxx xxxxxxx, 0,1 xx xxxxxxx xxxxxxxxxxx xxxxxxx (xxxxxxxxxx zhruba 10
8 xxxxxxxxxxxxxxx xxxxx) x 0,5 xx sterilního xxxxx x 2,0 xx xxxxxxxx agaru. X testech x xxxxxxxxxxxx xxxxxxxx xx xxxxxxx mísí 0,5 xx metabolické xxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxx-xxxxxxxxxxxxxxx xxxxxx (x xxxxxxx 5 - 30 % x/x v metabolické xxxxxxxxx xxxxx) x 2,0 ml vrchního xxxxx xxxxxxxx x xxxxxxxxxx x xxxxxxxxxx xxxxxx /testovaným xxxxxxxx. Xxxxx xxxxx zkumavky xx promísí x xxxxxx xx povrch xxxxx s minimálním xxxxxx. Xxxxxx xxxx xx nechá před xxxxxxxx ztuhnout.
Při xxxxxxxxxxxx xxxxxx
3) xx testovaná xxxxx / xxxxxxxxx xxxxxx xxxxx preinkubovat x xxxxxxxx xxxxxx (xxxxxxxxxxx xxxxxx 10
8 xxxxxxxxxxxxxxx xxxxx) x xxxxxxxxx xxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx (0,5 xx) xxxxxxx xx xxxx 20 xxx xxxx xxxx xxx 30 - 37 °X; xxxxx xx xxxxx x xxxxxxx xxxxxx x xxxxxx xx xxxxx x xxxxxxxxxx agarem. Xxxxxxx xx mísí 0,05 nebo 0,1 xx xxxxxxxxx látky/testovaného xxxxxxx, 0,1 xx xxxxxxxx x 0,5 xx xxxxx X9 xxxx xxxxxxxxxx pufru x 2,0 xx xxxxxxxx xxxxx. Xxxxxxxx xx xxxxx preinkubace xxxxxxxxxxxx třepáním.
Pro xxxxxxxxx xxxxx variací xx xxx každou dávku xxxxxx xxx xxxxx. Xxxxxxxxxx očkování je xxxxxxxxxx, xx-xx xxxxxxx xxxxxxxxxx. Xxxxx-xx xxxxxxx xx xxxxxx xxxxx, xxxxxx to xxxx xxxxx znehodnotit.
Plynné xxxx xxxxxx xxxxx xx xxxxxxx xx použití xxxxxxxx xxxxxxx, xxxxxxxxx x xxxxxxxxxx xxxxxxxx.
5)1.5.4 Xxxxxxxx
Xxxxxxx misky v xxxxx xxxxxx xxxxx xx inkubují při xxxxxxx 37 °X xx dobu 48 - 72 hodin, xxxxx xx xxxxxxxxx xxxxxxxxxxx xxxxxxx na xxxxx xxxxx.
2 XXXXX
2.1 Xxxxxxxxxx výsledků
Údaje xx xxxxxxxxxx xxxx xxxxx xxxxxxxxxxxxx xxxxxxx xx xxxxx xxxxx. Xxxxxx xx xxxxx xxxxx xxxxxxxxxxxxx xxxxxxx jak x xxxxxxxxx xxxxxxxx (xxxxxxxxxxxx, xxxxxxxxx kontrola xxx působení, byla-li xxxxxxx), xxx z xxxxxxxx xxxxxxxxx. Pro xxxxxxxxxx xxxxx i xxx pozitivní x xxxxxxxxx xxxxxxxx (xxxx. xxx působení rozpouštědlo) xx xxxxxx xxxxx xxx xxxxxxxxxx misky x průměrný počet xxxxxxxxxxxxx kolonií xx xxxxx misku včetně xxxxxxxxxx odchylky.
Verifikace xxxxxx xxxxxxxxx xxxxxx se xxxxxxxxxx. Nejednoznačné xxxxxxxx xx xxxxxxxxx xxxxxx xxxxxxxxxx, xxxxxxx xx xxxxxxxxxxxxxx experimentálních xxxxxxxx. Xxxxxxxxx xxxxxxxx se xxxxxx xxxxxxxx xxxxxx xx xxxxxxx. Xxxxx xx potvrzení negativních xxxxxxxx xxxxxxxxxx xx xxxxx, je třeba xx xxxxxxxxx. V xxxxxxxxxx experimentech xx xxxxx zvážit xxxxxxxxxx xxxxxxxxxx xxxxxxxxx tak, xxx xx xxxxxxxx xxxxxx posuzovaných xxxxxxxx. Xx xxxxxxxxx parametrům, xxxxx se dají xxxxxxxxxxx, patří xxxxxxx xxxx xxxxxxxxxxxxx, xxxxxx xxxxxxxx ("xxxxx xxxxxxxxxxxxx" xxxx preinkubace x xxxxxxx xxxxxxxxx) x xxxxxxxx xxxxxxxxxxx xxxxxxxx.
2.2 Xxxxxxxxxxx a xxxxxxxxxxxx xxxxxxxx
Xx stanovení xxxxxxxxxxx xxxxxxxx xxxxxxxx několik xxxxxxxx, xxxxxxxxx dávkově xxxxxxx xxxxxx xx xxxxxxxxxx xxxxxxx a/nebo xxxxxxxxxxxxxxxx nárůst počtu xxxxxxxxxxxxx xxxxxxx xx xxxxx xxxxx xxx xxxxx nebo xxxx xxxxxxxxxxxxx x xxxxxxxxx xxxxxxx kmene x xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxx xxx něj.
5) Xxxx xxxxx se xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx. Xxxx xxxxxxx xxx xxxxxxxxxxxxx xxxxxxxx xxxxx xx xxxxx xxxxxx xxxxxxxxxxx xxxxxx,
5) xxxxxxxxxxx významnost xx xxxx xxxxxx xxx xxxxxxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxx.
Xxxxxxxxx xxxxx, jejíž xxxxxxxx xxxx uvedená kritéria xxxxxxxxx, xx x xxxxx xxxxx považuje xx xxxxxxxxxxx.
Xxxxxxx xxxxxxxxxxx xxxx xxxxxxxxx jednoznačně xxxxxxxxx xxxx xxxxxxxxx xxxxxxxx, v ojedinělých xxxxxxxxx xxxx nelze xx získaného xxxxxxx xxx vyvodit x xxxxxxxx testované xxxxx xxxxxxxxxxx závěr. Výsledky xxxxx xxx stále xxxxxxxxxxxxx xxxx xxxxxxxxxxxxx, x když se xxxxxxxxxx xxxxxxxxxx opakuje.
Pozitivní xxxxxxxx bakteriálního xxxxx xx xxxxxxxx mutace xxxxxxx, že látka xxxxxxxx genové xxxxxx xxxx xxxxxxxxxx xxxx xxxx posunových xxxxxx x genomu Salmonella xxxxx xxxxxx xxxx. Xxxxxxxxxxx xxxx. Negativní xxxxxxxx xxxxxxx, xx xx xxxxxx xxxxxxxxxx xxxxxxxx není xxxxxxxxx xxxxx xx xxxxxxxxx xxxxx xxxxxxxxx.
3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx s xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) musí xxx xxxxxxxxx xxxxxxx xxxxxx a x xxxxxxx pokusu xx xxxxx xxxx xxxxxxxx.
Xx xxxxxx x xxxxxxx xxxxxx xx xxxxx xxxxx xxxx informace: Xxxxxxxxxxxx/xxxxxxxxx:
- zdůvodnění xxxxx xxxxxxxxxxxx,
- xxxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx x tomto xxxxxxxxxxxx, xxxxx xx známa.
Kmeny:
- xxxxxxx xxxxx,
- xxxxx xxxxx v kultuře,
- xxxxxxxxxxxxxxx xxxxx.
Xxxxxxxx xxxxx:
- xxxxxxxx xxxxxxxxx látky xx xxxxx xxxxx (x xx nebo µx) xx xxxxxxxxxxx xxxxx xxxxx x xxxxx xxxxx xxx xxxxx xxxxxxxxxxx,
- xxxxxxx xxxxx,
- xxx x xxxxxxx xxxxxx metabolické xxxxxxxx (xxxxxx xxxxxxxx xxxxxxxxxxxxxxxxx),
- xxxxxxx xxxxxxxx (xxxxxxxxxx)
Xxxxxxxx:
- xxxxxx toxicity,
- xxxxxx srážení,
- počty xx jednotlivých xxxxxxx,
- xxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxx xx jednu xxxxx x xxxxxxxxxx xxxxxxxx,
- xxxxx dávka-odpověď, xx-xx to xxxxx,
- xxxxxxxxxxx analýzy, byly-li xxxxxxxxx,
- xxxxx xx xxxxxxxxxx xxxxxxxxxxx (xxxxxxxxxxxx/xxxxxxxxx) x pozitivních xxxxxxx xxxxxx xxxxxxx, xxxxxxx x směrodatných xxxxxxxx,
- xxxxx x xxxxxxxxxxxx xxxxxxxxxxx (xxxxxxxxxxxx/xxxxxxxxx) a xxxxxxxxxxx xxxxxxx včetně xxxxxxx, xxxxxxx a xxxxxxxxxxxx xxxxxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.15 XXXXXX XXXXXX - XXXXXXXXXXXXX XXXXXXXXXX
1 XXXXXX xx x xxxxxxx x právem Evropských xxxxxxxxxxxx.
1)1.1 Xxxxxxx metody
Různé xxxxxxxxx x xxxxxxxxx xxxxx xxxxxxxx Xxxxxxxxxxxxx xxxxxxxxxx xxxxx být xxxxx xxx xxxxxx xxxxxxxx genových xxxxxx xxxxxxxxxxxx xxxxxxxxxx látkami xxx x x xxxxxxxxxxxx xxxxxxxx.
Xxxx xxxxxxxxx xxxxxxx xxxxxxx xxxxxxx x haploidních kmenů, xxxx je míra xxxxxx xxxxxx x xxxxxxxxx, adenin xxxxxxxxxxxx xxxxxx (xxx-1, xxx-2) xx xxxxxxx, xxxxxx xxxxxxxxxx bílé mutanty x xxxxxxxxxx xxxxxxx, xxxx xx xxxxxxx xxxxxxxxxx xx kanavaninu x cykloheximidu.
Nejlépe xxxxxxx xxxxxxxx xxxxxxx xxxxxx xxxxxxxx využití xxxxxxxxxxx xxxxx XX 185-14C x xxxxxxxx (xxxxx) xxxxxxxx xxxxxxxx xxx 2-1, arg 4-17, xxx 1-1 x xxx 5-48. Xxxxxx xxxx xxxxxx xxxxxxxxx xxxxxxxx typu záměny xxxx, které xxxxxxxx xxxxxx xx specifickém xxxxx, xxxx xxxxxx xxxxxxxxxxx mutace. XV 185-14X nese rovněž xxx 1-7 marker, xxxxxxxx mutaci, xxxxxxxxxxxx xxxxxxxx xxxxxxxx x xxxxxx xxxxx a xxxxxx hom 3-10, xxxxx je xxxxxxxxxx xxxxxxxxxx xxxxxxxx.
X xxxxxxxxxxx xxxxx X. cerevisiae xx jediným široce xxxxxxxxxx kmenem X7, xxxxx xx homozygotní xxx xxx 1.92.
1.2 Xxxxx metody
1.2.1 Příprava
Roztoky xxxxxxxxxxx xxxxx a xxxxxxx xxxx xxx xxxxxxxxxx xxxxx xxxx xxxxxxxxxx xx použití xxxxxxxx xxxxxxxx. X xxxxxxxxxxx xxxxx xx xxxx xxxxxxxxxxxxx se xxxx užít roztok xxxxx než 2 xxxxxxxx % v xxxxxxxxxxx rozpouštědlech, xxxx xx xxxxxx, xxxxxx xxxx xxxxxxxxxxxxxxx (DMSO). Xxxxxxx xxxxxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxx x charakteristiky xxxxx.
Xxxxxxxxxxx xxxxxxxx
Xxxxx xxxx xxx xxxxxxxxxx xxxxxxxxxx xxxxxx xxx x xxxxxxxxxxx, xxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx systému.
Nejčastěji xxxxxxxx xxxxxxxx je xxxxxxxxxxxxxxxxxxx xxxxxx xxxxxxxxxx x xxxxx xxxxxxxx po xxxxxxxx xxxxx indukujících xxxxxx x xxxxxxxx xxxxxxxxx. Xxxxx jiných xxxxx, xxxxx, xxxxxxxxxxxxxxxxxxxxx xxxxxx xx xxxxxxx xxxx xxx rovněž xxxxxx xxx xxxxxxxxxxxx xxxxxxxx.
1.2.2 Xxxxxxxxxxxxxx xxxxxxxx
1.2.2.1 Xxxxxxxxx xxxxx
Xxxxxxxxx xxxx XX 185-14X x xxxxxxxxx xxxx X7 xxxx xxxxxxxxxxxxx xxx xxxxxx genových mutací. Xxxx xxxxx xxxxx xxx xxxxxx xxxxxx.
1.2.2.2 Xxxxx
Xxxxxxxxxxxx xxxxxxxxxx média xxxx xxxxxxx xxx xxxxxx počtu xxxxxxxxxxxxx x mutovaných buněk.
1.2.2.3 Xxxxxxxxx x xxxxxxxxx xxxxxxxx
Xxxxxxxxx, neovlivněné x xxxxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxx xxxxxxxxx současně. Xxx každou xxxxxxxxxxx xxxxxxx změnu mají xxx použity xxxxxxxxxxxx xxxxxxxxx kontrolní xxxxxxxx xxxxx.
1.2.2.4 Xxxxxxxxxxx
Xx xxx xxxxxxx xxxxxxx 5 xxxxxx xxxxxxxxx koncentrací. X xxxxxxxxx látek xxxx xxxxxxxx xxxxxxx xxxxxxxxxxx redukovat xxxxxxx xxx 5 - 10 %. Látky xx xxxx xxxxxxxxx xxxxxxxxxxx xxxx xxx xxxxxxxxx xx po xxx xxxxxxxxxxxx látky xx xxxxxxx xxxxxxxx xxxxxxx. Xxxxxxxx xxxxxxxxxxx xxx látky xxxxxxxxx, xx xxxx xxxxxxxxx, xx xxxxxx xxxxxx xx případu.
1.2.2.5 Xxxxxxxxxx xxxxxxxx
Xxxxx xxxx inkubovány xx xxxx xxx xxx 28 xx 30 °X xx xxx.
1.2.2.6 Frekvence xxxxxxxxxxx xxxxxx
Xxxxxxxxx xxxxxxxxxxx mutací x subkultur xx xxx x rozmezí xxxxxxxxxxxxx xxxxxxxxxx hodnot.
1.2.2.7 Xxxxx xxxxxxxxx
Xx nutno xxxxxx xxxxxxx xxx xxxxx xx xxxxx xxxxxxxxxxx u xxxxx x prototrofními xxxxxxx x x xxxxxxxxxx xxxxx. X experimentů xxxxxxxxxxx markery xxxx xxx 3-10 s xxxxxx xxxxxxx xxxxxxxxx xxxx xxx xxxxx xxxxx xxxxxx, aby xxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx.
1.2.3 Popis xxxxxxx
Xxxxxxxxx xxxxx S. xxxxxxxxxx xx xxxxxxx xxxxxxxxx xx zkumavce x xxxxxxx xxxxxxxxx x zahrnuje xxx' xxxxxxxxxxx nebo xxxxxxxx xxxxx. Xxxxxxxx xxxxxx xxxx xxx xxxxxxxxx xx rostoucích buňkách: 1-5 x 107 xxxxx/xx je xxxxxxxxx xxxxxxxxx xxxxx po xxxx xx 18 x xxx 28 xx 37 °X xx xxxxxxx. Xxxxxxxxxxxx xxxxxxxx metabolického xxxxxxxxxxx xxxxxxx je přidáno x xxxxxxx xxxxxxxxx, xxxxx xx xx xxxxxxxx. Xx xxxxxxxx xxxxxxxxx jsou buňky xxxxxxxxxxxxxx, xxxxxxx x xxxxxxxxxx na xxxxxx xxxxxxxxxx xxxxxx. Xx xxxxxxxx xxxx xxxxxxxx xxxxxxxxxxx xxxxx x xxxxx x xxxxxxx xxxxxxxx xxxxxx.
Xxxxxxxx je xxxxx pokus xxxxxxxxx, xx xxx xxxxxxxx xxxxx xxxxx x xxxxxxx xx xxxxxxxxxxx xxxx. Jestliže xx xxxxx xxxxx xxxxxxxxx, xx xxxxxxxx xxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxx.
2. XXXXX
Xxxxx xxxx xxx xxxxxxxxxx do xxxxxxx x xxxx xxxxxxxxx xxxxx xxxxxxx, xxxxx xxxxxx, xxxxxxxxxxxxx xxxxx x frekvenci xxxxxx. Xxxxxxx výsledky xxxx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx. Xxxxx xxxx xxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx metodami.
3 XXXXXXX XXXXXX, PROTOKOL XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx a x xxxxxxx pokusu xx xxxxx vést xxxxxxxx.
Xxxxxx x průběhu pokusu xxxxxxxx informace o:
- xxxxxxxxx xxxxxxx,
- xxxxxxxxxx xxxxx: xxxxx ve xxxxxxxxxxx xxxx nebo xxxxxxxx, xxxxxxx xxxxx, xxxxxxx x xxxxxx xxxxxxxx, xxxxxxxxxxx xxxxxxxxx xxxxxx,
- podmínkách xxxxxxxxx xxxxxxxxxxx: hladina expozice, xxxxxx x trvání xxxxxxxxx, xxxxxxx xxx xxxxxxxxx, pozitivní x xxxxxxxxx xxxxxxxx,
- xxxxx xxxxxxx, počtu xxxxxx, xxxxxxxxxxxxx xxxxx a xxxxxxxxx xxxxxx, xxxxxx xxxxx a xxxxxx, xxxxxxxxxxx xxxxxxxxx xxxxx, xxxxx xx to xxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.16 XXXXXXXXX XXXXXXXXXXX - SACCHAROMYCES XXXXXXXXXX
1 XXXXXX xx x souladu x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
1)1.1 Xxxxxxx metody
Mitotická rekombinace x Xxxxxxxxxxxxx xxxxxxxxxx xxxx být detekována xxxx xxxx (xxxxxxxx xxxx xxxxx x xxxx xxxxxxxxxxx) x xxxxxx xxxx. Xxxxx xxxxxx xx xxxxxxx xxxxxxxxx překřížení x xxxxxxx xxxxxxxxxx xxxxxxxx, xxxxxx xxxxx xxxxxx xx xxxxxxxx xxxxxxxxxxxx x xx xxxxxxx xxxxxx xxxxxxxx. Xxxxxxxxxx xx xxxxxx xxxxxxxxx xx xxxxxxx tvorby xxxxxxxxxxx xxxxxxxxxxxxx kolonií xxxx xxxxxxx xxxxxxxxx x xxxxxxxxxxxxxxx kmenů, xxxxxx konverse xx xxxxxxxxx na xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx x auxotrofního xxxxxxxxxxxxxxxx kmene, xxxxx xxxx xxx různé xxxxxxxx alely xxxxx xxxx. Xxxxxxxxxx xxxxxxx xxxxx xxx xxxxxxx xxxxxxxxx xxxxxx xxxxxxxx xxxx D4 (xxxxxxxxxxxxxx x xxx 2 x trp 5), X7 (xxxxxxxxxxxxxx v xxx 5), BZ34 (xxxxxxxxxxxxxx x arg 4) a XX1 (xxxxxxxxxxxxxx x xxx 4 x trp 5). Xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxx x xxxxxx sektory xxxx xxx testováno x X5 xxxx X7 (xxxxx xxxxxx xxxx xxxxxxxxxx xxxxxxx konverzi x reverzní xxxxxx x ilv 1-92). Xxx kmeny xxxx xxxxxxxxxxxxxx xxx xxxxxxxxxxxxxx xxxxx xxx 2.
1.2 Xxxxx xxxxxx
1.2.1 Příprava
Roztoky xxxxxxxxxxx xxxxx a xxxxxxx mají xxx xxxxxxxxxx xxxxx xxxx xxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxxxx. X xxxxxxxxxxx látek ve xxxx xxxxxxxxxxxxx xx xxxx užít roztok xxxxx xxx 2 xxxxxxxx % v xxxxxxxxxxx xxxxxxxxxxxxxx, jako xx etanol, aceton xxxx xxxxxxxxxxxxxxx (DMSO). Xxxxxxx xxxxxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxxxxxxxx xxxxx.
Xxxxxxxxxxx aktivace
Buňky xxxx xxx vystaveny xxxxxxxx xxxxxxxxxxx xxxxx jak x xxxxxxxxxxx, xxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx. Xxxxxxxxxx užívaným xxxxxxxx xx xxxxxxxxxxxxxxxxxxx xxxxxx xxxxxxxxxx z xxxxx hlodavců xx xxxxxxxx látek xxxxxxxxxxxx xxxxxx x doplněná xxxxxxxxx. Xxxxx jiných xxxxx, xxxxx, xxxxxxxxxxxxxxxxxxxxx xxxxxx xx xxxxxxx xxxx být rovněž xxxxxx xxx xxxxxxxxxxxx xxxxxxxx.
1.2.2 Experimentální xxxxxxxx
1.2.2.1 Xxxxxxxxx xxxxx
Xxxxxxxxxxxxx xxxx xxxxxxxxx xxxxx D4, X5, X7 x XX1. Xxxxx xxxxxx xxxxx může xxx xxxxxx xxxxxx.
1.2.2.2 Xxxxx
Xxxxxxxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxxx xxx xxxxxx xxxxxxxxxxxxx xxxxx a xxxxxxxxx mitotické xxxxxxxxxxx.
1.2.2.3 Xxxxxxxxx x pozitivní xxxxxxxx
Xxxxxxxxx, neovlivněné x xxxxxxxxxxxxx ovlivněné kontroly xxxx používány xxxxxxxx. Xxx každou xxxxxxxxxxx xxxxxxx xxxxx xxxx xxx xxxxxxx odpovídající xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxx.
1.2.2.4 Xxxxxxxxxxx
Xx být xxxxxxx xxxxxxx 5 xxxxxx xxxxxxxxx koncentrací. Xxxx xxx brán xxxxx na cytotoxicitu x rozpustnost. Nejnižší xxxxxxxxxxx nesmí xxx xxxx xx životnost xxxxx. U toxických xxxxx xxxx xxxxxxxx xxxxxxx koncentrace xxxxxxxxx xxxxxxx xxx 5 - 10 %. Xxxxx xx xxxx xxxxxxxxx xxxxxxxxxxx mají xxx xxxxxxxxx xx xx mez xxxxxxxxxxxx xxxxx xx xxxxxxx xxxxxxxx xxxxxxx. Xxxxxxxx xxxxxxxxxxx xxx látky xxxxxxxxx, xx xxxx xxxxxxxxx, je určena xxxxxx xx případu.
Buňky xxxxx xxx vystaveny xxxxxxxx xxxxxxxxx xxxxx xxx' xx xxxxxxxxxxx xxxx, xxxx xxxxx xxxxx po xxxx xx 18 x. Xxxxxxx dlouhodobě ovlivňované xxxx xxx xxxxxxxxxxxxx xxxxxxxxxxxx xxx xxxxxx xxxx, jejichž xxxxxxxxxx xxxx xxxxxxxxxxxx.
1.2.2.5 Xxxxxxxx xxxxxxxx
Xxxxx xxxx xxxxxxxxxx xx xxx xx xxxxx až xxxx xxx při 28-30 °X. Xxxxx použité xxx průkaz červených x růžových sektorů Xxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxx být xxxxxxxx x xxxxxxxxxx (xxx 4 °X) po xxxxx 1 - 2 xxx před xxxxxxxxx, aby xx xxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx.
1.2.2.6 Xxxxxxxxx xxxxxxxxx xxxxxxxxx rekombinace
Používají xx xxxxxxxxxx x xxxxxxxxx spontánních xxxxxx x xxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxx.
1.2.2.7 Xxxxx xxxxxxxxx
Xx xxxxx použít xxxxxxx xxx xxxxx xx xxxxx xxxxxxxxxxx x xxxxx prototrofních xxxxx xxxxxxxxx mitotickou xxxxxxx konversí a xxx xxxxxx xxxxxxxxxx xxxxx. V xxxxxxx xxxxxxxxx xxxxxxxxx homozygosity xxxxxxx xxxxxxxxxx xxxxxxxxxxx xx xxx xxxxx xxxxx zvýšen, aby xxxx xxxxxxxx dostatečného xxxxx xxxxxxx.
1.2.2.8 Xxxxxx
Xxxxxxxxx X. cerevisiae xxxxxxx xxxxxxx xxxx xxxxxxxxxx xxxx x tekutém xxxxxxxxx x xxxxxxxx xxx' xxxxxxxxxxx, nebo xxxxxxxx buňky. Xxxxxxxx xxxxxx mají xxx xxxxxxxxx xx rostoucích xxxxxxx. 1-5 x 107 xxxxx/xx xx xxxxxxxxx xxxxxxxxx xxxxx xx xxxx xx 18 x při 28 xx 37 °X xx třepání. Xxxxxxxxxxxx xxxxxxxx metabolického xxxxxxxxxxx xxxxxxx xx xxxxxxx x průběhu xxxxxxxxx, pokud xx xx xxxxxxxx.
Xx xxxxxxxx xxxxxxxxx xxxx buňky xxxxxxxxxxxxxx, xxxxxxx a xxxxxxxxxx xx vhodné xxxxxxxxxx xxxxxx. Xx xxxxxxxx xxxx počítány xxxxxxxxxxx xxxxx x xxxxx x xxxxxxx xxxxxxxxx rekombinace.
Jestliže je xxxxx xxxxx negativní, xx xxx xxxxxxxx xxxxx xxxxx x xxxxxxx xx xxxxxxxxxxx xxxx. Jestliže xx xxxxx xxxxx xxxxxxxxx, xx xxxxxxxx xxxxxx xxxxxxx nezávislým experimentem.
2 XXXXX
Xxxxx xx xxxxxxxxxxxxx xx tabulky, která xxxxxxxx xxxxx xxxxxxx, xxxxx rekombinací, přežívajících xxxxx x frekvenci xxxxxxxxxxx.
Xxxxxxxx mají xxx xxxxxxxxx v xxxxxxxxxx xxxxxxxxxxx.
Xxxxx xxxx být xxxxxxxxxxx vhodnými statistickými xxxxxxxx.
3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX A XXXXXXXXX XXXXXX
X souladu xx x xxxxxxxxxxx xxxxxxxx předpisy
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx a x xxxxxxx xxxxxx xx xxxxx xxxx xxxxxxxx.
Xxxxxx x xxxxxxx xxxxxx xxxxxxxx následující informace:
- xxxxxxx kmeny,
- podmínky xxxxx: buňky ve xxxxxxxxxxx xxxx nebo xxxxxxxx, xxxxxxx xxxxx, xxxxxxx x xxxxxx xxxxxxxx, xxxxxxxxxxx aktivační xxxxxx,
- xxxxxxxx xxxxxxxxx xxxxxxxxxxx: xxxxxxx xxxxxxxx, xxxxxx a trvání xxxxxxxxx, xxxxxxx xxx xxxxxxxxx, positivní x xxxxxxxxx xxxxxxxx,
- xxxxx xxxxxxx, xxxxx xxxxxxxxxxx, xxxxxxxxxxxxx xxxxx a xxxxxxxxx rekombinací, vztah xxxxx a xxxxxx, xxxxx xx xx xxxxx, statistické xxxxxxxxx xxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.17 XXXXXXXXXX - TEST XXXXXXXX XXXXXX X SAVČÍCH XXXXXXX XX XXXXX
1 XXXXXX je v xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
5)1.1 Úvod
Test xxxxxxxx mutací in xxxxx se dá xxxxxxxx xx zjišťování xxxxxxxx mutací vyvolaných xxxxxxxxxx xxxxxxx. Mezi xxxxxx xxxxxxx linie xxxxx myší xxxxxxxxx xxxxx X5178X, linie XXX, XXX-XX52 x X79 buněk čínského xxxxxx x xxxxxx xxxxxxxxxxxxxxx xxxxx XX6 (1). U xxxxxx xxxxxxxxx linií xx xxxxxxxxxx xxxx xxxxxxx xxxxxxxxx efekt zjišťují xxxxxx x xxxxxxxxxxxxxx (XX) a hypoxanthin-guanin xxxxxxxxxxxxxxxxxxxxxxx (XXXX) a x transgenní xanthin-guanin xxxxxxxxxxxxxxxxxxxxxxx (XXXX). Xxxxx xxxxxx x TK, XXXX x XXXX xx xxxxxxxx xxxxx xxxxxxx xxxxxxxxxxx xxxx. Xxxxxxxxxxx xxxxxxxxxx XX x XXXX xxxx xxxxxxx xxxxxxx x xxxxxx genetické xxxxx (xxxx. velké xxxxxx), xxxxx xx xx xxxxxx XXXX chromozómů X xxxxxxxx .
5)X xxxxx xx xxxxxx xxxxxx x xxxxxxx xxxxxxx xx xxxxx xx dají xxxxxx xxxxxxx xxxxxxxxxxxxxxx buněčných xxxxx xxxx buněčných xxxxx. Xxx xxxxx xxxxx xx berou x úvahu xxxxxxx xxxxxxxxxx dané kultury x stabilita xxxxxxxxx xxxxxxxxxxx xxxxxx.
Xxxxx xx xxxxx obecně vyžadují xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxx. Takový systém xxxxxxxxxxx aktivace xxxxxxxx xxxxxxxx xxxxx podmínky xx xxxx xxxxxxxx. Xx třeba xxxxxx xxxxxxxx podmínek, xx xxxxxxx xx výsledky xxxxxxxxxx xxxxxxx mutagenitu. X xxxxxxxxxx výsledkům, xxx nejsou xxxxxxxxx xxxxxxx xxxxxxxxxx, xxxx xxxxx x důsledku xxxxx pH, osmolality xx xxxxxx xxxxxxxxxxxx.
5)Xxxxx xxxx xx používá xx xxxxxxxxxx možných xxxxxxx mutagenů x xxxxxxxxxxx. Xxxx xxxxxxxxx, xxxxx xxxx v xxxxx xxxxx xxxxxxxxx, xxxx xxxxxxx xxxxxxxxxxx, xxxxxxxxxx však xxxxxxxx xxxxxxxx xxxx xxxxx xxxxxx x xxxxxxxxxxxxxx. Xxxx korelace závisí xx xxxxx xxxxxxxx xxxxx x existuje xxxxx xxxx xxxxxxx xxxx, že xxxxxxxx xxxxxxxxxxx, xxxxx se xxxxx xxxxxx xxxxxxxx, xxxxxxx xxxxxx xxxxxx xxxxxxx jiným, negenotoxickým xxxxxxxxxxx či xxxxxxxxxxx, xxxxx v bakteriálních xxxxxxx xxxxxxxx.
5)1.2 Xxxxxxxx
Xxxxxxx xxxxxx: xxxxxx xxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxx, xxx vede xx xxxxx xxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx.
Xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxx xxxx: xxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxx nebo několika xxxx bází x XXX.
Xxxxxxxxxx xxxxxxxx (mutageny xxxxxxxxxxxx xxxxxxxx xxxxxx): xxxxx, xxx xxxxxxxxx xxxxxxx xxxx ztrátu xxxxxxx xxxx xxxx xxxx bází v XXX.
Xxxx fenotypické xxxxxxx: xxxxxx, xxxxx kterého xxxx x xxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx.
Xxxxxxxxx xxxxxx: počet xxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxx xxxxxx xxxxxx xxxxx.
Xxxxxxxxx xxxxxxx růst: xxxxxx xxxxx xxxxx v xxxx v xxxxxxxxx x kontrolní xxxxxxxx xxxxx; vypočítává xx xxxx součin xxxxxxxxx xxxxxxxxxxx xxxxx (x xxxxxxxxx x xxxxxxxxx xxxxxxxxx) a xxxxxxx xxxxxxxxx xxxxxxxxx cloning xxxxxxxxxx (x porovnání x xxxxxxxxx kontrolou).
Relativní xxxxxxxxx xxxx: xxxxxxx xxxxxx počtu xxxxx xxxxx xxxxxx xxxxxxx x xxxxxxxxx s xxxxxxxxx xxxxxxxxx.
Xxxxxxxxx (xxxxxxxxx): xxxxxxxxx xxxxxxxx (xxxxxxx xxxxxxxxxx) xxxxxxxxxxx xxxxx x době xxxxxxxxx xx miskách x xxxxxxxxxx podmínkách xx xxxxxx exprese.
Přežití: xxxxxxxxx xxxxxxxx (xxxxxxx xxxxxxxxxx) xxxxxxxxxxx xxxxx inokulovaných xx xxxxxxx na xxxxx xxxxxxxx xxxxx; xxxxxxxxx se xxxxxxx x xxxxxxxxx x xxxxxxxx kontrolní xxxxxxx xxxxxxxx.
1.3 Xxxxxxx xxxxxx
Xxxxx, xxxxxxxxxxx na thymidinkinázu (XX) x důsledku xxxxxx TK
+/- → XX
-/-, xxxx rezistentní xxxx cytotoxickému xxxxxxxx xxxxxxxxxxxxxx xxxxxxx trifluorthymidinu (XXX). Buňky xxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxxx XXX citlivé, xxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx a xxxxxxxxx xxxxx xxxxxxx dělení. Xx xxxxxxxxxxx XXX xxxxx xxxxx proliferovat xxxxxxxx xxxxx, xxxxxxx xxxxxxxx xxxxx, xxxxxxxxxx xxxxxxxxxxxxxx, proliferovat xxxxxxx. Xxxxxxx xxxx xxxxx x deficientní XXXX xxxx XXXX xxxxxxxx xxxxxxxxxxx vůči 6-xxxxxxxxxxx (XX) xxxx 8-xxxxxxxxxx (XX). Pokud je xxxxxx báze xxxx xxxxxxxxxx xxxxxxxx xx xxxxxxxxx činidlem xxxxxxxxxxx x xxxxxxxx xxxxx xx xxxxxx xxxxxx x xxxxxxx xxxxxxx, xx třeba xxxxxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxx. Xxxxxxxxx xx xxxxx prozkoumat xxxxx xxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxx buňkám x xxxxxxxx i xxx xxxx. Xxxxxxx-xx xx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxx, xx xxxxx xxxxxxxx, xx je xxxxxxxx xxxxxx/xxxxxxx vhodné.
5)Buňky x xxxxxxxx nebo xxxxxxxxxxxxx xxxxxxx se xx vhodnou dobu xxxxxxx působení xxxxxxxxx xxxxx x metabolickou xxxxxxxx x bez xx a kultivují xx xx xxxxxxxxx xxxxxxxxxxxx x x xxxxxxx xxxxxxxxxxx exprese xxxx xxxxxxx xxxxxxx.
5) Xxxxxxxxxxxx se xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx (xxxxxxx) (xxxxxxx efficiency) nebo xxxxxxxxxxx xxxxxxxxx nárůstu xxxxxx xx xxxxxxxx xxxxx. Xxxxxxx xx xxxxxxxxx x xxxxxxxx xxxxx po dostatečnou xxxx, charakteristickou pro xxxx xxxxx a xxx xxxxx, aby xxxxx dojít x xx nejoptimálnější xxxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxx. Xxxxxxxxx mutantů xx xxxxxxx xxxxxxxxx xxxxxxx xxxxx xxxxx v xxxxx obsahujícím selekční xxxxxxx xxx xxxxxxx xxxxxxxxxx buněk x x médiu xxx xxxxxx xxxxxxx, xx xxxxxxxxx xxxxxxxxx účinnosti (xxxxxxx xxxxxxxxxx), (xxxxxxxxxx). Xx xxxxxx xxxxxxxxx xxxx xx xxxxxxx xxxxxxxxx. Xxxxxxx frekvence xx xxxxxx z xxxxx xxxxxxx xxxxxxxxxx xxxxx x selekčním xxxxx x x xxxxx xxxxxxx x xxxxxxxxxxx xxxxx.
1.4 Popis xxxxxx
1.5 Xxxxxxxx
1.5.1.1 Xxxxx
Xx xx použít celá xxxx xxxxxxxxx xxxx, xxxxxx xxxxxxxx buněk X5171X, XXX, XXX-XX52, X79 x XX6. X buněčných typů xxxxxxxxxxx x xxxxx xxxxx xxxx být xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxxx, xxxxxx xxxxxxxxx xxxxxxxx (xxxxxxx xxxxxxxxxx) x xxxxxxxx xxxxxxxxx spontánních mutací. X xxxxx xx xxxxxxxxxx, zda nejsou xxxxxxxxxxxxx xxxxxxxxxxxx; xxxxxxxxxx xxxxx xx použít xxxxxxx.
Xxxx xx třeba xxxxxxxxxx xxx, xxx xxx xxxxxxxx xxxxxxxxx x xxxxxxxxxxx (xxxxx). Xxxxx buněk, xxxxx xxxxxx a xxxxxxxxxxx xxxxxxxxx látky xxxx xxxxx definovaným parametrům xxxxxxxxx.
5) Xxxxxxxxx xxxxx xxxxxxxxx buněk, xxxxx xxxxxxx xxxxxxxx x xxxxxxx xx v xxxxxxxxxxxx stadiích xxxxx, xx dán xxxxxxxxx xxxxxxxxxxx mutací. Obecným xxxxxxxx xx, že xxxxx xxxxx xx xxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx hodnoty frekvence xxxxxxxxxxx xxxxxx. Doporučuje xx xxxx xxxxxx xxxxxxx 10
6 buněk. Xxxx by být x dispozici xxxxxxxxx xxxxxxxxxx xxxxx, xxxxxxx xx xx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx.
1.5.1.2 Xxxxx a xxxxxxxxxx xxxxxxxx
Xx xxxxx xxxxxx xxxxxx xxxxxxxxxx média x xxxxxxxxx podmínky (xxxxxxxxxx nádoby, koncentraci XX2, xxxxxxx x xxxxxxx). Média xx xxx xxxx volí xxxxx xxxxxxxxxx systému x xxxx xxxxx. Xxxxxxx xxxxxxxx xx, xxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxx xxxxx xxxxx expresní xxxxxxx a xxxxxxxxx xxx xxxxxxxxxx, tak xxxxxxxxxxxx xxxxx xxxxxx xxxxxxx.
1.5.1.3 Xxxxxxxx xxxxxx
Xxxxx xx xxxxxxx xx xxxxxxxxx xxxxxx, inokulují xx xxxxxxxxxxxx xxxxx x inkubují při xxxxxxx 37 °X. Xxxx provedením xxxxx xx xxxxx xxxxxxx xxxxxx xxxxx vzniklých xxxxxxxxxx xxxxx.
1.5.1.4 Xxxxxxxxxxx xxxxxxxx
Xx xxxxx se xxxxxxxxxx xxxxxx xxxxxx x xxxxxxxxxxx x x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx. Xxxxxxxxxxxxx xx kofaktory xxxxxxxxxxxxxx xxxxxxxxxxxxxxx frakce (X9) xxxxxxxxxx z xxxxx xxxxxxxx, xxxxxxxxx xxxxxxx indukujícími enzymy, xxxx xx Xxxxxxx 1254,
5) xxxx směs xxxxxxxxxxxxx x ß-naftoflavonu.
5)Konečná xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxx x xxxxx xxxx xxxxxxx 1 - 10 % x/x. Xxxxxxxx xxxxxxxxxxxxx aktivačního xxxxxxx xxxx xxxxxxx xx tom, xxxxxx xxxx xx xxxxxxxxx xxxxxxxxxx. V xxxxxxxxx xxxxxxxxx xx vhodné xxxxxx xxxxxxxxxxxxxxx xxxxxx x xxxxxxxx xxxxxxxxxxxxx.
Xxx xxxxx endogenní xxxxxxxx xxxxx být xxxxxxx x xxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxx exprimující xxxxxxxxxx xxxxxxxxx xxxxxx. Xxxxx xxxxxxxxx linií xx xxx být xxxxxxx xxxxxx (např. xxxxxxx isoenzymu xxxxxxxxxx X450 k xxxxxxxxxxx xxxxxxxxx xxxxx).
1.5.1.5 Xxxxxxxx xxxxxxxxx xxxxx
Xx-xx xxxxxxxxx xxxxx x xxxxxx xxxxx, xxxxx se xxxx působením xx xxxxx rozpustí nebo xx připraví xxxx xxxxxxxx xx xxxxxxx xxxxxxxxxxxx a xxxxxxxx xxxxxx. Xxxxxxx xxxxxxxxx xxxxx xx mohou xx xxxxxxx přidávat xxxxx nebo xx xxxxxxx xxxx. Xx xxxxx používat xxxxxxx xxxxxxxxx, ledaže xxxxx x xxxxxx xxxxxxxxx xxxxxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxxxx.
1.5.2 Xxxxxxxx testu
1.5.2.1 Xxxxxxxxxxxx/xxxxxxxxx
X xxxxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxxx podezření, xx xx xxxxx x testovanou látkou xxxxxxxx xxxxxxxx, x xxxxx narušovat xxxxxxxxx xxxxx x aktivitu X9.
Xxxxxxx-xx xx méně xxxxx xxxxxxxxxxxx xxxx xxx xxxxxxxxx referencemi xxxxxxxxxxxxx xxxx xxxxxxxxxxxxx. Xxxxxxxxxx xx, xxx xxxxx xxx, xxx xx to xxxxx, xxxx na xxxxxx xxxxx xxxxxxxxx použití xxxx xxxxxxxxxxxx xxxx. Xx-xx xxxxxxxxx xxxxx xx xxxx nestálá, xxxx xxx xxxxxxx xxxxxxxxx rozpouštědlo xxxxx xxxxxxx. Xxxx xx xx odstranit molekulárním xxxxx.
1.5.2.2 Koncentrace
Mezi xxxxxxxx, xxx se xxxxxxx xxx xxxxxxxxxxx nejvyšší xxxxxxxxxxx, xxxxx xxxxxxxxxxxx, xxxxxxxxxxx x systému x xxxxx xX xxxx. xxxxxxxxxx.
Xxxxxxxxxxxx xx xxxxxxx x xxxxxxxxxxxx xxxxxxxx x xxx xx x hlavním xxxxxxxxxxx, xxxxxxx se xxxxxxx vhodné indikace xxxxxxx xxxxxxxxx x xxxxx xxxxx, xxxx xx relativní klonovací xxxxxxxx (xxxxxxx) xxxx xxxxxxxxx celkový xxxx. Xx xxxxxx stanovit xxxxxxxxxxxx x rozpustnost x xxxxxxxxxxx xxxxxxxxxxxxx.
Xxxxxxx xx xxxxxxxxx xxxxx xxxxxxxxxxxxxx koncentrace. Xxxxxxx-xx x xxxxxxxxxxxx. xxxx xxxx koncentrace xxxxxxxx xxxxxx od maximální xx nízké xxxx xxxxxx toxicity. Xx xxxxxxx xxxxxxx, xx xx xxxxxxxxxx koncentrace xxxxxxx lišit xxxx xxx xxxxxxxx, xxxxx xxxx xxxx xxxxxxxxx 2 x √10. Xxxxxxx-xx maximální xxxxxxxxxxx x xxxxxxxxxxxx, xxxx xx vést x xxxxxxxxxxx xxxxxxx (xxxxxxxxx xxxxxxxxx xxxxxxxxx) xxxx xxxxxxxxxxx xxxxxxxxx růstu x 10-20 %, xx xxxx xxxx xxx 10 %. X xxxxxxxxx xxxxxxxxxxx xxxxx xx maximální xxxxxxxxx dávka xxxx xxx nejnižší x xxxxxx 5 mg/ml, 5 µl/ml x 0,01 M.
U xxxxxxxxx xxxxxxxxxxxxx látek, xxx xxxx netoxické x xxxxxxxxxxxxx xxxxxxx xxx xx xxxxxxxxxxx při xxxxx xx xxx xxxxx xxxxxxxxxxx, xx xxx nejvyšší použitá xxxxxxxxxxx vyšší, xxx xx xxx xxxxxxxxxxxx xx finálním xxxxxxxxxxx xxxxx xx xxxxx xxxxxxxxx s xxxxxxxxxx xxxxxx. Xxxx xxx xxxxxx xxxxxxxxxx rozpustnost xx xxxxxxx a xx xxxxx xxxxxxxx, xxxxxxx se xxxxxxxxxxx xxxx během expozice x xxxxxxxx xxxxxxxxxxx xxxxx, X9, xxxx xxx. xxxxx. Xxxxxxxxxxxxx xx dá xxxxxxx x xxxxxxx okem. Xxxxxxxxx xxxxx xxx xx překážku xxx xxxxxxxxx xxxxx.
1.5.2.3 Xxxxxxxx
X xxxxx xxxxxxx xxxxxxxxxxx xx xxxxxx provést x xxxxxxxx xxxxxxxxx x xxxxxxxxx (rozpouštědlo, xxxxxxxxx) kontroly, a xx xxx s xxxxxxxxxxxx xxxxxxxx, tak xxx xx. Xxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxxxx, xxxx být xxxxxxxxx xxxxxxxx látka xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx x xxxxxxxx mutagenního xxxxxx. Xxxx xxxxx xxx xxxxxxxxx xxxxxxxx xxxxx například:
|
|
|
|
|
|
|
Xx
|
XXXX
|
xxxxx xxxxxxxxxxxxxx
|
|
|
| &xxxx;
|
&xxxx;
|
xxxxx xxxxxxxxxxxxxxx
|
|
|
| &xxxx;
|
XX (xxxx x xxxxx kolonie)
|
methyl xxxxxxxxxxxxxx
|
|
|
| &xxxx;
|
XXXX
|
xxxxx xxxxxxxxxxxxxx
|
|
|
| &xxxx;
|
&xxxx;
|
xxxxx xxxxxxxxxxxxxxx
|
|
|
|
Xxx
|
XXXX
|
3-xxxxxxxxxxxxxxxx
|
|
|
| &xxxx;
|
&xxxx;
|
X-xxxxxxxxxxxxxxxxxxx
|
|
|
| &xxxx;
|
&xxxx;
|
7,12-xxxxxxxxxxxxxxxxxxxx
|
|
|
| &xxxx;
|
XX (xxxx x xxxxx xxxxxxx)
|
Xxxxxxxxxxxxx
|
|
|
| &xxxx;
|
&xxxx;
|
xxxxxxxxxx xxxxxxxxxxxxxx
|
|
&xxxx;
|
| &xxxx;
|
&xxxx;
|
xxxxx[x]xxxxx
|
|
|
| &xxxx;
|
&xxxx;
|
3-xxxxxxxxxxxxxxxx
|
|
|
| &xxxx;
|
XXXX
|
X-xxxxxxxxxxxxxxxxxxx (xxx vysoké koncentrace X-9)
|
|
|
| &xxxx;
|
&xxxx;
|
xxxxx[x]xxxxx
|
|
|
Xxx xxxxxxxxx xxxxxxxx xx xxxxx xxxxxx x xxxx vhodné xxxxx; jestliže xx xxxxxxxxx xxxxxxxxx historické xxxxx o 5-xxxx-2'-xxxxxxxxxxxx (XXX 59-14-3, xxxxx XXXXXX 200-415-9), xxx xxxxxx i tuto xxxxxxxxxx látku. Xxx, xxx xx to xxxxx, je xxxxxx xxxxxx pro pozitivní xxxxxxxx látku ze xxxxxx chemické xxxxxxx.
Xxx xxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxxx xx xxxxx xxxxxx x xxxxxxxxx xxxxxxxx, xx xxxxx xx používá xxxxxxxxxxxx xxxx xxxxxxxxx x xxxxxxxxxxx xxxxx, xxxxxxxxxx xxxxxxx xxxxxxxx xxxx xxxxxxxxxxxxxx xxxxxxx. Xxxxxx xx rovněž xxxxx zařadit xxxxxxxx xxx xxxxxxxxxxx ovlivnění, xxxxxx existují historické xxxxx xxxxxxxxxxx, xx xxxxxxx xxxxxxxxxxxx/xxxxxxxxx xxxxxxxxxx xxxxx pro xxxxx xxxxxxxxxx xx xxxxxxxxx xxxxxx.
1.5.3 Xxxxxx
1.5.3.1 Xxxxxxxx xxxxxxxxxx xxxxxx
Xx xxxxxxxxxxxxx xxxxx xx působí xxxxxxxxxx látkou xxx x xxxxxxxxxxxx xxxxxxxx, xxx xxx ní. Xxxxxxxx xxxxxxx po xxxxxxx xxxx (xxxxxxx xx xxxxxx doba 3-6 xxxxx). Xxxx xxxxxxxx xxxx xxxxxxxxxx xxxxx nebo více xxxxxxxxx xxxxx.
Xxx xxxxxx xxxxxxxxxxx xx xxxxxxxxx xxxxxxx xxxxxxxxxx xxxx xxxxx xxxxx. Xxxxxxx-xx xx xxxxx jedna xxxxxxx, je třeba xxxxxx počet xxxxxxxxxxx xxx, xxx se xxxxxxxx xxxxxxxxx xxxxx xxxxxx x analýze (xx. xxxxxxxxx xxx xxxxxxxxxxxxxxxx xxxxxxxxxxx). Xxxxxxx x xxxxxxxxx kontrolou (xxxxxxxxxxxxx/xxxxxxxxx) xx xxxxxxxxx xxxxxxxxxx.
X případě plynných xxxx xxxxxxxx xxxxx xx xxxxx xxxxxxxx x xxxxx xxxxxx xxxxxxx, jako je xxxxxxx xxxxxxxxxx uzavřených xxxxxxxxxxxx xxxxx.
5)1.5.3.2 Xxxxxxxxx xxxxxxxxx, viability a xxxxxxx xxxxxxxxx
Xx xxxxxxxx xxxxxxxx xx xxxxx xxxxxxx a xxxxxxxxx xx xxxxxxxxx přežívání x xxxxxxxxxxx xxxxxxx. Xx expozici xx xxxxxxx xxxxxx x xxxxxxxx cytotoxicity xxxxxxxxxx xxxxxxxxx xxxxxxxxx - xxxxxxx xxxxxxxxxx nebo xxxxxxxxxxx celkového xxxxx.
Xxxxx xxxxx má xxxxxx xxxxxxxxx časový xxxxxxxx xxx xxxxx xxxxxxxxx xxxxxxx nově xxxxxxxxxxxx xxxxxxx (XXXX x XXXX xxxxxxxx minimálně 6 - 8 xxx, XX xxxxxxxxx 2 xxx). Xxxxx xx pěstují v xxxxx s x xxx xxxxxxxxxx xxxxxxx xxx xxxxxxxxx počtu xxxxxxx x klonovací xxxxxxxxx. Xx xxxxxxxx xxxx xxxxxxx xx xxxxx x analýzou xxxxxxxxxx (xxxxxxxxx k xxxxxxx četnosti mutantů) xxxxxxxxx buněk na xxxxxxxxxx xxxxxx.
Xxxxx xx xxxxx x testu X5178X XX+/- pozitivní, xx xxxxx xxxxxxxxx xx xxxxx x xxxxxxxxxxxxxxxx xxxxxx (nejvyšší xxxxxxxxx xxxxxxxxxxx) a xx xxxxxxxxxxx a xxxxxxxxxxx xxxxxxxxxx stanovit xxxxxxxx xxxxxxx. Xxxxx xx xxxxx x xxxxx testu xxxxxxxxx, xxxxx xx xxxxxxxx xxxxxxx x xxxxxxxxx x pozitivní xxxxxxxx. Xxxxxx xx může xxxxxxx x xx xxxxxxxx x TK6TK+/-.
2 XXXXX
2.1 Xxxxxxxxxx xxxxxxxx
Xxxx xxxx xxxxxx výsledky xxxxxxxxx cytotoxicity x xxxxxxxxxx, počty xxxxxxx x xxxxxxx frekvence x xxxxxxxxxxxxxxxx x xxxxxxxxxxx kultur. V xxxxxxx xxxxxxxxx xxxxxx x xxxxx L5178TK
+/- xx xxxxxxx xxxxxxx xxxxxx xxxxxxxx xxxxxx x xxxxxxx kolonií xxxxxxxxxxxx v jedné xxxxxxxxxxx testované xxxxx (xxxxxxxx xxxxxxxxx xxxxxxxxxxx) x v xxxxxxxxx x xxxxxxxxx xxxxxxxx. Xxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxxxx xxxxxxx i xxxxxx kolonií xxxx xxxxxxxx prostudovány x xxxxxxxxxxx.
5) Xxx xxxxx XX
+/- xx xxxxxxx xxxxxxx podle xxxxxxxx xxxxxxx xxxxxxxxxx xxxxx (xxxxx) a pomalého xxxxx (xxxx).
5) Mutanty, xxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxxx poškození, xxxx xxxxx xxxx xxxxxxxx, x xxxxx xxxxx xxxx xxxxxxx. Xxxxxxx xxxxxx xxxxxxxxx obvykle xxxx xx xxxxxx xxxxxx xxxx po xxxxxxxxxxxx viditelné xxxxxxxxxxxx xxxxxxx. Xxxxxx xxxxxx xxxxxxx xx asociována x xxxxxxxx látkám xxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx.
5) Méně xxxxxxx xxxxxxxxx xxxxxxx rostou xxxxxxxx rychlostí xxxx xxxxx xxxxxxxxxx x xxxxxxxxx xxxxx xxxxxxx.
Xx xxxxx xxxxxx xxxx xxxxxxx (xxxxxxxxx klonovací xxxxxxxx - xxxxxxxx xxxxxxx xxxxxxxxxx) xxxx xxxxxxxxx xxxxxxx růst. Xxxxxxx xxxxxxxxx se xxxxxxxxx xxxx xxxxx xxxxxxxxxx buněk xxxxxx xxxxxx xxxxxxxxxxxxx xxxxx.
Xxxxxxx xx individuální údaje x xxxxxxxxxxxx xxxxxxxxxx; xxxxxxx xx xxxxxxx xxxx xxxxxx x xxxxxxxxx xxxxx.
Xxxxxxxxxx zjevně xxxxxxxxx xxxxxx xx xxxxxxxxxx. Xxxxxxxxxxxxx výsledky xx xxxxxxxxx xxxxxx xxxxxxxxxx, xxxxxxx za xxxxxxxxxxxxxx xxxxxxxxxxxxxxxx podmínek. Xxxxxxxxx xxxxxxxx se xxxx potvrdit xxxxxx xx případu. X xxxxxxxxx, kdy se xxxxxxxxx xxxxxxxxxxx výsledků xxxxxxxxxx za xxxxx, xx xxxxx podat xxxxxxxxxx. V xxxxxxx xxxxxxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxx xx xxxxx x xxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx tak, xxx xx xxxxxxxxx xxxxxxx xxxxxxxx. X xxxxxxxxxx, xxxxx se xxxx x experimentu xxxxxxxxxxx, xxxxx xxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxx.
2.2 Xxxxxxxxxxx x interpretace xxxxxxxx
Xx xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxx několik xxxxxxxx, xxxxxxxxx na xxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxx nebo xxxxxxxxxxxxxxxx nárůst xxxxxxx xxxxxxxxx. Xxxxxxx xx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx. Při xxxxxxxxxxxxx xxxxxxxx testu xx xxxxx xxxxxx xxxxxxxxxxx xxxxxx. Xxxxxxxxxxx xxxxxxxxxx xx však xxxxxx být xxxxxxx xxxxxxxxx faktorem xxxxxxxxxxx xxxxxxxx.
Xxxxxxxxx xxxxx, při xxxxxx xxxxxxx výsledky xxxxxxxxx výše xxxxxxx xxxxxxxx, se v xxxxx xxxxxxx xxxxxxxx xx xxxxxxxxxxx. Většina xxxxxxxxxxx xxxx poskytuje xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxx, x xxxxxxxxxxx xxxxxxxxx xxxx xxxxx ze získaného xxxxxxx dat vyvodit x xxxxxxxx testované xxxxx definitivní xxxxx. Xxxxxxxx xxxxx xxx xxxxx nejednoznačné nebo xxxxxxxxxxxxx, i xxxx xx xxxxxxxxxx xxxxxxxxxx xxxxxxx.
Xxxxxxxxx xxxxxxxx xxxxx xx xxxxxx mutace x xxxxxxx xxxxxxx xx xxxxx xxxxxxx, xx xxxxxxxxx xxxxx xxxxxxxx v xxxxxxx xxxxxxx xxxxx xxxxxx xxxxxx. Xxxxxxxxxxxxxx xx xxxxxxxxxxxxxxxx xxxxxxxxx xxxxx xxxxx-xxxxxx. Xxxxxxxxx xxxxxxxx xxxxxxx. že xx xxxxxx experimentálních xxxxxxxx xxxxxxxxx látka x xxxxxxx savčích buněk xxxxxxxxxx xxxxxx xxxxxx.
3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx s xxxxxxxxxxx právními předpisy
9) xxxx xxx zpracován xxxxxxx xxxxxx a x průběhu xxxxxx xx nutno xxxx xxxxxxxx.
Xx xxxxxx o xxxxxxx xxxxxx xx xxxxx xxxxx xxxx xxxxxxxxx:
Xxxxxxxxxxxx/xxxxxxxxx:
- xxxxxxxxxx xxxxx xxxxxxxxxxxx/xxxxxxxx,
- xxxxxxxxxxx a xxxxxxxxx testované xxxxx x rozpouštědle/vehikulu, xxxxx xx xxxxx.
Xxxxx:
- xxx x xxxxx xxxxx,
- xxxxx buněčných kultur,
- xxxxxxxx počet pasáží ,
- xxxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxxx,
- xxxxxxx xxxxxxxxxxx.
Xxxxxxxx pokusu:
- xxxxxxxxxx xxxxx použitých xxxxxxxxxxx x počtu xxxxxx, včetně xxxx. xxxxx o xxxxxxxxxxxx x limitech v xxxxxxxxxxxx, jsou-Ii x xxxxxxxxx,
- xxxxxxx xxxxx, xxxxxxxxxxx XX2,
- koncentrace xxxxxxxxx xxxxx,
- xxxxx xxxxxxxx a přidané xxxxxxxxx xxxxx,
- inkubační xxxxxxx.
- xxxx xxxxxxxx,
- xxxx xxxxxxxx xxxxx,
- xxxxxxxx xxxxxxx xxxxx xxxxx expozice,
- typ x složení systému xxxxxxxxxxx aktivace, xxxxxx xxxxxxxx xxxxxxxxxxxxxxxxx,
- pozitivní x negativní kontroly,
- xxxxx xxxxxxxx xxxxxxx (xxxxxxxx xxxxxx počtu xxxxxxxxxxxxx xxxxx, xxxxxxxxx)
- xxxxxxxx xxxxxxx,
- kritéria, xxxxx xx studie xxxxxxx jako pozitivní, xxxxxxxxx xxxx nejednoznačná,
- xxxxxx zjišťování xxxxx xxxxxx x xxxxxxxxxx xxxxx,
- definice xxxxxxx, x nichž xx xxxxxxx xxxxxxxx x xxx (xxxxxx xxxxxxxxxx xxxxxxxx xxx rozlišování xxxx "xxxxxx" a "xxxxxxx" koloniemi).
Výsledky:
- známky xxxxxxxx,
- xxxxxx srážení,
- xxxxx x pH x xxxxxxxxxx během xxxxxxxx testované xxxxx, xxxx-xx xxxxxxxxx,
- xxxxxxxx xxxxxxx, je-li hodnocena, xxxxxxxxx pro xxxxxxxxx x pozitivní xxxxxxxx,
- xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx xxxx xxxxxxx xxxxxxx pomocí systému X5178X XX+/-
- xxxxx xxxxx- xxxxxx, xx-xx xx xxxxx,
- xxxxxxxxxxx xxxxxxx, xxxx-xx xxxxxxxxx,
- xxxxxxxx xxxxx x xxxxxxxxxxx (xxxxxxxxxxxx/xxxxxxxxx) a xxxxxxxxxxx kontrol,
- historické xxxxx x negativních (xxxxxxxxxxxx/xxxxxxxxx) x pozitivních xxxxxxx, xxxxxx rozpětí, xxxxxxx x směrodatných xxxxxxxx
- četnost xxxxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.18 XXXXXXXXX XXX XXXXXXXX - XXXXXXXXXXX XXXXXXX XXX - XXXXX XXXXX IN XXXXX
1 XXXXXX xx x xxxxxxx x xxxxxx Evropských společenství.
1)1.1 Xxxxxxx xxxxxx
Xxxx xxxxxxxxxxx xxxxxxx XXX (XXX) xxxxxxxx xxxxx xxxxxxxxx xxxxxxx DNA xx xxxxxx x xxxxxxxxxx xxxxx XXX obsahující xxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxx. Xxxx xx xxxxxxx xx inkorporaci xxxxxxxxx xxxxxxxx (3X-XxX) xx XXX savčích xxxxx, xxxxx xxxxxx x X fázi xxxxxxxxx xxxxx. Xxxxxxx 3X-XxX xx stanoven xxxxxxxxxxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxx metodou (XXX) x exponovaných xxxxxxx. Xxxxxxxxx xx xxxxx xxxxxxx kultury, xxxxx xx xxxxx xxxxxxxx xxxxxxx xxxxxxx hepatocytů xxxxxxx, xxxxx xxxx xxxxxxxxxx testovanou xxxxxx xxx x xxxxxxxxxxx, xxx x x xxxxxxxxxxxxx exogenního xxxxxxxxxxxxx xxxxxxxxxxx systému. XXX xxxx být také xxxxxxxxx v systému xx xxxx.
1.2 Xxxxx xxxxxx
1.2.1 Příprava
Testované xxxxx x xxxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxx xxxxxxxxxx xx xxxxxxxx xxxx xxxxxxxxxx v xxxxxxxxxxx médiu nebo xx xxxxxxx rozpouštědle. Xxxxx xxxxxx se xxxxxxx xxxxx kultivačním xxxxxx. Xxxxxxx xxxxxxxxxxx xxxxxxxxxxxx x xxxxxxx xxxxx nepříznivě xxxxxxxxxx xxxxxxxxx buněk.
Používají se xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, lidských xxxxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxxxx xxxxx (lidské diploidní xxxxxxxxxxx).
Xxxxx jsou exponovány xxxxxxxxx xxxxx x xxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx aktivačního xxxxxxx.
1.2.2 Experimentální xxxxxxxx
1.2.2.1 Xxxxx xxxxxx
Xxx xxxxx xxxxxxxxxxxxxx xxx xx xxxxxxx nejméně xxxx xxxxxxxxx xxxxxx xxx xxxxxxxxxxxxxxx x xxxxx xxxxxx (xxxx méně, xx-xx xx xxxxxxx xxxxxxxxxxxxx) pro LSC XXX.
1.2.2.2 Negativní x xxxxxxxxx xxxxxxxx
X každém xxxxxxxxxxx xxxx xxx xxxxxxxx xxxxxxxx negativní x xxxxxxxxx kontroly x xxxxxxxxxxx x x nepřítomnosti xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx.
Xxxx pozitivní xxxxxxxx xxx xxx xxxxxxx hepatocyty xxxxxx 7,12-xxxxxxxxxxxx-xxxxxxxxx (7,12-XXXX), xxxx 2-xxxxxxxxxxxxxxxxxx (2-XXX). Jako xxxxxxxxx xxxxxxxx pro xxxxxxxxxxxxx xxxxxxx xxxxx xxx pro autoradiografii, xxx x xxx XXX xxx xxxxxxxxxxx xxxxxxxx xxx xxxxxx 4-xxxxxxxxxxxxx-X-xxxx (4-XXX). Xxxx xxxxxxxxx kontrolu xxx xxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx xxx xxxxxx X-xxxxxxxx-xxxxxxxxxx.
1.2.2.3 Koncentrace xxxxxxxxx xxxxx
Xxxx xxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx. Nejvyšší koncentrace xxxx vyvolávat xxxxxxxxxxx xxxxx.
Xxxxx xx vodě xxxxxx xxxxxxxxx xxxx xxx testovány x xxxxxxxxxxxxx xx xx xxxxxxx xxxxxxxxxxxx za xxxxxxx vhodných xxxxxxx. Xxx xxxxxxxxx látky xx vodě xxxxx xxxxxxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxxxxx látky xxxxxx případ od xxxxxxx.
1.2.2.4 Buňky
Pro xxxxxxxxx xxxxxx xxxx být xxxxxxx xxxxxx xxxxxxx xxxxxx, xxxxxxxxxxx CO2, xxxxxxx x xxxxxxx. Xxxxxxxxxxxxx xxxxxxx xxxxx xxxx xxx xxxxxxxxxx xxxxxxxxxxxx xx přítomnost Xxxxxxxxxxx.
1.2.2.5 Xxxxxxxxxxx xxxxxxxx
Xxx xxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxxxxx aktivační xxxxxx xxxxxxxxx. Xxxxxxxxxxxxx xxxxxxx xxxxx a xxxxxxxxx xxxx exponovány testované xxxxx v xxxxxxxxxxx x nepřítomnosti vhodného xxxxxxxxxxxxx aktivačního xxxxxxx.
1.2.3 Xxxxxxx xxxxxxxxxx
1.2.3.1 Xxxxxxxx xxxxxx
Xxxxxxxxxxxxx xxxxxxx xxxxx xx xxxxxxxxxx xx xxxxxxx xxxxxxx (xxxxxxxxxx xxxx setřepáním xxxxx x povrchu xxxxxxxxxx xxxxxx), xxxxxxxxx xx xx xxxxxxxxxxxx xxxxx xx xxxxxx xxxxxxx x xxxxxxxx xxx 37 °X.
Xxxxxxxxxx xxxxxxx xxxxxxxxx hepatocytů xx xxxxxxxxxx xxx, xx xx xxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xx ve xxxxxxx xxxxx x xxxxxxx xxxxxxxxxx xxxxxx.
Xxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxx vhodné xxxxxx.
1.2.3.2 Xxxxxxxx xxxxxx testované xxxxx
Xxxxxxxx xxxxxxxxxx xxxxxxx. Xxxxxxx xxxxxxxxx hepatocyty xxxxxxx jsou exponovány xxxxxxxxx látce x xxxxx xxxxxxxxxxx 3X-XxX xx xxxxxxx xxxx. Xx xxxxxxxx xxxxxxxx xx médium xxxxxxxxxx, xxxxx xxxxxxx, fixovány x sušeny. Sklíčka xxxx xxxxxxxx xx xxxxxxxxxxxxxxxxx xxxxxx (xxxxxxxxxxxx xxxx xxx použit xxxxxxxxx xxxx), xxxxxxxxxx, xxxxxxxx, obarvena a xxxxxxxxxxx.
Xxxxxxxxxxxxx buněčné xxxxx x xxxxxxxxx
Xxxxxxxxxxxxxxxxx xxxxxxxx: Xxxxxxx xxxxxxx xxxx xxxxxxxxxx xxxxxxxxx látce xx xxxxxxx dobu x pak xxxx xxxxxxxxx působení 3H-TdR. Xxxx xxxxxxxx je xxxxxxx xx xxxxx xxxxxxxxx xxxxx, aktivitě xxxxxxxxxxxxx systému x xx xxxx xxxxx. X zachycení xxxxxxxxxx xxxxxxx XXX xx xxxxx 3X-XxX xxxxxx xxxxxxxx x xxxxxxxxxx xxxxxx xxxx několik xxxxx xx xxxxxxxx. Xxxxx xxxx těmito xxxxxxx xx xxxxxxxx xxxxxx xxxxxxxxx mezi xxxxxxxxxx látkou x 3X-XxX. X xxxxxxxx xxxx UDS x xxxxxxxxxxxxxxxxx xxxxxxxxx XXX xx xxxxx xxxxxxx xxxxxxxxxxx xxxxxx, nízký xxxxx séra xxxx xxxxxxxx xxxxxxxxxxx do xxxxxxxxxxxx média, xxx xxxxxxx xxxxxxxx xxxxxxxxxxxxxxxxx xxxxxxxxx XXX.
Xxxxxxxxx XXX xxxxxx XXX: Xxxx xxxxxxxx xxxxxxxxx látce xx xxxxx xxxxxxxx xxxxx xxxxx do X-xxxx, xxx bylo xxxxx xxxxxxx. Buňky xxxx xxx exponovány xxxxxxxxx xxxxx, jak xxxx xxxxxxx pro xxxxxxxxxxxxxxx. Xx konci xxxxxxxxx xx XXX xxxxxxxxxxx x buněk x xxxxxxxx xxxxxxx xxxxx XXX x xxxxx xxxxxx inkorporace 3X-XxX.
Xxxxxxxx xxxx xxxxxxx xx xxxxx uvedených xxxxxxxx lidské xxxxxxxxx, xx x xxxxxxxxxxxxxxx xxxxxxxxx suprese semikonzervativní xxxxxxxxx DNA xxxxxxxx.
1.2.4 Xxxxxxx
1.2.4.1 Xxxxxxxxxxx autoradiografie
Při xxxxxxxxxxxxx XXX v xxxxxxx kultuře xx xxxxx v S-fázi xxxxxxxxx. Hodnotí xx xxxxxxx 50 buněk x xxxxxx xxxxxxxxxxxxxxx xxxx. Xxxxxxxxx je xxxxx zakódovat před xxxxxxxxxxxxxx. X každém xxxxxxxxx se hodnotí xxxxxxx náhodně xxxxxxxxx xxxx. Xxxxxxxx xxxxxxxxxxxxxxx 3X-XxX x cytoplazmě xx xxxx x xxxx x velikosti xxx xxxxx x xxxxxxxxxx xxxxx xxxxxxxxx xxxxx.
1.2.4.2 Xxxxxxxxxxx XXX
Xxx xxxxxxxxx XXX XXX xx xxxxxxx xxxxxxxxx xxxxx xxxxxx xxx xxxxxx xxxxxxxxxxx testované xxxxx x xxx xxxxxxxx.
Xxxxxxxx xxxx xxx xxxxxxxxx x nezávislých xxxxxxxxxxxxx.
2 ÚDAJE
Údaje musí xxx xxxxxxx x xxxxxxxxx.
2.1 Xxxxxxxxxxx xxxxxxxxxxxxxxx
Xxxxxx xxxxxxxxxxx 3H-TdR xx xxxxxxxxxx a xxxxx xxx xxxxxxxxxx mimo xxxxxxx jádro xx xxxxxxxxxxxxx xxxxxxxx.
Xxxxxx xxxxxxxxxxx 3X-XxX do cytoplazmy x počet xxx x jádře xx xxxxxxxx pomocí xxxxxxx, xxxxxxx x modu.
2.2 Xxxxxxxxxxx XXX
Xxxxxxxxxxx 3X-XxX xx xxxxxxxxxxx xxxx xxx/µx XXX. Xxxxxxxx xxxxxxx xxx/µx XXX xxxxx xx směrodatnou xxxxxxxxx xx xxxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxxx.
Xxxxx se xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxx.
3 XXXXXXX XXXXXX, PROTOKOL XXXXXX X XXXXXXXXX XXXXXX
X souladu s xxxxxxxxxxx xxxxxxxx předpisy
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx x x xxxxxxx xxxxxx xx nutno xxxx xxxxxxxx.
Xxxxxx x průběhu xxxxxx xxxxxxxx xxxx xxxxxxxxx x:
- xxxxxxxxx xxxxxxx, xxxxxx xxxxxxx x číslu xxxxxx x xxxx xxxxxxxxx xxxxxxx, počtu buněčných xxxxxx,
- xxxxxxxx xxxxxxxxx x udržování xxxxxxx, xxxxx, teplotě, xxxxxxxxxxx XX2,
- xxxxxxxxx xxxxx, xxxxxxxxxxxx, xxxxxxxxxxxxx x xxxxxxxxxx jejich výběru x xxxxxxxxxxx,
- xxxxxxxxxxxx xxxxxxxxxx xxxxxxx,
- pokusném xxxxxxxx,
- pozitivních x xxxxxxxxxxx xxxxxxxxxx,
- xxxxxxxxx xxxxxxxxxxxxxxxxxxx xxxxxxxx,
- xxxxxxxxx xxxxxxxxx xxxxxx xxxxx xx X-xxxx,
- xxxxxxxxx xxxxxxxxx k xxxxxxxx XXX x k xxxxxxxxxxx xxxxxxxxx xxxxxx XXX při xxxxxx XXX,
- vztahu xxxxx/xxxxxx, xx-xx xx xxxxx,
- xxxxxxxxxxxx vyhodnocení.
Diskuse výsledků.
Závěry.
B.19 XXX - VÝMĚNA XXXXXXXXXXX CHROMADIT IN XXXXX
1 METODA xx x xxxxxxx x xxxxxx Xxxxxxxxxx společenství.
1)1.1 Xxxxxxx xxxxxx
XXX je xxxxxxxxxx test xxx xxxxxxx recipročních xxxxx XXX xxxx xxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx. XXX reprezentují výměny xxxxxxxxxxx sekvencí XXX xxxx xxxxxxxxxxxx xxxxxxxx x identických (xxxxxxxxxxx) xxxxxxxx. SCE xxxxxxxxxxxxx xxxxxxxx zlom x xxxxxxxx xxxxxxx, xxx xx xxxxx xxxx xxxxxxxx o molekulárním xxxxxxx xxxxxx xxxxxxx. Xxxxxxx SCE xxxxxxxx xxxxxxxxxx značení xxxxxxxxxxx xxxxxxxxx. Xxxx xx xxxxxxxx inkorporací xxxxxxxxxxxxxxxxx (XxxX) xx xxxxxxxxxxxxx XXX xx xxxx xxxx xxxxxxxxx xxxxx.
Xxxxx xxxxx xx vitro xxxx exponovány xxxxxxxxx xxxxx x xxxxxxxxxxx x xxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx, xx-xx xx xxxxxxxx. Xxxxxxxxx se xx xxxx dvou xxxxxxxxxxxx cyklů v xxxxx xxxxxxxxxxx XxxX. Xx xxxxx kultivace xx buňky xxxxxxx xxxxxxxxxxx xxxxxxxx vřeténka (xxxx. xxxxxxxxx) x xxxxxxxxx xxxxx x x-xxxxxxxx xxxxxx. Po xxxxxxxx xxxxxxxxx xxxx xxxxx xxxxxxxxxx x xxxxxxxxxx xxxxxxxxx xxx xxxxxxx chromozómů.
1.2 Popis xxxxxx
1.2.1 Xxxxxxxx
Xxxxxxxxx xx xxxxxxxxxxxx, (xxxxxx xxxxxxxxx) xxxx xxxxxxxxxxxxx xxxxxxx xxxxx (ovariální xxxxx xxxxxxxx xxxxxx). Xxxxxxx xxxxx xxxx xxx xxxxxxxxxxxx z xxxxxxxx xxxxxxxxxxx Xxxxxxxxxxxx,
Xxxxxxxxx xx xxxxxx kultivační média x xxxxxxxxxx xxxxxxxx (xxxxxxx, xxxxxxxxxx xxxxxx, xxxxxxxxxxx CO2 x xxxxxxx),
Xxxxxxxxx xxxxx xx xxxxxxxxx, nebo xxxxxxxxxx x xxxxxxxxxxx médiu xxxx ve vhodném xxxxxxxxxxxx. Výsledná koncentrace xxxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx, xxxxxxxx xxxxx xxxx xxxxxxxxx XXX,
Xxxxx xx xxxxxxxx xxxxxxxxx xxxxx x přítomnosti x xxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxx savčího metabolického xxxxxxxxxxx systému. Xxxxxxxxx xx xxxxxxx xxxxxxxxx xxxx x xxxxxxx (xxxxxxx) xxxxxxxxxxxx xxxxxxxxx, xxxxxxxx úroveň a xxxxxxxxxx xxxx xxxxxxxx xxxx xxxxxx xxx xxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxx.
1.2.2 Xxxxxxxxxxxxxx xxxxxxxx
1.2.2.1 Xxxxx xxxxxx
Xxx xxxxx xxxxxxxxxxxxxx xxx xx xxxxxxx nejméně xxx xxxxxxx.
1.2.2.2 Negativní x xxxxxxxxx xxxxxxxx
X xxxxxx xxxxxxxxxxx xxxx xxx xxxxxxxx pozitivní xxxxxxxx x xxxxxxx x xxxxxx mutagenním xxxxxxx x látky vyžadující xxxxxxxxxxxx xxxxxxxx. Xxxx xxxx xxx xxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxx rozpouštědlem.
Jako xxxxxxxxx xxxxxxxx lze xxxxxx:
- xxxxx působící mutageny: xxxxxxxxxxxxxxxxx
- xxxxxxx xxxxxxxx xxxxxxxx: xxxxxxxxxxxxx
Xx-xx xxxxx, xx možné zařadit xxxxx xxxxxxxxx kontrolu xx xxxxxx xxxxxxxx xxxxxxx xxxx je xxxxxxxxx látka.
1.2.2.3 Xxxxxxxxxxx
Xxxxxxx xx nejméně xxx xxxxx. Xxxxxxxx koncentrace xxxxxxxxx látky musí xxx xxxxxxxxxxxxx toxický xxxxxx, xxx xxxxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxx. Xx xxxx relativně nerozpustné xxxxx xx xxxxx xxxxxxxx xx na xxxxxxx xxxxxx rozpustnosti xx xxxxxxx xxxxxxxx xxxxxxx. Xxxxxxxx xxxxxxx xxxxxxxxxxx xx vodě xxxxxxxxx xxxxxxxxx xxxxx xx xxxxxx xxxxxxxxxxxx.
1.2.3 Xxxxx xxxxxxx
1.2.3.1 Xxxxxxxx xxxxxx
Xxxxxxxxxxxxx xxxxxxx linie xx xxxxxxxxxx ze xxxxxxx xxxxxxx (trypsinací xxxx xxxxxxxxxx xxxxx x povrchu xxxxxxxxxx xxxxxx), inokuluje se xx kultivačních nádob xx vhodné xxxxxxx x xxxxxxxx xxx 37 °X. Xxx xxxxxxxxxxxx xxxxxxx xx xxxxxxx xxxxxx xxxxx xxxxx x xxxxxxxxxx xxxxxx, aby na xxxxx xxxxxxxxx nevytvářely xxxx než x 50 % xxxxxxxxxxx xxxxxx. Xxx xxxx xxxxxx suspenzních kultur. Xxxxxx lymfocytární kultury xx xxxxxxxx x xxxxxxxxxxxxxx xxxx běžnými xxxxxxx x xxxxxxxx xxx 37 °X.
1.2.3.2 Xxxxxxxx kultur
Buňky jsou xxxxxxxxxx testované xxxxx x exponenciální fázi xxxxx po xxxxxxx xxxx. Ve xxxxxxx xxxxxxx xxxxx jedna xx xxx xxxxxx, xxx xxxxxxxx xxxx xxx xxxxxxxxxxx až xx xxx buněčné xxxxx, je-li xx xxxxx. Xxxxx, xxxxx xxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx, xxxx xxx xxxxxxxxxx xxxxxxxxxx xxxxxx x xxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx systému. Xx xxxxx xxxxxxxx xx xxxxxxxxx xxxxx x média xxxxxxxxxx, xxxxx xxxxxx a xxxx xxxxxxxxxxx v xxxxxxxx xxxxx x XxxX xxx xxxxxxxxxx xxxxx. Xxxxxxxxxxxx xxxxx xxx xxxxx exponovány xxxxxxxx x xxxxxxxxxx xxxxxx x BrdU xx dobu dvou xxxxxxxxx cyklů.
Lidské lymfocytární xxxxxxx xxxx exponovány xxxxxxxxxx xxxxxx, dokud xxxx v xxxxxxxxxxxxxxxxxxxxx xxxxxxxxxx.
Xxxxx jsou xxxxxxxxxxx x xxxxxx xxxxxxxxxx xxxxxx xx xxxxxxxx xxxxxxxxx xxxxx, xxxxx xxxxxxxx x xxxxxxxxxxxxxx xxxxxx buněčného xxxxx. Xxxxxxx kultury x XxxX xx xxxxx xxxxxxxx v xxxxx xxxx ve xxxxxx xxxxxxxxx xxxxxxx, xxx xx zabránilo xxxxxxxx XXX, xx které xx xxxxxxxxxxxxx XxxX.
1.2.3.3 Xxxxxxxxxx xxxxx
Xxxxx xx xxxxx hodiny xxxx xxxxxxxxx kultivace xx xx xxxxxx xxxxx xxxxxxxxx xxxxxxxx xxxxxxxx (xxxx. xxxxxxxxx). Každá xxxxxxx xx xxxxxxxxxx xxxxxxxxxx.
1.2.3.4 Xxxxxxxx xxxxxxxxx x xxxxxxx
Xxxxxxxxx xx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxxxxxxx xx znázornění XXX xxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxxx (xxxx. xxxxxxxxxxxxx xxxx Xxxxxx).
1.2.3.5 Xxxxxxx
Xxxxx analyzovaných buněk xx xxxxxxx xx xxxxxxxxx xxxxxxxxx XXX x kontrole. Obvykle xx xxxxxxx xxxxxxx 25 xxxxx xxxxxxxxxxxxxx xxxxxxxx xx xxxxxx xxxxxxx. Preparáty musí xxx xxxxxxxxxx xxxx xxxxxxxx. X xxxxxxxx xxxxxxxxxxx xx xxxxxxxxx xxxxx metafáze s 46 centromerami. X xxxxxxxxxxxxxxx xxxxx xxxxx xxxxxxxx, xxxxx se xxxx x ± 2 xxxxxxxxxx xx xxxxxxxxx xxxxx xxxxxxxxx. Xx xxxxx xxxxxxxx, xxx xx budou xxxxxxxxxx SCE x xxxxxxx xxxxxxxxxx. Xxxxxxxx xxxx být xxxxxxx x nezávislých xxxxxxxxxxxxx.
2 XXXXX
Xxxxx xx zapisují xx xxxxxxx. Zaznamenává xx počet XXX x xxxxx xxxxxxxx x počet XXX/xxxxxxxxx xxxxxx xxx každou xxxxxxxx x exponovaných x kontrolních xxxxxxxxx.
Xxxxx xx hodnotí xxxxxxxx xxxxxxxxxxxxx xxxxxxxx.
3 PROJEKT XXXXXX, XXXXXXXX XXXXXX X ZÁVĚREČNÁ XXXXXX
X xxxxxxx s příslušnými xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx a o
průběhu xxxxxx xx xxxxx xxxx xxxxxxxx.
Xxxxxx x xxxxxxx pokusu xxxxxxxx xxxx xxxxxxxxx o:
- xxxxxxxxx buňkách, xxxxxxxx xxxxxxxxx k udržování xxxxxxx,
- xxxxxxxxxxxx xxxxxxxxxx: xxxxxxx média, xxxxxxx, xxxxxxxxxxx XX2, xxxxxxxxxxx xxxxxxxxx xxxxx, rozpouštědle, xxxxxxxxxxxx nádobách, xxxxx xxxxxxxx, xxxxxxxxxx xxxxxx x xxxx xxxxxxxxxxx x xxxx délce xxxxxxxx, metabolickém xxxxxxxxxx xxxxxxx, xxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxx,
- xxxxx xxxxxx pro každý xxxxxxxxxxxxxx bod,
- xxxxxxx xxxxxxxx mikroskopických xxxxxxxxx
- xxxxx xxxxxxxxxxxxx xxxxxxxx (xxxxxxxx xxx xxxxxx xxxxxxx)
- xxxxxxxxx počtu XXX/xxxxx x SCE/chromozóm (xxxxxxxx pro xxxxxx xxxxxxx
- xxxxxxxxxx hodnocení XXX
- zdůvodnění xxxxxx xxxxxxxxxxx
- xxxxxx xxxxx/xxxxxx, xx-xx to xxxxx,
- xxxxxxxxxxxx xxxxxxxxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.20 XXXXXXXXX LETÁLNÍ XXXXXX XXXXXX XX XXXXXXX X DROSOPHILA MELANOGASTER
1 XXXXXX xx v xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
1)1.1 Princip xxxxxx
Xxxx na xxxxxxxxx xxxxxxx xxxxxx vázané xx pohlaví (SLRL) xx Xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx xxxxxx, xxx genových, xxx x malých xxxxxx, x xxxxxxxxxxx xxxxxxx xxxxx. Xx xx xxxx xx xxxxxxx xxxxxx xxxxxx xxx xxxxxxxx xxxxxx v xxxxxxxxx 800 xxxxxxxx xxxxxxxxxx X. Xxxx xxxxxxxxxxxx xxx 80 % všech xxxxxx X-xxxxxxxxxx. X-chromozóm xxxxxxxxxxxx xxxxxxxxx 115 xxxxxx xxxxxxxxxxx xxxxxx.
Xxxxxx v X-xxxxxxxxxx se xxxxxxxxxxx xxxxxxx x samců xxxxxxxxx xxxxxxxx xxx. Xxxx xx mutace xxxxxxx x xxxxxxxxxxxx xxxxx, xxx na xxxx přítomnost xxxxxxxx x absence xxxxxxx xx xxxx xxxx xxxxxxx potomků, xxxxx xx xxxxxxxx rodí xxxxxxxxxxxxx xxxxxx. XXXX xxxx je výhodný xxxxxxxx x xxxxxxxxxx xxxxxxx x uspořádání xxxxxxxxxx.
1.2 Popis xxxxxx
1.2.1 Xxxxxxxx
1.2.1.1 Xxxxxx
Xxxxxxxxx xx xxxxx dobře xxxxxxxxxx xxxxxx xxxxx x xxxxxx xxxxx Xxxxxx-5. Xxxxx xxx použity x jiné vhodné xxxxx xxxxxxx linie xxxxx x xxxxxxxxxxxx xxxxxxx X-xxxxxxxxxx.
1.2.1.2 Xxxxxxxxx xxxxx
Xxxxxxxxx látky se xxxxxxxxxxx ve xxxx. Xxxxx ve vodě xxxxxxxxxxx xx xxxxxxxxxxx xxxx xxxxxxxxxx ve xxxxxxx xxxxxxxxxxxx (xxxx. xxxx xxxxxxx x Xxxxxx-60 xxxx 80), xxxx aplikací xx xxxx ředí xxxxx, xxxx fyziologickým xxxxxxxx. Xxxxxxxxxx xx xxxxxxxxxx xxxxxxxxxxxxxxx (DMSO) jako xxxxxxxxx.
1.2.1.3 Počet xxxxxx
Xxxx xx xxxxxx určenou xxxxxxxxx. Spontánní frekvence xxxxxx x xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxx počet xxxxxxxxxxx xxxxxxxxxx, xxxxx xx xxxxx analyzovat.
1.2.1.4 Xxxxxx xxxxxxxx
Xxxxxxxx xxxxxxxxx xxxxx xx xxxxxxxxxxx xxx xx, injekčně xxxx xxxxxxxx xxxxxx xxxx xxxxx. Xxxxxxxxx xxxxxxxxx xxxxx xx xxxxxxx x cukerném roztoku. Xx-xx xx xxxxx, xxxxxxxxx xxxxx se xxxxxxxx x 0,7 % roztoku NaCl x xxxxxxxx xx xx xxxxxx xxxx xxxxxx dutiny.
1.2.1.5 Xxxxxxxxx x xxxxxxxxx xxxxxxxx
X xxxxxx xxxxxx xx xxxxxxxx negativní (x xxxxxxxxxxxxx) x xxxxxxxxx xxxxxxxx. Xxxxxxxx má xxxxxxxxx x xxxxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxx, není třeba xxxxxxxxx do experimentu xxxxxxxx xxxxxxxx.
1.2.1.6 Dávkování
Používají xx xxx xxxxx xxxxxxxxx xxxxx. Xxx xxxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxx jedna xxxxx xxxxxxxxx xx xxxxxxxxx tolerované koncentraci xxxx xxxxxxxxxxxx známky xxxxxxxx. Xxxxxxxxx xxxxx xx xxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxx.
1.2.2 Xxxxx xxxxxxx
Xxxxx divokého xxxx (xx xxxxx 3-5 dnů) xxxx xxxxxxxxx xxxxxxxxxx xxxxxx x xxxxxxxxxxxx kříženi x xxxxxxxxxx samicemi x xxxxx Muller-5 xxxx x xxxx xxxxxx xxxxxxxxx xxxxx (xxxxxxxxxxx xxxxxxx X-chromozómu). Xxxxxx jsou xxxxxxxx xx čerstvé xxxxxxxx xxxxxx xxxxx xxx xx xxx xxx, xxx xxx pokryt xxxx xxxxxxx xxxxxx xxxxxxxxxxx xxxxx. X xxxxxxx xxxxxx samic xx xxxxxxxx xxxxxxx xxxxx xxxxxxxxxxxxxx x xxxxxxx xxxxxxxxx látky x době xxxxxxxx xx xxxxx spermie, xx xxxxxxxxxx ve xxxxxxxx xxxx xxxxxxx xxxxxx, xxxxx xxxxxxxxxx, xxxxxxxxxxxx a spermatogonie.
Heterozygotní X1 samice narozené x tohoto xxxxxxx xxxx xxxx xxxxxxx xxxxxxxxxxxx (xx. xxxxx xxxxxx/xxxxxxxx) se svými xxxxxx. X F2 xxxxxxxx xx x xxxxx kultuře xxxxxxxxxxxxx xxxxxxx samců divokého xxxx. Jestliže v xxxxxxx xxxxxxxx X1 xxxxxx nesoucí xxxxxxx xxxxxx v xxxxxxxxxxx X-xxxxxxxxxx (xxxxxx xxxxxxxx xxxxx xxxxx x xxxxxxxxxx xxxxxxxxxxx), xxxxx xxxxxx samic se xxxxxxx xxxxxxxxx jsou xxxx xxxxxxxxx, xxx xx xxxxxxxx, xxx xxxxxxxx se xxxxxxx x xxxxxxx xxxxxxxxxx.
2 XXXXX
Xxxxxxx xxxxx xx xxxxxxxx do xxxxxxx. Xxxxx xx xxxxx xxxxxxxxxxx X-xxxxxxxxxx, počet xxxxxxxxxxx samců a xxxxx xxxxxxxxxx s xxxxxxx xxxxxx xxx xxxxxx koncentraci, xxx xxxxx xxxxxx xxxxxxx x xxx xxxxxxx xxxxxxxxxxx samce. Zaznamenává xx xxxxx xxxxxxxx xxxxxxx xxxxxxxxx pro xxxxxxx samce. Xxxxxxxx xx xxxx xxxxxxxx x nezávislém xxxxxxxxxxx.
Xxxxx xx xxxxxxxx xxxxxxx xxxxxxxxxxxx metodou. Xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxx x jednom xxxxx xx být xxxxx v xxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxxxxx způsobem.
3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX X ZÁVĚREČNÁ XXXXXX
X xxxxxxx s příslušnými xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx a o xxxxxxx xxxxxx xx xxxxx xxxx xxxxxxxx.
Xxxxxx x xxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxx x:
- xxxxxxxxx xxxxxxx, xxxx kmenech Xxxxxxxxxx, xxxx, počtu xxxxxxxxxxx xxxxx, xxxxx xxxxxxxxxx xxxxx, xxxxx xxxxxxxxx X2 xxxxxx, xxxxx X2 xxxxxx xxx xxxxxxx, xxxxx xxxxxxxxxx xxxxxxxxx letální xxxxxx xxx xxxxx xxxxxxx xxxxxxxxxxx xxxxx,
- kritériích xxx xxxxxxxx xxxxxxxxxxx xxxxxx,
- podmínkách xxxxx: xxxxxxxx xxxxx xxxxxxxxxxx x xxxxxx odběru xxxxxx, výše xxxxx, xxxxx o toxicitě, xxxxxxxxx (x xxxxxxxxxxxxx) x xxxxxxxxx kontroly,
- xxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx,
- xxxxxx xxxxxxxx/xxxxxx, xx-xx to xxxxx,
- xxxxxxxxx xxxxx,
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.21 XXXX XXXXXXXXXXXX SAVČÍCH XXXXX - XX XXXXX
1 XXXXXX xx x xxxxxxx x xxxxxx Xxxxxxxxxx společenství.
1)1.1 Xxxxxxx xxxxxx
Xxxxx xxxxx xxx použít xxx xxxxxxx fenotypických xxxx xx xxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxx spojených x maligní xxxxxxxxxxxx xx xxxx. Xxxxxxxxxx xx xxxxxxxxx xxxxx X3X14X1/2 , 3T3, XXX, Fischerových xxxxxxx x xxxx se xxxxx x změny xxxxxxx xxxxxxxxxx, xxxxxx xxxxxxx nebo změny x xxxxxxxx x xxxxxxxxxxxx agaru. Xxxx xx xxxxxxxxx systémy xxxxxxxxxx ostatní fyziologické xx xxxxxxxxxxxx změny x xxxxxxx po xxxxxxxx xxxxxxxxxxxxx xxxxxx. Xxxxx xxxxxxxx xx xxxxx testu není xxxxxxx karcinogenity. Xxxxxxx xxxxxxx jsou xxxxxxx xxxxxxx xxxxxxxxx. Xxxxxxxxxxxx xxxx být xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxx xx xxxxxxxxx xxxxxxxx kolonie (cloning xxxxxxxxxx) xxxx xxxxxxxxxx xxxxxxxxx xxxxx xxxxxxx. Xxx xxxxxxxxx xxxxxxxxxxxx xx xxxxxxx xx xxxxxxxxxxx, xx xxxxxxxx xxxxxxxxx látce xxxx xxxxxxxxxxxxx xxxxxxxxxx, xxx xxxxxx ji xxxxx xxxxxx k xxxxxx xxxxxxxxx xxxxxxxxxxxx xx xxxxx xxxxxxxxxxxxx, protože x některých xxxxx xxxxx k xxxxxxxxxxx xxxxxxxx xxxx k xxxxxxxxxx.
1.2 Popis xxxxxx
1.2.1 Xxxxxxxx
1.2.1.1 Buňky
Existuje xxxx xxxxxxxxx xxxxx x xxxxxxxxxxx použitelných x xxxxx transformace. Experimentátor xxxx xxxxxxxx, xx xxxxx xxxxxxx x xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xx expozici xxxxxx xxxxxxxxxxxx x xx xxxx xxxxxxxxx xxxxxxxxxx xx xxxxxx x xx je xxxxxxxxxxxxx xxxx oprávněnost a xxxxxxxxxxxx.
1.2.1.2 Xxxxxx
Xxxxxxx xxxxx x experimentální xxxxxxxx xxxx xxx vhodné xxx xxxxxxx xxxx xxxxxxxxxxxx.
1.2.1.3 Xxxxxxxxx xxxxx
Xxxxxxxxx xxxxx xx rozpouštějí xxxx suspendují x xxxxxxxxxxx xxxxx xxxx xx vhodném xxxxxxxxxxxx xxxx ovlivněním xxxxx. Xxxxxxx xxxxxxxxxxx xxxxxxxxxxxx x xxxxxxx nesmí xxxxxxxx životnost xxxxx, xxxxxxxx rychlost nebo xxxxxx transformace.
1.2.1.4 Xxxxxxxxxxx xxxxxxxx
Xxxxx xxxx xxxxxxxxxx xxxxxxxxx látce x xxxxxxxxxxx a xxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxx systému. Xxxxxxxxxxxx xxxxx xxx xxxxxxx xxxxx x vlastní xxxxxxxxxxxx xxxxxxxxx, jestliže xxxx vlastnosti xxxx xxxxxx pro xxxxxxxxx xxxxx.
1.2.2 Experimentální xxxxxxxx
1.2.2.1 Xxxxxxxxx a xxxxxxxxx xxxxxxxx
Xx xxxxxxx experimentu xxxx být xxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxx látek xxxxx xxxxxxxxxx x vyžadujících xxxxxxxxxxxx xxxxxxxx. Xxxx xxx xxxxxxxx xxxx xxxxxxxxx kontroly (x xxxxxxxxxxxxx).
Xxxxxxxx látek xxx xxxxxxxxx xxxxxxxx:
- přímo xxxxxxxx látky: xxxxxxxxxxxxxxxxx, ß-xxxxxxxxxxxx,
- látky xxxxxxxxxx xxxxxxxxxxxx xxxxxxxx: 2-acetylaminofluoren, 4-xxxxxxxxxxxxxxx-xxxxxx, 7,12-dimetylbenzantracen.
Je možné xxxxxxx další xxxxxxxxx xxxxxxxx xx xxxxxx xxxxxxxx xxxxxxx, jako xx xxxxxxxxx xxxxx.
1.2.2.2 Xxxxxxxxxxx
Xxxxxxx xx xxxxxxx 3 xxxxx. Tyto xxxxxxxxxxx xxxx vyvolávat xxxxxxx xxxxx závislý xx xxxxxxxxxxx, xxxxxxxx xxxxxxxxxxx způsobují nízkou xxxxxx přežívání buněk, x nejnižší xxxxxxxxxxx xx xxxxxxxxx xxxxx xxxxxxxxx xxxxxx jako x xxxxxxxxx kontrole. Xx xxxx xxxxxxxxx xxxxxxxxxxx látky je xxxxx testovat až xx xxxxxxx xxxxxx xxxxxxxxxxxx xx xxxxxxx xxxxxxxx postupů. Xxxxxxxx xxxxxxx koncentrace xx xxxx xxxxxxxxx xxxxxxxxx xxxxx xx určuje xxxxxxxxxxxx.
1.2.3 Xxxxx xxxxxxx
Xxxxx xxxx být xxxxxxxxxx xxxxxxxxxxx xxxx závislou xx xxxxxxxx testovacím xxxxxxx. Xx může xxxxxxxxx x opakovanou xxxxxxxx xxxxxxxxx látce xxxxxxxx s výměnou xxxxx (ev. výměnou xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx), xxxxxxxx se xxxxx x prolongovanou xxxxxxxx. Xxxxx bez xxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx musí xxx xxxxxxxxxx testované látce x xxxxxxxxxxx i xxxxxxxxxxxxx vhodného metabolického xxxxxxxxxxx xxxxxxx. Na xxxxx expozice xx x xxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx látka x xxxxxxxxx xxxxxxx xxxx xx xxxxxxxx xxxxxxxx pro xxxxxxxxxxxx. Xxx xx zaznamenáván xxxxxx xxxxxxxxxxxx. Xxxxxxx xxxxxxxx xxxx xxx xxxxxxx x xxxxxxxxxxx xxxxxxxxxxxxx.
2 XXXXX
Xxxxx xxxx xxx xxxxxxx x xxxxxxx. Xx vhodné xxxxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxxxxxx xxxx xxxxx xxxxxxxxxxxx xx počet xxxxxxxxxxxxx xxxxx. Xxxx xx třeba xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx metodami.
3 XXXXXXX POKUSU, XXXXXXXX XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx s xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx zpracován xxxxxxx xxxxxx x x xxxxxxx xxxxxx xx xxxxx vést xxxxxxxx.
Xxxxxx o xxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxx x:
- xxxxxxxxx xxxxxxx, metodách použitých x udržování kultury, xxxxx kultur,
- kultivačních xxxxxxxxxx: xxxxxxxxxxx xxxxxxxxx xxxxx, xxxx xxxxxxxx, xxxxxxxxxxxx, kultivačních xxxxxxxx, xxxxx a xxxxxxxxx xxxxxxxx, xxxxxxxxxxxx xxxxxxxxxx xxxxxxx, pozitivních x xxxxxxxxxxx kontrolách, xxxxxxx xxxxx xxxxx xxxxxxxx, xxxxxxxxxxx sledovaného fenotypu, xxxxxxx xxxxxxxxxxxx systému (xx-xx xx xxxxxx), xxxxxxxxxx výběru xxxxxxxxxxx,
- xxxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxxxxxxxxx buněk,
- xxxxxxxxxxxx xxxxxxxxxxx.
Xxxxxxx výsledků.
Závěry.
B.22 XXXXXXXXXX XXXXXXX TEST X XXXXXXXX
1 METODA xx v souladu x právem Evropských xxxxxxxxxxxx.
1)1.1 Princip xxxxxx
Xxxxxxxxxx xxxxxxxx způsobuje xxxxxxxxxxx xxxx fetální xxxx. Xxxxxxx xxxxxxxxxxxx letálních xxxxxx po xxxxxxxx xxxxxxxx látce xxxxxxxx, xx tato látka xxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxxxx zvířecího xxxxx. Xxxxxx xx xxxxxxx, xx xxxxxxxxxx xxxxxxx xxxxxx jsou způsobeny xxxxxxxxxx xxxxxxxxxx (xxxxxxxxxxxx x xxxxxxxxx abnormality). Xxxx embrya xxxxxxxxxx xxxxxx může xxx xxxx výsledkem xxxxxxxxx xxxxxx.
Xxxxx jsou xxxxxxxxxx xxxxxxxxx xxxxx x xxxxxx s neovlivněnými, xxxxxxxxxx xxxxxxxx. Xxxxx xxxxxx xxxxxxxxxxx xxxxx xxxxx být testována xxxxxxxx xxxxxxxx xx xxxx jdoucích xxxxxxxxx xxxxxx. Xxxxxxx xxxxxxx xxxxxxxxxx xx xxxxxxx x xxxxxxxxxx xxxxxxx xxx počet xxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxx vyjadřuje xxxxxxxxxxxxxxx xxxxxx. Preimplantační xxxxxx xx xxxxxxx na xxxxxxx xxxxx xxxxxxx xxxxxxx xxxx porovnáním xxxxx xxxxxxxxxx xx xxxxxx v xxxxxxxxxx x kontrolní xxxxxxx. Xxxxxxx dominantní xxxxxxxx xx xxxxxx xxx- x xxxxxxxxxxxxxxxxx xxxxx. Xxxxxxx celkové xxxxxxxxxx xxxxxxxx xx xxxxxxx xx xxxxxxxx živých xxxxxxxxxx xx samici x xxxxxxxxxx xxxxxxx x xxxxx xxxxxxxxxxx xx samici v xxxxxxxxx xxxxxxx. Xxxxxxx xxxxx xxxxxxxxxx v xxxxxxxx xxxxxxxxx xxxx xxx způsobeno xxxxxxx xxxxx (xx. xxxxxxxxxxxx x/xxxx spermatogonií).
1.2 Popis xxxxxx
1.2.1 Xxxxxxxx
Xxxxxxxxxx látku xxxxxxxxx, xxxx suspendovat xx xxxxxxxxxxxxx xxxxxxx. Xxxxx xxxxxxxxxxx ve xxxx se xxxx, xxxx xxxxxxxxxx ve xxxxxxx xxxxxxxxxxxx. Xxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxx x xxxxxxxxxx xxxxxx xxx vyvolávat xxxxxxx xxxxxx. Xxxx xxxxxxxx xx xxxxx xxxxxxxxxxx xxxxxxx naředěnou xxxxxxxxxx xxxxx.
1.2.2 Experimentální podmínky
1.2.2.1 Xxxxxx xxxxxxxx
Xxxxxxxxx xxxxx xx obvykle xxxxxx xxxxx xxxxxx. Xx xxxxxxx toxikologických informací xx xxxxx podávat xxxxx xxxxxxxxx. Obvyklý xxxxxx aplikace xx xxxxxx xxxxxx xxxx xxxxxxxxxxxxxxxxx injekce. Xxxxx xxx xxxxxx i xxxx způsoby xxxxxxxx.
1.2.2.2 Xxxxxxxxxxxxxx zvířata
Pokusná xxxxxxx xxxx xxxxxxx x xxxxxxx xx xxxx, xxxxxxx a xxxxx x souladu s xxxxxxxxxxx
§15 zvláštního xxxxxxxx xxxxxxxx
10) x xxxxxxxx xxx, xxx xxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx zvířat. Xxxx xxxxxxxx stanoví
§10 xxxxxxxxxx právního xxxxxxxx.
10) Xxxxxx, xxxxxxxx xxxxxxx xxxxxxx jsou náhodně xxxxxxxxx na xxxxxxxxxx x kontrolní xxxxxxx.
1.2.2.3 Xxxxx a pohlaví
Je xxxxx xxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxx samců x xxxxxxx na xxxxxxxxx xxxxxxxxxxx hodnocené xxxxxxxxxx xxxxxxxxxxxxxxx. Počet xx řídí xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx x silou xxxxxxxxxxxxx xxxxx. X xxxxxxxx xxxxxxx xx na xxxxxxx xxxx takový xxxxx xxxxx, xxx xx xxxxxxx 30 - 50 březích xxxxx xx xxxxxxxxxxx xxxxxxxx.
1.2.2.4 Xxxxxxxxx a xxxxxxxxx xxxxxxxx
Xxxxxxxxx x xxxxxxxxx (s xxxxxxxxxxxxx) xxxxxxxx musí xxx xxxxxxxx xx xxxxxxx xxxxxxxxxxx. Xxxxxxxx xxxx xx xxxxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx kontrol z xxxxxxxxx xxxxxxxxxxx, mohou xxx xxxxxxx. Xxxxx xxx xxxxxxxxx kontroly xxxx být xxxxxxx xx vhodných, xxxxxxx xxxxxxx, aby xxxx xxxxxxxxx citlivost testu (xxxx. XXX, intraperitoneálně, 10 xx.xx-1).
1.2.2.5 Xxxxxxxxx
Xxxxxxxxxx xx xxxxxxxxx 3 xxxxxxx xxxxxxx. Xxxxxxxx xxxxx xx vyvolávat xxxxxx xxxxxxxx, xxxx xxxxxxx xxxxxxxxx u xxxxxxxxxxxx xxxxxx. V xxxxxxxxx případech je xxxxxxxxxxx jedna xxxxxx xxxxx.
1.2.2.6 Limitní xxxx
Xxxxxxxxx xxxxx se podávají x xxxxx xxxxx 5 x.xx-1 xxxx x dávce 1 x.xx-1.xxx-1 při opakované xxxxxxxx.
1.2.3 Popis xxxxxxx
Xxxxxxxx xxxxxxx xxxxxxx. Xxxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxxx. Xxxx xxxx xxx xxxxxxx jiné xxxxxx.
Xxxxx samec je xxxxxxxxx křížen x xxxxxx xxxx dvěmi xxxxxxxxxxxxx, intaktními samičkami xx xxxxxxxx intervalech xx xxxxxxxx látky. Xxxxxxx musí xxx x xxxxx xxxxxxx xx xxxx xxxxxx xxxxxxx xxxxx xxxx, xxxx xxxxx xx xxxxxxxxx xxxxxxx xx xxxxxx, xx xxxxxxxxx xxxxx.
Xxxxx xxxxxx xx xxxxxxxx xx xxx xxxxxxxxx expozice x xxxx xxxxxxxxx xxxxxxx xxxxxx zárodečných xxxxx xxxxxxxxxxx po xxxxxxxx.
Xxxxxx xxxx utraceny xxxxxxxxxx xxxxxxxxx nebo xx xxxxxxx xxxxxxxxx xx xxxxx polovině xxxxxxxx x xxxxx dělohy xx xxxxxxxx x xxxxxx počtu mrtvých x xxxxxx xxxxxxxxxx. Xxxxxxxxx mohou xxx xxxxxxxxx k xxxxxx xxxxx xxxxxxx tělísek.
2 XXXXX
Xxxxx o xxxxx xxxxx, počtu xxxxxxx xxxxx x počtu xxxxxxxxxxxx samic jsou xxxxxxx x xxxxxxxxx. Xxxxxxxx každého páření xxxxxx identifikace každého xxxxx x xxxxxx xxxx xxxxxxx xxxxxxxxxx. Xxxxx xxxxxx xxxx xxx xxxxxx x xxxxx xxxxxx, x xxxxx podané xxxxx, x xxxxx živých x xxxxxxx xxxxxxxxxx.
Xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx xx založeno xx xxxxxxxx xxxxx xxxxxx xxxxxxxxxx xx xxxxxx x exponované xxxxxxx x počtem xxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxx. Xxxxx xxxxxxx ku xxxxx xxxxxxxxxxx x xxxxxxxxxx xxxxxxx xx stejnému xxxxxx x xxxxxxxxx xxxxxxx po xxxxxxx xxxxxxxx o postimplantačních xxxxxxxx
X xxxxxxx xxxx xxx xxxxx xxxxxxxx xxxxx x xxxxxx xxxxxxxx. Odhadují-li xx x preimplantační ztráty, xxxxxx xx. Xx xxxxx xxx xxxxxxxxxx xxxx rozdíl mezi xxxxxx corpora lutea x xxxxxx implantací xxxx jako xxxxxxx xxxxxxxxxx xxxxx implantací xx xxxxxx xx xxxxxxxx x kontrolou.
Údaje xxxx xxxxxxxxxxx vhodnými xxxxxxxxxxxxx metodami.
3 XXXXXXX XXXXXX, PROTOKOL XXXXXX X ZÁVĚREČNÁ XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx zpracován projekt xxxxxx x x xxxxxxx pokusu xx xxxxx xxxx protokol.
Zpráva x xxxxxxx xxxxxx xxxxxxxx xxxxxxxxx o:
- xxxxx, kmeni, věku x xxxxxxxxx zvířat, xxxxx xxxxxx xx xxxxxxx xxxxxxx v xxxxxxxxxxxx a xxxxxxxxxxx xxxxxxxxx,
- xxxxxxxxx látce, xxxxxxxxxxxx, dávkových hladinách x xxxxxxxx xxxxxx xxxxxx, negativních a xxxxxxxxxxx xxxxxxxxxx, xxxxxxx x xxxxxxxx,
- xxxxxxx xxxxxx x schématu xxxxxxxx,
- xxxxxxxx páření,
- xxxxxxxx x xxxxxxx xxxxxx,
- době usmrcení,
- xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx efektů,
- xxxxxx xxxxx/xxxxxxx,
- xxxxxxxxxxx xxxxxxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.23 XXXXXXX XXXXXXXXXXXXXX XXXXXXX X XXXXXXX SPERMATOGONIÍCH
1 XXXXXX xx v souladu x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
5)1.1 Úvod
Účelem xxxxx xx xx xxxx xxxxxxxxxxxxx xxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx aberace x savčích xxxxxxxxxxxxxxx.
5) Xxxxxxxxxxxx xxxxxxx xxxx xxxxxxx xxxxx: xxxxxxxxxxxx x xxxxxxxxxxxx. Xxxxxxx xxxxxxxx chemickými xxxxxxxx xxxx většinou xxxxxxxxxxxx, xxxxx k xxxxxxxx xxxxxxxxxxxxxx xxxx xxxxxxx xxxxxx. Xxxx xxxxxx xxxx xxxxxx k xxxxxxx numerických xxxxxxx x xxxxx se x xxxxxx účelu xxxxxxxxx. Xxxxxxxxxxxx xxxxxx x xxxxxxxx jevy xxxx x člověka xxxxxxxx xxxx genetických xxxxxx.
Xxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxxxx aberace x xxxxxxxxxxxxxxx, a xxxxx se xxxxxxxxxxx, xx dokáže xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxxxx xxxxxxx.
X xxxxx xx obvykle xxxxxxxxx xxxxxxxx. Xxxxx xxxxxxxxxxxxxx xxxxxx in xxxx xx xxxxxxxx xxxxxxxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxxxxx. Tato xxxxxx xxxxxxxxx xxxx xxxxxx buňky.
Aby xx xx xxxxxxxxxxxxxxx zjistily xxxxxxx xxxxxxxxxxxxxx xxxx, xx xxxxx xxxxxxxxxx xxxxx xxxxxx xx xxxxxxxx xxxxxxxxx xxxxx, xxxxx xxx se xxxxxxxxx xxxxxx v xxxxxxxxxxxx buněčném xxxxxx. Xxxxx xxxxxxxxx z xxxxxxxxxxx spermatogonií lze xxxxxx xxxxxxxx meiotických xxxxxxxxxx, kde se xxxxxxxx xxxxxxx xxxxxxxxxxxxxx xxxx x diakinéze 1, když xx xxxxxxxxx xxxxx mění xx spermatocyty.
Tento xxxx xx vivo je xxxxx xx xxxxxxxxxx, xxx xxxx xxxxxxxx xxxxxxx x xxxxxxxxxxx xxxxxxx xxxx xxxxxxx x buňkách zárodečných. Xxxxxx má test xxxxxx xxxx pro xxxxxxxxx xxxxxx xxxxxxxxxx xxx, xx umožňuje xxxxxxxxx xxxxxxx metabolismu xx xxxx, farmakokinetiky x xxxxxxxxxxx xxxxxxx XXX.
X xxxxxxx je xxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxx. Xxxxxxxx xxxxxxx xxxx představují xxxxxx reakcí xxxxxxxxxxx xxxxxxxx spermatogonií, kde xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxxx. Xxxxx xxxxxx xxxxxx xx xxxxxxx pak xxxxx xxxxxxxx xxxxxxxxxxxxx xxxxx, xxx xxxxxxxx xxx xxxxxxxxxx krevním xxxxxx xxxxx xxxxxxxxxx x xxxxxxxxxxxx bariéře Xxxxxxxxx buněk a xxxxxx-xxxxxxxxxxxx xxxxxxx.
Xxxxxxxx-xx xxxxxxx xxxx, že se xxxxxxxxx xxxxx xxxx xxxx reaktivní xxxxxxxxx xx cílové xxxxx xxxxxxxxx, xxxx tato xxxxx xxx xxxx xxxxxx.
1.2 Xxxxxxxx
Xxxxxxx chromatidového xxxx: xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx, xxxxx xx xxxxxxxxx xxxx xxxx xxxxx, xxxxxxxx xxxx xxxxxxxxx, xxxx zlom x opětovné xxxxxxx xxxx xxxxxxxxxxxx.
Xxxxxxx xxxxxxxxxxxxxx xxxx: xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx xxxx xxxxxxxxxx jako xxxx a xxxxxxxx xxxxxxx obou chromatid xx xxxxxxx xxxxx (xxxxxxxx xxxx xxxxxxx xxxx xxxxxxxxxxx chromozóm, xxxxxxxxxx xxxxxxxxx-xxxx)
Xxxx chromatidy: xxxx xxxx xxx xxxxxxxx xxxxxxxx kontinuity xxxxx nebo xxxx xxxxxxxxx za předpokladu, xx vzniklá xxxxxx xx struktuře xxxxxxxxxx xx větší, než xx xxxxx xxxxxxxxx xxxxxxxxxx. Xxxx xxx x xxxxxxxxx, xxxxxxx (xxxxxxxx) fragment v xxxxx xxxxx xx xxxxxxxxxxx (xxxx mimo xxx chromatidy), případně xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxx je xxxxxx x xxxxxxxx deletce.
Gap: xxxxxxxxxxxx xxxx xxxxx xxx xxxxx xxxxx xxxxxxxxxx x x xxxxxxxxxx xxxxxxxxx xxxxxxxxx.
Xxxxxxxxx xxxxxxx: xxxxx xxxxx xxxxxxxxxx oproti normálnímu xxxxx xxxxxxxxxxxxxxxxxx xxx xxxxxxx xxxxx.
Xxxxxxxxxxx: xxxxxxx xxxxxxxxxxx počtu xxxxxxxxxx (x) jiný než xxxxxxxxx počet (tedy 3x, 4x xxx.).
Xxxxxxxxxxxx xxxxxxx: změna xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx xx xxxxxx xxxxxxxx, xxxxxxxxxx xxxx xxxxxx x xxxxxxxxx, a xxxxxxxxxxxxxxxxxx xxxx xxxxxxxxxxxxxxxxxx xxxxxx.
1.3 Princip xxxxxx
Xxxxxxx xx vhodným xxxxxxxx xxxxxxxx xxxxxxxxx látce x ve xxxxxxx xxxx po xxxxxxxx xx xxxxxx. Před xxxxxxxxx xx xx xx působí xxxxxx xxxxxxxxxxx metafázi (xxxxxxxxx xxxxxxxxxxx xxxx Xxxxxxxxxx®. Xx xxxxxxxxxxx buněk xx xxx připraví xxxxxxxxx a xx xxxxxxxx se x xxxxxxxxxx analyzují xxxxxxxxxxxx xxxxxxx.
1.4 Xxxxx xxxxxx
1.4.1 Xxxxxxxx
1.4.1.1 Výběr živočišného xxxxx
Xxxxx xx používají xxxxx xxxxxxxx křečků x xxxx, xxx xxxxx použít samce xxxxxxxxxxx jiného xxxxxxxx xxxxxxx druhu. Xxxxxxxxx xx xxxxx xxxxxxxxxxx xxxxx mladých zdravých xxxxxxxxx xxxxxxx. Xxxxxxxxxx xxxxxxx xx xxx xxxxxxxx xxxxxx xxxx xxx xxxxxxxxx a x xxxxxxx xxxxxxx xxxxxx xxxxxxxxxx ± 20 % průměrné xxxxxxxxx.
1.4.1.2 Podmínky chovu
Všeobecné xxxxxxxx xxxxx xxxx xxxxxxx xx Xxxxxxxxxx xxxxx.
Xxxxxxx xx měla xxx 50 - 60 %.
1.4.1.3 Příprava xxxxxx
Xxxxxxx xxxxxxx jsou xxxxxxx x xxxxxxx xx druh, xxxxxxx x xxxxx x xxxxxxx s ustanovením
§15 zvláštního xxxxxxxx xxxxxxxx
10) a označena xxx, xxx xxxx xxxxx identifikace xxxxxxxxxxxx xxxxxx. Dobu xxxxxxxx xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10) Zdraví xxxxx dospělí xxxxxxx xx xxxxxxx rozdělí xx kontrolní x xxxxxxxxxxxxxx xxxxxxx.
1.4.1.4 Xxxxxxxx xxxxx
Xx-xx testovaná xxxxx x pevném xxxxx x xx-xx xx xxxxx, xxxxx xx xxxx podáním zvířatům xxxxxxxx nebo se xxxxxxxx xxxx xxxxxxxx xx vhodném rozpouštědle xxxx vehikulu. Kapalné xxxxxxxxx xxxxx xx xxxxx podávat xxxxx xxxx xx před xxxxxxxxx ředí. Xx xxxxx používat čerstvé xxxxxxxxx, ledaže údaje x xxxxxxxx (xxxxxxxxx) xxxxxxxxx, xx xxxxxxxxxx xx xxxxxxxxx.
1.4.2 Podmínky xxxxx
1.4.2.1 Rozpouštědlo/vehikulum
Rozpouštědlo/vehikulum v xxxxxxxxxxx xxxxxxx nesmí xxxxxxxxx toxické účinky x xxxxx x xxxxxxxxxx xxxxxx chemicky xxxxxxxx. Xxxxxxx-xx se xxxxxxxx xxxxx rozpouštědlo, xxxx být xxxx xxxxxxx podpořeno údaji x kompatibilitě x xxxxxxxxxx xxxxxx. Doporučuje xx, xxx xxxx xx xxxxxx xxxxx xxxxxxx xxxxx xxxxxxxxxxxx/ xxxxxxxxx.
1.4.2.2 Xxxxxxxx
Xx xxxxxxx xxxxx xx třeba xxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxx (xxxxxxxxxxxx/xxxxxxxxx) xxxxxxxx. Xx xxxxx xxxxxxxx se zvířaty xx xxxxx xxxxxxxxx xxxxxx.
Xxxxxxxxx xxxxxxxx xx xxxx ve xxxxxxxxxxxxxxx xxxxxxxxx chromozómové aberace xx vivo xxx xxxxxxx, kdy xxx xxxxxxxx xxxxxx detekovatelné xxxxxxx xxx spontánní xxxxxx.
Xxxxx xxx xxxxxxxxx xxxxxxxx se volí xxx, xxx xxxx xxxxxx patrné, ale xxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx zakódovaného xxxxxxxxx. Xxxxxxxxx xxxxxxxx je xxxxx podávat odlišným xxxxxxxx než xxxxxxxxxx xxxxx x xxxxxx xxxxxxxx x jednom xxxxxxx intervalu. Xxx xx to možné, xx třeba xxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxx chemické skupiny, xxxx je xxxxxxxxx xxxxx. Příklady xxxxx xxxxxxxx xxx pozitivní xxxxxxxx:
|
|
|
|
|
xxxxxxxxxxxxx
|
|
|
|
xxxxxxxxxx xxxxxxxxxxxxxx
|
|
&xxxx;
|
|
xxxxxxxxxxxxxx
|
|
|
|
xxxxxxxxx X
|
|
|
|
xxxxxxxxx xxxxxxx
|
|
|
|
xxxxxxxxxxxxxxxxx
|
|
|
Xxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxx xxxx experimentální xxxxxxx xxxx xx xxx xxxxxxxx xx xxxxx časových intervalů xxxxxxxxxx, xxxxx xxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxxxxxx údaje o xxxxxxxxx xxxxx s xxxxxxxxx x o xxxxxxxxxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxx. Xxxxxx xx xxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxx, xxxxxx xxxxxxxx xxxxxxxxxx nebo xxxxxxxxxxx xxxxx xxxxxxxxxxx, xx xxxxxxx xxxxxxxxxxxx xxxx vehikulum xxxxxxxxxx xxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxxx.
1.5 Xxxxxx
1.5.1 Xxxxx a xxxxxxx xxxxxx
X xxxxx zkušební x xxxxxxxxx xxxxxxx xxxx být xxxxxxxxx xxx xxxxxxxxxxxxxxxx xxxxx.
1.5.2 Xxxxxxxxx schéma
Testovaná látka xx xxxxxx xxxxxxx xxxxxxxxxxx nebo xx xxxx dávkách. Xxxxx xx xxxxx o xxxxxxxx xxxxx, xxxx xx x usnadnění xxxxxxxx xxxxxxxx, xx. xx dvě xxxxx xx xxx xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxx xxxxx. Jiné xxxxxx xxxxxxxxx xxxx xxx xxxxxxx xxxxxxxxxx.
X xxxxxxx skupiny s xxxxxxxx xxxxxx xx xxxxxx xx xxxxxxxx xxxxx odebírají dvakrát. Xxxxxxx xxxxxxxxx látka xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxx dělení, provádí xx xxxxx dřívější x xxxxx pozdější xxxxx xxxxxx 24 x 48 xxxxx xx xxxxxxxx. X xxxxxxxxx xxxxx (xx. xxxx xxxxx xxxxxxxx) xx xxxxx vzorků xxxxxxx xx 24 xxxxxxxx xxxx xx 1,5xxxxxxx xxxxx xxxxxxxxx xxxxx po xxxxxxxx, xxxxxx je xxxx xxxxxxxxx xxxxxx xxxxxxxx xxx xxxxxxx účinku.
5)Kromě xxxx mohou xxx xxxxxxx jiné xxxxxx xxxxxxxxx xxxxxx xxxxxx. Xxxx. xxxxx-xx xx x látku xxxxxxxxxxx xxxxx xxxxxxxxxx během xxxxxx xxxx xxxxx x účinky xxxxxxxxxxx xx X-xxxx xxxxx, xxxx xxxxxxxxx dřívější xxxx xxxxxx vzorku.
5)Zda xx xxxxxx xxxxxx xxxxx xxxxxxx xxxxxxxxx, xx xxxxxxxx xxxxxx xx případu. Xxxxx xx xxxxxxx xxxxxxxx xxxxx opakovaně, usmrcují xx xxxxxxx xx 24 xxxxxxxx (1,5xxxxxxx xxxxxxxxx cyklu) xx xxxxxxxx xxxxxxxx. Xxxxxx xxx xxxxxxxx i x xxxxxxx intervalech, xxxxxxxx-xx se xx xx xxxxxx.
Xxxx xxxxxxxxx xx xxxxxxxx intraperitoneálně xxxxxxxx xxxxxx xxxxx Xxxxxxxxx® xxxx xxxxxxxxxx x xxxxxxxx xx x nich xx xxxxxxx intervalu xxxxxxxx xxxxxx. X myší xx xxxxx xxxxxxxx xxxxxx 3-5 hodin, x čínských xxxxxx xxxxxx 4-5 xxxxx.
1.5.3 Xxxxxxxxx
Xxxxxxx-xx se studie xx zjištění xxxxxxx xxxxxxxx, xxxxxxx xxxxxx x xxxxxxxxx xxxxx xxxxxx xxxxx, xx xxxxx xx xxxxxxxx x téže xxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxx, kmene x xxxxxxxxx xxxxxx, xxxx se xxxxxxx x xxxxxx studii.
5) Xxx zjištění xxxxxxxx xx užívají xxx xxxxx xxxxxx interval xxxxxx vzorků xxx xxxxx xxx, xxx xxxxxxxxx xxxxxxx xx xxxxxxxxx xxxxxxxx x xxxxxxxx nízké xxxx xxxxxx. Pro xxxxxxxx xxx odběru vzorků xx xxx xxxxx xxxxxx xxxxx xxxxxxxx xxxxx. Xx je xxxxxxxxxx jako dávka xxxxxxxxxxxx xxxxxx známky xxxxxxxx, že xxx xxxxxxx xxxxxxx xx xxxxxxx režimu xxxxxxxx xx xxxxxx xxxx xxxxxxx.
Xxxxx, jež x xxxxxxx netoxických xxxxxxx xxxxxxxx xxxxxxxxxxx biologickou xxxxxxxx, jako xxxx xxxxxxx xxxx xxxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxx x xxxxxx xxxxxxxx xxx xxxxxxxxx dávek x vyhodnocují xx xxxxxx od xxxxxxx. Xxxxxxxx dávka může xxx xxxx definována xxxx xxxxx, která xxxx x určitým xxxxxxx xxxxxxxx xx xxxxxxxxxxxxxxx (xxxx. xxxxxx xxxxxx xxxxx xxxxxxxxxxxxx x xxxxx x xxxxx meiotické xxxxxxxx; xxxxx xxxxxx xxxx xxx xxxxx xxx 50 %).
1.5.4 Xxxxxxx xxxx
Xxxxxxxx xxxx xxx xxxxx minimálně 2000 xx/xx hmotnosti x xxxxx xxxxx xxxx xx dvou dávkách xxxxxxxx x xxxxx xxx xxxxxxxxxx žádné xxxxxxxxxxxxx xxxxxxx xxxxxx x xxxxxxxx xx xx základě údajů x xxxxxxx s xxxxxxxx xxxxxxxxx strukturou xxxxxxxxx xxxxxxxxxxxx, nemusí xxx xxxxxxxxx celá xxxxxx za xxxxxxx xxx xxxxxxxxx xxxxxx. Xxxxx očekávané xxxxxxx xxxxxxxx xx xxxx xxxxxx v xxxxxxxx xxxxx xxxxx xxxxx.
1.5.5 Xxxxxxxx xxxxx
Xxxxxxxxx xxxxx xx xxxxxxx xxxxxxxx xxx' xxxxxxxxx xxxxxx, xxxx xxxxxxxxxxxxxxxxx xxxxxxx. X xxxxxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxxxxx x xxxx xxxxxxx xxxxxxxx. Xxxxxxxxx xxxxx xxxxxxxx, xxxxx xx xx xxxxxx nebo xxxxxxx xxxxxxxx xxxxxxx, xxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxx x xxxx překročit 2 xx/100 x hmotnosti; xxxxx xxxxx musí xxx xxxxxxxxxx. X xxxxxxxx xxxxxxxxxx nebo xxxxxxxx látek, xxx xxxxxxxx xxxxxxxx xxx xxxxxxx xxxxxxxxxxxxx horší xxxxxx, xx třeba xxxxxxx xxxxxxxxxxx xxxxx xxx, xxx xxxxx xxx xx všech xxxxxxxxx xxxxxxxx stejný x xxxxxxxxxxxxxx xx xxx objemová variabilita.
1.5.6 Xxxxxxxx xxxxxxxxxx
Xxxxxxxx xx xxxxxxxx xxxxxxx xx xxxxxxxx z xxxxxxx xxxx x xxxx xxxxxx xxxxxxx suspenze, xx xxxxxx xx xxxxxx xxxxxxxxxxxx roztokem x xxxxxx xx. Xxxxxxx xxxxxxxx xx xxxxxx xx xxxxxxxx xxxx x xxxxxx.
1.5.7 Xxxxxxx
X xxxxxxx xxxxxxx xx xxxxxxxxx minimálně 100 dobře xxxxxxxxxxxxxx xxxxxxxx (xx. xxxxxxxxx 500 xxxxxxxx x xxxxx xxxxxxx). Tento xxxxx se xx xxxxxx, je-li xxxxx xxxxxxxxxxxx xxxxxxx xxxxxx. Xxxxxxx xxxxxxxxxxxxx xxxxxxxxx (xxxxxx pozitivních x xxxxxxxxxxx xxxxxxx) se xxxx xxxxxxxx nezávisle xxxxxxxx. Jelikož fixační xxxxxxx často xxxxx x rozbití xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxx x xxxxxx xxxxxxxxxx, xxxx xxx x xxxxx xxxx xxxxx xxxxx xxxxxxxxx x xxxxxxxxxxx buňkách xxxxx xxxxx 2x ± 2.
2 XXXXX
2.1 Zpracování xxxxxxxx
Xxxxx z jednotlivých xxxxxx xx xxxxxxxx xx xxxxxxx. Experimentální xxxxxxxxx xx xxxxxxx. X xxxxxxx xxxxxxx xx vyhodnocuje počet xxxxx xx strukturálními xxxxxxxxxxxxxx xxxxxxxxx a xxxxx xxxxxxx xx xxxxx xxxxx. U xxxxxxxxxxxxxxxx x kontrolních xxxxxx xx xxxxxxxxxxx xxxxxxxxxx xxxx strukturálních xxxxxxxxxxxxxx xxxxxxx, jejich xxxxx a xxxxxxx. Xxxx xx zaznamenávají xxxxxx, uvádějí xx, xxx xxxxxxx xx xx xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx.
Xx-xx xxxxxxxxxxx xxxxxx i xxxxxx, xxxxxxx xx u xxxxx pokusných xxxxxx x xxxxxx x xxxxxxxxx kontroly xxxxxxx xxxx cytotoxicity xxxxx xxxxx spermatogonií x xxxxx a xxxxx xxxxxxxxx xxxxxxxx, x xx tak, xx xx z xxxxxxx xxxxxxx xxxxxxx 100 xxxxxxxx xx buněk. Xx-xx analyzována xxxxx xxxxxx, xxxxxxx se xxxxxxxxx xxxxx u xxxxxxxxx 1000 xxxxx x xxxxxxx xxxxxxx.
2.2 Xxxxxxxxxxx x xxxxxxxxxxxx xxxxxxxx
Xx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx se xxxxxxx xxxxxxx xxxxxxxx, xxxxxxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxxxxxx xxxxxxxxx, xxxx xxxxxxxx xxxxxx xxxxx xxxxx x aberacemi xx xxxxxxx xxxxxxxxx jednorázovou xxxxxx a x xxxxxx časovým xxxxxxxxxx xxxxxx xxxxxx. Nejprve xx xxxxx uvážit xxxxxxxxxxx xxxxxxxxxx xxxxxxxx. Xxx xxxxxxxxxxxxx xxxxxxxx xxxxx xx možno xxxxxx xxxxxxxxxxx metody;
5) xxxxxxxxxxx xxxxxxxxxx by xxxx xxxxxx být xxxxxxx xxxxxxxxx faktorem xxxxxxxxxxx výsledku. Xxxxxxxxxxxxx xxxxxxxx je xxxxx xxxxxxxx dalším testováním, xxxxxxx xx modifikovaných xxxxxxxxxxxxxxxx xxxxxxxx.
Xxxxxxxxx xxxxx, xxx xxxxxx xxxxxxx xxxxxxxx xxxxxxxxx výše xxxxxxx xxxxxxxx, xx x xxxxx xxxxxxx xxxxxxxx xx nemutagenní.
Ačkoliv xxxxxxx experimentů vykazuje xxxxx xxxxxxxxx, xxxx xxxxxxxxx xxxxxxxx, xx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx účinku xxxxxxxxx xxxxx. Xxxxxxxx xxxxx xxx xxxxxxx, nebo xxxxxxxxxxxx xxx xxxxxx xx xxxxx xxxxxxxxxxx xxxxxxxxxxx.
Xxxxxxxxx xxxxxxxx xxxxx xxxxxxx, xx testovaná xxxxx vyvolává v xxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx aberace. Negativní xxxxxxxx xxxxxxx, xx xx daných xxxxxxxxxxxxxxxx xxxxxxxx testovaná xxxxx x xxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxx.
Xx xxxxx xxxxxxxxxx, xxxx xx pravděpodobnost, že xxxxxxxxx xxxxx xxxx xxxx metabolity xxxxxxxx xxxxxx xxxxx.
3 XXXXXXX XXXXXX, PROTOKOL XXXXXX X ZÁVĚREČNÁ ZPRÁVA
V xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx x x xxxxxxx xxxxxx je xxxxx xxxx xxxxxxxx.
Xx xxxxxx x xxxxxxx xxxxxx xx třeba xxxxx tyto informace:
Rozpouštědlo/vehikulum
- xxxxxxxxxx xxxxx xxxxxxxx,
- xxxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx v xxxxxxxxxxxx/xxxxxxxx, xxxxx je xxxxx.
Xxxxxxx xxxxxxx.
- xxxxxxx xxxxxxxxx xxxx/xxxx,
- počet x věk xxxxxx,
- xxxxx, xxxxxx xxxxxxxx, xxxxxx xxxx.,
- hmotnost xxxxxxxxxxxx xxxxxx na xxxxxxx xxxxx, včetně xxxxxxxxxxxx xxxxxxx, xxxxxxx x směrodatných xxxxxxxx xxx xxxxxxxxxx xxxxxxx.
Xxxxxxxx xxxxxx:
- xxxxx xx xxxxxx pro xxxxxx xxxxxxx toxicity, byla-li xxxxxxxxx,
- xxxxxxxxxx xxxxx xxxxxxxxx dávek,
- zdůvodnění xxxxxxx xxxxxxxx xxxxx,
- xxxxxxxxxxx o přípravě xxxxxxxxx látky,
- xxxxxxxxxxx x podávání xxxxxxxxx xxxxx,
- xxxxxxxxxx xxxx xxxxxxxx xxxxxx,
- případný xxxxxx xxxxxxxxxxx látky x xxxxxxx/xxxxx xxxx (xxx) xx faktickou xxxxx (xx/xx hmotnosti/den),
- xxxxxxxxxxx o xxxxxxx xxxxxxx x xxxx,
- xxxxxxxx xxxxxx podávání xxxxxxxxx xxxxx x xxxxxx xxxxxx,
- xxxxxx xxxxxxxxxx xxxxxxxx,
- xxxxx xxxxxxxxx xxxxxxxx, xxxx xxxxxxxxxxx x xxxxx xxxxxxxx,
- xxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx,
- xxxxxxxx xxx xxxxxxxxx xxxxxxx,
- xxxxx xxxxxxxxxxxxx xxxxx xx xxxxx xxxxx,
- xxxxxxxx, xxxxx xx xxxxxx xxxxxxx xxxx xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxxxxxxx.
Xxxxxxxx:
- xxxxxx xxxxxxxx,
- xxxxxxxxx xxxxx,
- xxxxx xxxxx xxxxxxxxxxxxx x xxxxx x xxxxx xxxxxxxxx xxxxxxxx,
- xxx x xxxxx xxxxxxx xxx xxxxxxx jedince xxxxxx,
- xxxxxxx počet xxxxxxx v xxxx xxxxxxx,
- xxxxx xxxxx x xxxxxxxxx na xxxxx xxxxxxx,
- xxxxx xxxxx-xxxxxxx, xx-xx to xxxxx,
- xxxxxxxxxxx analýzy, xxxx-xx provedeny,
- xxxxx xx souběžných negativních xxxxxxx,
- xxxxxxxxxx xxxxx x xxxxxxxxxxx xxxxxxx xxxxxx xxxxxxx, xxxxxxx x směrodatných xxxxxxxx,
- xxxxx ze xxxxxxxxxx xxxxxxxxxxx xxxxxxx,
- xxxxxxxx xxxxxxxxxx změny xxxxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.24 SPOT XXXX X XXXX
1 XXXXXX xx x xxxxxxx x právem Evropských xxxxxxxxxxxx.
1)1.1 Xxxxxxx xxxxxx
Xx xx xx xxxx xxxx na xxxxxx, x kterých xxxx xxxxxxxxxx xx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx. Xxxxxxxx xxxxxxx x xxxxxx jsou melanoblasty x cílovými xxxx xx, xxxxx xxxxxxxxxx xxxxxxxxxx xxxxx. Xxxxxx xxxx xxxxxxxxxxxx xxx xxxx xxxx xxxxxxxxxxxxx xxxxx xxxxx. Xxxxxx, xxxx ztráty dominantních xxxxx x genech xxxxxxxxxxxx jsou xxxxxxxxx xxxxxxxxxx xxxxxxxxx x xxxxxxxxx buňkách vytvářejících xxxxxx (xxxxx) xxxxxxxxx xxxxx srsti xxxxxxxxxx xxxx. Xxxxx potomků x xxxxxx skvrnami, xxxxxxxx, je zaznamenán x jejich xxxxxxxxx xx xxxxxxxxxx x xxxxxxxxx x potomků x xxxxxxx. Xxxx xxxx test xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxxxxxx xxxxxxx.
1.2 Xxxxx xxxxxx
1.2.1 Xxxxxxxx
Xxxxxxxxx xxxxx jsou rozpuštěny xxxx suspendovány x xxxxxxxxxxx fyziologickém xxxxxxx. Xxxxx xxxxxxxxxxx ve xxxx jsou xxxxxxxxxx xxxx xxxxxxxxxxxx ve xxxxxxx xxxxxxxxxxxx. Xxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxx x xxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxx xxxxx. Používají xx xxxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx.
1.2.1.1 Xxxxxxxxxxxxxx xxxxxxx
Xxxx kmene X (xxxxxxxxx, a/a; xxxxxxxxxx, xxxx xxx, xxx x/xxx x: xxxxx, x/x; dilute, xxxxx xxx, x xx/x xx; xxxxxxx spotting, x/x) xxxx xxxxxxx xxx x xxxxxx XXX (xxxxxx, nonagouti, xxxxxxxxxx, xx a xx/xx x xx; xxxxxx xxxxx, In xx/xx fz; xxxxx xx/xx) xxxx x xxxxxx X57 XX (xxxxxxxxx, x/x).
Xxxxx xxx xxxxxxx x jiná xxxxxxx, xx xxxxxxxxxxx xx budou xxxxxxx xxxxxxxxx xxxxxxx. Např. xxxxxxx mezi kmenem XXXX (xxxxxxxxx, a/a; xxxxxx, x/x) x XXX (nonagouti, a/a; xxxxx, b/b; xxxxxx x/x).
Xxxxxxx xxxxxxx jsou xxxxxxx x ohledem xx xxxx, xxxxxxx x stáří v xxxxxxx x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x označena xxx, xxx byla xxxxx xxxxxxxxxxxx jednotlivých xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 zvláštního xxxxxxxx předpisu.
10)1.2.1.2 Počet x xxxxxxx xxxxxx
Xxxxxxx xx dostatečný xxxxx xxxxxxxxxx samic, aby xxx zajištěn dostatečný xxxxx xxxxxx potomků xxx každou použitou xxxxx. Vhodná xxxxxxxx xxxxxx je závislá xx xxxxx xxxxx xxxxxxxxxxxx x ovlivněných xxxx a u xxxxxxxxxxx myší. Xxxxxxxxx xxxxxxxx xxxx xxxxxxxxxxx xxxxx x xxxxxxx, xx bylo hodnoceno xxxxxxx 300 potomků xxxxx xxxxxxxxxxx xxxxxxxx xxxxxx.
1.2.1.3 Xxxxxxxxx x xxxxxxxxx kontroly
Musí být xxxxxxx xxxxxxxx ovlivněné xxxxx xxxxxxxxxxxxx (negativní xxxxxxxx). Xx xxxxxxx xxxxxxxxxx xxxxx mohou xxx použity xxxxxxxxx xxxxxxx x xxxx xxxxxxxxxx xx xxxxxxxxxxx, xx xxxx homogenní. Xxxxxxx xxxxx x xxxxxxxxxxx kontrol získané x xxxx xxxxxxxxxx xxx expozici látce xx známým xxxxxxxxxx xxxxxxx xxxxx xxx x tomto testu xxxxxxx, xxxxxxxx x xxxxxxxxx xxxxx xxxxxx xxxxxxxxxx xxxxxxxxxx.
1.2.1.4 Xxxxxx xxxxxxxx
Xxxxxxx se xxxxxxx xxxxxx xxxxxxxx xxxxxx xxxx xxxxxxxxxxxxxxxxx xxxxxxx xxxxx myši. Xx-xx xx vhodné, xx xxxxx xxxxxx xxxxxxxxx xxxx jiný xxxxxx xxxxxxxx.
1.2.1.5 Dávkování
Používají xx xxxxxxx dvě xxxxx, x nichž xxxxx xxxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxx. U xxxxxxxxxxx xxxxx se xxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx.
1.2.2 Xxxxx xxxxxxx
Xxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx pouze jednou 8., 9., nebo 10. den xxxxxxxx, xxxxxxx xx 1. xxx xxxxxxxx xx xxxxxxxx xxx zjištění xxxxxxxxx xxxxx. Xxxx xxx xxxxxxxxxx 7.25, 8.25 x 9.25 xxx po xxxxxxxx. Xxxxxxxxx xxxxxxxxx látkou xxx xxxxxxx xxxxx xxxxxx xxx.
Xxxxxxx
X xxxxxx xx xxxxxxx x xxxxxxxxxxxx xxxxx skvrn xxxx xxxxxx x xxxxxxx xxxxxx po xxxxxx. Xxxxxxxxx se xxx xxxxx xxxxx
(x) xxxx xxxxxx x xxxxxxx 5 xx xx xxxxxxx ventrální xxxxx, o kterých xx xxxxxxxxxxx, xx xxxxxxx xxxxxxx buněk (XXXX);
(x) xxxxx skvrny xxxx agouti se xxxxxxxxx v xxxxx xxxxxxxx žláz, xxxxxxxxx, xxxxx, xxxx, oblasti xxxxxx x xxxxxxxxx xxxx x předpokládá xx, xx xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxxxxxx (MDS);
(c) zbarvené x xxxx xxxxxx xxxxxxx xxxxxxxxxx v xxxxx jako výsledek xxxxxxxxxxx mutací (RS).
Všechny xxx xxxxxxx jsou xxxxxxxxxxxxx, ale xxxxx xxxxxxxx, RS, je xxxxxxxxx relevantní. Xxxxxx x xxxxxxxxx mezi XXX x RS xx xxxxx vyřešit xxxxxxxxxxx xxxxxx xx xxxxxxxxxxxxxx mikroskopu.
Zaznamenávají xx xxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxx.
2 XXXXX
Xxxxxxx xxxx xxxx xxxxxxx xxxx xxxxxxx xxxxx xxxxxxxxxxx xxxxxxx a xxxxx xxxxxx xxxxxxxx xxxxx nebo xxxx xxxxx vyvolaných xxxxxxxxxxx xxxxxxxx. Xxxxx získané x xxxxxxxxxxx x xxxxxxxxxxxx xxxxxx se xxxxxxxxxxx vhodnými xxxxxxxx. Xxxxx jsou xxxx xxxxxxx jako xxxxxxx xxxxxxx xx xxx.
3 XXXXXXX POKUSU, XXXXXXXX XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx s xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx pokusu x x xxxxxxx xxxxxx xx xxxxx vést xxxxxxxx.
Xxxxxx x průběhu xxxxxx xxxxxxxx informace x:
- kmeni xxxxxxxx xxx xxxxxxx,
- počtu xxxxxxxxxx samic x xxxxxxxxxxxxxx x x xxxxxxxxx xxxxxxx,
- průměrné xxxxxxxxx vrhu x xxxxxxxxxxxxxx a v xxxxxxxxx xxxxxxx při xxxxxx x při xxxxxxxxx,
- dávkových úrovních xxxxxxxxx látky,
- použitém xxxxxxxxxxxx,
- xx xxxxxx xxx xxxxxxxx xxxx xxxxxxxxx látka xxxxxxxxxx,
- x xxxxxxx podání xxxxxxxxx látky,
- xxxxxxxx xxxxx xxxxxxxxxxx xxxxxxx, x jejich počet x XXXX, MDS x XX x xxxxxxxxxxxxxx a xxxxxxxxx xxxxxxx,
- xxxxxxx morfologických xxxxxxxxxxxx,
- xxxxxx xxxxx/xxxxxxx x XX, xx-xx xx možné,
- statistickém xxxxxxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.25 XXXXXXXX XXXXXXXXXXX U XXXX
1 XXXXXX je x xxxxxxx s právem Xxxxxxxxxx společenství.
1)1.1 Xxxxxxx xxxxxx
Xxxx na xxxxxxxx xxxxxxxxxxx x myší xxxxxxxx strukturální x xxxxxxxxx xxxxxxxxxxxx xxxxx x savčích xxxxxxxxxxx xxxxxxx zachycené v xxxxx generaci xxxxxxx. Xxxxxxxxxx xxxxx xxxx xxxxxxxxx xxxxxxxxxxx x x samičích xxxxxxx xxxxx xxxxxx X-xxxxxxxxxx. Xxxxxxxx translokací a XX-xxxxxx vykazují xxxxxxxx xxxxxxxxx, xxxxx xx xxxxxxx xxx xxxxx X1 xxxxxxxxx xxx xxxxxxxxxxxxxx xxxxxxx. Xxxxx xxxxxxxxx je xxxxxxxxx xxxxxxxxx xxxx translokací (X-xxxxxxx x x-x xxx). Xxxxxxxxxxx xxxx xxxxxxxxxxx mikroskopicky v xxxxxxxxxxx xxxxxxx xxxxx xx spermatocytů ve xxxxxx xxxxxxxxx-xxxxxxxx X, xxxx X1 xxxxx xx xxxxxxx potomků X1 xxxxx. Xxxxxx XX jsou cytogeneticky xxxxxxxxxxxxxx xxxxxxxxxxx pouze 39 xxxxxxxxxx x xxxxxxxx z xxxxxx xxxxx.
1.2 Xxxxx xxxxxx
1.2.1 Xxxxxxxx
Xxxxxxxxx látky xxxx xxxxxxxxxx x isotonickém xxxxxxxxxxxxx xxxxxxx. Xxxxxxxx xxxx xxxxxxxxxxx, xxxx xxxxxxxxxx, xxxx suspendovány xx xxxxxxx xxxxxxxxxxxx. Xxxxxxxxx se čerstvě xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx. Xxxxxxxx xxxx xxxxxxx xxxxxxxxxxxx xxx xxxxxxxxx xxxxxxxxx xxxxx, xxxxx reagovat x xxxxxxxxxx látkou xxxx xxxxxxxxx xxxxxxx xxxxxx.
1.2.1.1 Xxxxxx xxxxxxxx
Xxxxxxxx xx xxxxxxx xxxxxx xxxxxx xxxx intraperitoneální xxxxxxx. Xxxxx xxx xxxxxxx x xxxx xxxxxx xxxxxxx xxxxxxxx.
1.2.1.2 Experimentální Xxxxxxx
Xxx xxxxxxxxx xxxxxxx x xxxxxxxxxxxx verifikaci xx xxxxxx xxxxxxx xx myších. Nepožaduje xx xxxxx xxxxxxxxxx xxxx. Xxxxxxxx xxxxxxxx xxxx xx xxxx xxx xxxxx xxx xxx a měla xx xxx relativně xxxxxxxxxx. Xxxxxxxxx se xxxxxx, xxxxxxxx xxxxxxx xxxxxxx.
Xxxxxxx xxxxxxx jsou xxxxxxx s ohledem xx druh, xxxxxxx x xxxxx x xxxxxxx s xxxxxxxxxxx
§15 xxxxxxxxxx právního xxxxxxxx
10) a označena xxx, xxx xxxx xxxxx xxxxxxxxxxxx jednotlivých xxxxxx. Xxxx navykání xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10)1.2.1.3 Xxxxx xxxxxx
Xxxxx zvířat nutně xxxxxx xx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx a xx minimálním xxxxx xxxxxxxxxxxx xxxxxxxxxxx vyžadovaném xxx xxxxxxxxx xxxxxxxx.
Xxxx xx xxxxxxx xxxxxxx xxxxxxxx samců X1 xxxxxxx. Nejméně 500 xxxxx x F1 xxxxxxxx je xxxxxxxxx x každé exponované xxxxxxx. Xxxxxxxx xxxxx xxxxxxxxxxx také xxxxxx X1 generace xxxxxxx, xxx xx xxxxxxxx 300 xxxxx x 300 xxxxx.
1.2.1.4 Xxxxxxxxx x xxxxxxxxx kontroly
Mohou xx použít xxxxxxxxx xxxxxxxx xxxxxxx získané x předchozích pokusů. Xxxxxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx z xxxxxxxxx xxxxxx z xxxx xxxxxxxxxx, xxxxx xxx xxxxxxx.
1.2.1.5 Xxxxxxxxx
Xxxxxxx xx xxxxx xxxxx, xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxx, xxx xxx xxxxx xx xxxxxxxxxxx chování xxxx xxxxxxxxx. Xxx xxxxxxxxx xxxxxx dávka/odpověď xx xxxxx dvou xxxxxxx, xxxxxxx xxxxx. X netoxických látek xx xxxxxxx xxxxxxxx xxxxxxxxxxx xxxxx.
1.2.2 Xxxxx xxxxxxx
1.2.2.1 Xxxxxxxx x xxxxxxxxx
Xxxxxxxxx xx xxx xxxxxxx xxxxxxxx. Nejčastěji xx xxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxxxx. Xxxx xx možná xxxxxxxx podávání xxxxxxxxx xxxxx xxxx xxx x týdnu xx 35 dnů.
Počet xxxxxxxxx xx xxxxxxxx xx xxxxx xxxxxxxxx xxxxxxxxxxx x xxxx zajistit, xx všechna buněčná xxxxxx xxxxxxxxxxx xxxxx xxxxx xxxxxxxxxxx. Xx xxxxx období oplodňování xxxx xxxxxx samostatně xxxxxxxxx do xxxxx. Xx xxxxxx xx xxxxx zaznamenat datum, xxxxxxxx xxxx a xxxxxxx xxxxxx. Xx xxxx jsou xxxxx x xxxxxx xxxxxxx xxxxxxxx až xx xxxx xxxxxxxx xx xxxxxxxxxxx.
1.2.2.2 Xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxx
Xxxxxxx se xxxxx xx dvou xxxxxxx xxxxx. Xxxx fertility X1 potomků x xxxxxxxx verifikace možných xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxx xxxxx xxxxx X1 generace xxx xxxxxxxxxxx výběru xxxxxx xxxxx xxxxxxxxx.
(x) Xxxx xxxxxxxxx
Xxxxxxx xxxxxxxxx zvířat x X1 xxxxxxxx xx xxxx xxxxxxxx x velikosti xxxx x/xxxx xxxxxxxx xxxxxx xxxxxx samic. Kritéria xxxxxx xxxxxxxx x xxxxxxx fertility musí xxx xxxxxxxxx xxx xxxxx kmen xxxxxxxxx xxxx.
Xxxxxxxx vrhu: X1 xxxxx určení x xxxxxxxxx jsou xxxxxxxx xxxxxxxxxx xx xxxxx xx samicemi xx xxxxxxxx xxxxxxxxxxx xxxx xxxxxx skupiny. Xxxxx xxxx kontrolovány xxxxx xxxxxxxx 18. dnem xx oplodnění. Velikost xxxx x pohlaví X2 xxxxxxx jsou xxxxxxxxxxx xxx porodu, xxxx xxxx jsou xxxxxxxx. Xxxxxxxx jsou xxxxxxxxx F1 samice, X2 xxxxxxx malých xxxx xxxx xxxxxxxxxx xxx další testy. Xxxxxx-xxxxxxxxx translokací jsou xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx x jakéhokoliv xxxxxx mužského potomka. XX-xxxxxx xxxx určeny xxxxxx xxx ratio xxxx jejich xxxxxxx x 1:1 na 1:2 xxxxx vs. xxxxxx. X xxxxxxxxx xxxxx jsou xxxxxxxx X1 xxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxx, xxxxxxxx první X2 xxx xxxxxxxx, xxxx xxxxxxxxx xxxxxx určenou xxxxxxxx xxxxxxx, xxxxx xxxx xxxxxxxxxxx druhé x xxxxx vrhy.
F1 xxxxxxx, xxxxx xxxxxxx xxx xxxxxxxxxxxxx xxxx xxxxxxxx xx xxxxxxxxxxx xxx F2 xxxx, xxxx xxxx xxxxxxxxx xxx' xxxxxxxx xxxxxx xxxxxx, nebo jsou xxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxx.
Xxxxxxx obsahu xxxxxx: Xxxxxxx xxxxxxxxx vrhu x xxxxxx xxxxxxxxxxx xx způsobena xxxxx xxxxxx, xxxxx xxxxxx xxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx translokací x xxxxxxxxxxx zvířat. Xxxxxxxxx X1 samci xxxx xxxxxxxxxxx xxxxx xx 2 - 3 xxxxxxx. Oplodnění xx xxxxxxxx denní xxxxx xxxxxxxxx vaginální xxxxx. Xxxxxx jsou xxxxxxxx 14. -16. xxx a xxxx xxxxxxxxxxx živé x xxxxx xxxxxxx.
(x) Cytogenetická xxxxxxx
Xxxxxxx xxx-xxxxxx xxxx xxxxxxxxxx xxxxxxxxx x xxxxxx. Nosiči xxxxxxxxxxx xxxx xxxxxx na xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxx xx xxxxxx xxxxxxxxx - xxxxxxxx X x xxxxxxxxxx xxxxxxxxxxxxxx. Nález xxxxxxx xxxx xxxxx x xxxxxxxxxxxxxxx xxxxxxxxxx splňuje xxxxxxxxxx xxxxx, xx xxxxxxxxx xxxxx xx xxxxxxxxx xxxxxxxxxxx. Xxxxxxxx xxx xxxxxxxx xxxxx xx xxxxxxxx, xxxxxxx X, xxxxx jsou xxxxxxxxx xxxxxxxxxxxxx. Na xxxxxxx xxxxx xxxx xxx xxxxxxxxxxxxx vyšetřeno xxxxxxx 25 xxxxx x xxxxxxxxx - xxxxxxxx X. Xxxxxxx xxxxxxxxxxx xxxxxxxx xx xxxxxxxxxxxxxxx xxxx v xxxxxx dřeni xx xxxxxxxx x samců x malými xxxxxx x xxxxxxxxxx xxxxxx xxxx diakinézou, xxxx x X1 samic xxxxxxxxxxx X0. Přítomnost xxxxxxxxx xxxxxxxx x/xxxx xxxxxxxx xxxxxxxxxx x xxxxx x 10 xxxxx je důkazem xxx xxxxxxxxx xxxxx xxxxxxxxxxxx sterilitu (c-t xxx). Xxxxxxx X-xxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxx xxxxx být xxxxxxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxxx chromozómů. Přítomnost 39 xxxxxxxxxx xx xxxxx 10 xxxxxxxx xx důkazem xxx XX xxxxxx.
2 ÚDAJE
Získané xxxxx se xxxxxxxx xx xxxxxxx.
Xxx každý xxxxxxxx xxxxxxxxxxx xx xxxxxxxxxxx průměrná xxxxxxxx xxxx a xxxxx xxxxxxx (xxx xxxxx) xxx xxxxxxxx x xxx xxxxxxxxx.
Xxx xxxxx xxxxxxxxx X1 xxxxxx xx xxxxx xxxxxxxx xxxxxxxx vrhu xxxxxxxx x xxxxxxxxxxxx xxxxxxxxx xxxx X1 nosičů xxxxxxxxxxx. Xxx xxxxxxx xxxxxx xxxxxx xx xxxxx xxxxxxxx počet xxxxxx x xxxxxxx xxxxxxx x xxxxxxxx x xxxxxxxxxxxx počty xxxxxx x xxxxxxx xxxxxxx pro xxxxx xxxxxxxxxxx X1 xxxxxx xxxxxxxxxxx.
Xxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxx-xxxxxxxx I xx xxxxx počet xxxx xxxxxxxxxxxxxxx xxxxx a xxxxxxx počet xxxxx xxx každého xxxxxx xxxxxxxxxxx.
Xxx X1 xxxxxxxx xxxxxxx xx xxxxxxxxxxx xxxxx a xxxx xxxxxxxxxx. Xxxx se xxxxx váha xxxxxx x xxxxxxxxxxx o xxxxxxxxxxxxx xxxxxxx.
X X0 xxxxx xx xxxxx xxxxxxxx velikost xxxx, xxx ratio F2 xxxxxxx x xxxxxxxx xxxxxxxxxxxxx analýzy.
V případě, xx xxxxxx xxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxx možní nositelé X1 translokací, xx xxxxx v xxxxxxxxx xxxxx xxxxxxxxx x xxxxxxxxx počtu xxxxxxxxxxx xxxxxxxxxxxxxx heterozygotů.
Musí být xxxxxxx údaje x xxxxxxxxxxx a xxxxxxxxxxx xxxxxxxxxx.
3 PROJEKT XXXXXX, XXXXXXXX XXXXXX X XXXXXXXXX ZPRÁVA
V xxxxxxx x příslušnými xxxxxxxx xxxxxxxx
9) musí xxx xxxxxxxxx xxxxxxx xxxxxx x x xxxxxxx xxxxxx je xxxxx xxxx protokol.
Zpráva x xxxxxxx pokusu obsahuje xxxx xxxxxxxxx o:
- xxxxx myší, stáří x xxxx exponovaných xxxxxx,
- počtu xxxxxxxxxxxx xxxxxx xxx xxxxx xxxxxxx x exponovaných x kontrolních xxxxxxxxx,
- xxxxxxxxxxxxxxxx xxxxxxxxxx, xxxxxxxx xxxxx ovlivňování zvířat, xxxxxxx hladiny, xxxxxxxxxxxx x schéma xxxxxxxxxxx,
- xxxxx x pohlaví xxxxxx xx xxxxxx, xxxxx a pohlaví xxxxxxx xxxxxxxxx xxx xxxxxxx translokací,
- xxxx x kritériích xxxxxxx xxxxxxxxxxx,
- xxxxx x xxxxxxxx xxxxx xxxxxx xxxxxxxxxxx, xxxxxx xxxxx x březosti a xxxxxx dělohy,
- xxxxx xxxxxxxxxxxxx xxxxxx x xxxxxxxxxxxxx analýzy, xxxxxx xxxxxxx,
- xxxxxxxxxxx xxxxxxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.26 XXXX XXXXXXXXXXXX XXXXXX TOXICITY (90denní xxxxxx xxxxxx xxxxxxxx x opakovanou xxxxxxxx xxxxxxxxx)
1 METODA xx x xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
7)1.1 Xxxx
Xxx xxxxxxxxx a xxxxxxxxx xxxxxxxxx vlastností xxxxxxxx xxxxx lze xxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxx po xxxxxxx xxxxxxx informací x xxxxxxxx z xxxxx xxxxxx xxxxxxxx nebo xxxxxxxx xxx 28xxxxx xxxxxxxxx aplikaci. Xxxx 90xxxxx xxxxxx xxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxxx xxx xxxxxx, xxxxx xx mohlo xxxxxx vlivem xxxxxxxxx xxxxxxxx xxxxx x xxxxxxx xxxxxxx xxxxxx, xxxxxxxxxxxx xxxxx xx xxxxxxxxx x xxxx xx do dospělosti. Xxxxxx xx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxx účincích, xxxxx xxxxxx orgány a xxxxxx xxxxxxxx x xxxx xxxxxxxxxx xxxxx xxxxxxx xxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx, xxxxxx xxx xxxxxx při xxxxxx xxxxxx dávek xxx xxxxxxxxx studie x pro xxxxxxxxx xxxxxxxxxxxxxx kritérií pro xxxxxxxx xxxxxxx.
Xxxxxx klade xxxx xxxxx xx xxxxxxxxxxxx příznaky x xxxxxxxxx možné xxxxxxxxxxxx xxxxxx a účinky xx xxxxxxxxxx. Důraz xx xxxxx xxx xx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx, x xxxxx získat co xxxxxxx informací. Tato xxxxxx by xxxx xxxxxxx xxxxxxxxxxxx chemických xxxxx, které xx xxxxx vyvolat xxxxxxxxxxxx xx xxxxxxxxxxxx xxxxxx xxxx mít xxxxxxxxxx xxxx xx reprodukční xxxxxx, které xx xxxxxxxxxx xxxxx xxxxxx xxxxxxxx.
1.2 Definice
Dávka: xx xxxxxx množství xxxxxxxxx xxxxx. Xxxxx xx xxxxxxxxx bud' xxxx xxxxxxxx (x g, xx), xxxx xxxx xxxxxxxx xxxxxxxxx xxxxx xx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxx (xxxx. xx/xx) xxxx xxxx xxxxxxxxxx koncentrace x xxxxxxx (xxx) xxxx x xxxxx xxxx.
Xxxxxxxxx: xx xxxxxx xxxxxx xxxxxxxxxx xxxxx, xxxx xxxxxxx x xxxxxx xxxxxxxx.
XXXXX (xx xxxxxxxx xxxxxxx xxxxxx xxxxx): xx xxxxxxx xxx xxxxxxx xxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxxx, xxx xxxxx xxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx účinky xxxxxxxxxxx x podáváním xxxxx.
1.3 Xxxxxxx xxxxxx
Xxxxxxxxx xxxxx xx podává xxxxx orálně xx 90 xxx x xxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, x xx xxxxx xxxxxxx jedna úroveň xxxxx. Xxxxx xxxxxxxx xx zvířata xxxxxxx xxxxxxxx, aby xx xxxxxxxx xxxxxxxx xxxxxxxx. Xxxxxxx, xxxxx xxxxxx xxxxx xxxxxx xxxx xxxx utracena, i xxxxxxx, která xxxxxxx xxxxx xxxxxx, xx xxxxxxx.
1.4 Xxxxx xxxxxx
1.4.1 Xxxxxxxx xxxxxx
Xxxxxxx xxxxxxx xxxx xxxxxxx x xxxxxxx na xxxx, xxxxxxx x xxxxx x xxxxxxx x xxxxxxxxxxx
§15 zvláštního xxxxxxxx xxxxxxxx
10) a xxxxxxxx tak, aby xxxx možná identifikace xxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx právního předpisu.
10) Xxxxxxx xx xxxxxxx xxxxxxx xx xxxxxxxxx x xx xxxxxxxxxxxx xxxxxxxxxxxxxxxx skupin.
1.4.2 Xxxxxxxx xxxxx
Xxxxxxxxxx xxxxx xxx xxxxxxx sondou, x xxxxxxx xxxx v xxxxx xxxx. Xxxxxx xxxxxxxx xxxxxxxx xxxxxx xx účelu xxxxxx x na fyzikálních x chemických xxxxxxxxxxxx xxxxxxxxx xxxxx.
Xxxxx je xx xxxxxxxx, xxxxxxxxx xxxxx xx rozpustí xxxx xxxxxxxxxx ve xxxxxxx xxxxxxxx. Xxxxxxxxxx xx nejprve zvážit xxxxxxx xxxxxxx xxxxxxx, xxxxx xxxxxxx xxxx xxxxxx xxxx suspenze x oleji (např. xxxxxxxxxx) x xxx xxxxxxx v xxxxx xxxxxxxx. Xxx xxxxxxx xxxxxxxx xx třeba xxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx. Xx třeba xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxx xxxxxxxx.
1.4.3 Xxxxxxxxxxxxxx xxxxxxxx
1.4.3.1 Xxxxxxx xxxxxxx
X xxxxxxxx xx upřednostňují potkani, xxx xxx xxxxxx x jiný xxxx xxxxxxxx, xxxx. xxxx. Xxxxxxx xx xxxxx xxxxxx zvířata x xxxxx užívaných laboratorních xxxxx. Xxxxxx xxxx xxx xxxxxxxx a xxxxx xxx xxxxx. Xxxxxxxx xx xxxx xxxxx xx xxxxxxxx xx xxxxxxxxx x xxxxx než xxxxxxx xxxxxxxx xxxxx devíti xxxxx. Xx xxxxxxx xxxxxx xx xxx xxxxxxxx xxxxxxx hmotnosti xxxxxx xxxxxxxxx; xxx xxxxx pohlaví xxxxxx xx nemělo překročit ± 20 % xxxxxxx xxxxxxx. Je-li xxxxxx předběžnou studií xxx dlouhodobou studii xxxxxxxxx xxxxxxxx, xxxx xx xx v xxxx studiích xxxxxxxx xxxxxxx xxxxxxxx xxxxx x xxxxxxxx xxxxxx.
1.4.3.2 Xxxxx a pohlaví
Pro xxxxxx xxxxxxx xxxxx xx použije nejméně 20 zvířat (10 xxxxx x 10 xxxxx). Pokud se xxxxxxx budou xxxxxxxxx x průběhu xxxxxx, xx nutno zvýšit xxxxxxx xxxxx xxxxxx x xxxxx zvířat, xxxxx budou xxxxxxxx xxxx xxxxxx xxxxxx. Xx xxxxxxx dřívějších xxxxxxxx x xxxxxxxxx xxxxxxxx látce nebo xx xxxxxx příbuzné xxxxx xx xxxxx xxxxxx x xxxxxxx xxxxx (xxxxxxxxx) xxxxxxx xxxxxx 10 (5 xxxxxx xxxxxxx xxxxxxx) xx xxxxxxxxx skupiny x xx xxxxxxx x nejvyšší xxxxxx, xxx xx xx xxxxxxxx aplikace mohlo xxxxxxxx, zda xxxx xxxxxxxx účinky xxxxxx xxxx trvalé. Trvání xxxxxx následného pozorování xx stanoví x xxxxxxx na xxxxxxxxxx xxxxxx.
1.4.3.3 Xxxxxx xxxxx
Xxxxxxxxx-xx xx xxxxxxx xxxx (xxx 1.4.3.4), použijí xx xxxxxxx tři xxxxxx xxxxx x xxxxxxxx kontrola. Xxxxxx xxxxx mohou xxxxxxxx x xxxxxxxx xxxxxx xxx opakované aplikaci xxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxx na zjištění xxxxxxx účinných xxxxx x xxxx xx xxxxxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxxxx xxxxx x xxxxxxxxx xxxxx xxxx x xxxxxxxxxx xxxxxxx. Xxxxxxx-xx xxxx xxxxxxxxx-xxxxxxxx xxxxxx xx biologické xxxxxx xxxxxxxxx xxxxx, xx xxxxxxxx xxxxxxx dávky xxxxxxx xxxxxxx účinky, xxx xxxxxxxxxx xxxxx xxxxxxx xxxx xxxxx xxxxxxx. Xxxxx xxxxxxx xxxxx, xxxx xxx xxxxxx tak, aby xxxxxxxx toxické xxxxxx xxxxxxxxxxxx xxxxx dávky x aby x xxxxxxxx hladiny xxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx (XXXXX). Často je xxx xxxxxxxxxxxx dávek xxxxxxxxx dvoj- xx xxxxxxxxxxx poměr xxxx xxxxxxx; xx xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxx, než xxx xxxxxxxxx xxxx xxxxxxx xxxxxx široké (xxxx. xxxx xxx 6-10xxxxxxx).
Xxxxxxxxx xxxxxxx xx xxxxxxxx xxxxx látka xxxx, xxxxxxx-xx xx xxxxxxxxx, xx xxxxxxxxx xxxxxxx xxxxxxxx vehikulum. X xxxxxxxx xxxxxxxx testované xxxxx xx zachází xx xxxxxxx x xxxxxxxxx xxxxxxx xxxxxx xxxx s xxxxxxxxx. Xx-xx xxxxxxx xxxxxxxxx, xxxxxx xx xxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxx objemu. Xxxxxx-xx xx xxxxxxxxx xxxxx x xxxxxxx x xxxxxxxxx-xx omezení xxxxxx xxxxxxx, xxxxxxxxxx se xxxxxx paralelně xxxxxxx xx xxxxxxx xxxxxxxx xxxxxxx, xxx se xxxxxxx xxxx snížení xxxxxx xxxxxxx xxxxxxxxxxxxx xx xxxxxxxxxxxxxxx změn.
Má xx přihlédnout x x xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx a xxxxxxxxx xxxxxx: vliv xx xxxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxxxx xxxx xxxxxxx testované xxxxx; xxxx xx xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx, xxxxx xxxxx xxxxxx xxxx xxxxxxxx; xxxx xx xxxxxxxx xxxxxxx, vody xxxx xx xxxxxxxx xxxx xxxxxx.
1.4.3.4 Limitní xxxx
Xxxxx xxxx provedený xxxx xxxxxxxx xxxxxxx xx xxxxxxx xxxxxx 1000 xx.xx-1 tělesné hmotnosti xxxx xxxxx neukáže xxxxxxxxxxxxx xxxxxxxxxx účinky x pokud xx xx xxxxxxx údajů x látkách x xxxxxxxx xxxxxxxxxx nepředpokládá xxxxxxxx, není nutné xxxxxxx xxxxxxxxx xxxxxx xx xxxxx xxxxxxxx xxxxx. Tento xxxxxxx xxxx se xxxxxxxxx, xxxxxxxxx-xx údaje x xxxxxxxx xxxx xxxxxxx xxxxxxx xxxxx.
1.5 Xxxxxx
1.5.1 Xxxxxxxx
Xxxxxxxxx látka xx xxxxxxxx xxxxxxxx 7 xxx x xxxxx xx dobu 90 xxx. Xxxx xxxxx xxxxxxxx, např. 5 xxx x týdnu, xxxx xxx xxxxxxxxx. Xxxxxxxx-xx se testovaná xxxxx xxxxxx xxxx xxxxxxx, xxxx by xxx xxxxxxxx xxx x xxxxxx xxxxx. Xxxxxxxxx objem tekutiny, xxxxx xxx xxxxx xxxxxxxx, závisí na xxxxxxx xxxxxxxxx xxxxxxx. Xxxxx by neměl xxxxxxxxx 1 xx xx 100 g xxxxxxx xxxxxxxxx, x xxxxxxxx xxxxxxx xxxxxxx, xxx xxx podat xx 2 xx xx 100 g xxxxxxx hmotnosti. S xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxx látek, jejichž xxxxxx se zhoršují x xxxxxxxxxxx, xx xxxxx xxxxxxx podávaných xxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxx, xxx xxx xx xxxxx xxxxxxxxx xxxxx xxxxxxx xxx objem.
U látek xxxxxxxxxx xxxxxxxx xxxx x xxxxx xxxx xx důležité xxxxxxxx, xxx množství xxxxxxxx xxxxx xxxxxxxxxxx normální xxxxxx xxxx vodní xxxxxxxxx. Xxxxxx-xx xx xxxxxxxxx xxxxx x xxxxxxx, xxxx se xxxxxx xxx' konstantní xxxxxxxxxxx (v ppm xxxx xx.xx-1 xxxxxxx) xxxx xxxxxxxxxx xxxxxxxxx xx xxxxxx x xxxxxxx xxxxxxxxx zvířete; xxxxxxxx xxxxxxxxxxx xx xxxxx uvést. Xxxxxxxx-xx xx xxxxx sondou, xxxx xx xx xxx xxx xxxxx xxx ve xxxxxxx xxxx; je xxxxx xxxxxxxxx xxxxxxxxx xxx, xxx xxxx konstantní xxxxxxxx x xxxxxx xxxxxxx hmotnosti zvířete. Xx-xx 90xxxxx xxxxxx xxxxxxxxxx xxxxxx k xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx, má xxx x obou xxxxxxxx xxxxxxx stejná xxxxx.
1.5.2 Xxxxxxxxxx
Xxxx xxxxxxxxxx xx xxxxxxx 90 dní. Xxxxxxx v xxxxxxxxx xxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxxxx se xxxxxxxxx po xxxxxxx xxxx xxx xxxxxxxx, xxx xx xxxxxxxxx, xxx xxxxxxx xxxxxxxx xxxx xxxxxxx xxxxxx xxxxxxxxxxx.
Xxxxx xxxxxxxx xxxxxxxxxx xx xxxxx xxxxxxxx xxxxxxx xxxxxx xxxxx, xxxxxxx vždy ve xxxxxxx xxxxx xxxx, x xxxx očekávaného xxxxxxxxxxx xxxxxx. Klinický xxxx zvířat xx xxxxxxxxxxx. Xxxxxxx xxxxxxx xxxxx, xxxxxxx xx xxxxxxx x xx xxxxx xxxxxxx dne, xx xxxxxxx xxxxxxxxx x xxxxx xxxxxx xx xxxxxx xxxxxxxx xxxxx x příznaků xxxxxxxxxx.
Xxxxxxx jednou před xxxxx aplikací látky x xxxx jednou xxxxx xx xxxxxxx xxxxxxxx klinické pozorování xxxxx xxxxxx xx xxxxxx xxxxxxxxxxxxxxxxxxx xxxxxxxx. Xxxxxxxxxx xx třeba xxxxxxxx xxxx xxxxxxx xxxx, xxxxxxx ve xxxxxxxxxxx xxxxxxxxxxx prostoru x xxxxxxx xx xxxxxxx dobu. Výsledky xxxxxxxxxx xx xxxxxxx xxxxxxxxxxxxx, xxxxxxx x xxxxxxxx xxxxxxxxxxx systému (xxxxxx doby xxxxxxx, xxxxxx x xxxxxx), xxxxxxxxxxxxxxxxx x xxxxxxxxx xxxxxxxxxx. Je xxxxx xxxxxxxx, aby xx xxxxxxxx pozorování měnily xxxxxxxxx. Xxxxxxxxxx zahrnuje xxxxxxxxxxxx xxxxx xxxx, xxxxx, xxx x xxxxxxx, xxxxxxxxxx xxxxxxx x exkretů a xxxxx xxxxxxxxxxx funkcí (xxxxxx, xxxxxxxxxx, xxxxxxxx xxxxxx, poruchy xxxxxxx). Xxxxxxxxxxxxx xx xxxxx xxxxx x xxxxxx xxxx, dále reakce xx xxxxxxxxxx, xxxxxxxxxx xxxxxxxxxx nebo xxxxxxxxx xxxxxx, stereotypů (xxxx. xxxxxxxx čištění, opakované xxxxxxxx) xxxx bizarní xxxxxxx (např. xxxxxxxxxxxxxxx, xxxxx xxxxxxxx).
7)Xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxxxx xx xx xxxxxxx před podáváním xxxxxxxxx xxxxx x xx xxxxx studie, xxxxxxx x všech xxxxxx, xxx xxxxxxx x xxxxxxx s xxxxxxxx dávkou a x kontrolní skupiny. Xxxxxx-xx se xxxx xxxxx, xxxxxxx xx xxxxxxx zvířata.
Ke xxxxx xxxxxx, xxx xx xxxxx xxx v 11. xxxxx, xx xxxxxxxx xxxxxx na xxxxxxxxxx podněty
7) (např. xxxxxxxx, xxxxxxx x xxxxxxxxxxxxxxx),
7) xxxxx xx xxxx xxxxxx
7) x xxxxxxx xxxxxxxxx xxxxxxxx.
7) Xxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxx, xxxxx xx xxxxx x xxxxxxxxx xxxxxx, jsou xxxxxxx x příslušné xxxxxxxxxx. Xxx xxxx xxxxxx x alternativní xxxxxxx.
Xxxxxxxxxx xxxxxxxxx poruch xxx případně vynechat, xxxx-xx x xxxxxxxxx xxxx o funkčních xxxxxxxxxxxx x jiných xxxxxx x xxxxx xxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx žádné funkční xxxxxxx.
Xxxxxxxxx lze xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx x x skupin xxxxxxxxxxxx takové xxxxxxxx xxxxxxxx, xxxxx xx xxx xxxxxxxxxx xxxxxxxxx xxxxx xxxxxx.
1.5.2.1 Tělesná xxxxxxxx x xxxxxxxx xxxxxxx/xxxx
Xxxxxxx xxxxxxx se xxxx xxxxxxx xxxxxx xxxxx. Xxxxxx xxxxxxx xx xxxxxxxx nejméně xxxxxx týdně. Xxxxxxx-xx xx xxxxxxxx x xxxxx xxxx, také xxxxxxx jednou xxxxx xx xxxxxxxxx xxxxxxxx xxxx. Xx spotřebě xxxx je xxxxxxx xxxxxxxxxxx ve xxxxxxxx, xxx se xxxxxx xxxxxxxxx xxxxx x xxxxxxx xxxx xxxxxx, xxxxx xxxxx xxxx xxxxx xx xxxxx xxxxxx tekutin.
1.5.2.2 Xxxxxxxxxxx x klinická xxxxxxxxx
Xxxx xx odebírá z xxxxxxxx místa a xxxxxxxx xx za xxxxxxxx podmínek. Xx xxxxx testování se xxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxx nebo xxx něm.
Z xxxxxx xxxx na xxxxx xxxxxxxxx a xxxxx xxxxxx xx provádí xxxxxxxxxxx hematologická vyšetření: xxxxxxxxx hematokritu, koncentrace xxxxxxxxxxx, počet xxxxxxxxxx, xxxxxxx x xxxxxxxxxxxxx xxxxx leukocytů, počet xxxxxxxx, test xx xxxxxxxxxx xxxx x xxxxxxx se protrombinový xxx.
Xxxxxxxxxxx xxxxxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xx xxxxx - zvláště xx ledviny x xxxxx, xx xxxxxxx x xxxxxxxx xxxxxx xxxxxxxxxx každému xxxxxxx xxxxx xxxx xxxx xxx xxxxxxxx (xxxxx xxxxxx uhynulých nebo xxxxxxxxxx xxxxx xxxxxx). Xxxxxxx xxxx u xxxxxxxxxxxxxxx xxxxxxxxx xxx xxxxxxxx vzorky pro xxxxxxxxxxxx xxxxxxx x xxxxx studie. Xxxx xxxxxxx xxxx xx xxxxxxxxxx xxxxxx xxxxxxx xxxx noc xxxxxxx.
9) Xxxxxxxxx xxxxxx x xxxx zahrnuje xxxxxxxxx xxxxxx, xxxxxxxx, glukózy, xxxxxxxxx xxxxxxxxxxxx, močoviny, xxxxxx močoviny, kreatininu, xxxxxxxxx xxxxxxxx x xxxxxxxx, xxxxxxx dva xxxxxx indikující x xxxxxxxxxxxxxxx xxxxxx (xxxxxxxxx xxxxxxxxxxxxxxxxxxxxxx, aspartátaminotransferáza, xxxxxxxxx xxxxxxxxx, xxxxxxxxxxxxxxxxxxxxxxxxxx a xxxxxxxxxxxxxxxxxxxxx). Xxxxxxxx lze xxxx xxxxxxxxx xxxxxxx xxxxxx (jaterního xxxx xxxxxx xxxxxx) x xxxxxxxxx xxxxxxx může x xxxxxxxx xxxxxxxxx xxxxxxxxxx užitečné xxxxxxxxx.
Xxxxx xxxxxxx xx časově xxxxxxxxxx xxxx a xxxxxxxxx xxxx během xxxxxxxxxx xxxxx xxxxxx: xxxxxxxx xx xxxxx xxxxxx, objem, osmolalitu xxxx specifickou xxxxxxxx, xX, bílkoviny, xxxxxxx x krev/krvinky.
Dále xx xxxxx uvážit stanovení xxxxxxxxxxxxxx indikátorů xxxxxxxxx xxxxx x séru. Xxxxx xxxxxxxxx se xxxxxxx x xxxxx xxxxxxx nebo xxxxxxxxxxx x xxxxxxxx xx xxxxxx metabolické xxxxxx, xxxx. xxxxxxxxx xxxxxxx, xxxxxxx, triglyceridů xxxxxxx, xxxxxxxxxxxx xxxxxxx, xxxxxxxxxxxxxx x xxxxxxxxxxxxxx. Xxxxxxxx xxxxxx vyšetření xx xxxxxxxx podle příslušnosti xx xxxxxxxx skupin xxxxx xxxx xxxxxx xx xxxxxxx.
Xxxxxx xx xxxxx xxxxxxxxxx pružně, xxxx x xxxxx xxxxxxx živočišný druh x xxxxxxxxxx xx xxxxxxxxx xxxxxx dané xxxxx.
Xxxxx nejsou k xxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxxx hodnotách xxxxxxxxx hematologických xxxx xxxxxxxxxxxxx proměnných, je xxxxx zvážit xxxxxx xxxxxxxxx ještě xxxx xxxxxxxx xxxxxx; xxxxxx xx xxxxxxxxxxxx, xxx xx xxxx xxxx xxxxxxxxx x xxxxx xxxxxx xxxx aplikací.
7)1.5.2.3 Xxxxx
X xxxxx zvířat xxxxxxxxx xx xxxxxx xx provede xxxxxxxx xxxxx, xxxxxxxxxx xxxxxxx xxxxxxxxx vnějšího xxxxxxx xxxx, xxxxx xxxxxx x lebeční, xxxxxx x xxxxxx dutiny x xxxxxx obsahu. Xxxxx, xxxxxxx, xxxxxxxxxx, xxxxxxx, xxxxxxxxxx, děloha, xxxxxxxxx. xxxxxx, xxxxxxx, xxxxx x xxxxx xxxxx zvířat (kromě xxxx, xxxxx byla xxxxxxxx uhynulá xxxx xxxx xxxxxxxx x xxxxxxx testu) se xxxxxxx očistí od xxxxxxxx xxxxx x xx xxxxxxxx xx xxxxx xx xx xxxxxx stavu xxxxx, xxx xxxxxxx x xxxxxxxxx.
Xxxxxxxxxxx xxxxx xx xxxxx xxxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxx xxx daný xxx xxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxxx vyšetření: xxxxxxx xxxxx s xxxxxxxxxxxxxxx xxxxxx, xxxxx (xxxxxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxx xxxxx, xxxxxxx x prodloužené míchy), xxxxx (ve třech xxxxxxxx: krční, xxxxxxx xxxxxx x lumbální), xxxxxxxx, xxxxxx žláza, xxxxxxxxx xxxxxxx, xxxxxx, xxxxx, xxxxxx žlázy, xxxxxxx, xxxxx a xxxxxx střevo (včetně Xxxxxxxxxx xxxxx), xxxxx, xxxxxxxx, ledviny, xxxxxxxxxx, xxxxxxx, xxxxx, průdušnice x plíce (konzervované xxxxxxxxx fixačním roztokem x xxxxxxxxx xxxxxxxxx), xxxxx, gonády, xxxxxx, xxxxxxxx pohlavní orgány, xxxxxx mléčná žláza, xxxxxxxx, močový xxxxxx, xxxxxxx (xxx), xxxxxxxxxx xxxxxx (xxxxxxxxxx jedna xxx xxxxxx aplikace x xxxxx xxxxxxxx xxx xxxxxxx xxxxxxxxxxx xxxxxx), periferní xxxx (x. xxxxxxxxxxx nebo x. tibialis) nejlépe x xxxxxxxxx xxxxx, xxx xxxxxx xxxxx (x/xxxx xxxxxxx nátěr x xxxxxx kostní xxxxx), kůže x xxx (xxxx-xx xxx xxxxxxxxxxxxxxxx xxxxxxxxxxx pozorovány xxxxx). Xxxxx klinických xxxx xxxxxx nálezů xx xxxxx zkoumat x xxxxx xxxxx. Xxxxx orgán, xxxxx xx mohl xxx xxxxxxx orgánem pro xxxxxxxx testované xxxxx, xx xxxxx konzervovat.
1.5.2.4 Xxxxxxxxxxxxxxxx vyšetření
U všech xxxxxx skupiny, které xxxx podána xxxxxxxx xxxxx, x x xxxxxx xxxxxxxxx xxxxxxx xx xxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx a xxxxx. Xxxxx xx v xxxxxxxx x xxxxxxx xx xxxxxxx x xxxxxxxx dávkou xxxxxx xxxxxxxxx xxxxxxxxx testovanou xxxxxx, xx xxxxx xxxxxxx xxxxxxxxxxxx vyšetření xxxxxx xxxxx x x xxxxx xxxxxx x nižšími xxxxxxx.
Xxxxxxx xxxxxxxxxxxxx xxxx xx xxxxx xxxxxxxx.
X xxxxxx xxxxxxxxxxx xxxxxx, xxxxx xxxx do studie xxxxxxxx, xx třeba xxxxxxx histopatologické xxxxxxxxx xx zvláštním xxxxxxx xx xxxxxx x xxxxx, xx xxxxxxx xx xxxxxxxx xxxxxx x xxxxxxxxx exponovaných xxxxxx.
2 XXXX X XXXXXX XXXXX
2.1 Xxxxx
X xxxxxxxxx musí být xxxxx x xxxxxx xxxxxxxxxxx zvířeti. Xxxxxxx xxxxx xx xxxxxxxxxx xx xxxxxxx, uvádějící x xxxxx xxxxxxxxx xxxxxxx xxxxx použitých xxxxxx xx začátku xxxxx, počet xxxxxx xxxxxxxxx x xxxxxxx xxxxx xxxx xxxxxxxxxx x humánních xxxxxx, xxxx úhynu xxxxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxx; xxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx toxických xxxxxxxx xxxxxx xxxx nástupu, xxxxxx a závažnosti xxxxxxx xxxxxxxx, počet xxxxxx xxxxxxxxxxxx xxxx, xxx lézí x xxxxxxxx zvířat s xxxxxxxxxxxx xxxx xxxx.
Xxxxxxxx x xxxxxxx xxxxx xx třeba vyhodnotit xxxxxxx x uznávanou xxxxxxxxxxxx xxxxxxx. Xxxxxxxxxxxx xxxxxx je třeba xxxxxx již xxx xxxxxxxxx xxxxxx.
3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx s xxxxxxxxxxx xxxxxxxx předpisy
9) musí xxx xxxxxxxxx projekt xxxxxx x o xxxxxxx xxxxxx je xxxxx vést protokol.
Zpráva x xxxxxx obsahuje xxxxxxxxxxx xxxxxxxxx:
Xxxxxxxxx xxxxx:
- xxxxxxxxx xxxxxx, xxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxxx,
- xxxxxxxxxxxxx údaje
- xxxxxxxxx (xx-xx použito): xxxxxxxxxx xxxxx xxxxxxxx, xxxx-xx xx xxxx.
Xxxxxxx xxxxxxx:
- použitý xxxx x xxxx,
- počet, xxxxx x xxxxxxx xxxxxx,
- původ, xxxxxxxx xxxxx, xxxxxxx atd.,
- xxxxxxxx jednotlivých xxxxxx xx xxxxxxx xxxxx.
Xxxxxxxx xxxxx:
- xxxxxxxxxx xxxxxx xxxxxx xxxxx,
- xxxxxxxx xxxxx o úpravě xxxxxxxxx látky xxx xxxxxxxx, xxxxxxxx x xxxxxxxx xxxxxxx, x xxxxxxxxxx koncentracích, xxxxxxxxx x xxxxxxxxxx xxxxxxxxx,
- xxxxxxxx xxxxx x xxxxxxx aplikace xxxxxxxxx xxxxx,
- přepočet z xxxxxxxxxxx látky x xxxxxxx nebo vodě (xxx) xx skutečnou xxxxx xxxxx v xx.xx-1 xxxxxxx hmotnosti (xxxxx jde o xxxxxxxx v xxxxxxx xxxx vodě),
- podrobné xxxxx x xxxxxxx x kvalitě xxxx.
Xxxxxxxx
- xxxxxxx xxxxxxxx x xxxx změny,
- xxxxxxxx xxxxxxx x xxxxxxxx xxxx,
- údaje x xxxxxxxxx xxxxxxxx podle xxxxxxx a úrovně xxxxx, xxxxxx popisu xxxxxxxx xxxxxxxx,
- xxxxxx, xxxxxxxxx x xxxxxx xxxxxxxxxx nálezů, příp. xxx xxxx vratné xxxx nevratné,
- xxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx,
- xxxxxxxxx xxxxxxxxxx xx smyslové xxxxxxx, xxxxxxxx xxxx x motorické aktivity (xxxxx xxxx xxxxxxx),
- xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx x xxxxxxxxxxx výchozími (xxxxxxxxxx) xxxxxxxxx,
- výsledky xxxxxxxxxxx xxxxxxx x xxxxxxxxxxx výchozími (xxxxxxxxxx) xxxxxxxxx,
- xxxxxxx xxxxxxxx xx xxxxx studie x xxxxxxxxx orgánů x xxxxxx xxxxxxxxx xxxxxx k tělesné xxxxxxxxx,
- pitevní nálezy,
- xxxxxxxx xxxxx xxxxx xxxxxxxxxxxxxxxxxx nálezů,
- xxxxx x xxxxxxxx, xxxxx xxxx xxxxxxx,
- statistické xxxxxxxxxx xxxxxxxxx xxxxxxxx, xxx xx to xxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.27 XXXX XXXXXXXXXXXX ORÁLNÍ XXXXXXXX (90xxxxx studie xxxxxx xxxxxxxx s xxxxxxxxxx xxxxxxxx xxxxxxxxxxx)
1 XXXXXX xx x xxxxxxx x právem Xxxxxxxxxx xxxxxxxxxxxx.
7)1.1 Xxxx
Xxx xxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx xxx xxxxxxx xxxxxxxxx xxxxxxxxxxxx orální xxxxxxxx x opakovanou xxxxxxxx xx xxxxxxx prvních xxxxxxxxx x xxxxxxxx x testů akutní xxxxxxxx xxxx toxicity xxx 28xxxxx opakované xxxxxxxx. Tato 90xxxxx xxxxxx xxxxxxxxx xxxxxxxxx x možném xxxxxxxxx xxx xxxxxx, které xx xxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxx x průběhu xxxxxxx xxxxxx, zahrnujícího xxxxx xx xxxxxxxxx x růst xx xx xxxxxxxxxx. Xxxxxx xx xxxxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxx cílové xxxxxx x xxxxxx xxxxxxxx x xxxx xxxxxxxxxx odhad xxxxxxx xxx pozorovaného xxxxxxxxxxxx xxxxxx, kterou xxx xxxxxx xxx xxxxxx xxxxxx dávek xxx xxxxxxxxx studie x xxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxx.
Xxxx xxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxxx xx xxxxxxxxxxxx x xxxxxxx se pouze xxxxx, xxxx:
- xxxxxx xxxxxxxxxx x xxxxxx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx či xxxxxxxxxxxxxxx xx xx xxxxxx xxxxx než na xxxxxxxxxx xxxx xxxx
- xxxxxxxxxxxxxxx studie xxxxxxxxx, xx xxxxxxx xxxxxxxxxxxx xxxxx xxxxxxxxxx xx xxxxxxxxxxxx volbou laboratorního xxxxxxx, xxxx když
- xxxx konkrétní xxxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxx.
Xxx xxx Všeobecný xxxx, Xxxx X.
1.2 Xxxxxxxx
Xxxxx: xx xxxxxx množství xxxxxxxxx xxxxx. Dávka xx vyjadřuje bud' xxxx xxxxxxxx (v x, xx), nebo xxxx xxxxxxxx xxxxxxxxx xxxxx xx xxxxxxxx xxxxxxxxx testovaného xxxxxxx (xxxx. xx/xx) xxxx xxxx xxxxxxxxxx xxxxxxxxxxx x xxxxxxx (xxx) xxxx x pitné xxxx.
Xxxxxxxxx: je obecný xxxxxx xxxxxxxxxx xxxxx, xxxx xxxxxxx x xxxxxx xxxxxxxx.
XXXXX (no xxxxxxxx adverse xxxxxx xxxxx): xx xxxxxxx xxx xxxxxxx xxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxxxxx nejvyšší xxxxx xxxx xxxxxxxx, xxx xxxxx nejsou xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxxxx s xxxxxxxxx xxxxx.
1.3 Xxxxxxx xxxxxx
Xxxxxxxxx xxxxx xx xxxxxx denně xxxxxx xx 90 dní x odstupňovaných xxxxxxx xxxxxxxx xxxxxxxx pokusných xxxxxx, x xx xxxxx skupině xxxxx xxxxxx xxxxx. Během xxxxxxxx xx xxxxxxx xxxxxxx xxxxxxxx, xxx xx xxxxxxxx příznaky xxxxxxxx. Xxxxxxx, xxxxx xxxxxx xxxxx xxxxxx xxxx xxxx utracena, x xxxxxxx, xxxxx xxxxxxx xxxxx xxxxxx, xx pitvají.
1.4 Xxxxx xxxxxx
1.4.1 Xxxxx xxxxxxxxx xxxxx
Xxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxxx xx xxx; xx xxxxx definovat xxxxxxx - xxxxx xx xxxxxxx xxxxxx. Xxx xxxxxx x xxxx xxxxx, xxxx. xxxxxxx nebo xxxxxxxxxxx. Xxxxxxx se xxxxxxxxxxxx, xxxxxxx-xx xx, xxxx xx být zdůvodněno. Xxxxxxxxx se xxxxx, xxxxxx xxxxxxx, x xxxxxxx xxx xx xx x podáváním xxxxx ve xxxx 4-6 xxxxxx x xx xxxxxxx xxx 9 xxxxxx. Xxxxxxx-xx xx subchronický orální xxxx jako xxxxxxxxx xxxx před xxxxxxxxxxx xxxxxx, x obou xxxxxxxx xx má xxxxxx stejný xxxxxxxxx xxxx x xxxxxxx.
1.4.2 Xxxxxxxx xxxxxx
Xxxxxxxxx se xxxxxx xxxxxxx, xxxxx xxxxx xxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxxxxx xxxxxxx x xxxxx xxxx xxxx testem chována x xxxxxxxxxxxxxxxx podmínkách. Xxxx xxxxxxxxxxxx xxxxxx xx xxxxxxxx xxxxx x xx xxxxxx xxxxxx. Xxxxxxxxxx se xxxxxxx xxx xxx xxx psy či xxxxxxx x xxxxxxxxx xxxxx a xxxxxxx 2 týdny xxx xxxxxxx x xxxxxxxxx xxxxxxxx zařízení. Musí xx xxxxxx xxxx, xxxx, původ, xxxxxxx, xxxxxxxx x/xxxx xxx. Xxxxxxx xx xxxxxxx xxxxxxx do kontrolní x do xxxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxx. Xxxxx xx xxxx xxx xxxxxxxxxx xxx, aby xx xxxxx jejich xxxxxxxx minimalizovaly. Xxxxxxx xxxxxxx xx přiřadí xxxxxxxxx xxxxxxxxxxxxx xxxxx.
Xxxxxxx xxxxxxx xxxx xxxxxxx x ohledem xx xxxx, xxxxxxx a xxxxx x souladu x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx předpisu
10) x xxxxxxxx xxx, xxx byla xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx právního xxxxxxxx.
10)1.4.3 Xxxxxxxx dávek
Testovanou xxxxx xxx xxxxxxx x xxxxxxx xxxx x xxxxx vodě, xxxxxx xxxx x xxxxxxxx. Způsob orálního xxxxxxxx závisí xx xxxxx xxxxxx x xx xxxxxxxxxxx a xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx.
Xxxxx xx xx xxxxxxxx, testovaná xxxxx xx rozpustí nebo xxxxxxxxxx xx xxxxxxx xxxxxxxx. Xxxxxxxxxx xx xxxxxxx zvážit xxxxxxx xxxxxxx roztoku, xxxxx xxxxxxx nebo xxxxxx xxxx suspenze x xxxxx (např. kukuřičném) x xxx roztoku x jiném vehikulu. Xxx nevodná xxxxxxxx xx třeba znát xxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxxxx. Xx xxxxx xxxxxxxx xxxxxxxxx testované xxxxx x podmínkách aplikace.
1.5 Xxxxxx
1.5.1 Počet a xxxxxxx
Xxx xxxxxx xxxxxxx xxxxx xx použije xxxxxxx 8 zvířat (4 samice x 4 xxxxx). Xxxxxx-xx xx s xxxxxxxxxxx x xxxxxxx xxxxxx, xxx by být xxxxx počet zvýšen x xxxxx xxxxxx, xxxxx mají být x xxxxxxx xxxxxx xxxxxxxx. Xxxxx xxxxxx xx xxxxx xxxxxx xxxx být xxxxxxxxxx, xxx xxxx xxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx. Xx xxxxxxx dřívějších xxxxxxxx x testované xxxxxxxx xxxxx xxxx xx xxxxxx xxxxxxxx xxxxx xx třeba zvážit x xxxxxxx xxxxx (xxxxxxxxx) skupiny zvířat 8 (4 xxxxxx xxxxxxx xxxxxxx) xx xxxxxxxxx xxxxxxx a xx skupiny s xxxxxxxx xxxxxx, aby xx xx ukončení xxxxxxxx xxxxx xxxxxxxx, xxx xxxx xxxxxxxx xxxxxx vratné xxxx xxxxxx. Xxxxxx xxxxxx xxxxxxxxxx pozorování xx xxxxxxx s xxxxxxx xx xxxxxxxxxx účinky.
1.5.1.1 Xxxxxx dávek
Neprovádí-li se xxxxxxx test (xxx 1.5.3), xxxxxxx xx xxxxxxx 3 xxxxxx xxxxx x xxxxxxxx xxxxxxxx. Úrovně dávek xxxxx xxxxxxxx x xxxxxxxx studií xxx xxxxxxxxx aplikaci nebo xxxxxxxxxxxx xxxxxx xxxxxxxxxx xx zjištění xxxxxxx xxxxxxxx xxxxx x xxxx xx xxxxxxxxxxx xxxxxxx existující toxikologické x toxikokinetické údaje x testované látce xxxx x xxxxxxxxxx xxxxxxx. Nebrání-li tomu xxxxxxxxx-xxxxxxxx xxxxxx či xxxxxxxxxx účinky xxxxxxxxx xxxxx, xx xxxxxxxx xxxxxxx xxxxx xxxxxxx xxxxxxx účinky, ale xxxxxxxxxx xxxxx xxxxxxx xxxx velké xxxxxxx. Xxxxx xxxxxxx xxxxx xxxx xxx xxxxxx xxx, aby xxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxxx xxxxx xxxxx x xxx u xxxxxxxx xxxxxxx nebyly xxxxxxxxxx xxxxxxxxxx účinky (XXXXX). Xxxxx xx xxx xxxxxxxxxxxx xxxxx optimální xxxx- xx čtyřnásobný xxxxx mezi xxxxxxx; xx xxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxx, xxx xxx xxxxxxxxx xxxx xxxxxxx xxxxxx xxxxxx (xxxx. xxxx xxx 6-10xxxxxxx).
Xxxxxxxxx xxxxxxx xx nepodává xxxxx xxxxx xxxx, xxxxxxx-xx xx xxxxxxxxx, je xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx. X xxxxxxxx xxxxxxxx testované xxxxx xx xx zvířaty x xxxxxxxxx skupině xxxxxxx stejně xxxx x xxxxxxxxx. Xx-xx xxxxxxx vehikulum, xxxxxx xx kontrolní xxxxxxx x xxxxxxxxx použitém xxxxxx. Podává-li se xxxxxxxxx xxxxx x xxxxxxx x způsobuje-li xxxxxxx xxxxxx xxxxxxx, xxxxxxxxxx xx xxxxxx xxxxxxxxx xxxxxxx se xxxxxxx xxxxxxxx xxxxxxx, xxx xx odlišil xxxx snížení příjmu xxxxxxx nechutenstvím od xxxxxxxxxxxxxxx xxxx.
Xx se xxxxxxxxxxx x k xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx x ostatních xxxxxx: xxxx na xxxxxxxxxxx, xxxxxxxxxx, xxxxxxxxxxxx nebo xxxxxxx xxxxxxxxx látky; xxxx na xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx, xxxxx xxxxx xxxxxx xxxx xxxxxxxx; vliv xx xxxxxxxx potravy, xxxx xxxx xx xxxxxxxx stav xxxxxx.
1.5.1.2 Xxxxxxx xxxx
Xxxxx xxxx xxxxxxxxx xxxx popsanou xxxxxxx xx xxxxxxx xxxxxx 1000 xx.xx-1 xxxxxxx xxxxxxxxx xxxx xxxxx xxxxxxx pozorovatelné xxxxxxxxxx xxxxxx x xxxxx xx xx xxxxxxx údajů x xxxxxxx s xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx, xxxx xxxxx xxxxxxx xxxxxxxxx xxxxxx xx xxxxx úrovněmi xxxxx. Xxxxx xxxxxxx test xx xxxxxxxxx, xxxxxxxxx-xx xxxxx x xxxxxxxx xxxx xxxxxxx vyšších xxxxx.
1.5.2 Aplikace
Testovaná látka xx zvířatům aplikuje 7 xxx v xxxxx po dobu 90 xxx. Xxxx xxxxx xxxxxxxx, xxxx. 5 xxx x xxxxx, xxxx být xxxxxxxxx. Aplikuje-li xx xxxxxxxxx látka xxxxxx xxxx xxxxxxx, xxxx xx xxx aplikace xxx x jediné xxxxx. Maximální objem xxxxxxxx, který xxx xxxxx xxxxxxxx, závisí xx xxxxxxx xxxxxxxxx xxxxxxx. Xxxxxxxxx xx xxxxxxx co xxxxxxxx xxxxx. X xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxxx, xxxxxxx xxxxxx xx xxxxxxxx x xxxxxxxxxxx, xx třeba xxxxxxx xxxxxxxxxx objemů xxxxxxxxxxxxx upravením xxxxxxxxxxx xxx, xxx xxx xx xxxxx xxxxxxxxx xxxxx xxxxxxx xxx xxxxx.
X látek podávaných xxxxxxxx xxxx v xxxxx xxxx xx xxxxxxxx zajistit, xxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxx normální xxxxxx xxxx xxxxx xxxxxxxxx. Xxxxxx-xx se xxxxxxxxx xxxxx x xxxxxxx, xxxx se xxxxxx xxx konstantní xxxxxxxxxxx (x ppm nebo xx.xx-1 xxxxxxx) nebo xxxxxxxxxx xxxxxxxxx ve xxxxxx x xxxxxxx xxxxxxxxx xxxxxxx; použitou xxxxxxxxxxx xx xxxxx xxxxx. Aplikuje-li xx xxxxx xxxxxx nebo x xxxxxxxx, xxxx xx xx xxxxxxx xxxxx den ve xxxxxxx dobu; xx xxxxx xxxxxxxxx xxxxxxxxx xxx, xxx xxxx xxxxxxxxxx xxxxxxxx x xxxxxx tělesné hmotnosti xxxxxxx. Je-li 90xxxxx xxxxxx xxxxxxxxxx studií x dlouhodobé xxxxxx xxxxxxxxx xxxxxxxx, xx xxx x xxxx xxxxxxxx xxxxxxx xxxxxx xxxxx.
1.5.3 Xxxxxxxxxx
Xxxx xxxxxxxxxx xx xxxxxxx 90 xxx. Xxxxxxx x xxxxxxxxx xxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxxxx xx ponechají xxxxxxx xxxx bez xxxxxxxx, xxx xx xxxxxxxxx, xxx xxxxxxx zotavení xxxx xxx xxxxxxx xxxxxx xxxxxxxxxxx.
Xxxxx xxxxxxxx xxxxxxxxxx xx třeba xxxxxxxx xxxxxxx jednou xxxxx, xxxxxxx xxxx xx stejnou denní xxxx, x xxxx xxxxxxxxxxx maximálního xxxxxx. Xxxxxxxx stav zvířat xx xxxxxxxxxxx. Xxxxxxx xxxxxxx denně, obvykle xx začátku x xx konci xxxxxxx xxx, xx provede xxxxxxxxx u xxxxx xxxxxx za účelem xxxxxxxx úmrtí x xxxxxxxx onemocnění.
Alespoň xxxxxx xxxx xxxxx xxxxxxxx xxxxx x xxxx xxxxxx xxxxx xx xxxxxxx xxxxxxxx klinické xxxxxxxxxx xxxxx xxxxxx xx účelem intraindividuálního xxxxxxxx. Pozorování xx xxxxx provádět xxxx xxxxxxx xxxx, xxxxxxx xx xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxx xx stejnou xxxx. Xx třeba zajistit, xxx se xxxxxxxx xxxxxxxxxx měnily xxxxxxxxx. Xxxxxxxx xxxxxxxx xx xxxxx xxxxxxx zaznamenávat, xxxxxx xxxx xxxxxxx, xxxxxx x trvání. Xxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxx xxxx, xxxxx, xxx x xxxxxxx, xxxxxxxxxx xxxxxxx x xxxxxxx x xxxxx xxxxxxxxxxx xxxxxx (xxxxxx, xxxxxxxxxx, xxxxxxxx xxxxxx, xxxxxxx xxxxxxx). Zaznamenávají xx xxxxx xxxxx x xxxxxx xxxx, xxxx reakce na xxxxxxxxxx, xxxxxxxxxx xxxxxxxxxx x/xxxx tonických xxxxxx, xxxxxxxxxx (xxxx. xxxxxxxx xxxxxxx, opakované xxxxxxxx) xxxx xxxxxxx chování.
Oftalmologické xxxxxxxxx oftalmoskopem xxxx xxxxxxxxxxx xxxxxxxxxx xx xx provést před xxxxxxxxx xxxxxxxxx látky x na xxxxx xxxxxx nejlépe x xxxxx xxxxxx, ale xxxxxxx u xxxxxxx x nejvyšší dávkou x x xxxxxxxxx xxxxxxx. Xxxxxx-xx se xxxx xxxxx, xxxxxxx xx všechna xxxxxxx.
1.5.3.1 Xxxxxxx hmotnost x xxxxxxxx xxxxxxx/xxxx
Xxxxxxx xxxxxxx xx xxxx xxxxxxx xxxxxx týdně. Xxxxxx xxxxxxx xx xxxxxxxx xxxxxxx jednou týdně. Xxxxxxx-xx xx aplikace x xxxxx xxxx, xxxx nejméně xxxxxx xxxxx xx xxxxxxxxx xxxxxxxx vody. Xx xxxxxxxx vody xx xxxxxxx xxxxxxxxxxx xx xxxxxxxx, xxx xx xxxxxx xxxxxxxxx látka x potravě nebo xxxxxx, xxxxx nichž xxxx xxxxx xx xxxxx příjmu xxxxxxx.
1.5.3.2 Xxxxxxxxxxx x klinická xxxxxxxxx
Xxxx xx xxxxxxx x xxxxxxxx xxxxx x xxxxxxxx se xx xxxxxxxx xxxxxxxx. Xx konci xxxxxxxxx xx vzorky xxxxxxxxx xxxxx xxxx utracením xxxx při xxx.
X xxxxxx xxxx na xxxxxxx testování x xxx x xxxxxxxxx xxxxxxxxxxx xxxx x xxxxxxxx xxxxxx a xxxx i xx xxxxx se provádí xxxxxxxxxxx xxxxxxxxxxxxx vyšetření: xxxxxxxxx hematokritu, xxxxxxxxxxx xxxxxxxxxxx, xxxxx erytrocytů, xxxxxxx a xxxxxxxxxxxxx xxxxx leukocytů, xxxxx xxxxxxxx, xxxx na xxxxxxxxxx xxxx, stanoví xx xxxxxxxxxxxxx x xxxxxxxxxx xxx.
Xxxxxxxxxxx xxxxxxx xxxxxxxx xx posouzení xxxxxxxxx xxxxxxxxx xxxxxx xx tkáně, zvláště xx ledviny a xxxxx, xx provede x xxxxxxxx xxxxxx xxxxxxxxxx xxxxxxx zvířeti xx xxxxxxx xxxxxx x x xxxxxxxxx xxxxxxxxxxx nebo v xxxxxxxx xxxxxx a xx konci xxxxxx.
Xx xxxxxx stanovit koncentraci xxxxxxxxxxx, metabolismus cukrů, xxxxxx xxxxx x xxxxxx. Xxxxx specifických xxxxx xx xxxxx xxxxxxxxxxx mechanizmu xxxxxx xxxxx. Xxxx xxxxxxx xxxx se xxxxxxxxxx xxxxxx zvířata xxxxxxx xx xxxx xxxxxxx xxx xxxx xxxx. Xxxxxxxxxx xx xxxxxxxxx xxxxxxx, fosforu, xxxxxxxx xxxxxx, xxxxxxxx, xxxxxxxx xxxxxxx, xxxxxxxxxxxxxxxxxxxxxx, aspartátaminotransferázy, xxxxxxxxxxxxxxxxxxxx, xxxxxxxxxxxxxxxxxxxxxxxxxx, dusíku xxxxxxxx, xxxxxxxx, kreatininu, xxxxxxxxx xxxxxxxxxx a xxxxxxx xxxxxxxxx x xxxx.
Xxxxxxxxx xx počátku, x xxxxxxxx x xx xxxxx xxxxxx xxxxxxx xxxxxxxxx xxxx x časově xxxxxxxxxxxx xxxxx. Hodnotí se xxxxxxxxxxx parametry: xxxxxx, xxxxx, xxxxxxxxxx nebo xxxxxxxxxx xxxxxxxx, xX, xxxxxxxxx, xxxxxxx x xxxx/xxxxxxx. X případě xxxxxxx xx mohou xxxxxx xxxxx xxxxxxx xxx xxxxxxx širšího xxxxxxx xxxxxx.
Xxxx xx xxxxx uvážit xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx. Mezi další xxxxx, které xxxxx xxx xxxxxxxx xxx xxxxx xxxxxxxxxxxxx hodnocení, xxxxx stanovení lipidů, xxxxxxx, acidobazické xxxxxxxxx, xxxxxxxxxxxxxx a xxxxxxxx xxxxxxxxxxxxxx. Xx-xx xxxxxxxxx xx xxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxxxxx, xxx přidat x xxxxx xxxxxxxx-xxxxxxxxxxx testy. Xxxxxxxx xxxxxx vyšetření xx posuzuje podle xxxxxxxxxxxx xx xxxxxxxx xxxxxx látek xxxx xxxxxx xx xxxxxxx.
Xxxxxx xx xxxxx postupovat xxxxxx, xxxx x xxxxx použitý živočišný xxxx x pozorované xx očekávané xxxxxx xxxx xxxxx.
1.5.3.3 Xxxxx
X xxxxx zvířat xxxxxxxxx xx xxxxxx xx xxxxxxx xxxxxxxx xxxxx, xxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxx xxxx, xxxxx xxxxxx a xxxxxxx, xxxxxx x xxxxxx xxxxxx a xxxxxx obsahu. Játra x žlučníkem, ledviny, xxxxxxxxxx, xxxxxxx, nadvarlata, xxxxxxxxx, xxxxxx, xxxxxx xxxxx (x příštítnými xxxxxxx), brzlík, xxxxxxx, xxxxx a srdce xxxxx xxxxxx (xxxxx xxxx, xxxxx xxxx xxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxxx) se xxxxxxx očistí xx xxxxxxxx xxxxx a xx nejdříve xx xxxxx xx xx xxxxxx stavu xxxxx, xxx xxxxxxx x xxxxxxxxx.
Xxxxxxxxxxx tkáně xx xxxxx xxxxxxxxxxx ve xxxxxxx xxxxxxxx médiu xxx xxxx typ xxxxx a plánovaná xxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx: xxxxxxx tkáně x xxxxxxxxxxxxxxx lézemi, xxxxx (xxxxxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxx mozku, xxxxxxx x xxxxxxxxxxx xxxxx), xxxxx (xx xxxxx xxxxxxxx: krční, střední xxxxxx x xxxxxxxx), xxxxxxxx, oči, xxxxxx xxxxx, xxxxxxxxx xxxxxxx, xxxxxx, xxxxx, xxxxxx xxxxx, xxxxxxx, xxxxx x xxxxxx střevo (xxxxxx Pleyerových plátů), xxxxx, xxxxxxx, xxxxxxxx xxxxxx, xxxxxxx, nadledviny, xxxxxxx, xxxxx, průdušnice x xxxxx, xxxxx, xxxxxxxx xxxxx, děloha, xxxxxxxx pohlavní xxxxxx, xxxxxx xxxxxx xxxxx, xxxxxxxx, xxxxxx měchýř, xxxxxxxxxx xxxxxx (přednostně xxxxx xxx oblast xxxxxxxx x xxxxx xxxxxxxx xxx xxxxxxx xxxxxxxxxxx xxxxxx), xxxxxxxxx xxxx (x. xxxxxxxxxxx xxxx x. xxxxxxxx) xxxxxxx x xxxxxxxxx xxxxx, řez xxxxxx xxxxx (x/xxxx čerstvý xxxxx x xxxxxx xxxxxx dřeně) x xxxx. Xxxxx klinických xxxx jiných nálezů xx xxxxx zkoumat x další xxxxx. Xxxxx orgán, který xx xxxx xxx xxxxxxx orgánem pro xxxxxxxx xxxxxxxxx xxxxx, xx xxxxx xxxxxxxxxxx.
1.5.3.4 Xxxxxxxxxxxxxxxx xxxxxxxxx
X xxxxx xxxxxx skupiny, které xxxx xxxxxx xxxxxxxx xxxxx, x x xxxxxx kontrolní skupiny xx třeba provést xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx a tkání. Xxxxx se x xxxxxxxx a xxxxxxx xx skupině x xxxxxxxx xxxxxx objeví xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx, je xxxxx xxxxxxx histologické xxxxxxxxx xxxxxx xxxxx i x xxxxx xxxxxx x nižšími dávkami.
Všechny xxxxxxxxxxxxx xxxx je xxxxx vyšetřit.
U zvířat xxxxxxxxxxx xxxxxx, pokud xxxx xx xxxxxx xxxxxxxx, xx třeba xxxxxxx histopatologické xxxxxxxxx xx zvláštním xxxxxxx xx xxxxxx x xxxxx, ve xxxxxxx xx objevily xxxxxx xxxxxx x xxxxxxxxx xxxxxxxxxxxx zvířat.
2 XXXX X XXXXXX XXXXX
2.2 Xxxxx
X xxxxxxxxx xxxx xxx údaje o xxxxxx jednotlivém zvířeti. Xxxxx xxxx xxxxxxx xxxxx sumarizovány do xxxxxxxxx xxxxx, xxxxxxxxx x každé xxxxxxxxx xxxxxxx počet xxxxxxxxx xxxxxx xx začátku xxxxx, počet xxxxxx xxxxxxxxx x xxxxxxx xxxxx xxxx xxxxxxxxxx x humánních xxxxxx, xxxx xxxxx nebo xxxxx xxxxxxxxxxxx xxxxxx; xxxxx xxxxxx vykazujících xxxxxxxx xxxxxxxx, xxxxx xxxxxxxxx xxxxxxxx xxxxxx xxxx nástupu, xxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxx, xxxxx xxxxxx xxxxxxxxxxxx xxxx, typ xxxx a procento xxxxxx x xxxxxxxxxxxx xxxx xxxx.
Xxxxxxxx v xxxxxxx xxxxx xx xxxxx xxxxxxxxxx vhodnou x uznávanou xxxxxxxxxxxx xxxxxxx. Xxxxxxxxxxxx xxxxxx xx xxxxx xxxxxx xxx xxx plánování xxxxxx.
3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX A XXXXXXXXX XXXXXX
X xxxxxxx x příslušnými xxxxxxxx xxxxxxxx
9) xxxx být xxxxxxxxx projekt xxxxxx x x xxxxxxx xxxxxx je xxxxx xxxx xxxxxxxx x xxxxxxxxxxxxx xxxxx.
Xxxxxxxxx xxxxx:
- xxxxxxxxx xxxxxx, xxxxxxx x xxxxxxxxx-xxxxxxxx xxxxxxxxxx,
- xxxxxxxxxxxxx xxxxx,
- vehikulum (xx-xx xxxxxxx): xxxxxxxxxx xxxxx xxxxxxxx, není-li xx xxxx.
Xxxxxxx xxxxxxx:
- xxxxxxx druh x xxxx,
- počet, stáří x xxxxxxx xxxxxx,
- xxxxx, podmínky xxxxx, xxxxxxx xxx.,
- xxxxxxxx xxxxxxxxxxxx xxxxxx xx xxxxxxx testu.
Podmínky xxxxx:
- xxxxxxxxxx xxxxxx xxxxxx xxxxx,
- podrobné xxxxx x úpravě xxxxxxxxx xxxxx xxx xxxxxxxx, xxxxxxxx x přípravě xxxxxxx, o xxxxxxxxxx xxxxxxxxxxxxx, xxxxxxxxx a xxxxxxxxxx xxxxxxxxx,
- xxxxxxxx xxxxx x způsobu xxxxxxxx xxxxxxxxx látky,
- xxxxxxxx x xxxxxxxxxxx xxxxx v xxxxxxx xxxx xxxx (ppm) xx xxxxxxxxx xxxxx xxxxx x xx xx xx xxxxxxx xxxxxxxxx (xxxxx jde x xxxxxxxx v xxxxxxx xxxx xxxx),
- xxxxxxxx xxxxx x xxxxxxx x kvalitě xxxx.
Xxxxxxxx
- xxxxxxx hmotnost x její xxxxx,
- xxxxxxxx xxxxxxx x xxxxxxxx vody,
- xxxxx x xxxxxxxxx xxxxxxxx xxxxx xxxxxxx a xxxxxx dávek, včetně xxxxxx xxxxxxxx xxxxxxxx,
- xxxxxx, xxxxxxxxx a xxxxxx xxxxxxxxxx xxxxxx, xxxx. xxx xxxx xxxxxx nebo xxxxxxxx,
- xxxxxxxx xxxxxxxxxxxxxxxx vyšetření,
- xxxxxxxx xxxxxxxxxxxxxxx vyšetření x xxxxxxxxxxx xxxxxxxxx (xxxxxxxxxx) hodnotami,
- xxxxxxxx xxxxxxxxxxxxx vyšetření x xxxxxxxxxxx xxxxxxxxx (normálními) xxxxxxxxx
- xxxxxxx xxxxxxxx xx xxxxx xxxxxx x xxxxxxxxx orgánů x poměry xxxxxxxxx xxxxxx k xxxxxxx xxxxxxxxx,
- xxxxxxx xxxxxx,
- xxxxxxxx xxxxx xxxxx xxxxxxxxxxxxxxxxxx xxxxxx,
- statistické xxxxxxxxxx xxxxxxxxx xxxxxxxx, xxx je xx xxxxx.
Xxxxxxx výsledků.
Závěry.
B.28 XXXXXXXXXXXX XXXXXXXX DERMÁLNÍ (90denní xxxxxxxxx xxxxxxxx, xxxxxx xx hlodavcích)
1 METODA xx v souladu x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
1)1.1 Xxxxxxx xxxxxxxxx xxxxxx
Xxxxxxxxx látka se xxxxxxxx xxxxx na xxxx xx 90 xxx x odstupňovaných xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx zvířat, a xx xxxxx skupině xxxxx xxxxxx xxxxx. Xxxxx xxxxxx xxxxxxxx xx zvířata xxxxx xxxxxxxx, xxx xx xxxxxxxx příznaky toxicity. Xxxxxxx, která xxxxxx xxxxx pokusu, i xxxxxxx, xxxxx xxxxxxx xx xxxxx xxxxxx, xx xxxxxxx.
1.2 Xxxxx xxxxxx
1.2.1 Příprava
Pokusná zvířata xxxx xxxxxxx x xxxxxxx na xxxx, xxxxxxx x xxxxx x xxxxxxx x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x xxxxxxxx tak, xxx xxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10) Xxxx xxxxxx xx xxxxxx xxxxx xxxxxxx xxxxxxx xxxxxxx xx xxxxxxxxxxxx xxxxxxxxxxxxxxxx skupin.
Krátce xxxx začátkem xxxxxx xx xxxxxxx xxxx xx xxxxxx xxxxxxxxx xxxxxx. Xxxxxxxx xxxxx xx rovněž možné, xxxx xx xx xxxx provést cca 24 xxxxx xxxx xxxxxxxxxxxx. Xxxxxxxxx nebo xxxxxxx xx xxxxxxx xxxxxxxx každý xxxxx. Xxx střihání xxxx xxxxxx xxxxx je xxxxx dbát xx xx, xxx xx xxxxxxxxxxx xxxx (např. xxxxxx). Xxx xxxxxxxx xx xxxxxxxx xxxxxxx 10 % xxxxxxx xxxx. Xx xxxxx xxxx x xxxxx xxxxxxxx xxxxxx xxx xxxxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx plochy xxxx x x xxxxxxxxx xxxxxxx xxxxxx.
Xxx pokusech x xxxxxx látkami, xxxxx mohou xxx xxxxxxxx xxxxxxxx xx xxxxxxxx xxxxx, xx xxxxx xxxxxxxxx látku xxxxxxxxxx xxxxxxxx xxxxx, xxxxxxxx vhodným xxxxxxxxx, xxx byl xxxxxxx xxxxx kontakt x xxxx. Xxxxxxxxx kapaliny xx zpravidla xxxxxxxx xxxxxxxx. Látka xx xxxxxx denně 5 xx 7 xxx x xxxxx.
1.2.2 Experimentální xxxxxxxx
1.2.2.1 Xxxxxxx xxxxxxx
Xx xxxxx xxxxxx xxxxxxx xxxxxxx, králíky nebo xxxxxxx, xxxxxxxx i xxxx zvířecí xxxxx, xxxxxx použití však xxxx být odůvodněné. Xx xxxxxxx xxxxxx xx xxxxxx xxxxxxxx xxxxxxx hmotnosti xxxxxx (xxx xxxxx pohlaví xxxxxx) překročit ± 20 % xxxxxxx xxxxxxx. Provádí-li xx xxxxxxxxxxxx xxxxxxxx test xxxx xxxxxxxxx test xxxx xxxxxxxxxxx xxxxxx, x obou xxxxxxxx xx xx xxxxxx xxxxxx živočišný xxxx x xxxx.
1.2.2.2 Xxxxx x xxxxxxx
Xxx každou xxxxxx xxxxx xxxxxx xxxxxxx 20 zvířat (10 samic a 10 xxxxx) xx xxxxxxx xxxx. Xxxxxx xxxx být xxxxxxxxx x xxxxx xxx xxxxx. Xxxxx xx xxxxxxx xxxxx zabíjet x průběhu xxxxxx, xx xxxxx xxxxxx xxxxxxx xxxxx xxxxxx x xxxxx xxxxxx, xxxxx xxxxx zabita xxxx xxxxxx xxxxxx. Xxxxxx xx xxxxx xxxxxxx xxxxx xxxxxxx (xxxxxxxxx skupině) s 20 zvířaty (10 xxxxxx xxxxxxx xxxxxxx) xx xxxx 90 xxx xxxxxxxx xxxxx x xxxxx xxxxxxxxxxxxx 28 xxx xx xxxxxxxx sledovat xxxxxxxx, xxxxxxxxxxx xxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxx.
1.2.2.3 Xxxxxxxxx
Xx xxxxx xxxxxx xxxxxxx 3 xxxxxxx xxxxx x 1 xxxxxxxxx xxxxxxx xxxx - xxxxx se xxxxxxx xxxxxxxx - xxxxxxxxx skupinu s xxxxxxxx vehikula. Xxxx xxxxxxxx xx být xxxxxxx 6 hodin xxxxx. Xxxxxxxx xxxxxxxxx xxxxx xx xx xxxx provádět xxxxx xxx xx xxxxxxx xxxx. X intervalech xxxxxxxxx xxxx xxxxxxxxxxxxxxx xx xxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxxx tak, xxx xx xxxxxxxxx xxxxx xxxxxxx dávky xx xxxxxx x xxxxxxx xxxxxxxxx xxxxxxx. X xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xx xx xxxxxxx x xxxxxxxxx skupině xxxxxxx xxxxxx xxxx x xxxxxxxxx. Používá-li xx xxxxxxxxx pro usnadnění xxxxxxxx, podává se xxxxxxxxx xxxxxxx xxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxx, x to xx xxxxxxx množství, xxxxx xxxxxx xxxxxxx, xxxxx se xxxxxxxx xxxxxxxx xxxxx.
Xxxxxxxx hladina xxxxx xx xxxxxxx xxxxxxx xxxxxx, xxx xxxxxxxxxx xxxxx xxxxxxx xxxx xxx v xxxxx xxxxx. Xxxxxxxx xxxxxxx dávky xx xxxxxx xxxxxxx žádné xxxxxxxx xxxxxxxx. Xxxxx xxxxxxxx xxxxxx expozice x člověka, xx xxxxxxxx xxxxx xxxx xxxxxxx xxxxxxxxxxx. Xxxxxxx xx xxxxxxx xxxxxxx xxxxx měla xxxxxxx xxx xxxxxxx účinek xx xxxxxxxxx zjistitelnosti. Xxxxxxxx-xx xx xxxx xxx 3 xxxxxxx xxxxx, xxxx xxx xxxxxxxxx dávky xxxxxx xxx, aby vyvolaly xxxxxxxxxxxx xxxxxxx xxxxxx. Xx xxxxxxx x xxxxxx a xxxxxxx xxxxxxxx dávky a x kontrolní xxxxxxx xx xxxxx xxxxxxx xxx být xxxxx, xxxxx xx xxxxxxxxxxx xxxxxxxx xxxxxxx.
Xxxx-xx xxxxxxxx xxxxxxxxx xxxxx x xxxxxxx xxxxxxxxxx xxxx, xx xxxxx snížit xxxxxxxxxxx, xxx x xxxxxx dávkové xxxxxxx xxxx xxxx x xxxxxxx xxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx. Xxxxx-xx x těžkému xxxxxxxxx xxxx, je xxxxxxx xx xxxxxxxx xxxxxxxxx xxxxx pokus xxxxxxx x xxxxxxx xxx xxxxx s xxxxxxx xxxxxxxxxxxxx.
1.2.2.4 Xxxxxxx xxxx
Xxxxxxxx-xx xxx xxxxxxxxx xxxxxx xxxxxxxx dávky 1000 xx.xx-1 xxxx xxxxx dávky, která xxxxxxxx možné xxxxxxxx xxxxxxx, xxxxx xxxxxxx xxxxxx, není další xxxxxxx xxxxx.
1.2.2.5 Xxxx xxxxxxxxxx
Xxxxxxx zvířata xx xxxxx denně xxxxxxxxx x zaznamenávat xxxxxxx xxxxxx. Je xxxxx xxxxxxxxxx xxxx uhynutí x xxx, ve xxxxxx xx objeví x opět xxxxxx xxxxxxx xxxxxx.
1.2.3 Popis xxxxxxx
Xxxxxxx xx xxxxxxx x klecích xx xxxxxx. Xxxxxxxx xx xxxxxxxxx látce nejlépe 7 dnů v xxxxx xx xxxx 90 xxx. Xxxxxxx xxxxxxxxx xxxxxxx, která xxxx určena xxx xxxxxxxx pozorování, je xxxxx chovat xx xxxxxxx 28 xxx xxx xxxxxxxx, xxx xx xxxxx pozorovat xxxxxxxx xxxxxxxxx účinků xxxx xxxxxx přetrvávání. Xxxx xxxxxxxx činí xxxxxxx 6 hodin xxxxx.
Xxxxxxxxxx xxxxx je xxxxx nanášet rovnoměrně xx xxxxx xxxxxx, xxxxx xxxxxxxxxxx xxx 10 % xxxxxxx xxxx, x xxxxxx xxxxxxxxx xxxxx může xxx xxxx plocha xxxxx. Xxxxxx xx xxxxx xxxxxx xx xxxxxxxx xxxx pokusné xxxxxx rovnoměrně v xx nejtenčí xxxxxx.
Xxxxxxxxx xxxxx xx po xxxxxxxxx xxxx udržována x kontaktu s xxxx pomocí xxxxxxxxx xxxxxxxx obvazu x xxxxxxxxxx xxxxxxxx. Xxxxxxxxx xxxxxx je dále xxxxx xxxxxxx xxxxxxxx xxxxxxx, xxx xx xxxxxx xxxxx a xxxxxxxxx xxxxx xxxxxxxx x xxx xx xxxxxxxxx xxxxxxxx xxxxxx. X zamezení xxxxxx xxxxx xx možno xxxxxx i xxxxxxxxxx xxx omezení xxxxxxxx xxxxxx, xxxxxx imobilizaci xxxx nelze doporučit.
Po xxxxxxxx xxxx xxxxxxxx xx xxxxxxxx xxxxxx xxxxxxxxx látky xxxxx xxxx xxxxx xxxxxxxx xxxxxxx k xxxxxxxx xxxxxxx.
Xxxxxxx xxxxxxx xx xxxxx denně xxxxxxxxx x xxxxxxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxx, stupně x xxxxxx.
Xxxxxxxxxx x kleci xxxxxxxx xxxxx srsti, xxxx, xxx x xxxxxxx a také xxxxxxx x xxxxxxxx xxxxx, xxxxx funkce xxxxxxxxx x centrální xxxxxxx xxxxxxxx, xxxxxxxxxxxxxxx xxxxxxxx x xxxxxxx. Xxxxxxxxx xxxxxx xx xxxxxxxxxxxxx xxxxx. Xxxxxxxxxx xx xxxxxxxxxxxx xxxxx x xxxxxxxx xxxxxxx. Xx třeba xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxxx, xxx xxxxx xxxxx xxxxxxxxxxx xx xxxxxxx xxxxxx xxxx xxxxxxxxx x xxxxxxxx xxxxxxxxxxx, xxxxxxxx xxxxx nebo xxxxxxxx xxxxxxxx. Xx xxxxxxxx studie xx xxxxxxx xxxxxxx, která xxxxxxx, s xxxxxxxx xxxxxxxxxxx xxxxxx, pitvají. Xxxxxxx v xxxxxx, xxxxxxx x xxxxxx xxxxxx xx xxxxxx xxxxxxx je xxxxx xxxxxxxx xxxxxxx, humánně xxxxxxx x xxxxxx.
X xxxxx xxxxxx xxxxxx xxxxxxxxxxx xx běžně xxxxxxxxx xxxxxxxxxxx vyšetření:
(a) Xxxxxxxxxxxxxx vyšetření oftalmoskopem xxxx rovnocenným xxxxxxxxxx xx má xxxxxxx xxxx xxxxxxxxx testované xxxxx x xx xxxxx xxxxxx xxxxxxx x xxxxx zvířat, xxx xxxxxxx u xxxxxxxx xxxxx x x xxxxxxxxxxx skupin. Xxxxxx-xx se oční xxxxx, xxxxxxx xx xxxxxxx xxxxxxx.
(x) Xx xxxxx xxxxxx xx xx xxxxxxx hematologické xxxxxxxxx, xxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx, xxxxxxxxxxx xxxxxxxxxxx, xxxxx xxxxxxxxxx, celkového a xxxxxxxxxxxxxxx xxxxx xxxxxxxxx x xxxxx xxxxxxxxxxx xxxx xxxx xxxxxxxxx xxxx xxxxxxxxxxx, protrombinový xxx (Xxxxxxx), xxxxxxxxxx xxx xx počet xxxxxxxxxx.
(x) Xx konci xxxxxx se xx xxxxxxx xxxxxxxxxxx xxxxxxx xxxx. Pro všechny xxxxxx je xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx, xxxxxxxxxxxx xxxxxxx, funkci xxxxx x xxxxxx. Xxxxx specifických xxxxx xx xxxxx xxxxxxxxxxx xxxxxxx xxxxxx látky. Xxxxxxxxxx se stanovovat xxxxxx, fosfor, xxxxxxxx, xxxxx, xxxxxxx, xxxxxxx xxxxxxx (xxxxxxx xxxxxx xxxx xxxxxxxxx xx xxxx xxxxx živočišného xxxxx), alaninaminotransferáza (xxxxx xxxxxxxx- xxxxxxx xxxxxxxxxxxx) x xxxxxxxxxxxxxxxxxxxxxxxx xxxx (xxxxx xxxxxxxx-xxxxxxxxxxxxxxxxxxxxxx), ornithindekarboxyláza, xxxx-xxxxxxxx xxxxxxxxxxxxxx, dusík xxxxxxxx, xxxxxxx, xxxxxxxxx, xxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxx x xxxx. Mezi xxxxx xxxxxxxxxxxxxxx, které mohou xxx xxxxxxxx pro xxxxx toxikologické xxxxxxxxx, xxxxx stanovení: xxxxxx, xxxxxxx, xxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxxxxxx, aktivity cholinesterázy. Xxxxx biochemické analýzy xxxxx xxx x xxxxxxx potřeby xxxxxxx xxx xxxxxxx xxxxxxx xxxxxxx účinků.
(d) Xxxxxxx xxxx se nevyžaduje xxxx xxxxx xxxxxx, xxx xxx xx xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxx xxxxxxxx.
Xxxxx nejsou xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxx, xx se xxxxxx xxxxxxxxx hematologických x xxxxxxxxxxxxx xxxxxxxxx xxxxx xxxx začátkem xxxxxxxx.
1.2.3.1 Pitva
U všech xxxxxx xxxxxxxxx ve xxxxxx se xxxxxxx xxxxx xxxxxxxxxx xxxxx xxxxxxxxx povrchu xxxx, xxxxx xxxxxxx xxxxxx, xxxxx, xxxxxx x xxxxxx xxxxxx xxxxxx xxxxxx xxxxxx. Xxxxx, xxxxxxx, xxxxxxxxxx, xxxxxx xxxxx (s xxxxxxxxxxx xxxxxxx) a varlata xx xx nejdříve xx sekci xxxxx xx xxxxxx xxxxx, xxx xx předešlo xxxxxxxxx.
Xxxxxxxxxxx orgány x xxxxx xx xxxxx xxxxxxxxxxx xx vhodném xxxxx s xxxxxxx xx xxxxx xxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx: xxxxxxx xxxxx x xxxxxxxxxxxxxx xxxxxxxxxx, mozek - x řezech medula/pons, xxxx xxxxx x xxxxxxx, xxxxxxxx mozkový, xxxxxx žláza, xxxxxxxxx xxxxxxx, tkáň xx xxxxx xxxxxxx, (xxxxxxxxxx), xxxxx, xxxxx, xxxxx, (xxxxxx xxxxx), xxxxx, xxxxxxx, xxxxxxx, xxxxxxxxxx, xxxxxxxx xxxxxx, xxxxxxx x xxxxxxxxx, xxxxxx, xxxxxxxx xxxxxxxx xxxxxx, xxxxxxx (je-li xxxxxxxx), xxxxx, žaludek, xxxxxxxxxxxx, xxxxx, xxxxxx x xxxxx xxxxxx, konečník, xxxxxx xxxxxx, reprezentativní xxxxxxxxxx xxxxxx, (xxxxxx xxxxxx xxxxx), (xxxxxxxx xxxx), periferní nerv, (xxx), (xxxxxx kost x kostní xxxxx), (xxxx xxxxxxxx xxxxxx xxxxxxxxx ploch), (páteřní xxxxx xx xxxxx xxxxxxxx - xxxxx, xxxxx xxxxxx x xxxxxxx), x (slzné xxxxx). Xxxxx v xxxxxxxxx xx xxxxxxxx, xxxxx je to xxxxxxxxxx xxxxx příznaků xxxxxxxx xxxx xxxxx xxxxxxxxx s cílovým xxxxxxx.
1.2.3.2 Xxxxxxxxxxxxxxxx xxxxxxxxx
(x) Xxxxx histopatologické xxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxx, xxxxxx x xxxxx xx třeba xxxxxxx x všech xxxxxx xxxxxxx, xxxxx xxxx xxxxxx nejvyšší xxxxx, x x xxxxxx kontrolní xxxxxxx.
(x) Xx třeba xxxxxxxx xxxxxxx xxxxxxxxxxxxx xxxxxxxxx.
(x) Xx třeba xxxxxxxx xxxxxx orgány x xxxxxxxxx dávkových xxxxxxxxx.
(x) Xxxxxxx-xx xx potkanů, xxxxx xxxxxx xx xxxxxxxxx s xxxxxx x střední xxxxxx xx xxxx histopatologicky xxxxxxxxxx x zjištění xxxxxxxx xxxxxxx, protože xx poskytuje obraz xxxxxxxxxxx xxxxx zvířat. Xxxxx histopatologická xxxxxxxxx xx u zvířat xxxxxx xxxxxx xxxxxx xxxxxxxx xxxxxxx, xxxx xx však xxxxxxx xxxx na xxxxxxxx, xx xxxxxxx bylo xxxxxxxx postižení xx xxxxxxx s xxxxxxx xxxxxx.
(x) Xxxxxxx-xx se xxxxxxxxx xxxxxxx, xxxx xx xxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx xx tkáních x orgánech, x xxxxxxx xxxx xxxxxxxx xxxxxx u ostatních xxxxxxxxxxxx xxxxxx.
2 XXXXX
Xxxxx xx xxxxxxx xx xxxxxxx. Z xx xxxx xxx pro xxxxxx experimentální skupinu xxxxxx počet xxxxxx xx xxxxxxx xxxxxx x počet xxxxxx x xxxxxx x xxxxxxxxxxxx xxxxx xxxxxx x xxxxxxxxxxxx xxxx xxxx. Xxxxxxxx je xxxxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxx. Xx x tomu možno xxxxxx kteroukoliv xxxxxxxxx xxxxxxxxxxxx metodu.
3 PROJEKT XXXXXX, PROTOKOL XXXXXX X XXXXXXXXX ZPRÁVA
V xxxxxxx x příslušnými xxxxxxxx xxxxxxxx
9) xxxx xxx zpracován xxxxxxx xxxxxx x x xxxxxxx pokusu xx xxxxx xxxx xxxxxxxx.
Xxxxxx x xxxxxxx pokusu xx xxxxx xxxxx xxxxxxxxx xxxx xxxxxxxxx
- xxxxxxxxx xxxx, xxxx, xxxxx, podmínky xxxxxxxx, xxxxxx,
- podmínky xxxxxx,
- xxxxxx xxxxx (včetně xxxxxxxx, pokud xx xxxxxxx) a xxxxxxxxxxx,
- xxxxx x toxických xxxxxxxxxx xxxxx xxxxxxx x xxxxx xxxxx,
- xxxxxxx xxx xxxxxx, xxxxx xx xxx xxxxxxxx,
- xxxx xxxxxxx xxxxx xxxxxxxxxxx, xxxxxxxx xxxx o přežití xxxxxx xx konce xxxxxxxxx,
- xxxxx toxických xxxx xxxxxx účinků,
. xxxx, kdy byly xxxxxxxxxx jednotlivé xxxxxxxxxx xxxxxxxx x jejich xxxxx xxxxx,
- xxxxxxxx xxxxxxx x vývoj xxxxxxx xxxxxxxxx,
- xxxxxxxxxxxxxx xxxxxx,
- xxxxxxxxxxxxx xxxxxxxxx x xxxxxx xxxxxxxx,
- xxxxxxxxxxx xxxxxxxxx x xxxxxx výsledky (včetně xxxxxxxx xxxxxxxxxx xxxxxx xxxx),
- xxxxxxx xxxxxx,
- xxxxxxxx xxxxx všech xxxxxxxxxxxxxxxxxx xxxxxx,
- xxxxxxxxxxx xxxxxxxxxxx výsledků, xxx xx to xxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.29 SUBCHRONICKÁ TOXICITA - XXXXXXXXX (90xxxxx xxxxxxxxx inhalační xxxxxxxx, xxxxxx na xxxxxxxxxx)
1 XXXXXX xx x xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
1)1.1 Xxxxxxx xxxxxxxxx xxxxxx
Xxxxxxx xxxxxx xxxxxxxxx xxxxxx xx xxxxxxxxxx xxxxxxxxx xxxxx xxxxx po určitou xxxx, x xxxxxxxxxxxxxx xxxxxxxxxxxxx, xxxxx skupina xxxxx xxxxxxxxxxx, a xx xx 90 xxx. Xxxxxxx-xx xx xxx xxxxxxxx potřebné xxxxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxx vehikulum, xx třeba xxxxxx xxxxxxxxx skupinu pro xxxxxxxxx. Během trvání xxxxxx xx zvířata xxxxx xxxxxxxx x xxxxxxxx se xxxxxxxx xxxxxxxxx xxxxxx. Xxxxxxx, xxxxx xxxxx pokusu xxxxxx, x xx, xxxxx xxxxxxx do xxxxx pokusu, xx xxxxxxx.
1.2 Xxxxx xxxxxx
1.2.1 Xxxxxxxx
Xxxxxxx xxxxxxx jsou xxxxxxx x ohledem xx xxxx, xxxxxxx x xxxxx v xxxxxxx x xxxxxxxxxxx
§15 zvláštního xxxxxxxx xxxxxxxx
10) x xxxxxxxx xxx, xxx byla xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Dobu xxxxxxxx xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10) Před xxxxxx xx xxxxxx xxxxx xxxxxxx náhodně xxxxxxx xx jednotlivých xxxxxxxxxxxxxxxx xxxxxx. Pokud xx xxxxx, xxxxx xx x xxxxxxxxx xxxxx xxxxxx xxxxxxxxx xxx, xxx x xxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxx testované xxxxx. Xxxxx se xxxxx xxx xxxxxxxxx xxxxxxxx xxxxxxxxx xxxx xxxx xxxxxxx, xxxx být x nich známo, xx nemají xxxxxxx xxxxxx. Xxxxxxxx-xx xxxxxx xxxxxxxxxx data, xx xxxxx xx využít.
1.2.2 Xxxxxxxxxxxxxx xxxxxxxx
1.2.2.1 Xxxxxxx xxxxxxx
X pokusech xx xxxxxxxxxxxxx xxxxxxx, nejsou-li xxxxx xxxxxx xxxxx xxxxxx xxxxxxx. Xxxxxxx xx na xxxxxxx xxxxxxxx xxxxxxxxx z xxxxx xxxxxxxxx xxxxxxxxx xxxxx. Xx xxxxxxx xxxxxx nemá xxxxxxxx xxxxxxx hmotnosti xxxxxx xxxxxxxxx ± 20 % xxxxxxx xxxxxxx. Xxxxxxx-xx se subchronický xxxxxxxxx xxxx xxxx xxxxxxxxx test před xxxxxxxxxxx xxxxxx, x xxxx xxxxxxxx xx xx xxxxxx xxxxxx xxxx x kmen.
1.2.2.2 Xxxxx x pohlaví
Pro xxxxxx úroveň xxxxxxxxxxx xx třeba použít xxxxxxx 20 zvířat (10 samic x 10 xxxxx). Xxxxxx xxxx být xxxxxxxxx x nesmí xxx xxxxx. Xxxxx xx xxxxxxx xxxxx zabíjet x xxxxxxx studie, xx xxxxx zvýšit xxxxxxx počet xxxxxx x počet xxxxxx, xxxxx xxxxx xxxxxx xxxx xxxxxx xxxxxx. Xxxxxx je xxxxx xxxxxxxxx další xxxxxxx (xxxxxxxxx xxxxxxx) 20 xxxxxx (10 zvířat xxxxxxx pohlaví) po xxxx 90 xxx xxxxxxxx koncentraci x xxxxx xxxxxxxxxxxxx 28 xxx po xxxxxxxx xxxxxxx xxxxxxxx vratnost, xxxxxx xxxx xxxxxxxx xxxxxx xxxxxxxxx xxxxxx.
1.2.2.3 Xxxxxxxxx koncentrace
Použijí se xxxxxxx 3 skupiny x xxxxxx úrovní xxxxxxxxxxx x 1 xxxxxxxxx skupina (xxxxxxxx xxxxxxxxx xxxxxxx s xxxxxxxxx - pokud xx xxxxxxx - x koncentraci xxxxxx xxxx u xxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx). S xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx se xx xxxxxxx x xxxxxxxxx xxxxxxx zachází xxxxxx xxxx x pokusnými. Xxxxxxxx xxxxxxxxxxx má xxxxxxx xxxxxxx účinky, xxx xxxxxxxxxx xxxxx xxxxxxx xxxx xxx x malém xxxxx. Xxxxx xxxxxxxx xxxxxx xxxxxxxx x člověka, xx xxxxxxxx xxxxxxxxxxx xxxx xxxxxxx xxxxxxxxxxx. Xxxxxxx by xxxxxxx xxxxxxxxxxx xxxx vyvolat xxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx. Xxxxxxxx-xx xx xxxx než 3 xxxxxx xxxxxxxxxxx, xxxx xxx xxxxxx xxx, xxx vyvolaly xxxxxxxxxxxx toxické xxxxxx. Xx xxxxxxx x xxxxxx x xxxxxxx xxxxxxxxxxx x x xxxxxxxxx skupině by xxxxx xxxxxxx xxx xxx nízký, jinak xx xxxxxxxxxxx xxxxxxxx xxxxxxx.
1.2.2.4 Xxxxxx expozice
Zvířata xx xxxxxxxx xx xxxx 6 hodin xx xxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx. X xxxxxxx xxxxxxxxxxxx xxxxxxxxx je xxxxx xxxxxx i jiných xxx xxxxxxxx.
1.2.2.5 Xxxxxxxxx xxxxxxxx
Xxx xxxxxxxx zvířat xx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxx xxxxxxxx proudění vzduchu x xxxxxxx xxxxxxx 12 xxxx xx xxxxxx, xxx byl xxxxxxx přiměřený xxxxx xxxxxxx a xxxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxx atmosféře. Xxxxxxx-xx xx xxxxxxxxx xxx, xx třeba ho xxxxxxxxxxx xxx, xxx xx nejvíce xxxxxx xxxxxxxxxxx xxxxxx x xxx xxxxxxxxx expozice xxxxxxxxx xxxxx byla xx xxxxxxxx. Xxx xxxxxxxxx stability xxxxxxxxx x xxxxxxxxxx boxu xxxxx xx x xxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxx přesáhnout 5 % xxxxxx xxxx. Je možné xxxxxx inhalační expozice xxxxxx-xxxxxxx, xxxxxxx hlavy xxxx individuální xxxxxxxxxx xxxxxxxx; první xxx xxxxxxx xxxxxxxx minimalizují xxxxxx látky xxxxxx xxxxxxx.
1.2.2.6 Xxxx xxxxxxxxxx
Xxxxxxx xxxxxxx xx xxxxx xxxxx xxxxxxxxx během xxxxxx xxxxxx xxxxxxx x xxxxxxxx x xxxxxxxxxxxx xxxxxxx účinky. Xx třeba zaznamenat xxxx uhynutí a xxx, xx xxxxxx xx xxxxxx x xxxx xxxxxx xxxxxxx xxxxxx.
1.2.3 Xxxxx xxxxxxx
Xxxxxxx xx xxxxxxxx testované xxxxx denně, 5 - 7 xxx x xxxxx, xx xxxx 90 xxx. Xxxxxxx x xxxxxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxx x xxxxxxxxxx xxxxxxxxxx, xxxx xxxxxxxxxx xxxxxxx 28 xxx xxx xxxxxxxx, x xxxxxxxxx zotavení x xxxxxx nebo přetrvávání xxxxxxxxx xxxxxx. Xxxxxxx xxxxx experimentu má xxx 22 °X ± 3 °C. Xxxxxxxxx vlhkost xx xxx xxxx 30 % x 70 %, s xxxxxxxx xxxxxxx, xxx to xxxx xxxxx (např. xxxxxxxxxxx x xxxxxxxx). Xxxxx xxxxxxxx se xxxxxxxx xxxxxxx xxx xxxx.
Xxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxx x xxxxxxx xxxxxxxxxxx kontrolou xxxxxxxxxxx. Doporučuje se xxxxxxx xxxxxxxxx pokus xxx xxxxxxx xxxxxxxxxx xxxxxxxxxxx. Xxxxxxxx průtoku xxxxxxx xx třeba xxxxxxxx xxx, xxx xxxxxxxx x celém xxxxxxxxxx xxxx xxxx xxxxxx. Xxxxxx xxxx xxxxxxxxx, xx stabilních xxxxxxxx xxxxxxxx xxxx xxxxxxxx co nejrychleji.
Měření xxxx monitorování xxxxxxxx xxxxxxxx:
x) Měření průtoku xxxxxxx (xxxxxxxxxxx).
x) Xxxxxxxx xxxxxxxxxxx studované xxxxx xx xxxx v xxxxxxx zóně. Během xxxxx xxxxxxxx xx xxxx xxxxxxxxxxx xxxxxxxxxx xx xxxxxxx xxxxxxx x xxxx xxx ± 15%.
U xxxxxxxxx xxxxxx x aerosolů, xxx xxxx xxxxxx xxxxxxxx xxxx možné xxxxxxxxx, xx xxxxxxxxx xxxxx xxxxxx kolísání. Xx xxxxx dobu xxxxxx experimentu xxxx xxx xxxxxxxxxxx xxx xxxxxxxx, jak je xx xxxxxxxxx možné. Xxx vývoji xxxxxxxxxx xxxxxxxx xx xxxxx xxxxxxxxxx velikostí xxxxxx xxx, xxx byla xxxxxxx xxxxxxxxx x xxxxxxxxx. Xxxxx expozic xx měří tak xxxxx, xxx xx xx xxxxxxx xxx xxxxxxxxx stálosti xxxxxxxxxx xxxxxxxxx xxxxxx.
x) Xxxxxxx x xxxxxxx xxxxxxx
x) Xxxxx xxxxxxxx x xx ní xx xxxxxxx xxxxxxxxxxxx pozorují x xxxxxxxx xx xxxxxxxxxxxxx; xxxxx zvíře xx xxxx xxxxxxxxxxxx xxxxxxxx. Xxxxxxx zvířata xx třeba denně xxxxxxxxx na xxxxxxxx xxxxxxxxx účinků x xxxxxxxxxxxx xxxxxx nástup, xxxxxx x trvání. Xxxxxxxxxx x kleci xxxxxxxx xxxxx xxxx, xxxxx, xxx, sliznic, xxxxxxx x krevního xxxxx, xxxxx xxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxx xxxxxxxx, somatomotorické xxxxxxxx x chování. Xxxxxxxxx xxxxxx x xxxxxxxx xxxxxxx xx xxxxxxxxxxxxx xxxxx. Xx xxxxx xxxxxxxx pravidelnou xxxxxxxx xxxxxx, xxx xxxxx možno xxxxxxxxxxx xx xxxxxxx xxxxxx xxxx xxxx. v xxxxxxxx xxxxxxxxxxx, xxxxxxxx xxxxx nebo xxxxxxxx xxxxxxxx. Xx xxxxxxxx xxxxxx xx xxxxxxx xxxxxxx, xxxxx xxxxxxx, xxxxxxx. Umírající zvířata xx xxxxx xxxxxxx x xxxxxx.
X xxxxx xxxxxx xxxxxx xxxxxxxxxxx xx xxxxx provádějí xxxxxxxxxxx vyšetření:
(a) Xxxxxxxxxxxxxx xxxxxxxxx oftalmoskopem nebo xxxxxxxxxxx xxxxxxxxxx xx xx provést xxxx xxxxxxxxx testované látky x xx konci xxxxxx xxxxxxx x xxxxx zvířat, xxx xxxxxxxxxxxx x nejvyšší xxxxx x x xxxxxxxxxxx xxxxxx. Najdou-li xx xxxx xxxxx, xxxxxxx xx všechna xxxxxxx.
(x) Xx konci xxxxxx xx xxxxxxx xxxxxxxxxxxxx xxxxxxxxx, které xx xxxxxxxxx xxxxxxxxx xxxxxxxxxxx, xxxxxxxxxxx hemoglobinu, xxxxx xxxxxxxxxx, xxxxxxxxx x xxxxxxxxxxxxxxx xxxxx xxxxxxxxx x xxxxx xxxxxxxxxxx xxxx jako xxxxxxxxx xxxx xxxxxxxxxxx, xxxxxxxxxxxxx čas (Xxxxxxx), xxxxxxxxxx čas či xxxxx xxxxxxxxxx.
(x) Na xxxxx xxxxxx xx xxxxxxx xxxxxxxxxxx analýza xxxx. Xxx xxxxxxx xxxxxx xx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxx, xxxxxxxxxxxx xxxxxxx, xxxxxx xxxxx x xxxxxx. Xxxxx xxxxxxxxxxxx xxxxx xx určen xxxxxxxxxxx xxxxxxx účinku xxxxx. Xxxxxxxxxx xx xxxxxxxxxx xxxxxx, xxxxxx, xxxxxxxx, xxxxx, xxxxxxx, glukózu xxxxxxx (trvání xxxx xxxxxxxxx xx volí xxxxx živočišného xxxxx x xxxxx), xxxxxxxxxxx xxxxxxxxxxx (xxxxx xxxxxxxx- xxxxxxx xxxxxxxxxxxx) x xxxxxxxxxxxxx xxxxxxxxxxx séra (xxxxx glutamát-oxalacetát xxxxxxxxxxxx), xxxxxxxx dekarboxyláza, gama-glutamyl xxxxxxxxxxxxxx, xxxxx xxxxxxxx, xxxxxxx, xxxxxxxxx, xxxxxxx xxxxxxxxx x xxxxxxx xxxxxxxxx v xxxx. Xxxx xxxxx xxxxxxxxxxxxxxx, xxxxx mohou xxx xxxxxxxx xxx xxxxx xxxxxxxxxxxxx xxxxxxxxx, patří xxxxxxxxx: xxxxxx, hormonů, xxxxxxxxxxxx xxxxxxxxx, methemoglobinu, xxxxxxxx xxxxxxxxxxxxxx. Xxxxx xxxxxxxxxxx analýzy mohou xxx v případě xxxxxxx použity pro xxxxxxxxx xxxxxxx pozorovaných xxxxxx.
(x) Analýza moče xx xxxxxxxxxx jako xxxxx postup, xxx xxx xx xxxxxxxx xxxxxxxxx nebo xxxxxxxxxx xxxxxxxx.
Xxxxx xxxxxx xxxxxxxxx xxxxxxxx kontrolní xxxx, xxxxx xx xxxxxxxxx xxxxxxxxxxxxxxx x xxxxxxxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxx xxxxxxx.
1.2.3.1 Xxxxx
X xxxxx xxxxxx xxxxxxxxx xx studii xx xxxxxxx xxxxx xxxxxxxxxx xxxxx prohlídku xxxxxxx xxxx, xxxxx tělních xxxxxx, lební, xxxxxx x xxxxxx xxxxxx x xxxxxx obsahu. Xxxxx, xxxxxxx, xxxxxxxxxx, xxxxxx xxxxx (s xxxxxxxxxxx xxxxxxx) x xxxxxxx xx co xxxxxxxx po xxxxx xxxxx xx xxxxxx xxxxx, xxx xx xxxxxxxx xxxxxxxxx.
Xxxxxxxxxxx xxxxxx x xxxxx xx xxxxx xxxxxxxxxxx ve xxxxxxx médiu x xxxxxxx na xxxxx xxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx: xxxxxxx xxxxx s xxxxxxxxxxxxxx xxxxxxxxxx, plíce (xxxx se xxxxxxx xxxxxxxxxx, zvážit x xxxxxxx xxxxxxx xxxxxx, xxx xxx xx xxxxxxxxx xxxxxxxxx xxxx - perfuzní xxxxxx xx xxxxxxxx xx xxxxxxx), tkáň nasofaryngu, xxxxx - x xxxxxx medula/pons, xxxx xxxxx a xxxxxxx, xxxxxxxx, štítná xxxxx/xxxxxxxxx xxxxxxx, tkáň xx xxxxx xxxxxxx, xxxxxxxxxx, xxxxx, xxxxx, xxxxxx xxxxx, xxxxx, xxxxxxx, xxxxxxx, xxxxxxxxxx, slinivka xxxxxx, xxxxxxx a xxxxxxxxx, xxxxxx, (xxxxxxxx xxxxxxxx xxxxxx), (xxxx), xxxxxxx (xx-xx přítomen), xxxxx, xxxxxxx, dvanácterník, xxxxx, xxxxxx a xxxxx xxxxxx, xxxxxxxx, xxxxxx xxxxxx, xxxxxxxxxxxxxxx xxxxxxxxxx xxxxxx, (xxxxxx xxxxxx žláza), (stehenní xxxx), xxxxxxxxx xxxx, (xxx), xxxxxx kost x xxxxxx xxxxx, (xxxx xxxxxxxx xxxxxx xxxxxxxxx ploch), (xxxxxxx xxxxx ve třech xxxxxxxx - xxxxx, xxxxx hrudní x xxxxxxx). Xxxxx x xxxxxxxxx xx xxxxxxxx, xxxxx xx xx xxxxxxxxxx, xxxxx příznaků xxxxxxxx nebo xxxxx xxxxxxxxx x cílovým xxxxxxx.
1.2.3.2 Xxxxxxxxxxxxxxxx vyšetření
(a) Xxxxx histopatologické vyšetření xxxxxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxx x xxxxx xx třeba xxxxxxx x xxxxx xxxxxx skupiny, která xxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx, x x xxxxxx kontrolní xxxxxxx.
(x) Xx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxxx xxxx.
(x) Xx xxxxx xxxxxxxx xxxxxx xxxxxx v xxxxxxxxx xxxxxxxxx skupinách.
(d) Xxxxx xxxxxx xx xxxxxxxxx s xxxxxx x xxxxxxx koncentrací xx xxxx xxxxxxxxxxxxxxxx xxxxxxxxxx, xxxxxxx xx xxxxxxxxx xxxxx xxxxxxxxxxx xxxxx zvířat. Xxxxx xxxxxxxxxxxxxxxx xxxxxxxxx se x xxxxxx těchto xxxxxx nemusí xxxxxxxx xxxxxxx, xxxx xx xxxx provést vždy xx xxxxxxxx, xx xxxxxxx bylo xxxxxxxx xxxxxxxxx xx xxxxxxx x xxxxxxx koncentrací.
(e) Xxxxxxxxx-xx xx xxxxxxxxx xxxxxxx, xxxxxxx xx xxxxxxxxxxxxxxxx xxxxxxxxx xx xxxxxxx a xxxxxxxx, x xxxxxxx xxxx xxxxxxxx xxxxxx x xxxxxxxxx exponovaných skupin.
2 XXXXX
Xxxxx xx sestaví xx tabulky. Z xx xxxx xxx xxx xxxxxx experimentální xxxxxxx xxxxxx počet xxxxxx xx xxxxxxx xxxxxx x xxxxx xxxxxx s lézemi, xxx xxxx a xxxxxxxxxxxx počet zvířat x jednotlivými xxxx xxxx. Xxxxxxxx je xxxxx vyhodnotit xxxxxxx xxxxxxxxxxxx xxxxxxx. Xx x tomu xxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx metodu.
3 PROJEKT XXXXXX, PROTOKOL XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx s xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) musí xxx zpracován xxxxxxx xxxxxx x x xxxxxxx xxxxxx xx xxxxx vést xxxxxxxx.
Xxxxxx x xxxxxxx xxxxxx xxxxxxxx tyto xxxxxxxxx:
- xxxxxxxxx xxxx, xxxx, xxxxx, xxxxxxxx xxxxxxxx, xxxxxxx,
- podmínky xxxxxx:
- xxxxx expozičního zařízení xxxxxx konstrukce, typu, xxxxxxx, zdroje xxxxxxx, xxxxxxx xxxxxxxx xxxxxx x xxxxxxxx, xxxxxxxxxxxxxx xxxxxxx, xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx a xxxxxxx xxxxxxxx xxxxxx x xxxxxxxxxxxxxxx boxu, xxxxx xx používán. Xxxxxx xxxxxxxxx pro xxxxxx xxxxxxx, xxxxxxxx xxxxxxx, popřípadě xxxxxxxxx xxxxxxxxxxx a xxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxx,
- xxxxx o expozici xx xxxxxxx do xxxxxxx x xxxxxx xxxxx x xxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxxxxxx xxxxxxxxxxx (xxxx. směrodatnou xxxxxxxxx).
Xxxx obsahovat xxxx xxxxx:
x) xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx zařízením,
b) xxxxxxx x xxxxxxx xxxxxxx,
x) xxxxxxxxx xxxxxxxxxxx (xxxxxxx xxxxxxxx testované xxxxx přiváděné xx xxxxxxxxxxx zařízení, xxxxxx xxxxxxx xxxxxxx),
x) xxxxxx xxxxxxxx, pokud xxxx xxxxx,
x) xxxxxxxx koncentrace x dýchací xxxx,
x) xxxxxx xxxxxxxxx částic (xxxxx xxxxxxxx),
- xxxxx x xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx a xxxxx koncentrací,
- xxxxxx xxx xxxxxx, xxxxx xx xxxxx ji xxxxxxxx,
- xxxx uhynutí xxxxx xxxxxxxxxxx, případně xxxx x přežití xxxxxx do konce xxxxxxxxx,
- xxxxx xxxxxxxxx xxxx xxxxxx účinků,
- xxxx, xxx xxxx xxxxxxxxxx jednotlivé abnormální xxxxxxxx x xxxxxx xxxxx xxxxx,
- xxxxxxxx xxxxxxx x vývoj xxxxxxx xxxxxxxxx,
- xxxxxxxxxxxxxx xxxxxx,
- hematologická vyšetření x xxxxxx xxxxxxxx,
- xxxxxxxxxxx xxxxxxxxx a xxxxxx xxxxxxxx, (včetně xxxxxxxx xxxxxxxxxx xxxxxx xxxx)
- xxxxxxx xxxxxx,
- xxxxxxxx xxxxx xxxxx xxxxxxxxxxxxxxxxxx xxxxxx,
- statistické xxxxxxxxxxx výsledků, xxx xx xx xxxxx:
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.30 XXXXXXXXX XXXXXXXXX XXXXXXXX
1 XXXXXX xx x souladu x xxxxxx Evropských xxxxxxxxxxxx.
1)1.1 Xxxxxxx xxxxxxxxx xxxxxx
Xxxxxxxxx xxxxx xx podávána xxxxxxx 7 dnů x týdnu, xxxxxxx xxxxxx, xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, xxxxx xxxxx na skupinu, xx větší xxxx xxxxxx xxxxxx. Xxxxx x xx expozici xxxxxxxxx látce xxxx xxxxxxx denně xxxxxxxxxx xx účelem xxxxxxxxx xxxxxxx xxxxxxxx.
1.2 Popis xxxxxxxxx xxxxxx
1.2.1 Xxxxxxxx
Xxxxxxx xxxx xxxxxxx xxx xxxxxxxxxx xxxxx x xxxxxx, x jakých xxxxx xxxxx xxxxxx x aspoň 5 xxx xxxx xxxxxxxxx xxxxx. Xxxx xxxxxx xxxx xxxxxx, xxxxx xxxxxxx náhodně rozdělena xx exponovaných x xxxxxxxxxxx skupin.
1.2.2 Xxxxxxxxx xxxxxxxx
1.2.2.1 Xxxxxxxxxxxxxx zvířata
Pokusná xxxxxxx xxxx xxxxxxx x xxxxxxx xx xxxx, xxxxxxx x xxxxx x souladu x ustanovením
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x xxxxxxxx tak, xxx byla xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Xxxx navykání stanoví
§10 zvláštního xxxxxxxx xxxxxxxx.
10) Xxxxxxxxxxxx xxxxxx xx potkan. Xx xxxxxxx xxxxxxxxxxx studií xx xxxxx xxxxxx x další druhy (xxxxxxxx xxxx jiné). Xx xxxxx xxxxxx xxxxxx x xxxxx xxxxxxx xxxxx chovaných xxxxx xxxxxxxxxxxxx xxxxxx. Xxxxxxxx by xxxx xxx započata xx xxxxxxxx xx xxxxxxxxx xxxxxx. Xx začátku xxxxxx xx xxxxx xxxxxx xx váze xxxxxx xxxxx xxxx xxx ± 20% xx xxxxxxx. X xxxxxxx, že xxxxxxx xxxxxx xxxxxxxxx test xxxxxxxxxxxx xxxxxx toxicity, xx třeba použít xxxxxx druh x xxxx x obou xxxxxxxx.
1.2.2.2 Počet x xxxxxxx
Xxx xxxxxx xxxxxx xxxxx je třeba xxxxxx xxxxxxx 40 xxxxxx (20 samic x 20 xxxxx), xxxxxx x pro xxxxxxxxx xxxxxxx. Xxxxxx xx měly xxx xxxxxxxxx a neměly xx xxx březí. Xxxxx je xxxxxxx xxxxxxx xxxxxxx zvířata xxxx xxxxxxxxxx xxxxx, xx xxxxx xxxxxx xxxxxxxxx vyšší xxxxx xxxxxx.
X případě xxxxxx xxxxx zvířat (nehlodavců) xx xxxxx xxxxxx xxxxx počet xxxxxx, xxx xx méně xxx 4 od xxxxxxx pohlaví xx xxxxxxx.
1.2.2.3 Xxxxx x xxxxxxxxx xxxxxxx
Xx xxxxx xxxxxx xxxxx 3 xxxxx x 1 xxxxxxxxx xxxxxxx. Xxxxxxxx xxxxx xx xxxx xxxxxxx jasné xxxxxxx xxxxxxxx bez xxxxxxxx xxxxxxxxx. Xxxxxxxx xxxxx xx xxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxx. Xxxxxxx xxxxx by xxxx být xxxxxx xx xxxxxxxx pásmu xxxx xxxxxxxx x xxxxxxx xxxxxxx. Xxxxx xxxxx by xxx xxxx x úvahu xxxxxxxx xxxxxxxxxxx xxxxxx.
Xxxxxxx xxxx zvířata xxxxxxxxxx xxxxx. X xxxxxxx, xx testovaná látka xx xxxxxxxx v xxxxx xxxx nebo x potravě, xx xxxxx zajistit, xxx x xx xxxx xxxxxxx xxxxx xxxxxxx.
1.2.2.4 Xxxxxxxx
Xxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxxx x xxxxxx xxxxxx x xxxxxxxxxx xxxxxxx, xxxxx xxxxxxxx xxxxxxxxx látce.
Ve xxxxxxxxxx případech, xxxx xxxx xxxxxxxxx studie x xxxxxxxx xxxx xxxxxxx-xx xx xxx xxxxxx aplikaci xxxxxxxxxx, xxxxx xxxxxxxxxx xxxxxxxx xxxx xxxxxxxxxxxxxxxx, xxxxxx xx xxxxx negativní xxxxxxxxx xxxxxxx, xxxxx xxxx xxxxxxxxxx xxx xxxxxxxx.
1.2.2.5 Způsob xxxxxxxx
Xxx xxxxxx způsoby xxxxxxxx xxxx xxxxxx x xxxxxxxxx. Xxxxx xxxxxxx xxxxxx xxxxxx xx xxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxx.
Xxxxxxx dermální xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxx problémy. Xxxxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxx kožního xxxxxxxxx xxxx xxx xxxxxxxx xxxxxxxx z xxxxxxxx xxxxxxxx testu a xxxxxxxx rozsahu xxxxxxx xxxxxxxxxxx, odvozené x xxxxxxxxxxx xxxxx xxxxx xxxxxxxx.
Xxxxxx xxxxxx
Xxx, xxx xx testovaná látka xxxxxxxxx x xxxxxxxxxxxxxxxxxxxx xxxxxx x xx-xx xxxxxx jednou x xxxx, jimiž xxxx xxx xxxxxxxxx člověk, xxxx se přednost xxxxxx aplikaci, xxxxx xxxxxx xxxxx xxxx xxxxxx důvody. Xxxxxxx xxxxx xxxxxx xxxxxxxxxx xxxxx v potravě, xxxxxxxxxx x pitné xxxx xxxx podanou x xxxxxxx.
Xxxxxxx xx xx měla xxxxx xxxxxxx sedm xxx x xxxxx, xxxxxxx xxxxxxxxx 5 xxx x xxxxx xxxx xxxx x vymizení xxxxxxxx xxxx xxxxxx xxxxxxx "xxxxxxxxxxx" xxxxxxxx x xxxxxx xxx xxxxxxxx, x xxxxx xxxxxxxx výsledky x xxxxxxxx hodnocení. Xxxxxxx, xxxxxxxxx s ohledem xx xxxxxxxxx xxxxxxx, xxxxxxxxx 5 xxxx xxxxx je považováno xx xxxxxxxxxx.
Xxxxxxxxx xxxxxx
Xxxxxxx xxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxxxxxxxxx xxx xxxx způsoby aplikace, xxxx zde xxxxxxx xxxxxxxxxx xxxxxxxxx x xxxx xxxxx xxxxxx. Xxxxxxxxxxxxxxx instilace xxxx xxx platnou xxxxxxxxxxxx xx specifických xxxxxxxxx.
Xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxx lidské xxxxxxxx, xxxxx zvíře xx xxxxxxx xxxxxxxxxx xx xxxxxxxx koncentrace 6 xxxxx xxxxx po 5 dnů x xxxxx (xxxxxxxxxxx xxxxxxxx), xxxx x návaznosti xx možnou xxxxxxxx x xxxxxxxxx, 22-24 xxxxx denně po xxxx xxx v xxxxx (kontinuální expozice), x přibližně 1 xxxxxxx xxx xxxxxx xxxxxx denně ve xxxxxxx xxxx xxx, xxxxxxxx i xxx xxxxxxx expozičního boxu. X obou xxxxxxxxx xxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxxx koncentracím xxxxxxxxx látky. Hlavní xxxxxx xxxx xxxxxxxxxxxx x stálou xxxxxxxx xx x xxx, xx x xxxxxx xxxxxxx má zvíře 17-18 hodin xx xxxxx xxxxxx xxxxx xxxxxxxx x xxxxx xxxxxx obdobím xxxxx xxxxxxx.
Xxxxx xxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxx závisí xx xxxxxx studie x xx xxxxxx xxxxxxxx, xxxxx má xxx xxxxxxxxxx. Xxxxxxx, xx třeba xxxx x xxxxx určité xxxxxxxxx xxxxxx. Například, xxxxxx kontinuální expozice xxx simulaci podmínek xxxxxxx prostředí xxxxx xxx xxxxxxxx xxxxxxxx xxxxxxxx x krmení xxxxx xxxxxxxx a xxxxxxxx xxxxxxxxxxxxxxx (x xxxxxxxxxx) generace xxxxxxxx xxxx xxxxxx koncentrace xxx x xxxxxxx xxxxxxxxxxxx.
Xxxxxxxxx komory
Zvířata se xxxxxxxx x inhalačních xxxxxxxx, xxxxxxx konstrukce xxxxxxxx dynamický xxxxx xxx nejméně 12 xxxxx xxxxxxx xx xxxxxx, xxx xxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxxx expoziční xxxxxxxxx. Xxxxxxxxx x xxxxxxxxx xxxxxx xx xxxx xxx xxxxxxxxxx konstrukci, xxx xxx byly xxxxxxxxx podmínky srovnatelné xx xxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxxxx. Xxxxxx komory xx obvykle xxxxxxx xxxxx xxxxxxx a xxx xx xxxxx xxxxx xxxxxxxxx xxxxx xx okolního xxxxxxxxx. Xxxxxx xx xxxx xxxxxxxxxxxxx stísněnost testovaných xxxxxx. Xxxxxx xx x xxxxx xxxxxxx xxxxxxxx atmosféry v xxxxxx xxxxx zvířat xxxxx xxxxxxxxxx 5 % xxxxxx xxxxxx.
Xxxxxx xxxx xxxxxxxxxxxx zahrnuje:
(a) xxxxxx xxxxxxx: xxxxxxxx xxxxxxx xxxxxxx xxxxxxx xx xxxx být xxxxxxx kontrolována xxxxxxxxxxx;
(x) xxxxxxxxxxx: xxxxx xxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxx látky xxxxxx xxxxxxx více xxx ±15 % střední xxxxxxx;
(x) xxxxxxx x xxxxxxx: xxx hlodavce, xxxxxxx by xxxx xxx xxxxxxxxx x xxxxxxx 22 ± 2°X x vlhkost x xxxxxxxx 30 - 70 % xxxxx xxxxxxx, xxx xx voda xxxxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxx xxxxxx. Xxx xxxxxxxxx xx měly být xxxxxxxxxxxx průběžně;
(d) xxxxxx xxxxxxxxx xxxxxx: xxxx xx být stanovena xxxxxxxxxx velikosti xxxxxx x atmosféře xxxxx x xxxxxxxx xxxx xxxxxxx aerosolů. Xxxxxxxxxx xxxxxxx xx měly xxx v xxxxxxxxxxxx xxxxxxxxx pro xxxxxxx xxxxxxxxx xxxxx. Xxxxxx xxxxxxxxx xxxxx xx xxxxxxxxx z xxxxxxx xxxx xxxxxx. Vzorek xxxxxxx by xxx xxx xxxxxxxxxxxxxxx xxx xxxxxxxxxx xxxxxx, kterým xx xxxxx xxxxxxxxxx, x xxx xx xxxxxxxxxxxxx odpovídat celému xxxxxxxxxxxxxx aerosolu, x xxxx xxxxxx xxxx xxxxxxxx xxxx xxxxxxxxxxxx. Xxxxxxx velikostí xxxxxx xx xxxx xxx xxxxxxxxx xxxxx během xxxxxx generujícího xxxxxxx, xxx xxxxxxxxx stabilitu xxxxxxxx, a xxxx xxxxx xxxxxxx tak xxxxx, aby bylo xxxxx xxxxxxxx stabilitu xxxxxxxxxx xxxxxx, kterým xxxx xxxxxxx exponována.
1.2.2.6 Xxxxxx xxxxxx
Xxxxxxxx xxxxx xx xxxx trvat xxxxxxx 12 xxxxxx.
1.2.3 Xxxxx postupu
1.2.3.1 Pozorování
Pečlivé xxxxxxxx xxxxxxxxx xx xxxx xxx prováděno xxxxxxx xxxxxx denně. Xxxx xx xxx xxxxxxxxx i dodatečná xxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxx x xxxxxxxxxxxx xxxxx. Zvířata xx xxxxx xxxxxxx sledovat, xxx xx xxxxxxxxxx xxxxxxxx xxxxxxx x xxxxxxxx všech xxxxxxxxx xxxxxx, a také xx účelem xxxxxxxxxxxx xxxxx x xxxxxxxx xxxxxx, xxxxxxxx xxxx xxxxxxxxxxx.
Xxxxxxxxxx xx xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxxx x xxxxxx xxxx x xxxxx zvířat, x xxxx xxxxxxx xxxxxxx. Zaznamenává xx xxxx xxxxxxxx x xxxxxx xxxxxxxxx příznaků xxxxxx xxxxxxxxx xx xxxxx.
Xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxxx x xxxxx xxxxxx jednou xxxxx xxxxx prvních 13 xxxxx xxxxxx xxxxx x xxxxx jednou xx 4 týdny xx xxxxx xxxxxx. Xx xxxxx xxxxxxxx xxxxxx xxxxxxxx potravy (x vody xxx, xxx xx testovaná xxxxx xxxxxxxx x xxxxx xxxx) xxxxx xxxxx xxxxxxx 13 xxxxx a pak xxxxxxxxx xx xxxxxxxxxxxx xxxxxxxxxxx, ledaže xx xxxxxxxxx stav nebo xxxxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxxxx.
1.2.3.2 Xxxxxxxxxxxxx xxxxxxxxx
Xxxxxxxxxxxxx vyšetření (např. xxxxx xxxxxxxxxxx, xxxxxxxxxx, xxxxxxx xxxxx xxxxxxxxxx, xxxxxxx počet xxxxxx xxxxxxx, xxxxxxxx destiček, xxxx jiné ukazatele xxxxxxxxxxx) xx xxxx xxx xxxxxxxxx za 3 xxxxxx, 6 xxxxxx x xxxx x xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxx, a na xxxxx xx vzorcích xxxx xxxxxxxxxxxxx xx xxxxx xxxxxxxxxx, respektive xx 10 xxxxxxx, xx xxxxxxx z xxxxx skupiny. Xxx, xxx je xx xxxxx, xx xxxx xxx xxxxxx ve xxxxx xxxxxxxxxxx xx xxxxxxxx potkanů. Navíc xx potřeba xxxxxxx xxxxxx xxxx xxxxxx xx xxxxx nehlodavců.
Pokud xxxxxxxx xxxxxxxxx zvířat xxxxxxx xxxxxxxx zdravotní xxxx xxxxxx xxxxx xxxxxx, xxx xx xxx stanoven xxxxxxxxxxxxx xxxxx xxxxxx xxxxxxx.
Xxxxxxxxxxxxx xxxxx bílých xxxxxxx xx xxxxxxx ve xxxxxxxx od xxxxxx xx xxxxxxx x xxxxxxxx xxxxxx x x xxxxxxx. Pokud xxxx xxxx xxxx xxxxx x xxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxx xxxxxxx, xxxxxxx xx x x xxxxxxx x dávkou xxxxxxxx xxxxx.
1.2.3.3 Analýza xxxx
Xxxxxx xxxx 10 xxxxxxx xxxxxxx xxxxxxx xx xxxxxxx xxx xxxxxxx xxxxx xxxxx od xxxxxxxx xxxxxx x xx xxxxxxxx xxxxxxxxxxx xxxx hematologické xxxxxxx. Xxxxxxxxxxx xxxxxxxxx jsou xxxxxxxxx xxx' xx xxxxxxxx xxxxxxxxxxxx xxxxxx, xxxx xx směsném xxxxxx xxx xxxxxxx xxxxx xxxxx a xxxxxxx:
- xxxxxx xxxx, xxxxx a xxxxxxx x xxxxxxxxxxxx xxxxxx,
- xxxxxxxx, glukosa, ketolátky, xxxxxxx xxxxxxxx (xxxxxxxxxxxxxxxxx),
- xxxxxxxxxxxxx vyšetření xxxxxxxxx (xxxxxxxxxxxxxxxxx).
1.2.3.4 Xxxxxxxxxxx xxxxxxxxx
X xxxxxxxxx xxxxxxxxxxxxxx intervalech x na xxxxx xxxx xxxxxxxx xxxxxx xxxxxx xxx biochemická xxxxxx od xxxxx xxxxxxxxxx a 10 xxxxxxx obojího xxxxxxx x xxxxx xxxxxxx, xxxxx možno xx xxxxx xxxxxxx ve xxxxx intervalech. Xx xxxxxxxxxx xx xxxxx xxxx xxxxxxxx xxxxxx xxxx xxxxxx. X xxxxxx xxxxxx xx xxxxxxxxxx xxxxxx x xxxx xxxxxxxxx xxxxxxxxxxx xxxxxxx:
- xxxxxxx xxxxxxxxxxx xxxxxxxx,
- koncentrace xxxxxxxx,
- xxxxx xx xxxxxx xxxxx (xxxx. xxxxxxxx xxxxxxx xxxxxxxxx, xxxxxxxx xxxxxxxx pyruvát transaminázy (xxxx xxxxx xxxx xxxxxx xxxxxx xxxxxxxxxxxxxxxx), xxxxxxxx xxxxxx transaminázy (xxxx xxxxx xxxx xxxxxx aspartát xxxxxxxxxxxxxxxx), xxxx xxxxxxxx xxxxxxxxxxxxxx, xxxxxxx xxxxxxxxxxxxx,
- metabolismus xxxxxxx, např. xxxxxx xxxxxxx xxxxxxx,
- xxxxx xx xxxxxx ledvin, xxxx. dusík xxxxxxxx x xxxx.
1.2.3.5 Pitva
Kompletní xxxxx se xxxxxxx x všech zvířat, xxxxxx těch, xxxxx xxxxxxx xxxxx pokusu xxxx xxxx utracena x xxxxxx stavu. Xxxx xxxxxxxxx xx xxxxxxxx xxxxxx xxxx xxxxx xxxxxx xxx xxxxxxxxxxxxx xxxxx xxxxxx xxxxxxx. Xxxxxxx xxxxxxxxx xxxxxx nebo Xxxx, xxxxx xx mohly xxx xxxxxx, xx xxxxx xxxxxxx. Provádí xx porovnání xxxxxxxxxxxxxxxxxxxxxxx xxxx s mikroskopickými xxxxxx.
Xxxxxx x xxxxx xx xxxxxxxxxx xxx xxxxxxxxxxxxxxxx xxxxxxxxx. Xxxxxxx xx jedná x xxxxxxxxxxx orgány a xxxxx: mozek (xxxxxxxxxxx xxxxx/xxxxx, xxxxxxxxx xxxx, xxxx xxxxxxx), podvěsek xxxxxxx, štítnou žlázu x xxxxxxxxx xxxxxxx, xxxxxx. xxxxxxx x xxxxx, xxxxx, xxxxx, xxxxxxx xxxxx, játra, xxxxxxx, ledviny, xxxxxxxxxx, xxxxx, žaludek, xxxxxxxxxxxx, xxxxxxx, ileum, xxxxx xxxxxx, tračník, xxxxxxxx, xxxxxx xxxxxx, lymfatické xxxxxx, xxxxxxxx, gonády, xxxxxxxxx xxxxxxxx orgány, xxxxxx xxxxxx xxxxx, xxxx, xxxxxxxxx, xxxxxxxxx xxxxx, xxxxx (xxxxx, xxxxxx x xxxxxxx), xxxxxxx x xxxxxx xxxxx, xxxxxxxx xxxx xxxxxx xxxxxx, x xxx. Naplnění xxxx x xxxxxxxx měchýře xxxxxxxxx xx optimální xxxxxx xx xxxxxxxxxx xxxxxx tkání; xxxxxxxx xxxx x xxxxxxxxxxx xxxxxxxx xx xxxxxxx xxx odpovídající xxxxxxxxxxxxxxxx xxxxxxxx. Xx speciálních xxxxxxxx, xxxx jsou xxxxxxxxx xxxxxx, xx xxx studován celý xxxxxxxxxx xxxxx xxxxxx xxxx, xxxxxx x xxxxxx.
Xxxxxxxx: xxxxxx xxxxx x příštítnými xxxxxxx xx xxxxx nehlodavců xxxx být zvážena xxxxxx jako mozek, xxxxx, xxxxxxx, xxxxxxxxxx x gonády x 10 zvířat xx xxxxxxx a xx xxxxxxx x xxxxxxxx x xx xxxxx xxxxxxxxxx.
Xxxx-xx provedena xxxx xxxxxxxx xxxxxxxxx, xxxxxxxxx xxxxxxx x xxxxxx xxxxxxxx by xxxx xxx k xxxxxxxxx xxxx xxxxxxxxxxxxxx xxxxxxxxxx, xxxxxxx mohou xxx xxxxxxxxxx významné vodítko.
1.2.3.6 Xxxxxxxxxxxxxx
Xxxxxxx xxxxxxxxx xxxxx, xxxxxxx tumory x xxxx léze xxxxxxxxxxx xx x xxxxxxxxxx xxxxxx, xx xxxxxxxx xxxxxxxxxxxxx. Xxxxx jsou xxxxxxxxxx xxxxxxxxxxx xxxxxxx:
(x) xxxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx orgánů x xxxxx x xxxxxxxxxx xxxxxxx xxxxx xxxx xxxxxxxxxx:
1. x všech xxxxxx, xxxxx xxxxxxx xxxx xxxx utracena xxxxx xxxxxx,
2. x xxxxx xxxxxx xx xxxxxxx x xxxxxxx xxxxxx x kontrolní xxxxxxx
(x) orgány xx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxxxxx testovanou xxxxxx xxxx xxxxxxxx také xx xxxxxxxxx x xxxxxxx xxxxxxx,
(x) tam, xxx výsledky svědčí xxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxx xxxx xxxxxxxx xxxxxx, které by xxxxx xxxxxxxx xxxxxxxx xxxxxxx, skupina s xxxxxxxx xxxxx xxxxxx xx xxxxxxx xxxxxxxx xxxxxxxx,
(x) xxxxxxxxx x xxxxxxxxx xxxx, xxxxx xx xxxxxxxx vyskytují x xxxxxxxx xxxxx xxxxxx, ve xxxxxxxx xxxxxxxxxxxxx podmínkách, xx. xxxxxxxxxx xxxxxxxxx údaje, xxxx xxxxxxxx xxx xxxxxxx posouzení významnosti xxxx pozorovaných x xxxxxx x xxxxxxxxxxx xxxxxx.
2 XXXXX
Xxxxx se xxxxxxxxxx xx xxxxx xxxxxxx, xxxxxxxxxxx xxx xxxxxx testovanou skupinu xxxxx xxxxxx xx xxxxxxx xxxxx, xxxxx xxxxxx xxxxxxxxxxxx xxxx x xxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxx xxxx. Výsledky xx xxxx být vyhodnoceny xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx. Xxxxx být xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx.
3 XXXXXXX POKUSU, XXXXXXXX XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx x xxxxxxxxxxx právními xxxxxxxx
9) musí xxx xxxxxxxxx xxxxxxx xxxxxx x x průběhu xxxxxx xx xxxxx xxxx protokol.
Zpráva x xxxxx bude xxxxxxxxx xxxxxxxxxxx xxxxxxxxx:
- xxxxxxxxx xxxx, kmen, zdroj, xxxxxxxx xxxxxxxx, xxxxx,
- xxxxxxxx xxxxx,
- popis xxxxxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxx, xxxx, xxxxxxx, xxxxxx xxxxxxx, xxxxxxx xxx vytváření xxxxxx x aerosolů, xxxxxx xxxxxxxxxxx, zneškodňování xxxxxxx xxxxxxxxxxxxx x aparatury x způsobu umístění xxxxxx v xxxxxxxxxx xxxx, xxxxx xx xxxxxxx. Xxxx je xxxxx popsat zařízení xxx xxxxxx teploty, xxxxxxxx, x tam, xxx xx to xxxxxxx, xxxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxx xxxxxx xxxxxxxx,
- údaje x xxxxxxxx: xx xxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxx x xxxxxxxxxxx (xxxx. standardní odchylka) x xxxx xx xxxxxxxxx:
(x) xxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxx
(x) xxxxxxx x xxxxxxx xxxxxxx
(x) xxxxxxxxx xxxxxxxxxxx (xxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx do xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxx)
(x) xxxxxx xxxxxxxx, xx-xx xxxxxxx
(x) xxxxxxxx koncentrace v xxxxxxx xxxx
(x) mediány xxxxxxxxx xxxxxx (xx-xx xx xxxxxxxxxx)
- dávkové xxxxxx (xxxxxx xxxxxxxx, xx-xx xxxxx) a xxxxxxxxxxx,
- xxxxx x xxxxxxx odpovědi xxxxx xxxxxxx x dávky,
- xxxxxxxx (dávková) úroveň,
- xxxx xxxxx během xxxxxx xxxx xxx xxxxxxx xxxxxxx xx xx xxxxx,
- popis xxxxxxxxx a jiných xxxxxx,
- doba, xxx xxx xxxxxxxxx každý xxxxxxxxxx příznak a xxxx další xxxxx,
- xxxx x xxxxxxxx xxxxxxx x xxxxxxx xxxxxxxxx,
- oftalmologické nálezy,
- xxxxxxx xxxxxxxxxxxxx xxxxx x výsledky,
- testy xxxxxxxx biochemie a xxxxxxx xxxxxxxx (včetně xxxxxxxx analýzy xxxx),
- xxxxxxx xxxxxx,
- xxxxxxxx xxxxx xxxxx xxxxxxxxxxxxxxxxxx xxxxxx,
- xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxx xxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.31 XXXXXX XXXXXXXXXX XXXXXXXX XXXXXXXX
1 XXXXXX xx x xxxxxxx s xxxxxx Xxxxxxxxxx xxxxxxxxxxxx
7a).
1.1 XXXX
Xxxx xxxxxx xxxxxxxx xxxxxxxx toxicity xx xxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxx xx xxxxxx xxxxxxxxxx xxxxxxxx xx březí xxxxxxx xxxxx x xx organismus xxxxxxxxxx xx x děloze; xxxx xxxxxxxxx xxxxx xxxxxxxxx xxx hodnocení xxxxxx xx matku, xxx i xxxx xx xxxxxxx, xxxxxxxxxxxx xxxxxxxx xxxx xxxxxxx xxxx plodu. I xxxx funkční xxxxxxx xxxxx xxxxxxxxx část xxxxxx, xxxxxx xxxxxxxx xxxx metody. Xxxxxxx xx xxxx poruchy xxxxx xxx xxxxxxxxx x xxxxxxxxxx xxxxxx xxxx xxxx doplněk xxxx xxxxxx xxxxxx xxxxxxxx xxxxxx pro xxxxxx xxxxxxxx neurotoxicity. Xxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxx x xxxxxx postnatálních xxxxxx xxx v případě xxxxxxx získat z xxxxxxxxxxxxx xxxxxxx xxxxxxxx xxx xxxxxxxxxx a xxxxxxx xxxxxxxx xxxxxxxxxxxxx.
Xxxx xxxxxxxx metoda může xx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxx xx základě specifických xxxxxxxx xxxx. xxxxxxxxx-xxxxxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx. Xxxx xxxxxx xx xxxxxxxxxx, xxxxxxxx přesvědčivé xxxxxxx xxxxxx xxxxxx o xxx, díky této xxxxxx xxxx xxx xxxxxxx xxxxx vypovídací xxxxxxxx. X takovém xxxxxxx xx xxxxx xxxx xxxxxxx xxxxxx xxxxxxx xxxxxxxxxxxxx xx xxxxxx x studii.
1.2 XXXXXXXX
Xxxxxxxx xxxxxxxxxxx: studie xxxxxxxxxxxx xxxxxx xx xxxxxxxxxx xx organismus, xxxxx xxxxx vyplývat x expozice xxxx xxxxxxx, během xxxxxxxxxxxx xxxxxx xxxx x xxxxxxxxxxxx období až xx xxxx pohlavní xxxxxxxx. Xxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx 1) xxxx xxxxxxxxx, 2) strukturální xxxxxxxx, 3) xxxxxxx xxxx x 4) xxxxxxx xxxxxxx. Vývojová toxikologie xx xxxxxxx xxxxxxxx xxxxxxxxxxx.
Xxxxxxxxxx xxxxxx: xxxxxxxxx xxxxxxxx od normálního xxxxx xxxxxxx x xxxxxxxx, xxxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx, xxxxxxxxxxx se xxxx xx xxxxxxxxxxx xxxxxxxxx. Xxxxx jde o xxxxxxxxx xxxxxxxxxxx v xxxxxxxxx xxxxx xxxxxx, xxxxxxxx xxxxx xxxxx xxxxxxxxx xxxxxx, xxxxx xxxxx xxxxxxxxxx xxxxxx xxxxx, a to xxx před narozením, xxx i xx xxx.
Xxxxxxx růst: xxxxx xxxxxxxxx nebo velikosti xxxxxx xxxx xxxx x xxxxxxxxx.
Xxxxxxxx (xxxxxxxx): xxxxxxxxxxxx xxxxx xx xxxxxx, xxxxx zahrnují xxx malformace, xxx x odchylky
7a).
Malformace/velká xxxxxxxx: xxxxxxxxxxxx xxxxx xxxxxxxxxx xx xxxxxxxxx pro xxxxxxx xxxxx (xxxx xxx x xxxxxxx); xxxxxxx je vzácná.
Odchylka/malá xxxxxxxx: xxxxxxxxxxxx xxxxx, xxxxx xxxx xxxxx xxxx xx xxx xxxx xxxxxxxx xxxxxx xx xxxxxxx xxxxx; xxxx být xxxxxxxxx x x kontrolní xxxxxxxx xx xxxx xxxxxxxxxx xxxxxxx xxxxx.
Xxxxxxx: xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxxx vajíčka v xxxxxxxxx xxxx xxxxxx xx xxxxxxxxx xx xx narození, xxxxxx xxxxxxx zárodečných xxxxxxx, xxxxxx xxxx xxxxx.
Xxxxxxxxxx (xxxxxx): přichycení blastocysty x epitelové xxxxxxxx xxxxxx, xxxxxx xxxx xxxxxxxxx do xxxxxxxxx xxxxxxx x zahnízdění x xxxxxxx xxxxxxxx.
Xxxxxx: xxxx xxxx xxxxxxxx xxxx organismu, x xx xxxxxxx xxxx xxxxxxxxxx xx po xxxxxxxxx xxxxxxx xxxx, xx xx xxxxxx xxxxxx osa, a xxxxx nejsou přítomné xxxxxxx xxxxxx xxxxxxxxx.
Xxxxxxxxxxxxxx: xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxxx, xxxxx, xxxx nebo xxxxxxxxxxxxxxx xxxxxx.
Xxxxx: xxxxxxxxxx potomek x xxxx-xxxxxxxxxxxx xxxxxx.
Xxxxxxxxxxxx: xxxxxxxx škodlivá xxx xxxxxxxx xxxxxxxxx, xxxxx, xxxx xxxx životaschopnost xxxxx.
Xxxxxx: xxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxx - xxxxxx xxxx xxxxx xxxxxxxxxxx xxxxxx - x xxxxxx.
Xxxxxxxx: zárodek, xxxxx po xxxxxxxxxx xx xxxxxx xxxxxxx xxxxxxx x xxxxxxxxx xx xxxx se xxx xxxxxxxx.
Xxxx xxxxxxxx: xxxxx o xxxxxxxxxx (xxxxxxxxxx) xxx rozeznatelného xxxxxx/xxxxx.
Xxxxxx xxxxxxxx: xxxxx xxxxxx xxxx xxxx xx xxxxxxx xxxxxxxxxxxxxxx xxxxxxx.
1.3 REFERENČNÍ XXXXX
Xxxxx.
1.4 XXXXXXX XXXXXXXX XXXXXX
Xxxxxxx xx xxxxxxxx látka xxxxxx xxxxxx xxxxxxxx xxxxxxxx xx implantace xx xx dne xxxx xxxxxxxxxx xxxxxxxxx, xxxxx xx xx xxx xx xxxxxxx xxxxxxxxx očekávanému dni xxxx, aniž xx xxxxxxx ztráta údajů x xxxxxxxx předčasného xxxx. Zkušební xxxxxx xxxx xxxxxx xxxxxxxx xx xxxxxxxx období xxxxxxxxxxxx (xxxx. 5. - 15. xxx x xxxxxxxx a 6. - 18. xxx u xxxxxxx), xxx xxxxxxxxx rovněž xx xxxxxxxx účinků xxxx xxxxxxxxxx, pro xxxx xxxxxx xxxxxxx x xx xx xxx xxxx císařským xxxxx. Xxxxxx před xxxxxxxxx xxxxx xx xxxxxx xxxxxx, prozkoumá xx děložní obsah x u xxxxx xx vyhodnotí zevní xxxxxxxxx anomálie, xxxxx xxxxxxx xxxxx a xxxxxxx.
1.5 XXXXX XXXXXXXX XXXXXX
1.5.1 Xxxxx živočišných xxxxx
Xxxxxxxxxx xx provádět xxxxxxxx x xxxxxxxxxxxxxx xxxxx a xxxxxxxx xxxxxxxxxxx xxxxx x xxxxx, xxxxx xx xxxxx používají xxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx. Xxxxxxxxxxxxxxxx xxxxxx xxxxxxxx xx potkan x xxxxxxxxxxxxxxxx druhem xxxxxxxxxx xx xxxxxx. Xxxxxxx jiného druhu xx xxxxx xxxxxxxxx.
1.5.2 Xxxxxxxx xxxxx a xxxxxx
Xxxxxxx xx xxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxx xx měla xxx (22 ± 3) °C pro xxxxxxxx x (18 ± 3) °X xxx králíky. Xxxxxxxxx xxxxxxx by xxxx xxx xxxxxxx 30 %, xxxxxx xx xxxx xxxxxxxxx 70 % xxxxx xxxxxxx xxxxxxxxx x xxxxx xx hodnota 50 - 60 %. Xxxxxxxxx xx mělo xxx umělé, mělo xx se střídat 12 h světla x 12 x xxx, xxxx-xx v xxxxxx místnosti xxxxx xxxxxx. Xx krmení xxx xxxxxx obvyklé xxxxxx xxxxxx pro xxxxxxx xxxxxxx xx xxxxxxxxxxxxxx xxxxxxx x xxxxxxxxxx dodávkou pitné xxxx.
Xxxxxx xx mělo xxxxxxxx x xxxxxxx xxxxxxxx k tomuto xxxxx x xxxxxxx x příslušným xxxxxxx xxxxxxxxx
10), xxxxx není xxxxxxxxx projektem xxxxxx xxxxx. X xxxx xx xxxx xxxxxxxx xxxxxxxxxxxxxx xxxxx spářených xxxxxxxxx xxxxxx, xxxxxxxxx xx rovněž chov x malých xxxxxxxxxx.
1.5.3 Xxxxxxxx xxxxxxxxx xxxxxx
Xxxxxxx xxxxxxx xxxx vybrána x ohledem xx xxxx, pohlaví x xxxxx x xxxxxxx x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx předpisu
10) x xxxxxxxx xxx, xxx byla možná xxxxxxxxxxxx jednotlivých pokusných xxxxxx. Dobu navykání xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx
10). Xxxxxxx xxxxxxx by měla xxx xxxxxxxxxxxxxxxx xxxxx xxxxx, kmenu, xxxxxx, xxxxxxx, hmotnosti xxxx xxxxx. Xx-xx xx xxxxx, měla xx xxx xxxxxxx xxxxxxx xx xxxxx testovaných xxxxxx xxxxxxx hmotnost x xxx. Xxx xxxxxx xxxxxx xxxxx xx xxxxxxx xxxxx xxxxxxx xxxxxx, xxxxx xx měly být xxxxxxxxx. Xxxxxx xx xxxxx xx xxxxx xxxxxxxx xxxxx x xxxxx x xxxxxx xx xxxxxxxx x xxxxxx xxxxxxxxxx. X xxxxxxxx xx xxxxxx xxxx xxxxxxx den, xxx xx xxxxxxxx xxxxxxxxx xxxxx nebo xxxxxx; x králíků xx xxxx 0 xxxxxxx xxx páření xxxx umělé xxxxxxxxxx, xxxxx se xxxx xxxxxx xxxxxxx. Xxxxxxxxx xxxxxx se xxxxxxxx xxxxxxx xxxxxxx do xxxxxxxxxxx x xxxxxxxxxxxxxxxx xxxxxx. Xxxxx xx xxxx xxx xxxxxxxxxx xxx, xxx byl xxxx umístění klecí xxxxxxxxxxxxx. Každému pokusnému xxxxxxx xx xxxxxxx xxxxxxxxxxx identifikační xxxxx. Xxxxxxxx xxxxxxx se xxxxxxxxx samice xxxxxxx xx xxxxxxxxxxx x xxxxxxxxxxxxxxxx xxxxxx, a xxxx-xx xxxxxx xxxxxx x xxxxxx, xxxxxxx xx pokusná xxxxxxx x xxxxxxxxxxxx xxx xxxxxxxxxx do xxxxx xxxxxx. Xxxxxx xxx xx do xxxxx xxxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxx.
1.6 XXXXXX
1.6.1 Počet x xxxxxxx pokusných xxxxxx
Xxxxx xxxxxxxxxxxxxx x xxxxxxxxx xxxxxxx by xxxx xxxxxxxxx xxxxxxxxxx xxxxx xxxxx, xxxxxxx xxx xxxxx xxxxxxx xxxxxxxxx 20 xxxxx s xxxxxxxxxx xxxxx. Xxxxxxx x xxxx než 16 pokusnými xxxxxxx x xxxxxxxxxx xxxxx xxxxxx xxxxxx. Xxxxxxxxx xxxxx nemusí xxxxx xxxxxxxx znehodnocení xxxxxx xx předpokladu, xx xxxxxxxxxx xxxxxxxxx 10 %.
1.6.2 Příprava xxxxx
Xxxxx xx xxx xxxxxxxxx xxxxxxxxx xxxxxxx vehikulum xxxx jiná přísada, xx třeba xxxx x úvahu následující xxxxxxx xxxxx: xxxx xx xxxxxxxx, xxxxxxxxxx, xxxxxxxxxxxx x xxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxx; vliv xx xxxxxxxx xxxxxxxxxx zkoušené xxxxx, xxxxx xxxx xxxxxxxx xxxxx xxxxxxx xxxxx, x xxxx xx spotřebu krmiva xxxx xxxx anebo xxxxxxxxxx stavu xxxxxxxxx xxxxxx. Xxxxxxxxx xx xxxxxx xxx xxx xxxxxxxx xxxxxxx, xxx xx xxxxxx mít xxxx xx xxxxxxxxxxxx.
1.6.3 Xxxxxxxxx
Xxxxxxxx xxxxx xx xxxxxxx podává xxxxx xx implantace (xxxx. xxxx xxx po xxxxxxx) až xx xxx xxxx plánovaným xxxxxxxxx xxxxx. Xxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxx nevyplývá xxxxxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxx, xxx xxxxxxxx prodloužit xxx, xxx zahrnovala xxxx období xxxxxxx, xx spáření až xx xxx xxxx xxxxxxxxxx xxxxxxxxx. Je xxxxx, že xxxxxxxx xxxxxxxxx nebo xxxxx xxxxx xxxxxxxx xxxx xxxx k prenatální xxxxxx. X xxxxx xxxxxxxx xxxxxxxxxxx xxxxxxx x důvodů, xxxxx xxxxxx xxxxxxx x xxxxxxxx, xx xxxxx xxxxxxx jak xxxxxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxx, tak x xxxxxx způsobenému xxxxxxx xxxxxxx, xxxx xx xxxx. hluk.
Použijí xx xxxxxxx xxx úrovně xxxxx a xxxxxxxx xxxxxxxx. Zdravá pokusná xxxxxxx se náhodným xxxxxxx xxxxxxx xx xxxxxxxxxxx x xxxxxxxxxxxxxxxx xxxxxx. Úrovně xxxxx xx rozloží xxx, xxx xxxx xxxxxxx xxxxxx xxxxxxxxxxxx. Pokud xxxxxxxxxx žádné xxxxxxx xxxxxxxxx/xxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx, xxxxx xx xxxxxxxx dávka s xxxxx xxxxxxx určitou xxxxxxxxx toxicitu nebo xxxxxxxx xxx xxxxx (xxxxxxxx znaky xxxx xxxxxxx xxxxxxx xxxxxxxxx), xxx xxxxxxx xxxxxxx xxxx xxxxx xxxxxxx. Xxxxxxx jedna xxxxxxx xxxxxx dávky xx xxxx xxxxxxx xxxxxxxxx xxxxxxxxxxx toxické xxxxxx. Xxxxxxxx úroveň xxxxx xx neměla xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxx matku ani xxxxxxxxx xxxxxxxx. X xxxxxxx xx prokázání xxxxxxxx xxxxxx xxxxxxxxxxx x xxxxxxxxxx x x xxxxxx dávky xxx xxxxxxxxxxxx nepříznivého xxxxxx (NOAEL) xx xx xxxx xxxxxx xxxxxxxx xxxxxxxxxxx xxxxxx xxxxx. Pro xxxxxxxxx xxxxxxxxxx úrovní xxxxx xxxx xxxxxxx xxxxxxxxx xxxx- xx xxxxxxxxxxx xxxxxxxxx a xxxxx xx xxxxxxxxx přidání xxxxxx xxxxxxxxxx xxxxxxx xxx používání xxxxxxx xxxxxxxxx xxxx xxxxxxx (xxxx. xxxxxxxx xx xxxxxxxx 10). Ačkoliv xx cíleni stanovit xxxxxxx NOAEL pro xxxxxx, přijatelné jsou xxxxxx xxxxxx, které xxxx hodnotu xxxxxxxxx
7a).
Xxx xxxxxx xxxxxx xxxxx xx xxxxx xxxx x xxxxx jakékoliv xxxxxxxxxx xxxxx x xxxxxxxx a xxxx xxxx xxxxx xxxxxxxxx x xxxxxxxxxxx x xxxxxxxxxxxxxx xxxxxxxx látky xxxx xxxxx xxxxxxxxxx. Xxxx xxxxxxxxx pomohou xxxxxx xxx xxxxxxxxxxx xxxxxxxxxxxx dávkovacího režimu.
Použije xx xxxxxxxx xxxxxxxxx xxxxxxx. Xxxx xxxxxxx xx měla xxxxxx xxxxxxxx léčenou xxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxx s vehikulem, xxxxx xx xxxxxxxxx xxx podávání xxxxxxxx xxxxx xxxxxxx. Xxxx xxxxxxxx se xxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxxx. X pokusnými xxxxxxx x xxxxxxxxx xxxxxxx (xxxxxxxxxxx xxxxxxxxx) xx xxxxxxx stejně xxxx x xxxxxxxxx zvířaty x xxxxxxxxxxxxxx xxxxxxx. Xxxxxxxxx xxxxxxx x xxxxxxxxx xx xxxx xxxxxx vehikulum x xxxxxxxxx xxxxxxxxxx množství (xxxx u xxxxxxxxxxxxxx xxxxxxx x nejnižší xxxxxx).
1.6.4 Limitní xxxxxxx
Xxxxx xxxxxxx xx jedné xxxxxx xxxxx x xxxxxxxx xxxxxxx 1&xxxx;000 xx/xx xxxxxxx xxxxxxxxx xx den xxx xxxxxxx xxxxxxxx xxxxxxxx xxx použití xxxxxxx xxxxxxxxxxxx xxx xxxx xxxxxx žádnou xxxxxxxxxxxx xxxxxxxx xxx x xxxxxxx pokusných xxxxxx xxx x xxxxxx xxxxx, a xxxxx xx xxxxxxxxx účinek xxx na základě xxxxxxxxxxxx xxxxx (např. x xxxxxxxxxxxx x xxxxxxxx strukturou xxxx xxxxxxxxxxxx), xxxx xxxxxxxx xxxxxxxx x xxxxxxxxx xxxxxx xxxxxxxxxxx xxx xxxxxx xxxxx. Xx xxxxx, že xxxxxxxxxxxxx xxxxxxxx u xxxxxxx xx vyžádá xxxxxxx xxxxx xxxxxx xxxxx x xxxxxxx zkoušce. X xxxxxxx způsobů xxxxxxxx xxxxx, jako xx xxxxxxxxx xxxx xxxxx xxxxxxxx, xxxx xxx xxxxxxxxx dosažitelná xxxxxx xxxxxxxx dána xxxxxxxxx-xxxxxxxxxx xxxxxxxxxxx zkoušené xxxxx (např. kožní xxxxxxxx xx neměla xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx).
1.6.5 Xxxxxxxx dávek
Zkoušená xxxxx xxxx xxxxxxxxx xx obvykle xxxxxx xxxxxx xxxxxxxx. Pokud xx používá xxxx xxxxxx xxxxxxxx xxxxx, xxx xx xxxxxxxxxxxxxx xxxxx xxxxxxxxx a xxxxxxxx, přičemž xxxx xxx nezbytné xxxxxxx xxxxxxxxxxxx změny
7a). Zkoušená xxxxx xx xxxxxx xxxxx xxx xxxxxxxxx xx xxxxxxx dobu.
Obvykle xx xxxxx xxx xxxxxxxxxx xxxxxxx xxxxxxx xxxx xxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx. Je xxxx xxxxx xxxxxxx xxxxxx xxxxxxxxx xxxxxx xxxxx xxxxx posledního xxxxxxxxx xxxxxxxx. Xxxxx xx xx měla xxxxxx xx základě xxxxxxxxxxxx xxxxx, xxx xx xxxxxxxxx nadměrné xxxxxxxx x xxxxx.
Xxxxx je xxxx x xxxxxxxxxxxx xxxxx zaznamenána xxxxxxxx xxxxxxxx, xxxx xxxxxxx xxxxxxx se humánním xxxxxxxx xxxxxx. Xxxxx xxxxxxx březích xxxxxxxxx xxxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxxx, xxxx xx xx xxxxxx xxxxxxxx této xxxxxxx. Xx-xx látka podávána xxxxxxxxxxxxxxx xxxxxxxxx xxxxx, xxxx by xx xxxxxxxx xxxxxxxx xxxxxxx xx xxxxx jediné xxxxx pomocí xxxxxxx x výplachu žaludku xxxx xxxxxx xxxxxxxxx xxxxxx. Maximální xxxxxxxx xxxxxxxx, xxxxx lze xxxxxxxxxxx podávat, závisí xx xxxxxxxxx xxxxxxxxx xxxxxxx. Xxxx množství xx nemělo xxxxxxxxx 1 xx/100 x xxxxxxx xxxxxxxxx, x xxxxxxxx vodných xxxxxxx, xxx xxx xxxxxx 2 xx/100 x xxxxxxx hmotnosti. Xxxxx xx xxxx xxxxxxxxx xxxxxxx kukuřičný olej, xxxxxx xx množství xxxxxxxxx 0,4 ml/100 x xxxxxxx xxxxxxxxx. Xxxxxxxx v množství xxxxxxxx xxxxx xx xx xxxx xxxxxx xxxxxxxxxx koncentrací xxx, xxx se xxxxxxxxx xxxxxxxxxx množství xx xxxxx úrovních xxxxx.
1.6.6 Xxxxxxxxx samic
Klinická xxxxxxxxxx xx provádějí x xxxxxxxxxxxxx xxxxxxxxx jednou xxxxx, x to xxxxx xxx xxxxxxx xx xxxxxxx xxxx, x přihlédne xx x xxxx xxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xx xxxxxxxxx. Zaznamená xx xxxx xxxxxxxxx xxxxxx xxxxxx xxxxxxxxx, agónie, xxxxxxxxxxxx xxxx chování x xxxxx xxxxxxxx xxxxxx toxicity.
1.6.7 Tělesná xxxxxxxx a xxxxxxxx xxxxxx
Xxxxxxx xxxxxxx xx xxxxx během xxxxxxx xxx xxxxxxx anebo xxxxxxxxxx 3.xxx gestace, xxxxx xxxxxxx chovatel xxxxxx xxxxxxx xxxxxxx xxxxxxx xx xxxxxxx xxxx x dále xxxxx xxxxxxx dne xxxxxxxx látky, xxxxxxxxx xxxxx 3.den v xxxxxx xxxxxxxx xxxxx x v den xxxxxxxxxxx usmrcení.
Spotřeba xxxxxx xx xxxxxxxxx x xxxxxxxxx xxxxxxxxx x xxxx by xx xxxxxxxx xx xxx xxxxxxxxxx tělesné xxxxxxxxx.
1.6.8 Xxxxx
Xxxxxx xx xxxxxx xxxxx xxx xxxx xxxxxxxxxx xxxx xxxx. Xxxxxx xxxxxxxxxx xxxxxx xxxxxxx nebo xxxxxxxxxxx xxxx xxxxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxx xx usmrtí x xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx.
Xxxxxx se x xxxxxxxx xxxxxxxx xxxx xxxxx xxxxx xxxxxx xxxxxxxxxxxxx xxxxxxx xx xxxxxxxxxx odchylky xxxx xxxxxxxxxxx xxxxx. X cílem xxxxxxxxxxxxx xxxxxxxxxxxxxx xx xxxxxxxxxxx xxxxx během xxxxxxxxxx xxxx x následná xxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxx xxx xxxxxxxx xxxxxxxxxxxxxx skupiny.
1.6.9 Xxxxxxxxx xxxxxxxxx xxxxxx
Xxxxxxxx xx usmrcení xxxx xx xxxxxxxx xx xxxxxxx xx xxxxxxx xxxxx děloha x xxxxxx se xxxx xxxxxxxx. Xxxxxx, xxxxx xxxxxxxx o graviditě, xx dále xxxxxxx (xxxx. xxxxxx barvení xxxxxxxx xxxxxxx x xxxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxx nebo xxxxxxx xxxxxxxxxxxx metodou x xxxxxxx) a xxxxxxx se negravidní xxxx
7a).
Xxxxxxxx děloha xxxxxx xxxxxxxxx xxxxx xx xxxxx. Xxxxxxxx xxxxxxxx xxxxxx by se xxxxxx zjišťovat u xxxxxxxxx xxxxxx, která xxxxx studie xxxxxxx.
X xxxxxxx pokusných zvířat xx xxxxxx xxxxx xxxxxxx xxxxxxx.
X děložního xxxxxx se vyšetří xxxxx úhynů embrya xxxx plodu x xxxxx xxxxxxxxxxxxxxx plodů. Xxxxxx xx stupeň xxxxxxxx, xxx xxxx xxxxx xxxxxxxxx xxxxxxxxx xxxx xxxxxxx xxxxxxx (xxx část 1.2).
1.6.10 Xxxxxxxxx plodů
Zjistí se xxxxxxx a tělesná xxxxxxxx xxxxxxx plodu.
U xxxxxxx xxxxx xx xxxxxxx xxxxx odchylky
7a).
U xxxxx xx xxxxxxx xxxxx xxxxxx a xxxxxxx xxxxx (např. xxxxxxxx x xxxxxxxxxx xxxx anomálie)
7a). Xxxxxxxxxxxx xxxxxxxxx změn je xxxxxx, xxx nikoli xxxxxxxx. Pokud xx xxxxxxxxxxxx xxxxxxx, xxxx xx xx xxxxx xxxxxxxx kritéria definování xxxxxxxxxxxx xxxxxxxxx. Xxxxxxxx xxxxxxxxx xx xxxxx xxxxxxx xxxxxxxxxxxx soustavě, xxxxx xx vyšetří xx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxx.
X hlodavců xx xxxxxxxx přibližně xxxxxxxx xxxxxxx xxxx, x xxxxx xx xxxxxxx xxxxx xxxxxxx. Xxxxxx se xxxxxxxx x vyšetří xx xxxxxxxxxx změn xxxxxxx xxxxx xxxxxx uznaných xxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxxxx histologických xxxx xxxx xxxxxxxx xxxxx.
X nehlodavců, xxxx. xxxxxxx, se prozkoumají xxx změny xxxxxxx xxxxx, tak xxxxx xxxxxxx xxxxx xxxxx. Xxxxxxxx oddělením xxxxx xx u xxxxxx xxxxx xxxxxxx xxxxx xxxxxxx tkání, xxxxxxx xxxxx může xxxxxxxxx x xxxxxxx xxx xxxxx xxxxxxxxxxx xxxxxxx xxxxxx srdce
7a). Xxxxx xxxxxxxx plodů zkoumaných xxxxx způsobem se xxxxxx x použijí xx x xxxxxxxxxxx xxxx xxxxxxx xxxxx (xxxxxx xxx, xxxxx, xxxxxxx xxxxx x xxxxxx), x xx xxxxxx standardních metod xxxxxxxxxx xxxxxxxxxxxx) nebo xxxxxx xxxxxxxxx xxxxx. Xxxx xxxxxx x xxxxxxxxxxx xxxxxxxxxxxx plodů xx připraví x xxxxxxx na xxxxxxxxxx xxxx xxxxxxx za xxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxx xxxxxxxx.
2 XXXX
2.1 ZPRACOVÁNÍ XXXXXXXX
Xxxxxxxx xx xxxxxxxxxxx xx xxxxxxx xxxxxxxxxx pro xxxxxx a xxx xxxxxx xxxxxxx x x xxxxx xxxxxxx xxxxxxx x každé xxxxxxxx xx uvede xxxxx pokusných xxxxxx xx xxxxxxx zkoušky, xxxxx pokusných zvířat xxxxxxxxx během xxxxxxx xxxx xxxxxxxxxx z xxxxxxxxx důvodů, doba xxxxx xxxx humánního xxxxxxxx, počet xxxxxxx xxxxx, xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx příznaků xxxxxxxx xxxxxxxx xxxxxx xxxxxxx, trvání x xxxxxxxxxx xxxxxxxxxx toxických xxxxxx, typy xxxxxxxxxx xxxxxx/xxxxx x xxxxxxx xxxxxxxx údaje o xxxx.
Xxxxxxxxx xxxxxxxx se xxxxxxxxx vhodnou xxxxxxxxxxxx xxxxxxx, přičemž xxxx xxxxxxxx xxxxxxx xxx xx použije xxx. Xxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxxxxxx metoda; xxxxx xx xxxx xxxxxxx xxxxxx xxxxxx x xxxx být xxxxxxxxxx. Xxxxxx xx xxxxxx xxxxx získané x pokusných zvířat, xxxxx xxxxxxxxx až xx plánovaného usmrcení. Xxxx údaje xxx x xxxxxxx potřeby xxxxxxxx xx xxxxxxxxxxx xxxxxxx. Xxxxxx údajů xxxxxxxxx od xxxxxx xxxxxxxxx xxxxxx x xxxxxx xxxxxxxx xxxx xxxxxxxxxx xx xxxxxxx xxxxxxx xx xxxx xxx xxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxx.
2.2 XXXXXXXXX XXXXXXXX
Xxxxxxxx studie xxxxxxxxxx xxxxxxxx xxxxxxxx se xxxxxxxxx na xxxxxxx xxxxxxxxxx xxxxxx. Vyhodnocení xxxx xxxxxxxxx následující xxxxxxxxx:
- výsledky xxxxxxx x xxxxx x xxxxxx/xxxxx, xxxxxx xxxxxxxxx xxxxx xxxx xxxxxx xxxxxxx xxxx xxxxxxxx xxxxxxxxx xxxxxx zkoušené xxxxx a výskytem x xxxxxxxxxx xxxxx xxxxxx,
- xxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxx xxxxxxx xxxx, změn xxxxxxx xxxxx x xxxxxxx x xxxxx, pokud xxxx tato xxxxxxxxxxxx xxxxxxxxx,
- xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx k xxxxxxxx xxxxxxxxx xxxxxxxx xxxxxx,
- xxxxxxx xxxxxxx xxxxxxxxx xxx výpočtu xxxxx xxxxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxx,
- xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxx, xxxxx xx měla zahrnovat xxxxxxxxxx informace x xxxxxx xxxxxxx, aby xxxxxxxxx xxxxxxxxxxx xxxx xxxx analýzu přehodnotit x xxxxxxxxxxxxxx.
X xxxxxxxxx xxxxxx, xxxxx prokazuje xxxxxxxxxxxx xxxxxxxxx xxxxxx, xx xxxxx xxxxxx xxxxx xxxxxxx pro xxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx.
2.3 XXXXXXXXXXXX XXXXXXXX
Xxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx x xxxxxx opakované xxxxxxxx xxxxx xx březí xxxxxx x xx xxxxxxxxxxxx xxxxx xxxxxx xxxxxxxxx. Xxxxxxxx xxxxxx xx xxxx být xxxxxxxxx x souvislosti x výsledky xx xxxxxxxxxxxxxx, reprodukčních, toxikokinetických x xxxxxxx xxxxxx. Xxxxxxxx k xxxx, xx se xxxxx xxxxx jak na xxxxxxxxx všeobecnou toxicitu x xxxxxxxx xxxxx, xxx i xx xxxxxxxxx xxxxxxxx, umožní xxxxxxxx této xxxxxx xx xxxxxx xxxx xxxxxxxx mezi vývojovými xxxxxx xxxxxxxxxxxxx se x xxxxxxxxxxxxx všeobecné xxxxxxxx x mezi xxxxxx xxxxxxxxxx xxxxx xx xxxxxxxx, xxxxx xxxx xxxxxxx x xxx xxxxx xxxxxxx xxxxxxx
7a).
3 XXXXXXX XXXXXX, XXXXXXXX POKUSU X XXXXXXXXX XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9),10) musí xxx xxxxxxxxx xxxxxxx xxxxxx x x xxxxxxx xxxxxx je nutno xxxx protokol.
3.1 Zpráva x xxxxxxx xxxxxx xxxxxxxx xxxxxxxxxxx informace.
Zkoušená xxxxx:
- xxxxxxxxx povaha, x je-li to xxxxxxxx, fyzikálně-chemické xxxxxxxxxx,
- xxxxxxxxxxxx xxxxxx xxxxx XXX, xx-xx xxxxx xxxx přiděleno, xxxxxxx.
Xxxxxxxxx (xxxxx xxxx použito):
- xxxxxxxxxx xxxxxx xxxxxx xxxxxxxx, xxxxx není xxxxxxx xxxx.
Xxxxxxx xxxxxxx:
- xxxxxxx druhy a xxxxx,
- xxxxx x xxxxx pokusných xxxxxx,
- xxxxx, xxxxxxxx xxxxx, xxxxxx xxx.,
- individuální xxxxxxxxx pokusných xxxxxx xx xxxxxxx xxxxxxx.
Xxxxxxxx xxxxxxxx:
- xxxxxxxxxx xxxxxx xxxxxx xxxxx,
- xxxxxxxxxxx x xxxxxxxx xxxxxxx xxxxxxxx xxxxx/xxxxxx, xxxxxxxx xxxxxxxxxxx, xxxxxxxxx x xxxxxxxxxx přípravku,
- podrobné xxxxx o xxxxxxxx xxxxxxxx xxxxx,
- x xxxxxxx potřeby xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx (xxx) x krmivu/pitné xxxx xx skutečnou xxxxx (mg/kg xxxxxxx xxxxxxxxx na den), xx-xx xx možné,
- xxxxxxxx xxxxxxxxx,
- podrobné xxxxx o xxxxxxx xxxxxx x xxxx.
Xxxxxxxx:
Xxxxx x xxxxxxxxxx toxicity x xxxxx xxxxx xxxxx, např.:
- počet xxxxxxxxx xxxxxx xx xxxxxxx xxxxxxx, xxxxx xxxxxxxxx xxxxxx, xxxxx xxxxxxx, počet xxxxxxx xxxxxxxxx xxxxxx, xxxxx xxxxxxxxx xxxxxx, která xxxxxxxxx, a xxxxx xxxxxxxxx zvířat, xxxxx xxxxxxxxx xxxxx,
- den xxxxx xxxxx studie xxxxx zda xxxxxxx xxxxxxx xxxxxxx až xx xxx xxxxxxxx,
- xxxxxx xx xxxxx x pokusných xxxxxxxxx, xxxxx xxxxxxxxx do xxxxxxxxxxx usmrcení, xxxxxxxxx xx však xx xxxxxxxxxxxxx srovnání dat xxx skupiny,
- xxx xxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxx a xxxx následný průběh,
- xxxxxxx xxxxxxxx, xxxxx xxxxxxx hmotnosti x xxxxxxxxx xxxxxxxx xxxxxx, xxxxxx xxxxxxxxxx xxxxx x změně xxxxxxx xxxxxxxxx xxxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxx,
- xxxxxxxx xxxxxx, xxxx-xx xx, xxxxxxxx xxxx,
- xxxxxxx xxxxxx xxxxxx xxxxxxx hmotnosti,
- xxxxxxxxxxx xx xxxxxxx XXXXX xxx xxxxxx xx xxxxx x xxxxxxxx xxxxxx.
Xxxxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxx xxx xxxx x xxxxxxxxxx, xxxxxx
- xxxxx žlutých xxxxxxx,
- xxxxx xxxxxxxxxx, xxxxx x xxxxxxxx xxxxxx x xxxxxxx xxxxx x xxxxxxxx,
- xxxxx xxxxxxxxxxxxxx podílu xxx- x post-implantačních xxxxx.
Xxxxxxxxx xxxxxxxx xxxxxxxx xxxxx dávky pro xxxx x xxxxxx xxxxx, xxxxxx
- počtu x xxxxxxxxxxxxxx podílu xxxxxx xxxxxxx,
- xxxxxx xxxxxxx,
- fetální tělesné xxxxxxxxx, xxxxx možno xxxxx xxxxxxx a xxx xxx xxxxxxx xxxxxxxxx,
- xxxxxxx malformací, xxxxxxxxxx xxxxxxx tkání x skeletu a xxxxxx xxxxxxxxxx xxxxxxxx,
- xxxxxxxx kritérií xxxxxxxxxxxx,
- xxxxxxxxx počtu a xxxxxxxxxxxxxx xxxxxx xxxxx x xxxx s xxxxxxxxxx xxxxxxx a xxxxxxxxxx odchylkami, odchylkami xxxxxxx xxxxx x xxxxxx xxxx x xxxxxxx xxxxxxxxxxxxxx xxxxxxxx x jiných xxxxxxxxxx xxxxxxxx.
Xxxxxxx x interpretace xxxxxxxx.
Xxxxxx.
X.32 XXXX XXXXXXXXXXXXX
1 XXXXXX xx x xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
1)1.1 Xxxxxxx xxxxxx
Xxxxxxxxx látka xx xxxxxxxx obvykle 7 xxx x xxxxx, xxxxxxx xxxxxx, xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, 1 xxxxx na xxxxxxx, po xxxxx xxxx xxxxxx zvířat. Xxxxx x po xxxxxxxx xxxxxxxxx xxxxx xxxx zvířata xxxxx xxxxxxxxxx xx účelem xxxxxxxxx xxxxxxx xxxxxxxx, xxxxxxx xxxxxx xxxxxx.
1.2 Xxxxx metody
Pokusná zvířata xxxx xxxxxxx x xxxxxxx xx xxxx, xxxxxxx a xxxxx x xxxxxxx s xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) a xxxxxxxx xxx, xxx xxxx možná xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx právního xxxxxxxx.
10) Xxxx testem xx xxxxx xxxxxx xxxxxxx xxxxxxx xxxxxxx do xxxxxxxxxxx x xxxxxxxxxxxx xxxxxx.
1.3 Xxxxxxxxxxxxxx xxxxxxx
Xxxxxxxxxxxx xxxxxx xx xxxxxx. Xx xxxxxxx xxxxxxxxxxx xxxxxx je xxxxx xxxxxx x xxxxx xxxxx (xxxxxxxx x xxxxxxxxxx). Používají xx xxxxxx xxxxx xxxxxxx x xxxxx chovaných xxxxx laboratorních zvířat. Xxxxxxxx by měla xxx započata xx xxxxxxxx xx xxxxxxxxx xxxxxx. Xx xxxxxxx xxxxxx xx neměl xxxxxx x xxxxxxxxx xxxxxx činit xxxx xxx ± 20% xx průměru. V xxxxxxx, že xxxxxxx xxxxxx xxxxxxxxx xxxx xxxxxxxxxxxx xxxxxx xxxxxxxx, xx xxxxx xxxxxx xxxxxx druh x xxxx x obou xxxxxxxx.
1.4 Xxxxx x xxxxxxx
Xxx xxxxxxxx se xxxxx xxxxxxx 100 xxxxxx (50 xxxxx x 50 xxxxx) xxx xxxxxx xxxxxx xxxxx a souběžná xxxxxxxxx xxxxxxx. Xxxxxx xx xxxx být xxxxxxxxx a xxxxxxxxxx. Xx-xx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxx, xxxxx xx xxxxx xxxxxx x xxxxx zvířat, xxxxx budou takto xxxxxxxx před xxxxxx xxxxxx.
1.4.1 Xxxxxxx xxxxxx x xxxxxxxxx xxxxxxx
Xxxxx xx xxx xxxxxxxxx xxx xxxxxxx xxxxxx xxxxx xxxxxxxx kontrolní xxxxxxx. Nejvyšší xxxxxxx xxxxxx xx xxxx xxxxxxx xxxxxxxx minimální xxxxxxxx, xxxx je xxxxx xxxxxx váhových xxxxxxxxx (xxxx xxx 10 %), xxx xxxxxxxxxxxxxx xxxx xxxxxxxx xxxx xxxxxx xxxxxx xxxxxx účinky xxx xxxxxx.
Xxxxxxxx xxxxxxx xxxxxx xx xxxxxx xxxxxxxxxxxx x normálním xxxxxx, xxxxxxx a xxxxxx xxxxxx xxxxxxx nebo xxxxxxx xxxxxxxx xxxxxx xxxxxxxx. Obecně by xxxxxx xxx xxxxx xxx 10% vysoké xxxxx. Xxxxxxx xxxxx/xxxxx xx xxxxx xxxxxxxx xx středním xxxxx xxxx xxxxxxx x xxxxxx dávkou.
Volba dávkových xxxxxx by xxxx xxxx x úvahu xxxxxxxxx xxxxx a xxxxxx toxicity.
Expozice xx xxxxxxx xxxxxxx xxxxx. Xx-xx látka xxxxxxxx x xxxxx vodě xxxx xxxxxxxxx do xxxxxxx, měla xx xxx xxxxx k xxxxxxxxx.
1.4.2 Kontroly
Souběžná kontrolní xxxxxxx xx identická x každém ohledu x xxxxxxxxxxx skupinou, xxxxx xxxxxxxx xxxxxxxxx xxxxx.
Xx xxxxxxxxxx případech, xxxx xxxx xxxxxxxxx xxxxxx x aerosoly xxxx xxxxxxx-xx se xxx xxxxxx xxxxxxxx xxxxxxxxxx, xxxxx biologická xxxxxxxx není xxxxxxxxxxxxxxxx, xxxxxx xx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx, xxxxx xxxx xxxxxxxxxx xxx xxxxxxxx.
1.4.3 Způsob xxxxxxxx
3 hlavní xxxxx xxxxxxxx xxxx xxxxxx, xxxxxxxx x xxxxxxxxx. Xxxxx xxxxxxx podání xxxxxx xx xxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxxxxxx způsobu xxxxxxxx x člověka.
1.4.3.1 Xxxxxx xxxxxx
Xxx, kde se xxxxxxxxx xxxxx vstřebává x gastrointestinálního xxxxxx x xx-xx xxxxxx xxxxx x xxxx, xxxxx xxxx být xxxxxxxxx xxxxxx, dává xx přednost xxxxxx xxxxxxxx, xxxxx xxxxxx xxxxx tomu nějaké xxxxxx. Xxxxxxx mohou xxxxxx xxxxxxxxxx látku x potravě, rozpuštěnu x xxxxx xxxx xxxx podanou v xxxxxxx.
Xxxxxxx xx se xxxx xxxxx xxxxxxx 7 xxx x xxxxx, xxxxxxx dávkování 5 xxx x xxxxx může xxxx x xxxxxxxx xxxxxxxx xxxx naopak xxxxxxx "xxxxxxxxxxx" xxxxxxxx x xxxxxx xxx xxxxxxxx, x tudíž xxxxxxxx xxxxxxxx a xxxxxxxx xxxxxxxxx. Nicméně, především x ohledem na xxxxxxxxx xxxxxxx, xxxxxxxxx xxxxxxx xxxxx je xxxxxxxxxx xx xxxxxxxxxx.
1.4.3.2 Xxxxxxxx studie
Aplikace xxxxx xx xxxx může xxx xxxxxxx xxxx xxxxxxxx hlavní xxxxx xxxxxx x xxxxxxx x xxxx modelový xxxxxx xxxxxxxx kožního xxxxxxxxx.
1.4.3.3 Xxxxxxxxx xxxxxx
Xxxxxxx xxxxxxxxx studie xxxx xxxxxxxxx xxxxxxxxxxxxxxx xxx xxxx xxxxxxx xxxxxxxx, xxxx zde uvedeny xxxxxxxxxx informace x xxxx xxxxx xxxxxx. Xxxxxxxxxxxxxxx xxxxxxxxx xxxx xxx platnou alternativou xx xxxxxxxxxxxx xxxxxxxxx.
Xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx, xxxxx zvíře xx xxxxxxx xxxxxxxxxx po xxxxxxxx xxxxxxxxxxx 6 xxxxx xxxxx xx 5 xxx x xxxxx (xxxxxxxxxxx expozice), xxxx x návaznosti xx možnou xxxxxxxx x prostředí, 22-24 xxxxx denně xx 7 xxx x xxxxx (xxxxxxxxxxx xxxxxxxx), x xxxxxxxxx 1 xxxxxxx xxx xxxxxx xxxxxx xxxxx ve xxxxxxx xxxx xxx, xxxxxxxx x pro xxxxxxx expozičního xxxx. X xxxx xxxxxxxxx xxxx xxxxxxx obvykle xxxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxxx látky. Xxxxxx xxxxxx xxxx xxxxxxxxxxxx x stálou xxxxxxxx xx x tom, xx v první xx xxxxx 17-18 xxxxx xx xxxxx xxxxxx xxxxx expozice x xxxxx delším xxxxxxx xxxxx xxxxxxx.
Xxxxx xxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxx xxxxxx xx xxxxxx xxxxxx x xx xxxxxx xxxxxxxx, xxxxx xx xxx xxxxxxxxxx. Nicméně, je xxxxx xxxx v xxxxx určité xxxxxxxxx xxxxxx. Xxxxxxxxx, xxxxxx xxxxxxxxxxx xxxxxxxx pro xxxxxxxx podmínek xxxxxxx xxxxxxxxx mohou xxx xxxxxxxx nutností pití x krmení xxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxxxxxxx (x xxxxxxxxxx) xxxxxxxx xxxxxxxx nebo xxxxxx koncentrace par x xxxxxxx xxxxxxxxxxxx.
Xxxxxxxxx xxxxxx
Xxxxxxx xx xxxxxxxx x xxxxxxxxxxx xxxxxxxx, xxxxxxx xxxxxxxxxx zaručuje xxxxxxxxx proud pro xxxxxxx 12 xxxxx xxxxxxx za hodinu, xxx byl xxxxxxxx xxxxxxxxxx přísun kyslíku x xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx. Xxxxxxxxx x expoziční xxxxxx xx xxxx xxx xxxxxxxxxx xxxxxxxxxx, xxx xxx xxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx xx xxxxx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx xxxxx. Xxxxxx komory xx xxxxxxx udržuje xxxxx xxxxxxx x tím xx xxxxx úniku xxxxxxxxx látky xx xxxxxxxx xxxxxxxxx. Xxxxxx xx měly xxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxx. Xxxxxx by v xxxxx xxxxxxx xxxxxxxx xxxxxxxxx x komoře xxxxx xxxxxx xxxxx xxxxxxxxxx 5 % xxxxxx komory.
Měření nebo xxxxxxxxxxxx zahrnuje:
(a) Xxxxxx xxxxxxx: xxxxxxxx xxxxxxx xxxxxxx xxxxxxx xx xxxx xxx xxxxxxx xxxxxxxxxxxx kontinuálně.
(b) Xxxxxxxxxxx: xxxxx denní xxxxxxxx xx xxxxxxxxxxx testované xxxxx neměla xxxxxxx xxxx xxx ±15% xxxxxxx xxxxxxx.
(x) Xxxxxxx x xxxxxxx: xxx xxxxxxxx, xxxxxxx by xxxx být udržována x rozmezí 22 ± 2 °C x vlhkost x xxxxxxxx 30 - 70 % vyjma xxxxxxx, xxx je xxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxx x atmosféře komory. Xxx xxxxxxxxx by xxxx xxx xxxxxxxxxxxx xxxxxxxx.
(x) Xxxxxx xxxxxxxxx xxxxxx: xxxxxxx se xxxxxxxxxx velikostí xxxxxx x xxxxxxxxx komor x xxxxxxxx nebo xxxxxxx xxxxxxxx. Xxxxxxxxxx xxxxxxx mají být x respirabilní xxxxxxxxx xxx použité xxxxxxxxx xxxxx. Xxxxxx xxxxxxxxx xxxxx xx xxxxxxxxx x xxxxxxx zóny xxxxxx. Xxxxxx xxxxxxx xx xxx xxxxxxxxxxxxxxx xxx distribuci částic, xxxxxx xx xxxxx xxxxxxxxxx, a xxxxxxxxxxxxx xx odpovídat xxxxxx xxxxxxxxxxxxxx aerosolu, x xxxx xxxxxx xxxx xxxxxxxx xxxx respirabilní. Xxxxxxx xxxxxxxxx xxxxxx xx provádí často xxxxx xxxxxx xxxxxxxxxxxx xxxxxxx, xxx se xxxxxxxxx xxxxxxxxx xxxxxxxx, x xxxx během xxxxxxx xxx často, xxx bylo xxxxx xxxxxxxx stabilitu distribuce xxxxxx, xxxxxx xxxx xxxxxxx xxxxxxxxxx.
1.4.4 Trvání xxxxxx
Xxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxxx xxxx života xxxxxxx použitého xxx xxxx. Xxxx by xxx být xxxxxxx x 18 xxxxxxxx x myší a xxxxxx a 24 xxxxxxxx x xxxxxxx. Xxxxxxx, xxx xxxxxxx xxxxx zvířat s xxxxx dobou života, xxxxxxxxxx s nízkým xxxxxxxxxx xxxxxxxx tumorů, xx xxxx xxxxxxxx xxxxxx xxxx xxx xx 24 xxxxxx xxx myši a xxxxxx x za 30 xxxxxx xxx xxxxxxx. Xxxxxxxxxxxx, xxxxxxxx xxxxxx xxxxxxxxxxx studie xx xxxxxxxxxx, xxxx xxxxx xxxxxxxxxxxxx x xxxxxxxx xxxxx xxxx x kontrolní skupině xxxxxx xx 25 %. Xxx xxxxxxxx xxxxx, xx xxxxxx xx xxxxxxxx sexuální xxxxxx odpovědi, xx xxxxx xxxxxxx xxxxxxxx xxxxxx. Xxx, kde xxxxx xxxxxxxxx xxx xxxxxxx s xxxxxxx xxxxxx xx zjevných xxxxxxxxx xxxxxx, xxxxxx xx nutně vést x xxxxxxxx xxxxxx xxxxx, xxxxx ostatní xxxxxxx nevykazují toxické xxxxxxx, xxxxx by xxxxxx xxxxxxxx. Xxx xxxx možno xxxxx xxxxxxxxx výsledek xxxxx, xxxxx xxx xxxxxx xxxxxxxxxxxx xxxxx (xxxxxxxxx, xxxxxxxxxxxx xxxx x xxxxxxxx chyb obsluhy) x xxxxx xxxxxxx xxxxx xxx 10% x xxxxxxx xx xxxxx xxxxxxxxx nesmí xxx xxxxx xxx 50% x 18 xxxxxxxx x xxxx x xxxxxx x x 24 xxxxxxxx x xxxxxxx.
1.5 Xxxxx xxxxxxx
1.5.1 Xxxxxxxxxx
Xxxxx xxxxxxxxxx xxxxxx x klecích xxxxxxxx xxxxx xxxx x xxxxx, xxx x xxxxxxx, jakož x xxxxxxxxx, xxxxxxxxx, xxxxxxxxxxx a xxxxxxxxxxx xxxxxxxxx systému, somatomotorické xxxxxxxx x xxxxxxx.
Xxxxxxxxxx xxxxxxxx zvířat je xxxxx, aby xx xxxxxxxxx ztrátám zvířat xx studie v xxxxxxxx xxxxxxxxxxx, xxxxxxxx xxxxx xxxx xxxx x xxxxxxx. Xxxxxxx x agónii xxxx xxxxxxxx x xxxxxxx.
Xxxxxxxx xxxxxxxx a xxxxxxxxx xx měly být xxxxxxxxxxx x xxxxx xxxxxx. Zvláštní xxxxxxxxx xx xxxxx xxxxxxx xxxxxx xxxxxx: xxxx xxxxxxxx, xxxxxxxxxx, rozměry, xxxxxx a xxxxxxxx xxxxxxx xxxxxxxxxxx či xxxxxxxx tumoru se xxxxxxxxxxx.
Xx xxxxx provádět xxxxxx spotřeby xxxxxxx (x xxxx xxx, xxx xx xxxxxxxxx xxxxx podávána x xxxxx xxxx) xxxxx xxxxx prvních 13 xxxxx a xxx xxxxxxxxx xx tříměsíčních xxxxxxxxxxx, xxxxxx by xxxxxxxxx xxxx nebo xxxxx tělesné hmotnosti xxxxxxx nutnost xxxx xxxxxxxxx xxxxxxxxx.
Xxxxxxx xxxxxxxxx xx xxxxxxxxxxxxx individuálně x všech xxxxxx xxxxxx xxxxx během xxxxxxx 13 xxxxx xxxxxx xxxxx x xxxxx xxxxxx xx xxxxx týdny po xxxxx xxxxxx.
1.5.2 Klinická xxxxxxxxx
1.5.2.1 Xxxxxxxxxxx
Xxxxx xxxxxxxxxx xxxxxx x klecích xxxxxx o zhoršeném xxxxxxxxxx xxxxx xxxxxx xxxxx xxxxxx, xx xxxxx xxxxxxxx diferenciální xxxxx xxxxxx xxxxxxx.
Xx 12 xxxxxx, za 18 xxxxxx x xxxx xxxxxxxxx xxxxxx xx provede xxxxxx xxxxx xx xxxxx xxxxxx. Xxxxxxxxxxx bílých xxxxxxx xx xxxxxxx xx xxxxxxxx xx xxxxxx ve xxxxxxx x nejvyšší dávkou x x xxxxxxx. Xxxxx xxxx data, xxxxxxx údaje xxxxxxx xxxx utracením, xxxx xxxxx x vyšetření xxxxxxxxxxxxx xxxx xxxxxxx xxxxxxx, diferenciál xx xxxxxxx x x xxxxxxx x xxxxxx xxxxxxxx nižší, xxx xx vysoká dávka.
1.5.2.2 Xxxxx
Xxxxxxxxx xxxxx xx xxxx být xxxxxxxxx x xxxxx zvířat, xxxxxx xxxx, která xxxxxxx xxxxx pokusu xxxx byla utracena, xxxxxxx byla nemocná. Xxxxxxx xxxxxxxxx xxxxxx xxxx léze, nebo xxxx, xxxxx by xxxxx xxx xxxxxx, xx třeba xxxxxxx.
Xxxxxxxxxxx xxxxxx a xxxxx xx měly xxx xxxxxxxx xx vhodných xxxxxxx xxx xxxxx xxxxxxx histopatologické xxxxxxxxx: xxxxx (včetně xxxx xxxxxxxxxxx xxxxx/xxxxx, xxxxxxxxx xxxx, kory xxxxxxx), xxxxxxxx xxxxxxx, štítná xxxxx x příštítná xxxxxxx, tkáň xxxxx, xxxxxxx x xxxxx, xxxxx, aorta, xxxxxx xxxxx, játra, xxxxxxx, xxxxxxx, xxxxxxxxxx, xxxxxxxx, xxxxxx, xxxxxx, xxxxxxxxx xxxxxxxx orgány, xxxx, xxxxx, xxxxxxx, xxxxxxxxxxxx, xxxxxxx, ileum, slepé xxxxxx, xxxxxxx, xxxxxxxx, xxxxxx xxxxxx, reprezentativní xxxxxxxxxx uzlina, xxxxxx xxxxxx xxxxx, xxxxxxxxx xxxxxx, xxxxxxxxx nerv, xxxxxxx s xxxxxx xxxxx, stehenní kost xxxxxx xxxxxx, mícha xx xxxxx xxxxxxxx (xxxxx, xxxxxxx xxxxxx x xxxxxxx) a xxx.
Xxxxxxxx plic x xxxxxxxx xxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxx xxxxxxxx těchto xxxxx. Xxxxxxxx xxxx x xxxxxxxxxxx xxxxxxxx xx xxxxxxx pro xxxxxxxxxxxx xxxxxxxxxxxxxxxx vyšetření. X xxxxxxxxxxx xxxxxxxx by xxx xxx xxxxxxx xxxx xxxxxxxxxx xxxxx xxxxxx nosní xxxxxx, xxxxxx x xxxxxx.
1.5.2.3 Xxxxxxxxxxxxxxxx vyšetření
(a) Xxxxx xxxxxxxxxxxxxx se provede x xxxxxxxx x xxxxxxx xxxxx xxxxxx, xxxxx xxxxxxx xxxx xxxx xxxxxxxx xxxxx xxxxx x x xxxxx zvířat xxxxxxx xxxxxxxxx x x xxxxxxxx dávkou.
(b) Xxxxxxx xxxxxx viditelné okem x Xxxx, které xxxx xxxxxxxxx xxxx xxxxxx, xx xxxxxxx xxxxxxxxxxxxx x všech xxxxxx.
(x) Je-li xxxxxxxx xxxxxx x incidenci xxxxxxxxxxxxxx xxxx xxxx xxxxxxxx s vysokou xxxxxx x kontrolní xxxxxxxx, xxxxxxxxxxxxxxxx vyšetření xx xxxxxxx x xxxxx xxxxxx xx xxxxx x x xxxxxxx xxxxxxxxx.
(x) Je-li xxxxxxx xx xxxxxxx x xxxxxxx dávkou xxxxxxxxx nižší xxx x xxxxxxx, xxxx xx být kompletně xxxxxxxx x xxxxxxx x xxxxxxxxx nižší xxxxxx.
(x) Xx-xx xx xxxxxxx x xxxxxxx xxxxxx xxxxxx x xxxxxxxx toxických nebo xxxxxx účinků, xxxxx xx xxxxx ovlivnit xxxxxxxxxxxxx odpověď, xx xxxxx kompletně vyšetřit xxxxxxxx xxxxx xxxxxxxx xxxxxx.
2 ÚDAJE
Údaje se xxxxxxxxxx xx xxxxx xxxxxxx, xxxxxxxxxxx xxx xxxxxx testovanou xxxxxxx xxxxx xxxxxx xx xxxxxxx xxxxx, xxxxx xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx během xxxxx, xxxx xxxxxx xxxxxxxxx x xxxxx xxxxxx x tumory xxx xxxxxxxx. Xxxxxxxx se xxxxxxx odpovídající xxxxxxxxxxxx xxxxxxx. Xxxxx být xxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxx metody.
3 PROJEKT XXXXXX, XXXXXXXX XXXXXX X ZÁVĚREČNÁ ZPRÁVA
V xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx x x xxxxxxx xxxxxx je xxxxx vést protokol.
Zpráva x testu xxxx xxxxxxxxx následující xxxxxxxxx:
- xxxxxxxxx xxxx, xxxx, xxxxx, podmínky xxxxxxxx, xxxxx,
- xxxxxxxx xxxxx:
Xxxxx xxxxxxxxxxx xxxxxxxx:
xxxxxx xxxxxxxxxx, xxxx, xxxxxxx, zdroje xxxxxxx, systému xxx xxxxxxxxx xxxxxx a xxxxxxxx, metody klimatizace, xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxxxx x xxxxxxxxx x xxxxxxx xxxxxxxx xxxxxx x xxxxxxxxxx xxxx, xxxxx se xxxxxxx. Xxxx xx xxxxx xxxxxx xxxxxxxx xxx xxxxxx teploty, xxxxxxxx, x xxx, kde xx to xxxxxxx, xxxxxxxxx koncentrace nebo xxxxxxxxx xxxxxx xxxxxxxx. Xxxxx o xxxxxxxx: xx formě xxxxxxx xxxxxx xxxxxxxxxx xxxxxx x variability (xxxx. xxxxxxxxxx odchylka) x xxxx xx zahrnovat:
(a) xxxxxxxx xxxxxxx xxxxxxx x xxxxxxxxxx xxxxxxxx,
(x) xxxxxxx a vlhkost xxxxxxx,
(x) xxxxxxxxx xxxxxxxxxxx (xxxxxxx xxxxxxxx testované xxxxx xxxxxxxxxx do xxxxxxxxx aparatury děleno xxxxxxx xxxxxxx),
(x) povahu xxxxxxxx, xx-xx xxxxxxx,
(x) xxxxxxxx xxxxxxxxxxx v xxxxxxx xxxx,
(x) xxxxxx xxxxxxxxx částic (xxx xxx xx xxxxxxxxxx),
- xxxxxxx úrovně (xxxxxx xxxxxxxx, xx-xx užito) x xxxxxxxxxxx,
- xxxxxxxxx xxxxxx xxxxx xxxxxxx, xxxxx x xxxx xxxxxx,
- xxxx úmrtí xxxxx xxxxxx xxxx xxx zvířata xxxxxxx xx xx xxxxx,
- xxxxxx xxxxxxxxx xxxxxx xxxxx xxxxxxx x xxxxx,
- popis xxxxxxxxx x jiných xxxxxx,
- xxxx, xxx byl xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx a xxxx xxxxx vývoj,
- xxxx x spotřebě xxxxxxx x xxxxxxx xxxxxxxxx,
- xxxxxxx hematologické testy x xxxxxxxx,
- xxxxxx xxxxxxxxxxx-xxxxxxxxxx,
- detailní popis xxxxx xxxxxxxxxxxxxxxxxx nálezů,
- xxxxxxxxxxx xxxxxxxxxx výsledků x xxxxxxx použitých xxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.33 XXXXXXXXXXX XXXX XXXXXXXXX XXXXXXXX/XXXXXXXXXXXXX
1 XXXXXX xx x xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
1)1.1 Xxxxxxx xxxxx
Xxxxx xxxxxxxxxxxxx xxxxx xxxxxxxxx toxicity/karcinogenity xx xxxxx xxxxxxxxx x xxxxxxxxxxxx účinky látky x některého druhu xxxxx po xxxxxxxxxx xxxxxxxx.
Xxx tento xxxx xx xxxx karcinogenity xxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx x kontrolní xxxxxxxxx xxxxxxxx. Xxxxx použitá xxx xxxx xxxxxxxxx xxxxxxx xxxx být xxxxx xxx nejvyšší xxxxx xxxxxxx xxx xxxxx karcinogenity. Xxxxxxx x xxxxx xxxxxxxxxxxxx xxxx xxxxxxxx jak xx xxxxxxx xxxxxxxx, xxx xx xxxxxxxxxxxx xxxxxxx. Zvířata x xxxxxxxxxx satelitní skupině xxxx xxxxxxxxx xx xxxxxxx toxicitu.
Testovaná xxxxx xx podává obvykle 7 xxx x xxxxx, xxxxxxx cestou, xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxx, 1 dávka xx xxxxxxx, xx xxxxx xxxx xxxxxx xxxxxx. Během x xx xxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxxx xxxxx xxxxxxxxxx za xxxxxx xxxxxxxxx xxxxxxx xxxxxxxx a xxxxxx xxxxxx.
1.2 Popis xxxxxx
Xxxxxxx xxxxxxx xxxx xxxxxxx x ohledem na xxxx, xxxxxxx a xxxxx x xxxxxxx x ustanovením
§15 xxxxxxxxxx právního předpisu
10) x xxxxxxxx xxx, xxx xxxx xxxxx xxxxxxxxxxxx jednotlivých xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx právního xxxxxxxx.
10) Xxxx xxxxxx xx mladá zdravá xxxxxxx xxxxxxx rozdělí xx kontrolních a xxxxxxxxxxxx skupin.
1.2.1 Xxxxxxxxxxxxxx xxxxxxx
Xxxxxxxxxxxx druhem xx xxxxxx. Na xxxxxxx xxxxxxxxxxx studií xx xxxxx xxxxxx x xxxx druhy (xxxxxxxx x xxxxxxxxxx). Xxxxxxxxx xx xxxxxx xxxxx xxxxxxx z běžně xxxxxxxxx kmenů laboratorních xxxxxx. Expozice by xxxx být xxxxxxxx xx xxxxxxxx xx xxxxxxxxx xxxxxx. Xx xxxxxxx xxxxxx xx xxxxx xxxxxx x xxxxxxxxx xxxxxx činit xxxx xxx ± 20% xx průměru. X případě, xx xxxxxxx xxxxxx xxxxxxxxx xxxx subchronické xxxxxx xxxxxxxx, xx třeba xxxxxx xxxxxx druh x xxxx x xxxx studiích.
1.2.2 Počet x xxxxxxx
Xxx xxxxxxxx xx použije xxxxxxx 100 zvířat (50 xxxxx x 50 xxxxx) xx každou xxxxxx xxxxx a xxxxxxxx xxxxxxxxx xxxxxxx. Xxxxxx by xxxx xxx xxxxxxxxx x xxxxxxxxxx. Je-li xxxxxxxxx xxxxxxxx utrácení zvířat, xxxxx se zvýší x xxxxx xxxxxx, xxxxx xxxxx xxxxx xxxxxxxx xxxx xxxxxx xxxxxx.
Xxxxxxxxxx xxxxxxxxx xxxxxxx (xxxxxxx) xxx hodnocení xxxxxxxxx xxxx, než xxxx xxxxxx, xx xxxxx xxxx xxxxxxxxx 20 xxxxxx pro xxxxx pohlaví, zatímco xxxxxxxxx xxxxxxx xxxxxxx xx xxxx xxxxxxxxx 10 xxxxxx každého xxxxxxx.
1.2.3 Xxxxxxx xxxxxx x xxxxxxxxx xxxxxxx
Xxx xxxx xxxxxxxxxxxxx se xxxxx xxxxxxxxxxxx 3 xxxxxxx xxxxxx xxxxx xxxxxxxx xxxxxxxxx skupiny. Xxxxxxxx xxxxxxx xxxxxx xx xxxx xxxxxxx xxxxxxxx minimální toxicity, xxxx je xxxxx xxxxxx váhových xxxxxxxxx (xxxx xxx 10%), xxx xxxxxxxxxxxxxx xxxx xxxxxxxx doby xxxxxx xxxxxx jinými účinky xxx tumory. Xxxxxxxx xxxxxxx úroveň by xxxxxx xxxxxxxxxxxx x xxxxxxxxx xxxxxx, xxxxxxx x xxxxxx života xxxxxxx xxxx vyvolat xxxxxxxx známky xxxxxxxx. Xxxxxx xx xxxxxx xxx xxxxx xxx 10% xxxxxx xxxxx. Xxxxxxx dávku/dávky xx xxxxx stanovit ve xxxxxxxx pásmu xxxx xxxxxxx x xxxxxx xxxxxx.
Xxx xxxxx xxxxxxxxx xxxxxx by se xxxx xxxx x xxxxx xxxxxxxxx testy x studie xxxxxxxx.
Xxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxx x xxxxx zahrnuty xxxxxxxxx xxxxxxxxxx xxxxxxx a xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx. Xxxxxx xxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxxxx xx měla xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx.
Xxxxxxxx se provádí xxxxxxx xxxxx. Je-li xxxxx xxxxxxxx x xxxxx xxxx xxxx xxxxxxxxx do potravy, xxxx xx být xxxxx k xxxxxxxxx.
1.2.4 Xxxxxxxx
Xxxxxxxx kontrolní xxxxxxx xx xxxxxxxxx x xxxxxx xxxxxx s xxxxxxxxxxx xxxxxxxx, vyjma xxxxxxxx xxxxxxxxx xxxxx.
Xx xxxxxxxxxx xxxxxxxxx, xxxx xxxx xxxxxxxxx xxxxxx x xxxxxxxx xxxx xxxxxxx-xx se xxx xxxxxx aplikaci xxxxxxxxxx, xxxxx xxxxxxxxxx xxxxxxxx xxxx xxxxxxxxxxxxxxxx, xxxxxx xx xxxxx xxxxxxxxx xxxxxxxxx skupina, xxxxx xxxx xxxxxxxxxx xxx xxxxxxxx.
1.2.5 Způsob xxxxxxxx
Xxx xxxxxx cesty xxxxxxxx xxxx orální, xxxxxxxx x xxxxxxxxx. Xxxxx xxxxxxx xxxxxx xxxxxx xx xxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxxxxxxxxx testované xxxxx x pravděpodobnému xxxxxxx expozice x xxxxxxx.
1.2.5.1 Xxxxxx xxxxxx
Xxx, xxx se testovaná xxxxx vstřebává z xxxxxxxxxxxxxxxxxxxx traktu x xx-xx xxxxxx xxxxx x xxxx, xxxxx xxxx xxx xxxxxxxxx xxxxxx, dává se xxxxxxxx xxxxxx xxxxxxxx, xxxxx nejsou xxxxx xxxx nějaké xxxxxx. Xxxxxxx mohou xxxxxx xxxxxxxxxx látku v xxxxxxx, rozpuštěnu v xxxxx vodě xxxx xxxxxxx x tobolce.
Ideálně xx xx měla xxxxx podávat 7 xxx x xxxxx, xxxxxxx xxxxxxxxx 5 xxx x týdnu xxxx xxxx x xxxxxxxx toxicity xxxx xxxxxx xxxxxxx "xxxxxxxxxxx" xxxxxxxx x období xxx xxxxxxxx, x xxxxx xxxxxxxx výsledky x následné xxxxxxxxx. Xxxxxxx, xxxxxxxxx s xxxxxxx na xxxxxxxxx xxxxxxx, xxxxxxxxx xxxxxxx xxxxx xx xxxxxxxxxx xx xxxxxxxxxx.
1.2.5.2 Xxxxxxxx xxxxxx
Xxxxxxxx xxxxx xx xxxx xxxx být xxxxxxx xxxx xxxxxxxx xxxxxx xxxxx vstupu x člověka a xxxx modelový xxxxxx xxxxxxxx xxxxxxx poškození.
1.2.5.3 Xxxxxxxxx xxxxxx
Xxxxxxx xxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxxxxxxxxxxxxx xxx jiné xxxxxxx aplikace, xxxx xxx xxxxxxx podrobněji xxxxxxxxx o této xxxxx podání. Xxxxxxxxxxxxxxx xxxxxxxxx xxxx xxx xxxxxxx alternativou v xxxxxxxxxxxx situacích.
Dlouhodobé expozice xxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx, xxxxx xxxxx xx xxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxxxxx 6 hodin xxxxx po 5 xxx v xxxxx (xxxxxxxxxxx expozice), nebo x xxxxxxxxxx na xxxxxx xxxxxxxx v xxxxxxxxx, 22-24 hodin xxxxx xx 7 xxx x xxxxx (xxxxxxxxxxx xxxxxxxx), s xxxxxxxxx xxxxxx xxxxxxx xxx krmení xxxxxx xxxxx xx xxxxxxx xxxx xxx, použitou x xxx xxxxxxx xxxxxxxxxxx xxxx. X xxxx xxxxxxxxx xxxx xxxxxxx xxxxxxx exponována xxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx. Xxxxxx xxxxxx xxxx xxxxxxxxxxxx x xxxxxx xxxxxxxx xx x tom, xx x první xx xxxxx 17-18 hodin xx xxxxx xxxxxx xxxxx expozice s xxxxx xxxxxx xxxxxxx xxxxx xxxxxxx.
Xxxxx xxxxxxxxxxx xxxx xxxxxxxxxxx expozice xxxxxx xx xxxxxx xxxxxx x xx xxxxxx xxxxxxxx, která xx být simulována. Xxxxxxx, xx xxxxx xxxx v xxxxx xxxxxx xxxxxxxxx obtíže. Xxxxxxxxx, xxxxxx xxxxxxxxxxx xxxxxxxx pro simulaci xxxxxxxx xxxxxxx xxxxxxxxx xxxxx xxx narušeny xxxxxxxx xxxx a xxxxxx během xxxxxxxx x xxxxxxxx xxxxxxxxxxxxxxx (x spolehlivé) xxxxxxxx xxxxxxxx xxxx xxxxxx xxxxxxxxxxx par x xxxxxxx monitorování.
Expoziční komory
Zvířata xx xxxxxxxx x xxxxxxxxxxx komorách, jejichž xxxxxxxxxx xxxxxxxx dynamický xxxxx pro xxxxxxx 12 výměn xxxxxxx xx xxxxxx, xxx xxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx. Kontrolní a xxxxxxxxx xxxxxx xx xxxx xxx identickou xxxxxxxxxx, xxx xxx xxxx expoziční xxxxxxxx xxxxxxxxxxx ve xxxxx xxxxxxxxx xxxxx expozice xxxxxxxxx xxxxx. Uvnitř xxxxxx xx obvykle xxxxxxx xxxxx podtlak x tím se xxxxx xxxxx testované xxxxx xx xxxxxxxx xxxxxxxxx. Xxxxxx by xxxx minimalizovat xxxxxxxxxx xxxxxxxxxxx xxxxxx. Xxxxxx xx x zájmu xxxxxxx xxxxxxxx atmosféry x xxxxxx objem xxxxxx xxxxx xxxxxxxxxx 5 % xxxxxx xxxxxx.
Xxxxxx xxxx xxxxxxxxxxxx xxxxxxxx:
(x) průtok vzduchu: xxxxxxxx průtoku vzduchu xxxxxxx xx xxxx xxx nejlépe xxxxxxxxxxxx xxxxxxxxxxx,
(x) xxxxxxxxxxx: během xxxxx xxxxxxxx xx xxxxxxxxxxx testované xxxxx xxxxxx xxxxxxx více xxx ±15% xxxxxxx xxxxxxx,
(x) teplota a xxxxxxx: xxx xxxxxxxx, xxxxxxx xx xxxx xxx xxxxxxxxx x xxxxxxx 22 ± 2 °X x xxxxxxx v xxxxxxxx 30 - 70 % xxxxx xxxxxxx, xxx xx voda xxxxxxxxx x rozptýlení xxxxxxxxx látky x xxxxxxxxx xxxxxx. Xxx xxxxxxxxx xx měly xxx xxxxxxxxxxxx xxxxxxxx,
(x) xxxxxx xxxxxxxxx částic: xxxx by být xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx x xxxxxxxxx xxxxx x xxxxxxxx xxxx xxxxxxx xxxxxxxx. Xxxxxxxxxx xxxxxxx xx xxxx xxx x xxxxxxxxxxxx xxxxxxxxx xxx xxxxxxx testovací zvíře. Xxxxxx xxxxxxxxx komor xx odebírají x xxxxxxx xxxx xxxxxx. Xxxxxx xxxxxxx by xxx xxx xxxxxxxxxxxxxxx xxx distribuci xxxxxx, xxxxxx je xxxxx xxxxxxxxxx, x měl xx xxxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxxxx aerosolu, x xxxx xxxxxx xxxx xxxxxxxx xxxx xxxxxxxxxxxx. Xxxxxxx xxxxxxxxx xxxxxx by xxxx xxx xxxxxxxxx často xxxxx xxxxxx generujícího xxxxxxx, xxx xxxxxxxxx xxxxxxxxx xxxxxxxx, a xxxx xxxxx expozic xxx xxxxx, aby xxxx xxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxx částic, xxxxxx xxxx xxxxxxx xxxxxxxxxx.
1.2.6 Xxxxxx xxxxxx
Xxxxxx xxxxx karcinogenity xxxxxxxx xxxxx část xxxxxxxx xxxx xxxxxx xxxxxxx xxxxxxxxx xxx test. Xxxx xx xxx xxx xxxxxxx x 18 xxxxxxxx x xxxx a xxxxxx x 24 xxxxxxxx x potkanů. Xxxxxxx, xxx xxxxxxx kmeny xxxxxx s xxxxx xxxxx xxxxxx, xxxxxxxxxx x nízkým xxxxxxxxxx xxxxxxxx xxxxxx, by xxxx xxxxxxxx xxxxxxxxxxx xxxx být xx 24 xxxxxx xxx xxxx a křečky x xx 30 xxxxxx xxx xxxxxxx. Xxxxxxxxxxxx, ukončení xxxxxx xxxxxxxxxxx studie xx xxxxxxxxxx, xxxx počet xxxxxxxxxxxxx u xxxxxxxx xxxxx xxxx v xxxxxxxxx xxxxxxx xxxxxx xx 25 %. Xxx xxxxxxxx testu, xx xxxxxx xx xxxxxxxx sexuální xxxxxx xxxxxxxx, xxxxx xxxxxxx xx xxxxxxxx xxxxxx. Xxx, xxx uhyne xxxxxxxxx xxx xxxxxxx x xxxxxxx dávkou xx zjevných xxxxxxxxx xxxxxx, nemusí to xxxxx xxxx x xxxxxxxx xxxxxx xxxxx, xxxxx ostatní xxxxxxx xxxxxxxxxx xxxxxxx projevy, xxxxx by činily xxxxxxxx. Aby bylo xxxxx uznat xxxxxxxxx xxxxxxxx testu, xxxxx xxx xxxxxx xxxxxxxxxxxx xxxxx (autolýzou, xxxxxxxxxxxx xxxx x xxxxxxxx xxxx xxxxxxx) v xxxxx xxxxxxx xxxxx xxx 10% a xxxxxxx xx všech xxxxxxxxx xxxxx xxx xxxxx xxx 50% x 18 xxxxxxxx x myší x xxxxxx x x 24 xxxxxxxx u xxxxxxx.
Xxxxxxxxx xxxxxxx 20 xxxxxxxxxxx xxxxxx xxx xxxxx xxxxxxx x 10 xxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxx xxxxxxxxx pro xxxxxxxxx xxxxxxxxx toxicity xx xxxx být x xxxxxx xxxxx 12 xxxxxx. X xxxxxx xxxxxx xx mělo xxx xxxxxxxxx utracení xxx, xxx xxxxxxxx xxxxxxxx patologie, xxxxx xx vztah x xxxxxxxxx xxxxx, xx xxxxxxxxxxxxxx xxxxxxx xxxxxxxx.
1.3 Xxxxx xxxxxxx
1.3.1 Xxxxxxxxxx
Xxxxx xxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxx xxxxx xxxx a srsti, xxx a xxxxxxx, xxxxx x dýchacího, xxxxxxxxx, xxxxxxxxxxx a xxxxxxxxxxx xxxxxxxxx systému, xxxxxxxxxxxxxxx xxxxxxxx x xxxxxxx.
X xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx (xxxxxx) xx provádí v xxxxxxxxxxx intervalech xxxxxxxx xxxxxxxxx.
Xxxxxxxxxx xxxxxxxx zvířat xx nutná, aby xx xxxxxxxxx ztrátám xxxxxx ze xxxxxx xxxx. v xxxxxxxx xxxxxxxxxxx, xxxxxxxx tkání xxxx xxxx x xxxxxxx. Xxxxxxx x xxxxxx xx xxxx xxx xxxxxxxx a xxxxxxx.
Xxxxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxxx x xxxxxx xxxxxx x xxxxxxxxx xx zaznamenávají x xxxxx xxxxxx. Xxxxxxxx xxxxxxxxx xx xxxxx xxxxxxx xxxxxx tumorů: xxxx xxxxxxxx, lokalizace, xxxxxxx, vzhled x xxxxxxxx xxxxxxx viditelného xx xxxxxxxx xxxxxx xx zaznamenává.
Je xxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxx (x xxxx xxx, kde xx xxxxxxxxx xxxxx xxxxxxxx x xxxxx xxxx) xxxxx během xxxxxxx 13 xxxxx x xxx xxxxxxxxx ve xxxxxxxxxxxx intervalech, xxxxxx xx xxxxxxxxx xxxx xxxx xxxxx xxxxxxx xxxxxxxxx xxxxxxx nutnost xxxx xxxxxxxxx sledování.
Tělesné xxxxxxxxx xx zaznamenávají xxxxxxxxxxxx x xxxxx xxxxxx xxxxxx týdně xxxxx xxxxxxx 13 xxxxx období xxxxx x xxxxx xxxxxx xx xxxxx xxxxx xx xxxxx xxxxxx.
1.3.2 Xxxxxxxx xxxxxxxxx
1.3.2.1 Hematologie
Hematologická xxxxxxxxx (xxxx.xxxxx hemoglobinu, xxxxxxxxxx, celkový xxxxx xxxxxxxxxx, xxxxxxx xxxxx xxxxxx xxxxxxx, krevních xxxxxxxx nebo další xxxxxx xxxxxxxxxxx) by xxxx být xxxxxxxxx xx 3 xxxxxx, 6 měsíců x xxxx x přibližně xxxxxxxxxxxxxx xxxxxxxxxxx, x xx konci na xxxxxxxx xxxx xx 10 xxxxxxx xx xxxxxxx x xxxxx xxxxxxx. Tam xxx xx xx xxxxx, xxxxxx ve xxxxx xxxxxxxxxxx xx xxxx xxx od xxxxx xxxxxxx.
Xxxxx pozorování xxxxxx x klecích xxxxxx x zhoršeném xxxxxxxxxx xxxxx xxxxxx xxxxx xxxxxx, xx xxxxx xxxxxxxx diferenciální xxxxx xxxxxx xxxxxxx.
Xxxxxxxxxxxxx xxxxx xxxxxx xxxxxxx xx xxxxxxx ve vzorcích xx xxxxxx xx xxxxxxx s xxxxxxxx xxxxxx x x xxxxxxx. Pokud xxxx xxxx xxxx xxxxx x xxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxx xxxxxxx, xxxxxxxxxxx xx xxxxxxx x u xxxxxxx x xxxxxx nejblíže xxxxx, než xx xxxxxx xxxxx.
1.3.2.2 Xxxxxxx xxxx
Xxxxxx xxxx od 10 xxxxxxx xx xxxxxxx xxxxxxx xx xxxxxxx xxx xxxxxxx xx xxxxxxxx xxxxxx x ve xxxxxxxx xxxxxxxxxxx jako xxxxxxxxxxxxx xxxxxxx. Xxxxxxxxxxx xxxxxxxxx xxxx provedena buď xx xxxxxxxx xxxxxxxxxxxx xxxxxx, xxxx xx xxxxxxx vzorku pro xxxxxxx podle xxxxx x pohlaví:
- vzhled xxxx, xxxxx x xxxxxxx x xxxxxxxxxxxx xxxxxx,
- xxxxxxxx, xxxxxxx, xxxxxxxxx, xxxxxxx xxxxxxxx (xxxx-xxxxxxxxxxxxx),
- xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx (xxxx-xxxxxxxxxxxxx).
1.3.2.3 Biochemické xxxxxxxxx
X přibližně šestiměsíčních xxxxxxxxxxx x xx xxxxx xxxx xxxxxxxx xxxxxx vzorky xxx xxxxxxxxxxx xxxxxx xx xxxxx xxxxxxxxxx x 10 xxxxxxx obojího xxxxxxx, xxxxx xxxxx xxx xxxxx potkany xx xxxxx intervalech. Xx xxxxxxxxxx se xxxxx toho xxxxxxxx xxxxxx xxxx xxxxxx. X xxxxxx xxxxxx xx xxxxxxxxxx plasma x jsou provedeny xxxxxxxxxxx xxxxxxx
- xxxxxxx xxxxxxxxxxx xxxxxxxx,
- xxxxxxxxxxx xxxxxxxx,
- xxxxx xx xxxxxx xxxxx (např. xxxxxxxx xxxxxxx xxxxxxxxx, xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxx (xxxx xxxxx xxxx sérová xxxxxx xxxxxxxxxxxxxxxx), glutamát acetát xxxxxxxxxxxx (xxxx známá xxxx sérová xxxxxxxx xxxxxxxxxxxxxxxx), gama xxxxxxxx xxxxxxxxxxxxxx, xxxxxxxx xxxxxxxxxxxxx,
- xxxxxxxxxxxx xxxxx, xxxx. xxxxxx glukosa nalačno,
- xxxx xx xxxxxx xxxxxx, xxxx. xxxxx xxxxxxxx v xxxx.
1.3.2.4 Xxxxxxxxxxxxx patologické vyšetření
Kompletní xxxxx xx xxxxxxx x xxxxx xxxxxx, xxxxxx těch, která xxxxxxx xxxxx xxxxxx xxxx xxxx utracena x xxxxxx. Před xxxxxxxxx xx odeberou xxxxxx xxxx xxxxx xxxxxx xxx diferenciální xxxxx xxxxxx krvinek. Xxxxxxx xxxxxxxxx xxxx, xxxxxx nebo xxxx, xxxx léze, xxxxx xx mohly xxx xxxxxx, xx xxxxx xxxxxxx. Xxxx xx xxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx-xxxxxxxxxxxxx xxxx s xxxxxxxxxxxxxxx xxxxxx.
Xxxxxx x xxxxx xx uchovávají xxx histopatologické xxxxxxxxx. Xxxxxxx xx xxxxx x xxxxxxxxxxx orgány x tkáně: mozek (xxxxxxxxxxx xxxxx/xxxxx, xxxxxxxxx xxxx, kory xxxxxxx), xxxxxxxx mozkový, štítnou xxxxx a xxxxxxxxx xxxxxxx, thymus, xxxxxxx x plíce, xxxxx, xxxxx, xxxxxxx xxxxx, xxxxx, xxxxxxx, xxxxxxx, xxxxxxxxxx, jícen, žaludek, xxxxxxxxxxxx, xxxxxxx, xxxxx, xxxxx xxxxxx, tračník, xxxxxxxx, močový xxxxxx, xxxxxxxxxx xxxxxx, xxxxxxxx, xxxxxx, akcesorní xxxxxxxxxx xxxxxx, xxxxxx xxxxxx xxxxx, xxxx, svalovinu, xxxxxxxxx nervy, xxxxx (xxxxx, xxxxxx a xxxxxxx), xxxxxxx x xxxxxx xxxxx, xxxxxxxx xxxx včetně kloubů, x xxx. Xxxxxxxx xxxx a močového xxxxxxx fixativem xx xxxxxxxxx xxxxxx ke xxxxxxxxxx těchto xxxxx; xxxxxxxx plic x xxxxxxxxxxx xxxxxxxx xx xxxxxxx xxx odpovídající xxxxxxxxxxxxxxxx xxxxxxxx. Xx xxxxxxxxxxx studiích, jako xxxx xxxxxxxxx xxxxxx, xx xxx xxxxxxxx xxxx xxxxxxxxxx trakt xxxxxx nosu, xxxxxx x xxxxxx.
Xxxxxxxx: Xxxxxx xxxxx x xxxxxxxxxxx xxxxxxx xx xxxxx xxxxxxxxxx xxxx xxx xxxxxxx xxxxxx jako xxxxx, játra, ledviny, xxxxxxxxxx x xxxxxx x 10 xxxxxx xx xxxxxxx a xx xxxxxxx u xxxxxxxx a xx xxxxx xxxxxxxxxx.
Xxxx-xx xxxxxxxxx xxxx klinická vyšetřeni, xxxxxxxxx xxxxxxx x xxxxxx xxxxxxxx xx xxxx být x xxxxxxxxx xxxx xxxxxxxxxxxxxx xxxxxxxxxx, protože xxxxx xxx patologovi významné xxxxxxx.
1.3.2.5 Xxxxxxxxxxxxxx
Xxx xxxxxxxxx xxxxxxxxx toxicity:
Podrobné xxxxxxxxx xx xxxxxxx xx xxxxx xxxxxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxxxxx xxxxxxx x xxxxxxx xxxxxx a satelitní xxxxxxxxx skupiny. Pokud xx x xxxxxxxxx xxxxxxx exponované xxxxxxxx xxxxx xxxxxx patologické xxxxx xxxxxxxxx látkou, xxxxxxx xx xxxxxxxxxxxx xxxxxx xxxxxx xxxxx xxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxxxxxxx satelitních xxxxxx i xx xxxxx xxxxxxxxxxxx xxxxxx xxxxx studie věnované xxxxxxxxxxxxx xxx xxxxx xxxxxxxx.
Xxx testování karcinogenity:
(a) xxxxx histopatologie se xxxxxxx x xxxxxxxx x xxxxxxx xxxxx xxxxxx, která uhynula xxxx xxxx utracena xxxxx xxxxx x x xxxxx xxxxxx xxxxxxx xxxxxxxxx a x xxxxxxxx xxxxxx;
(x) xxxxxxx xxxxxx xxxxxxxxx xxxx x xxxx, xxxxx xxxx podezřelé xxxx xxxxxx, se xxxxxxx mikroskopicky u xxxxx skupin;
(c) xx-xx xxxxxxxx xxxxxx x xxxxxxxxx neoplastických lézí xxxx xxxxxxxx x xxxxxxx xxxxxx x xxxxxxxxx xxxxxxxx, histopatologické xxxxxxxxx se xxxxxxx x xxxxx orgánu xx tkáni x x xxxxxxx xxxxxxxxx;
(x) xx-xx xxxxxxx xx xxxxxxx x xxxxxxx xxxxxx podstatně xxxxx xxx u kontrol, xxxx xx být xxxxxxxxx xxxxxxxx i xxxxxxx x nejbližší xxxxx dávkou;
(e) xx-xx xx xxxxxxx x xxxxxxx xxxxxx doklad x vyvolání xxxxxxxxx xxxx xxxxxx xxxxxx, xxxxx by xxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxx, xx xxxxx kompletně xxxxxxxx xxxxxxxx xxxxx xxxxxxxx xxxxxx.
2 XXXXX
Xxxxx xx sumarizují xx xxxxx xxxxxxx, ukazujících xxx xxxxxx xxxxxxxxxx xxxxxxx xxxxx xxxxxx xx xxxxxxx xxxxx, xxxxx zvířat xxxxxxxxxxx xxxxxx zjištěné během xxxxx, xxxx jejich xxxxxxxxx x xxxxx xxxxxx s xxxxxx xxx xxxxxxxx. Xxxxxxxx xx xxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxx. Xxxxx xxx použity xxxxxxxxx xxxxxxxx statistické xxxxxx.
3 XXXXXXX POKUSU, XXXXXXXX XXXXXX X ZÁVĚREČNÁ XXXXXX
X xxxxxxx x xxxxxxxxxxx právními xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx pokusu x x xxxxxxx pokusu xx xxxxx xxxx xxxxxxxx.
Xxxxxx x xxxxx xxxx obsahovat xxxxxxxxxxx xxxxxxxxx:
- xxxxxxxxx druh, xxxx, zdroj, xxxxxxxx xxxxxxxx, xxxxx,
- xxxxxxxx xxxxx:
xxxxx xxxxxxxxxxx xxxxxxxx:
xxxxxx xxxxxxxxxx, xxxx, rozměrů, xxxxxx xxxxxxx, systému xxx xxxxxxxxx xxxxxx x xxxxxxxx, metody xxxxxxxxxxx, xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxxxx x aparatury x xxxxxxx xxxxxxxx xxxxxx v xxxxxxxxxx xxxx, xxxxx se xxxxxxx. Dále xx xxxxx popsat zařízení xxx měření teploty, xxxxxxxx x xxx, xxx xx to xxxxxxx, stability xxxxxxxxxxx xxxx velikostí částic xxxxxxxx.
Xxxxx x xxxxxxxx: xx xxxxx xxxxxxx xxxxxx průměrných xxxxxx x xxxxxxxxxxx (např. xxxxxxxxxx odchylka) by xxxx xxxxxxxxx:
(x) xxxxxxxx xxxxxx xxxxxxx x xxxxxxxxxx zařízení,
(b) xxxxxxx x vlhkost xxxxxxx,
(x) xxxxxxxxx xxxxxxxxxxx (xxxxxxx xxxxxxxx xxxxxxxxx látky xxxxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxxxx),
(x) xxxxxx vehikula, xx-xx xxxxxxx,
(x) skutečné xxxxxxxxxxx v dýchací xxxx,
(x) xxxxxx xxxxxxxxx xxxxxx (tam xxx xxxxxxxxxx),
- dávkové úrovně (xxxxxx xxxxxxxx, xx-xx xxxxx) x xxxxxxxxxxx,
- xxxx xxxxxxxxx tumorů xxxxx pohlaví, dávky x xxxx tumoru,
- xxxx xxxxx xxxxx xxxxxx xxxx zda xxxxxxx přežila xx xx xxxxx, xxxxxx xxxxxxxxxxx skupin,
- výskyt xxxxxxxxx účinků xxxxx xxxxxxx x xxxxx
- xxxxx xxxxxxxxx a xxxxxx xxxxxx,
- doba, xxx byl xxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxx x xxxx další xxxxx,
- xxxx o xxxxxxxx xxxxxxx x xxxxxxx xxxxxxxxx,
- xxxxxxxxxxxxxx xxxxxx,
- použité xxxxxxxxxxxxx xxxxx x xxxxxxxx,
- xxxxx klinické xxxxxxxxx x xxxxxxx xxxxxxxx (xxxxxx xxxxxxxx xxxxxxx xxxx),
- xxxxxx xxxxxxxxxxx-xxxxxxxxxx,
- xxxxxxxx xxxxx xxxxx xxxxxxxxxxxxxxxxxx xxxxxx,
- xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxx použitých xxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.34 XXXXXXXXXXX XXXXXXXX - JEDNOGENERAČNÍ XXXX
1 XXXXXX je x xxxxxxx x právem Xxxxxxxxxx společenství.
1)1.1 Princip xxxxxxxxx xxxxxx
Xxxxxxxxx xxxxx xx xxxxxx xxxxxxxx xxxxxxxx xxxxx x xxxxx x xxxxxxxxxxxxxx xxxxxxx.
Xxxxx dostávají xxxxxxxxxx xxxxx x xxxx xxxxx x xxxxxxx x xxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxx (xxxxxxxxx 56 xxx x myší a 70 xxx x xxxxxxx), aby xxx xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx testované xxxxx xx xxxxxxxxxxxxxx.
Xxxxxx xxxxxxxxxx xxxxxxxx (X) xxxxxxxxx xxxxx xx xxxx xxxxxxx 2 xxxxxxxxxx xxxxx, xxx byl xxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx testované látky xx estrus. Zvířata xxxx poté xxxxxxxxxx. X xxxx xxxxxxxxxxx xx xxxxxxxxx látka xxxxxx xxxxxxxx xxxx xxxxxxx, x xxxx xxxxxxxxx x kojení xxxxx samicím.
Pro xxxxxxxxx xxxxxxxx je třeba xxxxxx modifikovat.
1.2 Popis xxxxxxxxx metody
1.2.1 Příprava
Pokusná xxxxxxx xxxx vybrána x xxxxxxx na xxxx, xxxxxxx x xxxxx x souladu x ustanovením
§15 xxxxxxxxxx právního xxxxxxxx
10) x označena tak, xxx byla možná xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10) Před xxxxxxxxx xxxxx xx zdravá xxxxx dospělá xxxxxxx xxxxxxx xxxxxxx xx xxxxxxxxx x exponovaných xxxxxx.
Xxxxxxxxxx xx testovanou xxxxx podávat x xxxxxxx nebo x xxxxx vodě. Xxxx xxxxxxx xxxxxx xxxx xxxx přijatelné. Xxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxx způsobem x xxxxxxx xxxxxx xxxxx. Xxxxx se xxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxx xxxx jiné xxxxxxxx, musí xxx x xxxx xxxxx, xx nemají toxické xxxxxx. Xxxxx se xxxxxxxx 7 dnů x týdnu.
1.2.2 Pokusná xxxxxxx
1.2.2.1 Výběr xxxxx
Xxxx xx xxxxxxxx potkanům xxxx xxxxx. Xxxxxxxxx xx xxxxxx zvířata, xx xx xxxx xxxxxxxxx xxx jiné xxxxxxxxxxx. Xxxxxxxxx se xxxxx x nízkou xxxxxxxxx. Musí být xxxx xxxxxxxxxxxxxxxx co xx xxxxx, kmene, xxxxxxx a hmotnosti x/xxxx xxxx. Xxxxxxxx xxxx xxx ověřena xxxxxxx způsobem u xxxx xxxxxxx. Xxxxxxx x obou xxxxxxxxx, xxxxxxxxxx x xxxxxxxxx, xxxx xxx xxxxxxxxx xxxx xxxxxxxxx aplikace.
1.2.2.2 Xxxxx x xxxxxxx
Xxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxx musí xxx xxxxxxxxxx xxxxx xxxxxx, xxx xxxx xxxxxxxx xxx 20 xxxxxxx xxxxx x xxxxxxxxx xxxxxxx xxxxxxxx xxxxxx. Xxxxx je získat xxxxxxxxxx xxxxx xxxxxxxxxxx x xxxxxxxxx, x xxx zajistit spolehlivé xxxxxxxxx vlivu xxxxx xx xxxxxxxx, xxxxxx xxxxxxxxx x xxxxxxxx xxxxxxx x X xxxxxxxx, xxxxxx, růst x xxxxx xxxxxxxxx xxxxxxxx X, od xxxxxx xx odstavu.
1.2.3 Xxxxxxxx xxxxx
Xxxx x xxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxx. Xxxx xxxxxxx se xxxxxxx xxxxxx xxxxxxxx do xxxxxxxxxx porodních xxxx xxxxxxxxxx xxxxx x xx xxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxxx.
1.2.4 Xxxxxxxxx
Xxxxxxx xx xxxxxxx 3 exponované xxxxxxx x 1 xxxxxxxxx. Xxxxx xx xxxxxxx xxx xxxxxxxx xxxxxxxxx xxxxx vehikulum, xxx xxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx vehikulum x xxxxxxxxx xxxxxxxx xxxxxx. Pokud testovaná xxxxx snižuje xxxxxx x využití xxxxxxx, xx xxxxx uvážit xxxxxxx xxxxx kontrolní xxxxxxx, xxxxxxxxx xx xx výživy.
Testovaná xxxxx x xxxxxxxx koncentraci xx x xxxxxxxx xxxxxxx - pokud xx xxxx omezeno xxxxxx fyzikálně-chemickými xxxxxxxxxxx xxxx xxxxxxx xxxxxxxxxxxx xxxxxx - xxxxxxxxx xxxxxxxx, xxx žádná xxxxxxx x rodičovské xxxxxxxx. Xxxxxxx xxxxx(x) xx xxxx(x) vyvolat xxxxxxxxx xxxxxxx účinky, xxxxx xx xx xxxx xxxxxxx xxxxxxxxx xxxxx, x nejnižší xxxxx xx xxxxxx xxxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxxx účinky, ani x rodičů ani x potomstva.
Při xxxxxx xxxxxx xxxx v xxxxxxxxx se xxxxx xxxxxxx xxxxxxxxxxxx xx xxxxxxx hmotnosti zvířete x přizpůsobuje se xxxxx xxxxx xxxxx xxxxx xxxx. V xxxxxxx xxxxxxxxx xxxxx xxxxx xxxxx xxx xxxxxxxx xxxxxx xx xxxxxxx xxxxxxx xxxxxxxxx x nultém xxxx xxxxxx xxx od xxxxxxx xxxxxxxxxxx.
1.2.5 Limitní xxxx
X případě látek x xxxxxx xxxxxxxxx, xxxxx xx xxx xxxxx 1000 xx.xx-1 xxxxxxxxxxx žádným toxickým xxxxxxx xx xxxxxxxxxx, xxxxxx xx xxxxxxxx xxxxxx xx xxxxxx xxxxxxxxx xxxxxxxx. Xxxxx xxxxxxxxx studie ukáže, xx xxxxxx xxxxx, xxxxxxxxxxxx x xxxxx xxxxx xxxxxxxx xxxxxxxx, xxxx nepříznivé xxxxxx xx xxxxxxxx, xxxx xxxxx xxxxxxxx xxxxxx xx xxxxxx dávkových xxxxxxxx.
1.3 Xxxxx xxxxxxx
1.3.1 Xxxx xxxxxx
Xxxxx aplikace xxxxxx rodičovské xxxxxxxx (X) xxxxx ve xxxx 5 xx 9 xxxxx, po xxxxxxx xxxxxxxxx xxxxxxxxxxxx xx xxxxxxxxx. U xxxxxxx xxxxxxxx xxxxxxxxx 10 xxxxx před xxxxxxx xxxxxxxxxxx (8 xxxxx xxx xxxx). Xxxxx xx xxx' xxxxxx a xxxxxxx xx xxxxx xxxxxx xxxxxxxxxxx, xxxx se xxxxxxxxx x xxxxxxxx x xxxxx xxx xxxxxxx pro produkci xxxxxxx xxxx x xxxx pak xxxxxxxx x xxxxxxxxx xxxxx xxxx xxxxxx xxxxxx.
Xxxxx xxxxxxxx xxxxxxx rodičovské xxxxxxxx (X) xxxxx xx xxxxxxxxx xxxxxxxxxxxx x xxxxxxxxx aspoň 2 týdny xxxx xxxxxxx xxxxxxxxxxx. Xxxxx xxxxxxxx xxxxxxxxx xxx xx xxxx 3 xxxxx xxxxxx xxxxxxxxxxx, x xxxx gravidity xx xx xxxxxxxxx X1 generace. Xx xxxxxxxxx xxxxx dávkovacího xxxxx xxxxx xxxxxxxx x xxxxxxxxxxxx xxxxxxxxx xxxxx, např. x xxxxxxx metabolismu x/xxxx xxxxxxxxxxxx.
1.3.2 Xxxxxx xxx xxxxxxxxxxx
Xx xxxxx xxxxxx xxxxxxxx 1:1 (xxxxx xxxxxx x jeden xxxxx) xxxxx 1:2 (xxxxx samec xx xxxxx samicím).
V xxxxxxx 1:1 párovaní, samice xx xxxxxxx x xxxx samcem xx xxxxxxxx xxxxx do xxxxxxxxxx anebo po xxxx 3 týdnů. Xxxxx ráno xxxx xxxxxx xxxxxxxxx xx xxxxxxxxxx spermatu xxxx xxxxxxxxx xxxxx. Den 0 těhotenství je xxxxxxxxx xxxx xxx xxxxxx vaginální zátky xxxx xxxxxxxx.
Xxxxxxx, x xxxxxxx nedojde k xxxxxxxxx, xx xxxxx xxxxxxxx x xxxxx xxxxxxx xxxxx xxxxxxxxxxx xxxx. Xx xx xxxxx xxx' xxxxxxxxxxx xxxxx příležitosti x xxxxxxxxx s xxxxxxxxxxx xxxxxxx xxxx xxxxxxx, xxxx xxxxxxxxxxxxxx vyšetřením xxxxxxxxxxxxx orgánů nebo xxxxxxxxxx xxxxxxxxxx cyklu x spermatogenezy.
1.3.3 Xxxxxxxx xxxx
Xxxxxxxx xxxxxxxxx xxx xxxxxxxxx plodnosti xx xxxxxxxxx možnost xxxxxxx xxxxxxxx x xxxxxxx x xxx potomstvo xx xxxxxxxx xxxxxxxxx xxx xxxxxxxxxxxxx xxxxxxxxx xxxx. Xxxxx xx xxxxxxxx xxxx standardizuje, xx xxxxx dodržet xxxxxxxxxxx xxxxxx: xxxx 1. x 4. xxxx xx porodu xx xxxxxxxx všech xxxx upraví vyřazením xxxxxxxxxxxx jedinců xxx, xxx xx xxxxxxx xxxxx 4 samců x 4 xxxxx xx vrh; xxxxx xx není xxxxxxxxxxxx, xx možno xxxxxxxxxxxxxx xx xxxx xxxxx, xxxxxxxxx 5 xxxxx x 3 xxxxxx. Xxxx menší xxx 8 nelze xxxxxxxxxxxxxx.
1.3.4 Xxxxxxxxxx
Xxxxx zvíře xxxx xxx pozorováno alespoň xxxxxx za xxx. Xxxxxxxx xxxxx xxxxxxx, xxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxx toxicity, xxxxxx xxxxxxxxx, xx xxxxxxxxxxxxx. Příjem xxxxxxx xx xxxx denně xxx před xxx xxxxx xxxx xxxxxxxxxxx. Xxxxx xxxxxxxxx xx xxxxxx kontrolovat xxxxxx xxxxxxx xxxxx. Xx xxxxxx x x xxxxxxx laktace se xxxx xxxxxx potravy (x vody, xxxxx xx látka xxxxxx x xxxxx vodě) xx xxxxxx xxx, xxx xx xxxxxxxxx xxxxxx. Xxxxxxxxxx X xxxxxxx xx xxxx xxxxx xxx xxxxxxxx x pak xxxxx. Xxxxxxx pozorování xx xxxxxxxxxxxxx individuálně xxx xxxxx dospělé xxxxx.
Xxxx xxxxxxx se xxxxxx xx xxx 0 xxxxxxxxxxx. Každý xxx xx xx nejdříve xx porodu vyšetří x xxxxxxx xx xxxxx a xxxxxxx xxxxxx, xxxxx mrtvých x xxxxxx xxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxx.
Xxxxx xxxxxxx x xxxxxxx xxxxxxxx xx xxxxxxx dnu xx xxxxxxxx xxx vyšetření xx možné xxxxxxx. Xxxx xxxxxxx xx xxxxxxxxx x xxxx xxxx xx xxxxx xxxx xx xxxxxx, xx xxxxxxx a xxxxxx xxx x xxxxx xxxxx xxxxx xx ukončení xxxxxx, xxx jsou zvířata xxxxxxx individuálně. Pozorují xx x xxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx x xxxxxxx a xxxxxxxx xxxxx matek x xxxxxxxxx.
1.3.5 Xxxxxxxxx
1.3.5.1 Xxxxx
Xx xxxxxxxx xxxx úmrtí xx všechna zvířata xxxxxxxx P xxxxxxxxxxxxx xxxxxxx xx xxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxx xxxxx, xx xxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxxxxx xxxxxxx. Mláďata xxxxxxx xxxx xxxxxxxxx xx vyšetří xx xxxxxxx.
1.3.5.2 Xxxxxxxxxxxxxxxx xxxxxxxxx
Xxxxxxxxx, xxxxxx, děložní hrdlo, xxxxxx, xxxxxxx, epididymis, xxxxxxx xxxxx, xxxxxxxxxx xxxxx, xxxxxxxx, xxxxxxxx x xxxxxx orgány xxxxx zvířat xxxxxxxx X xx uchovají xxx xxxxxxxxxxxxx xxxxxxxxx. X případě, xx xxxx orgány nebyly xxxxxxx xxxxxxxxx x xxxxxx mnohadávkových studiích, xxxxxxx se xxxxxxxxxxxxx xxxxxxxxx x všech xxxxxx kontrolní xxxxxxx x skupiny xxxxxxxxxxx xxxxxxxx xxxxx x xxxx u xxxxxx, xxxxx zemřela x xxxxxxx pokusu.
Orgány, které xxxxxx xxxxxxxxxxx x xxxxxx xxxxxx xxxxxx, xx xxxxxxx x x P xxxxxx xxxxxxxxx dávkových xxxxxx. X těchto xxxxxxxxx xx mikroskopicky xxxxxxxxx xxxxxxx tkáně xxxxxxxxxxxxx xxxxxxxxx. Xxx xxx xxxx uvedeno, reprodukční xxxxxx zvířat xxxxxxxxxxx x xxxxxxxxxxx xx xxxx též xxxxxxxx xxxxxxxxxxxxx xxxxxxx.
2 XXXXX
Xxxx xx xxxxxxxxxx x xxxxxxxxx, xxx xx xxxxxx xxx xxxxxx xxxxxxxx skupinu xxxxx xxxxxx xx xxxxxxx xxxxxx, xxxxx xxxxxxxx xxxxx, xxxxx xxxxxxxxx xxxxx, xxx změn x xxxxxxxx zvířat xxxxxxxxx xxxx xxxxx.
Xxxxxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxx. Xxxx xx xxxxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxx.
3 XXXXXXX POKUSU, PROTOKOL XXXXXX A ZÁVĚREČNÁ XXXXXX
X xxxxxxx x xxxxxxxxxxx právními předpisy
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx a x průběhu pokusu xx xxxxx xxxx xxxxxxxx.
Xxxxxx x experimentu xx xxxx xxxxx xxxxx obsahovat následující xxxxx:
- druh /kmen xxxxxxxxx xxxxxx,
- xxxxx x xxxxxxx xxxxxx x xxxxxxxxxx xx xxxxx a xxxxxxx xxxxxx xxxxxxxxx xxxxxxxxx, xxxxxxx a xxxxxxxxxxxxxxxx,
- xxxx uhynutí x xxxxxxx studie xxxx xxx xxxxxxx xxxxxxx xx xxxxxxxx pokusu,
- xxxxxxx xxxxxxxxx hmotnost xxxxxxx xxxx, xxxxxxxxx xxxxxxxx xxxxxxxxxxxx mláďat x xxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxx,
- toxické x xxxxx xxxxxx xx xxxxxxxxxx, xxxxxxxxx x xxxxxxxxxxx xxxx,
- xxx, kdy byly xxxxxxxxxx jednotlivé xxxxxxxxxx xxxxxxxx a xxxxxx xxxxx vývoj,
- tělesná xxxxxxxx zvířat X xxxxxxxx,
- xxxxxxx nálezy,
- xxxxxxxx popis xxxxx xxxxxxxxxxxxxxx nálezů,
- statistické xxxxxxxxxx xxxxx údajů, xxxxx je xxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.35 XXXXXXXXXXXXX XXXXXX XXXXXXXXXXX XXXXXXXX
1 XXXXXX xx v souladu x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx
7a).
1.1 XXXX
Xxxx xxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xx xxxxxx x xxxxxxx xxxxxxxxxxx informací xxxxxxxxxx se xxxxxx xxxxxxxx látky na xxxxxxxxx a xxxxxxxxx xxxxx x samičí xxxxxxxxxxxx xxxxxxxx, včetně xxxxxx pohlavních xxxx, xxxxxxxxxx xxxxx, způsobu xxxxxxx při páření, xxxxxxx, xxxxxxx, xxxx, xxxxxxx, xxxxxxxxx, růstu x xxxxxx xxxxxxxxx. Xxxxxx může xxxxxx xxxxxxxxxx informace x xxxxxx zkoušené xxxxx xx neonatální xxxxxxxx, xxxxxxxxx x xxxxxxxxx xxxxxxxxx o prenatální x postnatální xxxxxxxx xxxxxxxx a xxxx xxxxxxx xxxx návod xxx xxxxx xxxxxxx. Xxxx xxxxxxxx xxxxx x xxxxxx generace X1 je xxxx xxxxxxxx xxxxxx xxxxxx xxxxxx x hodnocení xxxxxxxxx a xxxxxxxxxx xxxxx x xxxxxx xxxxxxxxxxxx xxxxxxxx x xxxxxx xxxxx x xxxxxx generace X2. X xxxxx xxxxxx xxxxx xxxxxxxxx x xxxxxxxx xxxxxxxx x xxxxxxxxx poruchách xxx xx xxxxxx xxxxxxxxx xxxxxxxx další xxxxx xxxxxx, xxxxxxx jako xxxxxx se xxxx xxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxx, xxxxx xxx xxxx xxxxxxx xxxxxxxx xxxxxxx x samostatných studiích xxxxxx vhodných xxxxx xxxxxxxx.
1.2 XXXXXXX XXXXXXXX XXXXXX
Xxxxxxxx xxxxx xx xxxxxx v xxxxxxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxx x samic. Xxxxxx x generace X xx xxxxx xxxxxx během xxxxx x xxxxx xxxxxxxxx xxxxxxx dokončeného xxxxxxxxxxxxxxxxxxx xxxxx (přibližně 56 xxx x xxxx x 70 xxx x xxxxxxx), xxx xxxx xxxxx xxxxxxxx xxxxxxxxx nepříznivé xxxxxx xx xxxxxxxxxxxxxx. Účinky xx xxxxxxx xx xxxxxxx xxxxxx parametrů xxx xxxxxxx (xxxx. xxxxxxxxxx x xxxxxxxx xxxxxxx) x x xxxxxxxx tkání a xxxxxxxx xxxxxxxxxxxxxx. Xxxx-xx x xxxxxxxxx informace x xxxxxxxxxxxxxx x xxxxxxxxxx xxxxxxxxxx dlouhých xxxxxx opakovaného xxxxxxxxx, xxxx. 90denní xxxxxx, xxxx do hodnocení xxxxx xxxxxxxxx xxxxx x xxxxxxxx P. Xxxx xxxxxx xxxx xxxxxxxxx xxxxxxx o xxxxxxxxx x xxxxxxxx X xx xxxx xxxxxx xxxxxxx xxx xxxxxxx xxxxxxxxxx vyhodnocení. Xxxxxxx z generace X xx látka xxxx xxxxx růstu x xxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx, xxx xxxx xxxxx xxxxxxx jakékoliv xxxxxxxxxx xxxxxx xxxxxxxx látky xx normální průběh xxxxxxxxxx xxxxx. Xxxxxxxx xxxxx xx xxxxxx xxxxxxxxxx (X) xxxxxxxx xxxxxxxxx xxxxxx během xxxxxx xxxxxx, následné xxxxxxxx x xx xx doby odstaveni xxxxxx xxxxxxxxx F1. Xx xxxxxxxxx se x xxxxxxxx F1 x xxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxx xx xx dospělosti, x průběhu xxxxxx x xxxxxxxx generace X2 x xx xx xxxx, xxx xxxxx k xxxxxxxxx xxxxxxxx F2.
U xxxxx xxxxxxxxx xxxxxx xx xxxxxxxxx xxxxxxxx sledování x xxxxxxxxxxx xxxxxxxxx xxxxxxxx toxicity, a xx xx xxxxxxxxx xxxxxxx na xxxx xxxx xx xxxxxxxxx x xxxxxxxxx xxxxx x xxxxxx rozmnožovací xxxxxxxx a na xxxx a vývoj xxxxxx potomstva.
1. XXXXX XXXXXXXX XXXXXX
1.3.1 Xxxxx xxxxxxxxxxx druhů
Nejvhodnějším xxxxxx xxx testování xx xxxxxx. Xxxxx xx xxxxxxx xxxx xxxxx, xx třeba podat xxxxxxxxxx x xxxxxxx xxxxxxxxxxxx úpravy. Xxxx xxxxxx xxxxxxxx xxxxx x xxxxx plodností xxxx x xxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxx. Na xxxxxxx xxxxxx xx xxxx xxx u xxxxxxxxxxx xxxxxxxxx xxxxxx jen xxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxx by xxxxxx xxxxxxxxx 20 % xxxxxxxx xxxxxxxxx u xxxxxxx xxxxxxx.
1.3.2 Podmínky xxxxx x krmení
Teplota xx xxxxxxxx xxxxxxxxx xxx pokusná zvířata xx měla být (22 ± 3) °X. Xxxxxxxxx xxxxxxx xx měla být xxxxxxx 30 %, xxxxxx xx však xxxxxxxxx 70 % xxxxx xxxxxxx xxxxxxxxx x xxxxx xx xxxxxxx 50 - 60 %. Xxxxxxxxx xx xxxx xxx xxxxx, xxxx xx xx střídat 12 x xxxxxx x 12 h tmy, xxxx-xx x xxxxxx xxxxxxxxx denní xxxxxx. Xx krmení xx xx xxxx používat xxxxxxx xxxxxx xxxxxx xxx xxxxxxx zvířata xx registrovaného xxxxxxx x neomezeným přísunem xxxxx xxxx. Xxxxx xxxxxx xxxx xxx xxxxxxxx nutností xxxxxxxx xxxxxxx přísadu xxxxxxxx xxxxx, xx-xx xxxxx xxxxxxxx xxxxx xxxxxxxx.
Xxxxxxx xxxxxxx lze chovat xxxxxxxxxx, xxxxx je xxxxxxx x klecích x malých skupinkách xxxxxxxxx zvířat xxxxxxxx xxxxxxx. Páření xx xxxx xxxxxxxx x xxxxxxx, xxxxx xxxx x xxxxxx účelu xxxxxx x xxxxxxx x příslušným xxxxxxx xxxxxxxxx
10), pokud xxxx xxxxxxxxx projektem xxxxxx xxxxx. Po xxxxxxx xx třeba umístit xxxxxxxxx xxxxxx xxxxxxxxxxxx xx klecí určených x xxxx xxxx xxxxx mláďat. Xxxxxxxxx xxxxxxx xxx xxxxxx xxxxxx v xxxxxx xxxxxxxxx x xxxxxxx xxxxx až xxx xxx xxxx vrhem. Xxxx xx blíží xxxx xxxx, xx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx poskytnout xxxxxx x definovatelný materiál xxx tvorbu xxxxxx.
1.3.3 Xxxxxxxx pokusných zvířat
Pokusná xxxxxxx xxxx xxxxxxx x ohledem xx xxxx, pohlaví a xxxxx v xxxxxxx x xxxxxxxxxxxx
§15 xxxxxxxxxx právního xxxxxxxx
10) x xxxxxxxx xxx, xxx xxxx xxxxx xxxxxxxxxxxx jednotlivých pokusných xxxxxx. Dobu navykání xxxxxxx
§10 zvláštního xxxxxxxx xxxxxxxx
10). Xxxxxxx xxxxxxx se xxxxxxxxxxxxxx xxxxx druhu, xxxxx, xxxxxx, xxxxxxx, xxxxxxxxx xxxx stáří. X xxxxxxxxx by xxxx xxx veškeré xxxxxxxxx x xxxxxxxxxxxxxx xxxxxxxx, xxx xx xxxxxxxx xxxxxxxxxx. Xxxxxxx xxxxxxx xx xxxxxxxx výběrem xxxxxxx xx kontrolních x xxxxxxxxxxxxxxxx xxxxxx (xxxxxxxxxx se rozdělení xxxxx tělesné hmotnosti). Xxxxx xx měly xxx xxxxxxxxxx xxx, xxx xxx xxxx xxxxxxxx xxxxx xxxxxxxxxxxxx. Xxxxxxx pokusnému xxxxxxx xx přiřadí jednoznačné xxxxxxxxxxxxx xxxxx. U xxxxxxxx X xx xxxx čísla xxxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxx. U xxxxxxxx X1 xx nutné xxxxxxxx tato čísla xx odstavení xxxxxxxxx xxxxxx xxxxxxxxx x xxxxxx. X všech xxxxxxxxx pokusných xxxxxx xxxxxxxx X1 xx xxxxx xxxxxxx xxxxxxxxxx xxxxx xxxx. Xxxxx xxxx se xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx xx xxxxxxxx po xxxxxxxx, xxx xx xxxxxxx xxxxxxxxxxxx xxxxxx xxxxxx xxxx jakékoliv xxxxxxx zkoušky.
Na xxxxxxx xxxxxxxx xxxxx musí xxx xxxxxxxxxx (X) xxxxxxxx xxxxxxxxx xxxxxx xxxxx xxxxxxxxx 5 xx 9 xxxxx. Xx-xx xx možné, xxxx xx xxx xxxxxxx zvířata xx xxxxx xxxxxxxxxx xxxxxx xxxxxxx xxxxxxxx x xxx.
1.4 XXXXXX
1.4.1 Xxxxx x xxxxxxx xxxxxxxxx xxxxxx
Xxxxx experimentální x xxxxxxxxx xxxxxxx xx xxxx xxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx xxxxxx, xxx bylo xxxxx xxxxxx minimálně 20 xxxxxxx xxxxx s xxxxxxxxx stejným xxxxxxxx xxxx. To xxxxxxxxxxxxx xxxxxx xxxxx x xxxxx, xxxxx vyvolávají xxxxxxxxx xxxxxx spojené x xxxxxxxx (xxxx. xxxxxxxxx, nadměrnou toxicitu xxx vysoké xxxxx). Xxxxx xx xxxxxx xxxxxxxxxx počet březích xxxxx, x tím xxxxxxxx významné xxxxxxxxx xxxxxxxxxx xxxx xxxxx xxxxxxxx plodnost, xxxxxxx, xxxxxxx samic x xxxxxxxx xxxx'xx, xxxx x xxxxx xxxxxxxxx xxxxxxxx F1 xx xxxx xxxxxx až xx xxxx xxxxxxxxxx x xxxxx xxxxxx xxxxxxxxx (X2) až xx odstavení. Nepodaří-li xx xxxx dosáhnout xxxxxxxxxxxx počtu xxxxxxx xxxxxxxxx zvířat (xx. 20), xxxxxx xx xxxxx xxxxxxxx xxxxxxxxxxxx xxxxxx, a xxxxx xx hodnocení mělo xxxx xxxxxxxx xxxxxxxxxxxx xxxxxx od xxxxxxx.
1.4.2 Xxxxxxxx dávek
Není-li xxxx xxxxxxxxx způsob xxxxxxxx (xxxx. xxxxx xxxx xxxxxxxxx), doporučuje xx xxxxxx xxxxxxxx xxxxxxxx xxxxx (x xxxxxx, xxxxx vodě nebo xxxxxx xxxxxxxxx xxxxx).
Xxxxxxxx xxxxx xx x xxxxxxx xxxxxxx rozpustí xxxx suspenduje ve xxxxxxx xxxxxxxx. Xx-xx xx xxxxx, doporučuje xx xxxxxx použití xxxxxxx xxxxxxx/xxxxxxxx, poté xxxxxxx roztoku/emulze x xxxxx (xxxx. x xxxxxxxxxx xxxxx) x xxxxxxx xxxxxxx x xxxxx vehikulu. U xxxxxx typu xxxxxxxx, xxx xx voda, xx třeba xxxx xxxx xxxxxxxxxxxxx charakteristiky. Xxxxxxx xx xxxxxxx xxxxxxxx látky x xxxxx xxxxxxxx.
1.4.3 Dávkování
Použijí xx xxxxxxx xxx xxxxxx xxxxx a xxxxxxxx xxxxxxxx. Xxxx-xx xxxxx limitována xxxxxxxxx-xxxxxxxxx xxxxxxxxx nebo xxxxxxxxxxxx xxxxxx xxxxxxxx xxxxx, xxxxx xx xxxxxxxx xxxxxx dávky tak, xxx vyvolala xxxxxxxx, xxx xxxxxxxxxxx xxxx xxxx xxxxx xxxxxxx. X xxxxxxx xxxxxxxxxxx xxxxxxxxx jsou obvykle xxxxx xxxxxxxxxx xxxxxx x úmrtností xxxxxxxxxxxx (X) xxxxxxxxx xxxxxx xxxxx než xxxxxxxxx 10 %. Ve xxxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxx x xxxxxxxxxx a x xxxxxxxx dávky xxx xxxxxxxxxxxxxxx nepříznivého xxxxxx (XXXXX) xx xxxxx xxxxxxxx posloupnost xxxxxx xxxxx. Pro xxxxxxxxx xxxxxxxxxx xxxxxx xxxxx xxxx xxxxxxx optimální xxxxxxxxx lišící xx xxxxxxxx 2 xx 4 x xxxxx xx xxxxxxxxx xxxxxxx xxxxxx zkušební skupiny xxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxx jednotlivými xxxxxxx (xxxx. lišících xx xxxxxxxx 10). X xxxxxx xx xxxxx xxxxxx xxxxxx xxx xxxx xxx xxxxxxxxxxx. Při xxxxxx xxxxxx dávek xx xxxxx vzít x xxxxx xxxxxxxxx xxxxxxxxxx xxxxx x xxxxxxxx, x to zvláště x případě xxxxxxxx xxxxxx xx opakované xxxxx. Xxxxxx xx xxxxx vzít v xxxxx jakékoliv xxxxxxxxxx xxxxxxxxx o xxxxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxxxxxx xxxxx. Xxxx informace xxxxx xxxxxxxxx xxxxxx xxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxx.
Xxxxxxxxx skupina xx xxxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxx x xxxxxxxxx, xxxxx xx xxxxxxxxx pro xxxxxxxx xxxxxxxx látky xxxxxxx. X xxxxxxxx xxxxxxxx xxxxxxxx xxxxx xx xxxxx x xxxxxxxxx zvířaty x xxxxxxxxx skupině xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxx x xxxxxxxxx xxxxxxx x xxxxxxxxxxxxxx xxxxxxx. Xxxxxxx-xx xx xxxxxxxxx, xxxx xx xxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxxxx xxxxxx. Xxxxxx-xx xx xxxxxxxx xxxxx x xxxxxx x xxxxxxxxx-xx snížený xxxxxx nebo xxxxxxx xxxxxx, xxx xx xxxxx xxxxxx xxxxxxx xxxxxxx xxxxxx krmené xxxxxxxxx xxxxxxx. Xxxxx xxx xxxxx xxxxxxxx xxxxxx krmené xxxxxxxxx xxxxxxx xxxxxx xxxxx xxxxxxx x xxxxxxxxxxxxxx xxxxxx xxxxxxxx k xxxxxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxxx na xxxxxxxxxxx parametry.
Pozornost xx xxxxx věnovat xxxxxxxxxxxx xxxxxxxx znakům xxxxxxxx x xxxxxx xxxxxx: xxxxxx xx xxxxxxxx, xxxxxxxxxx, xxxxxxxxxxxx, nebo xxxxxxx zkoušené xxxxx, xxxx vlivu na xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxx, xxxxx xxxxx xxxxxx xxxx toxikologické xxxxxxxxxx, x vlivu xx xxxxxxxx xxxxxx, xxxx nebo xxxxxxxx xxxx pokusných zvířat.
1.4.4 Xxxxxxx xxxxxxx
Xxxxx xxxxxx xxxxxx s xxxxxx xxxxxx dávky v xxxxxxxx alespoň 1&xxxx;000 xx /xx xxxxxxx xxxxxxxxx na xxx, xxxx rovnocenné xxxxxxxx xxxxx v xxxxxx xxxx xxxxx xxxx xxx xxxxxxxx xxxxx x xxxxxx xxxx xxxxx vodě xxxxxx xxxxxxx xxxxxxxxxxxx pro xxxx xxxxxx xxxxxxxx xxxxxx xxxxxxxxxxxx toxicitu xxx x xxxxxxxxxxxx xxxxxxxxx xxxxxx, xxx x xxxxxx potomstva x pokud xx xxxxxxxxx ani xxxxxxxx xx základě existujících xxxxx x strukturně/metabolicky xxxxxxxxxx xxxxxxxxxxxx, pak xxxx xxxxx uvažovat x kompletní studii xxxxxxxxxxx xxxxxxxx xxxxxx xxxxx. Xxxxxxx zkouška xx xxxxxxx, xxxxx xxxxxxxx x xxxxxxx xxxxxxxxxx použít xxxxx xxxxxx orální xxxxx. X xxxxxxx xxxxxxx xxxxxxxx xxxxx, xxxx xx xxxxxxxxx nebo xxxxx xxxxxxxx, může xxx xxxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxx-xxxxxxxxxx vlastnostmi zkoušené xxxxx.
1.4.5 Xxxxxxxx dávek
Zkoušená xxxxx xx podává xxxxxxxx zvířatům 7 xxx v xxxxx. Xxxxxxxxxxxxx xx xxxxxx xxxxxx podávání (x xxxxxx, xxxxx xxxx xxxx xxxxxxxxx xxxxxx). Xxxxx xx xxxxxxx xxxx xxxxxx xxxxxxxx, xx xxxxx xxxxx xxxxxxxxxx x provést xxxxxxxxxxxx modifikace. Xxxx xxxxxxxx xxxxxxxx xx xxxx xxx látka xxxxx xxxxxxxxxxxxxx experimentálního xxxxxx xxxxxxxx xxxxxxx xxxxxxxx. Objem xxxxxxxxxxx xxxxxxxx xxxxxxxx xx xxxxx xxxxxxxxx 1 xx/100 g tělesné xxxxxxxxx (0,4 xx/100 x xxxxxxx hmotnosti xx xxxxxxx pro xxxxxxxxx xxxx), xxxxxxxx xxxx xxxxx xxxxxxx, xxx lze použít 2 xx/100 x xxxxxxx xxxxxxxxx.
X xxxxxxxx xxxxxxxxxx xxxx xxxxxxxx xxxxx, u xxxxxxx xxxxx xxxxxxxxxxx xxxxxxx xxxxx xx zhoršení xxxxxx, xx měla xxx xxxxxxxxxxx objemu xxxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxx, xxx xxxx xxxxxxxxx, xx xxxxxxxx xxxxx xxxx xxxxxx xxx xxxxxxx xxxxx.
Xx xxxxxxxx xxxxxxxxxx xx podávání xxxxx žaludeční xxxxxx xxxxx mláďata dostávat xxxxxxxxx látku xxxxxxx xxxxxxx prostřednictvím mléka, xxxxx nezačne xxxxx xxxxxxxxx xx jejich xxxxxxxxx. Ve xxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxx x krmivu xxxx pitné xxxx xxxxx xxxxxxx navíc xxxxxxxx xxxxxxxxx xxxxx xxxxx, xxxxxxx xxxxxx xxxxx posledního xxxxx xxxxxxxxxx xxxxxx xxxx xxxx.
X xxxxx podávané xxxxxxx nebo pitnou xxxxx xx xxxxx xxxxxxxx xxxxxxxx, xxx xxxxxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxx xxxx xxxx, xxxxxxxxx vyváženosti xxxxxxx xxxxxx xxxx xxxx. Xx-xx xxxxxxxx xxxxx xxxxxxxx v xxxxxx, xx xxxxx xxxxxxxx xxx konstantní xxxxxxxxxxx (xxx) x xxxxxx, xxxx xxxxxxxxxx xxxxxx xxxxx xx xxxxxx x xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx. Xxxxxxx xxxxxx xxxxxxx xx třeba xxxxxxxxx. Xxxxx podávaná žaludeční xxxxxx se xxxxxx xxxxx xxx xxxxxxxxx xx xxxxxxx xxxx x xxxxxxx jednou xxxxx xx xxxxxxxxxx xxx, aby xx xxxxxxx xxxxxxxxxx xxxxxx xxxxx vzhledem k xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx. Při xxxxxxxxxxxxxx xxxxx xxxxx xxxxxxxxx x podávání látky xxxxxx je třeba xxxx x úvahu xxxxxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxxxx.
1.4.6 Xxxxxxxxxx xxxxxx
X xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxx xx x rodičovské xxxxxxxx (X) xxxxx x xxxxx xxxxxx xx 5. do 9. xxxxx xxxx. Xxxxx xxxxxxxx xxxxx x xxxxx a xxxxx xxxxxxxx F1 xx xxxxx zahájit xx xxxxxx xxxxxxxxx; stále xx třeba mít xx paměti, že x xxxxxxx, xxx xx xxxxxxxx xxxxx xxxxxx prostřednictvím xxxxxx xxxx xxxxx xxxx, xxxx xxxxxxxx x xxxxx xxxxxxxx xxxxxx X1 xxxxxxxx xxxxx xxx xxxxx xxxxxxxxxx xxxxxx. U xxxx xxxxxxx (X x X1) xx se xxxx x xxxxxxxxx xxxxx pokračovat xxxxxxx 10 xxxxx xxxx xxxxxxx xxxxxx. X xxxxxxxxxx se x xxxx xxxxxxx pokračuje x xxxxx dvoutýdenního xxxxxx xxxxxx. Nejsou-li xxxxx xxx nezbytní x xxxxxxxxx xxxxxxxxxxxxx xxxxxx, xxxx by xxx xxxxxxxx způsobem xxxxxxxx x xxxxxxxxx. X xxxxxxxxxx generace (X) xxxxx dávkování xxxxxxxxx x xxxxx xxxxxxxx a xx xx xxxxxxxxx xxxxxxxxx xxxxxxxx F X. Xxxxxxxxx xx xxxxx xxxxxxx modifikacím xxxxxxxxxxx xxxxxxxx na xxxxxxx xxxxxxxxxx xxxxxxxxx o xxxxxxxx látce, xxxxxx xxxxxxxxxxxx xxxxx o xxxxxxxx, xxxxxxx xxxxxxxxxxx xxxx bioakumulaci. Xxxxxxx xx xxxxx xxx xxxxxxxxxx xxxxxxx xxxxxxx xxxx vycházet x xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx. Xxxxxx xxxxxxxxx xx xxxx xxxxx xxxxxxx úpravě xxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx.
Xxxxxxxx xxxxx samcům x samicím generací X a X1 xxxxxxxxx až do xxxx xxxxxx xxxxxxxx. Xxxxxxx dospělí xxxxx x xxxxxx xxxxxxxx X a X1 xx humánním xxxxxxxx xxxxxx, pokud xxx xxxxxx nezbytní x xxxxxxxxx xxxxxxxxxxxxx účinků. Xxxxxxxxx xxxxxxxx X1, xxxxx xxxx xxxxxxx x páření, a xxxx potomstvo xxxxxxxx X2 xx xx xxxxxxxxx xxxxxxxx způsobem xxxxxx.
1.4.7 Páření
1.4.7.1 Připouštění xxxxxxxxxx xxxxxxxx (X)
X xxxxxxx xxxxxx xx xxxxx xxxxxx umístí x xxxxxx xxxxxx xx xxxxxxx úrovní xxxxx (xxxxxxxx 1:1), xxxxx xxxxxxx xx xxxxxxx, xxxx xx xxxx xxxxxxx 2 xxxxx. Každý xxx xx xxxxxx vyšetří xx xxxxxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxx. Xxxxxx dnem březosti xx xxx, xxx xx pozorována xxxxxxxxx xxxxx nebo xxxxxxx. X případě, xx xx xxxxxxx neúspěšné, xx xxxxx xxxxxxx xx xxxxx s xxxxxxxxxx xxxxxxxxx xx xxxxxx xxxxxxx. Xxxxxxx xxxx xx v xxxxxxxxx xxxxx xxxxxx. Xx xxxxx se xxxxxxxxx xxxxxx sourozenců.
1.4.7.2 Xxxxxx xxxxxxxx X1
X xxxxxx xxxxxxxxx xxxxxx xxxxxxxx F1 se xx xxxxxx produkce xxxxxxxx X2 xx xxxxxxxxx xxxxxx x xxxxxxx xxxx xxxxxxx xxxxx xxxxx x xxxxxx xxx xxxxxxx x xxxxxx xxxxxxxxx xxxxxxx ze stejné xxxxxxx xxxxxxx, xxx x odlišného xxxx. Xxxxx pokusných xxxxxx x xxxxxxx xxxx xx xxxxxxx náhodně, xxxxx xxxxxx xxxx xxxxxxxxx xxxxxxx z xxxxxx xxxx xxxxxxxxxx xxxxx výrazné odlišnosti x xxxxxxx xxxxxxxxx xxxx xxxxxxx. X xxxxxxx zjištěných odlišností xx x xxxxxxx xxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxx. Xxxxxxx xx xxxx nejlepší xxxxx xxxxx provádět xx xxxxxxx xxxxxxx xxxxxxxxx, xxx xxxxxxxxx se xxxx xxxxx xxxxx xx xxxxxxx xxxxxxx. Xxxxxxxxx xxxxxxxx X1 xx xx xxxxxx xxxxxxxxxx xxxx xxxxxxxxx xxxx xxxxxxxx zralosti.
Páry, x xxxxxxx nedojde x xxxxxxxxx, xx xxxxx vyšetřit za xxxxxx xxxxxxxx příčiny xxxxxxxxxxx. Tento xxxxxx xxxx xxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxx x xxxxxxxxx x xxxxxxxx xxxxxxxx x osvědčenou xxxxxxxxx, xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx orgánů xxxxx xxxxxxxxx estrálního xxxxx x xxxxxxxxxxxxxx.
1.4.7.3 Xxxxx xxxxxx
X určitých případech, xxxx xxxx. x xxxxxxxx velikosti xxxx xxxxxxxxx s xxxxxxxx xxxx xxx zjištění xxxxxxxxxxxxxxx xxxxxx xx xxxxxx xxxxxx, xx xxxxxxxxxx opětovné xxxxxxxxxx xxxxxxxxx pokusných xxxxxx x generace P x X1 xx xxxxxx produkce xxxxxxx xxxx. Xxxxxx xx xxxxxxxxxx znovu xxxxxxxxx xxxxxx nebo xxxxx, x xxxxxxx xxxxxxx x xxxxxxxx xxxxxx x osvědčenými xxxxxxxxx xxxxxxx. Xxxxx xx x xxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxx. xxxx xx xxx xxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxx xxxxx xx xxxxxxxxx xxxxxxxxxx xxxx.
1.4.7.4 Xxxxxxxx xxxx
Xxxxxxxx xxxxxxxx xx ponechá xxxxxxx xxxxxxxx vrhnout x xxxxxxx x xxxxx xxxxxxxxx xx xx xxxx odstavení. Standardizace xxxxxxxxx xxxx xx xxxxxxxxxx. Xxxxx xx xxxxxxxxxxxxx xxxxxxx, xx xxxxx používanou metodu xxxxxxxx popsat.
1.5 XXXXXXXXXX
1.5.1 Xxxxxxxx pozorování
Všeobecné xxxxxxxx xxxxxxxxxx se xxxxxxx xxxxx x v xxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxx xxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxx nejvyšších účinků xx xxxxxx látky. Xxxxxxxxxxx xx xxxxxxxx xxxxx chování, xxxxxx xxxxxxxxx xxxx xxxxxxxxxxxxxx xxxx a xxxxxxx xxxxxxxx xxxxxxxx. Alespoň xxxxxx xxxxx se x každého xxxxxxxxx xxxxxxx xxxxxxx xxxxx xxxxxxxxxxx vyšetření, xxxxx xx nejlepší provádět x xxxx xxxxxx xxxxxxxxx xxxxxxx. Xx-xx xx xxxxx, xxxxxxx xx dvakrát xxxxx, xxxxx xxxxxxx případně xxxxxx xxxxx, x xxxxx pokusných xxxxxx xxxxxxxxxx z xxxxxx xxxxxxxxx x xxxxxxxxx.
1.5.2 Xxxxxxx xxxxxxxx x xxxxxxxx xxxxxx/xxxx x xxxxxxxxxxxx pokusných zvířat
Rodičovská xxxxxxx zvířata (xxxxxxxx X x X1) xx zváží x xxxxx xxx xxxxxxxx xxxxx x xxxx xxxxxxx xxxxxx xxxxx. Xxxxxx rodičovské xxxxxxxx (X x X1) xx zváží 0., 7., 14. x 20. xxxx 21. xxx xxxxxxx, xxxxx xxxxxxxx dnů x xxxxxxx xxxxxxx xxx xxxxxx vrhů x xxxx v den xxxxxxxx pokusných xxxxxx. Xxxx pozorování se xxxxxxxxxxx individuálně x xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx. V xxxxxx xxxx pářením x xxxxx gestačního xxxxxx xx xxxxxxxx krmiva xxxx xxxxxxxxx každý xxxxx. Xxxxx xx xxxxx podává xx xxxx, xxxx xx xxxxxxxx xxxx xxxxxxx xxxxxx xxxxx.
1.5.3 Xxxxxxxx xxxxxx
Xxxx xxxxxxx x xxxxxxxxx i xxxxx xxxxxx xx x xxxxx generace X x X1 xxxxxxx xxxxx x xxxxxxxxxx xxxxxxxxxx cyklu xxxxxx xxxxxxxxxxx xxxxx, xxxxx xx nezíská xxxxx x xxxxxxxxxx. Xxx xxxxxxxxx xxxxxxxxxxx/xxxxxxxxxxxx xxxxx xx xxxxx xxxxxxxxx xxxxxxxx x xxxxxxxx xxxx xxxxxxxxx xxxx xxxxxxx xxxxxxxx
7a).
1.5.4 Xxxxxxxxx xxxxxxxx
X xxxxx xxxxx xxxxxxxx X x X 1 se xx utracení zaznamená xxxxxxxx xxxxxx x xxxxxxxxx x xxxxx x každého xxxxxx xx ponechá xxx xxxxxxxxxxxxxxxx vyšetření (viz xxxx 1.5.7, 1.5.8.1). Xxxxx varlata a xxxxxxxxxx x xxxxxxxxxx xxxxxxx deseti samců x každé xxxxxxxx X x F1 xx použijí pro xxxxxxx homogenizačně xxxxxxxx xxxxxxxxx a xxxxxxxxxx xxxxxxxxxxxxxx xxxxxx xxxxxxx. Xx xxxxxx podskupiny xxxxx xx shromáždí xxxxxxx x xxxxxxxxxx xxxxx xxxxxxxxx nebo xxxxxxx z xxxxxxxxx xx xxxxxx vyhodnocení xxxxxx xxxxxxxx a xxxxxxxxxx. Xxxxx xx xxxxxx účinky xxxxxxx x xxxxxxxx xxxxx xxxxx xxxx z xxxxxx xxxxxx k xxxxxxxxx xxxxxx x xxxxxx xxxxxx na xxxxxxxxxxxxxx, xxxxxxx xx xxxxxxxxx xxxxxxxx u xxxxx xxxxx x xxxxx xxxxxxx podle xxxxx, xxxxx xx xxxxxxx omezí pouze xx xxxxx x xxxxxxxxx xxxxxxx x xx xxxxxxx generace X x F1 x vysokou xxxxxx.
Xxxxxxxx xx xxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx x spermií x xxxxxxxx části xxxxxxxxx
7a). Xxxxxxxx xxxxxxx xxxxxxx xxx odvodit x xxxxxxxxxxx x xxxxxx xxxxxxx x xxxxxxxx používané k xxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx x xxxxx spermií xxxxxxxxx pomocí xxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxxxx xxxxx kaudální xxxxx. Xxxxx xxxxxx zhotoveny xxxxxxxxx záznamy xxxx xxxxxxxxxxxx xxxxx nejsou-li xxxxxx xxxxxxxx a xxxxxxx xxxxxxxxx xxxxxxx, xx xxxxx výpočet x vybrané podskupiny xxxxx xx xxxxx xxxxxxxxx skupin xxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxxx xxxxxx. V xxxxxx případech xx xxxxxxx xxxxxxx xxxxxxx x kontrolní xxxxxxx x x xxxxxxx x xxxxxxx xxxxxx. Xxxxx xx xxxxxxxx xxxxx xxxxxx spojené x xxxxxxxx (xxxx. xxxx na počet, xxxxxxxx nebo morfologii xxxxxxx), xxxx xxxxx xxxxxxxx xxxxxxx u xxxxxxxxx xxxxxxxxx xxxxxx. Xxxxx se zjistí xxxxxx spojené x xxxxxxxx x xxxxxxx x vysokou dávkou, xx nutné xxxxxxxxx x xxxxxxx s xxxxxxx xxxxxxx.
Xxxxxxxx xxxxxxxxxxxxxx xxxxxxx (nebo xxxxxxx x xxxxxxxxx) se xxxxxxxxx nebo xxxxxxxxx xx xxxxx okamžitě xx utracení. Xxxxxxx xx odeberou tak, xxx xxxxx k xxxxxxxxxxx poškození, x xxxxxx vhodných metod xx xxxxx pro xxxxxxx xxxxxxxx
7a). Procento xxxxxxxxxxx xxxxxxxxxxx spermií xx xxxxxxx subjektivně, xxxx objektivně. Xxxxx xx provádí počítačová xxxxxxx pohyblivosti
7a), spočívá xxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxxxxxx hodnotách xxxxxxxx xxxxxxxxx xxxxx a xxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxxx. Xxxxx xx xxxxxx videozáznam xxxxxx
7a) xxxxx xxxx xxxxxxxxx xxxxx xxxxx xxxxxxxxxxx xxxxx způsobem, stačí xxxxxxx xxxxxxxxx xxxxxxx xxxxx u kontrolní xxxxxxx x x xxxxxxx s vysokou xxxxxx x xxxxx x xxxxxxxx X x F1, xxxxx xxxxxxx ke xxxxxxxx xxxxxx xxxxxxxxx s xxxxxxxx. X takovém xxxxxxx xx xxxxx xxxxxxxxxx xxxxxx skupiny x nižší xxxxxx xxxxx. Pokud xxxxxx x dispozici žádné xxxxxxxxx záznamy xxx xxxxxxxxxxx, analyzují xx xxxxxx xxxxxxx xxxxxx xx xxxxx xxxxxxxxxxxxxxxx xxxxxx.
Xxxxxxx xx xxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxx (nebo spermií x xxxxxxxxx). Spermie (xxxxxxxxx 200 na xxxxxx) xx xxxxxxx xxxx xxxxxxxx, xxxxx xxxxxxxxx
7a) x xxxxxxxxxxx xx xxxx xxxxxxxx xxxx xxxxxxxxxx. Příklady xxxxxxxxxxxxxx xxxxxxxx spermií xx xxxx xxxxxxxxx xxxxxxx, xxxxxxxxx a xxxxxxxxxxxx xxxxxxxx xxxx xxxxxx. Xxxxxxxxx xx xxxxxxx u xxxxxxxxx xxxxxxxxx xxxxx xx xxxxx xxxxxx xxxxx xxxxxx xxxxx bezprostředně xx xxxxxxxx pokusných xxxxxx, xxxx xxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxxx nebo xxxxxxxxxxxx. Xxxx-xx stěry zakonzervované, xxx xx rovněž xxxxxxxxxx xxxxxxx. V xxxxxxx xxxxxxx xx xxxxxxxxx nejprve xxxxxxxxx xxxxxxx x skupiny x xxxxxxx xxxxxx. Xxxxx xx xxxxxxxx xxxxx xxxxxx xxxxxxx x xxxxxxxx (např. xxxxxx xx xxxxxxxxxx xxxxxxx), xxxx xxxxx xxxxxxxxxx ostatní xxxxxxx xxxxxxx. Pokud xx xxxxxx xxxxxx xxxxxxx x xxxxxxxx x xxxxxxx s xxxxxxx xxxxxx, xxx xx xxxxx xxxxxxxxx i xxxxxxx x nižšími xxxxxxx.
Xxxxx již xxxx xxxxxxxxxx xxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx x xxxxx xxxxxxx 90 dnů xxxxxxxx studie xxxxxxxxx xxxxxxxx, xxx xxxx xxxxx xx x xxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxx. Xxxxxxxxxx se xxxx xxxxxxx vzorky xxxx xxxxxxxxx xxxxxxx xxxxxxx x xxxxxxxx X uchovat pro xxxxxxxx xxxxxxxxx.
1.5.5 Xxxxxxxxx
Xxxxxxx xxxx xx xxxxxxx xx xxxxxxxx xx xxxx (v nultý xxx laktace), xxx xxxx možné xxxxxxxx xxxxx a xxxxxxx xxxxxx, xxxxx xxxxx x xxxx xxxxxxxxxx xxxxxx x přítomnost xxxxxxxxx xxxxxxxx. Xxxxxxx, xxxxx xxxx xxxxxxxx xxxxx x xxx 0, se vyšetří xx možné defekty x xxxxxxx smrti (xxxxxx-xx xxxxxxxxx) a xxxxxxx xx uchovají. Xxxx xxxxxxx xx xxxxxxxxx x individuálně xxxxx xxxxx po xxxxxxxx (x xxxxx xxx laktace) nebo xxxxx 1. xxx x xxxx xx xxxx x pravidelných xxxxxxxxxxx, xxxx. v 4., 7., 14., x 21. xxx xxxxxxx. Xxxxxxxxxxx xx xxxxxxx xxxx behaviorální xxxxxxxxxxx zjištěné u xxxxx nebo xxxxxx xxxxxxxxx.
Xxxxxxx xxxxx x xxxxxxxxx xx xxxxxxxxxxx xxxxxx podle přírůstku xxxxxxx xxxxxxxxx. Xxxxx xxxxxxx xxxxxxxxx (např. xxxxxxxx xxx a xxx, xxxxxxxxxxx xxxx, xxxx xxxxx) xxxxx xxxxxxxxxx doplňkové xxxxxxxxx, xxx u těchto xxxxx xx xxxx xxxxxxxx xxxxxxxxx v xxxxx kontextu údajů x xxxxxxxx xxxxxxxx (xxxx. xxxxx a xxxxxxx xxxxxxxx xxx xxxxxxxxxx otevření xxxx xxxxxxxx xxxxxxxxx)
7a). Xxxxxxxxxx xx provést xxxxxxx xxxxxxxxx (xxxx. pohybová xxxxxxxx, smyslové xxxxxx, xxxxxxxx ontogeneze) xxxxxxxxx xxxxxxxx X1 xxxx xxxx xx xxxxxxxxx, x to xxxxxxx xxxxxxxxx týkající xx xxxxxxxx zralosti, xxxxxx-xx xxxxxx vyšetření xxxxxxxx xxxxxxxxxxxx xxxxxx. X xxxxxxxxxxx xxxxxxx xxxxxxxx X1 xxxxxxxxx x xxxxxxxxxx xx xxxxx xxxxxxxx stáří, ve xxxxxx došlo x xxxxxxxxxxx otevření x xxxxxxxxx xxxxxxxxx. X xxxxxx generace X2 xx xxxxx změřit xxxxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxxx dne 0, xx-xx vyvolána změnami x xxxxxx pohlaví x xxxxxxxx F1 xxxx načasováním xxxxxxxx xxxxxxxx.
Xxxxxxx sledování xxx xxxxxxxx x skupin, xxxxx jinak xxxxxxxx xxxxx xxxxxx xxxxxxxxxxxx xxxxxx (xxxx. xxxxxxxx xxxxxxx přírůstku xxxxxxxxx xxx.). Pokud xx xxxxxxx xxxxxxx xxxxxxxxx, xxxxxx by se xxxxxxxx x mláďat xxxxxxxxx k xxxxxx.
1.5.6 Xxxxxxx pitva
Po xxxxxxxx xxxx uhynutí xxxxx xxxxxx xx všechna xxxxxxx xxxxxxx rodičovské xxxxxxxx (X x X1), xxxxxxx xxxxxxx xx xxxxxxx xxxxxxxxxx xxxx klinickými xxxxxxxx x xxxxxx xxxxx xxxxxxx vybrané xxxxx x každého xxxxxxx x xxxx z xxxx generací X1 x F2 xxxxxxxxxxxxx xxxxxxx na xxxxxxxxx xxxxxxxxxxxx abnormality xxxxx xxxxxxxxxxx xxxxx. Xxxxxxxxx xxxxxxxxx xx xxxxx xxxxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx. U xxxxxx, xxxxx xxxx humánním xxxxxxxx utracena xx xxxxx agónie, x x xxxxxxx xxxxxx, xxxxx xxxxxx rozložena, xx provede vyšetření xx účelem xxxxxxxx xxxxxxx defektů nebo xxxxxxx uhynutí. Xxxxxxx xx xxxxxxxx.
Xxxxxx xxxxx xxxxx xxxxxxxxxxx xx xxxxxxx xx přítomnost x xxxxx zachycených xxxxxxx x děloze.
1.5.7 Xxxxxxxx xxxxxx
X xxxxxxxx xxxxxxxx se u xxxxx rodičovských pokusných xxxxxx xxxxxxxx X x X1 xxxxxxx xxxxxxx xxxxxxxx x xxxxxxxx těchto orgánů (xxxxxx orgány xx xxxxx vážit xxxxxxxxxx):
- xxxxxx, xxxxxxxxx,
- xxxxxxx, xxxxxxxxxx (xxxxxx x xxxxxxxx),
- prostata,
- xxxxxxx xxxxx x xxxxxxxxxxxx xxxxxxx x xxxxxx xxxxxxxxxx x s xxxxxxxxx (jako jedna xxxxxxxx),
- xxxxx, játra, xxxxxxx, xxxxxxx, xxxxxxxx, xxxxxx žláza x xxxxxxxxxxx a známé xxxxxx orgány.
U xxxxxx xxxxxxxx F1 x X2 vybraných x xxxxx se stanoví xxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxx. X xxxxxxx náhodně xxxxxxxxx xxxxxxx x xxxxxxx xxxxxxx x vrhu (xxx xxxx 1.5.6) xx zváží xxxx xxxxxx: xxxxx, xxxxxxx x xxxxxx.
Xx-xx xx xxxxxxxxxxxx, xxxxxxxx xx xxxxxxxx xxxxxxx xxxxx x hmotnosti xxxxxx x xxxxxxxxxxx x xxxxxxxx xxxxxxxxxx x xxxxxx xxxxxxxx opakovaného xxxxxxxxx.
1.5.8 Xxxxxxxxxxxxxx
1.5.8.1 Rodičovská xxxxxxx xxxxxxx
Xxx histopatologické xxxxxxxxx se xxxxxxxx x xx xxxxxxx xxxxxxxxx uchovají tyto xxxxxx x xxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx (X x X1) xxxx xxxxxx xxxxxxxxxxxxxxx xxxxxx:
- pochva, xxxxxx x xxxxxxxx hrdlem x xxxxxxxxx (xxxxxxx xx xxxxxxx xxxxxxxxxxxx xxxxxxxxxx),
- xxxxx varle (xxxxxxx x Xxxxxxxx xxxxxxx nebo xxxxx xxxxxxxxxxxx prostředku), xxxxx xxxxxxxx, xxxxxxx xxxxx, xxxxxxxx x koagulační xxxxx,
- xxx dříve xxxxxx xxxxxx xxxxx xxxx xxxxxx xx xxxxx xxxxxxxxx xxxxxx xxxxxxxx X x X1 xxxxxxxxx x xxxxxx.
X všech xxxxxxxxx xxxxxx generace P x X1 xx xxxxxxx x xxxxxxx xxxxxx x z xxxxxxxxx xxxxxxx xxxxxxxxx x páření xx xxxxxxx xxxxxxxxx histopatologické xxxxxxxxx všech xxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxx x tkání. Xxxxxxxxx xxxxxxxxx u xxxxxxxxx xxxxxx xxxxxxxx X xxxx povinné. Provede xx xxxxxx xxxxxxxxx xxxxxx vykazujících změny xxxxxxx x xxxxxxxx xxxxx x xxxxxxxxx xxxxxx xx skupiny x xxxxxx x xxxxxxx xxxxxx, které xxxxx napomoci xxxxxxxx xxxxx XXXXX. Histopatologické xxxxxxxxx xx xxxxx xxxxxxx x reprodukčních xxxxxx pokusných zvířat xx xxxxxxx x xxxxxx a xxxxxxx xxxxxx, u xxxxxxx xx xxxxxxxxx xx xxxxxxxx plodnost, xxxx. x xxxx, u xxxxxxx xxxxxxx x xxxxxx, xxxxxxxxxx, xxxxxxxxx xxxx k xxxx xxxxxxxx xxxxxxxxx xxxx x xxxxxxx byl xxxxxxxx xxxxxxxx xxxxxx xxxx počet, xxxxxxxx xxxx xxxxxxxxxx xxxxxxx. Xxxxxxx xx xxxxxxx xxxxxxxxxxxxx xxxx, xxxx xxxx. xxxxxxx nebo xxxxxx.
Xx xxxxxx xxxxxxxx xxxxxx xxxxxxxxx s xxxxxxxx, jako xxxx xxxx. nevyvinuté xxxxxxxxxx, xxxxxxxxx vrstva xxxx xxx xxxxxxxxxxx xxxxx, xxxxxxxxxxx obří buňky xxxx xxxxxxxxx spermatických xxxxx x xxxxxx, xx xxxxxxx podrobné xxxxxxxxxxxxxxxx xxxxxxxxx xxxxxx (xxxx. pomocí Xxxxxxxx xxxxxxx, zalití xx xxxxxxxx a xxxxxxxx xxxx o xxxxxxxx 4 - 5 µx)
7a). Xxxxxxxxx xxxxxxxxxx xxxxxxxxxx by mělo xxxxxxxxx xxxxxxxxx xxxxx, xxxx x xxxxxxxx xxxxx, xxxxx lze xxxxxxxxx xxxxxxxxxxxx podélného xxxx. X xxxxxxxxxx xx vyšetří xxxxxxxxxxx xxxxxxxxxx, změna x xxxxxxxxxx xxxx xxxxx, xxxxxxxxx typy buněk x fagocytóza spermií. X vyšetření xxxxx xxxxxxxxxxxx xxxxxxxx xxx xxxxxx XXX a xxxxxxxxx hematoxylinem.
Postlaktační xxxxxxxx xx xxx xxxxxxxxx xxxxxxx a rostoucí xxxxxxxx x rovněž xxxxxxxx xxxxx xxxxxxx x období xxxxxxx. Xxxxxxxxxxxxxxxx xxxxxxxxx by xxxx xxxxxxx kvalitativní xxxxxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxx. X xxxxx generace X1 xx provede kvantitativní xxxxxxxxxxx xxxxxxxxx folikulů. X xxxxxxxxxxx xxxxxxxxx xxxxxxx xx xxxxx xxx statisticky xxxxxxxxxxxx xxxxx xxxxxxxxx xxxxxx, xxxxx řezů xxxxxxxxx x xxxxxxxx xxxxxx xxxx. X xxxxx xxxxxxx xxxxxxxx vaječníků x testované a xxxxxxxxx xxxxxxx xx xxxx vyšetření xxxxxxxxx xxxxxxx xxxxx původních xxxxxxxx, které xxx xxxxxxxxxxx s malými xxxxxxxxxx folikuly
7a).
1.5.8.2 Odstavená xxxxxxx
Xxx xxxxxxxxxxxxxxxx xxxxxxxxx xx xx vhodném xxxxxxxxx připraví x xxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxx x xxxxxx xxxxxx od xxxxx xxxxxx xx zevními xxxxxxxxxx xxxx klinickými xxxxxxxx x rovněž xx xxxxxxx xxxxxxx xxxxxxxxx xxxxxxx x xxxxxxx xxxxxxx x xxxx z xxxx xxxxxxxx F1 a X2, které xxxxxx xxxxxxx k xxxxxx. Xxxxxxxxx xxxxxxxxxxxxxxxx charakterizace xxxxxxxxxx tkání xx xxxxxxx xx xxxxxxxxxx xxxxxxx xx xxxxxx xxxxxxxxxxxx xxxxxxxx.
2 XXXX
2.1 XXXXXXXXXX XXXXXXXX
Xxxxxxxx se xxxxxxxxxxxxx individuálně a xxxxxx xx xx xxxxxxx xxx, xxx xxx x xxxxx xxxxxxxxxxxxxx xxxxxxx a xxxxx xxxxxxxx xxxxxx xxxxx xxxxxxxxx xxxxxx xx xxxxxxx xxxxxxx, xxxxx pokusných xxxxxx xxxxxxxxx xxxxx xxxxxxx xxxx xxxxxxxxxx x xxxxxxxxx důvodů, xxxx xxxxx xxxx humánního xxxxxxxx, počet xxxxxxxx xxxxx, počet xxxxxxx xxxxx, xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx, xxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxx nástupu, trvání x závažnosti xxxxxxxxx xxxxxxxxx xxxxxx, typy xxxxxxxxxx rodičovských xxxxxxxxx xxxxxx x xxxxxx xxxxxxxxx a xxxxxxx xxxxxxxx xxxxx o xxxx.
Xxxxxxxxx výsledky xx xxxxxxxxx xxxxxx xxxxxx, xxxxxxxxx xxxxxxxx statistické xxxxxx; xxxxxx xx xxxxx xxxx xxxxxxx xxxxxx xxxxxx a xx xxxxx xx xxxxxxxxx. Pro xxxxxxx xxx xx vhodné xxxxxx xxxxxxxxxxx xxxxxx xxxxx-xxxxxx. Xxxxxxxx xx xxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx x použité xxxxxx xxxxxxx x xxxxxxxxxxx xxxxxxxx, aby xxxx tuto xxxxxxx xxxxx vyhodnotit x xxxxxxxxxxxxx nezávislý xxxxxxxxx/xxxxxxxxx.
2.2 XXXXXXXXX VÝSLEDKŮ
Výsledky této xxxxxxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xx xxxxxxxxx xx xxxxxx x xxxxxxxxxxx xxxxxxx xxxxxx xxxxx x xxxxxxxxxxxxxxx xxxxxx. V hodnocení xxxx xxx uvedeno, xxx existuje xxxx xxxxxxxxxx souvislost xxxx xxxxxx xxxxxxxx xxxxx x xxxxxxxxxxx xxxx xxxxxxxxxxxxx, výskytem x xxxxxxxxxx xxxxxxxxxx včetně xxxxxxxxxxxxxxx lézí stanovených xxxxxxxx orgánů, xxxxx xx xxxxxxxx, xxxxxxxxxx xxxxxxxxxx, xxxxx na xxxxxxxxxxx xxxxxxxxx a xxxxxxxxx vrhu, změny xxxxxxx xxxxxxxxx, xxxxx xx xxxxxxxxx x xxxxx xxxxxxx xxxxxx. Xxx xxxxxxxxx výsledků xxxxxxx xx xxxxxxxxx x xxxxxxxxx-xxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx a xxxxxxxxxxxxxxxx údajům, jsou-li x xxxxxxxxx.
Xxxxxxx xxxxxxxxx xxxxxxx reprodukční xxxxxxxx xx xxxx xxxxxxxx xxxxxxxxxxx xxxxx úrovně xxxxx bez xxxxxx x xxxxxxxxxx nepříznivých xxxxxx xx xxxxxxxxxx, xxx, laktaci, xxxxxxxxxxx xxxxx xxxxxx růstu x pohlavního xxxxxx.
2.3 XXXXXXXXXXXX XXXXXXXX
Xxxxxxxxxxxxx xxxxxx xxxxxxxxxxx toxicity xxxxxxxx xxxxxxxxx x účinku xxxxxxxxx xxxxxxxx xxxxx xxxxx xxxxx fází xxxxxxxxxxxxx cyklu. Xxxxxx xxxxxxx poskytne xxxxxxxxx x xxxxxxxxxxxxx xxxxxxxxxxx x o xxxxxx, xxxxx, xxxxxxxxx x xxxxxxxxx potomstva. Výsledky xxxxxx se xxxxxxxxxxxx x xxxxxxxxxxx s xxxxxxxx ze xxxxxxxxxxxxxx, xxxxxxxxxxxxx, xxxxxxxxxxxxxxxxx x xxxxxxx xxxxxx. Xxxxxxxx xxxx studie lze xxxxxx x xxxxxxxxx xxxxxxx xxxxxxx zkoušení xxxxxxxx látky. Xxxxxxxxxxx xxxxxxxx této xxxxxx xx xxxxxxx xxxxx xxxxx x omezené xxxx. Největší xxxxxx xxxxxx xxxxxxxx spočívá x xxx, xx xxxxxxxxx xxxxxxxxx x xxxxxx xxxxx xxx xxxxxx a o xxxxxxxxx xxxxxxxx xxxxxxx
7a).
3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX X XXXXXXXXX XXXXXX
X souladu s xxxxxxxxxxx xxxxxxxx xxxxxxxx
9),10) xxxx být xxxxxxxxx projekt xxxxxx x x průběhu xxxxxx je nutno xxxx xxxxxxxx.
3.1 Zpráva x průběhu xxxxxx xxxxxxxx xxxx xxxxxxxxx:
Xxxxxxxx xxxxx:
- xxxxxxxxx xxxxxxxxxx x popřípadě fyzikálně-chemické xxxxxxxxxx,
- xxxxx x xxxxxxxx,
- čistota.
Vehikulum (v xxxxxxx potřeby):
- zdůvodnění xxxxxx xxxxxx xxxxxxxx, xxxxx xxxx použita xxxx.
Xxxxxxx xxxxxxx:
- xxxxxxx xxxx x xxxx,
- xxxxx, stáří x xxxxxxx xxxxxxxxx zvířat,
- xxxxx, xxxxxxxx xxxxx, xxxxxx, materiál xx xxxxxx hnízda atd.,
- xxxxxxxx jednotlivých pokusných xxxxxx na xxxxxxx xxxxxxx.
Xxxxxxxxxxxxxx xxxxxxxx:
- xxxxxxxxxx xxxxxx xxxxxx látky,
- xxxxxxxx xxxxx x xxxxxxx zkoušené xxxxx/xxxxxx, x dosažené xxxxxxxxxxx,
- xxxxxxx x xxxxxxxxxx xxxxxxxxxx,
- xxxxxxxx xxxxx x xxxxxxxx xxxxxxxx xxxxx,
- v případě xxxxxxx xxxxxxxx koncentrace xxxxxxxx látky (ppm) x xxxxxx/xxxxx vodě xx skutečnou xxxxx (xx/xx tělesné hmotnosti xx xxx), xx-xx xx xxxxx,
- podrobné xxxxx x kvalitě xxxxxx x xxxx.
Xxxxxxxx:
- xxxxxxxx krmiva a xxxx, xxxx-xx k xxxxxxxxx, využití xxxxxx (xxxxxxxxx xxxxxxx hmotnosti xx xxxx xxxxxxxxxxxxxx xxxxxx) a xxxxxxxx xxxxxxxx xxxxx x xxxxxxxxx zvířat generace X x F1 x xxxxxxxx období xxxxxxxxxx a xxxxxxxxx xxxxxxxx třetiny laktace,
- xxxxx o absorpci (xxxx-xx x dispozici),
- xxxxx o xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx x generace X x X1 xxxxxxxxx x xxxxxx,
- xxxxx x hmotnosti xxxx x xxxxxx,
- xxxxxxx xxxxxxxx při xxxxxxxx x xxxxx x xxxxxxxxx x xxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxxxx zvířat,
- povaha, xxxxxxxxx x xxxxxx (xxxx nástupu x xxxxxxxx xxxxxx) xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx (xxxxxxxx x nevratných změn),
- xxx xxxxx xxxxx xxxxxx xxxx údaj, xx xxxxxxx zvířata xxxxxxx až xx xxx xxxxxxxx,
- xxxxx x toxické xxxxxx xxxxx pohlaví x xxxxx, včetně koeficientů xxxxxx, xxxxxxxxx, xxxxxxx, xxxxxxxxxx, xxxxxxxxxxxxxxxx x xxxxxxx; xxxxxx by xxxx xxxxxx údaje xxxxxxx xxx xxxxxxx xxxxxx xxxxxxxxxxx,
- toxické xxxx xxxx xxxxxx xx xxxxxxxxxx, potomstvo, xxxxxxxxxxx xxxx atd.,
- xxxxxxx nálezy,
- xxxxxxxx xxxxx xxxxx histopatologických xxxxxx,
- xxxxx xxxxx x normálním xxxxxx x xxxxxxxx P x X1 a xxxxx xxxxx,
- xxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx, xxxxxxxx progresivně xxxxxxxxxxx xxxxxxx, xxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxx x procento spermií xx xxxxx xxxxxxxxxxxxxxxx xxxxxxxxxxxxx,
- xxxx xx xxxxxx včetně xxxxx xxx xxxx xxxxxxx,
- xxxxx gestace,
- xxxxx xxxxxxxxxx, xxxxxxx tělísek, xxxxxxxx vrhu,
- xxxxx xxxx xxxxxxxxxx xxxxxx x xxxxxxxxxxxxxxxxx ztrát,
- xxxxx xxxxxx s xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx x počet xxxxxxxxx xxxxxx, xxxxx xxx xxxxxxxxx,
- xxxxx o xxxxxxxxx vývojových znacích x mláďat x xxxxx údaje o xxxxxxxxxxxx vývoji; xxxxxxxxx xxxxxxx xxxxxxxx xxxxx xx xxxxx xxxxxxxxx,
- xxxxxxxxx xxxxx x xxxxxxxx xxxxxxxxxx mláďat x dospělých xxxxxxxxx xxxxxx,
- xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx, je-li xx xxxxx.
Xxxxxxx a interpretace xxxxxxxx.
Xxxxxx včetně hodnot XXXXX pro účinky xx samice x xxxxxxxxx.
X.36 TOXIKOKINETIKA
1 METODA xx x souladu x xxxxxx Evropských xxxxxxxxxxxx.
1)1.1 Xxxxxxx testovací xxxxxx
Xxxxxxxxx xxxxx xx xxxxxx vhodnou cestou. X závislosti xx xxxxxxxx studie xxxx xxx xxxxx podávána xxxxxxxxxxx xxxx opakovaně x xxxxxxx xxxxxxxxx xxxx xxxxx xxxx xxxxxxxx xxxxxxxx experimentálních xxxxxx. Xxxxx, xxxxxxxxxx xxxx xxxxxxxxxx, xxxx xxx podle xxxxx xxxxxx xxxxxxxxxxx v xxxxxxx xxxxxxxxxx, tkáních xxxxx v exkretech.
Studie xxxxx xxx xxxxxxxxx x "neznačenou" xx "xxxxxxxx" xxxxxx xxxxxxxxx xxxxx. Xxxxxxxx je xxxxxxx značení, xxxxxx xx xxx, xxx xxxxxxxx co xxxxxxx xxxxxxxxx o xxxxx xxxxxxxxx xxxxx x xxxxxxxxx.
1.2 Popis testovací xxxxxx
1.3 Xxxxxxxx
Xxxxxxx zvířata xxxx xxxxxxx x xxxxxxx xx druh, xxxxxxx x xxxxx x xxxxxxx x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x xxxxxxxx tak, xxx xxxx možná xxxxxxxxxxxx xxxxxxxxxxxx zvířat. Xxxx xxxxxxxx stanoví
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10) Xxxx xxxxxxxxx xxxxxxxxx xxxx zvířata xxxxxxx xxxxxxxxx do skupin. Xxx řešení xxxxxxxxxxx xxxxxx xx xxxx xxxxxx xxxxx xxxxxxx, xxxxxxx xx xxxxxxxxxxxxxxx xxxxxx.
1.3.1 Xxxxxxxxxxxxxx xxxxxxxx
1.3.1.1 Xxxxxxx xxxxxxx
Xxxxxxxxxxxxxxx studie xx provádějí xx xxxxxx či xxxx xxxxxxxx xxxxxxxxxxx xxxxxxx, xxxxxxxxx nebo xxxxxxxxxxx xxx xxxxx v xxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx se xxxxxxxxxx xxxxxx. Xxxxxxxx xxxx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx, xxxxxx by xxx xxxxxxxxxxx hmotnosti xxxxx než ± 20 % xxxxxxxx xxxxxxx.
1.3.1.2 Xxxxx x xxxxxxx
Xxx studiu xxxxxxxx x xxxxxxxxxx xx xxxxx xxxxxxx 4 xxxxxx xxx xxxxxx xxxxxxxxxxx dávku. Xxx xxxxxxxxx xxxx dávána xxxxxxxx určitému pohlaví, xxx xx xxxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxx provádět xxxxxx xx xxxx pohlavích. Xxxxxxxx jsou xxxxxxxx xxxxxxxx xxxxxxxx x xxxxxxx pohlaví, potom xx xxxxx testovat 4 xxxxxxx xxxxxxx xxxxxxx. V xxxxxxx xxxxxxxxx druhů zvířat (xxxxxx xxx xxxxxxxx) xx xxxxx xxxxxx xxxxx xxxxx xxxxxx.
Xx-xx xxxxxxxxx xxxxxxx xxxxxxxxxx, xxx xx xxx xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxx xxxxx xxxx v xxxxx xxx xxxxx zvířat, xxxxx xxxxx utracena x každém xxxxxxx xxxx, xxx počet xxxxxxxx xxxx, x xxxxx xxxx xxxxxxxxx xxxxxxxxx.
Xx-xx studován xxxxxxxxxxxx, xxx xx xxxxxxxx xxxxxxx xxxxxx úměrná xxxxxxxx studie.
Zahrnuje-li studie xxxxx xxxxx dávek x xxxxxxxxxxx xxxxxxxx xxxxxxxxx, pak xx xxxxxxx, aby xxxx xx skupině xxxxx xxxxxx, xxx v xxxxxx xxxxxxx intervalu xxx xxxxxxxxxx utrácení xxxxxx xxxx xx xxxxxxx xxxxxxxxx 2 xxxxxxx. Xxxxxxxx skupiny xxxx xxx xxxxxxxxxx, xxx xxx látku xxxxxxxxxx xxxx metabolity xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xx fázi retence, xxxxxxxxxxxx xxxxx x xxxxxxx.
1.3.1.3 Xxxxx
X případě xxxxxxxxxxxxx xxxxxx xx xxxxxxx nejméně 2 xxxxx xxxxx testované xxxxx, x xx xxxxx xxxxx, xx xxxxx xxxx xxxxx xxxxxxx xxxxxx x xxxxxx xxxxx, xx xxxxx mohou být xxxxxxxx xxxxx x xxxxxxxxxxxxxxxxx xxxxxxxxxxx nebo xxxxx xxxxxxxx xxxxxxx xxxxxx.
X xxxxxxx xxxxxxxxxxx xxxxxxxx xx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxxx xxxxx xxxxx. Xx xxxxxxxx podmínek xxxx xxx xxxxxxxx i xxxxxxxx xxxxxx dávky.
1.3.1.4 Xxxxxx xxxxxxxx
Xxxxxxxxxxxxxxx studie xx xxxxxxx xxxxxxx xxxxxxxx aplikace a, xx-xx xx xxxxxx, x se xxxxxxx xxxxxxxxx xxx, jak xxxx používány x xxxxxxxxx toxikologických studiích. Xxxxxxxxx xxxxx je xxx' xxxxxxxx xxxxxx xxxxxx xxxx x xxxxxxx, xxxx se xxxxxxxx xx kůži, xxxx inhalačně xxxx xx xxxxxxx xxxx xxxxxxx xxxxxxxxxxxxxxxx xxxxxx. Xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxx xxxx xxx xxxxxxxx xxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx při xxxxxx xxxxxxxxx xxxxxxxx. Xxxxx, xxxxxx xx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxx xxx získány xxxxxxxx xxxxxxxxx x xxxxxxxxxx látky v xxxxxxxxx.
Xxxx xx nutno xxxxxxxxx xx xxxxxx xxxxxxxxxxxx xxxxxxxx x xxxxxxxxxx xxxxxx. Pozornost xx potřeba věnovat x xxxxxxxx xx xxxxxxxxxxx v xxxxxxx, xx-xx testovaná xxxxx xxxxxx xxxxxx xxxx x xxxxxxx, a xxxxxxxx xxxxxxxxx xxxxx, xxxxxxx xx-xx xxxxxxxxx xxxxx xxxxxxxx v xxxxxxx.
1.3.1.5 Xxxx xxxxxxxxx
Xxxxxxx xxxxxxx se xxxxxxx xxxxx x xxxxxxxxxxxxx xx xxxxxxxx xxxxxxxx x další xxxxxxxx xxxxxxxx údaje spolu x xxxxx o xxxxxx xxxxxxx, xxxxxxxxx x trvání.
1.3.1.6 Xxxxx xxxxxxx
Xx xxxxxxx xxxxxxxxx xxxxxx xx testovaná xxxxx podána způsobem xxxxxxxxxx účelu. Xx xxxxxxxxxxxx xxxxxxxxx je xxxxx xxxxxx xxxxxxx xxxx podáním xxxxxxxxx xxxxx xxxxxxxxxx.
1.3.1.7 Xxxxxxxx
Xx xxxxxxxxx rychlosti x xxxxxxx xxxxxxxx xxxxxxxx xxxxx xxxxx xxx xxxxxxx různé metody x xxxx bez xxxxxxxxxx xxxxxxx (xxxxxxxxxx xxxxxxxx xx xxxxxx xx skupina, ve xxxxx je testovaná xxxxx xxxxxxxx xxxxxxx xxxxxxxx, který xxxxxxxxx xxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx), x to xxxx.:
- stanovení xxxxxxxx xxxxxxxxx xxxxx a xx. xxxxxx metabolitů x exkretech, xxxx. x xxxx, xxxxx, xxxxxxx, xxxxxxxxxxxx vzduchu x také xxxxxx xxxxxx x karkasu,
- xxxxxxxxx xxxxxxxxxx xxxxxxxx (xxxx. xxxxxx xxxxxx xxxxxxxx) xxxx xxxxxxxxxx x xxxxxxxxx x xxxxxxxx xxxxxxxxxx skupinou,
- xxxxxxxxx xxxxxxxx látky xxxx. jejích xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxxx a xxxxxxxxx x xxxxxxxx referenční xxxxxxxx,
- xxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxx x xx. xxxxxx xxxxxxxxxx v xxxxxx xx xxxx a xxxxxxxxx x xxxx xxxxxxxxx x referenční xxxxxxx.
1.3.2 Distribuce
V současné xxxx xxxx xxxxxxxx 2 xxxxxxxx, x xxxxx xxx xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxx xxx xxxxxxx xxxxx xx xxx:
- při xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxx získat xxxxxxxx xxxxxxxxxxxx informace;
- xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx stanovení xxxxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxx a xxxxxx xxxxxxxxxx xxxxxxxxxx x xxxxxxx x xxxxxxxx, xxxxxxxxx xx xxxxxx x xxxxxxx xxxxxxxx intervalech po xxxxxxxx xxxxxxxx.
1.3.3 Vylučování
Při xxxxxx xxxxxxxxxx se xxxxx moč, xxxxxxx, xxxxxxxxxxx xxxxxx a x určitých xxxxxxxxx xxxx. Xxxxxxxx xxxxxxxxx xxxxx a xxxxxx xxxxxxxxxx xxxxxxxxxx xx x xxxxxx exkretech xxxxxxxxx několikrát po xxxxxx xxxxx, x xx buď xx xxxxxxxxx 95 % x podaného xxxxxxxx xxxx xxxxxxx 7 xxx xx počátku xxxxxxxxxx.
Xx xxxxxxxxxxx xxxxxxxxx xx xxxxxxx vylučování xxxxxxxxx xxxxx x xxxxx x xxxx xxxxxxx xxxxxxxxxxx xxxxxx.
1.3.4 Xxxxxxxxxxxx
X xxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxxx xxxxx xx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxx. Xxxx xx xxx objasněna xxxxxxxxx xxxxxxxxxx a xxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxx, xxx je xxxxx xxxxxxxxx xx xxxxxx x předcházejících xxxxxxxxxxxxxxx xxxxxx. Xxx xxxxxxx informací x xxxxxxxxxxx může být xxxxxxxxx xxxxxxxxx xx xxxxx studií.
Další xxxxxxxxx x vztahu xxxx xxxxxxxxxxxx a xxxxxxxxx xxxxx lze xxxxxx x biochemických xxxxxx xxxx. xxxxxxx xxxxxx xxxxx xx xxxxxx xxxxxxxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx - XX xxxxxxx x xxxx xxxxx xxxxx xx xxxxxxxxxxxxx.
2 XXXXX
Xxxxxxx xxxxx xx podle xxxx xxxxxxxxx studie xxxxxxxxxx x xxxxxxxxx, xxxxx xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx.
Xxx každou xxxxxxxxxx xxxxxxx xx xxxxxx xxxxxxx a xxxxxxxxxxxxxxx variability ve xxxxxx x xxxx, xxxxx, xxxxx a xxxxxxx (xxxxx xx xx xxxxxxxx). Xxxx xxxxxxxxx x xxxxxxxx x rychlost xxxxxxxxxx xx xxxxxxx xxxxxxxx xxxxxxxx. X xxxxxxx xxxxxxxxxxxxx studií xx xxxx xxx identifikována xxxxxxxxx xxxxxxxxxx a xxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxx látky.
3 PROJEKT XXXXXX, PROTOKOL POKUSU X XXXXXXXXX XXXXXX
X xxxxxxx s příslušnými xxxxxxxx předpisy
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx a x xxxxxxx pokusu je xxxxx vést xxxxxxxx.
Xxxxx xxxx xxxxxxxxx xxxxxx xxxxxxxx xxxxxx x xxxxx následující xxxxx:
- xxxxxxxxx druh, kmen, xxxxx, životní podmínky, xxxxxx,
- xxxxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx, xxxxxxxx byl xxxxxx,
- xxxxxxxx xxxxx x xxxxxxxxx xxxxxx,
- xxxxxx(x) podání x xxxxxxx použitá xxxxxxxx,
- xxxxxxx a x xxxxxxx pozorované xxxxxx,
- xxxxxx xxxxxxxxx xxxxxxxxx xxxxx x xx. xxxxxx xxxxxxxxxx x xxxxxxxxxxx materiálu včetně xxxxxxxxxxxxx xxxxxxx,
- tabulky xxxxxxxx xxxxxxxxx xxxxx xxxxxxx, xxxxx, režimu, xxxx, xxxxx a xxxxxx,
- xxxxxxx xxxxxxx xxxxxxxxxxx a xxxxxxxxxx x xxxxxxxxxx na xxxx,
- xxxxxx xxxxx xxx xxxxxxxxxxxxxx x xxxxxxxxxxxx metabolitů x xxxxxxxxxxx xxxxxxxxx,
- metody xxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xx xxxxxxxxxxx,
- xxxxxxxxxx schéma xxx metabolismus.
Diskuse xxxxxxxx.
Xxxxxx.
X.37 XXXXXX NEUROTOXICITA XXXXXXXXXXX XXXXXXXXX XXXXXXX - XXXXXX XXXXXXXX
1 XXXXXX xx v xxxxxxx x právem Evropských xxxxxxxxxxxx.
4)1.1 Úvod
Při stanovení x vyhodnocení xxxxxxxxx xxxxxx látek xx xxxxxxxx xxxx x xxxxx schopnost xxxxxx xxxxxxx xxxxx xxxxxxx xxxxxxxxxx xxx neurotoxicity, xxxxx xxxxxx být xxxxxxx x xxxxxx xxxxxxxx xxxxxxxx. X xxxxxxxx organických xxxxxxxxx xxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxxx x xxxx xxx xxxxxxxxx touto xxxxxxx.
Xxxxxxxxxxx xxxxx xx xxxxx xxxxx xxx xxxxxxx xxx xxxxxxxxxxx látek, xxxxx mohou vyvolat xxxxxx xxxxxxxxxxxxxx. Xxxxxxxxx xxxxx x in xxxxx studií však xxxx xxxxx xxxxxxxxx xx xxxxx, že xxxxx xxxx schopnost xxxxxxx xxxxxx neurotoxicitu.
1.2 Xxxxxxxx
Xx xxxxxxx xxxxx xxxxxxxxxx x názvu xxxx xxxxxx jako "xxxxxxxxx xxxxxxxxxx xxxxxxx" xxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx, xxxxxxxxxx xxxx xxxxxxxxx kyseliny xxxxxxxxxx, fosfonové xxxx xxxxxxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxx xxxxxxxxxxxxxxxx, xxxxxxxxxxxxxxx xxxx xxxxxxxxxxxxxxxxxxxxx, nebo xxxx látky, xxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx, xxxxxxxxxxx x xxxxxxxxx xxxxx xxxx xxxxxxx.
Xxxxxx xxxxxxxxxxxxx xx xxxxxxx xxxxxxxxxxx xx xxxxxx, xxxxxxxx xxxxxxxxxx, xxxxxxx x míše x periferním nervu x pozdním xxxxxxxx xxxxxx příznaků, a xxxx xxxxxxxx a xxxxxxxxx specifické xxxxxxxx - XXX (neuropathy xxxxxx xxxxxxxx) x xxxxxxx xxxxx.
1.3 Referenční xxxxx
Xxxxxxxxxx látka xxxx xxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxx, xx x laboratorních xxxxxxxxxx xx reakce xxxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx.
Xxxxxxxxx xxxxxx používané referenční xxxxx s xxxxxxx xxxxxxxxxxxxx xxxxxxx je xxx-x-xxxxxxxxxxx (CAS 78-30-8, XXXXXX 201-103-5, chemický xxxxx: xxxx(2-xxxxxxxxxx) xxxxx xxxxxxxx fosforečné, syn: xxx-x-xxxxxxxxxxxx (XXXX).
1.4 Xxxxxxx xxxxxxxxx xxxxxx
Xxxxxxxxx xxxxx xx podává xxxxxx x xxxxxx xxxxx xxxxxxxx, xxxxxxxxx před xxxxxxx akutními xxxxxxxxxxxxx xxxxxx. Xxxxxxx xx xxxxxxxx xx dobu 21 dnů, xxxxxxxxxxx xx xxxxxx xxxxxxxxxx xxxxxxx, xxxxxx a xxxxxx. Biochemické xxxxxxxxx, xxxxxxx inhibice NTE, xx xxxxxxx x xxxxxx xxxxxxx xxxxxxxxx x xxxxx xxxxxxx, xxxxxxx 24 a 48 hodin xx xxxxxx xxxxx. 21 xxx po xxxxxx xxxxx xxxx zbývající xxxxxxx xxxxxxxx a xx xxxxxxxxx histopatologické xxxxxxxxx xxxxxxxxx nervových xxxxx.
1.5 Xxxxx xxxxxx xxxxxxxxx
1.5.1 Xxxxxxxx
Xxxxx xxxxxx xxxxxxx slepice xxx xxxxxxxxxxxxxxx virových xxxxxxxxxx x xxxxxxxxxxxxxx xxxxx x x xxxxxxxx xxxxx se xxxxxxx xxxxxxx do experimentální x xxxxxxxxx xxxxxxx. Xxxxxxx xxxxxxx jsou xxxxxxx s xxxxxxx xx druh, xxxxxxx x xxxxx x xxxxxxx x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x označena xxx, aby byla xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Dobu xxxxxxxx xxxxxxx
§10 zvláštního xxxxxxxx předpisu.
10) Xxxxxxxxx xx xxxxxxxxxx xxxxx xxxxx xxxx ohrady xxxxxxxxxx xxxxx xxxxx xxxxxx x xxxxxx xxxxxxxxxx xxxxx.
Xxxxxxxxx látka xx xxxxxx xxxxxx xxxxxx, xxxxxxxxxxxx xxxxxxxxx xxxx xxxxx srovnatelnou xxxxxxx. Xxxxxxxx se xxxxxxxx xxxxxxxx nebo xxxxxxxxxx xx xxxxxxx xxxxxxxx, jako xx xxxxxxxxx kukuřičný olej. Xxxxx xxxxx xx xxxxxx rozpustit, xxxxx xxxxx xxxxx xxxxxxx xxxxx v xxxxxxxxxxxx xxxxxxxxx by xx xxxxxxxx xxxxxxxxxx xxxxxxxx. X xxxxxxxxx xxxxxx xxxx xxx xxxxx xxxx určeny xxxx xxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxxxx.
1.5.2 Experimentální xxxxxxxx
1.5.2.1 Xxxxxxx zvířata
Doporučují xx xxxxx nosnice kura xxxxxxxx (Xxxxxx gallus xxxxxxxxxx) ve xxxx 8 xx 12 xxxxxx. Xxxxxxxxx xx xxxxxxx o xxxxxxxxxx xxxxxxxxx a xxxxxxx xx xx xxxxxxxx, xxxxx dovolují xxxxx xxxxx.
1.5.2.2 Počet x xxxxxxx
Xxxxx xxxxxxxxx skupiny xx xxxxxxx jak xxxxxxxxx xxxxxxx x xxxxxxxxx, tak pozitivní xxxxxxxxx skupina. X xxxxxxxx xxxxxxxx xxxxxxxxx xxxxx se xx xxxxxxx x xxxxxxxxx xxxxxxx xxxxxxx xxxxxx xxxx s xxxxxxxxx.
X xxxxx xxxxxxx xx xxx xxxxxxxxxx xxxxx xxxxxx, aby alespoň 6 x nich xxxxx xxx xxxxxxxx xxx xxxxxxxxxxx vyšetření (3 xxxxx x 3 druhý den xx xxxxxx) x xxx 6 x xxxx xxxxxxx xxxxxxxxxx xxxxxxxx 21 xxx.
Xxxxxxxxx xxxxxxxxx skupina xx xxxx testovat xxxxxxxx xxxx xx může xxxxxx xxxxxxxxx xxxxxxx x nedávné xxxxxxxx. Xx xxx alespoň 6 xxxxxx, kterým xx xxxxxx xxxxx xxxxxxxxxxxx pozdní neurotoxicitu, 3 xxxxxxx xxxx xxxxxx xxx biochemii x 3 slepice xxx histologii. Xxxxxxxxxx xx periodicky doplňovat xxxxxxxxxx údaje, xxxx xx x provádějící xxxxxxxxxx změní xxxxxxx xx xxxxxxxxxx xxxxx xxxxx (xxxx. xxxxxxx, xxxxxxx, xxxxxxxx xxxxx).
1.5.2.3 Xxxxx xxxxx
Xx být xxxxxxxxx xxxxxxxxx studie x využitím xxxxxxxxxxx xxxxx xxxxxx x xxxxxx x xxxxxxx xxxxxxxx xxxxx, aby xx xxxx stanovit xxxxxx, xxxxx xxxx xxxxxxx x hlavní xxxxxx. Určitá úmrtnost xx x xxxx xxxxxxxxx xxxxxx nezbytná xxx xxxxxxxxx přiměřené xxxxx v xxxxxx xxxxxx. Xxx xx xxxxxxxxx xxxxx xxx xxxxxx xxxxxxxxxxx xxxxxx, xxxxxxx xx xxxxxxx xxxx jiný xxxxxxxx xxxxxxxxx, o kterém xx xxxxx, xx xxxxxxxxxxxxx x xxxxxxxx xxxxxxxxxxxxxx xxxxxx. X xxxxxx xxxxxxxxx neletální xxxxx testovaných xxxxx xxxx být použito xxxxxxx xxxx xxxxxxxxxxx xxxxx (viz xxxxxx X.1 xxx). Xxxxxxxxxx xxxxx pro xxxxxxx xxxx xxxx toxikologické xxxxxxxxx xxxxx být xxxx nápomocné xxx xxxxxx xxxxx.
Xxxxxx xxxxx xxxxxxxxx xxxxx x xxxxxx studii by xxxx xxx xx xxxxxxxx x xxxxxxxxxxxx x xxxxxxxxx předběžné xxxxxx xxxxxx dávky x hornímu xxxxxx xxxxx 2000 xx.xx-1 xxxxxxx hmotnosti. Případné xxxxx xx xxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxx xxxxx xxxxxx, xx xx šesti xxx xxxxxxxxx x xx 21 dnech xxxxx xxx xxxxxxxxxx. Xxxxxxx xxxx jiný ochranný xxxxxxxxx, x xxxxxx xx známo, xx xxxxxxxxxxxxx x xxxxxxxx xxxxxxxxxxxxxx xxxxxx, xx xx xxxxxx jako xxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxx xxxxxx.
Xxxxxxxx xxxx x dávkou nejméně 2000 xx.xx-1 xxxxxxx xxxxxxxxx, xx použití xxxxxxx xxxxxxxxx xxx xxxx studii, nevyvolá xxxxx xxxxxxxxxx xxxxxxx xxxxxx a xxxxxxxx xxxxx údajů x xxxxx x příbuznou xxxxxxxxxx není xxxxx xxxxxxxx xxxxxxxx, pak xxxx třeba xxxxxxxx x xxxxxx x xxxxxxx xxxxx xxxxx. Xxxxxxx xxxx xx xxxxxxxxx, xxxxx xxxxxxxx, xxxxxxxxxxx xx x xxxx, xxxxxxxxx xxxxxxx xxxxxxx ještě xxxxx xxxxxx xxxxx.
Xxxx xxxxxxxxxx xx 21 xxx.
1.5.3 Xxxxx xxxxxxx
Xx xxxxxxxx xxxxxxxxxx, ochraňujícího xxxx xxxxxx xx následky xxxxxxxx xxxxxxxxxxxxx xxxxxx, xx testovaná xxxxx xxxxxx v xxxxxx xxxxx.
1.5.3.1 Xxxxxxxxx xxxxxxxxxx
Xxxxxxxxxx xx xxxxx okamžitě xx xxxxxx xxxxx. Xxxxxxx xxxxxxx se xxxxxxx xxxxxxxx několikrát x xxxxxxx xxxxxxx 2 dnů a xxx xxxxx jednou xxxxx xx xxxx 21 xxx xxxx xxxxx xxxxxxx utraceny xxxxx xxxxx. Veškeré xxxxxxxx xxxxxxxx xx xxxxxxxxxxxxx, xxxxxx xxxxxxx, xxxx, xxxxxx x xxxxxx xxxxxxxxxxxx xxxxxxx. Xxxxxx se xxxxxxx xxxxx nejméně čtyřstupňové xxxxxxxx x zaznamenává xx paréza. Xxxxxxx xxxxxxx xxxxx se xxxxxxx xxxxxxxxxx patologické xxxxx xxxxxx x xxxxx x vystaví xxxxxx motorické aktivitě xxxx xxxx. xxxxxxxxxxx xx xxxxxxx, xxx xx xxxxxxxxx posouzení xxxxxxxxxxx xxxxxxxxx xxxxxx. Xxxxxxxxx xxxxxxx x xxxxxxx xx závažnými x xxxxxxxxxxxxxxx xxxxxxxx xxxxxxx x xxxxxxx xx xxxxx xxxxxxx, xxxxxxxx způsobem xxxxxxx x pitvat.
1.5.3.2 Xxxxxxx xxxxxxxx
Xxxxxxx xxxxxxx xx xxxxx xxxxx xxxx xxxxxxx xxxxxxxxx látky x pak xxxxx xxxxxx xxxxx.
1.5.3.3 Xxxxxxxxx
6 xxxxxx xxxxxxx xxxxxxxxx x xxxxx xxxxxxxxx x xxxxxxxxx xxxxxxx x vehikulem x 3 xxxxxxx x xxxxxxxxx xxxxxxxxx xxxxxxx (xx-xx xxxxxxx použita) xx usmrtí x xxxxxxx dnech xx xxxxxxxx xxxxx. Pro xxxxxxx xxxxxxxx NTE xx xxxxxx xxxxx x lumbální mícha. Xx vhodné xxxxxxxxxxxx xxxx xxxxxx ischiadicus x xxxxxxxxxx jeho xxxx xx inhibici XXX. Xxxxx se xxxxxxxx 3 slepice x xxxxxxxxx a xxxxx xxxxxxxxx skupiny xx 24 xxxxxxxx x xxxxx tři xx 48 hodinách, 3 slepice x xxxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxxx xxxxx xx 24 xxxxxxxx. Xxxxxxxx pozorování klinických xxxxxxxx naznačuje, xx xxxxxxx látka se x organismu pohybuje xxxxx xxxxxx (xxxxxxx xx xxxxxx xxxxxxxxxxxxx xxxxxxxx), pak xx xxxxxxxxxx xxxxxxx xxxxxx xxxxx xxxxxxx xx 3 zvířat, x xx xxxx 24 xx 72 hodinami xx xxxxxx xxxxx.
X xxxxxx xxxxxx xxxxx xx xxxxxxxx provede xxxx analýza xxxxxxxxxxxxxxxxxxxx (XXxX). Xx xxxx xxxx však xxxxxx xxxxxxxxx reaktivace XXxX, xxx xxxx vést x xxxxxxxxx Xxxxx xxxx xxxxxxxxxx XXxX.
1.5.3.4 Xxxxx
Xxxxx xxxxx xxxxxx (xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx pro špatný xxxxxxx xxxx) zahrnuje xxxxxxxxxxxxx posouzení xxxxx xxxxx a míchy.
1.5.3.5 Xxxxxxxxxxxxxxxx vyšetření
Nervová tkáň x xxxxxxxxxx zvířat (xxxxxxxxxxx pro xxxxxxxxxxx xxxxxx) xx xxxxxxxxxxxx xxxxxxx. Xxxxx se xxxxxx in xxxx xx xxxxxxx xxxxxxxxxx xxxxxxx. Xxxxxxx xx: xxxxxxx (xxxxxxx xxxxxxx xxx), prodloužená xxxxx, xxxxx - xxxx xxxxx xx xxxxxxxxx x xxxxx xxxxx xxxxx, střední xxxxxx x xxxxxxxxxxxxx, z xxxxxxxxxxx xxxxx xx xxxxxxx xxxxxxxx část x x. tibialis (x xxxx xxxxx x m.gastrocnemius) a x x. ischiadicus. Xxxx xx xxxxx xxxxxxxxxxxx barvivy xx xxxxxx x xxxxx.
2 XXXX X XXXXXX XXXXX
Xxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxxx touto xxxxxxx (biochemie, histopatologie x xxxxx xxxxxxx) xxxxx xxxxxxxxxx xxxxx xxxxxxxxx xx xxxxxx xxxxxxxxxxxxx. Neprůkazné xxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxxx další sledování.
Uvádějí xx údaje pro xxxxxxxxxx xxxxxxx. Xxxxx xx dále xxxxxxx xx xxxxxxx. X xx xxxx xxx xxx xxxxxx experimentální xxxxxxx xxxxxx xxxxx xxxxxx na xxxxxxx xxxxxx x xxxxx xxxxxx xxxxxxxx poškození, xxxxx xxxxxxx nebo xxxxxxxxxxx xxxxxx, typy x xxxxxx xxxxxx xxxxxxxxx xxxx xxxxxx x xxxxxxxx zvířat xxxxxxxxxxxx xxxxx xxx x xxxxxx poškození xxxx účinku.
Výsledky xxxxxx xx vyhodnotí x xxxxxxxx výskytu, závažnosti x korelace xxxx xxxxxxx chování, xxxxxxxxxxxxx x xxxxxxxxxxxxxxxxxx xxxxxx x xxxxxxx pozorovanými xxxx x xxxxxxxxxxx x xxxxxxxxxxx xxxxxx.
Xxxxxxx xxxxxxxx je třeba xxxxxxxxxx xxxxxxx a xxxxxx xxxxxxxxx statistickou xxxxxxx. Xxxxxxxxxxx metody xx xxxxx xxx x době xxxxxxxxx xxxxxx.
3 XXXXXXX XXXXXX, XXXXXXXX POKUSU X XXXXXXXXX XXXXXX
X souladu x xxxxxxxxxxx právními xxxxxxxx
9) musí být xxxxxxxxx xxxxxxx xxxxxx x o průběhu xxxxxx xx xxxxx xxxx xxxxxxxx.
Xxxxxxxxx xxxxxxx:
- xxxxxxx xxxxxxx;
- xxxxx x xxxxx zvířat;
- xxxxx, xxxxxxxx xxxxxxxx xxx.;
- hmotnosti xxxxxxxxxxxx xxxxxx xx xxxxxxx xxxxxx.
Xxxxxxxx testování:
- podrobné xxxxx o přípravě, xxxxxxxxx x homogenitě xxxxxxxxx látky;
- xxxxxxxxxx xxxxxx xxxxxxxx;
- xxxxxxxx xxxxx o způsobu xxxxxxxx xxxxxxxxx látky;
- xxxxxxxx xxxxx x xxxxxxx a xxxxxxx xxxx;
- zdůvodnění xxxxxxx xxxxxx dávek;
- xxxxxxxxxxx xxxxxxxxxx xxxxx, včetně xxxxxxxxxx xxxxx x xxxxxxxx, xxxxxx x xxxxxxxxx xxxxx xxxxxxxxxx xxxxx;
- podrobné xxxxx x podání xxxxxxxxxx xxxxxxxxx.
Xxxxxxxx:
- xxxxx o xxxxxxx hmotnosti;
- údaje x xxxxxxxxx xxxxxxxxxx xxxxx dávkových xxxxxx, xxxxxx xxxxxxxxx;
- charakter, xxxxxx x xxxxxx xxxxxxxxxx xxxxxxxx (ať xxxxxxxx xxxx xxxxxxxxxx);
- xxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx a jejich xxxxxxxx;
- pitevní xxxxxx;
- xxxxxxxx xxxxx xxxxx xxxxxxxxxxxxxxxxxx xxxxxx;
- xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx, x xxxxxxx xx xx xxxxx.
Xxxxxxx.
Xxxxxx.
X.38 POZDNÍ NEUROTOXICITA XXXXXXXXXXX XXXXXXXXX FOSFORU
28DENNÍ XXXXXXXXX XXXXXXXX
1 METODA xx x xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
4)1.1 Xxxx
Xxx xxxxxxxxx x xxxxxxxxxxx xxxxxxxxx xxxxxx xxxxx xx xxxxxxxx xxxx x xxxxx xxxxxxxxx xxxxxx xxxxxxx xxxxx vyvolat xxxxxxxxxx xxx xxxxxxxxxxxxx, xxxxx xxxxxx být xxxxxxx x xxxxxx xxxxxxxx toxicity. X xxxxxxxx xxxxxxxxxxx sloučenin xxxxxxx byly xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxxxxxx x mají být xxxxxxxxx xxxxx xxxxxxx.
Xxxxxxxxxxx xxxxx in vitro xxxxx xxx použity xxx xxxxxxxxxxx xxxxx, xxxxx xxxxx vyvolat xxxxxx xxxxxxxxxxxxxx. Xxxxxxxxx xxxxx z in xxxxx xxxxxx xxxx xxxx možno xxxxxxxxx xx xxxxx, že xxxxx xxxx xxxxxxxxx xxxxxxx pozdní neurotoxicitu.
Tento 28xxxxx test pozdní xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxx x možném zdravotním xxxxxx xxxxxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx. Xxxxxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxxx xx xxxxx x xxxx xxxxxxxxxx xxxxx xxxxxxx xxxxxxxxx xxxxxx, xx kterém nejsou xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxx. Tato xxxxxx xx xxxxxxx xxx xxxxxxxxx xxxxxxxx bezpečné xxxxxxxx.
1.2 Xxxxxxxx
Xx skupiny xxxxx označených x xxxxx xxxx xxxxxx xxxx "organické xxxxxxxxxx xxxxxxx" patří xxxxxxxxxx xxxxxxxxx organické xxxxxx, xxxxxxxxxx nebo anhydridy xxxxxxxx fosforečné, xxxxxxxxx xxxx amidofosforečné xxxx xxxxxxxxxxx kyselin xxxxxxxxxxxxxxxx, xxxxxxxxxxxxxxx xxxx amidothiofosforečných, xxxx xxxx látky, xxxxx xxxxx xxxxxxxx xxxxxx xxxxxxxxxxxxx, pozorovanou x xxxxxxxxx xxxxx xxxx xxxxxxx.
Xxxxxx xxxxxxxxxxxxx xx xxxxxxx xxxxxxxxxxx xx ataxií, distální xxxxxxxxxx, xxxxxxx v xxxx a periferním xxxxx x xxxxxxx xxxxxxxx těchto xxxxxxxx x xxxx xxxxxxxx x xxxxxxxxx specifické xxxxxxxx - NTE (xxxxxxxxxx xxxxxx xxxxxxxx) x xxxxxxx xxxxx.
1.3 Xxxxxxx xxxxxxxxx xxxxxx
Xxxxxxxxx xxxxx se xxxxxx xxxxx xxxxxx xxxxxxxx xx dobu 28 xxx. Xxxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxx xxxxx, zaznamenává xx xxxxxxxxxx chování, ataxie x xxxxxx xxxxx 14 xxx xx xxxxxxxx xxxxx. Biochemické xxxxxxxxx, xxxxxxx xxxxxxxx XXX, xx xxxxxxx x xxxxxx xxxxxxx xxxxxxxxx x každé xxxxxxx 24 x 48 xxxxx xx xxxxxxxxx xxxxxx látky. 2 týdny xx xxxxxxxx xxxxx xxxx xxxxxxxxx slepice utraceny x je xxxxxxxxx xxxxxxxxxxxxxxxx vyšetření xxxxxxxxx xxxxxxxxx xxxxx.
1.4 Xxxxx xxxxxxxxx metody
1.4.1 Xxxxxxxx
Xxxxxxx xxxxxxx jsou vybrána x ohledem xx xxxx, xxxxxxx, x xxxxx x xxxxxxx x ustanovením
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x xxxxxxxx xxx, xxx xxxx xxxxx xxxxxxxxxxxx jednotlivých xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10)Xxxxx xxxxxx xxxxxxx xxxxxxx xxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx a xxxxxxxxxxxxxx xxxxx a x xxxxxxxx xxxxx xx xxxxxxx přiřadí xx experimentální x xxxxxxxxx xxxxxxx. Nejméně 5 dní xxxx xxxxxxxxx xxxxxx xxxx xxxxxxx xxxxxxx v xxxxxxxxxx xxxxx x xxxxxx, v jakých xxxxx během experimentu.
Používají xx xxxxxxxxxx velké xxxxx nebo xxxxxx xxxxxxxxxx xxxxx pohyb xxxxxx x xxxxxx xxxxxxxxxx xxxxx.
Xxxxxxxxx xxxxx xx xxxxxx xxxxxx, xxxxx 7 xxx x xxxxx, xxx' xxxxxx, želatinovými xxxxxxxxx xxxx xxxxx srovnatelnou xxxxxxx. Tekutiny se xxxxxxxx xxxxxxxx xxxx xxxxxxxxxx ve vhodném xxxxxxxx, jako xx xxxxxxxxx xxxxxxxxx xxxx. Xxxxx xxxxx xx xxxxxx xxxxxxxxx, xxxxx xxxxx xxxxx xxxxxxx xxxxx x xxxxxxxxxxxx xxxxxxxxx xx xx xxxxxxxx dostatečně xxxxxxxx. X xxxxxxxxx nosičů xxxx xxx xxxxx xxxx určeny xxxx xxxxxx jejich xxxxxxxxxxxxx xxxxxxxxxx.
1.4.2 Xxxxxxxxxxxxxx podmínky
1.4.2.1 Xxxxxxx zvířata
Doporučují xx xxxxx xxxxxxx kura xxxxxxxx (Xxxxxx xxxxxx xxxxxxxxxx) ve xxxx 8 až 12 xxxxxx. Používají xx xxxxxxx x xxxxxxxxxx xxxxxxxxx x xxxxxxx xx xx xxxxxxxx, xxxxx dovolují xxxxx xxxxx.
1.4.2.2 Xxxxx x xxxxxxx
Xx xxxxx použít xxxxxxx 3 xxxxxx xxxxx x 1 xxxxxxxxx skupinu x xxxxxxxxx. S výjimkou xxxxxxxx testované xxxxx xx se zvířaty x xxxxxxxxx xxxxxxx xxxxxxx xxxxxx jako x xxxxxxxxx.
X xxxxx xxxxxxx xx xxx xxxxxxxxxx počet xxxxxx, xxx xxxxxxx 6 x xxxx xxxxx xxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx (3 x xxxxxx ze 2 časových xxxx) x xxx 6 x nich přežilo xxxxxxxxxxxxx xxxxxxxxxx xx xxxxxxxx xxxxxxxx.
1.4.2.3 Xxxxx xxxxx
Xxxxxxx xxxxxx xx xxxxx x přihlédnutím xx 3 výsledkům x akutního xxxxx xx pozdní xxxxxxxxxxxxx x x xxxxxx xxxxxx x toxicitě xxxx kinetice xxxxxxxxx xxxxx. Xxxxxxxx úroveň xxxxx xx vyvolat xxxxxxx účinky, xxxxxxx xxxxxxxx xxxxxx neurotoxicity, xxxxxxxxxx žádné xxxxxxx xxx zřejmé utrpení. Xxxx xx zvolí xxxx xxxxxxxxxxx xxxxx xxxxxxxx, který xxxxxx xxxxxxxx xxxxxxxxx xxxxxx xx xxxxx. Xxxxxxxx xxxxx xx xxxxxx xxxxxxx xxxxx xxxxxxxx xxxxxxxx.
1.4.2.4 Xxxxxxx test
Jestliže xxxx x xxxxxx xxxxxxx 1000 xx.xx-1 xxxxxxx xxxxxxxxx x xxx, za xxxxxxx xxxxxxx popsaných xxx xxxx xxxxxx, nevyvolá xxxxx pozorované xxxxxxx xxxxxx a jestliže xxxxx údajů u xxxxx x xxxxxxxxx xxxxxxxxxx xxxx xxxxx xxxxxxxx xxxxxxxx, xxx xxxx třeba xxxxxxxx x xxxxxx x xxxxxxx xxxxx dávky. Xxxxxxx xxxx xx xxxxxxxxx, pokud xxxxxxxx xxxxxxxxxxx se x xxxx naznačuje xxxxxxx xxxxxxx xxxxx xxxxx xxxxxx dávky.
1.4.2.5 Xxxx xxxxxxxxxx
Xxxxxxx xxxxxxx xx xxxxxxxx xxxxxxx xxxxxx xxxxx xx dobu xxxxxxxx a 14 xxx xx ní, xxxx xx utracení x do xxxxx xxxxx xxxxx.
1.4.3 Xxxxx xxxxxxx
Xxxxxxxxx látka xx xxxxxx 7 xxx x xxxxx xx 28 xxx.
1.4.3.1 Xxxxxxxxx xxxxxxxxxx
Xxxxxxxxxx xx začít xxxxxxxx xx xxxxxx xxxxx. Všechny xxxxxxx xx xxxxxxx xxxxxxxx xxxxxxx xxxxxx xxxxx xx 28 dnů x xxxxxxx 14 xxx po xxxxxxxx xxxxxxxx, xx xxxxxxxx xxxxx xxxxx. Xxxxxxx xxxxxxxx xxxxxxxx xx xxxxxxxxxxxxx, xxxxxx xxxxxxx, xxxx, xxxxxx x xxxxxx. Pozorování xx xxxxxxxxx xxxxxxxxxxx chování, xxx xxxx xx xx xx omezovat. Xxxxxx se hodnotí xxxxx xxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxx, zaznamenává xx xxxxxx. Xxxxxxx xxxxxxx xxxxx se xxxxxxx vyjmou z xxxxx x xxxxxxx xxxxxx xxxxxxxxx aktivitě, xxxx xxxx. vystupování xx xxxxxxx, xxx xx usnadnilo xxxxxxxxx xxxxxxxxxxx toxických účinků. Xxxxxxxxx xxxxxxx xx xxxxxxxxx a xxxxxxxxxxxxxxx xxxxxxxx xxxxxx x xxxxxxx je xxxxx xxxxxxxx, xxxxxxxx xxxxxxxx xxxxxxx x pitvat.
1.4.3.2 Xxxxxxx hmotnost
Všechny slepice xx zváží xxxxx xxxx xxxxxx xxxxxxx xxxxxxxxx xxxxx a xxx alespoň xxxxxx xxxxx.
1.4.3.3 Biochemie
Šest xxxxxx xxxxxxx xxxxxxxxx x xxxxx xxxxxxxxx x xxxxxxxxx skupiny x xxxxxxxxx xx xxxxxx x xxxxxxx xxxxx xx aplikaci poslední xxxxx. Xxx xxxxxxx xxxxxxxx XXX xx xxxxxx mozek x xxxxxxxx mícha. Je xxxxxx vypreparovat xxxx xxxxxx ischiadicus x xxxxxxxxxx jeho tkáň xx xxxxxxxx XXX. Xxxxxxx se xxxxxxxx xxx slepice x xxxxxxxxx x xxxxx xxxxxxxxx skupiny po 24 xxxxxxxx a xxxxx xxx po 48 hodinách xx xxxxxxxxx xxxxxx xxxxx. Xxxxxxxx údaje x xxxxxx studie xxxx xxxxxx studií (xxxx. xxxxxxxxxxxxxxxxx) naznačují, xx xx výhodnější jiná xxxx xxxxxxxx po xxxxxxxx aplikaci, xxx xx xxxxxxxxxx xxxxxx xxxx xxxx a xxxxxxxxxx xxxxx x xxxxxxxxxxx.
X xxxxxx vzorků xxxxx xx xxxxxxxx xxxxxxx xxxx xxxxxxx xxxxxxxxxxxxxxxxxxxx (XXxX). Xx xxxx může xxxx xxxxxx spontánní xxxxxxxxxx XXxX, xxx xxxx xxxx k podcenění xxxxx jako xxxxxxxxxx XXxX.
1.4.3.4 Xxxxx
Xxxxx všech xxxxxx (xxxxxxxxx xxxxxxxxxx x xxxxxxxxxx xxx xxxxxx xxxxxxx xxxx) xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx xxxxx a xxxxx.
1.4.3.5 Xxxxxxxxxxxxxxxx xxxxxxxxx
Xxxxxxx xxxx z xxxxxxxxxx xxxxxx (nepoužitých pro xxxxxxxxxxx studie) se xxxxxxxxxxxx vyšetří. Xxxxx xx xxxxxx in xxxx za xxxxxxx xxxxxxxxxx xxxxxxx. Xxxxxxx xx: xxxxxxx (střední xxxxxxx xxx), xxxxxxxxxxx xxxxx, xxxxx (xxxx xxxxx xx xxxxxxx x xxxxx xxxxx xxxxx, xxxxxxx xxxxxx x xxxxxxxxxxxxx), x xxxxxxxxxxx nervů xx xxxxxxx distální část x xxxxxx tibialis (x jeho xxxxx x nervus gastrocnemius) x z nervus xxxxxxxxxxx. Xxxx xx xxxxx specifickými barvivy xx xxxxxx a xxxxx.
Xxxxxxx xx xxxxxxx xxxxxxxx xxxxx všech xxxxxx kontrolní skupiny x xxxxxxx s xxxxxxxx xxxxxx. Pokud xx xxxxxx u xxxxxx skupiny x xxxxxxxx xxxxxx známky xxxxxx, provede xx xxxxxxxxxxxx vyšetření x xx slepicích ze xxxxxx, které xxxxxxx xxxxx střední x xxxxxx.
2 SBĚR X XXXXXX ÚDAJŮ
Pokud jsou xxxxxxxx xxxxxxx xxxxx xxxxxxx (xxxxxxxxx, xxxxxxxxxxxxxx x xxxxx xxxxxxx) xxxxxxxxx, xxxxx xx xxxxxxxxx další testování xx xxxxxx neurotoxicitu. Xxxxxxxxxx nebo xxxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxx xxxxxxxxx.
Xxxxxxx xx xxxxx pro xxxxxxxxxx xxxxxxx. Údaje xx xxxx sestaví xx xxxxxxx. X ní xxxx xxx xxx xxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxx počet xxxxxx xx xxxxxxx xxxxxx x počet xxxxxx xxxxxxxx poškození, xxxxx xxxxxxx xxxx biochemické xxxxxx, xxxx x xxxxxx xxxxxx xxxxxxxxx xxxx účinků x xxxxxxxx zvířat vykazujících xxxxx xxx x xxxxxx xxxxxxxxx nebo xxxxxx.
Xxxxxxxx xxxxxx se xxxxxxxxx x hlediska xxxxxxx, xxxxxxxxxx x xxxxxxxx mezi xxxxxxx xxxxxxx, biochemickými x xxxxxxxxxxxxxxxxxx xxxxxx x xxxxxxx xxxxxxxxxxxx jevy x xxxxxxxxxxx a xxxxxxxxxxx xxxxxx.
Xxxxxxx výsledky xx třeba xxxxxxxxxx xxxxxxx a xxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxx. Xxxxxxxxxxx metody xx xxxxx xxx x xxxx xxxxxxxxx xxxxxx.
3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx x x průběhu xxxxxx xx xxxxx vést xxxxxxxx.
Xxxxxx x xxxxxx xxxxxxxx tyto informace, xxxxx xxxxx být xxxxxxx
Xxxxxxxxx xxxxxxx:
- xxxxxxx xxxxxxx,
- počet x xxxxx xxxxxx,
- xxxxx, xxxxxxxx ustájení xxx.,
- xxxxxxxxx xxxxxxxxxxxx zvířat xx začátku studie.
Podmínky xxxxxxxxx.
- podrobné xxxxx x xxxxxxxx, stabilitě x homogenitě xxxxxxxxx xxxxx,
- xxxxxxxxxx xxxxxx xxxxxxxx,
- xxxxxxxx xxxxx x xxxxxxx xxxxxxxx xxxxxxxxx xxxxx,
- podrobné xxxxx o xxxxxxx x xxxxxxx vody,
- xxxxxxxxxx vybrané xxxxxx xxxxx,
- xxxxxxxxxxx xxxxxxxxxx xxxxx, xxxxxx xxxxxxxxxx xxxxx x xxxxxxxx, xxxxxx x xxxxxxxxx xxxxx xxxxxxxxxx xxxxx,
- xxxxxxxxxx doby xxx xxxxx xx biochemické xxxxxxxxx, je-li jiná xxx 24 x 48 xxxxx.
Xxxxxxxx:
- xxxxx x xxxxxxx hmotnosti,
- xxxxx x toxických xxxxxxxxxx xxxxx xxxxxxxxx xxxxxx, včetně úmrtnosti,
- xxxxxx xxx xxxxxx (XXXXX),
- xxxxxxxxx, stupeň x xxxxxx klinických xxxxxxxx (xx vratných xxxx xxxxxxxxxx),
- xxxxxxxx xxxxx biochemických vyšetření x jejich xxxxxxxx,
- xxxxxxx xxxxxx,
- xxxxxxxx xxxxx všech xxxxxxxxxxxxxxxxxx xxxxxx,
- xxxxxxxxxxx vyhodnocení xxxxxxxx, x xxxxxxx xx xx xxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
X.39 XXXX XXXXXXXXXXX XXXXXXX DNA V XXXXXXX XXXXXXXXX BUŇKÁCH XX XXXX
1 XXXXXX xx x xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
5)1.1 Xxxx
Xxxxxx xxxxx xxxxxxxxxxx xxxxxxx XXX (xxxxxxxxxxx DNA synthesis, XXX) x xxxxxxx xxxxxxxxx buňkách xx xxxx je určit xxxxx, xxxxxxxxxxxx xxxxxxxx XXX x xxxxxxxxx xxxxxxx pokusných zvířat.
5)Tento xxxx xx xxxx xxxxxxxxxxx xxxxxx pro xxxxxxxxxx xxxxxxxxxxxxx xxxxxx xxxxxxxxxx xxxxx v xxxxxxx. Xxxxxxxx xxxxx xxxxxxxx poškození DNA x jaterních buňkách x xxxx následnou xxxxxxxx. Xxxxx xxxx xxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx absorbovaných xxxxxxxxx; xxxx proto xxxxxxx xxxxxxxx xxx detekci xxxxxxxxx XXX in xxxx.
Xxxxxxxx-xx doklady x xxx, že se xxxxxxxxx xxxxx xx xxxxxx xxxxx nedostane, xxxx tento xxxx xxxxxx.
Xxxxxxxx neplánované syntézy XXX (XXX) se xxxxxxx xxx, že xx xxxxxxx absorpce xxxxxxxxx xxxxxxxxxx x xxxxxxx, xxxxx neprocházejí xxxxxxxxxx (X-xxxx) syntézou XXX. Nejběžnější xx xxxxxx, xxx xxxxx xx xxxxxxxxxxxxxxxxx xxxxxxx xxxxxxxx značený xxxxxxx (3X-XxX). Pro xxxxx XXX xx xxxx xx xxxxxxxxxx xxxxxxxxx xxxxxxx játra. Xxxx xxxxx xxx xxxxx xx xxxx také xxxxx použít, nejsou xxxx předmětem této xxxxxx.
Xxxxxxx odpovědi xxxxxx xx počtu xxxx XXX, jež xxxx x xxxxx xxxxxxxxx xxxxxxxxxx x nahrazeny. Xxxxx je metoda XXX xxxxxxx xxxxxx x xxxxxxx xxxxx xxxxxxxxxxxx "xxxxxxxxx xxxxxx" (20 - 30 xxxx), xxxxxxx xxx xxxxx indukující "xxxxxxxxxx xxxxxx" (1 - 3 xxxx) je xxxx xxxxxxx. Xxxx xxxx docházet k xxxxxxx x xxxxxxxx xxxxxxxxxx, xxxxxxxx xxxxxxxx xxxx xxxxxx replikace xxxx DNA. Rozsah xxxxxxxx XXX xxxxxx xxx x xxxxxxxxx xxxxxxx xxxxxxxx. Xxxxxx xx xxxxx, že xxxxxxx xxxx xxxx x DNA reagovat, xxx xxxxxxxxx XXX xxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx. Xx, xx UDS xxxx xxxxxxxxxxx o mutagenní xxxxxxxx specifické xxxxxxxxx, xx xxxxxxxx xxxx xxxxxxxxxxx citlivostí, xxxxxxx xxxxxxxxx xxxxxxxx x xxxxx xxxxxx.
1.2 Xxxxxxxx
Xxxxx x reparaci: xxx xxxxxxx grain (NNG) xxxxx xxx xxxxxx, xxxxxx xxxxxxxxx xxxxxxx, xxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxxxx test.
Net xxxxxxx xxxxxx (XXX): xxxxxxxxxxxxx xxxx XXX xxxxxxxx xxxxx při xxxxxxxxxxxxxxxxxxx xxxxxxx UDS, xxxxxxxxx xxxx xxxxxx xxxx xxxxxx xxx v xxxxx (XX) a xxxxxxxxx počtem xxx x xxxxxxxxxx (XX): XXX = XX - XX. Xxxxx XXX se vypočítávají xxx xxxxxxxxxx buňky x xxxxxxxx xxxxxxxxxxx xx xxxxx x xxxxxxx, v xxxxxxxxxxx xxxxxxxxx xxxx.
Xxxxxxxxxxx syntéza XXX (xxxxxxxxxxx XXX xxxxxxxxx, XXX): opravná xxxxxxx XXX xx xxxxxx x xxxxxxxxxx xxxxx XXX obsahujícího xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxx xxxxxxxxxx činidlem.
1.3 Xxxxxxx xxxxxx
Xxxx XXX x xxxxxxx jaterních buňkách xx xxxx xxxxxxxx xxxxxxxxx syntézu DNA xx excizi x xxxxxxxxxx xxxxxxxx XXX xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxx xxxx fyzikálním působením. Xxxx vychází obvykle x inkorporace 3X-XxX xx DNA xxxxxxxxx xxxxx, charakteristických xxxxxx xxxxxx xxxxx x X-xxxx buněčného cyklu. Xxxxxxxxxxx 3H-TdR xx xxxxxxx stanoví autoradiograficky, xxxxxxx tato xxxxxxxx xxxx xxx náchylná x xxxxxxxxxxxx s xxxxxxx v X-xxxx, xxxx xx xxxx. xxxxxxxxxxx metoda.
1.3.1 Xxxxx xxxxxx
1.3.2 Xxxxxxxx
1.3.2.1 výběr xxxxxxxxxxx xxxxx
Xxxxx se xxxxxxxxx xxxxxxx, lze xxxxx xxxxxx jakýkoliv xxxxxx xxxxx druh. Xxxxxxxxx xx běžné xxxxxxxxxxx xxxxx mladých xxxxxxxx dospělých jedinců. Xxxxxxxxxx xxxxxxx by xxx xxxxxxxx studie xxxx xxx xxxxxxxxx x x každého xxxxxxx xxxxxx xxxxxxxxxx ± 20 % xxxxxxxx xxxxxxxxx.
1.3.3 Xxxxxxxx xxxxx
Xxxxxxxxx xxxxxxxx xxxxx xxxx xxxxxxx v xxxxxxxx Všeobecný xxxx. Xxxxxxx xx xxxx xxx 50 - 60 %.
1.3.3.1 Xxxxxxxx xxxxxx
Xxxxxxx xxxxxxx jsou xxxxxxx x ohledem xx druh, xxxxxxx x xxxxx x xxxxxxx s xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx xxxxxxxx
10) x xxxxxxxx xxx, xxx xxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxx xxxxxxx
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx.
10) Zdraví xxxxx xxxxxxx jedinci xx náhodně rozdělí xx kontrolní a xxxxxxxxxxxxxx xxxxxxx. Xxxxxxx xx xxxxxxxxxxx xxxxxx x xxxxx xx xxxxx uspořádat xxx, xxx xx minimalizovaly xxxxxxxx vlivy xxxx, xxx x xxx xxxx xxxxx xxxxxxxx.
1.3.3.2 Xxxxxxxxx látka/příprava
Je-li xxxxxxxxx xxxxx x pevném xxxxx x xx-xx xx xxxxx, xxxxx xx xxxx podáním xxxxxxxx xxxxxxxx nebo xx připraví xxxx xxxxxxxx xx xxxxxxx xxxxxxxxxxxx xxxx xxxxxxxx. Xxxxxxx xxxxxxxxx látky xx mohou xxxxxxx xxxxx xxxx xx xxxx xxxxxxxxx xxxx. Xx xxxxx používat xxxxxxx xxxxxxxxx, xxxxxx xxxxx x stálosti (xxxxxxxxx) xxxxxxxxx, že xxxxxxxxxx xx neovlivní.
1.3.4 Xxxxxxxx xxxxx
1.3.4.1 Xxxxxxxxxxxx/xxxxxxxxx
Xxxxxxxxxxxx/xxxxxxxxx x xxxxxxxxxxx xxxxxxx xxxxx xxxxxxxxx xxxxxxx xxxxxx x xxxxx x xxxxxxxxxx látkou xxxxxxxx xxxxxxxx. Xxxxxxx-xx xx xx xxxxxx xxxxx xxxxxxxxxxxx, musí xxx xxxx xxxxxxx xxxxxxxxx údaji x xxxxxxxxxxxxx x testovanou xxxxxx. Doporučuje xx, xxx xxx xx xx možné, xxxx xx xxxxxx xxxxx xxxxxxx vodné xxxxxxxxxxxx/xxxxxxxxx.
1.3.4.2 Xxxxxxxx
Xx xxxxxxx xxxxx xx xxxxx pro xxxxx pohlaví xxxxxxx xxxxxxxx xxxxxxxxx x xxxxxxxxx (xxxxxxxxxxxx/xxxxxxxxx) xxxxxxxx. Xx třeba zacházet xx xxxxxxx xx xxxxx xxxxxxxxx xxxxxx.
Xxxxxxxxx xxxxxxxx xx xxxx xxxxxxxxx XXX xxx xxxxxxx, xxx lze xxxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxx nad spontánní xxxxxx. Xxxxxxxxx xxxxxxxx xxxxxxxxxx metabolickou xxxxxxxx xx xxxxxxxxx x xxxxxxx xxxxxxxxx xx xxxxxxx vysoké xxxxxx. Xxxxx při xxxxxxxxx xxxxxxxx xx xxxx xxx, xxx byly xxxxxx xxxxxx, xxx xxxxxx nenapovídaly hodnotiteli xxxxxxxxx zakódovaného xxxxxxxxx. Xxxx látky pro xxxxxxxxx xxxxxxxx xxxxx xxxxxxxxx:
|
|
|
|
|
|
xxxxx x xxxxxxxxx (2 - 4 hodiny)
|
N-nitrosodimethylamin
|
|
|
|
odběr x intervalu (12 - 16 xxxxx)
|
X-2-xxxxxxxxxxxxxxxxx (2-XXX)
|
|
|
Xx možno použít x xxxx vhodné xxxxx. Je xxxxx xxxxxxxx xxxxxxxxx xxxxxxxx xxxxx xxxxxx, xxx xx podávána xxxxxxxxx xxxxx.
1.4 Xxxxxx
1.4.1 Xxxxx x xxxxxxx zvířat
V xxxxx xxxxxxx xxxx xxx xxxxxxxxx 3 xxxxxxxxxxxxxx xxxxxxx. Pokud xxxxxxxx xxxxxxxxxx xxxxxxxx, xxx pro xxxxxxxx xxxxxxx negativní x xxxxxxxxx xxxxxxxx xxxxxxxxx 1 nebo 2 xxxxxxx.
Xxxxx x době, xxx xx studie xxxxxxx, existují xxxxx xx studií s xxxx xxxxxxxxxx xxxxxx xxxxxxxxxxxxx týž xxxxxxxxxxx xxxx, prokazující, že xxxx xxxxx xxxxxxxxx xxxxxx x xxxxxxxx xxxxxxxxx xxxxxxx, je xxxxx xxxxxxx xxxxxxxxx xxxxx xx jednom xxxxxxx, xxxxxxx xx xxxxxxx. Xxx, xxx xxxxxxx expozice testovaným xxxxxx může xxx xxxxxxxx xxxxxxxxxx, xxx xx tomu xxxxxxxxx x některých xxxxxxxxxxxxxxx xxxxxxxxx, xxxxxxx xx xxxx na xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx.
1.4.2 Dávkovací xxxxxx
Xxxxxxxxx látka xx xxxxxxx xxxxxx jednorázově.
1.4.3 Xxxxxxxxx
Xxxxxxx xx používají 2 různé xxxxx. Xxxxxxxx xxxxx je xxxxxxxxxx xxxx dávka xxxxxxxxxxxx xxxxxx známky xxxxxxxx, že xxx xxxxx dávce xx xxxxxxx xxxxxx xx xx xxxxxxxx xxxxxxx xxxxxx. Xxxxx xxxxx xxxxxxxxxxx xxxxxx 50-25 % o xxxxx xxxxx.
Xxxxx, xxx x xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxxxx specifickou xxxxxxxxxxx xxxxxxxx, xxxx jsou xxxxxxx nebo mitogeny, xxxxx xxxxxxxxxxxx xxxxxxx x xxxxxx kritérií xxx xxxxxxxxx xxxxx x vyhodnocují se xxxxxx od xxxxxxx. Xxxxxxx-xx xx studie xx zjištění xxxxxxx xxxxxxxx, xxxxxxx potřebné xxxxx nejsou x xxxxxxxxx, xx xxxxx xx realizovat x xxxx xxxxxxxxxx x xx použiti xxxxxxxx xxxxxxxxxxx xxxxx, kmene, xxxxxxx x xxxxxxxxx xxxxxx, xxxx se xxx použijí x xxxxxx xxxxxx.
Xxxx xxxxxxxx xxxxx xxx také xxxxxxxxx xxxxx vyvolávající xxxxxx xxxxxx toxicity x játrech (xxxx. xxxxxxxxxx xxxxx).
1.4.4 Xxxxxxx xxxx
Xxxxxxxx xxxx při xxxxx xxxxxxxxx 2000 xx/xx xxxxxxxxx xxxxxx x 1 nebo 2 xxxxxxx xxx xxx xxxxxxxxxx xxxxx xxxxxxxxxxxxx toxické xxxxxx x xxxxxxxx xx xx xxxxxxx xxxxx x xxxxxxxxxx příbuzných xxxxxxx xxxxxxxxx xxxxxxxxxxxx, xxxxxx xx xxxxxxx xxxxx studie. Podle xxxxxxxxx xxxxxxx xxxxxxxx xxxx xxx použita x limitním xxxxx xxxxx xxxxx.
1.4.5 Xxxxxxxx xxxxx
Xxxxxxxxx xxxxx se xxxxxxx vpravuje žaludeční xxxxxx. X xxxxxxxxxxxx xxxxxxxxx xxxxx xxx xxxxxxxxxx i jiné xxxxxxxxx xxxxx. Xxxxxxxxxxxxxxxxx xxxxxxxx xx xxxx xxxxxxxxxxxx, xxxxxxx xx xx xxx xxxxx xxxxx vystavit xxxxxxxx xxxxxxxxx xxxxx xxxxx, xxxxxx xxxxxxx xxxxxx. Xxxxxxxxx xxxxx kapaliny, xxxxx xx dá xxxxxx nebo xxxxxxx xxxxxxxx vpravit, xxxxxx xx velikostí xxxxxxxxx xxxxxxx a nemá xxxxxxxxx 2 ml/100 x xxxxxxxxx organismu; xxxxx dávky musí xxx xxxxxxxxxx. X xxxxxxxx xxxxxxxxxx xxxx xxxxxxxx xxxxx, jež xxxxxxxx xxxxxxxx při xxxxxxx xxxxxxxxxxxxx xxxxx xxxxxx, xx xxxxx xxxxxxx koncentrace xxxxx xxx, aby xxxxx xxx xx všech xxxxxxxxx xxxxxxxx xxxxxx x xxxxxxxxxxxxxx se xxx objemová xxxxxxxxxxx.
1.4.6 Xxxxxxxx xxxxxxxxx xxxxx
Xxxxxxx xxxxx xx z xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxx 12 - 16 hodin xx xxxxxx xxxxxxxxx xxxxx. Xxxxxxx xx zapotřebí xxxxx xxxxx xxxxx (xxxxxxx 2 - 4 xxxxxx xx xxxxxx xxxxx), xxxxxx xx xx 12 - 16 xxxxxxxx xxxxxxxxx xxxxxx zjevná. Xx xxxxx xxxxx xxxxxx i jiné xxxx odběru xxxxxx, xx-xx xx xxxxxxxxxx xx základě xxxxxxxxxxxxxxxxx xxxxx.
Xxxxxxxxxx xxxxxxx savčích xxxxxxxxx xxxxx xx xxxxxxx zakládají perfuzí xxxxx xx xxxx xxxxxxxxxxx. Xx xxxxx xxxxxxxx, xxx se xxxxxxx xxxxxxxxxxx xxxxxxx xxxxx xxxxx xxxxxxxxx xx vhodnému xxxxxxx. Xxxxxxx buňky xx xxxxxx z xxxxxxxxx xxxxxxxx xxxx mít xxxxxxxxx 50% xxxxxxxxxxxxxxx.
1.4.7 Xxxxxxxxx UDS
Čerstvě xxxxxxxxx xxxxx xxxxxxx xxxxx xx xx vhodnou xxxx (např. 3 - 8 xxxxx) xxxxxxx xxxxxxxx v xxxxx xxxxxxxxxxx 3X-XxX. Xx xxxxxxxx xx xxxxxx xxxxxxxx; buňky xx xxxxx mohou xxxxxxxxx x xxxxx xxxxxxxxxxx xxxxxxxx xxxxxxxxxxx xxxxxxxxx, xxx xx xxxxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxx (xxx. "xxxx xxxxx"). Xxxxx se xxx xxxxxxx, xxxxxx a xxxxxx. Při xxxxxxx xxxxxxxxxxx intervalech xxxxxx xx "cold chase" xxxxxxxx. Xxxxxxx x xxxxxxxxx xx ponoří xx autoradiografické xxxxxx x xxxxxxxx xx xx xxx (např. xx dobu xxxxxxx xxxx xxxx týdnů x chladničce), xxxxxxxx, xxxxxx x xxxxxxxx xx exponovaná xxxxxxxx xxxx. Z xxxxxxx xxxxxxx xx xxxxxxxx 2 xxxx 3 xxxxxxxxx.
1.4.8 Xxxxxxx
Xxxxxxxxxxxxx preparáty xxxx xxxxxxxxx xxxxxxxxxx xxxxx buněk x xxxxxxxx xxxxxxxxxx, aby xxxx xxxxx XXX xxxxxxxxxx. Mikroskopicky se xxxxxxx zjevné xxxxxx xxxxxxxxxxxx (např. xxxxxxx, xxxxxxx úroveň xxxxxxxxxxxxxx xxxxxxx).
Xxxxxxxxx xx xxxx xxxxxxxxx xxx xxxxxxxx. Xxxx xx xxxxxxxxx 2 preparátech z xxxxxxx jedince xx xxxxxxx xxxxxxx 100 xxxxx; xxxxx je xxxxx xxxx xxx 100 xx xxxxxxx, xxxx xx xxx xxxxxxxxxx. Xxx xxxxxxxx xxx xx nevyhodnocují xxxxx v X-xxxx. xxx xxxxx buněk x S-fázi se xxxxxxxxxx.
Xxxxxxx xxxxxxx xx xxxxxxx xxxxxx inkorporace 3X-XxX do xxxxx x xxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxx xxxxxxx, xxxxxxxxxx xxxxx depozice xxxxxxxxxx xxxxx.
Xxxxx xxxxx xx xxxxxxx x xxxxx zrn odpovídajících xxxxxxxx jádrům (NG) x x průměrného xxxxx xxx v xxxxxxxxxxxxxxxxx xxxxxxxxx (CG) xxxxxxxxxxxxxx jádrům. Xxxx xxxxxxx XX xx xxxxxxx xxx' počet xxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxxx cytoplasmy, xxxx xxxxxxxx xxxxxxx xxxx až xxx xxxxxxx xxxxxxxxx xxxxxxx x blízkosti dotyčných xxxxxxxxx xxxxx. Xx xxxxxxxxxxxxx zdůvodnění mohou xxx xxxxxxx, x xxxx xxxxxxx xxxxxxxxx xxxxx xxxxx (xxxx. xxxxxxxx xxxxxx buněk).
2 XXXXX
2.1 Xxxxxxxxxx xxxxxxxx
Xxxxxxxx xxxxxxxx údaje x xxxxxxxxxxxx xxxxxxxxx x xxxxxx. Mimoto xx xxxxxxx xxxx shrnou x xxxxxxxxx xxxxx. Xxx každou buňku, xxxxxxx xxxxxxx x xxxxxx dávku x xxx se xxxxxxx xxxxx počet ,xxxxxxx xxxxx" (XXX) xxxxxxxxx xxxxx XX od xxxxx XX. Xxxxxxxx-xx xx "buňky x xxxxxx", xxxx xxx xxxxxxxx, kterými xx xxxx xxxxx určují, xxxxxxxxxx x xxxxxxxxx xxxx x xxxxxxxxxxxx xxxx souběžných xxxxxxxxxxx xxxxxxx. Xxxxxxxxx výsledky xx mohou xxxxxxxxxx xxxxxxxxxxxxx metodami; pokud xx xxxxxxxxxxx xxxxx xxxxxxx, xx xxxxx xx xxxxxx x xxxxxxxxx ještě xxxx xxxxxxxxx xxxxxx.
2.2 Xxxxxxxxxxx x xxxxxxxxxxxx výsledků Xxxxxxxx xxx pozitivní/negativní xxxxxx xxxxxxxx:
Xxxxxxxxx
(X) xxxxxxx XXX nad xxxxxx xxxxxxxxxx xxxxxx, zdůvodněným xx základě historických xxx xxxx laboratoře, xxxx
(XX) xxxxxxx XXX xxxxxxxx xxxxx xxx x xxxxxxxx kontroly.
Negativní
(I) xxxxxxx XXX xx xxxxxx/xxx úrovní xxxxxxxxxxxx xxxxx u xxxxxxx, xxxx
(XX) hodnoty XXX xxxxxx xxxxxxxxxxxxx xxxxx xxx xxxxxxxx xxxxxxxx.
Xx xxxxx xxxxxx biologickou xxxxxxxxxx xxxxxxxxx xxx, xxx znamená, xx xx xxxxx xxxx x xxxxx xxxxxxxxx, xxxx jsou xxxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxx, xxxxx xxxxx-xxxxxxx x xxxxxxxxxxxx. Při vyhodnocování xxxxxxxx xxx použít xxxxxxxxxxx xxxxxx; statistická xxxxxxxxxx by xxxx xxxxxx být xxx xxxxxxxxx xxxxxx xxxxxxxxxxxx xxxxxxxx.
Xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxx xxxxxxxxx xxxxxxxx, x xxxxxxxxxxx xxxxxxxxx však xxxxx ze získaného xxxxxxx xxx xxxxxxx x aktivitě xxxxxxxxx xxxxx xxxxxxxxxxx xxxxx. Xxxxxxxx xxxxx být xxxxx xxxxxxxxxxxxx xxxx xxxxxxxxxxxxx, i xxxx xx xxxxxxxxxx xxxxxxxxxx xxxxxxx.
Xxxxxxxxx xxxxxxxx xxxxx XXX xx xxxxxxx xxxxxxxxx xxxxxxx xx xxxx xxxxxxx, xx xxxxxxxxx xxxxx xxxxxxxx x xxxxxxx xxxxxxxxx xxxxxxx in xxxx xxxxxxxxx XXX, které xxx xxxxxxx neplánovanou xxxxxxxx XXX xx xxxxx. Xxxxxxxxx xxxxxxxx xxxxxxx, že za xxxxxx xxxxxxxxxxxxxxxx podmínek xxxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxxxxxxxx XXX, xxx xx xxxxx xxxxxx xxxxxxxxxxx.
Xx xxxxx xxxx x úvahu, xxxx xx xxxxxxxxxxxxxxx, xx testovaná látka xxxxxxx xxxxxxxx použití xxxx je specifická xxx xxxxxxx xxxxxxx xxxx (např. systémová xxxxxxxx).
3 PROJEKT POKUSU, XXXXXXXX XXXXXX A XXXXXXXXX ZPRÁVA
V xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx x x xxxxxxx xxxxxx xx xxxxx xxxx xxxxxxxx.
Xx xxxxxx x xxxxxxx xxxxxx xx xxxxx xxxxx xxxx informace: Xxxxxxxxxxxx / vehikulum
- xxxxxxxxxx xxxxx xxxxxxxx,
- rozpustnost x xxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxxxxx/xxxxxxxx, xxxxx xx xxxxx.
Xxxxxxx xxxxxxx:
- použitý xxxxxxxxx xxxx/xxxx,
- xxxxx, xxx x xxxxxxx jedinců,
- xxxxx, xxxxxx xxxxxxxx, xxxxxx xxxx.,
- hmotnost xxxxxxxxxxxx zvířat na xxxxxxx xxxxx, včetně xxxxxxxxxxxx xxxxxxx, xxxxxxx x xxxxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx skupiny.
Podmínky xxxxxx:
- xxxxxxxxx a xxxxxxxxx (rozpouštědlo/vehikulum) kontroly,
- xxxxx xx xxxxxx xxx xxxxxx xxxxxxx, xxxx-xx xxxxxxxxx,
- zdůvodnění xxxxxxxxx xxxxxx dávek,
- xxxxxxxxxxx o přípravě xxxxxxxxx látky,
- xxxxxxxxxxx x podávání testované xxxxx,
- xxxxxxxxxx xxxxxxx xxxxxxxx,
- xxxxxxxx xxxxxx x xxxxxxx, xx xx látka xxxxxxx xx xxxxxxxx oběhu xxxx xx cílové xxxxx,
- případný xxxxxx xxxxxxxxxxx xxxxx x xxxxxxx/xxxxx xxxx (ppm) xx faktickou xxxxx (xx/xx hmotnosti /xxx),
- xxxxxxxxxxx o xxxxxxx xxxxxxx x xxxx,
- xxxxxxxx xxxxxx xxxxxxxx xxxxxxxxx xxxxx x xxxxxx vzorků,
- xxxxxx xxxxxxxxxx xxxxxxxx,
- metoda xxxxxxxx x xxxxxxxxx xxxxxxxxx buněk,
- xxxxxxx xxxxxxxxxxxxxxxxx xxxxxx,
- xxxxx xxxxxxxxxxxx xxxxxxxxx x xxxxx xxxxxxxxxxx xxxxx,
- xxxxxxxx xxxxxxx,
- xxxxxxxx, xxxxx se xxxxxx xxxxxxx jako xxxxxxxxx, xxxxxxxxx xxxx xxxxxxxxxxxxx.
Xxxxxxxx:
- xxxxxxxx hodnoty xxxxx xxxxxxxxxx zrn x xxxxxxx, cytoplazmě a "xxx xxxxxxx xxxxxx" xxx jednotlivé preparáty, xxxxxxx x xxxxxxx,
- xxxxx xxxxx-xxxxxxx, xxxxx xx x xxxxxxxxx,
- xxxxxxxxxxx xxxxxxxxx, bylo-li xxxxxxxxx,
- xxxxxx xxxxxxxx,
- xxxxx xx xxxxxxxxxx xxxxxxxxxxx (xxxxxxxxxxxx/xxxxxxxxx) x xxxxxxxxxxx kontrol,
- historické xxxxx x xxxxxxxxxxx (xxxxxxxxxxxx/xxxxxxxxx) x xxxxxxxxxxx xxxxxxx xxxxxx xxxxxxx, xxxxxxx a směrodatných xxxxxxxx,
- počet "xxxxx x xxxxxx", xxx-xx xxxxxxxx,
- počet buněk x S-fázi, xxx-xx xxxxxxxx,
- xxxxxxxxxxxxxxx buněk.
Diskuse xxxxxxxx.
Xxxxxx.
X.40 LEPTAVÉ XXXXXX XX XXXX
1 XXXXXX xx x xxxxxxx x xxxxxx Evropských xxxxxxxxxxxx.
6)1.1 Xxxx
Xxxxxxxx xxxxxxx xxx xxxxxxxx xxxxxxxxxxxxxx xxxxx (European Centre xxx xxx Xxxxxxxxxx xx Alternative Xxxxxxx, XXXXX, Xxxxx Research Xxxxxx, Xxxxxxxx Xxxxxxxxxx) xxxxxxxxx jakožto vědecky xxxxxxx xxx xxxxx xx vitro xx xxxxxxx xxxxxx xx xxxx: test xx xxxxxxxx xxxxxx transkutánního xxxxxxxxxxxx xxxxxx xxxx xxxxxxx (xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx, XXX) x xxxx xxxxxxxxxxx modelu xxxxxx kůže.
6) Validační xxxxxx XXXXX xxxxxxxxx, xx oba testy xxxxxx xxxxxxxxxx xxxxxxxxxx xxxx známými xxxxxxx xxxxxxxxxxx a neleptajícími xxxx. Mimoto xxxx xxxxxxxxxxx x xxxxxx xxxxxx xxxx xxxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxx (xxxxx xxxxx způsobující xxxxx poleptání kůže X35, x ostatní xxxxx xxxxxxxxxxx poleptání xxxx, X34).
6) Je xxxxxx popis x xxxxxxx xxxx testů; xxxxx mezi xxxxx xxxxx závisí xx xxxxxxxxxxx xxxxxxxxxxx x xx xxxxxxxxxxxx xxxxxxxxx.
1.2 Xxxxxxxx
Xxxxxxxxx kůže: způsobení xxxxxxxxxx xxxxxxxxx xxxxx xxxx xx xxxxxxxx xxxxxxxxx xxxxx.
1.3 Xxxxxxxxxx xxxxx
Xxxxx xxxxxxxxxx xxxxx xxxx xxxxxxxxxxxxx, xxx xxxx xxxx. 1.5.3.4 x 1.7.2.3.
1.4 Xxxxxxx xxxxxx - test XXX xx kůži xxxxxxx
Xxxxxxxxx xxxxxxxx xx xxxxxx xx xxxx xx 24 hodin xx xxxxxxxxxxx povrch xxxxxxx xxxx odebrané x xxxxxxx xxxxxxx xxxxxxxxxx humánním xxxxxxxx. Xxxxx, které xxxx xxxxxxx xxxxxx, xxxx xxxxxxxxxxxxxx xxxxx xxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxx a xxxxxxxxx xxxxxx stratum corneum. Xxxx xxxxxxxxx se xxxx jakožto xxxxxx xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx (XXX) xxx xxxxxxx xxxxxxxx xxxxxxx (5 kΩ).
6) Xxxxxxxx x xxxxxxxxxx látky XXX pod prahovou xxxxxxx nesnižují. V xxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxx xxxxx (xxxxxxx xxxxxxxx viz x xxx.
6) xx xxxxx xx zkušebního xxxxxxx xxxxxxx xxxx xxxxxx barviva, xxx xx snížil xxxxx xxxxxxxxx xxxxxxxxxxx xxxxxxxx, xxx xx x xxxxxx xxxx chemických xxxxx vyskytují.
6)1.5 Popis xxxxxx - xxxx XXX xx xxxx xxxxxxx
1.5.1 Xxxxxxx zvířata
Pokusná xxxxxxx xxxx xxxxxxx x ohledem xx xxxx, xxxxxxx x xxxxx x souladu x xxxxxxxxxxx
§15 xxxxxxxxxx xxxxxxxx předpisu
10) x označena tak, xxx xxxx xxxxx xxxxxxxxxxxx jednotlivých xxxxxx. Xxxx xxxxxxxx stanoví
§10 zvláštního xxxxxxxx xxxxxxxx.
10)Xxx xxxxxxxx kožních xxxxxxx xxxx používáni xxxxx (20 xx 23xxxxx) xxxxxxx, Wistar xxxx srovnatelný xxxx. Xxxxxx nůžkami na xxxxxxx xx xxxxxxx xxxxxxxx srst z xxxxxxxx x xxxxx xxxxxx. Xxxxxxx xx xxx xxxxx pečlivým xxxxxxxx a xxxxxx xx xxxxxx xx xxxxxxx xxxxxxxxxxx, xxxxxxxxx xxxxxxxxxxxxx, xxxxxxxxxx, chloramfenikolu xxxx xxxxxxxxxxxx, v xxxxxxxxxxxxx inhibujících xxxx xxxxxxxx. Třetí xxxx xxxxxx xxx xx xxxxxx xxxxx se xxxxxxx xxxxx xxxxxxxxxxx xxxxx x xxxxx 3 dní xx xxxxxxx. Xxx xxxxxxxx xxxxxxx xxxxxx xxxxxxx xxx zvířata starší xxx 31 dní.
1.5.2 Xxxxxxxx xxxxxxx xxxx
Xxxxxxx xx xxxxxxxx způsobem xxxxxx, xxxxx xx xxxx x xxxxxxxx xxxxxx x z xx se opatrně xxxxxxx xxxxxxxxxx tuk. Xxxx xx xxxxxxx xxxx xxxxx xxxxxxxxxxxxxxxxxxxxxxxx (XXXX) trubice, x xx xxxxxxxxxxx xxxxxxx x xxxxxxx. Přes xxxxx xxxxxxx se xxxxxxxx xxxxxx X-xxxxxxx, xxxxxx xx xxxx xxxxxx, x xxxxxxxxxx xxxx xx xxxxxxx. Xxxxxxx xxxxxxx a X-xxxxxxx ukazuje xxx. 1. Xxxxxx X-xxxxxxx xx xxx zatěsní xxxxxxx xx xxxxx XXXX trubice žlutou xxxxxxxxx. Xxxxxxx xx xxxxxx do nádoby xxxxxxxxxx xxxxxx síranu xxxxxxxxxxx (154 mM), xxx xx xxxxxxxxxxx xxxxxxxxxx sponou (obr. 2).
1.5.3 Xxxxx xxxxxxx
1.5.3.1 Xxxxxxxx xxxxxxxxx xxxxx
Xx-xx xxxxxxxxx xxxxx v xxxxxxx xxxxx, xxxxxx xx xx xxxxxxxxxxx xxxxxx xxxxxx xxxxxxx (xxx. 2). Je-li xx stavu xxxxxx, xxxxxx se xx xxxxxx x xxxxxxx xxxxxxxx, xxx xx xxxxxx xxxx xxxxxx xxxxxxxxx, xx xxxxxx xxxxx xx přidá 150 µx xxxxxxxxxxxx xxxx x trubicemi xx jemně zatřepe. Xxxxxxxxx látka xxxx xxx x xxxx xxxxxxxxx xxxxx kontakt. X xxxxxxxxx xxxxxxx xxxxx toho xxx xxxxxxxxx zahřátím xxxxx xx 30 °C, xxx xx xxxxxxxxx, xxxx xxxxxxxxxx zrnitého xxxxxxxxx na xxxxx xxxxxx. Xxxxxxx xx xxxx 3 terčíky xxx xxxxxx xxxxx. Xxxxx xx xxxxxx xx xxxx 24 xxxxx (xxx xxx 1.5.3.4) x xxxxxxxx xx xxxxxxxxxx xxxxxxx xxxxxxxxx xxxx xxxxx xxxxxxxxx 30 °X xxx xxxxxx, xxxxx xx xxxxx xxxxxxxxx. Xxxxxxxxxx xxxxxxxxx látky, xxxxx x trubici xxxxxx, xx xx xxxxxxxx xxxxxxxxx prudkým xxxxxxx xxxx xxxxx xxxxxx 30 °C.
1.5.3.2 Xxxxxx XXX
Xxxxxxxxxxxx xxxxxxxxxx xxxxx (XXX) xx xxxx xxxxxx nízkonapěťového xxxxxxxxxxxx xxxxxx xxx xxxxxxxx xxxxx (xxxx. XXX 401 nebo 6401 xx ekvivalentního). Xxxx xxxxxxx xxxxxxxxxxxx xxxxxx xx sníží xxxxxxxxx xxxxxx xxxx xxxxxxxxx dostatečného objemu 70% ethanolu, xxxxxx xx xxxxxxx xxxxxxxxx. Xx xxxxxxxx sekundách xx ethanol xxxxxxxx xxx, že se xxxxxxx xxxxx, x xxxx xx xxxxxxxxx xxxxxxxxx 3 mililitrů 154 xX xxxxxxx xxxxxx xxxxxxxxxxx. Elektrody xxxxxx xx xxxxxxx xx xxx xxxxxx xxxx x xxxxx xx xxxxx x xΩ/xxxxxx (obr. 2). Xxxxxxx xxxxxxxx x xxxxx xxxx elektrody xxx krokosvorkou xxxxxxx xxx. 1. Xxxxxx xxxxxxx (xxxxx) xxxxxxxxx xx během měření xxxxx navrch XXXX xxxxxxx tak, xxx xxxx do xxxxxxx xxxxxx xxxxxxxxxxx ponořena xxxx xxxxxx xxxxx xxxxxxxxx. Vnější (tenká) xxxxxxxxx se uloží xx xxxxxxxxxxx xxxxxxx xxx, xxx ležela xx dně. Je xxxxx xxxxxxxxx konstantní xxxxxxxxxx xxxx xxxxxx xxxxxx xxxxxxxxx xxxxxx x xxxxxxx PTFE xxxxxxx (xxx. 1), xxxx vzdálenost má xxxx xx xxxxxxxx xxxxxxx xxxxxx.
Xxxxxxxxxxxx, že xx-xx xxxxxxxx xxxxx xxxxx než 20 xΩ, xxxx xx xxx důsledek xxxx, xx testovaná látka xxxxxxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxx. Xx xxxxx xx xxxxxxx xxxxx povlak odstranit, xxxxxxxxx xxx, xx xx PTFE xxxxxxx xxxxxx xxxxxx x xxxxxxxx x xxxxxx 10 sekund xx xxxxxxxxxx, roztok xxxxxx xxxxxxxxxxx xx xxxxxx x měření xxxxxx xx xxxxxxx x xxxxxxxx xxxxxxxx.
Xxxxxxxx xxxxxxxx xxxxxxx XXX xx xxxxxxxxxxx, xxxxx xxxxxxx xx xxxxxxxx pozitivní x xxxxxxxxx xxxxxxxx xxxx x rozmezích xxxxxxxxxxxx xxx xxxx xxxxxx. Xxxxxxxxxx kontrolní xxxxx a xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx odporu xxx xxxxxxxxxxx xxxxxx x xxxxxxxxx jsou xxxx:
|
|
|
|
|
Pozitivní
|
10 X kyselina xxxxxxxxxxxxxx (36%)
|
|
|
Xxxxxxxxx
|
xxxxxxxxxxx xxxx
|
|
1.5.3.3 Xxxxxxxxxxxx postup xxx xxxxxxxxx xxxxxxx xxxxx x xxxxxxxxx xxxxxxxxx xxxxx
Xxxxx xx při xxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxx (xxxxxxxxxx) xxxx xxxxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxx XXX xxxxx xxxx xxxxx 5 xΩ, xxx na xxxx xxxxx xxxxxxx xxxxxxxxx xxxxxxx (penetrace) xxxxxxx. Xxxxx postupem xx xxxxxx, xxx xx nejedná o xxxxxxxx falešně xxxxxxxxx.
6)1.5.3.3.1 Xxxxxxxx x xxxxxxxxxx xxxxxxx sulforhodaminu B
Po xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx se na xxxxxxxxxxx xxxxxx xxxxx xxxxxxx xxxxxx xx 2 xxxxxx po 150 µx 10% (x/x) xxxxxxx sulforhodaminu X x xxxxxxxxxxx xxxx. Xxxxxxx kůže xx xxx zhruba xx xxxx 10 xxxxxx oplachují xxxxxxx xxxxxxx xxxxxxxxx xxxx, xxxxx xx nejvýše xxxxxxxxx xxxxxxx. Xxx xx xx odstranit xxxxxxxxxx (xxxxxxxxxx) xxxxxxx. Xxxxx terčík kůže xx xxx xxxxxxx xxxxx x XXXX xxxxxxx a xxxxx xx xxxxxxx (xxxx. xx 20 xx xxxxxxxxxx xxxxx xxx xxxxxxxxxx) xxxxxxxxxx 8 xx xxxxxxxxxxxx vody. Xxxxxxx se xx xxxx 5 xxxxx xxxxx xxxxxx, xxx xx xxxxxxxxxx veškeré xxxxxx xxxxxxxxxxxx (nenavázaného) xxxxxxx. Xxxxx xxxxxx xx opakuje. Xxx xx xxxxxxx xxxxxx x vloží xx xxxxxxx s 5 xx 30 % (x/x) roztoku xxxxxxxxxxxxxx xxxxxxx (SDS) x xxxxxxxxxxx xxxx, xxx xx xxxx noc xxxxxxxx xxx xxxxxxx 60 °X. Xx xxxxxxxx xx xxxxxxx xxxxxx x xxxxxxxxxx x zbývající xxxxxx xx xxxxxxxxxx po xxxx 8 xxxxx xxx xxxxxxx 21 °X (xxxxxxxxx xxxxxxxxxx xxxx -175). Xxxxxx 1 xx supernatantu xx xxx xxxxx 30 % (w/v) xxxxxxxx XXX x xxxxxxxxxxx xxxx x xxxxxxxxx xxxxxx 1 x 5 (v/v) (xx. 1 xx xxxxxxxxxxxx + 4 xx xxxxxxx XXX). Xxxxxxx xxxxxxx (XX) xxxxxxx se xxxx xxx xxx 565 xx.
1.5.3.3.2 Xxxxxxx xxxxxx xxxxxxx
Xxxxx xxxxxxxxxxxxxx X x xxxxxxx se xxxxxxxx x hodnoty XX (xxxxxxx extinkční xxxxxxxxxx sulforhodaminu X xxx 565 nm xxxx 8,7 . 104; xxxxxxxxxx hmotnost = 580). Xxxxx xxxxxxxxxxxxxx X xx xxxxxxxx pro xxxxx xxxxxx xxxx zvlášť x xxxxxxx se xxxxxxxx xxxxxxx. Xxxxxxxx xxxxxxx xxxxxxxxxx barviva xx akceptována za xxxxxxxx, xx xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx xx akceptovatelného rozsahu xxxx xxxxxx. Xx xxxxxxxxxxxxxx xxxxxxx xxxxxx xxxxxxx xx u xxxxxxxxxxx xxxxx xxx xxxx xxxxxx a xxxxxxxxxxxxxxx uspořádání xxxxxxxx:
|
|
|
Xxxxxxx xxxxxx barviva (μx/xxxxxx)
|
|
Xxxxxxxxx
|
10 X xxxxxxxx xxxxxxxxxxxxxx
|
|
|
Xxxxxxxxx
|
xxxxxxxxxxx voda
|
|
1.5.3.4 Xxxxxxxxxx xxxxxxxxx
Xx možné xxxxxx xxxxxx dobu xxxxxxxx xxxxxxxxx xxxxx xx xxxxxx xxxx (např. 2 hodiny) xx xxxxxx xxxxxxxxx silně xxxxxxxxxxx xxxxx. Xx xxxxxxxxxxx xxxxxx však xxxx xxxxxxxx, xx xxxx XXX přeceňuje xxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx xxxxxxxxxxxx xx xxxxxxx xxxx xx 2 xxxxxx,
6) xxxxxxxx xxxxxxxx správnou xxxxxxxxxxxx xxxxxxxxxxx x xxxxxxxxxxxxx xxxxx xx 24xxxxxxxxx xxxxxxxx.
Xxxxxxx xxxxxxx XXX mohou xxx xxxxxxxxx xxxxxxxxxxx x xxxxxxx xxxxxxxx xxxxxxxxx x experimentálním postupem. Xxxxxxx xxxxxxx xxx xxxxxxx xxxxxx 5 xΩ byla xxxxxxxxx xx xxxxxxx xxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxxx x xxx xxxxxxxx xxxxxxx xxxxxxxxx xxx. Xxxxx xx xx xxxxxxxx xxxxxxxx xxxxxxx xxxxxxx, mohlo xx xxx xxxxx xxxxxxx xxxxxx prahových x kontrolních hodnot. Xxxxx xx xxxxxxxxxx xxxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxx otestováním xxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx z xxxxx, xxx xxxx xxxxxxx xxx xxxxxxxxx xxxxxx.
6)1.6 Xxxxxxx xxxxxx - xxxx x xxxxxxx xxxxxx xxxx
Xxxxxxxxx xxxxxxxx xx xxxxxx xxxxxxx xx dobu xx 4 xxxxx na xxxxxxxxxxxx xxxxx xxxxxx xxxx, xxxxxxxxxxx zrekonstruované xxxxxxxxx s xxxxxxx xxxxxxx xxxxxxx. Xxxxxxxxx xxxxxxxx se pozná xxxxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxx "XXX reduction xxxxx" (XXX = 3-[4,5-dimetylthiazol-2-yl]-2,5 xxxxxxx xxxxxxxxxxx xxxxxx) xxx xxxxxxxx xxxxxxx xxxxxxxxxxx pro xxxxx xxxxxxxxx xxxx. Xxxxxxx xxxxx vychází x xxxxxxxxxxx, xx látky xxxxxxxxxxx xxxxxxxxx kůže xxxx ty, xxxxx xxxxxx proniknout skrze xxxxxxx corneum (difúzí xxxx xxxxx) x xxxx xxxxxxxxxx cytotoxické, xxx přivodily xxxx xxxxx x xxxxxxxx xxxxxxxxx vrstvách.
1.7 Xxxxx xxxxxx - test x modelem xxxxxx xxxx
1.7.1 Xxxxxx xxxxxx xxxx
Xxxxxx lidské xxxx xxxxx xxxxxxxx z xxxxxxx xxxxxx, musí xxxx splňovat xxxxxx xxxxxxxx. Model xxxx xxx xxxxxxx xxxxxxx xxxxxxx x podkladovou xxxxxxx xxxxxx xxxxx. Xxxxxxxxx funkce xxxxxxx xxxxxxx musí být xxxxxxxxx xxxxxxxxx. Xx xxx xxxxxxxx xxx, xx xxxxx xxxx xxxxxxxxxxx vůči xxxxxxxxxxxx xx xxxxxxxx látek, x nichž xx xxxxx, xx jsou xxx buňky xxxxxxxxxxx, xxxxx xxxx normálně xxxxx xxxxxxx corneum xxxxxxxxxxxx. Xxxxx musí xx xxxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxx xxxxxxxxx reprodukovatelné xxxxxxxx.
Xxxxxxxxx xxxxxx xxxxx x xxxxxx musí xxx xxxxxxxxxxx x xxxx, xxx xx xxxx dobře xxxxxxxx xxxx xxxxxxx xxxxxxxxx x negativní kontroly. Xxxxxxxxx xxxxx (xxxxxx xxxxxxxxx xxxxxxxxx xxxxxxx XXX, xx. XX xxxxxxxx) xx expozici xxxxx xxxxxxx xxxx xxxxxxxxx kontrola xxxx xxxxx v přijatelných xxxxxx pro xxxx xxxxx. Podobně x xxxxxxx látky xxx xxxxxxxxx xxxxxxxx (ve xxxxxxxx x látkami xxx xxxxxxxxx xxxxxxxx) xxxx hodnoty xxxxxxxxxx xxxxxx xx xxxxxxxx xxxx. Xx xxxxx xxxxxxxx, aby bylo xxxxxxxxx, xx použitý xxxxxxxxx model odpovídá xxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxx.
6)1.7.2 Xxxxx xxxxxxx
1.7.2.1 Nanesení xxxxxxxxxxx materiálu
Je-li testovaná xxxxx xxxxxx, xxxxxx xx xxx, aby xxxxxxxxx xxxxxx xxxx (xxxxxxxxx množství 25 µx/xx2).
Xx-xx xxxxx, xxxxxx xx xxx, aby xxxxxxxxx kůži, x xxxxxxxx se zvlhčí, xxx xx x xxxx xxxxxxxx xxxxx xxxx. Xxxxx xx xx xxxxx, pevné xxxxx xx před xxxxxxxx roztírají na xxxxxx. U xxxxxx xxxxxxxx xxxx xxx xxxxxxxxx, xx xx xxxxxx pro xxxxxx xxxxxx xxxxx
6) Po xxxxxxxx xxxx xxxxxxxx xx xxxxxxxx x xxxxxxx kůže xxxxxxx xxxxx xxxxxxxxxxxxx roztokem.
1.7.2.2 Xxxxxx životnosti xxxxx
X xxxxxx xxxxxxxxxx xxxxx xx dá xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxx. Xxxxxxxxxx xx xxxxxxx xxxxxxx XXX, x xxxxx xxxx xxxxxxxxx že v xxxxxxx laboratořích poskytuje xxxxxx a reprodukovatelné xxxxxxxx.
6) Xxxxxx kůže xx xx dobu 3 xxxxx ponoří xx xxxxxxx XXX x xxxxxxxxxxx 0,3 xx/xx xxx xxxxxxx 20 - 28°C. Xxxxxxxxx modrý formazanový xxxxxxx xx pak xxxxxxxxx (xxxxxxxx xxxxxxxxxxxxx) x xxxxxxxxxxx xxxxxxxxx xx xxxxxxx xxxxxxx XX xxx xxxxxx xxxxx 545 až 595 nm.
1.7.2.3 Xxxxxxxxxx xxxxxxxxx
Xxxxxxx xxxxx xxxx x xxxxxx xxxxxxxx xxxx působení, promývacího xxxxxxx atd. xxxx xx xxxxxxxxx xxxxx xxxxxxxx vliv. Xxxxxxxxxx xx xxxxxx i xxxxxxxxx model xxxxxxxxxxx xx použití řady xxxxxxxxxxxx xxxxxxxxx xxxxxxxxx x xxxxx použitých xx xxxxxxxxxxx xxxxxx XXXXX.
6) Xx xxxxxxxx xxxxx, xxx bylo xxxxxxxxx, xx xx xxxxxxx metoda xx xxxxxxx xxxxxx xxxxx xxxxx reprodukovatelná xxxxx xxxxxxxxxxxxx xxxxxxxxx xxx x xxxxx dané xxxxxxxxxx, xxx mezi xxxxxxx xxxxxxxxxxxx. Xxxxxxxxx xxxx metoda xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx xxxxxxxxxx xxxxx
6) x xxxxxxxx xxxxxx xxxxxxxxxxx xxxxxx musí xxx xxxxxxxxxx x takovém xxxxxxxx xxxxxxxx, xx xxxxxx články xxxx xxxxxxxxxxx xxxxxxxxxx odbornou xxxxxx.
2 XXXXX
2.1 Xxxxxxxxxx xxxxxxxx
2.1.1 Xxxx XXX xx xxxx xxxxxxx
Xxxxxxx xxxxxx (v xΩ) xxx xxxxxxxxx xxxxxxxx, xxxxxxxxx a negativní xxxxxxxx a xxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xx xxxxxxx x xxxxxxxxx xxxxx, x to data xxx xxxxxxx xxxxxxxxx x opakované xxxxxxxxxxx, xxxxxxxx xxxxxxx x x xxxx xxxxxxxx xxxxxxxxxxx.
2.1.2 Xxxx x xxxxxxx xxxxxx kůže
Hodnoty XX x xxxxxxxxx xxxxxxxx životaschopných buněk xx xxx xxxxxxxxx xxxxxxxx, pozitivní x xxxxxxxxx kontroly a xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxx x xxxxxxxxx xxxxx, a xx xxxx xxx xxxxxxx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxx, průměrné xxxxxxx a z xxxx xxxxxxxx klasifikace.
2.2 Xxxxxxxxxxx x interpretace xxxxxxxx
2.2.1 Xxxx TER xx xxxx potkana
Pokud xx průměrná xxxxxxx XXX pro testovaný xxxxxxxx xxxxx xxx 5 xΩ, xx xxxxx xxxxxxxxxxx. Je-li xxxxxxx XXX nižší xxxx xxxxx 5 xΩ x xxxxxxx xx xxxxxx o xxxxxxxxx aktivní xxxxx (xxxxxxxxx) xx neutrální xxxxxxxxxx xxxxx, pak xxxxxxxxx látka xxxxxxx xxxxxx má.
U xxxxxxxxx xxxxxxxxx xxxxx (detergentů) x neutrálních xxxxxxxxxxx xxxxx, xxx xxxxxxxxx xxxxxxx XXX xxxxxxxxxxxxx 5 xΩ, lze xxxxxxx xxxxxxx penetrate xxxxxxx. Xx-xx xxxxx xxxxxxx v xxxxxxx xxxxx nebo rovný xxxxxxxxxx obsahu xxxxxxx x xxxxxxx xxx xxxxxxxx xxxxxxxxx pozitivní xxxxxxxx x 36 % XXx, xx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxxx x tedy xx xxxxxxx xxxxxx, xxxxxx je-li xxxxx xxxxxxx v terčíku xxxxx, je testovaná xxxxx xxxxxxx xxxxxxxxx x tedy xxxxxxx xxxxxx xxxx.
2.2.2 Test x modelem xxxxxx xxxx
Xxxxxxx XX xxx xxxxxxxxx kontrolu představuje 100% xxxxxxxxxxxxxxx xxxxx. X hodnot OD xxx xxxxxxxxxx zkušební xxxxxx se xxxxxxx xxxxxxxxxxxx životnost xxxx xxxxxxxxx kontrole. Xxxxxxxx xxxxxxxxx xxxxx životaschopných xxxxx, xxxxx xxxxxxxx xxxxx, které nezpůsobují xxxxxxxxx xxxx, od xxxx, které xxxxxxxxx xxxxxxxxx, xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxx, musí xxx x xxxxxxxxxx xxxxxx xxxxx xxxxxxxxx předtím, xxx xx xxxxxx xxxxxxxxxx, x xxxxxxxxx xxxxxxxxx xxxxxx xx xxxx xxxxxxxx, xx xx xxxx hraniční xxxxxxx odpovídající.
6)3 XXXXXXX XXXXXX, XXXXXXXX XXXXXX X XXXXXXXXX XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9) musí xxx xxxxxxxxx xxxxxxx xxxxxx x x xxxxxxx xxxxxx xx xxxxx vést xxxxxxxx.
Xx xxxxxx x xxxxxxx xxxxxx je xxxxx xxxxx xxxx xxxxxxxxx:
Xxxxxxxxx xxxxx:
- identifikační údaje, xxxxxxxxx stav, popřípadě xxxxxxxxx-xxxxxxxx xxxxxxxxxx; pokud xx používají xxxxxxxxxx xxxxx, xxxxxx xx xxxx údaje x xxx xx.
Xxxxxxxx xxxxxx:
- xxxxxxxx xxxxx xxxxxxxxx xxxxxxx,
- xxxxx x xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx.
Xxxxxxxx:
- tabulka xxxxxx xxxxxx (test XXX) xxxx procentuální podíl xxxxxxxxxxxxxxx buněk (test x modelem xxxxxx xxxx) xxx testovaný xxxxxxxx, xxxxxxxxx x xxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx, a to xxxxx xxx všechny xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx x xxxxxxxx xxxxxxx;
- popis všech xxxxxx xxxxxxxxxxxx efektů.
Diskuse xxxxxxxx.
Xxxxxx.
-
X.41 XXXXXXXXXXXX - XXXX XXXXXXXXXXXX 3T3 XXX IN XXXXX
1 XXXXXX je x xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx.
6)1.2 Xxxx
Xxxxxxxxxxxx xx xxxxxxxxxx jako xxxxxxx odezva (xxxxxx), x níž xxxxxxx. xx-xx kůže poprvé xxxxxxxxx xxxxxxx chemickým xxxxxx x xxxxxxxx xxx světlu, xxxx xx-xx podobně kůže xxxxxxx po xxxxxxxx xxxxxx xxxxxx xxxxx.
Xxxxxxxxx xxxxxxx v rámci xxxxx fototoxicity 3X3 XXX xx xxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxxxxx potenciálu xxxx xxxxxxxxx látky, xxxx xx xxxxxxxx, xxx xxxx xxxxx xx xxxxxxx x xxxxxxxx xxxxxxxxxxxxxx x xxxxxxxxxxx xxxxxx představuje možné xxxxxxxxx nebo xxxxxx.
Xxxxxxxxxxxxxx xxxxxxxxx testu in xxxxx xx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxx a xxxxxx, tímto xxxxxx xx xxxxx xxxxxxx xxxxxxxxxx, které xxxx xxxxxxxxxxx in vivo xx xxxxxxx xxxxxxxx x xxxxxxxxxx x xxxx, x xxxxxxxxxx, xxx xxxxxx xxxx xxxxxxxxxxxx xx topickém xxxxxxxx xx xxxxxxx.
Xxxx xxxxxxxxxxxx 3X3 XXX xx xxxxx xxx xxxxxxxxxx x xxxxxxxxx x rámci xxxxxxxxxx xxxxxxxx EU/COLIPA x xxx 1992 - 1997
6) xxxxxxx validní xxxxxxxxxxx in xxxxx xxxx xxxxxx xxxxxxxxxx xxxxxx xx xxxx. X roce 1996 xxxxxxxxxx xxxxxxxx schůze XXXX xxxxxxx xxxxxxxxxx xx xxxxx xxxxx xxx hodnocení xxxxxxxxxxxx.
6)Xxxxxxxx xxxxx xxxxxxxxxxxx 3T3 XXX xx xxxxx xxxx xxxxxxxxx x xxxxxxxx xxxxxx xxxxxxxxxxxx/xxxxxxxxxxx xx xxxx x xxxxxx x xxxx x xxxx xxxxxxxx, xx xxxxx test xx xxx xxxxxxx xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxx. Xxxx xxxx xxxxxxx k xxxx, xxx xxxxxxxxxxx xxxx xxxxxxxxxx xxxxxx, jež xxxxx z xxxxxxxxxxxxx xxxxxxxx xxxxx x xxxxxx xxxxxxxxx, xxxx xx fotogenotoxicita, xxxxxxxxxxx xxxx xxxxxxxxxxxxxxxxx, i xxxx xxxx xxxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx, xxxxxxx xxx xxxxx xxxxxxxxxxxx 3T3 XXX xx xxxxx xxxxxxxxx. Xxxx xxxx xxxxxx uspořádán xxx, xxx xxxxxxxxx hodnocení xxxxxx fototoxicity.
Sekvenční xxxxxxx xxxxxxxxx fototoxicity x xxxxxxxxxx xxxxx xx xxxxxxxx viz xxxxxxx.
1.3 Xxxxxxxx
Xxxxxxxxx: intenzita ultrafialového (XX) xx xxxxxxxxxxx xxxxxx xxxxxxxxxxxx xx xxxxxx; xxxxxx ve X/x2 xxxx x xX/xx2.
Xxxxx xxxxxx: xxxxxxxx (= xxxxxxxxx x xxx) xxxxxxxxxxxxxx (UV) xxxx xxxxxxxxxxx (VIS) xxxxxx xxxxxxxxxxxx na xxxxxx, xxxxxxxxx v xxxxxxx (= X x s) xx xxxxxxxx xxxxxxx, xxxx. X/x2 xxxx X/xx2.
Xxxxx xxxxxxxx xxxxx xxxxxxxxxxxxxx xxxxxx: xxxxx doporučení XXX (Xxxxxxxxxx Xxxxxxxxxxxxx xx X'Xxxxxxxxx) xx xxxxxxx xxxxxxxx XXX (315 - 400 xx), XXX (280 - 315 xx) x XXX (100 - 280 xxx). Xxxxxxxxx se x xxxx vymezení: za xxxxxxx mezi xxxxx XXX x XXX xx xxxxx považuje 320 nm x XXX xx xxxxx xxxx na XX-X1 x XX-X2 s xxxxxxx xxxxxx x 340 xxx.
Xxxxxxxxxxxxxxx (xxxxxxxxx) xxxxx: xxxxxxxx, xxxxxx xx xxxx xxxxxxx xxxxxxxx xxxxxxx populace (xxxx. xxxxxx barviva xxxxxxxxxxxx xxxxx buňku, xxxxxxxxx xxxxxxx, do xxxxxxxxx xxxxxxxx), xxx xxxxx xxxxxxxxx xxxxxxxx xxxxx xxxxxx x xxxx uspořádání koreluje x xxxxxxxx xxxxxx xxxx. xxxxxxxxxx (xxxxxxxxx) xxxxx.
Xxxxxxxxx životaschopnost (viabilita) xxxxx: životaschopnost xxxxx xxxxxxxxx x xxxxxxxxx x negativními xxxxxxxxxx (xxxxxxxxxxxx), které xxxxxx xxxxx procedurou xxxxx (xxx +UV xxxx -XX), xxxxx xxx xxxxxxxx testované látky.
Predikční xxxxx: xxxxxxxxxx, kterým xx výsledky testu xxxxxxxx xxxxxxxxxxxx xx xxxxxxxx toxického xxxxxxxxxx. X tomto xxxxxxxxxx xxxxxx pro test xx xxxxx x xxxxxxxxxxxx xxxxxxxx xxxxx xx xxxxxxxxxxxx 3X3 XXX xx vitro x predikci xxxxxxxxxxxxx xxxxxxxxxx použít xxxxxxx XXX x XXX.
XXX (xxxxx xxxxxxxxxx xxxxxx, xxxxxxxxxxxx faktor): xxxxxxxxxx xxxxxxxxxxxxx poměr 2 xxxxxx účinných cytotoxických xxxxxxxxxxx (EC50) xxxxxxxxx xxxxx xxxxxxxxx x xxxxxxxxxxxxx (-XX) a x xxxxxxxxxxx (+UV) xxxxxxxxxxxxxxx XXX/XXX xxxxxxx.
XXX (xxxx xxxxx xxxxxx, xxxxxxx fotoefekt): xxxx xxxx xxxxxxxx x xxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxx 2 xxxxxx xxxxxxxxxxx-xxxxxx xxxxxxxxx x xxxxxxxxxxxxx (-UV) x x xxxxxxxxxxx (+XX) xxxxxxxxxxxxxxx UVA/VS ozáření.
Fototoxicita: xxxxxx xxxxxxx xxxxxx (xxxxxx), xxxxx vzniká xx první expozicí xxxx xxxxxx xxxxx x následné xxxxxxxx xxxx xxxxxx, nebo xxxxxx, která xx xxxxxxx xxxxxxxx xxxxxxxx xxxx xx xxxxxxxxxx xxxxxx xxxxxx xxxxx.
Xxxxxxxxxxx: xxxxx úroveň xxxxx "xxxxxxxxxxxx", týkající xx xxxxx těch xxxxxxxxxxxxx xxxxxx, x nimž xxxxxxx v xxxx xxxx, xx na xx působí (topicky xxxx xxxxxx xxxxxxx) xxxxxx látka. Xxxx xxxxxxxxxxx xxxxxx xxxxx xxxx x xxxxxxxxxxxxxx xxxxxxxxx xxxxx (xxxxxx xxxxxxx jako xxx xxxxxxxxx slunění).
Fotoalergie: získaná xxxxxxxxxxxx xxxxxxxxxx, xxxxx xx xxx xxxxxx xxxxxxxx látky x xxxxxx neprojevuje, x xxx xx xxxxxxxxx xxxxxxxxxxxx až dvoutýdenní xxxxxxxx xxxxxxx x xxxx, aby se xxxxxxxxxx xxxx xxxxxxxxx.
Xxxxxxxxxxxxxxxx: xxxxxxxxxxx xxxxxx (xxxxxx) x xxxxxxxxxxx projevy, xx které dochází xxxx, xx byly xxxxx xxxxxxxxx negenotoxické xxxxx XXX/XX záření x xxxxxxxxxxxxx látky.
Fotokarcinogenita: xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxx světla x xxxxx. Xxxxx xx xxxxxxxxxxxx vyvolaná XX xxxxxxx zesílena látkou, xxxxxxx x xxxxxxxxxxxxxxxxxxx.
1.4 Xxxxxxxxxx xxxxx
Xxxxx xxxxxxxxxxxxxx xxxx látky xxx xxxxxxxxx kontrolu, xxxxx xx souběžně xxxxxxxxx xxx každé studii, xx xxx xxxxxxxx xxxxx xx fototoxicitu 3X3 XXX xxxxxxxxxx xxxxxx xxxx xxxxxxxxxx xxxxx xxxxxxxxx z xxxxx, které xxxx xxxxxxx xxx xxxxxxxxxxxxxxxx xxxxxxxxxxx xxxxxx xxxxx.
6)1.5 Xxxxxxx úvahy
Fototoxické xxxxxx xxxx pozorovány u xxxx xxxxx,
6) xxxxxxx xxxxxxx xxxxxxxxx xxxxx xx xx, že xxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxx xxxxxxxxxx záření. Xxxxx xxxxxxx xxxxxx xxxxxxxxxx (Xxxxxxxxxxx-Xxxxxxxx zákon) vyžaduje xxxxx xxxxxxxxxx dostatečnou xxxxxxxx xxxxxxxxxx xxxxx. Xxxxx xx xx xxxxxxx, xxx xx xxxxx uvažovat x xxxxxxxxxxx testování podle xxxxxx xxxxxxxxxxx xxxxxx, xxxx xxxx stanovit xxxxxxxxx spektrum xxxxxxxxx xxxxx x XXX/XXX xxxxxxx (xxxxxxxxx podle xxxxxxxx metody XXXX x. 101). Xxxxx xx molární xxxxxxxxx/xxxxxxxxx xxxxxxxxxx xxxxx xxx 10 xxxxx x xxx
-1 x cm
-1, xxxx látka fotoreaktivní xxxxxxxxx x není xxxxx ji xx xxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxx xxx xxxxxx xx xxxxxxxxxxxx 3T3 XXX xx vitro, xxx žádným xxxxx xxxxxxxxxxx testem (tabulka x. 9).
1.6 Xxxxxxx xxxxxx
Xxxx xxxxxxxx xxxxx xxxxxxxxxx, xxxxxxx může xxxxxxxx světla (xxxxxxxxx) xxxxxxxxxxx vyústit ve xxxxxxxxxxxx reakci,
6) xxxxxxx xxxxxxx xxxxx x xxxxxxxxx buněk. Proto xx test fototoxicity 3X3 XXX in xxxxx xxxxxxx na xxxxxxxxx cytotoxicity látky xxxxxxxxx v přítomnosti x nepřítomnosti necytotoxické xxxxx UVA/VIS záření. Xxxxxxxxxxxx xx xxx xxxxx testu xxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxx, neutrální xxxxxxx (xxxxxxx xxx, NR),
6) 24 xxxxx xx xxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxx.
Xxxxx Xxxx/x 3X3 xx xxxxxxxxx xx xxxx 24 xxxxx xxx, xxx xx xxxxxxxxx xxxxxxx xxxxx x jedné xxxxxx (xxxxxxxxx). Xxx xxxxxx testovanou xxxxx xx xxxxxxxxxxx dvě xxxxxxxx xx 96 xxxxxxx x látkou x xxxx různých xxxxxxxxxxxxx xx xxxx 1 xxxxxx. Jedna x xxxx destiček xx xxx xxxxxxx xxxxxxxxxxxxxxx XXX/XXX xxxxxx x xxxxx 5 X/xx2 XXX (+XX xxxxxxxxxx), xxxxx destička xx xxxxxxxx x xxxxx (-XX xxxxxxxxxx). X obou xxxxxxxxxx xx xxx médium xxxxxxx xxxxxx kultivačním x po xxxxxxx 24 xxxxxxxx xxxxxxxxx xx pomocí xxxxxxxxxxx xxxxxxxxx xxxxxxx (neutral xxx xxxxxx, NRU) xx dobu 3 xxxxx xxxxxxx xxxxxxxxxxxxxxx xxxxx. Xxx xxxxxx x osmi xxxxxxxxxxx xx stanoví relativní xxxxxxxxxxxxxxx buněk, vyjádřená xxxx procento hodnot x xxxxxxxxxxx kontrol. X xxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx se xxxxxxxxx xxxxxxxxxxxx závislé xxxxxx xxxxxxx v přítomnosti (+XX) x x xxxxxxxxxxxxx (-UV) xxxxxx, xxxxxxx na xxxxxx XX50, tj. při xxxxxxxxxxx inhibující životaschopnost xxxxx x 50 % v porovnání x xxxxxxxxxx xxx xxxxxxxxx.
1.7 Xxxxxxxx xxxxxxx
Xxxxxxxxx xxxxx xxxx xxxxxx XXX, xxxxxxxxxx údaje: x xxxxx xx xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxxx xxxx xxxxxx XXX. Buňky xx xxxxxx x xxxxxxx, která se xxxxxxx xxx testu xxxxxxxxxxxx 3X3 XXX xx xxxxx, xxxxxx xxx xx xxxxxxx xxxxxx XXX x xxxxx 1 - 9 J/cm2 x xxxxx xxx xx xxxxxx XXX xxxxxxx xxxxxxxxxxxxxxx xxxxx. Xxxxx xxxxxxx kritéria xxxxxxx, xxxxxxxx jejich xxxxxxxxxxxxxxx xx xxxxxxx dávkou XXX xxxxxx 5 X/xx2 není xxxxx xxx 80 % xxxxxxxxxxxxxxxx kontrolních xxxxxx xxxxxxxxxxxx v temnu. Xxx nejvyšší xxxxx XXX záření 9 X/xx2 xxxx být xxxxxxxxxxxxxxx xxxxx než 50 % xxxxxxxxxxxxxxxx xxxxxx xxxxxxxxxxxx x xxxxx. Tato xxxxxxxx xx xxxxxxx zhruba xx každé desáté xxxxxx xxxxx.
Xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxx xxxx xxxxxx XXX, běžný xxxx: xxxx xxxxxxx xxxxxxxx jakosti, jestliže xxxxxxxxx xxxxxxxx (xxxxx x Xxxxxxx vyváženém xxxxxx roztoku [Earl's xxxxxxxx xxxx xxxxxxxx, XXXX] s 1 % xxxxxxxx dimethylsulfoxidu (XXXX) nebo xxxxxxxx (XxXX) xxxx xxx xxxx xxxxxxxx v xxxxxxxxxxx (+UVA) xxxxxxxxxxxxxxx xxxxxxxxx 80% v xxxxxxxxx x neozářenými xxxxxxx x xxxx xxxxxxxxxxxx x xxxxx xxxxxxxxxx xxxxxxxxxxx x xxxxx (-XXX).
Xxxxxxxxxxxxxxx xxxxxxxxxxx xxxxxxx: xxxxxxxxx xxxxxxx xxxxxxx (XX540 NRU) xxxxxx v NR xxxxxxxx negativních kontrol xxxxxxx, xxx xxxxx 1 x 104 xxxxx xxxxxxxxxx x xxxxx xxxxx xxxxxx xxxxx xxxx dnů xxxxx x xxxxxxxx xxxxx zdvojnásobení. Test xxxxxxx xxxxxxxx akceptovatelnosti, xx-xx průměrná xxxxxxx XX540 XXX x xxxxxxx bez xxxxxxxxx xxxxx xxxx rovna 0,2.
Xxxxxxxxx xxxxxxxx: xxx xxxxxx xxxxx xx xxxxxxxxxxxx 3T3 XXX xx xxxxx xx xxxxx xxxxxxx xxxxxxxx xxxx xx známou xxxxxxxxxxxx xxxxxx. Xxx xxxxxxxxx xxxxxx XX/XXXXXX xxx xxxx xxxxx xxx pozitivní xxxxxxxx xxxxxx chlorpromazin (XXX); xxxxx xx xxxx xxxxx xxxxxxxxxx. Xxx XXX xxxxxxxxx xxx xxxxxxxxxxxx xxxxxxxxx v xxxxx xxxxxxxxxxxx 3X3 XXX in xxxxx xxxx xxxxxxxxxx tato xxxxxxxx akceptovatelnosti: CPZ xxxxxxx (+UVA): EC50 = 0,1 - 2,0 µx/xx, XXX xxxxxxxxx (-UVA): XX50 = 7,0 - 90,0 µg/ml. Fotoiritační xxxxxx (XXX), xxx. xxxxx xxxxxxx EC50, xx xxx xxxxxxxxx 6.
Xxxxx XXX xx xxx xxxxxxxxx xxxxxxxxx xxxxxxxx xxxx xxxxxx x jiné xxxxx xxxxxxxxxxx xxxxx, xxxxx xxxx xxxxxx xxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxx (xxxxxxxxx) xxxxx. V xxxxxxx případě je xxxxx xx xxxxxxx xxxxxxxxxxxx dat xxxxxxxxx xxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxxxxxx xxxxxxx xxxxxx XX50 x XXX xxxx XXX (xxxxxxx xxxxxxxxx).
1.8 Xxxxx xxxxxx
1.8.2 Xxxxxxxx
1.8.2.1 Buňky
Při validační xxxxxx xxxx použita xxxxxxxxxxxxx buněčná linie xxxxxx xxxxxxxxxxx Xxxx/x 3X3 xxxx 31, x xx xxx x XXXX xxxx x XXXXX; xx xx xxxxx xxxxxxxxxx. Xxxxx xxxxxxxx xxxxxxxxx xx xxxx x xxxxxxxx xxxxxx x xxxx buňky xxxx xxxxxxx linie, xxxxx xx kultivační xxxxxxxx xxxxxx xxxxx xxxxxx xxxxxxxxxxxx xxxxxx; xx xxxx xxxxx xxxxxxxx, xx jsou xxxxxx xxxxxx.
X buněk xx xxxxx xxxxxxxxxx xxxxxxxxxxx, xx nejsou xxxxxxxxxxxxx xxxxxxxxxxxx, x smí xx xxxxxx jen x případě, že xx výsledek xxxxxxxx xxxxxxxxxx.
Xxxxxxx xxxxxxxxx xxxxx xxxx XXX xxxxxx xxxx x xxxxxx xxxxxx xxxxxxxx, je xxxxx xxxxxxxx xxxxx Xxxx/x 3X3 z xxxxxx x nejnižším xxxxxx, xxxxx xxxxx xxxxxx xxx 100. Xxxxxxxxx xxxxx Balb/c 3X3 xxxx XXX xxxxxx je xxxxx xxxxxxxxxx xxxxxxxxxxx, x xx xxxxxxxx xxxxxxxx xxxxxxx popsaným v xxxxx metodickém xxxxxx.
1.8.2. Xxxxx a xxxxxxxxxx xxxxxxxx
Xxx rutinní pasážování xxxxx x během xxxxxxx je xxxxx xxxxxxxx xxxxxx xxxxxxxxxx xxxxx x xxxxxxxxx xxxxxxxx. X xxxxxxx xxxxx Xxxx/x 3T3 xx jedná x XXXX (Xxxxxxxxxx xxxxxxxxxx Xxxxxxxx xxxxx) xxxxxxxxx 10 % xxxx xxxxxxxxxxxx xxxxx, 4 xX xxxxxxxxx, xxxxxxxxxxx x xxxxxxxxxxxxxx a x xxxxxxxx xx xxxxxx prostředí při xxxxxxx 37 °C/7,5 % CO2. Je xxxxxxxx, aby xxxxxxxx xxxxxxxxx zajišťovaly xxxxxxx xxxxxx x normálním xxxxxxxxxxx xxxxxxx xxx xxxx xxxxx xxxx. xxxxxxxx xxxxx.
1.8.2.3 Příprava xxxxxx
Xxxxx xx zmražených xxxxxxxxx xxxxxx se xxxxxx x xxxxxxxxx xxxxxxx x xxxxxxxxxxx xxxxx a xxxxxxxxx xxxxxx xx xxxx xxxxxxxx v xxxxx xx xxxxxxxxxxxx 3X3 XXX in vitro xxxxxxxx.
Xxx xxxx xxxxxxxxxxxx xx xxxxx nasadí x xxxxxxxxxxx xxxxx x xxxxxx xxxxxxx, xxx na konci xxxxx (xx. xxx xx xxxxxxxxx xxxxxxxxxxxxxxx xxxxx 48 hodin xx nasazení) xxxxxxx xx konfluenci (ke xxxxxxxx v xxxxxxxxx, xxxxxxxxxx xxxxxx xxxxx). X případě xxxxx Xxxx/x 3X3 xxxxxxxxxxxxx x xxxxxxxxxx x 96 xxxxxxx se xxxxxxxxxx xxxxxxx 1 x 104 buněk x xxxxx jamce.
Pro xxxxxx testovanou xxxxx xx xxxxx xxxxxxxx xxxxxxxxx xx xxx xxxxxxxx s 96 xxxxxxx, které xxx xxxxxxxxxx xxxxx xxxxxxxx xx identických kultivačních xxxxxxxx, s xxxxxxxx xxxx, xxx xx xxxxx x destiček xxxxxxxxx (+UVA/VIS) a xxxxx je uchovávána x xxxxx (-XXX/XXX).
1.8.2.4 Xxxxxxxxxxx aktivace
Zatímco xxx xxxxx testech in xxxxx xxx xxxxxxxxx xxxxxxxxxxxxx nebo xxxxxxxxxxxxxx xxxxxxxxxx je xxxxxxx xxxxxxxxxx použití xxxxxxxxxxxxxxxx xxxxxxx, xxxx v xxxxxxx xxxxxxxxxxxxxxx xxxxx xxxxx xxxxx, xxx xx k xxxx, xxx xxxxxxxx xxxx xxxxxxxxx xx xxxx xxxx xx vitro, xxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx. Xxxxxxxxx xx xxxxx xxx xx xxxxx, xxx xx xxxxxxx odůvodněné, aby xx xxxxx test xxxxxxxx x nějakým xxxxxxxxxxxx aktivačním systémem.
1.8.2.5 Xxxxxxxxx xxxxx/xxxxxxxx
Xxxxxxxxx xxxxx xxxx být xxxx xxxxxxxx xxxxxxx připravena, xxxxxx xxxxx x xxxx xxxxxxxxx xxxxxxxxx, xx se xx xxxxxxxxx. Xxxxx xx xxxxxxxxxxxxx, že xx xxxxx k fotodegradaci, xxxx xx příprava xxxxxxxx xxx xxxxxxxx xxxxxxx.
Xxxxx xx rozpustí x xxxxxxxxxx xxxxxx xxxxxxx, xxxxxxxxx x Xxxxxxx vyváženém xxxxxx xxxxxxx (EBSS) xxxx xx xxxxxxxxxxxxx roztoku xxxxxxxxxx xxxxxxxx (xxxxxxxxx xxxxxxxx saline, XXX), xxxxx - xxx xxxxxxx dojít x xxxxxxxxxxxx xxxxx ozařování - xxxxx xxxxxxxxx xxxxx xxxxxxxxxx xxxxxx xxx xxxxxxx xxxxxxxxxx xX, xxxxxxxxxx xxxxxx.
Xxxxx xx xxxxxxxxx xxxxx xx xxxx xxxxxxx xxxxxxxxx, xxxxxxxx xx xx xxxxxxx rozpouštědle x xxxxxxxxxxx stonásobně xxxxx, xxx xx xxxxxxxxxx xxxxxxx xxxxxxxxxxx, x xxxxxxxx xx xxxxx x poměru 1 - 100 xxxxxxxxxx solným xxxxxxxx. Xxxxx xx používá xxxxxxxxxxxx, xxxx xxx xxxxxxxx x konstantním xxxxxx 1 % (x/x) ve xxxxx xxxxxxxxx, tj. ve xxxxx koncentracích testované xxxxx x x xxxxxxxxxxx xxxxxxxxxx.
Xxxx xxxxxxxxxxxx xx xxxxxxxxxx xxxxxxxxxxxxxxxx (XXXX) nebo xxxxxxx (XxXX). Xxxxxx mohou xxx x xxxxx xxxxxxxxxxxx s xxxxxx xxxxxxxxxxxxx, xxxxxxxxx aceton, xx však xxxxx xxxx xxxxxxx xxxxxx xxxxxx specifické vlastnosti, xxxx je xxxxxxxx xxxxxx x xxxxxxxxxx xxxxxx, xxxxxxxxx fototoxického xxxxxx xxxx xxxxxxxxxxx xxxxxxxx.
Xxx xx xxxxxxxxx xxxxxxxxxxx, xx xx xxxxxx xxxxxxx xxxx. xxxxxxxxxx, xxxxxxxxx xxxxx xx 37°C.
1.8.2.6 0zařování XX xxxxxxx/xxxxxxxx
Xxxxxxxx xxxxx: xxxxx xxxxxxxxx xxxxxxxxxx xxxxxx a správná xxxxxxxx xx xxx xxxxxxxxx fototoxicity xxxxxxxx xxxxxxxx. Xxxxxx x XXX a xx xxxxxxxxx xxxxxxx xx xxxxxxx spojováno s xxxxxxxxxxxxxxxxx,
6) kdežto záření XXX xx x xxxxx xxxxx xxxx xxxxxxxxxx, je přímo xxxxxx xxxxxxxxxxx, xxxxxxx xxxx cytotoxicita xx xxx přechodu od 313 nm x 280 xx zvyšuje xxxxxxxxxxxxx.
6) Xxxx kritéria xxx xxxxx světelného xxxxxx xxxxx xxxxxxx xxxxxxxxx, xxx emitoval xxxxxx xxxxx, xxx xxxxxxxxx látka xxxxxxxxx, x xxx xxxx xxxxxxxx xxxxx (dosažitelná xx přiměřenou dobu) xxxxxxxxxxx xx xxxxxxxx xxxxxxx fotosenzibilizujících xxxxx. Xxxx nesmějí být xxxxxxx xxxxxx xxxxx x xxxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxx - xxxxx xxx x xxxxxxxxxx xxxxx (xxxxxxxxxxxx oblast).
Za optimální xxxxxxxx xxxxx xx xxxxxxxxx xxxxxxx simulátory, xxxxx xx simuluje xxxxxxxx xxxxxx. Xxxx xxxx xxxxxxxxxx xx xxxxxxxxx xxxxxxxx xxxxxxx x dále (vysokotlaké) xxxxxxx halogenové výbojky - ty xxxx xx xxxxxx, xx xxxxxxxx xxxx xxxxx x xxxx levnější, xxxxxxxx xxxxxx xxxx xxxxxxx xxxx. Xxxxxxx xxxxxxx solární simulátory xxxxxxx xxxxxxxx xxxxxxxx xxxxxx XXX, je xxxxx xxxxxx xxxxxxxxx xxx, xxx xx xxxx xxxxxx cytotoxické xxxxxx xxxxxxxxxx xxxxxxxxx.
Xxx xxxx xx xxxxxxxxxxxx 3X3 XXX xx xxxxx xx třeba xxxxxx xxxxxxxx záření, xxx se xxxxxx XXX prakticky xxxxxxxxxxx (XXX:XXX ~ 20: 1). Příklad xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx záření xxxxxxxxx xxxxxxxxxx xxxxxxxxx xxx xxxxxxxxx studii xxxxx xx xxxxxxxxxxxx 3X3 XXX xx xxxxx xxx publikován.
6)Dozimetrie: xxxxxxxxx xxxxxx (xxxxxxxxx) xx musí xxxxxxxxxx xxxx xxxxxx xxxxxx xxxxxxxxxxxx kontrolovat xxxxxx xxxxxxxx xxxxxxxxxxxxxxx UV-metru, xxxxx xxxx být xxxxxxxxxx xxx xxxx xxxxx. Xxxxxxxxx XX-xxxxx xx třeba xxxxxxxxxxx, x čemuž se xxxxxxxxxx použít xxxxx, xxxxxxxxxx UV-metr xxxxx xxxx x xxxxxxxxx. Xxxxxxx xx, xxxx xx v delších xxxxxxxxxxx měří xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxx a xxxxxxxxxx xx xxxxxxxxx širokopásmového XX-xxxxx xxxxxx spektroradiometru; xxxxxx instrumentace xxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx.
Xxx validační xxxxxx bylo xxxxxxxx, xx dávka XXX xxxxxx 5 X/x2 xx xxx xxxxx Xxxx/x 3X3 xxxxxxxxxxxxx x xxxxxx dostatečně xxxxx, aby xxxxxxxxxx x slabě xxxxxxxxxxx xxxxx. Aby xx xxxx dávky xxxxxxx xxxxx 50 xxxxx, xxxx xxx xxxxxxxxx xxxxxxxxx na 1,666 xX/xx2. Xxxxxxx-xx xx xxxx xxxxxxx xxxxx xxxx xxxx zdroj xxxxxx, xxxx xx xxxxx xxxxxx XXX xxxxxxx tak, xxx xxxxx nepoškozovala x xxxx dostatečná x xxxxxxx standardních xxxxxxxxxx. Xxxx xxxxxxxx xxxxxxxx xx xxxxxxxxxx podle xxxxxx:
xxxxx xxxxxxxxxx xxxxxx (X/xx2 x 1000) (1 X = 1 X.x)
x (xxx) = ___________________________________
xxxxxxxxx xxxxxxx (xX/xx2 x 60)
1.8.3 Xxxxxxxx xxxxx
Xxxxxxxxx koncentrace xxxxxxxxx látky xxxx xxxxxxxx xxxxxxx 100 µx/xx, xxxxx xxxxxxx xxxxxxxxxxx látky xxxx xxxxxxxxxx při xxxxxxxxxxxxx xxxxxxx, xxx xxxxxxx xxxxxxxxxxxxx se xxxxxxx xxxxxxx falešně xxxxxxxxxxx xxxxxxxx.
6) Hodnota xX xxx nejvyšší koncentraci xxxxxxxxx xxxxx musí xxx přijatelná (xxxxxx xX 6,5 - 7,8).
Xxxxxx koncentrací xxxxxxxxx xxxxx při xxxxxxx xxxxxx (+XXX) x xxx xxx (-XXX) xx xxxxx stanovit x rámci předběžných xxxxxxxxxxx. Rozsah x xxxxxx xxxxxxxxxxxx řady xx xxxxx xxx, xxx xxxxxx závislosti xxxxxxxxxxx-xxxxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxxxx xxxxx. Xxxxxxx se xxxxxxxxxxxx xxxxxxxxxxx řada (s xxxxxxxxxxx xxxxxxxx xxxxxx).
1.8.4 Xxxxx xxxxxxx
1.8.4.1 Xxxxx xxx
Xxxxxxxx xx suspenze 1 x 105 xxxxx/xx v xxxxxxxxxxx xxxxx. Xx xxxxxxxxxxx xxxxx 96 jamkové xxxxxxxxxxxxx destičky xxx xxxxxxx kultury xx xxxxxxxxxx xx 100 µx xxxxxxxxx xxxxx (= xxxxx xxxxx), xx xxxxxxxxx jamek xx xxxxxxx po 100 µx xxxxxxx xxxxxxxx o xxxxxxx 1 x 105 xxxxx/xx (=1 x 104 xxxxx xx xxxxx). Xxx xxxxxx xxxxxxxxxx xxxxx se xxxxxxxx dvě destičky - xxxxx pro xxxxxxxxx xxxxxxxxxxxx (-XXX), xxxxx xxx xxxxxxxxx xxxxxxxxxxxxxxxx (+UVA).
Buňky xx xxxxxxxx po xxxx 24 xxxxx (7,5 % XX2, 37 °X), xxx xx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx. Xxxx inkubační xxxx xxxxxxxx regeneraci x xxxxxxxxx xxxxx x xxxxxx xxxxxxxxxxxxx xxxx.
1.8.4.2 Xxxxx xxx
Xx xxxxxxxx xx kultivační xxxxxx x buněk xxxxxxxx x xxxxxxx xxxxxxx xxxxxxx 150 µx XXXX/XXX xx xxxxxx xxxxx. Přidá xx 100 µx XXXX/XXX xxxxxxxxxxxx xxxxxxxxxx látku x příslušné koncentraci xxxx xxxxx xxxxxxxxxxxx (xxxxxxxxx xxxxxxxx). Testovaná xxxxx se xxxxxxx x 8 koncentracích. Xxxxx x testovanou xxxxxx se xxxxxxxx x temnu xx xxxx 60 xxxxx (7,5 % CO2, 37 °X).
Xxxx xxxxx x XXX (+XXX) xx xxxxxxx xxx, xx se buňky xx xxxxxxxx xxxxxxx xxxxxxx po dobu 50 xxxxx skrz xxxxx xxxxxxxx x 96 xxxxxxx xxxxxxx XXX x xxxxxxxxx 1,7 xX/xx2 (= xxxxx 5 X/xx2). Xxx nedocházelo ke xxxxxxxxxx vody xxx xxxxxx, xx třeba xxxxxx xxxxxxxxxxx. Xxxxxxxxxx xxxxxxxx (-XXX) xx xx dobu 50 xxxxx (= xxxxxxxxx xxxx UVA) xxxxxxxxxx xx xxxxxxxx xxxxxxx x xxxxxx xxxx.
Xxxxxx xx odstraní a xxxxx xx promyjí xxxxxxx 150 µx XXXX/XXX. Xxxx xx xxxxxx xxxxxxxxxxx médiem x xxxx xxx (18 - 22 xxxxx) xx inkubují (7,5 % CO2, 37 °X).
1.8.4.3 Třetí xxx
Xxxxxxxxxxxxx xxxxxxxxx
Xxxxx se xxxxxxxxxx xxx xxxxxxxxxxx x xxxxxxx kontrastem. Xxxxxxxxxxx se změny xxxxxxxxxx buněk xxxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxx. Tato kontrola xx xxxxxxxxxx, xxx xx eliminovaly xxxxxxxxxxxxxx xxxxx, ale xxx xxxxxxxxxxxxx xxxxxxxxxxxx xxxx xxxxxxxxxxxx xx tyto xxxxxxx xxxxxxxxx.
Xxxx xxxxxx xxxxxxxxx xxxxxxx (NR)
Buňky xx xxxxxxx objemem 150 µl xxxxxxxxxxxx XXXX/XXX.. Xxxxxxxxx xxxxxx xx xxxxxxxx xxxxxx xxxxxxxx. Xxxxx xx 100 µx xxxxx x NR x xxxxxxxx xx xxx 37 °C xx xxxxxxxx xxxxxxxxx x 7,5 % CO2 xx dobu 3 xxxxx.
Xx inkubaci se xxxxxx x NR xxxxxxxx x xxxxx xx promyjí objemem 150 µl XXXX/XXX, xxxx se pak xxxxx a důkladně xxxxxxxx (xx také xxxxx xxxxxxxx xxxxxxxxxxxxxx x xxxxxxxx xxxxxx).
Xxxxx xx přesně 150 µx xxxxxxx xx xxxxxxxx NR (xxxxxxx xxxxxxxxxx xxxx xxxxxxx/ xxxxxxxx xxxxxx).
Xxxxxxxxxxxxx destičky xx xx xxxx 10 xxxxx xxxxxx xxxxxx xx xxxxxxxx, xxxxx se XX x xxxxx xxxxxxxxxxxxx x xxxxxxxxx xx xxxxxxxxx xxxxxx.
Xx xxxxxxxxxxxxxxxx xx změří xxxxxxx xxxxxxx xxxxxxxx NR xxx 540 xx xx použití xxxxxxx xxxxxx jako srovnávacího xxxxxxx. Xxxxx xx xxxxxxxx ve xxxxxxx xxxxxxx (např. ASCII) xxx xxxxx analýzu.
2 XXXXX
2.2 Kvalita x xxxxxxxx údajů
Údaje xxxx xxxxxxxxx xxxxxxxxxxx analýzu xxxxxx xxxxxxxxxxx-xxxxxx při xxxxxxxx XXX/XXX xxxxxx x bez xx. Xx-xx zjištěna cytotoxicita, xxxxxxxxxxxx xxxxxx x xxxxxx xxxxxxxxxxxx xxxxxxxxxxx xx nastaví xxx, xxx xx xxxxxxxxxxxxxx xxxxx daly xxxxxxxx xxxxxxx. Xxxxxxx xxxxxxxxx xxxxx xxxx být xx do xxxxxxxxxx xxxxxxx xxxxxxxxxxx 100 µx/xx x xxxxxxxxxxx xx xxx (-UVA) xxxxxxxxxxxxx, xxx xxx xxxxxxxxx (+UVA) vysoce xxxxxxxxxxx, může xxxxx x xxxx, xx xx xxxxxxxxxxxx xxxxxxx x xxxx xxxxxxx xxxxxxxxxxx xxxxx muset xxxxxx xxxxx, xxx xxx splněn požadavek xxxxxxxxx xxxxxxx dat. Xxxxx xxxx xxxxxxxxxxxx xxxxxxxx v xxxxx x obou xxxxx xxxxxxxxxxx (xxx xxx -XXX, xxx při +XXX), xxxxxxxxx xxxxxxxxx x velkým xxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxx xx xx xxxxxxxx xxxxxxxxxxx.
Xxxx-xx xxxxxxxx hraniční - xxxxxx xxxxxx xxxx predikčního xxxxxx - xx třeba xxxx xxx xxxxxxx xxxxxxxx.
Xxxxxxxx-xx xx xxxxxxxxx xxxxx za potřebné, xxxx být xxxxxxxx xxxxxxxx xxxxxxxxxxxxxx podmínky, xxx se xxxxxxx xxxxxxx výsledku. Xxxxxxxx xxxxxxxxx v tomto xxxxx xx příprava xxxxxxx xxxxxxxxx látky, xxxxxxxxxxxx xxx jeho xxxxxxxxx je xxxxxxx xxxxxx xxxxxxxx (spolurozpouštědlo, xxxxxxxxx, xxxxxxxxxx). Xxx xxxx xxxxxxxx x xxxxxxx xxxxxxxxx doby xxxx xxxxxxxxxx. X xxxxx, xxx xxxx xx vodě nestálé, xxxx xxx xxxxxxxx xxxx zkrácení doby.
2.3 Xxxxxxxxxx xxxxxxxx
Xxxxx xx xx možné, stanoví xx xxxxxxxxxxx xxxxxxxxx xxxxx vedoucí k 50 % xxxxxxxx xxxxxxxxx xxxxxx XX (XX
50). Xx xxx xxxxxx tak, xx xx xx data xxxxxxxxxxx-xxxxxx použije xxxxxxxxx xxxxxx xxxxxx xxxxxxxxxx xxxxxxx (nejlépe Hillova xxxxxx xxxx logistická xxxxxxx) xxxx se xxxxxxx xxxx xxxxxx xxxxxx xxxxxxxxx.
6) Xxx xx hodnota XX
50 xxxxxxx pro xxxxx xxxxxxx, xx třeba xxxxxxxxxxxx kvalitu proložení. X xxxxxxx xxxxxxx XX
50 xx také xxxxx xxxxxx xxxxxxxx xxxxxx. V xxxxx xxxxxxx se xxxxxxxxxx xxxxxx pravděpodobnostní papír (xxx x: log, xxx x: probit), xxxxxxx po této xxxxxxxxxxxx bývá xxxxxx xxxxxxxxxxx-xxxxxx xxxxxx téměř xxxxxxxx.
2.4 Xxxxxxxxxxx xxxxxxxx (xxxxxxxxx modely)
2.4.2 Xxxxxxxxx xxxxx, xxxxx 1: xxxxxxxxxxxx faktor (XXX)
Xxxxx xx xxxxxxx úplné xxxxxx xxxxxxxxxxx-xxxxxx xxx xx přítomnosti (+XXX), xxx xx xxxxxxxxxxxxx (-XXX) xxxxxx, xx xxxxxxxxxxxx xxxxxx (XXX) xxxxxxxx xxxxx xxxxxx
&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx; XX50 (-XX)
XXX = _____________
&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx; XX50 (+UV)
PIF &xx; 5, nepředpovídá xxxxx fototoxický xxxxxxxxx, xxxxxx PIF ≥ 5 fototoxický xxxxxxxxx xxxxxxxxxx.
Xx-xx xxxxx cytotoxická xxxxx xxx +XXX, xxxxxx při -UVA xx xxxxxxxxxxxxx, xxxx xx PIF xxxxxxxxx, x když se xxxxx x výsledek, xxxxx xxxxxxxx, xx xxxxx xx xxxxxxxxxxx xxxxxxxxx. V xxxxxxx xxxxxxx xx xx xxxxxxxxx xx. "> XXX", xxxx se xxxx xxxxxxxxxxxx (-UV) xxxxxxx až po xxxxxxxxx zkušební xxxxxxxxxxx (Xxxx) a tato xxxxxxx xx xxxxxx xx xxxxxx:
&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx; Xxxx (-XX)
&xx; XXX = ___________
&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx; EC50 (+XX)
Xxxxx xx dá vypočítat xxxxx "&xx;XXX", xxx xxxxx xxxxxxx &xx; 1 předpovídá xxxxxxxxxxx xxxxxxxxx.
Xxxxxxxx se xxxx xxxxxxxxx ani XX50 (-XX), ani XX50 (+XX), xxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxxxx až xx xxxxxxxx zkušební xxxxxxxxxxx, xx xx xxxxxxxx xxxx, xx xxxxx nemá žádný xxxxxxxxxxx potenciál. V xxxxxxx xxxxxxx se xxxxxxx formální "PIF = * 1", xxxx se xxxxxxxxxxxxxx xxxxxxxx
&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx; Xxxx (-UV)
PIF = *1 = _________________
&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx;&xxxx; Xxxx (+XX)
Xxxxx xx dá získat xxxxx xxxxxxx "XXX = * 1", xxxxxxxxxx to, že xxxx xxxxxxxx žádný xxxxxxxxxxx xxxxxxxxx.
X xxxxxxxxx (x) x (x) xx xxxxx xxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxx xxxxxxx x xxxxx koncentrace, xxxxx xx při testu xxxxxxx.
2.4.3 Predikční xxxxx, xxxxx 2: xxxxxxx xxxxxxxxx (XXX)
Xx xxxxx xxxx xxxxxx xxxxxxx xxxxx xxxxxx xxx xxxxxxxx xxxxxxxxxxxxx potenciálu, xxxxxxxxxxxxx xx xxxxxxx xxx z xxxxxxxxx xxxxxx XX/XXXXXX
6) a xxxxxxxxxxxx xx podmínek xxxxx xxxxxx stanovení xxxxxxxxxxxx xx vitro x xxxxx XX xxxxxx.
6) X tomto xxxxxx xxxx xxxxxxxxx xxxxxxx xxxxxx PIF x xxxx xxxxxxxxx, xxx xxxxx xxxxxx xxxxxxx XX
50. X xxxxx xxxxxx xx xxxxxxx veličina "xxxxxxx xxxxxxxxx" (MPE) založená xx porovnání xxxxxx xxxxxxx xxxxxx xxxxxxxxxxx-xxxxxx. Xxx xxxxxxxx xxxxxx XXX xxx xx Xxxxxxxxxxx univerzitě v Xxxxxxx vyvinut xxxxxxxxx xxxxxxxxxx software, xxxxx xxx xxxxxxx xxxxxx.
2.5 Xxxxxxxxxxxx xxxxxxxx
Xxxxxxxxx xxxxxxxx xxxxx (XXX ≥ 5 xxxx XXX ≥ 0,1) ukazuje, xx xxxx xxxxx xx xxxxxxxxxxx potenciál. Xxxxx se x xxxxxx výsledku xxxxx xxx xxxxxxxxxxxxx nižších xxx 10 µx/xx, xx xxxxxxxxxxxxx, xx xxxxx bude xxxxxxx xxxx xxxxxxxxx také xx xxxxxxx expozičních xxxxxxxx xx xxxx. Xxxxx-xx se xxxxxxxxx xxxxxxxx pouze xxx xxxxxxxx xxxxxxxx xxxxxxxxxxx (100 µg/ml), bude xxx xxxxxxxxx xxxxxxxxxxxxx xxxx fototoxické xxxxxxxxxx xxxx látky xxxxxxxx xxxxxxxxx dalších informací. Xxx xxxxx xxxxxx xxxxxxxxx o penetraci, xxxxxxxx x možné xxxxxxxxx látky v xxxx, nebo xxxxx x testování xxxx xxxxx v xxxxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxx, xxxxxxxxx xx xxxxxxx xxxxxx xxxxxx kůže xx xxxxx.
Xxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxx 3X3 XXX xx xxxxx (XXX &xx; 5 xxxx MPE &xx; 0,1) ukazuje, xx xxxxxxxxx xxxxx není xxxxxxxxxxx pro použité xxxxx buňky x xxxxxx xxxxxxxxxx. V xxxxxxxxx, xxx by xx látka xxxx xxxxxxxx i xxx xxxxxxxx koncentraci 100 µx/xx, xxxxxxxxx xxxxxxxx xxxxxxx, xx xxxxx xxxx žádný xxxxxxxxxxx xxxxxxxxx x xxxxxxxxxxxx xx xxxx xx xx považovat xx xxxxxxxxxxxxxxxx. X případech, xxx xxxx xxx xxxxxxx xxxxxxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxx (XX50 +XX x EC50 -XX), je xxxxxxxxxxxx xxx xxxxxx. Naproti xxxx xxxxx xxxxxx xxxxxxxxx xxxxx xxxxxxxx (+XX xxx -XX) x pro omezenou xxxxxxxxxxx xxxxx xx xxxxxx xxxxxxxxx koncentrace 100 µx/xx, xx xxxxx xxxxxxxxx tento xxxx pro danou xxxxx xx xx xxxxx xxxxxx a xxxx by xx xxxxxxxx o jiném, xxxxxxxxxxxx xxxxx (xxxxxxxxx x xxxxxxxx xxxxxx xxxx xx vitro xxxx xxxxxx xxxx xx xxxx xxxx xxxx xx xxxx).
3 XXXXXXX POKUSU, XXXXXXXX XXXXXX A XXXXXXXXX XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx předpisy
9) xxxx xxx xxxxxxxxx xxxxxxx xxxxxx a x xxxxxxx pokusu xx xxxxx xxxx xxxxxxxx.
Xx zprávě o xxxxxxx pokusu xx xxxxx xxxxx xxxx xxxxxxxxx:
Xxxxxxxxx xxxxx:
- xxxxxxxxxxxxx xxxxx x xxxxx XXX, je-li známo,
- xxxxxxxxx xxxxxx a xxxxxxx,
- xxxxxxxxx-xxxxxxxx xxxxxxxxxx, xxx xxxx x xxxxxxxxx xxxxx xxxxxxxx,
- xxxxxxxxx x fotostabilita, xxxx-xx xxxxx.
Xxxxxxxxxxxx:
- zdůvodnění xxxxx xxxxxx rozpouštědla,
- xxxxxxxxxxx xxxxxxxxx xxxxx x xxxxx xxxxxxxxxxxx,
- xxxxxxxxxxx xxxxx xxxxxxxxxxxx x xxxxxxxxx médiu (XXXX xxxx XXX).
Xxxxx:
- xxx x xxxxx xxxxx,
- xxxxxxxxxxxx xxxxxxxxxxx,
- xxxxx xxxxxxx xxxxxx, xx-xx xxxxx,
- citlivost xxxxx vůči záření XXX xxxxxxxxx pomocí xxxxxxxxxxx xxxxxxxx, xxx xx x testu xx xxxxxxxxxxxx 3X XXX in xxxxx xxxxxxx.
Xxxxxxxx pokusu (x) - xxxxxxxx xxxx xxxxxxxxxx x xx xxx:
- xxx a xxxxxxx kultivačního média,
- xxxxxxxx xxxxxxxx (xxxxxxxxxxx XX2, xxxxxxx, xxxxxxx),
- xxxx xxxxxxxx (zpracování xxxx ní a xx xx),
- popis x zdůvodnění jakýchkoli xxxx
Xxxxxxxx pokusu (x) - xxxxxxxxx látkou.
- xxxxxxxxxx volby xxxxxxxxxxx xxxxxxxxx xxxxx, které xx xxxxxxx x xxxxxxxxxxx xxxxxxxxx XX/XXX xxxxxxx x bez xxx,
- x případě xxxxxxx xxxxxxxxxxxx testované xxxxx x xxxxxxx xxxxxxxxxxxx zdůvodnění xxxxxxxx xxxxxxxxx koncentrace,
- typ x xxxxxxx působícího xxxxx (pufrovaný xxxxx xxxxxx),
- xxxx xxxxxxxxxxx xxxxxx.
Xxxxxxxx xxxxxx (c) -xxxxxxxxx:
- xxxxxxxxxx xxxxx xxxxxx xxxxxxxxxx zdroje,
- xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxxxxxxxx zdroje,
- xxxxxxxxxxxxxxx xxxxxxxxxxxx/xxxxxxxx xxxxxxxxx xxxxxx (xxxxxx),
- charakteristika xxxxxxxxxx x xxxxxxxxxxx x xxxx xxxxxxxxx,
- xxxxxxxxxx xxxxxxxxxx zdroje xx xxxxxxxxxxx xxxxxxx,
- iradiace XXX (x xX/xx2) xxx xxxx vzdálenosti,
- xxxx xxxxxxxx UV/VIS xxxxxx,
- xxxxx záření XXX (xxxxxxxx x xxx) x X/xx2,
- xxxxxxx buněčných xxxxxx xxxxx ozařování a xxxxxx souběžně xxxxxxxxxxxx x xxxxx.
Xxxxxxxx xxxxxx (x) - xxxx XXX:
- xxxxxxx média x XX,
- xxxx xxxxxxxx x XX,
- xxxxxxxxx xxxxxxxx (koncentrace XX2, xxxxxxx, xxxxxxx),
- xxxxxxxx xxxxxxxx XX (xxxxxxxxx činidlo, doba xxxxxxxx),
- xxxxxx xxxxx, xxx xxxxx se xxxxxxxxxxxxxxxxxxx odečítala xxxxxxx xxxxxxx XX,
- druhá xxxxxx délka (xxxxxxxxxx), xxxx-xx použita,
- xxxxxxx xxxxxxxxxxxx xxxxxxx pro xxxxxxxxxxxxxxxxx (xxxxxx), xxxxx xxx použit.
Výsledky:
- xxxxxxxxxxxxxxx xxxxx xxx xxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxx, xxxxxxxxx x xxxxxxxxxx xxxx xxxxxxxx xxxxxxxxxxxxxxxx xxxxxxx,
- xxxxxx xxxxxxxxxxx-xxxxxx (xxxxxxxxxxx xxxxxxxxx xxxxx xx relativní xxxxxxxxxxxxxxx xxxxx) xxxxxxx xxxxxxxxxx xxxxxxxxxxx +XXX x -XXX,
- analýza křivek xxxxxxxxxxx-xxxxxx: xxxxx xxxxxxxx xxxxxxx hodnot EC50 (+XXX) x XX50 (-XXX),
- porovnání xxxx xxxxxx xxxxxxxxxxx-xxxxxx xxxxxxxxx xx xxxxxxx xxxxxxxxx XX/XXX světlem - xxxxxxxx buď xxxxxxxxxxxxxx xxxxxxx (XXX) xxxx xxxxxxxxx fotoefektu (MPE),
- xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx,
- xxxxxxxx akceptovatelnosti xxxxx (x) - xxxxxxxx xxxxxxxxx xxxxxxxx:
- xxxxxxxxx xxxxxxxxxxxxxxx (optická denzita xxxxxxxx XX) xxxxxxxxx x xxxxxxxxxxx buněk,
- xxxxxxxxxx údaje negativních xxxxxxx, xxxxxx x xxxxxxxxxx odchylka,
- xxxxxxxx xxxxxxxxxxxxxxxxx xxxxx (x) - souběžná xxxxxxxxx xxxxxxxx:
- hodnoty XX50 (+XXX), XX50 (-UVA) x PIF látky xxxxxxx xxx xxxxxxxxx xxxxxxxx,
- historické údaje xxxxx použité pro xxxxxxxxx kontrolu: hodnoty XX50 (+XXX), EC50 (-XXX) x XXX, xxxxxxx x xxxxxxxxxx xxxxxxxx.
Xxxxxxx xxxxxxxx.
Xxxxxx.
Xxxxxxx x. 9
X.42 SENZIBILIZACE XXXX: XXXXXXX X XXXXXXXXXX XXXXXXXXX XXXXXXXXXXXX XXXXX
1 XXXXXX je x xxxxxxx x právem Xxxxxxxxxx xxxxxxxxxxxx
7a).
1.1 XXXX
Xxxxxxx x xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx uzlin (XXXX) xxxx xxxxxxxxxx xxxxxxxxxx x uznána, xxx xxxxxxxxx její xxxxxxx xxxx nové xxxxxx
7a). Xxxxx xx o xxxxxx xxxxxx xxxxxxxx xx xxxxxxxxx zvířatech xxxxxxxxx na xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxxxxxx kůži. Xxxxx xxxxxx (B.6) xxxxxxx xxxxxxx xx xxxxxxxxx, x to xxxxxxx xxxxxxxxxxxxx xxxxxxx na xxxxxxxxx a Xüxxxxxx xxxx
7a).
XXXX xxxxxxxxx xxxxxxxxxxxx xxxxxx xxx xxxxxxxxxxxx xxxxxxxxxx látek xxxxxxxxxxxxx xxxxxxxxxxxxx xxxx x xxx xxxxxxxxx, xx xxxxxxxx xxxxx xxxxxx xxxxxxxx potenciál xxxxxxxxxxxxxx xxxx. Xx xxxx xxxxxxxxx, xx xx xx metoda XXXX xxxx ve xxxxx xxxxxxxxx používat namísto xxxxxxx xx xxxxxxxxx; xxxxxxx xx xxxxx, xx xxxx metoda xx xxxxxxx hodnotu x xx xx xxx xxxxxx xxxx xxxxxxxxxxxx xxxxxx, xxxxx xxxxxxxxx xxx xxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxx xxxxx xxxxxxxxxxx.
XXXX xxxxxxxxx xxxxxx xxxxxx, xxxxx xxx o xxxxxxx pokrok a xxxxx xxxxxxx xxxxxxxx xxxxxxxxx xxxxxx. Xxxxxx xxxxxx indukční xxxx xxxxxxxxxxxxx xxxx x xxxxxxxxx xxxxxxxxxxxxx xxxxx, xxxxx jsou xxxxxx xxx xxxxxxxxx xxxxxx xxxxx x xxxxxx. Xxxxxxxx xxxxx x xxxxxxxx metod XXXX x xxxxxxx xxxxx xxxxxxxxx x xxxxx xxxxxxx byly xxxxxxxxxxx
7a).
Xxxxx xxxx je xxxxx poznamenat, xx xxxxx xxxx xxxxxxx xxxxx xxxxxxxxxxxxxxx xxxxx, xxxxx se doporučují xxxx vhodné xxxxxxxxx xxxxxxxxx xxxxx x xxxxxxx xx xxxxxxxxx, xxxx xxxxxx xxxx xxx xxxxxx XXXX
7a).
XXXX xx xxxxxxx in xxxx x xxxx xxxxxx xxxxxxxxxxx používání xxxxxxxxx xxxxxx xxx xxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx. Xxxx xxxxxx xxxx umožňuje xxxxxx počet pokusných xxxxxx, xxxxx xxxx x xxxxxx xxxxx xxxxxxxx. Kromě toho XXXX xxxxxx xxxxxxxxx xxxxxxxx xxxxxxx, xxxxx xx xxxxxxx xxxxxxx xxxxxxxxx ke zkoušení xxxxxxxxx senzibilizace. Xxxxxx XXXX xx xxxxxxxx xx posouzení xxxxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxxxx xxxxxxx během xxxxxxxx xxxx senzibilizace. Xx xxxxxx xx xxxxxxx xx morčatech metoda XXXX xxxxxxxxxx vyvolávání xxxxx přecitlivělosti navozené xxxxxxxxxx xxxxxx. Xxxxx xxxx xxxxxx XXXX xxxxxxxxxx ani používání xxxxxxxxx, xxx xx xxxx x xxxxxxx xxxxxxxxxxxxx xxxxxxx xx xxxxxxxxx. Xxxx xxxx xxxxxx XXXX xxxxxxx xxxxxxx xxxxxxxxx xxxxxx. Xxx x xxxx xxxxxx, které xx xxxxxx XXXX xx xxxxxxxx s xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx xx xxxxxxxxx, je xxxxx xx uvědomit, xx xxx xxxxxxxx xxxxxx xxxxxxx, xxxxx xx xxxxx xxxxxxx xxxxxxx xxxxxxxxxx zkoušek na xxxxxxxxx (xxxx. xxxxxxx xxxxxxxxx výsledky xxx xxxxxxx XXXX x xxxxxxxx xxxx, xxxxxxx xxxxxxxxx xxxxxxxx x xxxxxxxx látek xxxxxxxxxxxxx xxxxxxxxxx xxxx)
7a).
1.2 XXXXXXX XXXXXXXX XXXXXX
Xxxxxxxx xxxxxxx xxxxxx LLNA xxxxxxx x xxx, že xxxxxxxxxxxxxxx navozují primární xxxxxxxxxxx xxxxxxxxx v xxxxxxxxxxxx uzlinách xxxxxxxxxxx xxxxx aplikace xxxxxxxx xxxxx. Xxxx zmnožení xx xxxxxx xxxxxxxxxx xxxxx (x potenciálu xxxxxxxx) x xxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxx xxxxxxx xxxxxxxxxxxx, xxxxxxxxxxxxxxx xxxxxx senzibilizace. XXXX xxxxxxx tuto xxxxxxxxxxx xxxx xxxxx xxxxx-xxxxxx x xx xxxxx xxxxxx xx xxxxxxxxx xxxxxxxxxxx ve xxxxxxxxxx xxxxxxxxx x xxxxxxxxxxx x xxxxxx, xxxxxx xx xxxxxx xxxxxxxxx. Xxxxx xxxxxxxxxxx u xxxxxxxxxxxx skupin a x xxxxxx s xxxxxxxxx, nazvaný xxxxx xxxxxxxxx, xxxx xxx xxxxxxx 3, xxx xxx xxxxxxxxx xxxxx xxxx xxxxxxxx xxxx xxxxx xxxxxxxxxxxxxx xxxx. Xxxxxx, xxxxx xxxx xxx popsané, xxxx xxxxxxxx xx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx pro xxxxxx xxxxxxxxxxx buněk. Xxx xxxxxxxxx xxxx xxxxxxxxxxx je však xxxxx použít x xxxxx xxxxxxx vyhodnocení, x to xx xxxxxxxxxxx, xx jsou xxxxxxxxxx a xxxxxxxx xxx xx vhodné xxxxxxx xxxxxx, xxxxxx xxxxxxx xxxxxx a xxxxxx xxxxxxxx.
1.3 XXXXX XXXXXXXX METODY
1.3.1 Přípravy
1.3.1.1 Xxxxxxxx chovu a xxxxxx
Xxxxxxx xxxxxxx xx xxxxxxx odděleně. Teplota xx zkušební xxxxxxxxx xxx xxxxxxx xxxxxxx xx měla xxx (22± 3)°X. Xxxxxxx xx xxxxxxxxx vlhkost xxxx xxx xxxxxxx 30 % x xxxxxx by s xxxxxxxx čištění místnosti xxxxxxxxx 70 %, xx xxxxx hodnota 50 - 60 %. Xxxxxxxxx xx xxxx být umělé, xxxx xx se xxxxxxx 12 h xxxxxx x 12 x tmy, xxxx-xx x chovné xxxxxxxxx xxxxx xxxxxx. Ke xxxxxx xxx xxxxxx xxxxxxx krmivo xxxxxx xxx xxxxxxx xxxxxxx xx xxxxxxxxxxxxxx xxxxxxx x xxxxxxxxxx dodávkou xxxxx xxxx. Pokusná xxxxxxx mohou xxx xxxxxxx x klecích xx xxxxxxxxx podle xxxxx x xxxxxxx x xxxxxxxxxx xxxxxxx xxxxxxxxx
10), xxxxx xxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxx, xxx xxxxx xxxxxxxxx zvířat v xxxxx xxxxx xxxxxx xxxxxxxxxx pozorování xxxxxxx xxxxxxxxx zvířete.
1.3.1.2 Xxxxxxxx xxxxxxxxx xxxxxx
Xxxxxxx zvířata xxxx xxxxxxx x xxxxxxx xx xxxx, xxxxxxx a xxxxx x xxxxxxx x xxxxxxxxxxx
§15 zvláštního xxxxxxxx předpisu
10) a xxxxxxxx tak, xxx xxxx možná identifikace xxxxxxxxxxxx xxxxxxxxx zvířat. Xxxx xxxxxxxx stanoví
§10 xxxxxxxxxx xxxxxxxx xxxxxxxx
10). Před xxxxxxxx xxxxxxxx xxxxx xx xxxxxxx xxxxxxx xxxxxxx xxxxxxx, aby xx xxxxxxx, xx nemají xxxxx xxxxxxxxxxxxx kožní xxxx.
1.3.2 Xxxxxxxx podmínky
1.3.2.1 Xxxxxxx xxxxxxx
Xxxxxx zvoleným xxx xxxx xxxxxxx xx xxx. Používají xx xxxxx dospělé xxxxxx xxxx x xxxxx XXX/Xx xxxx XXX/X, xxxxx xxxx xxx xxxxxxxxx a xxxxxxx být březí. Xx xxxxxxx podávání xxxxx xx xxxxxxx xxxxxxx měla být xxxxxxxxx 8 až 12 týdnů stará x odchylky x xxxxxxxxx xxxxxxxxx xxxxxx xx měly být xxxxx xxxxxxxxx x xxxxxx xx xxxxxxxxx 20 % průměrné xxxxxxxxx. Xxxxxxx xxxxx x xxxxx by xx xxxx používat xxxxx xxxxx, xx-xx x xxxxxxxxx xxxxxxxx xxxxx, které by xxxxxxxxxx, xx v xxxxx xxxxxx v xxxxxx XXXX xxxxxxxx xxxxxxxxxx xxxxx xxxxxxxxxx xxxxxxxxxx xxxx kmeny xxxx pohlavími.
1.3.2.2 Xxxxxxxx xxxxxxxxxxxxx
Xxxxxxxxx xxxxxxxx xx xxxxxxxxx x xxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxxx x xxxxxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxxx xxxxxxx. Xxxxxxxxx xxxxxxxx xx xxxx xxxxxxx xxxxxxxxx xxxxxx v XXXX xxx xxxxxx xxxxxxxx, u xxxxx xx xxxxxxx xxxxxxx xxxxxx xxxxxxxxx (XX) &xx; 3 xx xxxxxxxx x negativní xxxxxxxxx xxxxxxxx. Je xxxxx zvolit xxxxxxx xxxxxxxxx xxxxxxxxx dávku, xxx xxxxxx byla xxxxxxxx, nikoliv xxxx xxxxxxxx. X xxxxxxxxxxxx xxxxxx xxxxx 2-xxxxxxxxxxxxxxxxx (XXX 101-86-0, XXXXXX 202-983-3) x 2-xxxxxxxxxxxxxxxxxxxx (XXX 149-30-4, XXXXXX 205-736-8). Xxxxx existovat xxxxxx okolnosti, xx xxxxx xxx xxx xxxxxx zdůvodnění použít xxxx xxxxxxxxx látky, xxxxx xxxxxxx výše xxxxxxx xxxxxxxx. X xxxx se xxx xxxxxx zkoušku obvykle xxxxxxxx xxxxxxxxx kontrolní xxxxxxx, xxxxx xx xxxxxx xxxxxxxxxx xxxxxxx, xxx xxxx xxxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxxxxx xxxxx x xxxxxxxxx xxxxxxxx prokazující xxxxxxxxxx dostatečné xxxxxx xxxxx xxxxx měsíců xxxx xxxxxxx časového xxxxxx. X takovém xxxxxxx xxxx xxx xxxxxxxxx xxxx xxxxx xxxxxxxxx s xxxxxxxxxxx xxxxxxxxxx x xxxxxxxxxxx, xxxxx by neměly xxx delší xxx 6 měsíců. Xxxxxxx xx se xxxxxxxxx xxxxxxxxx xxxxx měly xxxxxxxx ve vehikulu, x kterém xx xxxxx, že xxxxxxxx xxxxxx xxxxxxx xxxxxx (xxxx. aceton, xxxxxxx xxxx), xxxxx xxxxxx xxxxxx xxxxxxx, xxx xx x důvodů xxxxxxxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxx x xxxxxxxx xxxxxxxxxxxxxx vehikula (xxxxxxxx/xxxxxxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxx). X xxxxxxx xxxxxxx xx xxxxx xxxxxxxx xxxxxx interakci xxxxxxxxx xxxxxxxx x xxxxx xxxxxxxxxxxxx xxxxxxxxx.
1.3.2.3 Xxxxx xxxxxxxxx xxxxxx, xxxxxx xxxxx x výběr xxxxxxxx
Xx xxxxxx xxxxxxxx xxxxxxx xx použijí xxxxxxx xxxxx xxxxxxx xxxxxxx, xxxxxxx xx xxxxxxx xxxxxxxxx tři xxxxxxxxxxx xxxxxxxx látky, xxxx se použije xxxxxxxxx xxxxxxxxx xxxxxxx, xxxxx se podává xxxxx vehikulum xxxxxxxx xxxxx, x v xxxxxxx potřeby pozitivní xxxxxxxx. Xxxxxxxx xx xxxxxxxxxxx xxxxx x xxxxxxxxxxxx pokusných xxxxxxxxx, xxxxxxx xx xx xxxxxx xxxxxxxx xxxxxxx xxxxxxxxx pět xxxxxxxxx xxxxxx. X xxxxxxxx xxxxxxxx xxxxxxxx látky xx x xxxxxxxxx xxxxxxx v kontrolní xxxxxxx xxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx jako x pokusnými xxxxxxx x experimentální xxxxxxx.
Xxxxx xxxxxxxxx a vehikula xx měla xxx xxxxxxxx xx xxxxxxxxxxxx xxxxxxxxx x xxxxxxxxxx
7a). Xxxxx xx xxxxxxxx x xxxx xxxxxxxxxxx 100 %, 50 %, 25 %, 10 %, 5 %x 2,5 %, 1 %, 0,5 % xxx. Xxx xxxxxx tří xx xxxx xxxxxxxx xxxxxxxxxxx xx xxxxx xxxxxx xxx xxxxxxxxxx údaje x akutní toxicitě x xxxxx dráždivosti, xxxx-xx k dispozici, xxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx, xxx xxx xxxxxxxx xxxxxxxxxx xxxxxxxxxx toxicitu x xxxxxxxx xxxxxxxxxx xxxx
7a).
Xxxxxxxxx xx xxxx xxx xxxxxxx xxx, xxx xx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxx x xxxxxxxxxxx x xxxxxxxx xxxxxxx/xxxxxxxx xxxxxx xxx aplikaci xxxxxxxx xxxxx. Xxxxxxxxxxxxx xx xxxxxxxx x xxxxxxxxxxxx xxxxxx: aceton/olivový xxxx (4:1 xxx.), X,X-xxxxxxxxxxxxxxxx, xxxxxxxxxxxxxxxx, xxxxxx-1,2-xxxx x xxxxxxxxxxxxxxxx
7a) , xxxxx mohou xxx xxxxxxx x jiná xxxxxxxx, jsou-li xxxxxxxxxx xxxxxxxxxx vědecké xxxxxx. X xxxxxxxx případech xxxx být xxxxxxxx xxxxxx jako doplňující xxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxx nebo komerční xxxxxxxxx xxxxxxxxx, x xxxx xx xxxxxxxx xxxxx uváděna xx xxx. Zvláštní xxxxxxxxx xx xxxxx xxxxxxx xxxxxxxxx xxxx, xxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxx xx xxxxxxxx xxxxxxxx, xxxxx xxxxxx xxxx x xxxxxxx xxxxx x xxxxxxx. X tohoto důvodu xxxx xxxxxx používat xxxx xxxxxxxxx pouze xxxx.
1.3.3 Zkušební postup
1.3.3.1 Xxxxxxxxxxxx zkoušky Xxxxxxxxxxx xxxxxxx xx následující:
- Xxx 1:
Xxxxx xxxxxxx xxxxx xx individuálně xxxxx a zaznamená xx xxxx xxxxxxxx. Xxxxxxx xx xxxxxxxx xxxxxxxx 25 µx xxxxxxxxxxx ředění xxxxxxxx xxxxx, xxxxxxxxx xxxxxxxx xxxx xxxxxxxxx xxxxxxxxx xxxxx (xxxxx xxxxxxxxx) xx xxxxxxxx část xxxx uší.
- Xxx 2 x 3:
Xxxxxxxx xx postup xxxxxxxx xxxxxxxxx x den 1.
- Xxx 4 x 5:
Žádná xxxxxxxx.
- Xxx 6:
Xxxxxxxxx se xxxxxxxx xxxxxxx xxxxxxxxx xxxxxxx. Přes xxxxxx xxxx xx všem xxxxxxxx x xxxxxxxxxx xxxxx xxxxxxx 250 µx xxxxxxxxxxxxxx xxxxxxx xx xxxxxxxxxx xxxxx (XXX), xxxxxxxxxxxx 20 µXx (7,4.105 Bq) [3X]xxxxxxxxx (xxxxxxxxxxx na xxxxxxx), nebo xxx xxxx xxxxx přes xxxxxx xxxx xxxxxxxxx 250 µx PBS xxxxxxxxxxxx 2 µCi (7,4.104 Bq) [125X]xxxxxxxxxxxxxxx x 10-5 X xxxxxxxxxxxxxxxxx.
X xxx xxxxx xxxxxxx xx myši xxxxxx. Xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx uzliny z xxxx uší xx xxxxxx x xxxxxxxxx xx x XXX xxxxxxxx xxx xxxxx xxxxxxxx xxxxxxx (xxxxxx xxxxxxxx xxxxxxxxxx xxxxxxx), xxxx se xx xxxxxxx xxxxxxxxx xxxxxxx xxxxx xxx xxxxxxxxxxxx xxxxx x xxxxx xx xx XXX xxxxxxxxxxxx xxx xxxxx xxxxxxx zvíře (metoda xxxxxxxxxxxxxx xxxxxxxx k xxxxxxxx xxxxxxxx )
7a).
1.3.3.2 Xxxxxxxx xxxxxxx xxxxxxxx
Xxxxx xxxxxxxx xxxxxxx xxxxxxxx x buňkami xxxxxxxxxxxx xxxxx (XXX) xxx xx xxxx exponované xxxxxxx, nebo xxxxxxxxxxx xx xxxxxxxxxxxx pokusných xxxxxx se xxxxxxxx xxxxxx xxxxx mechanické xxxxxxxxxx přes 200 µx sítka z xxxxxxxxxxxxx xxxxx. Xxxxxxxxxx xxxxx se dvakrát xxxxxxxxxxx x dostatečném xxxxxxxx XXX x xxxxxxx xx xxxxxxxx x xxxxxxx x 5% trichloroctovou xxxxxxxxx (XXX) xxx 4 °X xx xxxx 18 h
7a). Xxxxxxxx xx xxx resuspenduje x 1 ml XXX x xxxxxxxx xx xxxxxxxxxxxxx xxxxx xxxxxxxxxxxx 10 xx xxxxxxxxx xxxxxxxxxxxx xxx xxxxxx aktivity
3X, xxxx xx xxxxxxx xxxxx xx zkumavek xxx měření xxxxxxxx
125X.
1.3.3.3 Stanovení xxxxxxx xxxxxxxxxxx (xxxxxxxxxxxxx radioaktivity)
Inkorporace [3X]xxxxxxxxx xx xxxx (ß-xxxxxxxxxxx xxxxxxx x xxxxxxx xx x xxxxxxxxx xx xxxxxx (xxx). Xxxxxxxxxxx [125X]xxxxxxxxxxxxxxx xx xxxx xxxxxxxxxxxxxxx xxxxxxxx 125X a xxxxxx xx xxxxxxx x xxx. X xxxxxxxxxx xx xxxxxxxx xxxxxxxx xx inkorporace xxxxxxx v dpm xx zkušební xxxxxxx (xxxxxx sdružení) nebo x xxx xx xxxxxxx xxxxx (xxxxxxxxxxxx xxxxxxx).
1.3.3.4 Xxxxxxxxxx
1.3.3.4. Xxxxxxxx xxxxxxxxxx
Xxxxxxx zvířata xx xxxxx xxxxxx denně xxxxxxx xxxxxxxx xx xxxxxxxx klinické xxxxxxxx, xx xxx xx xxxxx xxxxxxxxx podráždění x místě xxxxxxxx, xxxx xx formě xxxxxxxxx toxicity. Xxxxxxx xxxxxxxxx xx systematicky xxxxxxxxxxxxx, xxxxxxx záznamy xx xxxxx xxxxxx xxx xxxxx xxxxxxx xxxxx.
1.3.3.4.2 Xxxxxxx xxxxxxxx
Xxx xx uvedeno x xxxxxxxx 1.3.3.1, tělesnou xxxxxxxx x xxxxxxxxxxxx xxxxxxxxx xxxxxx xx xxxxx zaznamenat na xxxxxxx zkoušky x x xxx xxxxxxxxxxx xxxxxxxx xxxxxxxxx zvířat.
1.3.4 Xxxxxxx xxxxxxxx
Xxxxxxxx se xxxxxxx jako xxxxx xxxxxxxxx (XX). Xxx xxxxxx sdružení xxxxxxxxxx xxxxxxx xx XX xxxxxxx xxxx podíl xxxxxxxx xxxxxxxxxxxxx aktivity x xxxxxxxxxxxx experimentálních xxxxxx x xxxxxxxx xxxxxxxxxxxxx xxxxxxxxx skupiny x xxxxxxxxx; xxxxx xx xxx xxxxxxxx xxxxxxx XX. Při xxxxxxxxxxxxx xxxxxxxx xx XX xxxxxxx jako xxxxx xxxxxxxx xxxxxxx xxx na xxxxxxx xxxxx xxx u xxxxx exponované xxxxxxx, xxx x xxxxxxxxx xxxxxxxxx xxxxxxx, x xxxxxxxx xxxxxxx xxx xx pokusné xxxxx x xxxxxxxxx xxxxxxx x xxxxxxxxxxxxx/xxxxxxxxx. Xxxxxxxx xxxxxxx XX pro xxxxxxxxx xxxxxxx s xxxxxxxxx je proto 1.
Xxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxx výpočtu XX xxxxxx xxxxxxx statistickou xxxxxxx xxx. Xxx xxxxxx xxxxxx metody xxx xxxxxxxxxxxx xxxxxxx xx xxxx být xxxxxxxxxxxxxx xxxxx xxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxx xxxxxxxxxxxxx xxxxxxxx, xxxxx si xxxxx xxxxxxx transformaci xxx xxxx neparametrickou xxxxxxxxxxxx xxxxxxx. Správný xxxxxxx x xxxxxxx xxx xxxxxxx ve xxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxxx dat xxxxxxxxxxxx xxxxxxxxx xxxxxx x xxxxxxx x xxxxxxxxx x proložení xxxxxxxx křivky xxxxxxxxxx xxxxxx xx xxxxx xxx xxxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx
7a). X xxxxxx xxxxxxx xx však xxxxxxxxxxxxxx musí xxxxxxxxxx xxxxx "xxxxxxx" reakce x xxxxxxxxxxxx xxxxxxxxx xxxxxx x xxxxx xxxxxxx, xxxxx mohou xxxxxxxxx použití jiného xxxxxxxxx odezvy (xxxx. xxxxxxx mediánu xxxxxxx xxxxxxx) xxxx vyřazení xxxxxx xxxxxxxxx xxxxxx.
Xx xxxxxxxxxxx, xxx jde x pozitivní xxxxxx, xx xxxxxxxx xxxxx xxxxxxxxx ≥ 3 x xxxxxxxxxx xx xxxxxxxxx xxxxxx na xxxxx a xxxxxxxxx xxxxxxxxxxx xxxxxxxxxx
7a).
Xx-xx xxxxxxxx xxxxxxxx získané xxxxxxxx, xx xxxxx věnovat xxxxxxxxx různým vlastnostem xxxxxxxx xxxxx, včetně xxxx, xxx xx xxxx xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxxxxxx xxxx, xxx xxxxxxxxx xxxxxxxx podráždění xxxx x xxxx xxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xx xxxxx
7a).
2 XX
Xxxx xx xxxxxx xx xxxxxxx, přičemž pro xxxxxx dávkovou xxxxxxx xx xxxxxx průměrné x individuální xxxxxxx xxx x xxxxxx xxxxxxxxx (xxxxxx xxxxxxxxx xxxxxxx x vehikulem).
3 XXXXXXX POKUSU, XXXXXXXX XXXXXX X ZÁVĚREČNÁ XXXXXX
X souladu x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9),10) xxxx xxx xxxxxxxxx xxxxxxx pokusu x x xxxxxxx xxxxxx xx nutno xxxx xxxxxxxx.
3.1 Zpráva o xxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxx:
Xxxxxxxx látka:
- xxxxxxxxxxxxx xxxxx (xxxx. xxxxx XXX, xx-xx x xxxxxxxxx; zdroj, xxxxxxx, xxxxx xxxxxxxxx; xxxxx xxxxx),
- xxxxxxxxxx x xxxxxxxxx-xxxxxxxx xxxxxxxxxx (xxxx. xxxxxxxx, xxxxxxx, xxxxxxxxxxx),
- jedná-li xx x xxxx, složení x poměrné procentuální xxxxxxxxxx xxxxxx.
Xxxxxxxxx:
- identifikační xxxxx (čistota; xxxxxxxxx xxxxxxxxxxx; xxxxxxx objem),
- xxxxxxxxxx xxxxxx vehikula.
Pokusná xxxxxxx:
- použitý xxxx xxxx,
- mikrobiologický xxxx xxxxxxxxx xxxxxx, xx-xx xxxx,
- xxxxx, xxxxxxxx xxxxx, krmivo xxx.,
- xxxxx, xxxxx x xxxxxxx pokusných xxxxxx.
Xxxxxxxx xxxxxxxx:
- xxxxxxxxxxx x xxxxxxxx x aplikaci xxxxxxxx xxxxx,
- xxxxxxxxxx xxxxxx xxxxx, xxxxxx xxxxxxxx x xxxxxxxxxx xxxxxx, xxxxx xxxx xxxxxxxxx; použité koncentrace xxxxxxxx a xxxxxxxx xxxxx x celkové xxxxxxxxxx xxxxxxxx látky,
- xxxxxxxxxxx o xxxxxxx xxxx x krmiva (xxxxxx xxxxx/xxxxxx xxxxxx, xxxxxx xxxx).
Xxxxxxxx spolehlivosti:
- xxxxxx výsledků z xxxxxxxx xxxxxxxx xxxxxxxxxxxxx, xxxxxx xxxxxxxxx x xxxxxxx xxxxx, koncentraci x xxxxxxxx,
- xxxx xx souběžných nebo xxxxxxxxxx xxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxxxxx skupin xxx xxxxx xxxxxxxxx.
Xxxxxxxx:
- xxxxxxxxxxxx hmotnosti xxxxxxxxx xxxxxx xx xxxxxxx xxxxxxxx x x xxxx xxxxxxxxxxx usmrcení,
- xxxxxxx xxxxxxxxxx (xxxxxxxx xxxxxx) x individuálních (xxxxxxxxxxxx xxxxxxx) xxxxxx xxx x xxxxxx xxxxxxx xxxxxx x xxxx xxxxxxxx a xxxxxx xxxxxxxxx xxx xxxxxxxxxx dávkové xxxxxxx (xxxxxx kontrolní xxxxxxx x xxxxxxxxx),
- xxxxxxxx xxxxxxxxxxx xxxxxxx,
- u xxxxxxx xxxxxxxxx xxxxxxx xxxxxx xxxxxx nástupu xxxxxxxx xxxxxxxx, xxxxxx xxxxxxx xxxxxxxxxx x xxxxx aplikace, pokud x němu dojde.
Diskuse x interpretace výsledků.
- xxxxxxx xxxxxxxx k xxxxxxxxx, k xxxxxxx xxxxxxxxxx xxxxxx na xxxxx x x xxxxxxxxx xxxxxxxxxxxx xxxxxxxx x xxxx a xxxxx, xxx lze xxxxxxxx xxxxx považovat xx xxxxxxxxxxxxxx xxxx.
Xxxxxx.
X.43 XXXXXXX XXXXXXXXXXXXX XX XXXXXXXXXX
1 XXXXXX xx x xxxxxxx x xxxxxx Xxxxxxxxxx xxxxxxxxxxxx
7a).
Xxxx xxxxxxxx xxxxxx byla xxxxxxxx za xxxxxx xxxxxxx xxxxxxxxx, které xxxx xxxxxxxx xx xxxxxxxxx xxxx k xxxxx xxxxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxxx chemických látek x dospělých pokusných xxxxxx. Xxxx metodu xxx xxx xxxxxxxxxx x xxx existujícími xxxxxxxxxx metodami pro xxxxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxx, xxxx xx lze provést xxxx xxxxxxxxxxx xxxxxxx. Xxx usnadnění xxxxxxxxx xxxxxx xxxxxxxxxx na xxxx xxxxxxxx xxxxxx xx xxxxxxxxxx prostudovat Xxxxxxxxxx OECD x xxxxxxxxxxx x xxxxxxxx xxxxxxxx xxxxxxxxxxxxx (XXXX Xxxxxxxx Xxxxxxxx on Xxxxxxxxxxxxx Xxxxxxx Xxxxxxxxxx xxx Xxxxxxx)
7a). Xx xx xxxxxxx důležité xxxxx, je-li xxxxx xxxxxx xxxxx xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxx xxxx xxxxxxxxxx xxx xxxxxxx používáni xxxx metody. Doporučení xxxx připravena xxx xxxxxxxxx xxxxxx zkušebních xxxxxxx xxx xxxxxxxxxx xxxxxxxx xxxxxxx. Xxxxxxxxx xxxxxxxx neurotoxicity xxxx xxxxxxxxx xxxx xxxxxx.
1.1 XXXX
Xxx xxxxxxxxxx a xxxxxxxxxxxxx toxických vlastností xxxxxxxxxx xxxxx je xxxxx xxxxxxxx zvážit xxxxxxxxx neurotoxických xxxxxx. Xxx metoda zkoušení xxxxxxxxx xxxxxxxx xx xxxxxxxxx dávce xxxxxxxx xxxxxxxxx, xxxxx xxxx xxxxxx xxxxxxxxxxx xxxxxxxxxxxxx. Xxxxxxxxxxx xxxxxxxx metodu xxx používat při xxxxxxxxx xxxxxx xx xxxxxx xxxxxxx xxxxxxx xxxxxxxxx o xxxxxxxxxxxxxx xxxxxxxx xxxxxxxxxx xxx xxxxxx xxxxxxxxx xxxxxxxx xx opakovaných xxxxxxx, xxxx xxx jejich xxxxxxxxx. Z xxxx x xxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxx xxxxxxxxxx xxxxx však xxxx xxxxxxxxx, že xx xxxxx xxx xxxxxxxx xxxxxxxxx xxxxxx xxxx xxxxxx, xxxxx neexistují xxxxx x potenciální xxxxxxxxxxxxx xx xxxxxx xxxxxxxxx toxicity xx xxxxxxxxxxx dávkách. Xxxx xxxxx xxxxxxxx xxxxxxxxx
- xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxx neuropatologických lézí x jiných xxxxxxxx xxxxxxxx xxx xxxxxxxx xxxxxxxxx toxicity xx xxxxxxxxxxx xxxxxxx, xxxx
- xxxxxxxxxx xxxxxxxxx nebo xxxx xxxxxxxxx, xxxxx xxxxxxxxxxx látku xxxx xx xxxxxxx neurotoxickými xxxxxxx.
Xxxxx xxxx mohou xxxxxxxxx x další xxxxxxx, xxx je xxxxxxx této xxxxxx xxxxxx; další xxxxxxxxxxx xxxx uvedeny x xxxxxxxxxx
7a).
Xxxx metoda xxxx xxxxxxxx xxx, xxx xx xxxx xxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxxx xxx potvrzování specifické xxxxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxxxxx chemických xxxxx x při xxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx.
Xxxxx xx xx xxxxxxxxxxxxx xxxxxxxxxx neuropatie xxxxxxxxxx neuropatologické xxxx xxxx neurologické xxxxxxxxx, xxxx xxxx. záchvaty, xxxxxxxx nebo třes. X xxxx xxxx xxxxxxxxxx xxxxxxxxx xxxxxxxx xxxxxxxxxxxxx, xxxx je xxx jasné, že xxxxxxxx xxxxx xxxxx xxxxxxxx xxxxxxxx xxx xxxxxxx xxxxxx (xxxx. xxxxxx motorické xxxxxxxxxx, xxxxxxxxxx xxxxxxx, xxxxxxx xxxxx x xxxxxx), xxxxx xx xxxxxx xxxxxxxxxx xxx xxxxxxxxxx, xxx v xxxxxx xxxxxx zkoušek.
Tato metoda xxxxxxxx xxxxxxxxxxxxx xx xxxxxxxx xxx, xxx xxxxxxxxxx xxxxxxx xxxxxxxxxxxxxxxxx x neuropatologické xxxxxx xx xxxxxxx hlodavce. Xxxxxxx behaviorální xxxxxx x při xxxxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxxxx xxxxxxx xxxxxxxxxx xxxx xx xxxxxxxxxx, xxxxxxxxx xx, xx xxxxxxx xxxxxxxxxxxx xxxxx xxxx xxxxxxxxxx xxx xxxxxxx xxxxxx. X xxxxxx xxxxxx by se xxxx xxxxxxxxx zjištěné xxxxx xxxxxxxxxx v xxxxxxxx x histopatologickými, xxxxxxxxxxxxxxx nebo xxxxxxxxxxxxx xxxxxxxx. Xxxxxxxx xxxxxxxxxx x xxxx metodě xx xxxxxx xxxxxxxxxxxxxx x xxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxxxxxxx specifické xxxxxxxxxxxxxxxx x behaviorální xxxxxxx, xxxxx xxx xxxxx xxxxxxxx xxxxxxxxxxxxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxx
7a).
Xxxxxxxxxxxx xxxxx xxxxx xxxxxxx xx xxxxxxxx cílových xxxxxxxx x xxxxx xxxxxxxxx xxxxxxx x xxxxxxxxxxxxxxx xxxxxxx mechanismů. Xxxxxxx neexistuje xxxxxx xxxx zkoušek xxx xxxxxxxxx neurotoxického potenciálu x xxxxx xxxxx, xxxx být xxxxxxxx xxxxxx xxxxxxx xxxxxxx xx vivo xxxx xx vitro, xxxxx xxxx xxxxxxxxxx xxx xxx xxxxxxxxxx nebo xxxxxxxxx xxxxxxxxxxxxx.
Xxxx zkušební xxxxxx xxx xxxxxx xxxx xxxxxxxx x xxxxxxxxxxxx OECD o xxxxxxxxxxx x xxxxxxxx xxxxxxxxx xxxxxxxxxxxxx (OECD Xxxxxxxx Document on Xxxxxxxxxxxxx Testing Xxxxxxxxxx xxx Xxxxxxx)
7a) při xxxxxxxxx zkoušek xxxxxxxx x další xxxxxxxxxxxxxx xxxx xxxxxxx citlivosti xxxxxxxxxxxx xxxxxx dávka-odezva x xxxxx lépe xxxxxxxxx xxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxx, xxxxx xxxxxxxx známá xxxx očekávaná rizika xxxxxxxxxx xxxxx. Xxx xxxxxxxxx xxxxxxxxx zkoušky, xxxxx xx identifikovaly x xxxxxxxxxx xxxxxxxxxxxx xxxxxxxxxxx (neurotoxické xxxxxxxxxx) xxxx xxxxxxxx xxxxx, xxxxx xxx xxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxxxxxx x xxxxxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxx. Xxxxxx xxxxxx xxxxxx replikovat údaje xxxxxxxx xxxxxxxxxxxx xxxxxxx xxxxxxxxxxxx x této xxxxxx, jsou-li xxxxxx xxxxx xxx x xxxxxxxxx x xxxxxxxxxx xx xx nezbytné x xxxxxxxxxxxx výsledků x této xxxxxx.
Xxxxxxx-xx xx xxxx zkouška xxxxxxxxxxxxx xxxxxxx xxxx x kombinaci, poskytuje xxxxxxxxx, xxxxx xxxxx
- xxxxx, zda xxxxxxxx xxxxxxxx látky xxxxxxxxx xxxxxxx xxxxxx xxxxxx, xxxx vratně,
- xxxxxxx x charakterizaci xxxx xxxxxxxxx systému xxxxxxxxx x xxxxxxxx xxxxxxxx xxxxx x přispět x xxxxxxxxx mechanismů xxxxxx,
- stanovit xxxxxx xxxx dávkou x xxxxxxx x časem x xxxxxxx x xxxxx odhadnout xxxxxx xxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxxxx (NOAEL) (xxxxxx xxx xxxxxx pro xxxxxxxxx xxxxxxxxxxxxxx xxxxxxxx xxx xxxxxxxxx xxxxx).
Xxxx xxxxxxxx metoda používá xxxxxx aplikaci zkušební xxxxx. Jiné xxxx xxxxxxxx (např. xxxxx xxxx xxxxxxxxx) xxxxx xxx vhodnější x xxxxx xx xxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxxxx xxxxxxx. Výběr xxxxxxx xxxxxxxx xxxxxx xx xxxxxxx xxxxxxxx xxxxxxx x xx xxxxxxxxxx xxxxxxxxxxxxxxx nebo xxxxxxxxxxx xxxxxxxxxxx.
1.2 XXXXXXXX
Xxxxxxxxxx účinek: xx xxxxxxxxx xxxxx xxxxxxx x xxxxxxxx, xxxxx xxxxxxx schopnost xxxxxxxxx přežít, xxxxxxxxxxx xx xxxx xx xxxxxxxxxxx xxxxxxxxx.
Xxxxxxxxxxxxx: xx xxxxxxxxxx xxxxx struktury xxxx xxxxxx nervového xxxxxxx, která je xxxxxxxxx xxxxxxxx xxxxxxxxxx, xxxxxxxxxxxx nebo xxxxxxxxxxx xxxxxxxx.
Xxxxxxxxxxxx agens: je xxxxxxxxx xxxxxxxx, xxxxxxxxxx xxxx xxxxxxxxx činitel, xxxxx má xxxxxxxxxxxx xxxxxxxxx.
1.3 XXXXXXX ZKUŠEBNÍ XXXXXX
Xxxxxxxx chemická xxxxx xx xxxxxx xxxxxx x xxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxx. Xxxxxxx se xxxxxxxx xxxxxxxx opakovaných xxxxx a xxxxxxxxx xxxxx xxxx být xxx 28xxxxx, nebo xxxxxxxxxxxx (90 xxx), xxxx xxxxxxxxx (1 xxx nebo xxxx). Xxxxxxx xxxxxxxxx x xxxx zkušební metodě xxx xxxxxx i xxx xxxxxx xxxxxx xxxxxxxxxxxxx. Pokusná xxxxxxx xxxx xxxxxxxxx xx xxxxxx xxxxxxxx nebo xxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxx xxxxxxxxxxxxxx xxxxxxxx. Xxxxx xxxxxxx xxxxxxxxxxxx období xx xxxxxxx xxxx xxxxx xxxxxxx, xxxxx xx xxxxx xxx xxxxxxxxx xxxxxxxxxxxxxx xxxxxxx. Xx konci xxxxxxx xx u xxxxxxxxxx xxxxxxxxx xxxxxx xxxx xxxxxxx x každé xxxxxxx xxxxxxx perfuze xx xxxx x xxxxxxxx xx x xxxxxxx xxxx xxxxx, xxxxx x xxxxxxxxxxx xxxxx.
Xxxxx xx zkouška xxxxxxx xxxx xxxxxxxxxx xxxxxxx xxx xxxxxxxxx xxxxxxxxxxxxx nebo xxxxxxxxxxxxxx xxxxxxxxxxxxxx xxxxxx, lze xxxxxxx zvířata x xxxxx xxxxxxx, xxxxx xxxxxx xxxxxxx k xxxxxxx x k xxxxxxxxxx xxxxxxxxxxxxxxxxxx xxxxxxxxx (xxx tabulka 12), xxxxxx xx specifickým xxxxxxxxxxxxxxxxxx, xxxxxxxxxxxxxxxxx, neurochemickým xxxx xxxxxxxxxxxxxxxxxxxx vyšetřením, xxxxx xxxxx xxxxxxx xxxxx xxxxxxx ze xxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxxx x xxxx xxxxxx
7a). Xxxx xxxxxxxxxx xxxxxxx xxxxx xxx xxxxxxx xxxxxxxx tehdy, xxxxxxxx xxxxxxxxx xxxxxxxxxx nebo xxxxxxxxxxxxx xxxxxx naznačují xxxxxxxxxx xxx nebo xxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx látky. Xxxxxxxxx xxxxxxx xxxxxxx lze xxxxxxxx použít x xxxxxxxx jiným xxxxxxxxxx, xxxx jsou např. xxxxxxxxx požadovaná xx xxxxxxxxxx metodách u xxxxxx xxxxxxxx po xxxxxxxxxxx dávkách xx xxxxxxxxxx.
Xxxxx xx xxxxxxx xxxx xxxxxxxx xxxxxx xxxxxxxxx x postupy x xxxxxx zkušebních xxxxx, je nezbytný xxxxxxxxxx xxxxx xxxxxxxxx xxxxxx, xxx xxxx xxxxxxx xxxxxxxxx xxx xxxxxxxxxx x xxxx xxxxxxxx.
1.4 POPIS XXXXXXXX XXXXXX
1.4.1 Xxxxx xxxxxxxxxxx xxxxx
Xxxxxxxxxxxxxxxx druhem hlodavce xx potkan, x xxxx lze xx xxxxxxxxxxxxx zdůvodnění xxxxxx x xxxx druhy xxxxxxxx. Použity xx xxxx být xxxxx xxxxxxxxx xxxxxxxxxxx kmeny xxxxxxx xxxxxxxx dospělých xxxxxxxxx xxxxxx. Samice xxxx být xxxxxxxxx x nesmějí xxx xxxxx. Xxxxxxxx xxxxx xx mělo xxxxx xx xxxxxxxx po xxxxxxxxx, nejlépe když xxxxxxx xxxxxxx dosáhnou xxxxx xxxxx xxxxx x x xxxxxx xxxxxxx xxxxx, než xxxxxxxx stáří devíti xxxxx. Pokud xx xxxx xxxx zkouška xxxxxxxxx x dalšími xxxxxxxxx, je xxxxx, xx požadavky xxxxxxxx xx stáří xxxxxxxxx xxxxxx xxxxx xxxxxxxxx xxxxxx změny. Xx xxxxxxx xxxxxx xx xxx xxx x xxxxxxxxxxx xxxxxxxxx zvířat xxx xxxxxxxxx xxxxxxx xxxxxxxxx x xxxxx xx xxxxxxxxx 20 % xxxxxxxx xxxxxxxxx x xxxxxxxxxxxx xxxxxxx. Xxxxx xx xxxx xxxxxxxxxxx xxxxxx xxxxxxx xxxxxxxxxx krátkodobá xxxxxx xxxxxxxx xx opakovaných xxxxxxx, je xxxxx x xxxx studií xxxxxx pokusná xxxxxxx xx xxxxxxxx xxxxx x stejného xxxxxx.
1.4.2 Xxxxxxxx xxxxx a xxxxxx
Xxxxxxx ve xxxxxxxx xxxxxxxxx pro pokusná xxxxxxx xx měla xxx (22 ± 3) °C. Relativní xxxxxxx xx xxxx xxx alespoň 30 %, neměla xx xxxx xxxxxxxxx 70 % xxxxx xxxxxxx xxxxxxxxx a xxxxx xx xxxxxxx 50 - 60 %. Xxxxxxxxx xx xxxx xxx xxxxx, xxxx xx xx xxxxxxx 12 h světla x 12 h xxx, xxxx-xx x xxxxxx místnosti xxxxx xxxxxx. Náhlé hlasité xxxxx xx xxxxx xxxxxx na xxxxxxx. Xx krmení xx xx xxxx xxxxxxxx xxxxxxx xxxxxx určené xxx xxxxxxx xxxxxxx xx registrovaného výrobce x xxxxxxxxxx xxxxxxxx xxxxx vody. Na xxxxx xxxxxx může xxx xxxx xxxxxxx xxxxxxxx vhodnou xxxxxxx xxx xxxxxxxxx xxxxx, xx-xx xxxxx xxxxxxxx xxxxx metodou. Xxxxxxx xxxxxxx xxx xxxxxx xxxxxxxxxx, anebo xx xxx xxxxxxx x xxxxxxx x xxxxxx xxxxxxxxxx tvořených pokusnými xxxxxxx xxxxxxxx xxxxxxx x xxxxxxx x xxxxxxxxxx právním xxxxxxxxx
10), xxxxx xxxx stanoveno xxxxxxxxx pokusů xxxxx.
1.4.3 Xxxxxxxx xxxxxxxxx xxxxxx
Xxxxxxx xxxxxxx xxxx vybrána x xxxxxxx na xxxx, xxxxxxx x xxxxx x souladu x ustanovením
§15 xxxxxxxxxx právního předpisu
10) x označena xxx, xxx xxxx xxxxx xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx. Xxxx navykání xxxxxxx
§10 xxxxxxxxxx xxxxxxxx předpisu
10). Pokusná xxxxxxx by xxxx xxx xxxxxxx xxxxxxxxx xx xxxxxxxxxxx a xxxxxxxxxxxxxxxx skupin. Klece xx xxxx být xxxxxxxxxx xxx, xxx xxx xxxx xxxxxxxx xxxxx xxxxxxxxxxxxx. Xxxxxxxxxx xxxxxxx zvířata se xxxxxxxxxxx xxxxxxxxxxxx x xxxxxx xx xx xxxxx nejméně xxx xxx xxxx začátkem xxxxxx, aby si xxxxx xxxxxxxx xx xxxxxxxxxxx xxxxxxxx.
1.4.4 Xxxxxx xxxxxxxx a příprava xxxxx
X této xxxxxxxx xxxxxx se xxxxx xxxxxxxxx x xxxxxx xxxxxx xxxxxxxx zkoušené xxxxx. Xxxxxx xxxxxxxx xxx xxxxxxxx prostřednictvím xxxxxxxxx sondy, xxxxxx, xxxxx vody nebo xxxxxxx. Xxxxxx lze x xxxx xxxxxxx xxxxxxxx (např. xxxxx xxxx xxxxxxxxx), xxxxx xx xxxxx xxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxxx. Xxxxx xxxxxxx aplikace xxxxxx xx xxxx xxxxxxxx xxxxxxx x xx dostupných xxxxxxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxxxxx. Xx xxxxx uvést xxxxxx pro výběr xxxxxxx aplikace a xxxxxxxxxxxx xxxxxxxxxx postupů x xxxxx xxxx xxxxxxxx metody.
Zkoušená xxxxx xx xxxxx xxxxxxx xxxxxxxx xxxx suspenduje xx vhodném vehikulu. Xx-xx xx xxxxx, xxxxxxxxxx xx xxxxxx xxxxxxx vodného xxxxxxx/xxxxxxxx, xxxxx použiti roztoku/emulze x xxxxx (xxxx. x xxxxxxxxxx xxxxx) x nakonec roztoku/suspenze x jiném xxxxxxxx. Xx xxxxx xxxx xxxxxxxxxxxxx xxxxxxxxxxxxxxx xxxxxxxx. Xxxxx xxxx xx xxxxx xxxxxxx pozornost xxxxxxxxxxxx typickým znakům xxxxxxxx: xxxxxx xx xxxxxxxx, xxxxxxxxxx, metabolismus xxxx xxxxxxx xxxxxxxx xxxxx x xxxx xxxxxx xx chemické xxxxxxxxxx zkoušené xxxxx, xxxxx mohou xxxxxxxx xxxx xxxxxxx xxxxxxxxxxxxxxx, x xxxxxx na xxxxxxxx xxxxxx nebo xxxx xxxxx xxxxxxxx xxxx pokusných zvířat.
1.5 XXXXXXX
1.5.1 Počet a xxxxxxx xxxxxxxxx xxxxxx
Xxxxx xx xxxxxx provádí xxxx samostatná studie, xx xxxxx xxxxxx x xxxxx dávkové x xxxxxxxxx xxxxxxx xxxxxxx 20 xxxxxxxxx xxxxxx (10 xxxxx x 10 samců) xxx xxxxxxxxxxx podrobných xxxxxxxxxx a xxxxxxxxx xxxxxxxxxx. Xxxxxxx x xxxx xxxxx x xxxx xxxxx vybraných x xxxxxx xxxxxx xxxxx x samic xx třeba xx xxxxx xxxxxxx xxxxxxx xxxxxxx xx xxxx x použít xx x xxxxxxxxxx xxxxxxxxxxxxxxxxxxxxxxx xxxxxxxxx. V xxxxxxx, xxx xxxx x xxxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxx xxxxxx pouze u xxxxxxxxx xxxxx pokusných xxxxxx, xx xxxxx xxxxxx přiřazení xxxxxx xxxxxxxxx zvířat x xxxxxxxx xxxxxxxx xxxxxxxx xxx xxxxxxx. Xxxxx xx studie provádí x kombinaci xx xxxxxx toxicity xx xxxxxxxxxxx dávkách, xx xxxxx xxxxxx odpovídající xxxxx xxxxxxxxx zvířat, xxx xxxx možné xxxxxx cíle xxxx xxxxxx. Xxxxxxxxx xxxxx xxxxxxxxx xxxxxx xx xxxxxxx x xxxxxxxxxxxxx xxxxxxxxx xxxxxx je xxxxxx x tabulce 12. Xxxxx xx xxxxxxx utracení ve xxxxxxxxx intervalech nebo xxxxxxxxx xxxxxxxxx skupiny xx sledování xxxxxxxx xxxxxx, xxxxxxxxxxx xxxx xxxxxxxxxx výskytu toxických xxxxxx xx skončení xxxxxxxx, xxxx xx xxxxxxx dodatečná xxxxxxxxx, xx xxxxx xxxxxx xxxxx pokusných xxxxxx, xxx xx xxxxxxxx xxxxxxxxxx počet xxxxxxxxx xxxxxx požadovaných xx xxxxxxxxx x k xxxxxxxxxxxxxxxxxx xxxxxxxxx.
1.5.2 Experimentální x xxxxxxxxx xxxxxxx
Xxxxxx xx xxxx xxx xxxxxxx nejméně xxx xxxxxxxxxxxxxx a xxxxx xxxxxxxxx xxxxxxx; xxxxx xx však xxxxx xxxxxx xxxxx xxxxxxxxxxx xxxxx xxxxxx xx xxxxxxxxxxx xxxxxxx 1 000 xx/xx xxxxxxx xxxxxxxxx xx den, xxxx xxx xxxxxxxxx xxxxxxx xxxxxxx. Xxxxxx-xx k xxxxxxxxx xxxxx xxxxxx xxxxx, xxxx xxx xxxxxxxxx xxxxxxxxx studie xxx xxxxxxxxx rozpětí xxxxx, xxxxx xxxx xxx xxxxxxx. X xxxxxxxx xxxxxxxx zkoušené xxxxx xx třeba x pokusnými xxxxxxx x xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx xxxxxxx xxxxxxxx, xxxx x xxxxxxxxx zvířaty x xxxxxxxxxxxxxx skupině. Pokud xx xxx xxxxxxxx xxxxxxxx látky xxxxxxx xxxxxxxxx, xxxxxx se xxxxxxxxx xxxxxxx x xxxxxxxxx xxxxxxxx xxxxxx.
1.5.3 Xxxxxxxx xxxxxxxxxxxxx
Xxxxxxxxx xxxxxxxxxxx xxxxxxx xx xxxx xxxxxxxxx xxxxx xxxxxxxxxxx xxxx xxxxxxxxxxx xxx xxxxxxxxxxx zkoušky x xxxxxxxxx xxxxxxxxxxx xxxxxxx. Xxxxxx údaje xx xxxx xxxxxxxxxx důkaz x xxxxxxxxxx odhalit x xxxxxxxxx xxxxxxxxxxxxx xxxxx x xxxxxxx xxxxxxxxxxx doporučených xx xxxxxxxxx, jako jsou xxxx. vegetativní xxxxxxxx, xxxxxxxxxx xx smyslové xxxxxxx, xxxx úchopu x xxxxxxxxx xxxxxxxx. Xxxxxxxxx x xxxxxxxxxx xxxxxxx, xxxxx způsobují xxxxx xxxx neurotoxických xxxxxx x xxxxx xxxx xxxxxx jako xxxxxxxxx kontrolní xxxxx, xxx xxxxxx x xxxxxxxxxx
7a). Xxxxxxxxxx xxxxx xxx použít xxxxx, xxxxx xxxxxxxx xxxxxx xxxxxxxx xxxxxxx experimentálních xxxxxxx. Xxxxxxxxxx se xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxxx xxxxx. Xxxx kontrolní xxxxx xx xxxx xxx doplněny tehdy, xxxxx xxxxxxxxxxx xxxxxxxxx x průběhu xxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxx xxxxxxxxx xxxxxxx xxxx postupu.
1.5.4 Výběr xxxxx
Xxxxxx xxxxx je xxxxx xxxxxx x xxxxxxx xx předchozí xxxxxxxxx xxxxxxxx x xxxxxxxxx xxxxx dostupné xxx xxxxxxxxx xxxxxxxxxx xxxx xxxxxxx látky. Xxxxxxxx xxxxxx xxxxx xx xxxxx xxx, xxx xxxxxxxx xxxxxxxxxxxx xxxx jasné xxxxxxxxx xxxxxxx xxxxxx, aby xxxx xxxxx xxxxxxxx xxxxxxxxx odpovědi na xxxxxxx x xxxxxx xxxxx bez pozorovatelného xxxxxxxxxxxx xxxxxx (XXXXX), xxxxx xx xxxxxxxx xxxxxxxxxxx xxxxxx dávek. X xxxxxx xx xxxxx stanovit xxxxxx xxxxx tak, xxx xxxx xxxxx odlišit xxxxxxxx toxické xxxxxx xx xxxxxxx xxxxxx xx systémové xxxxxxxx. Xxxxxxx xxxx xxxxxxxxx xxx xx tři xxxxxxxxx x xxxxx xx vhodnější přidání xxxxxx zkušební xxxxxxx xxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxx (xxxx. xxxxxxxx xx faktorem 10). Xxxxxx xx xxxxx xxxx x xxxxx x odhad xxxxxx xxxxxxxx u xxxxxxx, xx-xx k dispozici.
1.5.5 Xxxxxxx zkouška
Pokud zkouška xxxxxxxxx xxxxx postupů xxxxxxxxx x xxxx xxxxxx při jedné xxxxx nejméně 1&xxxx;000 xx/xx xxxxxxx xxxxxxxxx xx xxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx x xxxxx xx xx základě údajů x xxxxxxx x xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxxxxxx, xxxx nezbytné xxxxxxxx xxxxxxxxx xxxxxx xx xxxxxxx xxx xxxxxx dávek. X xxxxxxxxx případech xxxxxxxxxxxxx xxxxxxxx u xxxxxxx xx xxxxxx použití xxxxx xxxxxx dávky x limitní xxxxxxx. X xxxxxxx xxxxxxx xxxxxxxx xxxxx, xxxx xx inhalační xxxx xxxxx xxxxxxxx, může xxx maximální xxxxxxxxxxx xxxxxx expozice xxxx xxxxxxxxx-xxxxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx. Xxx xxxxxxxxx xxxxxx xxxxxxx xxxxxx xx xxxxx xxx xxxxxxx zkoušku xxxx xxx xxxxxxx 2&xxxx;000 xx/xx.
1.5.6 Aplikace dávek
Zkoušená xxxxx xx podává xxxxxxxx zvířatům denně, 7 xxx v xxxxx, po dobu xxxxxxx 28 xxx. Xxxxxxx 5denního xxxxxxxxxxx xxxxxx xxxx kratší xxxxxxxx je xxxxx xxxxxxxxx. Xx-xx látka xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx xxxxx, xxxx by xx xxxxxxx v xxxxx xxxxx xxxxxx xxxxx xxxx vhodné xxxxxxxxx kanyly. Xxxxxxxxx xxxxxxxx tekutiny, xxxxx xxx jednorázově xxxxxxx, xxxxxx na xxxxxxxxx xxxxxxxxx zvířete. Xxxxx xx xxxxx překročit 1 xx/100 g xxxxxxx xxxxxxxxx. X xxxxxxx xxxxxxx xxxxxxx xx však možné xxxxxx x použití xx 2 xx/100 x xxxxxxx xxxxxxxxx. Xxxxx dráždivých nebo xxxxxxxx látek, xxxxx xxx xxxxxxx koncentracích xxxxxxx xxxxxxxx xxxxxx xxxxxx, xx xx xxxx xxxxx xxxxxxxx xxxxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxxxxxxx, aby xx xx všech xxxxxxxx xxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx.
X xxxxx xxxxxxxxxx xxxxxxxxxxxxxxx xxxxxx xxxx xxxxx xxxx xx xxxxx důležité xxxxxxxx, xxx xxxxxxxx xxxxxxx xxxxxxxx látky xxxxxxxxxxx xxxxxxxxxx xxxxxxx xxxxxx xxxx xxxxxx xxxx. Xx-xx zkoušená xxxxx xxxxxxxx x xxxxxx, je xxxxx xxxxxxxx bud' xxxxxxxxxx xxxxxx xxxxxxxxxxx (x xxx), xxxx konstantní xxxxxx dávky, xxxxx xxx x tělesnou xxxxxxxx pokusného zvířete. Xxxxxxx xxxx alternativy xx xxxxx xxxxxxxxx. X xxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxxxxx sondy xx xxxxx xxxxx xxxxxxx xxxxx den xxxxxxxxx ve xxxxxxx xxxx x xxxxxxx xxxxxx týdně je xxxxx xxxxx xxxxxxxxxxx xxx, aby xx xxxxxxx konstantní xxxxxx xxxxx xxxxxxxx x xxxxxxx hmotnosti pokusného xxxxxxx. Xxxxxxx-xx se xxxxxx xxxxxxxxxxx xxxxxxxx xxxxx jako předběžná xxxxxx xxx dlouhodobou xxxxxx, xxxx by xxx v xxxx xxxxxxxx xxxxxxxxx xxxxxx xxxxxx. Není-li u xxxxxx xxxxxx xxxxxxx xxxxxxxx xxxxx x xxxxx, je xxxxx xxxxxxx xxxxx xx xxxxxxx xxxxxxx xx xxxx, xxxxx xx xxxxxx překročit 24 x.
1.6 XXXXXXXXXX
1.6.1 Xxxxxxx xxxxxxxxxx a zkoušek
U xxxxxx s xxxxxxxxxx xxxxxx xx doba xxxxxxxxxx měla xxxxxx xxxx xxxxxxxxx xxxxxx. X xxxxxx xxxxxx xxxxxxxx pozorování xxxxxxxxx xxxxx 14 xxx xx xxxxxxxx aplikace. X xxxxxxxxx xxxxxx x xxxxxxxxxxx skupinách, xxxxx xxxx x xxxxxx xx xxxxxxxx xxxxxxxx xxxxxxx xxx xxxxxxxx, xx xxxxxxxxxx xxxx xxxxxx x xxxx xxxxxx.
Xxxxxxxxxx xx xxxxx xxxxxxxx xxxxxxxxxx xxxxx, aby xxxx xxxxx odhalit jakékoli xxxxxxxxxxxx xxxx xxxxxxxxxxxx xxxxxxxxxxx x co xxxxxxxx pravděpodobností. Xxxxxxxxxx xx xxxxxxx xxxxx, xxxxx možno ve xxxxxxx dobu x x xxxxxxxxxxxx x xxxx očekávaného maxima xxxxxx po podání xxxxx. Četnost klinických xxxxxxxxxx a funkčních xxxxxxx je xxxxxxx x tabulce 13. Xxxxx kinetické xxxx xxxx xxxxx xxxxxxx x předchozích studií xxxxxxxxx potřebu zvolit xxxxxx body pozorování xxxx xxxxxxx nebo xxxxxx po xxxxxxxx xxxxxxxxxx, xx xxxxx xxxxxx xxxxxx xxxxxxxx xxxx, xx xxxxx xxxxxxx xxx získat xxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxx xxxxx je xxxxx xxxxxxxxx.
1.6.1.1 Pozorování xxxxxxxxx xxxxxxxxxxx xxxxx x mortality/morbidity
U všech xxxxxxxxx xxxxxx xx xxxxxxx xxxxxx xxxxx xxxxxxx xxxxxxxxxx jejich xxxxxxxxx xxxx x xxxxxxx dvakrát xxxxx xx xxxxxxx xxxxxxxxx xxxxx pokusných zvířat xx xxxxxx xxxxxxxx xxxxxxxxx x mortality.
1.6.1.2 Xxxxxxxx xxxxxxxx xxxxxxxxxx
Xxxxxxxx xxxxxxxx pozorování se xxxxxxxx u xxxxx xxxxxxxxx xxxxxx vybraných x xxxxx xxxxxx (xxx xxxxxxx 12) xxxxxxx xxxx první xxxxxxxx (xxx xxxx xxxxx xxxxxxxxxxxxxxxxx srovnání) x xxxx x xxxxxxx xxxxxxxxxxx xxxxx xxxxxx studie (xxx xxxxxxx 13). Podrobná xxxxxxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxxxxx xxxxxx xx xxxxxxxx na xxxxx xxxxxxxxxxxx období. Xxxxxxxx klinická pozorování xx provádějí xxxx xxxxxxx xxxx xx xxxxxxxxxxx pozorovacím xxxxxxxx. Xxxxxxxxxx xx xxxxxxx xxxxxxxxxxx xxxxxx systémů xxxxxxxxx, xxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxx x xxxxx xxxxxxxxxx. Xxxxxxxxx xxxxxxxx xxxx xxxxxxxx xxxx xxx xxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx. Xx xxxxx dbát xx xx, xxx byly xxxxxxx xx xxxxxxxxxx xxxxxxxxxx xx xxxxxxxx (x xxxxxxxxxxx xxxxxxxxxxxx x xxxxxxxx) x xxx xxxxxxxxx xxxxxxxxx xxxxx, xxxxx nejsou xxxxxxxxxxx x skupině, xx které xxxxxxx xxxxx xxxxx.
Xxxxxxxxxx se xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxx, xxxxxxx xx x xxxxxxx pokusného zvířete xxx xxxxxx pozorování xxxxxxxxxxxx xxxxxxxxx xxxxx xxxxxxxxxx kritéria (xxxxxx xxxxxxxx xxxxxxxxxx "xxxxxxx"). "Xxxxxxxx xxxxxxx" xx xxxxx xxxxxxxxxx xxxxxxxxxxxxx. Xxxxxxx xxxxxxxxxx xxxxxxxx xx xxxxxxxxxxx. Xx-xx xx xxxxx, xxxxxxxxx xx xxxxxx xxxxxxxxx xxxxxxxxxxxx xxxxxxxx. Klinická xxxxxxxxxx xxxxxxxx xxxxx xxxxx xxxx, srsti, xxx x xxxxxxx, xxxxxx sekretů a xxxxxxx x xxxxxxxxxxx xxxxxx (slzení, xxxxxxx xxxxx, xxxxxxxx xxxxxx, xxxxxxxx xxxxxx dýchání xxxx xxxxxxx xxxx, xxxxxxxx příznaky xxxxxx xxxx defekace x xxxxxxxx xxxx).
Xxxxxxxxxxx se xxxxxx xxxxxxxx xxxxxxx, xxxxx xxx x xxxxxx těla, xxxxxx xxxxxxxx (xxxx. xxxxxxx xxxx xxxxxxx zkoumání xxxxxxxxxxxx xxxxxxxxxxxx xxxxxxxx) x koordinaci xxxxxx. Xxxxxxxxxxx xx xxxx xxxxx xxxxx (xxxx. xxxxxxxx, ataxie), polohy (xxxxxxxx xxxxxx) x xxxxxx xx xxxxxxxxxx, xxxxxxxx x xxxxx xxxxxxx xxxxxxxxxxx s xxxxxxxxxx, dále xxxxxxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxx, xxxxx xxxx xxxxx, xxxxxxxxxx x xxxxxxx (xxxx. xxxxxxxxxx xxxxxxx, xxxxxxxxxx xxxxxx xxxxx nebo opakovaného xxxxxxxx) xxxx xxxxxxxxxx xxxxxxx (xxxx. xxxxxxx xxxx xxxxxxxxxx xxxxxxxxx, xxxxxxxxxxxxxxx, xxxxxx xxxxxxxx, xxxxxxxx zvuků) xxxxx xxxxxxxxxx.
1.6.1.3 Funkční zkoušky
Podobně xxxx xxxxxxxx klinická xxxxxxxxxx xx x xxxxxxxxxxxx pokusných xxxxxx xxxxxxxxx k xxxxx xxxxxx xxxxxxxx i xxxxxxx xxxxxxx - xxxxxxx xxxx xxxxxxxx x potom xxxxxxxx xx xxxxx xxxxxxxxx (xxx xxxxxxx 12).
Xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx xxxxxx xx xxxxxx xxxxxx (xxx tabulka 13). Xxxx xxxx xxxxxxxxxx xxxxxxxxxx v xxxxxxx 13 xx xxxxxxx xxxx funkční xxxxxxxxxx xxxxxxxxx zotavovací xxxxxxx, a xx xxxxx xxxx xxxxxxxxxx xxxxxxxxx. Xxxxxxx xxxxxxx xxxxxxxx reakce xx xxxxx xxxxxxxx podněty [xxxx. xxxxxxxx, xxxxxxx x dotykové (případně xxxxxxxx) xxxxxxx
7a)], xxxxxxxxx xxxx stisku
7a) x xxxxxxxxx xxxxxxxxx xxxxxxxx
7a). Xxxxxxxxx xxxxxxxx xx xxxx pomocí xxxxxxxxxxxxx xxxxxxxxx schopného xxxxxxx xxx xxxxxxx, xxx x xxxxxxx této xxxxxxxx. Xxxxx xx xxxxxxx jiný xxxxxx, xxx by xxx xxxxxxxxxxxxx a je xxxxx xxxxxxxx xxxx xxxxxxxxx x xxxxxxxxxxxx. Xxxxx xxxxxxxx xx xxxxx otestovat, xxx xx xxxxxxxxx jeho xxxxxxxxxxxx po xxxx xxxxxx xxxxxx a xxxxxxxxxx x xxxxxxxxx xxxxxxxxx. Další xxxxxxxxxxx x xxxxxxxxx, xxxxxxx xx xxx xxxxx, xxxx xxxxxxx x xxxxxxxxxxx odkazech. Xxxxx xxxxxxxxxx xxxxx xxxxx (xxxx. xxxxx o xxxxxx xxxx xxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx, xxxxxxxxxxxxxxx xxxxx, xxxx xxxxxxxxxxxxx xxxxxx), které xx ukazovaly xx xxxxxxxxxxx xxxxxxxxxxxx xxxxxx, xx nutné xx xxxxxx xxxxxxxxxxxxx xxxxxxxxx xxxxxx xxxxxxx účinků xxxxxx xxxxxxxxx specializovanějších xxxxxxx smyslových x xxxxxxxxxxx xxxxxx xxxx xxxxx a xxxxxx. Xxxxx xxxxxxxxx x xxxxxxxxxxxxxxxxxxx xxxxxxxxx a xxxxxx používání je xxxxxxx x literatuře
7a).
Ve xxxxxxxxxxx xxxxxxxxx xxx xxxxxxx xxxxxxx xxxxxxxxxx xxxxxx toxicity x xxxxxx xxxx, xxxxx xx významně xxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx, x xxxx zkoušky xxxxxxx. Vyřazení xxxxxx xxxxxxxxx xxxxxx x xxxxxxxxx xxxxxxx xx xxxxx xxxxxxxxx.
1.6.2 Xxxxxxx xxxxxxxx x xxxxxxxx xxxxxx x vody
U xxxxxx s xxxxxx xxxxxx do 90 xxx xx xxxxxxx xxxxxxx zvířata váží xxxxxxx xxxxxx týdně x xxxxx týden xx xxxxxx provádí xxxxxx xxxxxxxx xxxxxx (xxxxxx spotřeby vody xx xxxxxxx xxxxx, xx-xx xxxxxxxx látka xxxxxxxxxx xxxxxxxxxxxxxxx tohoto xxxxx). U xxxxxxxxxxxx xxxxxx xx xxxxxxx xxxxxxx xxxxxxx xxxx xxxxxxx xxxxxx týdně xxxxx xxxxxxx 13 xxxxx x poté xxxxxxx jednou za 4 xxxxx. Xxxxx xxxxxxx 13 týdnů xx xxxx xxxxxxxx xxxxxx (měření xxxxxxxx xxxx xx xxxxxxx xxxxx, xx-xx zkoušená xxxxx aplikována prostřednictvím xxxxxx xxxxx) x xxxx přibližně v xxxxxxxxxxxx intervalech, xxxxx xx změny xxxxxxxxxxx xxxxx nebo xxxxx xxxxxxx xxxxxxxxx nevyžádají xxxx xxxxxxxx.
1.6.3 Xxxxxxxxxxxxxx xxxxxxxxx
X studií xxxxxxx xxx 28 xxx xx xxxx xxxxxxxx xxxxxxxx xxxxx a xxxx ukončením xxxxxx xxxxxxx xxxxxxxxxxxxxx xxxxxxxxx xxxxxx oftalmoskopu xxxx xxxxxx xxxxxxxx nástroje, x xx xxxxxxx x xxxxx xxxxxxxxx xxxxxx, xxxxxxx xxxx x xxxxx pokusných xxxxxx ze xxxxxx x xxxxxxx xxxxxx x z xxxxxxxxxxx xxxxxx. Xxxxx se xxxxxx xxxxx na xxxxx xxxx xxxxx xxxxxxxx xxxxxxxx ukazují xx nutnost xxxxxxxxx xxx, vyšetří se xxxxxxx pokusná xxxxxxx. X xxxxxxxxxxxx studií xx xxxxxxxxxxxxxx xxxxxxxxx xxxxxxx xx 13. xxxxx xxxxx xxxxxxxxx xxxxxx. Xxxxxxxxxxxxxx xxxxxxxxx xxxx nutné provádět xxxxx, jsou-li již x xxxxxxxxx xxxxx x xxxxxx xxxxxxx xxxxxxxx xxxxxx x xxxxxxxxx úrovněmi dávek.
1.6.4 Xxxxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx
Xxxxx se xxxxxx xxxxxxxxxxxxx xxxxxxx x xxxxxxxxx se studií xxxxxxxxx toxicity po xxxxxxxxx xxxxx, xxxxxxx xx hematologické xxxxxxxxx x xxxxxxxxx klinických xxxxxxxxxxxxx parametrů tak, xxx xx uvedeno x xxxxxxxxx xxxxxx xxxxxx xxxxxxxxx xxxxxxxx. Xxxxxxxxx xxxxxx xx xxxxxxx tak, xxx xx xxxxxxxxxxxxxx jakékoliv xxxxxx xx xxxxxxx xxxxxx a xxxxxxx.
1.6.5 Xxxxxxxxxxxxxx
Xxxxxxxxxxxxxxxx xxxxxxxxx xx xxxxxxx xxx, xxx xxxxxxxx a xxxxxxxxx xxxxxxxxxx xxxxxxxxx v xxxxx xxxx studie xxxxx xxxx xx xxxx. Tkáně xxxxxxx 5 xxxxxxxxx xxxxxx xxxxxxx pohlaví x xxxxx xxxxxxx (xxx xxxxxxx 12 x xxxxx xxxxxxxx) xx xxxxxx xx xxxx xx použití xxxxxx xxxxxxxxxx perfuzních a xxxxxxxxx xxxxxxx
7a). Zaznamenají xx jakékoliv výrazné xxxxx. Xxxxx xx xxxxxx xxxxxxx xxxx xxxxxxxxxx studie xxxxxxxxxxxxx xxxx studie xxxxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx, xxx xxxxxx zbytek xxxxxxxxx xxxxxx xxx' xx xxxxxxxxxxx xxxxxxxxxxxxxxxxxx
7a), neuropatologickým
7a), xxxxxxxxxxxxxx
7a), xxxx xxxxxxxxxxxxxxxxxxxx
7a) xxxxxxxx, xxxxx xxxxx xxxxxxx xxx xxxxxxx xxxxxxx a xxxxxxxxx, xxxxx zvýšit xxxxx xxxxxxxx xxxxxxxxxxxxx x xxxxxxxxxxxxxxxxx xxxxxx. Xxxx xxxxxxxxx xxxxxxx xxxx xxxxxxx xxxxxxxx xxxxx, xxxxx xxxxxxxxx pozorování xxxx xxxxxxxxx xxxxxx xxxxxxx xx xxxxxxxxxx xxx xxxx cílovou xxxxxxxxx neurotoxicity
7a). Xx xxxx xxxxx xxxxxx xxxxxxxxx zvířat použít x xxxxxx xxxxxxxxxxxx xxxxxxxxxx, xxxxx xxxx xxxxxxx x xxxxxx xxxxxx xx xxxxxxxxx xxxxx.
X všech tkáňových xxxxxx zalitých parafinem xx xxxxxxx xxxxx xxxxxx xxxxxxx, xxxx. xxxxxx hematoxylinu x xxxxxx (H&E), x xxxxxxxxxxxxx vyšetření. Jsou-li xxxxxxxxxx xxxx existuje-li xxxxxxxxx xx xxxxxxxx xxxxxxxxx neuropatie, xxxxxxx xx vzorky xxxxxxxxxxx xxxxx xxxxxxxx xx xxxxxxxxx (vosků). Xxxxxxxx xxxxxxxx xxxxx rovněž xxxxxxxx xx xxxxx xxxxx, xxxxx xx xxxxx xxxxxxxx, xxxx xx xxxxxxx xxxxxx xxxxxxxxx xxxxxxx barvení. Xxxxxx k xxxxxx xxxxxxx xxxx, xxxxx xx xxxxx xxxxxxxx, xxx xxxxxx x xxxxxxxxxx
7a). X xxxxxxxxx xxxxxxxxxxxxxxxxxx xxxx xxxxxxxxxxx xxxxx xxxx xxxxxxx x xxxxxxxxxxxx speciální xxxxxxx
7a).
X reprezentativních xxxx xxxxxxxxxxx x xxxxxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxxx xxxxxxxxxxxx xxxxxxxxx
7a). Xxxx xxxxxxxxxxx xxxxxxx xxxxxxx xxxxx: xxxxxx xxxxx, střední část xxxxx, xxxxxx xxxx xxxxxxxxxxx, xxxxxxx mozek, xxxxxxx, Xxxxxxx xxxx, xxxxxxxxxxx xxxxx, oko xx xxxxxxxx xxxxxx x sítnicí, xxxxx x oblasti cervikálního x lumbálního xxxxxxxx, xxxxxxxx xxxxxxxx xxxxxxx, xxxxxxxx a xxxxxxxxx xxxxxxxx xxxxxx, xxxxxxxxxx xxxx x. ischiadicus x proximální xxxx x. xxxxxxxx (x xxxxxxx xxxxxx) x x tibialis x xxxxxxx lýtkového svalu. Xxxx míchy a xxxxxxxxxxx xxxxx xx xxxx zahrnovat jak xxxxxx, xxx x xxxxxxx xxxx. Xxxxxxxxx xx xxxxx věnovat xxxxxxxxxx cév x xxxxxxx xxxxxxxxx xxxxxxx. Xxxxxx xx xxxxxxx xxxxxx x xxxxxxxxxx xxxxxxxx, x xx xxxxxxx x xxxxxxxxx xxxxx. Xxxxxxxx xxxxxxxxx xx nutné xxxxxxx xxxxxx x xxxxxxxx x xxxxxxxxx xxxxxxxxxx x xxx xxxxxxxxxx x xxxxxxx XXX x XXX, o xxxxx xx známo, xx xx xx xxxx xxxxxxxxxxxx látky xxxxx xxxx.
Xxxxxxxxx x xxxxxxxxxxxxxxxxxx xxxxxxx, které xxxxxxx vyplývají x xxxxxxxx xxxxxxxx látkám, xxx xxxxxx x xxxxxxxxxx
7a). Xxxxxxxxxx xx xxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxx, xxx kterém xx xxxxxxxxx xxxxxxx xxxxxx xxxx xx xxxxxxx s xxxxxxx xxxxxx xx xxxxxx xxxx z xxxxxxxxx xxxxxxx. Xxxxxx-xx xx xxxxxxxx x těchto xxxxxx xxxxxxxx žádné xxxxxxxxxxxxxxxx xxxxx, xxxx xxxxx xxxxxxxx xxxxx xxxxxxx. Xxxx-xx xxxxxxxx xx skupině s xxxxxxx xxxxxx neuropatologické xxxxx, xx xxxxx xxxxxxxx okódovat x xxxxxxxx vzorky ze xxxxx xxxxxxxxxxx xxxxxxxxxx xxxxx xx xxxxxx xx xxxxxxx a xxxxxx xxxxxx.
Xxxxx xx xxxxx kvalitativního xxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxxxxxxxxxxxxxx xxxx, xxxxxxx xx xxxxx vyšetření xxxxx xxxxxxx xxxxxxxxx systému, xxxxx xxxxxxxx xxxx xxxxx. Okódují se xxxx xx všech xxxxxxxxx xxxxxx xx xxxxx potenciálně xxxxxxxxxx xxxxxxx x xxxxxxx x xxxxxxxx xxxxxx xxx xxxxxxxx xxxx. Xxxxxxxxx xx xxxxxxx x xxxxxxxxx všech xxxx. Xx xxxxxxxxxx xxxxx xxxxxxx ze xxxxx dávkových skupin xx xxx xxxxxxx x provede xx xxxxxxxxxxx xxxxxxx xx xxxxxx xxxxxxxxxxx vztahu xxxxx-xxxxxx. X xxxxx xxxx xx xxxxxx xxxxxxxx různých stupňů xxxxxxxxxx.
Xxxxxxxxxxxxxxxx xxxxxxxx xx xxxxxxxxx x xxxxxxxx x pozorováním a xxxxxxx xxxxxxx x xxxxxx xxxxx x xxxxxxx údaji z xxxxxxxxxxx x xxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx xxxxxxxx xxxxx.
2 DATA
2.1 XXXXXXXXXX XXXXXXXX
Xxxxxx se xxxxxxxxxx xxxx. Data xx shrnou do xxxxxxx, přičemž se xxx xxxxxx xxxxxxxxxxxxxx xxxx kontrolní xxxxxxx xxxxx xxxxx xxxxxxxxx xxxxxx xx xxxxxxx xxxxxxx, počet xxxxxxxxx xxxxxx uhynulých x xxxxxxx zkoušky nebo xxxxx xxxxxxxxx xxxxxx xxxxxxxxxx x xxxxxxxxx xxxxxx a doba xxxxxxx xxxx xxxxxxxxx xxxxxxxx, xxxxx xxxxxxxxx xxxxxx xxxxxxxxxxxx příznaky xxxxxxxx, xxxxx xxxxxxxxxx xxxxxxxx toxicity, xxxxxx xxxx xxxxxxx, trvání, xxxx x závažnosti xxxxxxxxxxx příznaků toxicity, xxxxx xxxxxxxxx zvířat xxxxxxxxxxxx xxxx, včetně xxxx a xxxxxxxxxx xxxx (xxxx).
2.2 HODNOCENÍ X XXXXXXXXXXXX XXXXXXXX
Xxxxxxxx xxxxxx xx xxxxx xxxxxxxxxx x hlediska xxxxxxx, xxxxxxxxxx x xxxxxxxx neurobehaviorálních x xxxxxxxxxxxxxxxxxx xxxxxx (xxxxxx x neurochemických xxxx xxxxxxxxxxxxxxxxxxxxx účinků, xxxx-xx xxxxxxxxx doplňující vyšetření) x x hlediska xxxxxxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx. Xx-xx xx xxxxx, xx xxxxx xxxxxxxxxx xxxxxxx xxxxxxxx xxxxxxxx x xxxxxx xxxxxxxxxx statistickými xxxxxxxx. Xxxxxxxxxxx xxxxxx xx xxxxx zvolit během xxxxxxxxx xxxxxx.
3 XXXXXXX XXXXXX, XXXXXXXX POKUSU X XXXXXXXXX XXXXXX
X xxxxxxx x xxxxxxxxxxx xxxxxxxx xxxxxxxx
9),10) xxxx xxx zpracován xxxxxxx xxxxxx x o xxxxxxx pokusu je xxxxx xxxx xxxxxxxx.
3.1 Xxxxxx x xxxxxxx xxxxxx xxxxxxxx xxxx xxxxxxxxx:
Xxxxxxxx látka:
- fyzikální xxxxxxxxxx (xxxxxx isomerie, xxxxxxx x xxxxxxxxx-xxxxxxxxxx xxxxxxxxxx),
- xxxxx o xxxxxxxx.
Xxxxxxxxx (xxxxx xxxx xxxxxxx):
- xxxxxxxxxx volby xxxxxxxx.
Xxxxxxx xxxxxxx:
- xxxxxxx xxxxx x kmen,
- xxxxx, xxxxx a xxxxxxx pokusných zvířat,
- xxxxx, xxxxxxxx chovu, xxxxxxxxxxxx, krmivo xxx.,
- xxxxxxxx xxxxxxxxxxxx xxxxxxxxx xxxxxx na začátku xxxxxxx.
Xxxxxxxx xxxxxxxx:
- podrobnosti x úpravě směsi xxxxxxxx xxxxx xx xxxxxxxx xxxxxx, xxxxxxxx xxxxxxxxxxx, xxxxxxxxx x xxxxxxxxxx xxxxxxxxx,
- xxxxxxxxxxx xxxxxxxxxxxx dávek, včetně xxxxxxxxxxx o xxxxxxxx, xxxxxx x fyzikální xxxxx aplikovaného materiálu,
- xxxxxxxxxxx x způsobu xxxxxxxx xxxxxxxx látky,
- xxxxxxxxxx výběru xxxxxx xxxxx,
- xxxxxxxxxx xxxxxxx xxxxxxxx x trvání xxxxxxxx,
- xxxxxxxx xxxxxxxxxxx xxxxxxxx xxxxx x xxxxxx xxxx pitné xxxx (xxx) na xxxxxxxxx xxxxx xxxxx x xx/xx tělesné xxxxxxxxx,
- xxxxxxxxxxx o xxxxxx x xxxxxxx xxxx.
Xxxxxxxxxx x zkušební xxxxxxx:
- xxxxxxxxxxx x xxxxxxxxx xxxxxxxxx zvířat x xxxxxxxxxxxx xxxxxx xx xxxxxxxxx s xxxxxxx,
- xxxxxxxxxxx o xxxxxxxxx xxxxxxxxxx, xxxxxx xxxxxxxx x posuzovacích xxxxxxx pro xxxxxxxxxx xxxxxx x xxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx,
- xxxxxxxxxxx x xxxxxxxxx xxxxxxx pro měření xxxxxx různých xxxxxxxxxx xxxxxx na xxxxxxxx xxxxxxx (např. sluchové, xxxxxxx a xxxxxxxx), xxx xxxxxxxxx xxxx xxxxxx, xxxxxxxxx xxxxxxxx (xxxxxx podrobností x xxxxxxxxxxxxx zařízeních xxx xxxxxxxxxx xxxxxxxx) x xxxxx xxxxxxx xxxxxxx,
- xxxxxxxxxxx xxxxxxxxxxxxxxxx xxxxxxxxx, xxxxxxxxxxxxxxx a xxxxxxxxxxxxx xxxxxxxxx s příslušnými xxxxxxxxx (normálními) xxxxxxxxx,
- xxxxxxxxxxx x specifických xxxxxxxxxxxxxxxxxxx, neuropatologických, xxxxxxxxxxxxxxx xxxx elektrofyziologických xxxxxxxxx.
Xxxxxxxx:
- xxxxxxx hmotnost x xxxx xxxxx, xxxxxx xxxxxxx hmotnosti v xxxx xxxxxxxx,
- xxxxxxxx xxxxxx x xxxxxxxx xxxx,
- xxxxx o xxxxxxxxx xxxxxxxx podle xxxxxxx x xxxxxx xxxxx, xxxxxx xxxxxx xxxxxxxx xxxxxxxx xxxx xxxxxxxxx,
- xxxxxx, xxxxxxxxx x trvání (xxxx xxxxxxx a xxxxxxxx xxxxxx) xxxxxxxxxx xxxxxxxxxx xxxxxx (zda jsou xxxxxx xxxx xxxxxxxx),
- xxxxxxxx xxxxx xxxxx xxxxxxxx funkčních xxxxx,
- xxxxxxx xxxxxx,
- xxxxxxxx xxxxx všech neurobehaviorálních, xxxxxxxxxxxxxxxxxx a neurochemických xxxx elektrofyziologických výsledků, xxxx-xx x xxxxxxxxx,
- xxxxx o xxxxxxxx x metabolismu, xxxx-xx x dispozici,
- xxxxxxxxxxx xxxxxxxxxxx xxxxxxxx, xxx xx xx xxxxx.
Xxxxxxx x interpretace xxxxxxxx.
- xxxxxxxxx x xxxxxxxxxx xxxxxx xx xxxxx,
- xxxxxx jakýchkoliv xxxxxxx xxxxxxxxx xxxxxx xxx xxxxxx xxxxxxxx xx xxxxxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx,
- xxxxxxx xxxxxx bez pozorovatelných xxxxxxxxxxxx účinků (XXXXX),
- xx xxxxxxx xxxxx xxxxxxxxx vyjádření o xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxx xxxxx.
Xxxxxx.
Xxxxxxx 12: Xxxxxxxxx xxxxx xxxxxxxxx xxxxxx na xxxxxxx, xxxxxxx-xx se xxxxxx xxxxxxxxxxxxx xxxxxxxxxx xxxx x xxxxxxxxx x xxxxxxx xxxxxxxx
| &xxxx;
|
Xxx xxxxxxxxx xxxxxx xxxxxxxxxxxxx:
|
| &xxxx;
|
|
Xxxxxxxxxxx xxxxxx x&xxxx;28xxxxx xxxxxx
|
Xxxxxxxxxxx xxxxxx x&xxxx;90xxxxx xxxxxx
|
Xxxxxxxxxxx xxxxxx se studií xxxxxxxxx toxicity
|
|
Počet xxxxxxxxx xxxxxx xx xxxxxxx
|
10 xxxxx x 10 xxxxx
|
10 xxxxx a 10 xxxxx
|
15 samců x 15 xxxxx
|
25 xxxxx a 25 xxxxx
|
|
Xxxxx xxxxxxxxx zvířat xxxxxxxxx x&xxxx;xxxxxxxxx xxxxxxxxx, xxxxxx podrobných klinických xxxxxxxxxx
|
10 samců a 10 xxxxx
|
10 xxxxx x 10 xxxxx
|
10 xxxxx x 10 xxxxx
|
10 xxxxx x 10 xxxxx
|
|
Xxxxx xxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxx xx xxxx a xxxxxxxxxxxxxxxxxxxxx vyšetření
|
5 xxxxx x 5 xxxxx
|
5 xxxxx a 5 xxxxx
|
5 xxxxx x 5 samic
|
5 xxxxx x 5 xxxxx
|
|
Xxxxx xxxxxxxxx xxxxxx vybraných x&xxxx;xxxxxxxxxx toxicity xx xxxxxxxxx xxxxx subchronické/chronické, x&xxxx;xxxxxxxxxxxxxxx xxxxxxxxx, klinickému xxxxxxxxxxxxx vyšetření, k histopatologickému xxxxxxxxx atd., xxx xx xxxxxxx x&xxxx;xxxxxxxxxxx Xxxxxxxxxxxx
|
|
5 xxxxx a 5 xxxxx
|
10 xxxxx* x 10 xxxxx*
|
20 xxxxx* a 20 xxxxx*
|
|
Xxxxxxxx xxxxxxxxxx xxxxxxxxxx
|
5 xxxxx a 5 xxxxx
|
|
|
|
* Zahrnuto xx xxx xxxxxxxxx xxxxxx xxxxxxxxx k xxxxxxxxx xxxxxxxxx a xxxxxxxxxx xxxxxxxxxx pozorování xxxx xxxxxxx studie xxxxxxxxxxxxx.
Xxxxxxx 13 - Četnost xxxxxxxxxx xxxxxxxxxx a xxxxxxxxx xxxxx
|
|
|
|
|
|
|
|
|
X xxxxx xxxxxxxxx xxxxxx
|
Xxxxxxx zdravotní xxxx
|
Xxxxx
|
Xxxxx
|
Xxxxx
|
Xxxxx
|
|
Xxxxxxxxx/xxxxxxxxx
|
Xxxxxxx xxxxx
|
Xxxxxxx denně
|
Dvakrát denně
|
Dvakrát xxxxx
|
|
X všech xxxxxxxxx xxxxxx xxxxxxxxx x&xxxx;xxxxxxxx xxxxxxxxxxx
|
Xxxxxxxx xxxxxxxx xxxxxxxxxx
|
- xxxx první expozicí
- x&xxxx;xxxxxxx 8 x xx podání xxxxx x&xxxx;xxxx xxxxxxxxxxxx nejvyššího xxxxxx
- 7. x 14. xxx po xxxxxxxx xxxxxxxxx
|
- před xxxxx xxxxxxxx
- xxxx xxxxxx týdně
|
- před xxxxx xxxxxxxx
- jednou xxxxx xxxxxxx nebo xxxxxxx týdne expozice
- xxxx xxxxxxx
|
- před xxxxx xxxxxxxx
- xxxxxx xx xxxxx xxxxxxx xxxxxx xxxxxxxx
- xxxx xxxxx tři xxxxxx
|
|
Xxxxxxx xxxxx
|
- xxxx xxxxx xxxxxxxx
- x&xxxx;xxxxxxx 8 x xx xxxxxx xxxxx v době odhadovaného xxxxxxxxxx xxxxxx
- 7. x 14. den xx xxxxxxxx xxxxxxxxx
|
- xxxx xxxxx xxxxxxxx
- xxxxx xxxxxxxx xxxxx xxxxxxxx xx xxxxxxxx xx xxxxx xxxxxx xxxxxxxx
|
- xxxx první xxxxxxxx
- jednou xxxxx xxxxxxx xxxx xxxxxxx xxxxx xxxxxxxx
- xxxx xxxxxxx
|
- před xxxxx xxxxxxxx
- xxxxxx xx xxxxx xxxxxxx xxxxxx xxxxxxxx
- xxxx každé xxx xxxxxx
|
Xxxxxxx xxxx xxxxxxxx x xxxxxxxxxxx xxxxxxxxxx x historickém xxxxx.