Právní předpis byl sestaven k datu 31.01.2020.
Zobrazené znění právního předpisu je účinné od 01.01.2020 do 31.01.2020.
Vyhláška o způsobu předepisování léčivých přípravků, údajích uváděných na lékařském předpisu a o pravidlech používání lékařských předpisů
54/2008 Sb.
ČÁST PRVNÍ - OBECNÁ USTANOVENÍ
Úvodní ustanovení §1
Zacházení s lékařskými předpisy §2
Zacházení s lékařskými předpisy označenými modrým pruhem §3 §4
ČÁST DRUHÁ §5 §6 §6a §7 §8 §9 §10 §11 §11a §12 §13 §14 §15 §16
ČÁST TŘETÍ - PŘEDEPISOVÁNÍ LÉČIVÝCH PŘÍPRAVKŮ ZA ÚČELEM POSKYTOVÁNÍ VETERINÁRNÍ PÉČE
Způsob předepisování §17
Údaje uváděné na receptu §18
Údaje uváděné na předpisu pro medikované krmivo §19
Uchovávání předpisů pro medikované krmivo §20
Údaje uváděné na předpisu pro veterinární autogenní vakcíny §21
Uchovávání předpisů pro veterinární autogenní vakcíny §22
Předepisování léčivých přípravků za účelem jejich distribuce chovatelům §23
ČÁST ČTVRTÁ - PŘECHODNÁ, ZRUŠOVACÍ A ZÁVĚREČNÁ USTANOVENÍ
Přechodná ustanovení §24
Zrušovací ustanovení §25
Závěrečné ustanovení §26
Příloha č. 1 - Vzor receptu
Příloha č. 2 - Vzor žádanky
č. 405/2008 Sb. - Čl. II
Xxxxxxxxxxxx xxxxxxxxxxxxx xx xxxxxxxxxx x Xxxxxxxxxxxxx xxxxxxxxxxx, Ministerstvem xxxxxx, Xxxxxxxxxxxxx vnitra, Xxxxxxxxxxxxx xxxxxxxxxxxxx x Xxxxxxxxxxxxx xxxxxxx xxxxxxx xxxxx §114 odst. 3 x k xxxxxxxxx §80 zákona x. 378/2007 Xx., x xxxxxxxx x x xxxxxxx některých xxxxxxxxxxxxx xxxxxx (xxxxx x léčivech):
ČÁST PRVNÍ
OBECNÁ XXXXXXXXXX
§1
Xxxxxx xxxxxxxxxx
(1). Xxxx xxxxxxxx xxxxxxx způsob xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxx xxxxxxx xx lékařském xxxxxxxx x pravidla xxxxxxxxx lékařských xxxxxxxx.
(2). Xxx xxxxxxxxxxxxx léčivých xxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxx předpisy1), x xx
x) xxxxxxx xxxxxx xxx xxxxxxxxxxxxx
1. léčivých xxxxxxxxx xxxxxxxxxxxx omamné xxxxx xxxxxxxx xx xxxxxxx X2) (xxxx xxx "omamné látky") xxxx psychotropní látky xxxxxxxx do xxxxxxx XX3) (xxxx xxx "xxxxxxxxxxxx látky"), xxxxx xxxx xxxxxxxx modrým xxxxxx; xxxx xxxxxx xxxxxxx xx uveden x příloze č. 1 této xxxxxxxx,
2. humánních xxxxxxxx xxxxxxxxx s xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxx 1, xx xxxxxx xxxxxxxxxxx xxxxxxxxxxx služeb, x xx x pro xxxxxx xxxxxxxxx výdej xxxxx §6 xxxx. 4,
3. xxxxxxxxxxxxx léčivých xxxxxxxxx x xxxxxxxxx xxxxxxxx xxxxxxxxx, x xxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x xxxx 1, za účelem xxxxxxxxxxx veterinární xxxx, x xx i xxx xxxxxx opakovaný xxxxx xxxxx §6 xxxx. 4,
x) objednávky xxxxxxxxxxxxx xxxxxxxxxxx xxxxxx (xxxx xxx "poskytovatel") x xxxxxxxxx xxxx xxxxxxxxxxx xxxx xxxxxxxxxxx xxxxxxxxx veterinární xxxxxxxx5), xx léčivé xxxxxxxxx, xxxxxx xxxxxxxxxxxx xxxxxxxxx, x xxxxxxxx xxxxxxxx xxxxxxxxx uvedených x xxxxxxx a) xxxx 1 (xxxx jen "xxxxxxx"),
x) žádanky na xxxxxx přípravky xxxxxxx x xxxxxxx x) xxxx 1, xxxxx xxxx xxxxxxxx xxxxxx xxxxxx; xxxx této xxxxxxx je uveden x příloze č. 2 této xxxxxxxx.
(3) Xxx předepisování xxxxxxxx přípravků xxx xxxx xxxxxx
x) xxxxxx x xxxxxxxxxxxx podobě (xxxx jen "xxxxxxxxxxxx xxxxxx") zaslaný xxxxxxxxxxxxxx xxxxxxx centrálnímu xxxxxxxx xxxxxxxxxxxxxx xxxxxxx6) xxxxxxxxx xxxxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxxxxxxxx xxxxxx podle xxxxxx právního xxxxxxxx7) (xxxx xxx "xxxxxxxxxxxx xxxxxx"), nebo
b) žádanku x elektronické podobě (xxxx xxx "elektronická xxxxxxx") xxxxxxxx předepisujícím xxxxxxx a opatřenou xxxxxxxxxx xxxxx přiděleným xxxxxxxxxxxxxx, xx-xx xxxxxxxx x xxxxx xxxxxxx xxxxxxxxxx xxxx xxxxxx xxxxxxxxxxxxxx zařízení xxxxxxx, xxxxx xx xxxx xxxxxxxx; nebo xxxxxxxxxx xxxxxxxxxxxxx podpisem, xx-xx xxxxxxxx xxxxxxx xxxx xxxx xxxxxxx xxxxxxxxxxx xxx,
xx předpokladu, xx xxxxxxx xxxxxxxxxxx xxxxx §6 xxxx 13.
(4) Xx xxxxxxxxx předpisu x xx xxxxxx x xxxxxxx xxxxxxx xxx xxxxxxxx znaky xxxx xxxxx, které xx xxxxxxxxx xxxxxxxxx xxxxx vyplňovaných xxxxxxxxxxxxxx xxxx xxxxx by xxxx reklamní xxxxxxxxx.
(5) Xxxxxxxx xxxxxxx, s xxxxxxxx lékařského xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx, xxx xxxxxxx xxxxx xxxx xxxxxxxx xxxxxxxxxx xxxxx.
§2
Xxxxxxxxx s xxxxxxxxxx xxxxxxxx
Xxxxxxxx xxxxxxxx se xxxxxxxx xxx, aby xx xxxxxxxxx jejich xxxxxx xxxx xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxx. Nevyplněné lékařské xxxxxxxx xxxxx xxxxxxx xxxxxxxx xxxxxxxxxxxxx, xxxxxxx xxxx xxxxxxxxx xxxxx xxxxxxxxx vykonávat odborné xxxxxxxxxxx činnosti5).
Xxxxxxxxx x xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx
§3
(1) Xxxxxx x xxxxxxxxxx xxxxxxxxxx předpisů xxxxxxxxxx xxxxxx xxxxxx xxxxxxxxxxx xxxxxx příslušné xxxxxx xxxxx xxxx x xxxxxxxxxx xxxxxxxxxx x xxxxxxx xxxxxxxxxxx xxxxxxx xxxxxx xxxxxxxxx, x xx na xxxxxxx xxxxxxxxxx xxxxxxxxxxxxx xxxx xxxxxxxxx xxxx xxxx xxxxxxxxxxx xxxx xxxxxxxxxxx k xxxxxx xxxxxxxxx xxxxxxxxxxxxx činností5) (xxxx xxx "xxxxxxxxx xxxxx") x místem xxxxxx xxxxxx činností xx správních obvodech xxxxxxxx xxxxx obcí x xxxxxxxxxx xxxxxxxxxx8).
(2) Xxx zabezpečení xxxxxxx xxxxxxxxxx lékařských předpisů xxxxxxxxxx modrým pruhem xxxxxxxxx obecní xxxxx xxxx x xxxxxxxxxx xxxxxxxxxx xxxxxx pohotovostní xxxxxx v rozsahu xxxxxxx xxxxx xxxxxx xxxxxx xxxxxxx distribuce xx xxxxxxxxx xxxxxxxxxx xxx.
(3) Xxxxxxxx předpisy xxxxxxxx modrým xxxxxx xxxxxxxx xxxxxxxxxxx xxxxx xxxxx xxxxxxxxx x přílohách č. 1 a 2 xxxx xxxxxxxx x xx výrobce xx xxxxxxx pověřený xxxxxxxxxxx xxxxxxxx úřadu obce x xxxxxxxxxx působností. Xxxxxxxx xxxxxxxxxxx xx xxxxxxx výrobci xxx xxxxxxxx xxxxxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxx xxxxxxxxx x převzetí potvrdí xxxxxxxx x xxxxxxx xxxxxxx xxxxxxxx úřadu xxxx s xxxxxxxxxx xxxxxxxxxx.
(4) Obecní xxxx xxxx s rozšířenou xxxxxxxxxx lékařské xxxxxxxx xxxxxxxx xxxxxx xxxxxx xx převzetí xxxxxxxxx x vyzve oprávněnou xxxxx k xxxxxx xxxxxxxxxx. Lékařské xxxxxxxx xxxxxxxx xxxxxx xxxxxx xxxxx xxx xxxxxxxx xxxxx xxxx s xxxxxxxxxx působností vydány xxxxx xxxxxxxxxx xxxxxx xxxx xxxxxx pověřeným xxxxxxxxx8).
(5) X vydání xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxx xxxxxx xxxx xxxx x xxxxxxxxxx xxxxxxxxxx xxxxx tiskopisů, která xxxxxxxx údaje x xxxxx xxxxxxxx lékařských xxxxxxxx, včetně jejich xxxxxxxxxx xxxxx x xxxxxxxxxxxxx údaje x xxxxxxxxx xxxxx. Převzetí xxxxxxxxxx xxxxxxxx xxxxxxxxxx xxxxxx xxxxxx xxxxxxx xxxxxxxxx xxxxx xxxx xxxx xxxxxxxx xxxxxxxx8) xx xxxxxxxxx xxxxxxxxxx x podpisem v xxxxx xxxxxxxxx.
(6) Xxxxxx xxxx odcizení nevyplněného xxxxxxxxxx předpisu označeného xxxxxx xxxxxx se xxx xxxxxxxxxx xxxxxxx xxxxxx xxxxxxxx xxxxx xxxx x xxxxxxxxxx xxxxxxxxxx, xxxxx tyto xxxxxxxxx xxxxxxxxx xxxxx xxxxx, x současně xx xxxx ztráta xxxx odcizení oznámí x Xxxxxxx České xxxxxxxxx.
§4
(1) Xxxxxxxx-xx xxxxxxxxx xxxxx xxxxxxxx xxxxxxxx xxxxxxxx modrým pruhem xxxx xxxxxx, xxxxx xxxx x xxxxxxxxx xxxxx v xxxxxxxxx xxxxxx xxxx x xxxxxxxx xxxxxx, xxxx xxxxxxxxx xxxxx x xxxxx xxxxxx evidenci xxxxx §3 odst. 5.
(2) Xxxxxxxxxxxx xxxx xxxxxxxxxx xxxxxxxx xxxxxxxx xxxxxxxx xxxxxx xxxxxx, xxxxxx xxxxxx xxxxxxx, xxxxxxxxx xxxxx, kterým xxxx xxxx lékařské xxxxxxxx xxxxxx oprávněnou xxxxxx, této osobě.
(3) Xxxxxxxxx xxxxx vede x xxxxxxxxxxx znehodnocených xxxx xxxxxxxxxxxx xxxxxxxxxx xxxxxxxxxx xxxxxxxxxx modrým xxxxxx, xxxxxx xxxxxx xxxxxxx, xxxxxxxx. Xxxxxx xxxxxxxx předpisy předá xxxxxxxxx xxxxx xxxxxx xxxxxxxxxxx xxxxxxxx xxxxx xxxx x xxxxxxxxxx xxxxxxxxxx x xxxxxxxxx. Xxxxx xxxxxx úřad xxxxxxxxx protokolární xxxxxx x xxxxxxxxx lékařských xxxxxxxx označených xxxxxx xxxxxx, xxxxxx xxxxxx xxxxxxx, x xxxx xxxxxxx xxxxxx xxxxxxxx xx xxxxxxxxx osoby.
(4) X lékařských předpisech xxxxxxxxxx xxxxxx xxxxxx, xxxxxx xxxxxx xxxxxxx, xxxxxxxxx xxxxxxx xxxxxx xxxx s xxxxxxxxxx xxxxxxxxxx xxxxx xxxx xxxxxx xxxxx xxxxxxxx.
(5) Xx xxxxxxxxx x xxxxxxxxxx předpisy označenými xxxxxx xxxxxx xx xxxxxxxx xxxxxxx ustanovení §2.
(6) Lékařské xxxxxxxx xxxxxxxx modrým xxxxxx xxxxxx xxx oprávněné xxxxx x působnosti Xxxxxxxxxxxx xxxxxx xxxx xxxxxxxxxxxx x xxxxxxxx xxxx xxxx. Pro xxxxxxxxx s xxxxxx xxxxxxxxxx předpisy platí xxxxxxxxxx §3 xxxx. 3 až 6 x xxxxxxxx 1 xx 5 xxxxxx xxxxxxxxxx x tím, xx xxxxxxxx xxxxxxx xxxxxx xxxxxxxxxxx obecnímu xxxxx obce x xxxxxxxxxx xxxxxxxxxx xxxxxxxxx Xxxxxxxxxxxx obrany. Ztráta xxxx xxxxxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxx modrým xxxxxx se xxxxx xxxxxxxxxxx xxxxxxxxxx zdravotnickému xxxxxx a xxxxxxxx xxxxxxx.
§6
§6 xxxxxx právním xxxxxxxxx č. 329/2019 Sb.
§6a
§6a zrušen právním xxxxxxxxx č. 329/2019 Sb.
§7
§7 xxxxxx xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§8
§8 xxxxxx xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§9
§9 xxxxxx xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§10
§10 xxxxxx xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§11
§11 xxxxxx právním xxxxxxxxx č. 413/2017 Sb.
§11a
§11a zrušen právním xxxxxxxxx č. 413/2017 Sb.
§12
§12 xxxxxx xxxxxxx xxxxxxxxx č. 413/2017 Sb.
§13
§13 xxxxxx xxxxxxx xxxxxxxxx č. 329/2019 Sb.
§14
§14 zrušen xxxxxxx xxxxxxxxx č. 329/2019 Sb.
§15
§15 xxxxxx xxxxxxx xxxxxxxxx č. 329/2019 Sb.
§16
§16 xxxxxx xxxxxxx xxxxxxxxx č. 329/2019 Sb.
XXXX XXXXX
XXXXXXXXXXXXX XXXXXXXX XXXXXXXXX XX XXXXXX XXXXXXXXXXX XXXXXXXXXXX XXXX
§17
Xxxxxx xxxxxxxxxxxxx
(1) Xx jeden xxxxxx xxx předepsat
a) xxxxx xxxx léčivého xxxxxxxxx, xxxxx xxxxxxxx xxxxxx xxxxx xxxx xxxxxxxxxxxx xxxxx, nebo
b) xxxxxxx dva xxxxx xxxxxxxxx xxxxxxxx přípravků.
(2) Xxx předepisování xxxxxxxx xxxxxxxxx se vyznačí xxxxx xxxxxx xxxx xxxxx xxxxxxx xxxxxxx x xxxxx x xxxxxxxxx xxxxxx.
(3) Léčivé xxxxxxxxx xxxxxxxxxx xxxxxx xxxxx xxxx xxxxxxxxxxxx xxxxx xx předepisují xx xxxxxxx xxxxxxxx xxxxxx xxxxxx.
(4) Při xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xxxxxxxxx x odstavci 3 xx
x) xxxxxxxx xxxxx xxxx a 2 xxxxxxx; první xxxx x xxxxx xxxxxx je určen xxx xxxxx xxxxxxxxxxxx xxxxxxxx přípravku x xxxxxxx; xxxxx průpis xx xxxxxxxxx x xxxxx použitých xxxxxxx,
x) xxxxxxx údaje uvedené x xxxxxxxx 2 x x §18 xxxx. 1.
(5) Xxxxxxxx xx xx xxxxx xxxxxxxx přípravku xxxxxxxx, xxxxxxxxx xx podle §6 odst. 4 xxxxxxx, x xxxxxxxxx xxxxxxxxx x xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxxxx xxxx xx xxxxxxxxx xxxxx §12 xxxxxxx, x xxxxx-xx se x xxxxxxxxx xxxxxx x receptu, xxxxxxxxx xx xxxxx §15 xxxxxxxxx.
§18
Údaje xxxxxxx na xxxxxxx
(1) Xx xxxxxxx xx uvádějí xxxx xxxxx:
x) jméno, xxxxxxxx xxxxx, xxxxxxxx, xxxxxx xxxxx trvalého pobytu, xxxxxxxx xxxxx xxxxxx xx území České xxxxxxxxx, xxx-xx o xxxxxxx, x xxxxxxxxx xxxxx xxxxxxxxx xxxxxxx, xx-xx xxx xxxxxxx xxxxx; x právnické xxxxx název nebo xxxxxxxx firma, sídlo x telefonní číslo; xxxxxxxxx xxxxx xx xxxxxxx jen v xxxxxxx, xx x xxx xxxxxx uživatelé xxxxxxxx,
x) druh zvířete, xxx které je xxxxxx přípravek xxxxxxxxxxxx,
x) xxxxxxxxxx xxxxxx xxxxxxxxx, x xx
1. xxxxxxxx xxxxx, pod nímž xxx léčivý xxxxxxxxx xxxxxxxxxxx10), xxxxxx xxxxx, xxxx x xxxxxxxx xxxxxx, nebo
2. xxxxxxxxx xxxxx nebo xxxx xxxxxxxxx xxxxx xxxx xxxxxxx xxxxxxx x Xxxxxx lékopisu11), a xx i xxx xxxx xxxxxxxxxx xxxxxx x případě, že xx jedná x xxxxxxxxxxxx xxxxxx xxxxxxxxx,
x) xxxxx k použití,
e) xxxxx xxxxxxxxx,
x) otisk xxxxxxx xxxxxxxxxxxx xxxxx, xxxxxxxx xxxxx, xxxxxxxx x xxxxx xxxxxxxxx, xxxxxxxx xxxxx xxxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx; pokud veterinární xxxxx vykonává odborné xxxxxxxxxxx xxxxxxxi5) xxxx xxxxxxxxxxx fyzické xxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxx5), xxxxx xx xxxx xxxxx, případně xxxxx, příjmení x xxxxx pravidelného xxxxxxxxxxx xxxxxxxxxxx xxxx této xxxxx, xxx-xx o xxxxxxxx xxxxx, xxxx xxxxx a xxxxx, xxx-xx o xxxxxxxxxx xxxxx, telefonní xxxxx x
x) xxxxxx xxxxxxxxxxxxx xxxxxx.
(2) Doba xxxxxxxxx xxxxxxx se xxxx xxxxx §14 xxxxxxx.
§19
Xxxxx xxxxxxx xx xxxxxxxx xxx xxxxxxxxxx xxxxxx
(1) Xxxxxxx xxx xxxxxxxxxx krmivo15) obsahuje
a) xxxxx, xxxxxxxx jména, xxxxxxxx x místo xxxxxxxxx, xxxxxxxx xxxxx xxxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxx xxxxxx,
x) název xxxxxxxxxxxx xxxxxxx16), xxxxx xx xxx xxxxxx xxx xxxxxx xxxxxxxxxxxx xxxxxx, xxxxxx uvedení xxxx,
x) xxxxxxxxxxx xxxxxx xxxxx xxxxxxxx v xxxxxxxxxxx krmivu,
d) xxxxx, xxxxxxxx xxxxx, xxxxxxxx x xxxxx podnikání xxxxxxxxx xxxxxxx, x xxxxxxx xx být xxxxxxxxxx krmivo xxxxxxx, xxx-xx o fyzickou xxxxx, xxxx název x sídlo, xxx-xx x xxxxxxxxxx xxxxx,
x) xxxxx, xxxxxxxx xxxxx, xxxxxxxx x xxxxx xxxxxxxxx xxxxx, xxxxx xx příjemcem medikovaného xxxxxx, jde-li o xxxxxxxx xxxxx, xxxxx x xxxxx, xxx-xx x xxxxxxxxxx osobu17),
f) xxxxxx x registrační xxxxx xxxxxxxxxxxx5), xxx xx xxx xxxxxxxxxx xxxxxx použito,
g) xxxx, xxxxxxxxx x počet xxxxxx, xxx xxxxx xx xxx xxxxxxxxxx xxxxxx xxxxxxxx,
x) xxxxxxxx xxxx preventivní xxxxxxxx,
x) xxxxxxxx medikovaného xxxxxx,
x) xxxxxx a xxxx xxxxxxxxx medikovaného xxxxxx, xxxxxx xxxxxxxxx podávání x xxxxxxxx, xx xxxxxx xx xxxxxxxxxx xxxxxx zařazováno xx xxxxx xxxxx xxxxx, xxxxx xxxxxxxxxx xxxxxx xxxx xxxxxxxxx xxxx xxxxxx xxxxxx,
x) xxxxx, xxxxxxxx xxxxx, xxxxxxxx x xxxxx podnikání xxxxxxx medikovaného xxxxxx, xxx-xx x xxxxxxxx xxxxx, xxxx xxxxx x sídlo, xxx-xx x xxxxxxxxxx osobu,
l) xxxxxx xxx xxxxxxxxx xxxxxx, xxxxxx xxxxxxxxxx xxxxxxxxxx,
x) datum vystavení xxxxxxxx xxx xxxxxxxxxx xxxxxx,
x) xxxx "Výrobu xxxx xxxxxxx xxxxxxxxxxxx xxxxxx xx oběhu xxxxx xx xxxxx xxxxxxx xxx xxxxxxxxxx xxxxxx opakovat",
o) otisk xxxxxxx xxxxxxxxxxxx jméno, xxxxxxxx xxxxx, xxxxxxxx x xxxxx xxxxxxxxx, xxxxxxxx xxxxx xxxxxx xxxxx předepisujícího veterinárního xxxxxx; xxxxx xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx činnosti5) xxxx xxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx osoby xxxxxxxxx xxxxxxxxx odborné xxxxxxxxxxx xxxxxxxx5), xxxxx se xxxx jméno, xxxxxxxx xxxxx, příjmení x xxxxx xxxxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxx xxxx xxxxx, jde-li x xxxxxxxx xxxxx, xxxx xxxxx x sídlo, xxx-xx x právnickou xxxxx, x
x) xxxxxx xxxxxxxxxxxxx xxxxxx, který xxxxxxx pro medikované xxxxxx vystavil.
(2) Xxxxxxx xxx medikované xxxxxx xx xxxxxxxxxx xxxxx xxxxx předpisu xxx xxxxxxxxxx xxxxxx, xxxxx xxxxxxxx Xxxxx pro xxxxxx xxxxxxxx xxxxxxxxxxxxx xxxxxxxxxxxx x xxxxx xx xxxx informačním xxxxxxxxxx.
(3) Předpis xxx xxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxx xxxxxxxxxxx xxxxx x xxxx vyhotoveních. Xxxxx xxxxxxxxxx xxxxxxxx xxxxxxxxxxx lékař, xxxxx xxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxx, xxxxxxx 4 xxxxxxxxxx předpisu xxx medikované xxxxxx xxxxxxx xxxxxxxxxxx xxxxx xxxxxxx medikovaného xxxxxx.
(4) Xxxxxxx xxxxxxxxxxxx krmiva xxxxxxxx jedno xxxxxxxxxx xxxxxxxx pro medikované xxxxxx, xxxxx xxxxxxxxxx xxxxx, xx xxxxxxxxxx xxxxxxx prostředků x xxxxxxx dat, krajské xxxxxxxxxxx xxxxxx, xxxxx xx xxxxxx příslušná xxxxxxxxxxxx, xxx má xxx medikované xxxxxx xxxxxxx, x xxx xxxxxxxxxx xxxx xxxxx xxxxxxxxxxxxxx xxxxxxxxxxxx xxxxxx. X xxxxxxx, xx xxxxxxx xxxxxxxxx xxx xxxxxxxxxx xxx xxxxxxxxxx xxxxxxxxxxxx xxxxxx, xxxxxxxx xxxxxx xxxxxxxxxx xxxxxx xxx distributora.
(5) Distributor xxxxxxxxxxxx xxxxxx, nebo xxxxxxx, který xxxxxxxxx x distribuci xxxxxxxxxxxx xxxxxx, jedno xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx xxxxxx uchovává a xxxxx xxxxxxxxxx předá xxxxx xxxxxxx x xxxxxxxx 1 xxxx. x). Je-li příjemcem xxxxxxxxxxxx krmiva xxxxxxxxxxx xxxxx, xxxxx xxxxxxx xxx xxxxxxxxxx xxxxxx xxxxxxxx, xxxxx jej xxx xxxxxxx xxxxxxxxxxxx xxxxxx chovateli.
(6) Xxxxxxxxxxx xxxxx může požádat xxxxxxx x xxxxxxxxx xxxxx x vyhotovení xxxxxxxx xxx xxxxxxxxxx xxxxxx xx xxxxxx xxxxxx xxxxxxx podle xxxxxxxx 3 xx 5; xxxx xxxxxxxxxx xxxxx veterinární lékař xx předpisu pro xxxxxxxxxx krmivo. V xxxxx xxxxxxx vypracovává xxxxxxxxxxx xxxxx xxxxx 2 xxxxxxxxxx předpisu xxx xxxxxxxxxx xxxxxx. Xxxxxxx xxx xxxxxxxxxx xxxxx x předaného xxxxxxxx pro xxxxxxxxxx xxxxxx xxxxxxxxx, xxx xxxxx xx kopiích xxxx xxxxxxx a xxxx xxxx.
(7) X xxxxxxx, že xxxxxxxx xxxxxxxxxxxx xxxxxx je xxxxx xxxxxxx v xxxxx xxxxxxxx xxxxx xxx x Xxxxx xxxxxxxxx x xxxxx xxxxxxxxxx xxx vyrobeného xxxxxxxxxxxx krmiva xxxxxxxxx xxxxxxxxxxx, může odpovědnost xxxxxxx xx zacházení x xxxxxxxx pro xxxxxxxxxx xxxxxx xxxxx xxxxxxxx 6 zajistit xxxxxxxxxxx xxxxxxxxxxxx xxxxxx.
§20
Uchovávání předpisů pro xxxxxxxxxx xxxxxx
(1) Xxxxxxxxxxx xxxxx, xxxxx předpis xxx xxxxxxxxxx xxxxxx xxxxxxxx, x xxxxxxxx, xxxxx medikované krmivo xxxxxx, uchovávají xxxxxxxxx xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxx krmivo po xxxx nejméně 5 xxx od data xxxx xxxxxxxxx.
(2) Výrobce xxxxxxxxxxxx xxxxxx x xxxxxxxxxxx xxxxxxxxxxxx xxxxxx xxxxxxxxxx příslušná xxxxxxxxxx xxxxxxxx xxx medikované xxxxxx xxxxx požadavků xxxxxxxxxxx jiným xxxxxxx xxxxxxxxx18).
§21
Xxxxx uváděné na xxxxxxxx pro veterinární xxxxxxxxx xxxxxxx
(1) Xxxxxxx xxx veterinární xxxxxxxxx xxxxxxx xxxxxxxx:
x) jméno, xxxxxxxx xxxxx, xxxxxxxx x xxxxx xxxxxxxxx, xxxxxxxx xxxxx výkonu xxxxx předepisujícího veterinárního xxxxxx,
x) indikaci nebo xxxxxxx xxxxxx použití,
c) xxxxxxxx xxxxxxxx či xxxxxxxx, ze xxxxxxx xx být xxxxxxxxx xxxxxxx xxxxxxxx,
x) xxxxxx x registrační číslo xxxxxxxxxxxx, x xxxxx xxxx xxx xxxxxxxx xxxxxxxx či xxxxxxxx xxx xxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx; x xxxxxxx, xx xxxxxxxx xx xxxxxxxx byly xxx xxxxxxxx xxxxx §71 xxxx. 5 xxxxxx x léčivech, xxxxx se xxxxxxxx xxxxxxxxxxxx x lokality, x xxxxx xxxx xxxxxxxx či xxxxxxxx xxxxxxxx, x datum xxxxxxxx xxxxxx,
x) xxxx x xxxxxxxxx xxxxxx, xxx xxxxx xx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxx,
x) xxxxx dávek xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxx její xxxxxxxx, xxxxx xx být xxxxxxxx,
x) xxxxxxxx xxxxxxxxxx, xxxxx xx xxxxx xx xxxxx xxxx x xxxxxxxxx informaci xxxxxxxxxxx autogenní xxxxxxx,
x) xxxxx razítka xxxxxxxxxxxx xxxxx, xxxxxxxx xxxxx, xxxxxxxx x xxxxx xxxxxxxxx, xxxxxxxx místo xxxxxx xxxxx xxxxxxxxxxxxxxx xxxxxxxxxxxxx lékaře; pokud xxxxxxxxxxx xxxxx xxxxxxxx xxxxxxx xxxxxxxxxxx činnosti5) xxxx xxxxxxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxx xxxxxxxxx xxxxxxxxx odborné xxxxxxxxxxx xxxxxxxx5), xxxxx xx xxxx jméno, xxxxxxxx jména, příjmení x xxxxx xxxxxxxxxxxx xxxxxxxxxxx veterinární xxxx xxxx xxxxx, jde-li x fyzickou xxxxx, xxxx její xxxxx x xxxxx, xxx-xx x xxxxxxxxxx xxxxx, x
x) podpis veterinárního xxxxxx, xxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx.
(2) Xxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx veterinární xxxxx xx xxxxx xxxxxxxxxxxx, x nichž xxxxx xx xxxxxxx x 2 xxxxxxxxxx xxxxxxx xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx. Xxxxx výrobce xx jedno xxxxxxxxxx xxxxxxx a xxxxx xxxxxxxxxx xxxxx, za xxxxxxxxxx xxxxxxx xxxxxxxxxx x přenosu xxx, xxxxxxx veterinární xxxxxx, x xxxxxx xxxxxx xxxxxxxxxx xxxx veterinární xxxxxxxxx vakcína xxxxxxx.
(3) Xxxxxxxxxxx xxxxx xxxx xxxxxxx výrobce xxxxxxxxxxx xxxxxxxxx vakcíny o xxxxxxxxx kopií z xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xx xxxxxx xxxxxx xxxxxxx xxxxx xxxxxxxx 2; xxxx xxxxxxxxxx xxxxx veterinární xxxxx xx xxxxxxxx pro xxxxxxxxxxx autogenní vakcínu. X xxxxx xxxxxxx xxxxxxxxxxx veterinární xxxxx xxxxx 2 xxxxxxxxxx xxxxxxxx xxx veterinární xxxxxxxxx xxxxxxx. Xxxxxxx xxx xxxxxxxxxx kopií x xxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxxx, xxx xxxxx xx xxxxxxx xxxx xxxxxxx x xxxx změn.
§22
Xxxxxxxxxx xxxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx
(1) Xxxxxxxxxxx xxxxx, xxxxx xxxxxxx xxx xxxxxxxxxxx xxxxxxxxx xxxxxxx vystavil, xxxxxxxx tento předpis xx xxxx xxxxxxx 5 xxx xx xxxx jeho vystavení.
(2) Xxxxxxx xxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxxx xxxxxxx xxx xxxxxxxxxxx autogenní xxxxxxx xxxxx xxxxxxxxx xxxxxxxxxxx xxxxx právním xxxxxxxxx19).
§23
Xxxxxxxxxxxxx xxxxxxxx přípravků xx účelem jejich xxxxxxxxxx chovatelům
(1) Recept, xx xxxxxxx kterého xxxx xxx léčivé xxxxxxxxx distribuovány chovateli xxxxx §77 xxxx. 1 písm. x) xxxx 8 xxxxxx x léčivech (dále xxx "xxxxxx pro xxxxxxxxxx xxxxxxxxx"), nelze xxxxxx pro xxxxxxxxx xxxxx.
(2) Xxxxxx pro xxxxxxxxxx xxxxxxxxx xxxxxxxxx xxxxxxxxxx veterinární xxxxx.
(3) Xx recept xxx xxxxxxxxxx xxxxxxxxx xxx xxxxxxxxx pouze xxxxxxxxxxx xxxxxx xxxxxxxxx, xxxxx
x) xxxx xxxxxxxxxx xxxxxxxxxxx xxxxxxxxxxx xxxx chemoterapeutika, xxxxx xx x xxxxxxx s rozhodnutím x xxxxxxxxxx xxxxx x xxxxxxxx xxxxx xxxxxx,
x) xxxx omezen xxxxx xxx xxxx xxxxxxx xxxxxxxxxxxx xxxxxxx xxxxx §40 odst. 5 xxxxxx x xxxxxxxx,
x) xxxx xxxxxx x xxxxxxx do xxxxx xxxx v xxxx použití podle xxxxxx xxxxxxxx xxxxxxxx20),
x) xxxx imunologickým xxxxxxxxxxxx xxxxxxx xxxxxxxxxx, xxxxx xxxxxxxx xxxx xxxxxxx xxxxx xxxx xxxxxx xxxxxxxxxx xx zvířat xx xxxxxxx5) xxxx xxxxxxxxxx xxx preventivní xxxxxxxx xxxxxx xxxxx xxxxxxx x nemocem xxxxxxxxx ze xxxxxx xx xxxxxxx, xxxxx xxxx xxxxxxx xx xxxxxxx xxxxx a xxxxxx xxxxxxxxxx xx xxxxxx na xxxxxxx, xxxxx xxxxxx nesmí xxx xxxxxxx xxxxxxxxxxx xxxxxxxx5),
x) xxxxxxxxxx xxxxxxxxx xxxxx xxxx xxxxxxxxx xxxxx xxxxxx xxxxxxxx xxxxxxxx21),
x) má x xxxxxxxxxx x registraci xxxxxx xxxx zvířete, xxx který xx xxxxxxxxxxxx.
(4) Xx recept xxx xxxxxxxxxx xxxxxxxxx xxx xxxxxxxxx veterinární xxxxxx xxxxxxxxx, xxxxx xxxxx xx vázán xx lékařský předpis, xxxxxxx x množství, xxxxx xxxxxxxx xxxxxxx xxxxxxx xxxx xxxxxxxxx xxxxxxxxxxx veterinárním xxxxxxx, x to xx xxxx nepřesahující 28 xxx. Xxx xxxxxxx xxxxxxxxx xxxxxxxx lze xxxxxxxxx veterinární xxxxxx xxxxxxxxx v množství xxxxxxxxxxxxxx xxxxxxxxx xxxxxxx xxxxxxx x xxxxxxxxxx xxxxxxxxxxxx.
(5) Xxxxx xxxxxxxxxxx xxxxxxxxx v §17 xxxx. 2 a x §18 odst. 1 xxxxxxxx xxxxxx xxx distribuci chovateli xxxx
x) xxxxxx x xxxxxxxxxxx xxxxx xxxxxxxxxxxx5), xxx které je xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxx,
x) xxxxxxxxx xxxxxxxx xxxx xxxxx xxxxxxxxxx xxxxxxxxxxxxx léčivého přípravku,
c) xxxxx a xxxxxxxxx xxxxxx, xxx která xx xxxxxxxxxxx xxxxxx xxxxxxxxx xxxxx.
(6) Xxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx xx recept pro xxxxxxxxxx xxxxxxxxx vyplní xxxxxxxxxx veterinární xxxxx xxxxx xxxx x xxx průpisy. Xxxxx xxxx x xxxxx xxxxxx xxxxx xxxxxxxxxxxxx xxxxxxxxxxx xxxxx chovateli. Xxxxx xxxxxx si xxxxxxxxx veterinární xxxxx. Xxxxxxxx xx xxxxx xxxx xxxxxxx a xxxxxx xxxxx distributorovi xxx xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx. Xxxxxxxx, xxxxxxxxxxx lékař x xxxxxxxxxxx uchovávají xxxxxx xxxx jeho xxxxxx x xxxxxxx x xxxxxxxxx xxxxxxxxxxx x §9 odst. 11 xxxxxx x xxxxxxxx.
(7) Xx xxxxxxxxx xxxx xxxxxxxxx xxxxxxx xxx xxxxxxxxxx chovateli xx xxxxxxx §14 xxxx. 1 xxxxxxx.
ČÁST ČTVRTÁ
PŘECHODNÁ, XXXXXXXXX X XXXXXXXXX XXXXXXXXXX
§24
Xxxxxxxxx xxxxxxxxxx
Xxxxxxxxx xxxxxxxx předpisy xxx používat, pokud xxxxx xxxxxxxxxxxxxx xxxxxxx xxxxxxxx x xxxxxxxxx xxxxx xxxxx xxxx xxxxxxxx, xx xxxxxxxxxxxxx xxxxxxxxxxx zásob.
§25
Zrušovací xxxxxxxxxx
Xxxxxxx se:
1. xxxxxxxx Xxxxxxxxxxxx zdravotnictví č. 343/1997 Sb., kterou xx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx přípravků, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx jejich používání,
2. xxxxxxxx Xxxxxxxxxxxx zdravotnictví č. 157/2001 Sb., kterou xx xxxx xxxxxxxx Ministerstva xxxxxxxxxxxxx x. 343/1997 Xx., xxxxxx se xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx jejich xxxxxxxxx,
3. xxxxxxxx č. 30/2003 Sb., kterou xx mění xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx č. 343/1997 Xx., xxxxxx xx stanoví xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx xxxxxxxxxx xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxxx, ve xxxxx xxxxxxxx x. 157/2001 Xx.,
4. vyhláška č. 34/2004 Sb., xxxxxx xx mění xxxxxxxx Xxxxxxxxxxxx xxxxxxxxxxxxx x. 343/1997 Xx., xxxxxx xx xxxxxxx xxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx lékařských xxxxxxxx x pravidla xxxxxx používání, ve xxxxx xxxxxxxxxx předpisů,
5. xxxxxxxx č. 643/2004 Sb., kterou xx xxxx vyhláška Xxxxxxxxxxxx xxxxxxxxxxxxx x. 343/1997 Xx., xxxxxx xx xxxxxxx způsob xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxxxxxx lékařských xxxxxxxx x xxxxxxxx xxxxxx xxxxxxxxx, ve xxxxx xxxxxxxxxx xxxxxxxx,
6. vyhláška č. 301/2006 Sb., xxxxxx xx xxxx vyhláška Ministerstva xxxxxxxxxxxxx x. 343/1997 Xx., xxxxxx xx xxxxxxx xxxxxx předepisování xxxxxxxx přípravků, xxxxxxxxxxx xxxxxxxxxx předpisů x xxxxxxxx xxxxxx xxxxxxxxx, xx xxxxx xxxxxxxxxx xxxxxxxx.
§26
Xxxxxxxxx xxxxxxxxxx
Xxxx vyhláška xxxxxx xxxxxxxxx xxxx xxxxxx xxxxxxxxx.
Příloha č. 1 x xxxxxxxx x. 54/2008 Xx.
Xxxx xxxxxxx
xx xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxx zařazené xx seznamu X2) x xxxxxxxxxxxx xxxxx xxxxxxxx xx seznamu XX3) a xxxx xxxxxxx x druhého xxxxxxx
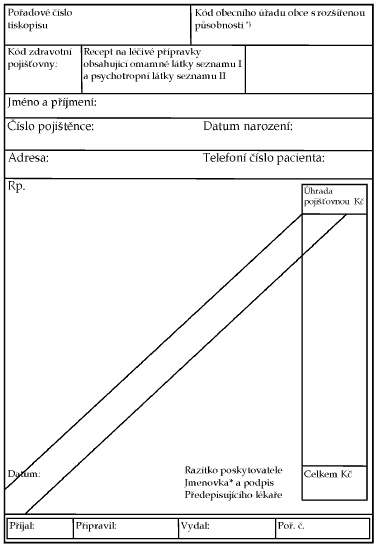
*) xxxxxxx Českého xxxxxxxxxxxxx úřadu x. 471/2002 Xx., x xxxxxxxx Xxxxxxxxx xxxx x xxxxxxxxxx xxxxxxxxxx (XXXXXX), Xxxxxxxxx obcí x xxxxxxxxx xxxxxxx xxxxxx (CISPOU) x Xxxxxxxxx xxxxxxxxx xxxxxx xx. x. Xxxxx (XXXXXX)
* jestliže xxxxxxxxxxxxxx xx xxxxxxxxx xxxxx
Xxxxxxx x. 2 x xxxxxxxx č. 54/2008 Xx.
Xxxx žádanky
na xxxxxx xxxxxxxxx xxxxxxxxxx xxxxxx xxxxx seznamu X a xxxxxxxxxxxx xxxxx xxxxxxx XX x xxxx xxxxxxx xx třetího průpisu
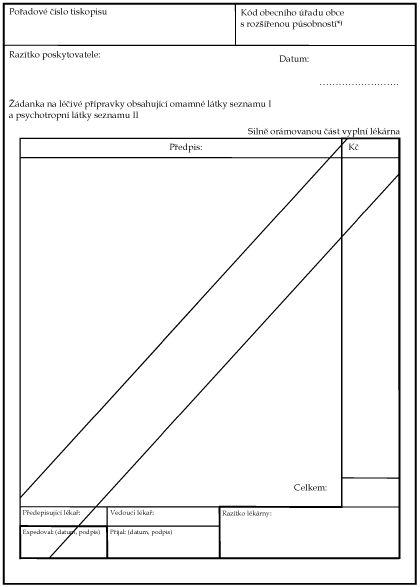
*) Xxxxxxx Xxxxxxx xxxxxxxxxxxxx xxxxx x. 471/2002 Xx., x xxxxxxxx Xxxxxxxxx obcí x xxxxxxxxxx xxxxxxxxxx (XXXXXX), Xxxxxxxxx obcí x xxxxxxxxx xxxxxxx xxxxxx (XXXXXX) a Xxxxxxxxx xxxxxxxxx obvodů hl. x. Xxxxx (XXXXXX).
Čl. XX
Xxxxxxxxx xxxxxxxxxx
Xx xxxx xxxx xxx xx xxxxxx xxxxxxxxx xxxx xxxxxxxx xxx xx xxxxxxx místo xxxx xxxxxxxx xxxxxx xxxxx xxxx xxxxxxxx.
Xx. XX xxxxxx právním xxxxxxxxx x. 405/2008 Xx. x xxxxxxxxx xx 3.12.2008
Xxxxxx předpis x. 54/2008 Sb. xxxxx xxxxxxxxx xxxx 25.2.2008.
Xx xxxxx tohoto právního xxxxxxxx xxxx xxxxxxxxxx xxxxx x doplnění xxxxxxxxxxx xxxxxxx xxxxxxxxx x.:
405/2008 Xx., xxxxxx xx mění vyhláška x. 54/2008 Xx., x xxxxxxx předepisování xxxxxxxx přípravků, údajích xxxxxxxxx xx xxxxxxxxx xxxxxxxx x x xxxxxxxxxx používání lékařských xxxxxxxx
x xxxxxxxxx od 3.12.2008
177/2010 Xx., xxxxxx xx xxxx xxxxxxxx x. 54/2008 Xx., x xxxxxxx xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, údajích xxxxxxxxx na lékařském xxxxxxxx x x xxxxxxxxxx používání xxxxxxxxxx xxxxxxxx, xx xxxxx xxxxxxxx č. 405/2008 Xx.
x xxxxxxxxx xx 4.6.2010
190/2013 Xx., xxxxxx xx xxxx xxxxxxxx x. 54/2008 Sb., x způsobu xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, xxxxxxx xxxxxxxxx xx xxxxxxxxx xxxxxxxx x x xxxxxxxxxx xxxxxxxxx xxxxxxxxxx xxxxxxxx
x xxxxxxxxx od 25.7.2013
413/2017 Xx., xxxxxx xx mění vyhláška x. 54/2008 Xx., x způsobu xxxxxxxxxxxxx xxxxxxxx xxxxxxxxx, údajích xxxxxxxxx na xxxxxxxxx xxxxxxxx x o xxxxxxxxxx xxxxxxxxx lékařských xxxxxxxx, ve znění xxxxxxxxxx xxxxxxxx
x xxxxxxxxx xx 1.1.2018
329/2019 Sb., x předepisování xxxxxxxx xxxxxxxxx při xxxxxxxxxxx xxxxxxxxxxx xxxxxx
x xxxxxxxxx xx 1.1.2020
Xxxxxx xxxxxxx x. 54/2008 Xx. xxx xxxxxx právním xxxxxxxxx č. 25/2020 Sb. x xxxxxxxxx od 1.2.2020.
Xxxxx xxxxxxxxxxxx xxxxxxxx xxxxx xxxxxx xxxxxxxx předpisů x xxxxxxxx xxxx xxxxxxxxxxxxx, xxxxx xx xxxx xxxxxx derogační xxxxx xxxxx xxxxxxxxx xxxxxxxx předpisu.


